文章信息
- 王小红, 杨智杰, 刘小飞, 林伟盛, 杨玉盛, 刘志江, 赵本嘉, 苏瑞兰
- WANG Xiaohong, YANG Zhijie, LIU Xiaofei, LIN Weisheng, YANG Yusheng, LIU Zhijiang, ZHAO Benjia, SU Ruilan
- 中亚热带山区土壤不同形态铁铝氧化物对团聚体稳定性的影响
- Effects of different forms of Fe and Al oxides on soil aggregate stability in mid- subtropical mountainous area of southern China
- 生态学报, 2016, 36(9): 2588-2596
- Acta Ecologica Sinica, 2016, 36(9): 2588-2596
- http://dx.doi.org/10.5846/stxb201408021542
-
文章历史
- 收稿日期: 2014-08-02
- 网络出版日期: 2015-08-26
2. 湿润亚热带山地生态国家重点实验室培育基地, 福州 350007;
3. 三明市三元区林业局, 三明 365002
2. State Key Laboratory Breeding Base of Humid Subtropical Mountain Ecology, Fujian Normal University, Fuzhou 350007, China;
3. Sanyuan Forestry Bureau, Sanming 365002, China
土壤团聚体是土壤结构的基本单元,在调节土壤肥力,维持土地生产力上具有重要作用[1],而且影响着土壤孔隙度、透水性、抗蚀性等[2],其稳定性是反映土壤结构的重要指标。同时,土壤团聚体是土壤固碳的主要场所[3],其对土壤有机碳的物理保护被认为是有机碳稳定性的重要机制[4]。铁铝氧化物、腐殖质及层状硅酸盐是土壤复合体的基本组成成分,它们之间的相互胶结,可显著影响土壤的某些理化性质[5]。铁铝氧化物-高岭石复合物具有结构稳定和表面活性强的特性,对土壤团聚体的形成、稳定和性质有重要影响[6]。同时,铁铝氧化物可在有机无机复合过程中充当“桥”的作用[7],红外光谱和核磁共振分析显示,铁铝氧化物可通过腐殖质表面的羟基或羧基与矿物表面进行配位体交换,与胡敏酸、富啡酸形成稳定的有机无机复合体[8],有研究认为这种有机无机复合过程是团聚体形成的基础[9]。但学界对铁铝氧化物对团聚体形成的作用仍存在争议,体现在结晶度、颗粒大小、氧化物分布和氧化物作用的程度上[10]。目前针对我国南方地带性土壤铁铝氧化物的研究已多有报道[11, 12, 13],但关于铁铝氧化物对团聚体形成与稳定的作用的相关报道较少[14, 15].因此,本文以中亚热带地区本底条件一致的3种林分土壤作为研究对象,研究了不同形态铁铝氧化物与水稳定性大团聚体数量及团聚体稳定性的关系,旨在探讨亚热带森林土壤中铁铝氧化物在土壤形成与稳定中的作用,为揭示热带亚热带土壤团聚体形成与稳定性机制提供一定的依据。
1 材料与方法 1.1 样地概况试验地位于福建省大武夷山常绿阔叶林野外定位研究站三明观测站(26°19′ N,117 °36′ E),该区域东南面和西北面分别与戴云山脉和武夷山脉相连,属中亚热带季风气候,年均气温19.1 ℃,年均降雨量1749 mm(集中于3—8月份),年均蒸发量1585 mm,相对湿度81%,成土母岩为花岗岩。
米槠天然更新次生林(次生林,naturally regenerated Castanopsis carlesii forest)是米槠天然林经过强度择伐后封山育林,经次生演替形成,海拔330 m,坡度45°,林龄在35a左右,乔木层有米槠(Castanopsis carlesii)、闽粤栲(Castanopsis fissa)、黄丹木姜子(Litsea elongata)、新木姜子(Neolitsea aurata)等,灌木层及草本层包括木荚红豆(Ormosia xylocarpa)、褐毛石楠(Photinia hirsuta)、罗浮栲(Cinnanomum chekiangense)、狗脊(Woodwardia prolifera)、黑莎草(Gahnia tristis Nees)、油草(Leptochloa chinensis)等。米槠人促林(Castanopsis carlesii plantation)是在米槠天然林经过强度择伐后的天然更新的基础上,并在更新过程适当增添人为措施来辅助天然更新,林龄在37a左右,海拔335 m,坡度38°,林下植被主要有木荷(Schima superba)、东南野桐(Malloyus lianus)、灰木(Symplocos paniculata)、鼠刺(Itea chinensis)、毛叶冬青(Ilex pubilimba)、石栎(Lithocarpus glabra)、鳞子莎(Lepidosperma Labill)、狗脊、扇叶铁线蕨(Adiantum flabellulatum)。杉木人工林(Chinese fir plantation)则是米槠天然林经皆伐火烧炼山等营林活动后建立的人工纯林,林龄在37a左右,海拔301 m,坡度30°,林下植被主要以狗骨柴(Tricalysia dubia)、毛冬青( Ilex pubescens)、芒萁(Dicranopteris dichotoma)为主。
1.2 样品采集与处理2014年4月于上述3种林分分别布设3个10 m×10 m样方,每个样方依网格状9点取样,取样时先移除地表的枯枝落叶,取0—10 cm土层原状土壤,同一样方土壤混合。在室内将取回的原状土壤,剔除可见的石砾、根系及其他杂质,按四分法分成两份,一份用于土壤水稳定性团聚体的测定;一份用于土壤的理化性质的测定。
1.3 实验方法水稳定性团聚体的测定采用Six等[16]的方法,并稍作修改,即称取50 g风干土样置于套筛(2、0.25、0.053 mm)顶层筛上,浸泡10 min,启动湿筛仪,以上下振幅3 cm,频率为30次/min,时间为2 min。待筛分完毕后,将留在各层筛上的物质洗入已称重的铝盒,通过0.053 mm筛的悬液静置48 h,用吸管移去上层清液,获得的 < 0.053 mm粉粘粒团聚体洗入已称重的铝盒。将获得的各粒径水稳定性团聚体在60℃烘干至恒重,做3次平行。
由于砂粒并不是团聚体的一部分,以及砂粒并不与有机质结合[16],因此本文中依据Denef等[17]的方法对>0.053 mm不同粒径团聚体进行去砂矫正处理。
土壤中不同形态铁铝氧化物的提取及测定采用鲁如坤等[18]的方法:即游离结晶态铁铝氧化物采用连二亚硫酸钠-柠檬酸钠-重碳酸钠(dithionite-citrate-bicarbonate,DCB)提取,无定形铁铝氧化物采用草酸铵-草酸(acid ammonium oxalate,AAO)提取,络合态铁铝氧化物采用焦磷酸钠(sodium pyrophosphate,SP)提取。
土壤其他理化性质(表 1)的测定:土壤pH值采用1∶2.5土水比例电位法,以pH仪测定;土壤颗粒组成采用土壤粒径分析系统(SEDIMAT 4—12)测定;土壤C、N采用碳氮元素分析仪(vario MAX)测定。
| 林分 Forest | 米槠次生林NR | 米槠人促林CC | 杉木人工林CF |
| 土壤容重 Soil bulk/(g/cm3) | 0.97 ± 0.05 | 1.21 ± 0.05 | 1.41 ± 0.11 |
| pH | 4.13 ± 0.14 | 4.32 ± 0.31 | 4.70 ± 0.03 |
| 土壤有机碳SOC/(g/kg) | 24.98 ± 0.51 | 21.21 ± 1.68 | 19.58 ± 0.42 |
| 氮N/(g/kg) | 1.67 ± 0.12 | 1.57 ± 0.18 | 1.38 ± 0.04 |
| 石砾 Grit particle/% | 8.07 ± 2.85 | 8.56 ± 3.05 | 13.30 ± 2.52 |
| 砂粒 Sand particle/% | 36.62 ± 7.75 | 46.00 ± 4.70 | 36.56 ± 1.86 |
| 粉粒 Silt particle/% | 30.09 ± 1.65 | 25.2 ± 0.75 | 31.81 ± 3.65 |
| 粘粒 Clay particle/% | 25.19 ± 3.31 | 20.7 ± 2.41 | 18.34 ± 4.49 |
| NR:米槠次生林naturally regenerated Castanopsis carlesii forest;CC:米槠人促林Castanopsis carlesii assisted regeneration forest;CF:杉木人工林Chinese fir plantation;± 0.05:标准差 | |||
去除砂粒矫正后的各粒级团聚体重量(%)的计算采用Denef等[17]的公式:
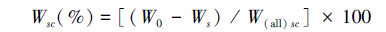
式中,Wsc为去除砂粒后的团聚体重量比;W0为某粒径初始团聚体重量;Ws为同一粒径团聚体中砂粒重量;W(all)sc为去砂后各粒径团聚体重量之和。
土壤团聚体平均重量直径(MWD)的计算采用郑子成等[19]的方法:
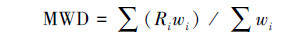
式中,Ri为某粒级团聚体平均直径;wi为湿筛后某粒级团聚体的重量。
数据处理采用Excel 2007软件,数据分析采用SPSS 17.0软件,显著性分析采用LSD检验法,绘图采用Origin Pro 7.5软件。
2 结果与分析 2.1 不同林分土壤铁铝氧化物的差异如表 2所示,不同形态铁铝氧化物含量在0.74—12.41 g/kg之间,以Fed含量最高,达到9.56—12.41 g/kg,远高于其他铁铝氧化物含量,而Als含量(0.74—1.16 g/kg)最低,整体上呈现出Fed>>Ald>Feo>Alo>Fes>Als。不同林分铁铝氧化物含量有较大差异,但都表现出米槠次生林>米槠人促林>杉木人工林。除Fed含量无显著差异外,其他形态铁铝氧化物均有显著差异,其中米槠次生林Feo和Fes含量显著高于米槠人工林和杉木人工林,而后两林分差异不显著;Ald、Alo及Als含量则表现出各林分间差异显著。
| (g/kg) | ||||||
| 林分Forest | Fed | Feo | Fes | Ald | Alo | Als |
| 米槠次生林 NR | 12.41 a | 3.53 a | 1.79 a | 5.82 a | 2.51 a | 1.16 a |
| 米槠人促林 CC | 12.12 a | 2.11 b | 0.92 b | 5.61 ab | 2.23 ab | 0.91 b |
| 杉木人工林 CF | 9.56 a | 1.77 b | 0.83 b | 4.35 b | 1.92 b | 0.74 c |
| NR:米槠次生林natural regeneration Castanopsis carlesii forest;CC:米槠人促林Castanopsis carlesii assisted regeneration forest;CF:杉木人工林Chinese fir plantation;Fed、Ald:游离结晶态铁铝氧化物;Feo、Alo: 无定形铁铝氧化物;Feo、Alo: 络合态铁铝氧化物;不同小写字母表示不同林分同一类型氧化物含量差异显著(P < 0.05 | ||||||
>0.25mm水稳性大团聚体含量是判定土壤质量好坏的重要指标,同时也是衡量土壤抗侵蚀能力的指标之一,数量越多,土壤稳定性和抗蚀能力越高。如表 3所示,米槠次生林>0.25 mm水稳定性大团聚体数量所占比例为82.41%,分别是米槠人促林和杉木人工林>0.25 mm水稳定性大团聚体数量的1.08和1.18倍,三林分之间差异显著。平均重量直径(MWD),尤其是水稳定性团聚体的MWD是评价土壤团聚体稳定性的常用指标,MWD值越大,表明团聚体团聚度越高,稳定性越好。米槠次生林、米槠人促林及杉木人工林MWD值分别为2.93、2.81和2.43 mm,其中米槠次生林与米槠人促林差异不显著,但显著高于杉木人工林。
| 林分Forest | >0.25 mm 大团聚体 macro-aggregates/% | MWD/mm |
| 米槠次生林 NR | 82.41a | 2.93a |
| 米槠人促林 CC | 76.25b | 2.81a |
| 杉木人工林 CF | 69.71c | 2.43b |
| NR:米槠次生林natural regeneration Castanopsis carlesii forest;CC:米槠人促林Castanopsis carlesii assisted regeneration forest;CF:杉木人工林Chinese fir plantation;MWD:平均重量直径 mean weight diameter;不同小写字母表示同一指标林分间差异显著 | ||
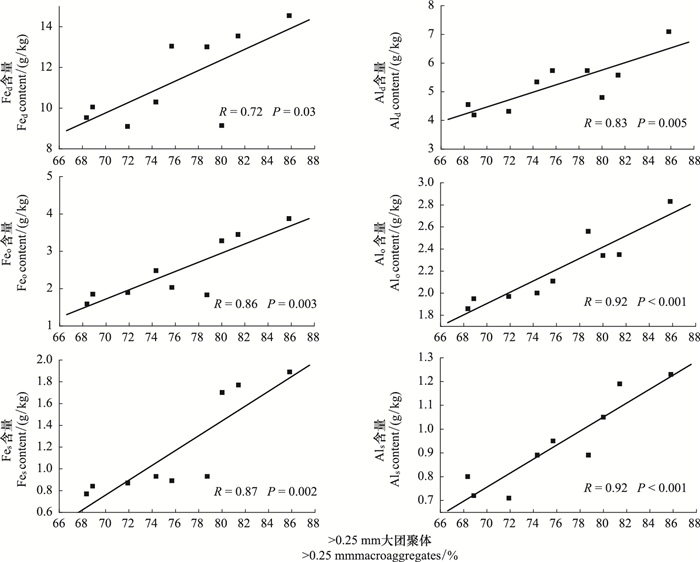
通过线性拟合>0.25 mm大团聚体数量与不同形态铁铝氧化物含量发现,两者相关性达到显著甚至极显著水平(图 1),但不同形态铁铝氧化物其相关系数R和显著性P值存在较大差异。如图 1所示,Fed、Feo及Fes与>0.25 mm水稳定性大团聚体数量的线性关系分别为Y=0.26X-8.48(R=0.72;P=0.03),Y=0.12X-6.89(R=0.86;P=0.003)和Y=0.07X-4.00(R=0.87;P=0.002),其中Feo及Fes与>0.25 mm水稳定性大团聚体数量达到极显著相关,说明尽管土壤中Feo及Fes含量远低于Fed,但更有助于形成大团聚体。土壤中氧化铝与>0.25 mm水稳定性大团聚体数量的关系如图 1所示,Ald、Alo及Als与>0.25 mm水稳定性大团聚体数量的线性关系分别为Y=0.13X-4.54(R=0.83;P=0.005),Y=0.05X-1.63(R=0.93;P < 0.001)和Y=0.03X-1.30(R=0.92;P < 0.001),均达到极显著的水平,以Alo及Als与>0.25 mm水稳定性大团聚体数量的相关系数R最高,显著性最佳,表明无定形和络合态氧化铝比游离结晶态氧化铝更有利于促进大团聚体的形成。与同一形态的氧化铁相比,氧化铝与>0.25 mm水稳定性大团聚体数量的相关系数R更高,且显著性水平更高,表明相对于含量较多氧化铁,含量相对较少氧化铝在促进大团聚体形成中的作用更为突出。
|
| 图 1 水稳定性大团聚体数量与铁铝氧化物的关系 Fig.1 Linear relationships of >0.25 mm water-stable macroaggregates and Fe and Al oxides |
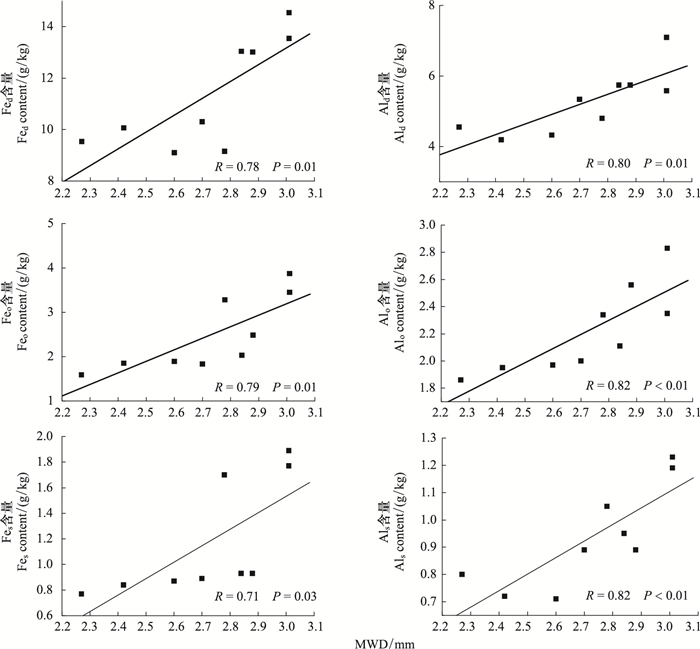
表征团聚体稳定性的平均重量直径(MWD)与不同形态铁铝氧化物的相关性均达到显著性水平,因氧化物的形态和类型有所差异(图 2)。如图 2所示,Fed、Feo及Fes与MWD的线性关系分别为Y=6.54X-6.44(R=0.78;P=0.01),Y=2.60X-4.62(R=0.79;P=0.01)和Y=1.29X-2.33(R=0.71;P=0.03),均达到显著性水平,以Feo相关系数R最高,表明土壤中Feo更有利于团聚体的稳定。土壤中氧化铝与MWD的关系如图 2所示,Ald、Alo及Als与MWD的线性关系分别为Y=2.68X-2.52(R=0.80;P=0.01),Y=1.04X-0.62(R=0.82;P < 0.01)和Y=0.61X-0.71(R=0.82;P < 0.01),除Ald与MWD的线性关系为显著水平外,Alo及Als与MWD的线性关系均达到极显著,说明无定形和络合态氧化铝更有利于团聚体的稳定。与同一形态的氧化铁相比,氧化铝与MWD的相关系数R更高,且显著性水平P更高,表明氧化铝更有助于团聚体的稳定。
|
| 图 2 MWD与铁铝氧化物的关系 Fig.2 Linear relationships of MWD and Fe and Al oxides |
氧化铁的形成与转化受温度、pH值、共存矿物等因素的影响,南方高温多雨,年降雨量多于蒸发量,土壤发育程度高,风化和淋溶作用强烈,因此在南方酸性及近中性的土壤条件下易形成结晶良好的赤铁矿[20]。吴金明等[21]对我国几种地带性土壤的无机胶体的研究指出红壤中氧化铁多以游离氧化铁的形式存在,本研究3种林分土壤均以游离结晶态氧化铁含量最高,与之相似,但与Qafoku[22]指出土壤中的氧化铁多以结构和成分不确定的弱结晶水铁矿的形式存在有所不同。不同林分>0.25 mm大团聚体数量及MWD值均呈现出米槠次生林>米槠人促林>杉木人工林,一方面这是因为人为干扰强度的增加,使土壤团聚体经常受到干扰,使受团聚体保护的土壤有机质暴露在外加快分解,而且也使团聚体稳定的胶结物质产生减少。如毛艳玲等[23]研究土地利用变化对团聚体稳定性及碳组分的影响指出,天然林开垦成果园及坡耕地后,>0.25 mm大团聚体数量及MWD均显著下降。同时,干扰的增加可能对土壤中无机胶结物质产生了一定的影响,从而影响了大团聚体的形成与稳定。黄丹丹等[24]发现游离态铁铝氧化物含量呈现出免耕地显著高于垄作地和秋翻地,非晶质铁铝也以免耕地含量最高,可能是对土壤的扰动加剧了土壤的淋溶作用和铁铝氧化物的转化,这有待进一步的研究。
一般认为,在土壤有机质含量较高且粘土矿物和铁铝氧化物含量较低时,土壤有机质的团聚作用占主导地位[4];而当有机质含量不高且粘土矿物和铁铝氧化物含量较高时,团聚体的形成主要靠粘粒的内聚力及铁铝氧化物的胶结作用[14, 25]。铁铝氧化物对团聚体稳定性的影响主要是通过三种机制:铁铝氧化物在溶液中充当絮凝剂;充当黏粒和有机分子的胶结剂;作为凝胶在黏粒表面沉淀[26]。然而不同形态铁铝氧化物结晶度[12]、比表面积[27]、官能团结构[28]、表面电荷[21]等特性的差异造成其胶结腐殖质[29]及黏土矿物[30]的能力各异,因而对土壤团聚体的作用的大小有所差别[31]。研究发现铁铝氧化物含量与>0.25 mm大团聚体数量及MWD值间显著的相关性表明不同形态的铁铝氧化物均有助于大团聚体的形成及稳定,这与Moghimi等[32]的研究结果一致。胡国成等[15]发现经DCB去除游离氧化铁后,砖红壤粘粒( < 2 μm)含量明显增加,而2000—250 μm颗粒含量下降了6.63倍;Peng等[33]发现经DCB及AAO溶液处理后,CK处理0.25—2 mm大团聚体分别下降了4.94和4.09倍,0.053—0.25 mm微团聚体分别下降了4.98和4.17倍。一方面土壤中的铁铝氧化物作为键桥将粘粒结合,提高胶结强度,产生稳定而不可分散的团聚体[34]。另一方面铁铝氧化物可呈胶膜状包被在黏土颗粒表面,其由溶胶转化为凝胶时可将土壤胶结在一起,凝胶干燥脱水后形成的团聚体具有相当的水稳定性[10]。对比不同形态氧化铁与氧化铝与>0.25 mm大团聚体及MWD值相关性发现,氧化铝与>0.25 mm大团聚体及MWD值的相关系数R更高及P更显著,表明氧化铝对黏土矿物及腐殖质的胶结作用可能强于氧化铁,更有助于大团聚体的形成及稳定。这与氧化铝在土壤中的形态[10]、表面电荷密度[35]等有关。Schulten等[35]依照静电学原理计算得出Al3+离子电荷/半径的比率大于Fe3+,指出氧化铝对胡敏酸和富里酸的吸附能力强于氧化铁。魏世勇等[11]指出Al、Fe电负性分别为1.61、1.83,与腐殖酸的配位交换反应的能力Al2O3 >Fe2O3。张琪等[10]指出氢氧化铝难以分散,当土壤和粘粒含有表面积很大的氢氧化铝时,就能产生稳定的团聚体。Barthès等[36]发现热带低活性黏质土壤中稳定性大团聚体与DCB法和AAO法提取的铁铝氧化物呈极显著相关性,但与氧化铝的相关系数R和显著性P值更高。
尽管有研究指出晶质氧化铁常与黏土矿物结合,这种复合物的形成可提高土壤团聚体的稳定性,图 1和图 2亦得到证实,但与游离态铁铝氧化物相比,无定形态及络合态的铁铝氧化物更能促进大团聚体的形成与稳定。无定形氧化铁是氧化铁中活性羟基的主要贡献者,羟基的释放量最高,而羟基作为金属离子配位体,可以与F-离子或其他配位体发生交换进入土壤溶液中充当絮凝剂[11]。Diuker等[31]通过线性拟合发现,Feo与>0.25 mm大团聚体数量及MWD值呈极显著线性相关,却并未观察到Fed与>0.25 mm大团聚体数量及MWD值的相关性。无定形铁铝氧化物具有更大的表面积,更高的表面活性,尽管含量相对较低,但胶结能力更强。Barberis等[36]指出,针铁矿(无定形氧化铁)表面带有较多的羟基,更易与高岭石等黏土矿物结合,其胶结能力强于赤铁矿(晶质氧化铁)。Fes、Als与>0.25 mm大团聚体数量及MWD值相关性亦达到显著性水平(图 1,图 2),这可能与络合态铁铝氧化物的特性有关,其本身即是铁铝氧化物与有机质的胶结[29],铁铝氧化物与多功能团有机络合物的结合可作为土壤颗粒团聚的稳定剂,形成的粘粒-多价金属-有机质复合体提高了团聚体稳定性[5]。有机络合物强烈地吸附在铁铝氧化物沉淀产物的表面,并嵌入这些矿物胶体的网络结构中[37],有机物获得“空间隔离”保护不易分解,而且有机物占据铁铝氧化物的配位键可干扰铁铝氧化物的形态转化,阻碍铁铝氧化物的结晶作用。
4 结论(1)3种林分土壤铁铝氧化物含量均呈现出游离结晶态(Fed、Ald)>>无定形(Feo、Alo)>络合态(Fes、Als),米槠次生林>米槠人工林>杉木人工林。
(2)>0.25 mm水稳定性大团聚体数量以米槠次生林最高,杉木人工林最低,3种林分差异显著,MWD值趋势与之相似,但米槠次生林与米槠人工林无显著差异。
(3)不同形态铁铝氧化物与>0.25 mm水稳定性大团聚体数量及MWD值均显著甚至极显著相关,表明铁铝氧化物促进了大团聚体的形成与稳定;氧化铝与>0.25 mm水稳定性大团聚体数量及MWD值的相关系数R及P更佳表明氧化铝更有利于团聚体的形成与稳定;与游离结晶态铁铝氧化物相比,无定形及络合态铁铝氧化物与>0.25 mm水稳定性大团聚体数量及MWD值的更高的相关系数R及显著性P表明无定形及络合态铁铝氧化物对团聚体的作用更大。
| [1] | 史奕, 陈欣, 闻大中. 东北黑土团聚体水稳定性研究进展. 中国生态农业学报, 2005, 13(4): 95-98. |
| [2] | Kodešová R, Kočárek M, Kodeš V, imůnek J, Kozák J. Impact of soil micromorphological features on water flow and herbicide transport in soils. Vadose Zone Journal, 2008, 7(2): 798-809. |
| [3] | 窦森, 李凯. 土壤团聚体中有机质研究进展土壤团聚体中有机质研究进展. 土壤学报, 2011, 48(2): 412-418. |
| [4] | Six J, Elliott E T, Paustian K. Soil macroaggregate turnover and microaggregate formation: a mechanism for C sequestration under no-tillage agriculture. Soil Biology and Biochemistry, 2000, 32(14): 2099-2103. |
| [5] | 魏朝富, 谢德体, 李保国. 土壤有机无机复合体的研究进展. 地球科学进展, 2003, 18(2): 221-227. |
| [6] | Goldberg S. Interaction of aluminum and iron oxides and clay minerals and their effect on soil physical properties: a review. Soil Science, 1989, 20(11/12): 1181-1207. |
| [7] | Kleber M, Sollins P, Sutton R. A conceptual model of organo-mineral interactions in soils: self-assembly of organic molecular fragments into zonal structures on mineral surfaces. Biogeochemistry, 2007, 85(1): 9-24. |
| [8] | 魏世勇, 谭文峰, 刘凡. 土壤腐殖质-矿物质交互作用的机制及研究进展. 中国土壤与肥料, 2009, (1): 1-6. |
| [9] | Bronick C J, Lal R. Soil structure and management: a review. Geoderma, 2005, 124(1): 3-22. |
| [10] | 张琪, 方海兰, 史志华, 李朝霞, 蔡崇法. 侵蚀条件下土壤性质对团聚体稳定性影响的研究进展. 林业科学, 2007, 43(S1): 77-82. |
| [11] | Hou T, Xu R K, Tiwari D, Zhao A Z. Interaction between electrical double layers of soil colloids and Fe/Al oxides in suspensions. Journal of Colloid and Interface Science, 2007, 310(2): 670-674. |
| [12] | 魏世勇, 刘茜, 刘凡, 冯雄汉, 谭文峰. Fe (Ⅱ) 存在条件下氧化铁-高岭石复合物的形成与转化. 土壤学报, 2010, 47(6): 1134-1143. |
| [13] | 魏世勇, 刘凡, 冯雄汉, 谭文峰. 针铁矿-高岭石二元体的微观结构与形成机制. 土壤学报, 2011, 48(2): 320-330. |
| [14] | 章明奎, 何振立. 成土母质对土壤团聚体形成的影响. 热带亚热带土壤科学, 1997, 6(3): 198-202. |
| [15] | 胡国成, 章明奎. 氧化铁对土粒强胶结作用的矿物学证据. 土壤通报, 2002, 33(1): 25-27. |
| [16] | Six J, Elliott E T, Paustian K, Doran J W. Aggregation and soil organic matter accumulation in cultivated and native grassland soils. Soil Science Society of America Journal, 1998, 62(5): 1367-1377. |
| [17] | Denef K, Six J, Merckx R, Paustian K. Short-term effects of biological and physical forces on aggregate formation in soils with different clay mineralogy. Plant and Soil, 2002, 246(2): 185-200. |
| [18] | Lu R K. Soil Agricultural Chemical Analysis Method. Beijing: China Agriculture Science and Technique Press, 1999: 60-71. |
| [19] | 郑子成, 李廷轩,张锡洲,王永东,杨玉梅,汪曦微. 不同土地利用方式下土壤团聚体的组成及稳定性研究. 水土保持学报, 2009, 23(5): 228-231, 236-236. |
| [20] | Cudennec Y, Lecerf A. The transformation of ferrihydrite into goethite or hematite, revisited. Journal of Solid State Chemistry, 2006, 179(3): 716-722. |
| [21] | 吴金明, 刘永红, 李学垣, 凌婉婷, 董元彦. 我国几种地带性土壤无机胶体的表面电荷特性. 土壤学报, 2002, 39(2): 177-183. |
| [22] | Qafoku N P. Chapter two-terrestrial nanoparticles and their controls on soil-/geo-processes and reactions. Advances in Agronomy, 2010, 107: 33-91. |
| [23] | 毛艳玲, 杨玉盛, 刑世和, 陈光水, 崔纪超. 土地利用方式对土壤水稳性团聚体有机碳的影响. 水土保持学报, 2008, 22(4): 132-137. |
| [24] | 黄丹丹. 不同耕作方式下黑土团聚体及胶结物质组成的研究[D]. 长春: 吉林农业大学资源与环境学院, 2012: 27-29. |
| [25] | Oades J M, Waters A G. Aggregate hierarchy in soils. Soil Research, 1991, 29(6): 815-828. |
| [26] | 谭文峰, 周素珍, 刘凡, 冯雄汉, 李学垣. 土壤中铁铝氧化物与黏土矿物交互作用的研究进展. 土壤, 2007, 39(5): 726-730. |
| [27] | Pronk G J, Heister K, Kögel-Knabner I. Iron oxides as major available interface component in loamy arable topsoils. Soil Science Society of America Journal, 2011, 75(6): 2158-2168. |
| [28] | 徐建民, 赛夫, 袁可能. 土壤有机矿质复合体研究Ⅸ. 钙键复合体和铁铝键复合体中腐殖质的性状特征. 土壤学报, 1999, 36(2): 168-178. |
| [29] | 付庆灵, 邓雅丽, 胡红青, 蔚霞, 韩晓芳, 李妍. 南方主要土壤中铁铝氧化物对土壤吸附Bt蛋白的影响. 中国农业科学, 2012, 45(23): 4836-4843. |
| [30] | 张先伟, 孔令伟. 2014 氧化铁胶体与黏土矿物的交互作用及其对黏土土性影响. 岩土工程学报, 2014, 36(1): 65-74. |
| [31] | Duiker S W, Rhoton F E, Torrent J, Smeck N E, Lal R. Iron (hydr) oxide crystallinity effects on soil aggregation. Soil Science Society of America Journal, 2003, 67(2): 606-611. |
| [32] | Moghimi A H, Hamdan J, Shamshuddin J, Samsuri A W, Abtahi A. Mineralogy and aggregate stability of soils in the arid region of Southeastern Iran. African Journal of Agricultural Research, 2012, 7(11): 1639-1649. |
| [33] | Peng X, Yan X, Zhou H,Zhang Y Z, Sun H. Assessing the contributions of sesquioxides and soil organic matter to aggregation in an Ultisol under long-term fertilization. Soil and Tillage Research, 2015, 146: 89-98. |
| [34] | Sung C T B. Aggregate Stability of Tropical Soils in relation to their organic matter constituents and other soil properties. Pertanika Journal ofTropical Agricultural Science, 2012, 35(1): 135-148. |
| [35] | Schulten H R, Leinweber P. New insights into organic-mineral particles: composition, properties and models of molecular structure. Biology and Fertility of Soils, 2000, 30(5/6): 399-432. |
| [36] | Barthès B G, Kouakoua E, Larré-Larrouy M C, Razafimbelo T M, de Luca E F, Azontonde A, Neves C S V J, de Freitas P L, Feller C L. Texture and sesquioxide effects on water-stable aggregates and organic matter in some tropical soils. Geoderma, 2008, 143(1/2): 14-25. |
| [37] | Greathouse J A, Johnson K L, Greenwell H C. Interaction of natural organic matter with layered minerals: recent developments in computational methods at the nanoscale. Minerals, 2014, 4(2): 519-540. |
 2016, Vol. 36
2016, Vol. 36




