文章信息
- 赵红梅, 赵文岩, 胡瑞生
- ZHAO Hongmei, ZHAO Wenyan, HU Ruisheng
- 表面活性剂对链霉素在内蒙古牧区土壤中吸附解吸的影响
- Effect of surfactants on sorption and desorption of streptomycin on soil of Inner Mongolian pastoral area
- 生态学报, 2014, 34(16): 4549-4554
- Acta Ecologica Sinica, 2014, 34(16): 4549-4554
- http://dx.doi.org/10.5846/stxb201212271881
-
文章历史
- 收稿日期:2012-12-27
人类排放的生活、医疗和工业废水中含有大量的表面活性剂和有机物,通过各种途径进入土壤/沉积物环境后,不仅会造成环境的有机复合污染,同时表面活性剂对共存的有机污染物的吸附/解吸行为也会产生强烈的影响[1, 2, 3],链霉素属于离子型极性有机化合物,它属于氨基糖甙碱性类抗生素,起到了干扰结核杆菌蛋白质合成的作用,从而杀灭或者抑制结核杆菌生长的作用。链霉素兽药在内蒙古牧区使用比较广泛,而且体内代谢率低(10%—40%)。目前,表面活性剂对亲水性抗生素在土壤表面吸附 / 解吸的影响报道较少,鉴于此本研究以土壤和链霉素为对象,选择了3种表面活性剂,分析不同类型表面活性剂对链霉素在内蒙古牧区土壤中吸附解吸特征的影响。
1 材料与方法 1.1 土壤样品土样采自内蒙古呼和浩特近郊的表层土壤(0—30cm)作为实验中的土壤样品,采样方法参照土壤环境监测技术规范中的相关步骤进行 (HJ/T 166—2004)。土壤去除碎石、败叶等杂物,在空气中自然风干,样品用研钵捣碎研细、过80目孔径筛,备用。按经典方法分析土壤理化性质. 各土壤样品的理化性质如表 1所示。
| 土壤采集点 Sampling locations | 有机质/% Organic material | 阳离子交换量/(cmol/kg) Cation exchange capacity | pH | 机械组成Mechanical components/(g/ kg) | ||
| 砂粒Sand | 粉粒Silt | 粘粒Clay | ||||
| 呼和浩特近郊 Inner Mongolia pastoral area | 2.5 | 11.0 | 7.9 | 76.00 | 11.00 | 13.00 |
实验中所使用的链霉素(STR,纯度 >90%)为Bgm Schlosser Str.生产(德国),链霉素在25℃的溶解度为20g/L,阳离子表面活性剂 CTAB、阴离子表面活性剂SDBS和非离子表面活性剂TX-100为分析纯,其理化性质如表 2所示[4, 5]。将链霉素用去离子水配制成100μg/mL溶液备用。表面活性剂SDBS、CTAB 和TX-100用去离子水分别配制成0,0.1,1 和5倍临界胶束浓度的系列溶液(下分别简述为0、 0.1CMC、1CMC 、和 5CMC)。
| 表面活性剂 Surfactant | 分子式 Chemical structure | 相对分子质量 Molecular weight | 临界胶束浓度 Critical micelle concentration/ (mg /L) | 亲水亲油平衡系数 hydrophilic-lipophilic balance | 类型 Nature |
| 十六烷基三甲基溴化铵CTAB | C19 H42 BrN | 364 | 335 | 15.8 | 阳离子型 |
| 十二烷基苯磺酸钠SDBS | C18H29Na3OS | 348 | 418 | 11.0 | 阴离子型 |
| 曲拉通100 TX100 | C8H17C6H4O(OCH2CH2)9.5H | 625 | 181 | 13.5 | 非离子型 |
(1)吸附实验 分别取适量的土壤样品和一系列不同浓度的链霉素溶液(5、10、15、20、25、30、35、40 μg/L)放入 50 mL聚四氟乙烯离心管(带Teflon盖子)中,加入0. 0 1 mol ·L-1CaCl2溶液调节溶液的离子强度,加入200 mg/L NaN3抑制微生物的生长[6, 7],控制固液比(1g ∶ 10mL),密封后置于振荡器中于25℃下恒温避光振荡24h[8],取上清液用0.45μm的尼龙滤膜过滤,测定上清液中链霉素的浓度,每组实验做2组平行实验,并做不加吸附剂的空白对照实验,测定链霉素的回收率。实验结果表明,添加不同浓度的链霉素,测得的回收率均在95%以上,所以实验过程中由容器壁造成的损失可忽略不计。链霉素的吸附量用原始溶液浓度与平衡后水相浓度的差计算求得,表面活性剂对链霉素在土壤中吸附解吸的影响实验中,SDBS、CTAB和TX-100的添加浓度分别为0. 1CMC、1CMC 、和 5CMC。
(2)解吸实验 分别取适量的土壤样品和一系列不同浓度的链霉素溶液(5—40mg/L)放入 50 mL聚四氟乙烯离心管(带Teflon盖子)中,加入相同体积的链霉素,控制固液比(1g ∶ 20mL),密封后置于振荡器中于25℃下恒温避光振荡24h,取上清液用0.45μm的尼龙滤膜过滤,倒掉上层清液用相同体积不含链霉素的表面活性剂溶液替换,其他条件同吸附实验,恒温(25℃避光振荡24h,平衡后4000 r/min离心分离,取上清液用0. 45μ m尼龙滤膜过滤,测定上清液中链霉素的浓度,以上过程重复 3 次.
1.4 分析检测和数据处理链霉素的测定采用高效液相色谱法,取10mL上清液,加1mL 0.01mol/L NaOH溶液,在60℃水浴下加热30min,冷却至室温,再加0.5mL,0.1%的硫酸铁胺使链霉素发生麦芽酚反应,以便于紫外检测。实验所用仪器为美国Thermo Eleotron Corporation,检测器为FINNIGAN SURVEYOR PDA plus detector检测器,色谱柱采用Thermo Scientific 31605型C18 反相色谱柱 (4. 6 mm × 250 mm); 流动相为乙腈 ∶ 水 =20 ∶ 80;流动相流速为 1 mL/min,进样量为10μL,实验测得链霉素保留时间为5.32min。本研究的吸附解吸数据用 Freundlich 吸附方程拟合:
Cs= Kf ·Cen
式中,Ce为液相平衡浓度(mg/L),Cs为固相吸附量(mg/L),Kf为 Freundlich吸附能力参数[(mg/kg-1)/(mg/L-1)n)],n为吸附等温线的非线性因子。土壤对STR的解吸滞后性可用解吸滞后指数(HI)来表示:
HI=ndes/nads
式中,ndes和nads分别为吸附和解吸过程的非线性指数。
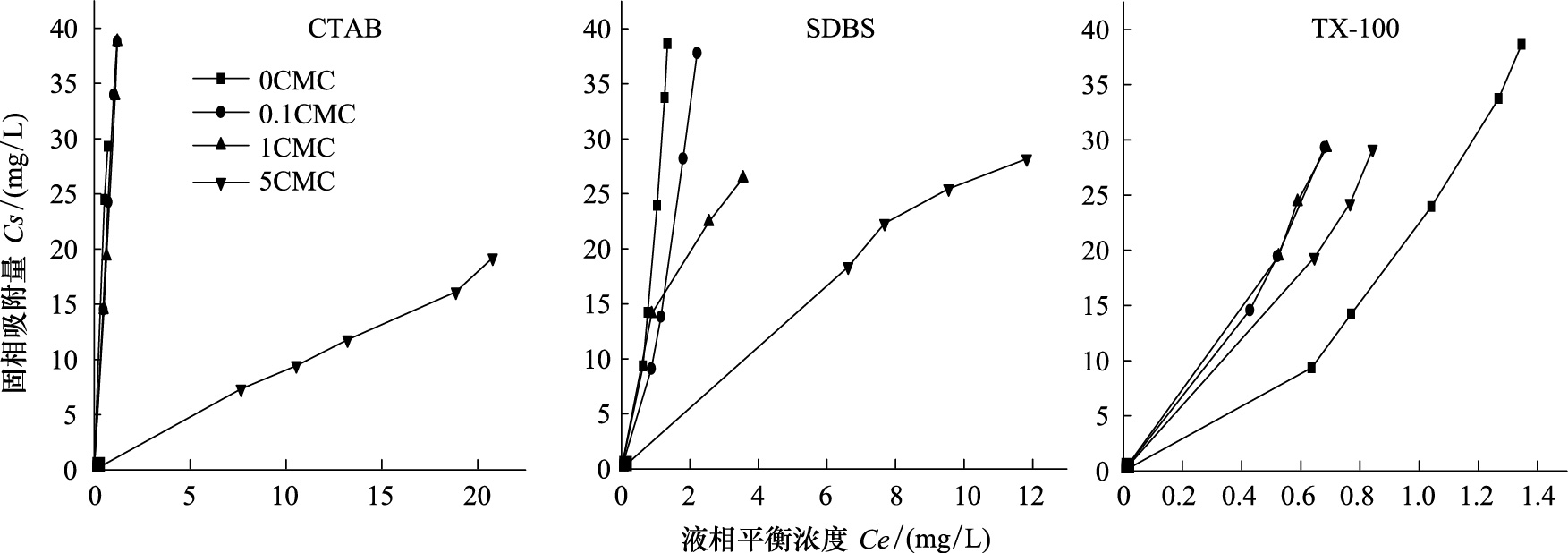
2 结果与讨论 2.1 表面活性剂对链霉素在土壤表面吸附特征的影响在CTAB、SDBS和 TX100存在的情况下,链霉素在土壤表面的吸附/解吸等温线如图 1所示.Freundlich方程对链霉素的吸附/解吸数据的拟合效果较好,拟合参数见表 3。表 3表明,CTAB、SDBS和TX100的存在均增加了土壤对STR吸附等温线的线性程度。当CTAB、SDBS和TX100的浓度从0CMC升高到5CMC时,STR的吸附线性因子n值分别从1.845降低到0.941 、1.514 和0.707。有机物在土壤中的吸附是有机污染物在土壤有机质和水两相的分配过程及污染物在土壤颗粒表面的吸附过程,而分配过程更倾向于线性吸附[9]。在不同类型的表面活性剂影响下,土壤对STR的吸附特性发生了一定的变化。由图 1可知,STR的吸附等温线接近线性模型。Nadeem 等[10]曾报道用表面活性剂改性过的土壤具有更大的比表面积、孔径和孔体积,使土壤对有机污染物更具有亲和力,并可以给有机污染物提供更多的吸附位点。不同类型表面活性剂对STR在土壤表面吸附/解吸行为的影响差别较大,这主要取决于它们的化学结构、临界胶束浓度和添加浓度。从图 1可以看出,非离子表面活性剂TX-100能够促进土壤对STR的吸附。但是随着TX-100浓度添加的不同,其促进作用也不同。TX-100在低浓度时(0.1CMC和1CMC)下,能够促进STR在土壤上的吸附,Kd值从22.3分别增大到38.19和40.4。随着 TX-100的浓度增加到5CMC,TX100 对STR的吸附表现出抑制作用,Kd值降低到32.07。与TX-100正好相反,阴离子表面活性剂SDBS和阳离子表面活性剂CTAB的存在抑制了STR在土壤表面的吸附(图 1)。当 SDBS 的浓度从0CMC增加到0.1CMC、1 CMC 、5 CMC时,Kd 值分别从22.3降低到13.75、10.71和2.68。当 CTAB 的浓度从0CMC增加到0.1CMC、1 CMC 、5 CMC时,Kd 值分别从22.3降低到22.2、21.9、0.91。这说明土壤对STR的吸附能力随着SDBS、CTAB添加浓度的增大而减小。
|
| 图 1 在CTAB、SDBS和TX-100存在下,链霉素在土壤中的吸附等温线 Fig. 1 Sorption isotherms of STR on soil in the presence of CTAB,SDBS and TX-100 |
在STR、表面活性剂、土壤和水共存的体系中主要存在以下 4 种作用:①表面活性剂与STR在土壤表面的竞争吸附作用:②不同形态表面活性剂(单体、胶束和半胶束)之间的平衡作用;③STR在表面活性剂单体和胶束中的分配作用;④吸附在土壤中的半胶束对STR的吸附作用[11, 12]。土壤对STR的吸附是这4 种作用共同作用的结果。因此,CTAB 、SDBS 和 TX100 对STR在土壤吸附/解吸的不同影响主要取决于表面活性剂在土壤中的吸附作用以及它们对STR的增溶作用。以下讨论造成这种差异的原因。
表中Ce为液相平衡浓度(mg/L),Cs为固相吸附量(mg/L),表面活性剂在土壤表面的吸附机制主要包括以下 5 种作用:离子交换、疏水键结合、氢键结合、离散力和静电吸引作用[13]。CTAB抑制STR在土壤中的吸附这主要是因为CTAB分子中的亲水性基团[(CH3)3 NR]+由于带正电荷,通过静电吸引作用更容易吸附在带负电荷的土壤中[14],吸附在土壤中的CTAB可形成半胶束,从而占据了带正电荷的STR在土壤中的吸附位点,CTAB分子与STR在土壤中的这种竞争吸附作用最终降低了STR在土壤中的吸附量。阴离子表面活性剂SDBS由于带负电荷,在土壤中的吸附能力远远低于CTAB,这使得SDBS分子与STR在土壤中的竞争吸附作用明显降低,。但是,由于SDBS 的存在很大程度上增加了带正电荷的STR在水中的溶解度。最终,SDBS对STR的这种强增溶作用降低了STR在土壤中的吸附量。与CTAB和SDBS不同,低浓度非离子表面活性剂 TX-100(<5CMC),由于其在土壤中的吸附作用。吸附态TX-100对STR的分配作用最终导致STR的吸附量增加。随着TX-100的浓度增加到5CMC时,高浓度的TX-100能够抑制STR在土壤中的吸附主要是由于TX-100对STR的强增溶作用[15]。
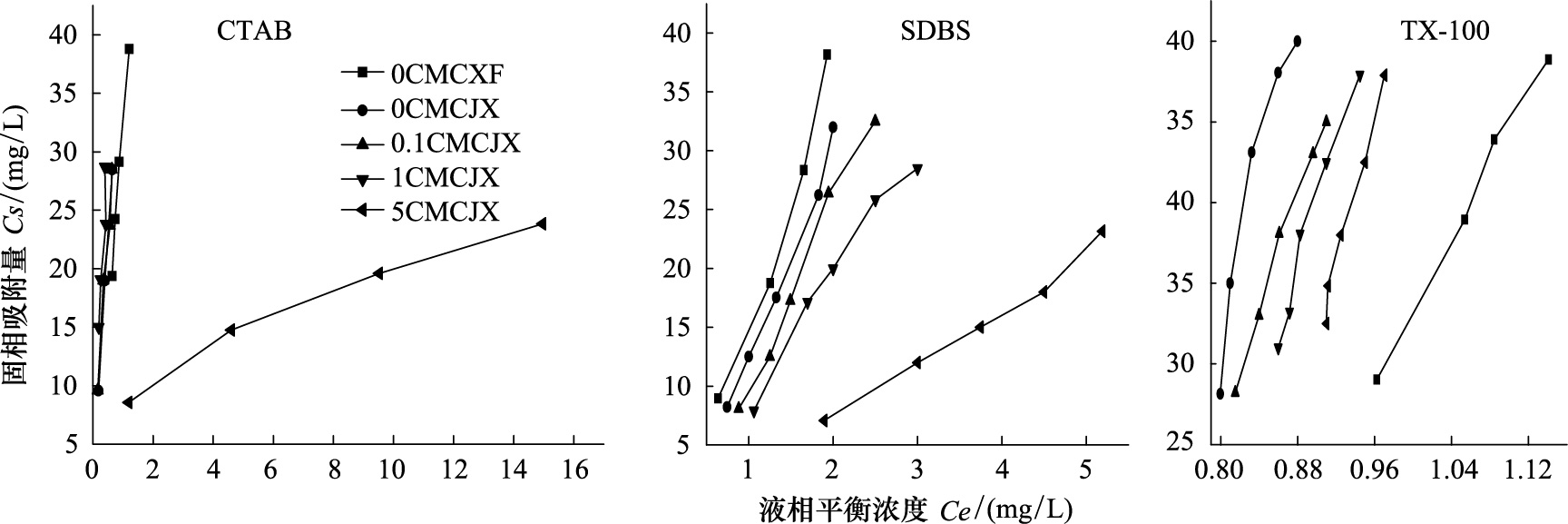
2.2 表面活性剂对STR解吸滞后性的影响图 2中显示了3种表面活性剂TX-100、SDBS及CTAB对污染土壤中链霉素解吸作用的影响结果。在3种表面活性剂的存在下,土壤对STR的解吸滞后指数如表 3所示。滞后指数是吸附不可逆程度的量化指标。当HI接近1时,解吸速率和吸附速率接近,其吸附和解吸附等温线重合,说明吸附过程是可逆的;当HI< 1 时,解吸速率小于吸附速率,说明存在滞后作用,吸附过程是不可逆的[16]。当HI> 1 时,解吸速率大于吸附速率,说明不存在滞后作用[17]。相当于相同的时间里解吸下来的STR要比吸附上的快。从表 2可以看出,STR在土壤中的滞后指数HI =0.594,说明吸附是完全不可逆的,并且CTAB、SDBS和TX100的存在强烈响了STR的解吸滞后性。SDBS和TX100的存在在很大程度上增加了STR在土壤中的吸附可逆性,并且吸附可逆程度随着SDBS和TX100浓度的升高而升高。 随着SDBS和TX100浓度的增加,滞后指数最高分别可升高到3.055和4.236。这是因为SDBS、TX100对STR的增溶作用促使STR从土壤相进入水相中。与SDBS和TX100不同,CTAB 的存在在很大程度上增加了STR在土壤中解吸的滞后性。但是,当CTAB的浓度从0CMC增加到0.1CMC和1CMC时,)滞后指数HI分别从0.594增加到0.649和0.776。但是,当CTAB的浓度增加到5CMC时,滞后指数又降低到了0.428。这说明随着溶液中CTAB浓度的增加,STR更难从土壤中解吸下来,这主要是由于CTAB更易吸附到带负电的土壤上而STR可以分配到吸附态CTAB中。Parker 等[18]也曾报道吸附态的表面活性剂较天然沉积物有机质对有机污染物的吸附能力更强,从而可以抑制有机污染物的解吸。
|
| 图 2 在CTAB、SDBS和TX-100存在下,链霉素在土壤中的解吸等温线 Fig. 2 Desorption isotherms of STR on soil in the presence of CTAB,SDBS and TX-100 |
| 项目 Item | 表面活性剂浓度 Concentration of surfactants (CMC) | n | Kf | lgKf | R2 | Kd | |
| 吸附Adsorption | 对照 | 0 | 1.845 | 1.5237 | 0.1829 | 0.9997 | 22.3 |
| CTAB | 0.1 | 0.995 | 32.961 | 1.518 | 0.9958 | 22.2 | |
| 1 | 0.998 | 31.182 | 1.4939 | 0.9986 | 21.9 | ||
| 5 | 0.941 | 1.053 | 0.0224 | 0.9927 | 0.91 | ||
| TX100 | 0.1 | 1.508 | 52.3480 | 1.7189 | 0.9999 | 38.19 | |
| 1 | 1.498 | 52.1795 | 1.7175 | 0.98 | 40.4 | ||
| 5 | 1.514 | 37.1877 | 1.5704 | 0.9877 | 32.07 | ||
| SDBS | 0.1 | 1.559 | 11.0739 | 1.0443 | 0.9997 | 13.75 | |
| 1 | 0.449 | 14.8594 | 1.172 | 0.9994 | 10.71 | ||
| 5 | 0.707 | 5.0396 | 0.7024 | 0.9947 | 2.68 | ||
| 项目 Item | 表面活性剂浓度 Concentration of surfactants (CMC) | n | Kf | lgKf | R2 | Kd | |
| 解吸Desorption | 对照 | 0 | 1.096 | 12.218 | 1.087 | 0.9958 | 0.594038 |
| CTAB | 0.1 | 0.7726 | 39.409 | 1.5956 | 0.9836 | 0.776482 | |
| 1 | 0.6482 | 45.646 | 1.6594 | 0.9960 | 0.649499 | ||
| 5 | 0.4029 | 7.9616 | 0.901 | 0.9998 | 0.428162 | ||
| TX-100 | 0.1 | 6.3884 | 68.897 | 1.8382 | 0.9721 | 4.23634 | |
| 1 | 5.512 | 52.3359 | 1.7188 | 0.939 | 3.679573 | ||
| 5 | 5.8277 | 44.9056 | 1.6523 | 0.9946 | 3.849207 | ||
| SDBS | 0.1 | 1.483 | 9.7118 | 0.9873 | 0.9992 | 0.951251 | |
| 1 | 1.3721 | 7.8487 | 0.8948 | 0.9595 | 3.055902 | ||
| 5 | 1.1664 | 3.3197 | 0.5211 | 0.9978 | 1.649788 |
(1)阳离子表面活性剂CTAB、阴离子表面活性SDBS和非离子表面活性剂 TX100的存在均增加了土壤对STR吸附等温线的线性程度。
(2)CTAB 的存在可以抑制STR在土壤表面的吸附同时抑制了STR的解吸。SDBS 的存在降低了STR在土壤中的吸附量并增加了吸附过程的可逆性。TX-100对STR在土壤中的吸附的影响取决于其添加浓度。低浓度的TX-100对STR的吸附促进作用大于高浓度。
| [1] | Rodriguez-Cruz M S, Sanchez-Martin M J, Sanchez-Camazano M. Surfactant-enhanced desorption of atrazine and linuron residues as affected by aging of herbicides in soil. Archives of Environmental Contamination and Toxicology, 2006, 50(1): 128-137. |
| [2] | Zhang J H, Zeng J H. Adsorption of toluene and naphthalene on Beijing soils and its influence factor. Environmental Science, 2006, 27(9): 1889-1894. |
| [3] | Zhang J H, Zeng J H. Influence of surfactant on sorption of diesel oil on soils. Environmental Chemistry, 2007, 26(5): 610-613. |
| [4] | Shen X Y, Sun Y L, Ma Z Y, Zhang P, Zhang C L, Zhu L Z. Effects of mixed surfactants on the volatilization of naphthalene from aqueous solutions. Journal of Hazardous Materials, 2007, 140(1/2): 187-193. |
| [5] | Pan G, Jia C X, Zhao D Y, You C, Chen H, Jiang G B. Effect of cationic and anionic surfactants on the sorption and desorption of perfluorooctane sulfonate (PFOS) on natural sediments. Environmental Pollution, 2009, 157(1): 325-330. |
| [6] | Cornelissen G, Gustafsson Ö. Sorption of phenanthrene to environmental black carbon in sediment with and without organic matter and native sorbates. Environmental Science and Technology, 2004, 38(1): 148-155. |
| [7] | Wen B, Zhang J J, Zhang S Z, Shan X Q, Khan S U, Xing B S. Phenanthrene sorption to soil humic acid and different humin fractions. Environmental Science and Technology, 2007, 41(9): 3165-3171. |
| [8] | Fytianos K, Voudrias E, Papamichali A. Behavior and fate of linear alkylbenzene sulfonate in different soils. Chemosphere, 1998, 36(13): 2741-2746. |
| [9] | Si Y B, Zhou J, Wang X X, Zhou D M. Adsorption of bensulfuron-methyl in soils. Environmental Science, 2003, 24(3): 122-125. |
| [10] | Nadeem M, Shabbir M, Abdullah M A, Shan S S, McKay G. Sorption of cadmium from aqueous solution by surfactant-modified carbon adsorbents. Chemical Engineering Journal, 2009, 148(2/3): 365-370. |
| [11] | Jafvert C T. Sediment- and saturated-soil-associated reactions involving an anionic surfactant (dodecyl sulfate). 2. partition of PAH compounds among phases. Environmental Science and Technology, 1991, 25(6): 1039-1045. |
| [12] | Liu Z B, Laha S, Luthy R G. Surfactant solubilization of polycyclic aromatic hydrocarbon compounds in soil-water suspensions. Water Science and Technology, 1991, 23(1/3): 475-485. |
| [13] | Cheremisinoff P N, Ellerbusch F. Carbon Adsorption Handbook. Michigan: Ann Arbor Science Publishers, 1978: 241-279. |
| [14] | Langley L A, Villanueva D E, Fairbrother D H. Quantification of surface oxides on carbonaceous materials. Chemistry of Materials, 2006, 18(1): 169-178. |
| [15] | Zhang J H, Cheng C R, Zhang W H, Li G Z. Effect of surfactants on sorption and desorption of benzo pyrene onto black carbon. Environmental Science, 2012, 33(5): 1639-1645. |
| [16] | Pusino A, Pinna M V, Gessa C. Azimsulfuron sorption-desorption on soil. Journal of Agricultural and Food Chemistry, 2004, 52(11): 3462-3466. |
| [17] | Zhang J Q, Dong Y H. Adsorption and desorption of norfloxacin on four typical soils in China. Environmental Science, 2007, 28(9): 2134-2140. |
| [18] | Parker S K, Bielefeldt A R. Aqueous chemistry and interactive effects on non-ionic surfactant and pentachlorophenol sorption to soil. Water Research, 2003, 37(19): 4663-4672. |
| [1] | 朱兆良. 农田中氮肥的损失与对策. 土壤与环境, 2000, 9(1): 1-6. |
| [6] | 陈德章, 王明星, 上官行健, 黄俊, Rasmussen R A, Khalili M K A. 我国西南地区的稻田CH4排放. 地球科学进展, 1993, 8(5): 47-54. |
| [8] | 丁维新, 蔡祖聪. 氮肥对土壤甲烷产生的影响. 农业环境科学学报, 2003, 22(3): 380-383. |
| [12] | 谢春生, 唐拴虎, 徐培智, 张发宝, 陈建生. 一次性施用控释肥对水稻植株生长及产量的影响. 植物营养与肥料学报, 2006, 12(2): 177-182. |
| [14] | 郑圣先, 聂军, 戴平安, 郑颖俊. 控释氮肥对杂交水稻生育后期根系形态生理特征和衰老的影响. 植物营养与肥料学报, 2006, 12(2): 188-194. |
| [15] | 李方敏, 樊小林, 陈文东. 控释肥对水稻产量和氮肥利用效率的影响. 植物营养与肥料学报, 2005, 11(4): 494-500. |
| [17] | 聂军, 郑圣先, 戴平安, 肖剑, 易国英. 控释氮肥调控水稻光合功能和叶片衰老的生理基础. 中国水稻科学, 2005, 19(3): 255-261. |
| [22] | 梁建生, 曹显祖, 张海燕, 宋平, 朱庆森. 水稻籽粒灌浆期间茎鞘贮存物质含量变化及其影响因素研究. 中国水稻科学, 1994, 8(3): 151-156. |
| [24] | 余柳青, 渠开山, 周勇军, 李迪, 刘小川, 张朝贤, 彭于发. 抗除草剂转基因水稻对稻田杂草种群的影响. 中国水稻科学, 2005, 19(1): 68-73. |
| [25] | 李奕林. 水稻根系通气组织与根系泌氧及根际硝化作用的关系. 生态学报, 2012, 32(7): 2066-2074. |
 2014, Vol. 34
2014, Vol. 34




