文章信息
- 丘清燕, 姚快乐, 刘骏, 葛志强, 许文斌, 刘红晓, 胡亚林
- QIU Qingyan, YAO Kuaile, LIU Jun, GE Zhiqiang, XU Wenbin, LIU Hongxiao, HU Yalin
- 易分解有机碳对不同恢复年限森林土壤激发效应的影响
- Effects of labile organic carbon input on the priming effect along an ecological restoration gradient
- 生态学报. 2019, 39(13): 4855-4864
- Acta Ecologica Sinica. 2019, 39(13): 4855-4864
- http://dx.doi.org/10.5846/stxb201805040995
-
文章历史
- 收稿日期: 2018-05-04
- 网络出版日期: 2019-04-17
2. 中国科学院华南植物园, 中国科学院退化生态系统植被恢复与管理重点实验室, 广州 510650
2. Key Laboratory of Vegetation Restoration and Management of Degraded Ecosystems, Chinese Academy of Sciences, Guangzhou 510650, China
土壤有机碳库是陆地生态系统最大的碳库, 其微小的改变都将引起大气中CO2浓度的急剧改变[1]。外源易分解有机物的输入可以加快或减缓原有土壤有机碳(SOC)的矿化, 即形成正或负激发效应[2]。当前大量的研究表明, 易分解有机物添加加快原有土壤有机碳的分解(即, 产生正激发效应)[3-5], 但也有些研究结果显示易分解有机物对土壤有机碳分解没有影响[6]或是减缓土壤有机碳分解(即, 负激发效应)[7]。虽然传统的观点认为, 土壤激发只能持续相对较短的时间, 但是近期研究发现, 即便添加的易分解有机物被完全分解后, 激发效应仍可以持续数周甚至数个月, 并最终影响土壤碳平衡[8-9]。在植物-土壤系统中, 由于凋落物、根系分泌物以及土壤微生物的裂解死亡都源源不断地向土壤中输入新鲜易分解有机物。因而, 研究植物-土壤系统中易分解有机物输入对土壤有机碳矿化的影响, 对于评估与预测土壤碳库的稳定性具有重要的意义。
当前大多数研究认为, 虽然土壤激发效应是由易分解有机物输入诱导的, 但是激发的强度与方向受土壤养分(尤其是土壤氮)可利用性的控制[3, 10-11]。在研究土壤氮可利用性对土壤激发效应影响时, 绝大多数研究都直接向土壤中添加可利用氮[3, 11]。这就导致微生物在利用这部分氮时与微生物通过分解土壤复杂有机质获得氮素在氮的获取方式上有所不同, 无法模拟实际条件下镶嵌在复杂土壤有机质中养分元素的实际状况[12]。因而, 根据土壤养分可利用性的自然变化梯度来研究土壤养分可利用性的变化对土壤激发效应的影响显得更具有实际意义。处于同一恢复系列不同恢复阶段的森林土壤具备上述这一特征, 而且同一恢复系列也将土壤形成因子(母质、气候、植被、地形、时间)的变异减小到了最低限度, 是研究土壤养分可利用性变化对土壤激发效应影响的一个极好的模式系统[13]。
福建省长汀县是中国南方红壤地区的典型水土流失区, 该区曾因为植被稀少、山岭裸露、气候炎热, 而被称之为“火焰山” [14]。自20世纪80年代以来, 当地开展大量的水土保持与生态恢复实践, 使得治理区植被覆盖率显著提高[15]。在植被恢复过程中, 由植物凋落物或是根系分泌物向土壤中输入的易分解有机物随之增加[16], 而且凋落物的归还也进一步改变了土壤碳、氮、磷等养分状况, 使得处于不同恢复阶段森林土壤的碳氮磷化学计量特征呈现明显的差异性[17]。那么, 在植被恢复过程中, 易分解有机碳的输入将对不同恢复阶段具有不同养分特征的土壤有机质的分解有何影响仍不清楚。而且, 当前有关激发效应的研究中少有关注易分解有机碳对不同时间序列侵蚀红壤恢复区森林土壤激发效应影响的研究, 这也限制了我们对该地区不同恢复年限森林土壤碳库稳定性的认识。
鉴于此, 本研究拟以福建省长汀县具有相似立地条件和样地情况的不同恢复年限(裸地、5年、15年、30年)马尾松林以及天然林为研究对象, 通过向土壤中添加13C标记葡萄糖来研究易分解有机碳输入对不同恢复年限森林土壤激发效应的影响, 探明处于不同恢复阶段森林土壤有机碳的分解对易分解有机碳输入的响应是否存在差异, 这种差异是否与不同恢复阶段土壤养分状况改变有关?研究结果将为预测植被恢复过程中易分解有机物输入对土壤碳库和碳循环的影响提供数据支持, 以便更好地进行森林生态系统碳管理。
1 材料与方法 1.1 试验地概况试验土壤于2017年8月29日采自福建省长汀县河田镇(116°18′—116°31′E, 25°33′—25°48′N), 该地区属于典型的中亚热带季风气候区, 年平均降水量约1737 mm, 年平均温度17.5—18.8℃[17]。河田镇属河谷盆地, 海拔300—500 m。土壤为中粗粒花岗岩发育的红壤, 抗蚀能力低。该地区地带性植被为常绿阔叶林, 不同恢复阶段森林植被以马尾松为主。本研究采集土壤有未经治理的来油坑裸地, 经过治理的恢复年限为5年、15年与30年的马尾松林以及当地村民为保护风水而得以保存下来的天然林, 天然林估计林龄在70—110年左右。不同恢复年限马尾松林的本底条件与未治理地基本相似。
1.2 土壤样品的采集土壤样品采集时在每种恢复样地选择3个有代表性的样地, 进行多点采样, 采集0—20 cm土层的土壤, 并将来自同一恢复样地的土壤均匀混合, 过2 mm筛, 剔除石粒和根系。一部分土壤样品风干后测定土壤pH、有机碳与全氮含量, 另一部分土壤用于室内培养实验。供试土壤基本理化性质见表 1。
| 土壤性质 Soil properties |
裸地 Bare soil |
5年松林 5-year-old pine forest |
15年松林 15-year-old pine forest |
30年松林 30-year-old pine forest |
天然林 Natural forest |
| 总碳Total carbon/(g/kg) | 1.24 | 6.33 | 6.14 | 12.00 | 13.13 |
| 总氮Total nitrogen/(g/kg) | 0.10 | 0.27 | 0.28 | 0.45 | 0.85 |
| 硝态氮Nitrate nitrogen/(mg/kg) | 0.91 | 0.96 | 0.57 | 0.55 | 5.31 |
| 铵态氮Ammonium nitrogen/(mg/kg) | 8.91 | 8.59 | 10.00 | 15.90 | 48.69 |
| 微生物量碳Microbial biomass carbon/(mg/kg) | 62.24 | 117.89 | 253.71 | 227.83 | 268.95 |
| 土壤容重Bulk density/(g/cm3) | 1.02 | 1.00 | 1.05 | 1.08 | 0.98 |
| pH | 3.90 | 4.04 | 4.02 | 4.07 | 3.92 |
称取相当于干土重40 g的鲜土于玻璃培养瓶中(瓶高h=11 cm, 半径r=3.5 cm), 用去离子水调节土壤水分含量到田间持水量的60%。每个恢复阶段的森林土壤设置2个处理(添加99% 13C标记葡萄糖与不添加葡萄糖), 每个处理3个重复, 并设置4次破坏性取样, 即总培养数为120个。将装好土的培养瓶放在25℃恒温培养箱中预培养7 d, 使土壤中的微生物比较稳定。预培养后向实验组添加1 g/kg 13C标记葡萄糖(相当于0.4 g C/kg), 葡萄糖以溶液的形式添加, 添加时将葡萄糖溶液(4 mL)均匀滴在土壤表面上。对照组添加等量的去离子水, 并盖上带有孔隙的培养瓶盖子, 使培养过程保持通气状态。然后把培养瓶再次放入25℃恒温生化培养箱内培养59 d。为了确保培养瓶中水分稳定每隔5 d采用称重法补充水分。在本实验中裸地、5年、15年、30年马尾松林以及天然林不添加和添加葡萄处理依次表述为B, BG, 5F, 5FG, 15F, 15FG, 30F, 30FG, NF, NFG。
1.3.2 气体采集与测定在气体采集的前1 h将各培养瓶的盖子打开, 使其与周围环境空气混合均匀。取样时, 密封瓶口, 用注射器抽取玻璃瓶内的气体5 mL, 隔1 h后, 再抽取第二针气体。本实验培养周期为59 d, 分别在葡萄糖添加后的第1、2、4、5、7、9、13、21、29、39、48、54 d和59 d进行气体采集, 累计采样13次。在采集完两次气体样品(10 mL)之后再采集200 mL的同位素气体样品, 并将其注入到提前抽好真空的气袋里。
CO2浓度的测试分析采用气相色谱法(岛津Shimadzu, GC-2014C, Japan)。CO2检测器为氢火焰离子检测器(FID), 载气为高纯度的N2, 流速为30 mL/min, H2为燃气, 流速为30 mL/min, 空气为助燃气, 流速为400 mL/min, 检测器温度为200℃, 分离柱温度为55℃。CO2气体的δ13C同位素值采用同位素比值质谱仪法进行测定(IRMS, Isoprime 100, UK)。
1.3.3 气体通量的计算
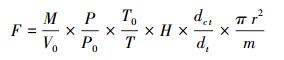
|
(1) |
式中, F为土壤CO2排放通量, M为气体的摩尔质量(g/mol), V0为标准状态下(温度273 K, 气压101.3 kPa)气体摩尔体积(22.41 L/mol), T0和P0分别为标准状态下空气的绝对温度和气压, P为采样时气压, T为采样时的绝对温度, dCt/dt为观测时间内培养瓶内气体浓度随时间变化的直线斜率, 正值表示排放, 负值表示吸收, H为培养瓶瓶口到培养土壤的高度, r表示培养瓶半径, m表示干土质量。

|
(2) |
式中, Fi表示连续两次采样时CO2气体平均排放通量(单位为μg C/kg/h), Di表示采样的间隔天数(d), n表示采样次数。
1.3.4 不同来源碳对CO2排放的贡献土壤排放的总CO2中来自葡萄糖的比例

|
(3) |
式中, f表示葡萄糖来源CO2排放占土壤总CO2排放的比例, 其中δp表示葡萄糖的δ13C值, δck表示未添加葡萄糖土壤排放的CO2的δ13C值, δt表示添加葡萄糖土壤排放的CO2的δ13C值。
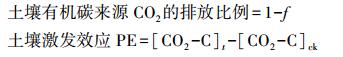
|
式中, [CO2-C]t表示葡萄糖处理下来自土壤有机碳矿化的CO2排放速率; [CO2-C]ck表示未添加葡萄糖的土壤的CO2排放速率;
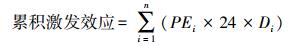
|
PEi表示连续两次采样时土壤激发效应平均值(单位为μg C/kg/h), Di表示采样的间隔天数(d), n表示采样次数。
采用一级动力学方程对土壤有机碳来源CO2的排放进行模拟。
在土壤培养的第7、21、39 d和59 d进行破坏性取样, 测定土壤微生物碳含量、DOC含量以及土壤可利用氮(NH4+-N + NO3--N)含量。土壤微生物生物量采用氯仿熏蒸法测定[18]。土壤DOC采用去离子水浸提(水土比5 : 1), 浸提液用TOC分析仪(Shimadzu TOC, Kyoto, Japan)进行测试。土壤矿质氮的测定采用2 mol/L KCl浸提1 h后用全自动间断化学分析仪(SmartChem)进行分析测试。
1.4 统计分析采用SPSS 16.0 (SPSS, Chicago, IL, USA)进行统计分析。用ANOVA最小显著性差异法(LSD)分析葡萄糖添加对不同恢复阶段森林土壤不同来源CO2排放、MBC、DOC以及土壤可利用氮的影响。用线性回归方程拟合了土壤可利用氮变化与土壤累积激发效应的回归关系。统计显著性水平设置为P < 0.05。作图采用SigmaPlot 12.5 (Systat Software Inc., California, USA)。
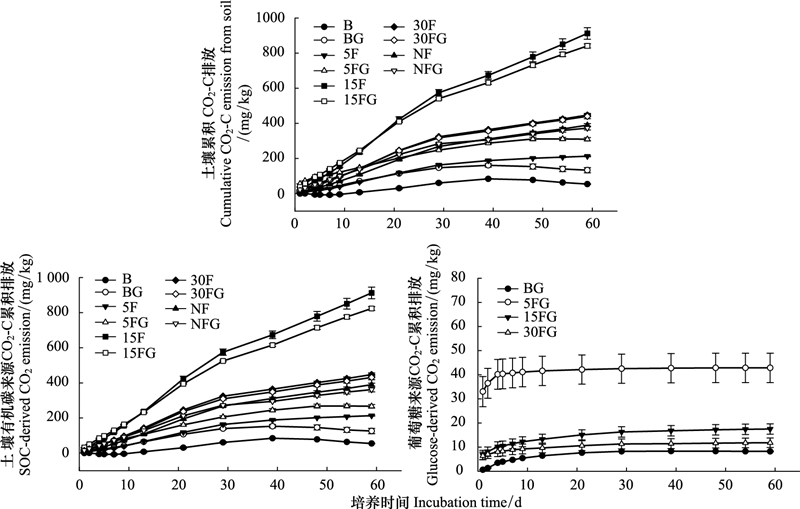
2 结果与分析 2.1 CO2排放土壤总CO2与土壤有机碳来源CO2的排放模式相似。即, 随着恢复年限的增加呈现先增加后下降的趋势(图 1)。15年马尾松林土壤有机碳来源CO2的累积排放量最高((913±33) mg/kg), 其排放量分别是裸地、5年、30年马尾松林以及天然林土壤累积矿化量的17、4、2倍和2倍(图 1)。葡萄糖添加对各恢复阶段森林土壤有机碳来源CO2排放的影响程度因不同恢复阶段而异。葡萄糖的添加显著降低了15年马尾松林土壤有机碳来源CO2的排放, 使其排放量减少了10%±1%。然而, 葡萄糖的添加却显著促进了裸地与5年马尾松林土壤有机碳来源CO2的排放, 使其排放量分别提高了131%±27%与25%±5%。葡萄糖的添加虽然降低了30年马尾松林与天然林土壤有机碳来源CO2的排放, 但是差异并未达到显著水平(P>0.05)。采用一级动力学方程对土壤有机碳来源CO2排放量进行模拟, 结果发现, 15年马尾松林具有最大的潜在碳矿化量, 其次为天然林、30年马尾松林、5年马尾松林以及裸地(表 2)。葡萄糖的添加显著降低了15年马尾松林与天然林的潜在碳矿化量, 但是显著提高了裸地、5年马尾松林及天然林土壤有机碳的分解速率常数(表 2)。
|
| 图 1 不同土壤碳源累积CO2-C排放动态(平均值±标准误, n=3) Fig. 1 Dynamics of cumulative CO2-C emission derived from different carbon sources (means±SE, n=3) B:裸地Bare soil; BG:裸地+葡萄糖Bare soil + glucose; 5F:5年松林5-year-old pine forest; 5FG:5年松林+葡萄糖5-year-old pine forest + glucose; 15F:15年松林15-year-old pine forest; 15FG:15年松林+葡萄糖15-year-old pine forest + glucose; 30F:30年松林30-year-old pine forest; 30FG:30年松林+葡萄糖30-year-old pine forest + glucose; NF:天然林Natural forest; NFG:天然林+葡萄糖Natural forest + glucose |
| 处理Treatment | 潜在碳矿化量/(mg/kg) Potential mineralizable carbon | 分解速率常数/d Decomposition constants |
| 裸地Bare soil | 101.23f | 0.02bc |
| 裸地+葡萄糖Bare soil + glucose | 158.92f | 0.05a |
| 5年松林5-year-old pine forest | 318.61e | 0.02cd |
| 5年松林+葡萄糖5-year-old pine forest + glucose | 319.26e | 0.04b |
| 15年松林15-year-old pine forest | 1807.28a | 0.01d |
| 15年松林+葡萄糖15-year-old pine forest + glucose | 1372.31b | 0.02cd |
| 30年松林30-year-old pine forest | 615.59c | 0.02bc |
| 30年松林+葡萄糖30-year-old pine forest + glucose | 597.58c | 0.02bc |
| 天然林Natural forest | 644.62c | 0.02c |
| 天然林+葡萄糖Natural forest + glucose | 447.70d | 0.03b |
| 同一列不同字母表示差异达显著水平(P < 0.05) | ||
葡萄糖来源CO2的排放量在5年马尾松林中最高, 其排放量分别是裸地、15年、30年马尾松林与天然林的5.2、2.5、4.8倍与3.9倍(图 1)。葡萄糖来源CO2的排放主要集中在培养的前13 d, 这一期间葡萄糖累积CO2排放量约占整个培养期间累积排放量的69%—97%。从整个培养期来看, 裸地、5年、15年、30年马尾松林以及天然林葡萄糖的累积CO2排放量占碳添加量的21%、107%、44%、22%和30%。
2.2 土壤激发效应葡萄糖添加初期促进了各恢复阶段森林土壤有机碳的矿化, 即呈现正的激发效应(图 2)。然而, 随着培养时间的推移, 土壤激发效应的方向在15年、30年马尾松林以及天然林中从正激发转变为负激发, 在裸地与5年马尾松林中, 激发的方向大体保持正的激发效应, 但是激发的强度逐渐减弱(图 2)。

|
| 图 2 土壤激发效应与累积激发效应动态 Fig. 2 Dynamics of soil priming effect and cumulative priming effect (means±SE, n=3) |
从累积激发效应来看, 葡萄糖的添加显著促进了裸地与5年马尾松林土壤有机碳的矿化, 其矿化量分别比其余3个林型增加了87—160 mg/kg与69—143 mg/kg, 差异均达显著水平(P < 0.05, 图 2)。葡萄糖的添加对30年马尾松林与天然林土壤有机碳的矿化无明显影响, 但是其显著减缓了15年马尾松林土壤有机碳的矿化。
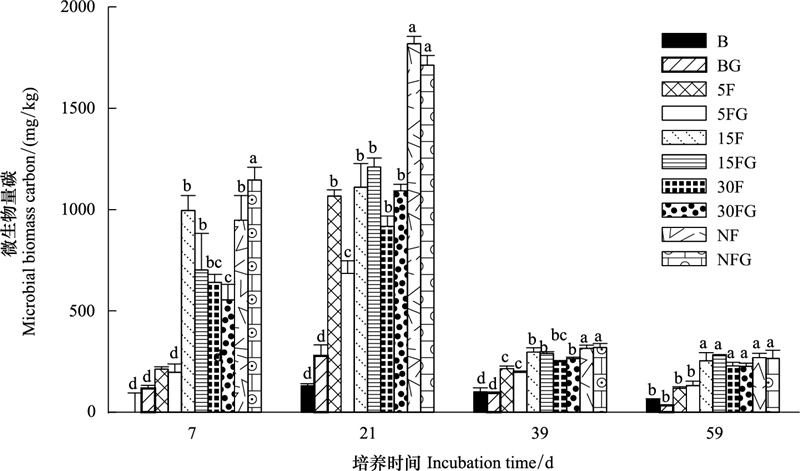
2.3 微生物量碳在整个培养过程中, 葡萄糖的添加并未显著改变各恢复阶段森林土壤的MBC含量(5年马尾松林第21天除外)。但就不同恢复阶段森林土壤MBC含量而言, 天然林与15年马尾松林土壤MBC略高于30年马尾松林, 但它们的MBC均显著高于裸地与5年马尾松林(P < 0.05, 图 3)。土壤MBC在培养的第21天达到最大值, 但是随着培养的进行土壤MBC显著降低。
|
| 图 3 土壤微生物碳随时间的变化(平均值±标准误, n=3) Fig. 3 Dynamics of soil microbial biomass carbon (means±SE, n=3) |
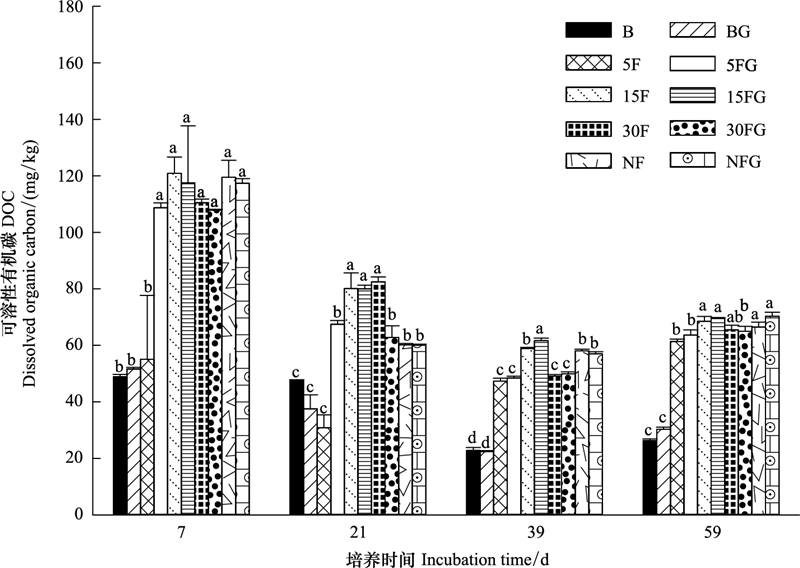
在整个培养过程中, 葡萄糖的添加主要提高了培养前期5年马尾松林土壤DOC的含量(P < 0.05), 而对其他恢复阶段森林土壤DOC含量无明显影响。就不同恢复阶段森林土壤DOC而言, 15年、30年马尾松林以及天然林具有较高的土壤DOC含量, 它们的DOC含量显著高于5年马尾松林与裸地(P < 0.05, 图 4)。
|
| 图 4 土壤可溶性有机碳随时间的变化(平均值±标准误, n=3) Fig. 4 Dynamics of soil dissolved organic carbon (means±SE, n=3) |
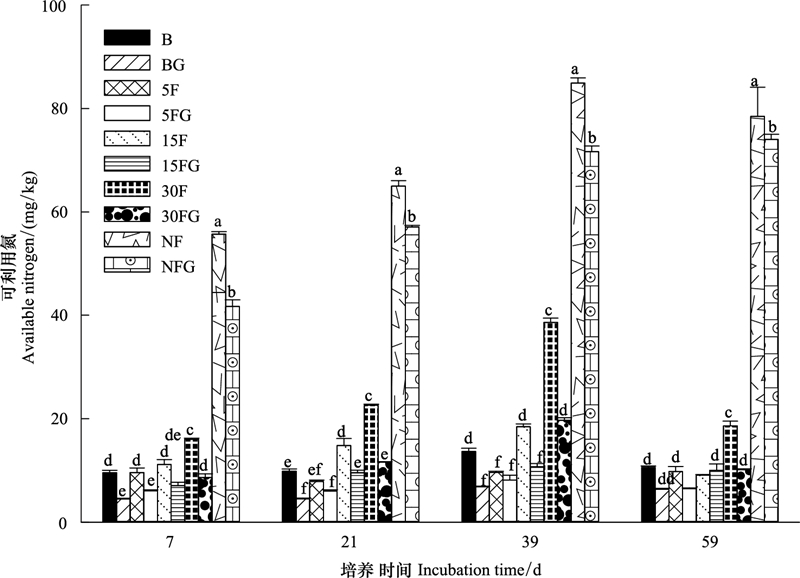
土壤可利用氮含量随着森林恢复年限的增加呈增加趋势, 而且天然林土壤可利用氮的含量显著高于其他林型(P < 0.05), 其含量大约是裸地、5年、15年和30年土壤可利用氮含量的4—6, 6—7, 3—6, 1—3倍(图 5)。葡萄糖的添加显著降低了土壤中可利用氮的含量, 而且这种降低在裸地、5年和30年马尾松林中表现最为明显。在培养结束时, 添加葡萄糖与不添加葡萄糖土壤可利用氮的变化百分比与土壤累积激发效应之间存在显著的正相关关系(图 6)。
|
| 图 5 土壤可利用氮随时间的变化(平均值±标准误, n=3) Fig. 5 Dynamics of soil available nitrogen (means±SE, n=3) |

|
| 图 6 可利用氮的变化与土壤累积激发之间的关系 Fig. 6 Relationships between the change of available nitrogen and cumulative priming effect |
在本研究中, 土壤有机碳来源CO2的排放随着森林恢复年限的增加呈现先增加后下降的趋势, 表明处于恢复中期的森林土壤具有较快的碳周转速率。这一研究结果与前人的研究结果相似。例如, Kukumgi等[19]对不同演替阶段云杉林土壤呼吸的研究发现, 处于演替中期(14—25年)的云杉林比演替早期(2—4年)、演替中后期(31—82年)的云杉林具有更强的土壤呼吸。Wang等[20]对加拿大北方森林的研究也发现, 土壤呼吸随着林龄(11—130年)的增加而降低。Saiz等[21]对爱尔兰中部北美云杉林土壤呼吸的研究发现, 11年云杉林具有最强的土壤呼吸速率, 随着林龄的增加土壤呼吸下降, 当林龄达到47年时土壤呼吸基本达到平衡。处于演替中期的森林土壤具有较高的土壤呼吸呼吸速率可能与演替中期植物光合作用的大量产物主要向土壤根部输送, 进而提高土壤细根生物量以及根系分泌物的含量, 从而促进了土壤呼吸[21-22]。虽然在本研究中, 用于试验的土壤已过2 mm筛, 剔除了根系, 但是研究发现15年马尾松林土壤DOC含量要高于其他林型。因而, 15年马尾松林土壤CO2排放量较高可能与其具有较高的DOC含量有关。
3.2 易分解有机碳添加对土壤激发效应的影响从本研究来看, 葡萄糖添加对土壤激发效应的影响与森林恢复年限有关。葡萄糖添加主要促进了恢复初期土壤有机碳的矿化, 对恢复后期森林土壤有机碳矿化的影响并不明显(图 2), 这表明处于恢复初期的森林SOC对外源易分解有机碳输入极为敏感, 而到了恢复中后期森林SOC稳定性较高, 不易受外源有机碳输入的影响。目前, 关于易分解有机物对不同演替阶段土壤激发效应的影响是否与演替阶段有关还存在较大争议。例如, Guelland等[23]对10、70年与120年老土壤有机碳的研究发现, 植物凋落物输入对土壤有机碳自身矿化无明显影响, 即激发效应并不显著。然而, Blagodatskaya等[24]发现葡萄糖添加主要促进了十几年年龄SOC的矿化, 当土壤年龄超过这个限度时则促进作用不明显。Sullivan等[12]对美国亚利桑那州原生演替的研究则发现, 葡萄糖添加后土壤激发效应随着演替的进行呈现“U”型变化趋势。即, 在演替的初期与演替的后期呈现正激发效应, 但是在演替中期呈现负激发效应。其认为出现这种变化模式是因为演替早期的土壤受土壤氮素可利用性的限制, 而演替后期的土壤则受土壤磷可利用性的限制, 相比之下处于演替中期的土壤受这两种元素的限制并不明显。Guenet等[25]的研究结果也显示, 光裸地土壤有机碳矿化对外源易分解有机物输入的响应比常年耕地更为敏感。在本研究中, 葡萄糖添加后裸地、5年马尾松林土壤的激发效应要强于30年马尾松林与天然林, 这可能是因为裸地与5年马尾松林土壤的氮可利用性明显小于30年马尾松林和天然林(图 5)。土壤养分可利用性较低由易分解有机物诱导的土壤激发效应较强[10]。而且从土壤可利用氮的相对变化与土壤累积激发效应来看, 土壤氮固持越强, 其引起的土壤激发效应也越强。裸地、5年马尾松林土壤的激发效应强, 主要在于它们自身土壤氮素含量低, 在葡萄糖添加后微生物需要通过分解土壤中原有SOC释放的氮素来满足自身对氮的需求。15年马尾松林土壤激发效应在培养的中后期呈现负的激发效应除了与Sullivan等[12]所认为的演替中期土壤受氮磷限制并不明显有关外还可能与培养中后期土壤微生物大量裂解死亡后将原本被这些微生物固持的13C标记葡萄糖释放出来, 被剩余微生物所利用有关。因为有研究表明, 微生物碳氮比比土壤有机质碳氮比低, 从而更易被微生物利用[2, 10]。
在整个培养过程中, 葡萄糖的添加并未显著提高不同恢复阶段森林土壤的MBC。Rousk等[26]在研究不同葡萄糖添加量(0—4000 μg C/g)对土壤激发效应的影响时也发现, 土壤微生物碳量变化并不明显, 而且过高的葡萄糖碳添加抑制了土壤细菌的生长, 但是促进真菌的生长。由于大多研究表明, 易分解有机物的输入既可以加快原有SOC的分解也可以减缓原有SOC的分解, 这主要与土壤中真菌和细菌的相对丰度发生变化有关。由于细菌属于r-策略者其主要分解易分解有机物, 而真菌属于K-策略者其可以分解较难分解的SOC, 细菌与真菌相对丰度的变化直接影响SOC的分解[27-28]。因而, 在本研究中, 葡萄糖添加初期促进SOC矿化除了与土壤氮素可利用性改变有关外还可能与葡萄糖添加促进了土壤真菌的生长但是抑制了土壤细菌的生长, 抑或是葡萄糖添加促进了土壤真菌和细菌的生长, 但是真菌的增长幅度比细菌快有关。随着培养的进行, 土壤激发强度减弱, 土壤MBC也减少, 表明随着培养的进行, 葡萄糖不断被分解, 其为微生物生长所提供的能量逐渐减少, 微生物活性的降低减弱了激发强度。Xiao等[29]对广西红壤的研究也发现, 易分解有机碳输入后土壤MBC与土壤激发效应随着培养的进行逐渐减弱。
4 结论外源易分解有机物对不同恢复年限森林土壤有机碳矿化的影响与恢复年限有关。恢复早期森林土壤对外源易分解有机碳输入的响应极为敏感, 但是到了恢复中期, 外源有机物的输入减缓了土壤有机碳的矿化, 促进土壤有机碳的积累。恢复后期森林土壤具有较强的稳定性, 其对外源易分解有机物输入的响应并不明显。
| [1] |
Lal R. Soil carbon sequestration to mitigate climate change. Geoderma, 2004, 123(1/2): 1-22. |
| [2] |
Kuzyakov Y, Friedel J K, Stahr K. Review of mechanisms and quantification of priming effects. Soil Biology and Biochemistry, 2000, 32(11/12): 1485-1498. |
| [3] |
Chen R R, Senbayram M, Blagodatsky S, Myachina O, Dittert K, Lin X G, Blagodatskaya E, Kuzyakov Y. Soil C and N availability determine the priming effect:microbial N mining and stoichiometric decomposition theories. Global Change Biology, 2014, 20(7): 2356-2367. DOI:10.1111/gcb.2014.20.issue-7 |
| [4] |
Guenet B, Neill C, Bardoux G, Abbadie L. Is there a linear relationship between priming effect intensity and the amount of organic matter input?. Applied Soil Ecology, 2010, 46(3): 436-442. DOI:10.1016/j.apsoil.2010.09.006 |
| [5] |
Kuzyakov Y. Review:factors affecting rhizosphere priming effects. Journal of Plant Nutrition and Soil Science, 2002, 165(4): 382-396. DOI:10.1002/1522-2624(200208)165:4<382::AID-JPLN382>3.0.CO;2-# |
| [6] |
Dalenberg J W, Jager G. Priming effect of some organic additions to 14C-labelled soil. Soil Biology and Biochemistry, 1989, 21(3): 443-448. DOI:10.1016/0038-0717(89)90157-0 |
| [7] |
Blagodatskaya E, Kuzyakov Y. Mechanisms of real and apparent priming effects and their dependence on soil microbial biomass and community structure:critical review. Biology and Fertility of Soils, 2008, 45(2): 115-131. DOI:10.1007/s00374-008-0334-y |
| [8] |
Fontaine S, Bardoux G, Abbadie L, Mariotti A. Carbon input to soil may decrease soil carbon content. Ecology Letters, 2004, 7(4): 314-320. DOI:10.1111/ele.2004.7.issue-4 |
| [9] |
Wang H, Xu W H, Hu G Q, Dai W W, Jiang P, Bai E. The priming effect of soluble carbon inputs in organic and mineral soils from a temperate forest. Oecologia, 2015, 178(4): 1239-1250. DOI:10.1007/s00442-015-3290-x |
| [10] |
Fontaine S, Henault C, Aamor A, Bdioui N, Bloor J M G, Maire V, Mary B, Revaillot S, Maron P A. Fungi mediate long term sequestration of carbon and nitrogen in soil through their priming effect. Soil Biology and Biochemistry, 2011, 43(1): 86-96. DOI:10.1016/j.soilbio.2010.09.017 |
| [11] |
Wang Q K, Wang S L, He T X, Liu L, Wu J B. Response of organic carbon mineralization and microbial community to leaf litter and nutrient additions in subtropical forest soils. Soil Biology and Biochemistry, 2014, 71: 13-20. DOI:10.1016/j.soilbio.2014.01.004 |
| [12] |
Sullivan B W, Hart S C. Evaluation of mechanisms controlling the priming of soil carbon along a substrate age gradient. Soil Biology and Biochemistry, 2013, 58: 293-301. DOI:10.1016/j.soilbio.2012.12.007 |
| [13] |
Bradford M A, Fierer N, Reynolds J F. Soil carbon stocks in experimental mesocosms are dependent on the rate of labile carbon, nitrogen and phosphorus inputs to soils. Functional Ecology, 2008, 22(6): 964-974. DOI:10.1111/fec.2008.22.issue-6 |
| [14] |
徐涵秋, 何慧, 黄绍霖. 福建省长汀县河田水土流失区植被覆盖度变化及其热环境效应. 生态学报, 2013, 33(10): 2954-2963. |
| [15] |
杨冉冉, 徐涵秋, 林娜, 何慧, 曾宏达. 基于RUSLE的福建省长汀县河田盆地区土壤侵蚀定量研究. 生态学报, 2013, 33(10): 2974-2982. |
| [16] |
刘翥, 杨玉盛, 司友涛, 康根丽, 郑怀舟. 植被恢复对侵蚀红壤可溶性有机质含量及光谱学特征的影响. 植物生态学报, 2014, 38(11): 1174-1183. |
| [17] |
张秋芳, 陈奶寿, 陈坦, 吕茂奎, 杨玉盛, 谢锦升. 不同恢复年限侵蚀红壤生态化学计量特征. 中国水土保持科学, 2016, 14(2): 59-66. |
| [18] |
Vance E D, Brookes P C, Jenkinson D S. An extraction method for measuring soil microbial biomass C. Soil Biology and Biochemistry, 1987, 19(6): 703-707. DOI:10.1016/0038-0717(87)90052-6 |
| [19] |
Kukumägi M, Ostonen I, Uri V, Helmisaari H S, Kanal A, Kull O, Lõhmus K. Variation of soil respiration and its components in hemiboreal Norway spruce stands of different ages. Plant and Soil, 2017, 414(1/2): 265-280. |
| [20] |
Wang C K, Bond-Lamberty B, Gower S T. Soil surface CO2 flux in a boreal black spruce fire chronosequence. Journal of Geophysical Research:Atmospheres, 2002, 108(D3): 8224. DOI:10.1029/2001JD000861 |
| [21] |
Saiz G, Byrne K A, Butterbach-Bahl K, Kiese R, Blujdea V, Farrell E P. Stand age-related effects on soil respiration in a first rotation Sitka spruce chronosequence in central Ireland. Global Change Biology, 2006, 12(6): 1007-1020. DOI:10.1111/gcb.2006.12.issue-6 |
| [22] |
Tang J W, Bolstad P V, Martin J G. Soil carbon fluxes and stocks in a Great Lakes forest chronosequence. Global Change Biology, 2009, 15(1): 145-155. DOI:10.1111/gcb.2009.15.issue-1 |
| [23] |
Guelland K, Esperschütz J, Bornhauser D, Bernasconi S M, Kretzschmar R, Hagedorn F. Mineralisation and leaching of C from 13C labelled plant litter along an initial soil chronosequence of a glacier forefield. Soil Biology and Biochemistry, 2013, 57: 237-247. DOI:10.1016/j.soilbio.2012.07.002 |
| [24] |
Blagodatskaya E, Khomyakov N, Myachina O, Bogomolova I, Blagodatsky S, Kuzyakov Y. Microbial interactions affect sources of priming induced by cellulose. Soil Biology and Biochemistry, 2014, 74: 39-49. DOI:10.1016/j.soilbio.2014.02.017 |
| [25] |
Guenet B, Juarez S, Bardoux G, Abbadie L, Chenu C. Evidence that stable C is as vulnerable to priming effect as is more labile C in soil. Soil Biology and Biochemistry, 2012, 52: 43-48. DOI:10.1016/j.soilbio.2012.04.001 |
| [26] |
Rousk J, Hill P W, Jones D L. Priming of the decomposition of ageing soil organic matter:concentration dependence and microbial control. Functional Ecology, 2015, 29(2): 285-296. DOI:10.1111/fec.2015.29.issue-2 |
| [27] |
Fontaine S, Mariotti A, Abbadie L. The priming effect of organic matter:a question of microbial competition?. Soil Biology and Biochemistry, 2003, 35(6): 837-843. DOI:10.1016/S0038-0717(03)00123-8 |
| [28] |
de Graaff M A, Classen A T, Castro H F, Schadt C W. Labile soil carbon inputs mediate the soil microbial community composition and plant residue decomposition rates. New Phytologist, 2010, 188(4): 1055-1064. DOI:10.1111/j.1469-8137.2010.03427.x |
| [29] |
Xiao D, Huang Y, Feng S Z, Ge Y H, Zhang W, He X Y, Wang K L. Soil organic carbon mineralization with fresh organic substrate and inorganic carbon additions in a red soil is controlled by fungal diversity along a pH gradient. Geoderma, 2018, 321: 79-89. DOI:10.1016/j.geoderma.2018.02.003 |
 2019, Vol. 39
2019, Vol. 39