文章信息
- 李杨, 潘珉, 何锋, 宋任彬, 杜劲松
- LI Yang, PAN Min, HE Feng, SONG Renbin, DU Jinsong.
- 不同底质对海菜花叶绿素荧光诱导动力学参数及净光合速率的影响
- Effects of different substrates on parameters of chlorophyll a fluorescence induction kinetics and net photosynthesis rate of Ottelia acuminata (Gagnep.) Dandy
- 生态学报. 2017, 37(8): 2809-2817
- Acta Ecologica Sinica. 2017, 37(8): 2809-2817
- http://dx.doi.org/10.5846/stxb201510102043
-
文章历史
- 收稿日期: 2015-10-10
- 网络出版日期: 2016-10-29
海菜花 (Ottelia acuminata (Gagnep.) Dandy), 学名水车前, 为水鳖科沉水植物[1]。20世纪60年代以前, 海菜花群落在滇池占优势地位, 于70年代起逐渐消失, 最终在滇池中灭绝[2]。海菜花在滇池水体中消失的原因较多, 大多数观点认为海菜花对水环境要求较高, 当水环境恶化后不适合海菜花生长而导致海菜花消失[2-4];杨君兴通过研究滇池水环境、水生植物与鱼产量变化关系认为由于人工放养大量草食性鱼类导致了海菜花在滇池中灭绝[5]。2007年, 海菜花在滇池回植并取得了一定进展[6], 并在野外调查中再次发现海菜花[5], 曾经被视为对污染敏感的海菜花被认为可作为治理富营养化水体的理想物种。
许多研究注意到沉水植被对富营养化水体的修复作用, 且已有较多的研究, 对恢复沉水植物涉及的主要影响因子如:光、水体及水质、温度、重金属等进行了大量的研究[7-12]。底质对沉水植被的影响也有较多的研究[13-16]。其中尹延震研究了底质对海菜花株高、叶片及生物量的影响[17], 但未见到底质对海菜花光合生理的影响研究。
叶绿素荧光诱导动力学曲线主要反映了的原初光化学反应及光合机构结构和状态的的变化;当环境条件变化时, 叶绿素荧光的变化可以在一定程度上反映环境因子对植物的影响, 通过对不同环境条件下快速叶绿素荧光诱导动力学曲线的分析, 可深入了解外界环境对植物光合机构的影响以及光合机构对环境的适应机制。目前在富营养化水体中回植海菜花的尝试已经逐步开展[6, 17], 但对回植过程中能否直接利用富营养化湖泊底泥作为底质或是需要添加养分含量较少的土壤来改良种植底质却未有明确的结论。因此利用叶绿素荧光诱导动力学曲线的相关参数可以研究海菜花对不同底质的适应状况, 进而从光合生理方面着手研究不同底质对海菜花的影响并对后期回植海菜花有一定的指导意义。
1 材料与方法 1.1 试验材料海菜花:采集于大理洱海种植基地, 保有一定水分的方式运送到昆明后立即进行种植。
底质:分别在滇池周边采集不同的土壤、沙以及大理洱海种植基地内的底泥做为种植底质, 底质类型分别为:1) 红壤:采自昆明西山, 2) 沙壤:采自昆明梁王河河岸边, 3) 湖沙:采自滇池白鱼口, 4) 洱海底泥:采自大理洱海海菜花种植基地内 (图例中为“洱海”), 同时作为对照, 5) 粘土:采自滇池底泥堆场, 6) 滇池底泥:采自滇池草海 (图例中为“滇池”)。底质采集后测定其全磷、全氮、有机质及pH。土壤全磷的测定采用硝酸高氯酸消煮钒钼黄比色法, 土壤全氮的测定采用硫酸双氧水消煮凯氏定氮法, 土壤有机质的测定采用重铬酸钾容量法, 土壤pH测定采用酸度计法, 底质土样数据监测数据如下:
| 底质类型Type of substrate | 全磷/(g/kg) Total Phosphorus | 全氮/(g/kg) Total Nitrogen | 有机质/% Organic Matter | pH |
| 红壤Red soil | 0.163 | 0.581 | 10.8 | 5.9 |
| 沙壤Sandy soil | 0.145 | 2.64 | 8.72 | 7.21 |
| 湖沙Sand of lake | 0.084 | 0.28 | 0.58 | 7.62 |
| 洱海底泥Sediment of Er′hai | 1.33 | 3.84 | 17.5 | 8.1 |
| 粘土Clay | 1.75 | 1.63 | 17.9 | 7.83 |
| 滇池底泥Sediment of dianchi | 1.93 | 3.19 | 28.1 | 7.68 |
将上述不同种类的底质放在各自编号的花盆中, 花盆直径为13cm, 然后将长势接近的海菜花种植在上述底质中, 种植前将海菜花原有的叶及花苞全部去除以保证其生长状态接近, 同一种类型底质上种植的海菜花质量见表 2;种植好后压实土壤防止海菜花因浮力作用漂浮到水面, 将花盆放入深度为120cm的玻璃缸中, 玻璃缸四周用两层黑色遮阳网围挡营造湖底的生长环境。每个玻璃缸中都放入不同底质种植的海菜花各1盆, 每个缸中总计放入6盆。共设置6个玻璃缸, 玻璃缸放置在同一地点, 以保证外界环境条件的一致性。缸中的水抽取滇池草海的水并用300目的滤网过滤以去除较大的藻团及其他植物断枝。
| 底质类型Type of substrate | 红壤Red soil | 沙壤Sandy soil | 湖沙Sand of lake | 洱海底泥Sediment of Er′hai | 粘土Clay | 滇池底泥Sediment of Dianchi |
| 1 | 0.061 | 0.064 | 0.061 | 0.061 | 0.052 | 0.063 |
| 2 | 0.061 | 0.059 | 0.05 | 0.051 | 0.061 | 0.053 |
| 3 | 0.056 | 0.053 | 0.06 | 0.056 | 0.062 | 0.057 |
| 4 | 0.058 | 0.055 | 0.052 | 0.054 | 0.054 | 0.056 |
| 5 | 0.058 | 0.053 | 0.053 | 0.063 | 0.058 | 0.051 |
| 6 | 0.064 | 0.062 | 0.064 | 0.064 | 0.054 | 0.052 |
| Mean±SD | 0.060±0.003 a | 0.058±0.005 a | 0.057±0.005 a | 0.058±0.005 a | 0.057±0.004 a | 0.055±0.004 a |
| 表中数据单位为kg, 每组数据均值用“平均值±标准差”表示;小写字母相同表示数值间差异不显著 (P < 0.05) | ||||||
在40d时, 选取6个玻璃缸中生长条件较好的5个缸中的海菜花进行生长指标的统计, 记录不同底质上生长的海菜花叶片数量以及叶片长度, 叶片长度不计入叶柄长度。80d时, 同样按之前选定的5个缸中的海菜花进行叶片数量及叶片长度的统计。
1.2.3 海菜花实验样品采集在40d时, 采集之前生长指标测定时选定的5个缸中的海菜花进行实验, 叶片选取规则为按生长顺序选取, 如同样顺序的叶片有大面积破损则选取临近的叶片进行实验。海菜花实验样品采集后放在各自标记的大烧杯中, 烧杯中放入适量清水避免叶片失水。80d时, 同样选择之前选定的5个缸中的海菜花进行实验。
1.2.4 海菜花光合生理实验海菜花叶片采摘后立即进行实验, 先将叶片用暗适应叶夹暗适应20min, 之后用Handy PEA植物效率仪 (Hansatech, UK) 测定不同底质类型上海菜花叶片的叶绿素荧光诱导动力学曲线及叶绿素荧光参数;Handy PEA的饱和脉冲光设定为3000μmol m-2 s-1。每个不同底质上种植的叶片测定5次。
叶绿素荧光实验测定结束后剪取面积为4.84cm2的海菜花叶片, 利用Chlorolab2液相氧测定系统 (Hansatech, UK) 测定其光合速率。在反应杯中加入10mL的浓度为0.1mol/L的NaHCO3溶液提供碳源;光强设定为1000μmol m-2 s-1。每个不同底质上种植的叶片测定5次。
1.3 数据处理海菜花叶片数量及叶片长度经统计后按均值±标准差 (Mean±SD) 表示。
光合放氧数据利用邵毅[18]的方法将放氧速率换算为CO2吸收速率。
叶绿素荧光快速诱导动力学曲线数据按照Strasser的O-J-I-P test的分析方法计算各种荧光参数[19-20]。数据采用Excel和SPSS 13进行统计分析。多样本间的比较采用单因素方差分析 (One-way ANOVA) 及Duncan与Scheffe多重比较 (P < 0.05)。
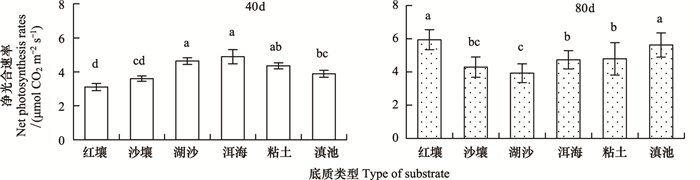
2 结果与分析 2.1 不同底质对海菜花叶片净光合速率的影响通过研究不同底质条件下海菜花叶片的净光合速率差异及变化规律表明, 不同底质条件及不同的种植时间, 海菜花的净光合速率有较大的差异 (图 1)。种植40d海菜花的净光合速率表明, 在湖沙和大理洱海底泥上种植的海菜花净光合速率最高, 且两个数据间差异不显著;而红壤上种植的海菜花净光合速率最低, 仅为大理洱海底泥上种植海菜花的63.6%。当种植海菜花80d时, 红壤和滇池草海底泥上种植的海菜花的净光合速率最高, 而在湖沙上种植的海菜花净光合速率变为最低, 红壤和滇池底泥上种植海菜花的净光合速率比在湖沙上种植的海菜花分别要高51.5%和43.3%。从时间推移上来看, 在种植40d的时候, 红壤上种植的海菜花净光合速率在所有类型的底质中最低, 但是到了80d时, 其光合速率变为最高;反观湖沙上种植的海菜花, 种植40d的时候, 其净光合速率几乎与洱海底泥的一致, 但种植80d时其净光合速率反而降到了最低, 同时其他底质类型上种植的海菜花的净光合速率都有所增加。因此可以确定底质对海菜花的净光合速率有一定的影响。
|
| 图 1 种植40d和80d后不同底质对海菜花叶片光合速率的影响 Fig. 1 Effects of different substrate on net photosynthetic rate of O. acuminate at 40-day and 80-day 图中小写字母的异同表示数值差异是否显著 (P < 0.05);洱海代表洱海底泥, 滇池代表滇池底泥 |
植物的初始荧光Fo反映的是光系统Ⅱ(PSⅡ) 所有反映中心全部开放时的荧光产量;最大荧光Fm则反映PSⅡ所有反应中心均关闭时的荧光;可变荧光Fv反映了PSⅡ原初电子受体QA的还原情况;Fv/Fm代表PSⅡ最大光化学量子产量, 能反映PSⅡ的内禀光能转换效率[21];PIABS代表性能指数, 比起Fv/Fm能更好的反映胁迫对植物光合机构的影响[22-24]。
海菜花种植40d后, 不同底质对海菜花的叶绿素荧光参数产生了不同的影响 (表 3)。滇池底泥上的海菜花初始荧光Fo显著高于洱海底泥上种植的海菜花, 粘土上种植的海菜花的初始荧光Fo最小, 其他底质上种植的海菜花的初始荧光Fo与洱海底泥上种植的海菜花无显著差异。红壤上种植的海菜花的最大荧光Fm和可变荧光Fv比洱海底泥上种植的海菜花分别低52.5%和58.8%, 且差异显著;而滇池底泥上种植的海菜花最大荧光Fm和可变荧光Fv与洱海底泥上种植的海菜花差异不显著。衡量植物抗逆性的参数PSⅡ最大光化学量子产量 (Fv/Fm) 也表明红壤上种植的海菜花的最低, 比洱海底泥上种植的海菜花低了13.3%, 其他底质上的海菜花之间差异不显著;性能指数 (PIABS) 下降意味着PSⅡ的光合结构和功能都受到了比较大的伤害[25], 性能指数 (PIABS) 也表现了与Fv/Fm同样的规律, 且数值上差异更大, 表现为红壤上种植的海菜花叶片光合能力较低。海菜花种植80d后, 不同底质对海菜花的叶绿素荧光参数产生了不同的影响之外, 对海菜花的影响也与种植40d时的情况发生了变化 (表 4)。此时不同底质下海菜花的各荧光参数变为湖沙上的海菜花最低, 而红壤上种植的海菜花的各荧光参数与洱海底泥上种植的海菜花之间已无明显差异;从性能指数来看, 种植于滇池底泥上的海菜花最高, 高于洱海底泥上的海菜花46.3%。表明种植80d后, 红壤上的海菜花叶片光合能力有所提升, 但湖沙的光合能力却相应降低。
| 底质类型Type of substrate | 红壤Red soil | 沙壤Sandy soil | 湖沙Sand of lake | 洱海底泥Sediment of Er′hai | 粘土Clay | 滇池底泥Sediment of Dianchi |
| Fo | 199.5±47.4 b | 202.0±33.9 b | 226.0±29.7 b | 238.5±12.0 b | 184.7±9.1 a | 259.0±31.1 c |
| Fm | 766.5±26.2 a | 1197.0±1.4 b | 1405.0±259.8 bc | 1615.0±33.9 c | 1168.0±62.00 b | 1306.5±113.8 bc |
| Fv | 567.0±73.5 a | 995±32.5 b | 1179±230.5 bc | 1376.5±21.9 c | 983.3±53.0 b | 1047.5±82.7 b |
| Fv/Fm | 0.739±0.071a | 0.831±0.028 b | 0.838±0.01 b | 0.852±0.004 b | 0.842±0.001 b | 0.802±0.007 b |
| PIABS | 0.25±0.21 a | 1.32±0.32 b | 1.0±0.17 b | 1.47±0.01 b | 1.18±0.13 b | 1.28±0.56 b |
| 表中数据为平均值±标准差;小写字母的异同表示数值差异是否显著 (P < 0.05); Fo:初始荧光minimal fluorescence;Fm:最大荧光maximal fluorescence;Fv:可变荧光variable fluorescence;Fv/Fm:光系统Ⅱ最大光化学量子产量maximum photochemical efficiency of PSⅡ;PIABS:性能指数performance index on absorption basis;表中数据为平均值±标准差;小写字母的异同表示数值差异是否显著 (P < 0.05) | ||||||
| 底质类型Type of substrate | 红壤Red soil | 沙壤Sandy soil | 湖沙Sand of lake | 洱海底泥Sediment of Er′hai | 粘土Clay | 滇池底泥Sediment of Dianchi |
| Fo | 215.7±27.3b | 215.6±15.0b | 157.7±26.2a | 226.7±29.5b | 183.6±19.3a | 215.0±37.7b |
| Fm | 1396.6±215.1b | 1377.8±143.2b | 867.9±196.0a | 1396.1±188.5b | 1182.7±134.7b | 1352.9±279.1b |
| Fv | 1180.9±189.5b | 1162.1±132.0b | 710.1±170.5a | 1169.4±161.3b | 999.1±115.9b | 1137.9±242.5b |
| Fv/Fm | 0.845±0.008b | 0.843±0.010b | 0.817±0.012a | 0.837±0.008b | 0.845±0.004b | 0.840±0.007b |
| PIABS | 1.30±0.24b | 1.43±0.32bc | 0.78±0.15a | 1.21±0.21b | 1.72±0.31cd | 1.77±0.53d |
通过研究不同底质上海菜花叶片叶绿素荧光参数和性能指数差异后, 为了解不同底质对海菜花光合生理的影响, 进一步分析了海菜花叶片PSⅡ反应中心能量流动比活性参数, 比活性参数可以更确切地反映植物的光合器官对光能的吸收、转化和耗散等状况[19]。ABS/RC表示单位反应中心吸收的光能;DIo/RC代表单位反应中心耗散的能量;TRo/RC代表单位反应中心捕获的用于还原QA的能量;Eto/RC代表单位反应中心捕获的用于电子传递的能量;RC/CSo代表单位面积中活性反应中心的密度[20, 26]。
种植40d后, 不同底质上种植的海菜花叶片单位反应中心吸收光能 (ABS/RC) 差异不大, 仅红壤和滇池底泥上种植的海菜花之间差异显著。但是红壤上种植的海菜花叶片的单位反应中心耗散的能量 (DIo/RC) 较多, 分别为洱海底泥和滇池底泥上种植海菜花的2.48倍和1.55倍。且红壤上种植的海菜花叶片上单位反应中心捕获的用于还原QA的能量 (TRo/RC) 略微高于其他底质上种植的海菜花;但是反应中心捕获的用于电子传递的能量 (Eto/RC) 很低, 仅为洱海底泥和滇池底泥上种植海菜花的59.7%和43.7%, 表明红壤上种植的海菜花叶片吸收的光能中用于电子传递的能量低于其他底质上种植的海菜花, 但是耗散的能量却增加。从单位面积中活性反应中心的密度 (RC/CSo) 看到, 红壤上种植的海菜花的反应中心数量显著降低 (表 5)。
| 底质类型Type of substrate | 红壤Red soil | 沙壤Sandy soil | 湖沙Sand of lake | 洱海底泥Sediment of Er′hai | 粘土Clay | 滇池底泥Sediment of Dianchi |
| ABS/RC | 3.33±0.45 a | 2.79±0.13 ab | 2.60±0.068 ab | 2.42±0.07 a | 2.58±0.13 ab | 2.88±0.02 b |
| DIo/RC | 0.887±0.353b | 0.473±0.1 a | 0.422±0.0327 a | 0.358±0.021 a | 0.407±0.018 a | 0.571±0.023 a |
| TRo/RC | 2.44±0.10c | 2.32±0.03bc | 2.18±0.05 ab | 2.07±0.05a | 2.17±0.11ab | 2.31±0.00bc |
| Eto/RC | 0.47±0.16 a | 0.981±0.013 bc | 0.726±0.0398 b | 0.787±0.047 b | 0.782±0.011 b | 1.076±0.282c |
| RC/CSo | 59.5±6.2 a | 72.1±8.8 ab | 87.0±13.09 bc | 98.4±2.2 c | 71.8±3.2 ab | 89.8±10.1 bc |
| ABS/RC:反应中心吸收的光能absorption flux per reaction center;DIo/RC:单位反应中心耗散的能力dissipated energy flux per reaction center;TRo/RC:单位反应中心捕获的用于还原QA的能量trapped energy flux per reaction center;Eto/RC:单位反应中心捕获的用于电子传递的能量electron transport flux per reaction center;RC/Cso:单位面积中活性反应中心的密度density of reaction center | ||||||
种植80d后, 不同底质上海菜花叶片的PSⅡ反应中心能量流动比活性参数与种植40d的时候发生了变化 (表 6)。在湖沙上的海菜花叶片的单位反应中心的吸收的光能 (ABS/RC) 和单位反应中心耗散的能量 (DIo/RC) 均略高于其他底质上的种植的海菜花, 其捕获的用于还原QA的能量 (TRo/RC) 和用于电子传递的能量 (Eto/RC) 与其他底质上种植的海菜花差异不大, 但单位面积的活性反应中心数量显著降低。与此同时, 红壤上的海菜花各参数与洱海底泥上的海菜花之间差异不显著。表明种植80d后, 在湖沙上种植的海菜花光合能力降低, 而红壤上的海菜花光合能力有所提升。
| 底质类型Type of substrate | 红壤Red soil | 沙壤Sandy soil | 湖沙Sand of lake | 洱海底泥Sediment of Er′hai | 粘土Clay | 滇池底泥Sediment of Dianchi |
| ABS/RC | 2.33±0.23b | 2.26±0.15b | 2.54±0.15c | 2.29±0.25b | 2.00±0.23a | 2.00±0.01a |
| DIo/RC | 0.361±0.030b | 0.355±0.028b | 0.465±0.025c | 0.372±0.044b | 0.311±0.033a | 0.320±0.022a |
| TRo/RC | 1.97±0.20 b | 1.91±0.13 b | 2.07±0.15 b | 1.91±0.21 b | 1.69±0.19 a | 1.68±0.08 a |
| Eto/RC | 0.693±0.048a | 0.707±0.083a | 0.633±0.084a | 0.658±0.051a | 0.645±0.050a | 0.664±0.084a |
| RC/CSo | 93.0±11.9b | 95.4±2.7bc | 62.0±7.8a | 99.4±10.6bc | 92.1±7.6b | 107.7±20.7c |
植物生物量的差异也是植物对外界环境响应的一个指标, 当光合生理发生变化后, 最终会影响其生物量的积累。在40d和80d同步观测不同底质上海菜花的叶片数量和叶片长度可以发现, 不同底质上海菜花的叶片数量在40d和80d的时候均无显著性差异, 但是叶片长度则有所差异。滇池底泥上种植的海菜花在40d和80d的时候其叶片长度均长于其他底质上种植的海菜花, 而在红壤上种植的海菜花的叶片长度在40d和80d时均短于其他底质上种植的海菜花。滇池底泥上种植的海菜花的叶片长度比红壤上种植的海菜花在40d和80d时分别长3.61cm和4.52cm (表 7)。表明红壤上种植的海菜花其叶片生长受到红壤的影响, 而且可能由于前期光合作用受到抑制从而导致后期其叶片长度短于其他底质上的海菜花。
| 底质类型Type of substrate | 叶片数量Leaf number | 叶片长度Leaf length/cm | |||
| 40d | 80d | 40d | 80d | ||
| 红壤Red soil | 9.6±1.3 a | 11.0±2.0 a | 20.89±5.87 b | 22.20±4.14 c | |
| 沙壤Sandy soil | 9.5±1.8 a | 12.3±1.4 a | 22.12±5.80 ab | 24.58±3.67 b | |
| 湖沙Sand of lake | 9.5±2.1 a | 12.7±1.0 a | 22.68±6.37 ab | 24.61±3.09 b | |
| 洱海底泥Sediment of Er′hai | 9.7±3.8 a | 14.3±3.6 a | 21.72±6.22 ab | 24.79±3.78 b | |
| 粘土Clay | 9.5±1.9 a | 11.2±2.3 a | 21.25±6.41 ab | 23.77±3.77 b | |
| 滇池底泥Sediment of Dianchi | 9.2±1.3 a | 13.7±2.5 a | 24.50±6.31 a | 26.72±3.91 a | |
本研究从光合生理入手探究不同底质对海菜花生长的影响, 发现不同底质对海菜花叶片的光合能力有不同的影响。总的来说, 种植40d的时候, 红壤显著降低了海菜花叶片的光合能力, 而到种植80d的时候, 红壤对海菜花叶片的光合能力未有明显的影响, 反而是湖沙上的海菜花光合能力显著下降, 但是红壤上种植的海菜花由于前期光合能力受到影响从而使得后期在叶片长度上的影响一直持续。
种植40d后, 洱海底泥上海菜花叶片的光合参数与滇池底泥上种植的海菜花光合能力接近 (表 3, 表 5)。而红壤对海菜花叶片光合能力的影响主要集中在吸收能量后耗散的增加和用于电子传递的能量减少, 同时表现为单位面积上活性反应中心的减少 (表 3, 表 5);结合土壤的理化性质可知 (表 1), 红壤的pH值呈酸性, 王利等的研究表明单位面积上有活性的反应中心的密度 (RC/CSo) 随着土壤pH值的降低而显著减少[27]。红壤上种植的海菜花由于单位面积上活性反应中心的数量降低, 因此捕获的用于电子传递的能量较低, 只能通过能量的耗散将过多的能量消耗以保护光合机构[21, 28]。通常光合作用电子传递伴随着类囊体腔内的质子积累, 会在叶绿体间质和类囊体腔中形成一个pH梯度差 (ΔpH) 和电势差, 在这个梯度差的驱动下, 质子穿过类囊体膜后驱动ATP合酶合成三磷酸腺苷 (ATP) 进一步驱动碳同化[29]。本研究测定的红壤的pH值仅为5.9, 可能导致红壤上海菜花叶片的叶绿体间质和类囊体腔的pH梯度 (ΔpH) 减小, 进而引起ATP合酶合成的ATP数量减少, 当ATP数量减少后, 将降低3-磷酸甘油酸 (3-PGA) 形成3-磷酸甘油醛 (GPA), 并影响核酮糖-1, 5二磷酸 (RuBP) 的再生[30];同时, 类囊体腔内pH降低还会导致PQH2的氧化速度降低, 最终使得电子传递链的速度慢下来, 并活化激发能的非光化学淬灭 (NPQ)[29], 在本研究中表现为能量耗散的增加;同时葛顺峰等的研究表明苹果对氮的利用率随土壤pH的降低而降低[31]。因此海菜花在红壤上种植40d时, 由于红壤pH为酸性可能会降低海菜花叶片的光合能力, 同时由于光合能力的降低最终导致叶片长度的缩短。
种植80d时, 红壤对海菜花光合能力的影响基本消除, 而湖沙上种植的海菜花的光合能力最低。研究表明土壤的pH一般随着水分含量的增加而升高, 酸性土壤淹水后, 在嫌气条件下形成的还原性碳酸铁、锰呈碱性可导致土壤pH升高[32]。当土壤pH升高后, 土壤的酸胁迫可能消除, 此时红壤上海菜花的光合能力与洱海底泥和滇池底泥上种植的海菜花之间差异不明显 (表 4)。湖沙上种植海菜花叶片的单位反应中心吸收的光能 (ABS/RC) 和单位反应中心耗散的能量 (DIo/RC) 略高于其他底质上的种植的海菜花, 其余指标与其他底质上的差异不大, 但是单位面积活性反应中心数量 (RC/CSo) 降低 (表 6), 这可能是由于湖沙中的养分少导致的, 但在种植初期植物可以从富营养化水体中吸收养分, 当种植时间延长, 水体中养分耗尽, 出现养分不足后影响其光合能力, 但是湖沙上的海菜花叶片长度虽然短于滇池底泥上的海菜花叶片长度, 但相较红壤上的海菜花叶片长度来说要长, 且与其余底质上的海菜花叶片长度差异不明显 (表 7)。红壤上的海菜花的光合能力在前期可能受到红壤较低的pH的抑制, 因此在光合产物的累积上可能受到影响, 从而导致其叶片长度一直较其他底质上海菜花的叶片短。表明酸性土壤上的海菜花虽然能够生长, 但其生长受到一定的抑制, 且这种影响在短期内也较难以通过酸性胁迫的解除而消失。海菜花多生活在水质较好的水体中, 但本研究结果表明, 营养较为丰富且pH偏碱性的底质对海菜花的生长有利。
4 小结本研究中, 滇池底泥上种植的海菜花叶片的光合能力与原生境洱海底泥上种植的海菜花之间没有明显差异, 甚至部分光合指标还优于洱海底泥上种植的海菜花。同时红壤在种植初期对海菜花可能会产生酸胁迫, 但是当水淹没红壤一段时间后, 由于土壤的理化性质改变而解除了胁迫, 但是叶片的长度已受到影响, 且在短期内该影响持续存在。同时湖沙对海菜花的光合性能在后期产生胁迫的原因可能是营养缺乏, 虽然光合参数表现为光合性能下降, 但是从表观上 (叶片数量及长度) 并未发现对其生长有太多影响。因此, 在海菜花回植过程中对土壤的选取时可就地选取湖中的底泥作为底质, 尽量不要选取酸性土壤作为底质, 而养分较为丰富的湖泊底泥有利于海菜花的生长, 该结论也能与尹延震的研究结论相互印证[17]。
| [1] | 李恒. 海菜花属的分类、地理分布和系统发育. 植物分类学报, 1981, 19(1): 29–42. |
| [2] | 李恒. 滇池海菜花的盛衰. 云南大学学报:自然科学版, 1985, 7(S): 138–142. |
| [3] | 曲仲湘, 李恒. 滇池植物群落和污染//《滇池污染与水生生物》研究课题协作组. 滇池污染与水生生物. 昆明: 云南人民出版社, 1983: 7-16. |
| [4] | 戴全裕. 云南抚仙湖、洱海、滇池水生植被的生态特征. 生态学报, 1985, 5(4): 324–335. |
| [5] | 杨君兴, 舒树森, 陈小勇. 草鱼引入对滇池湖体海菜花消亡的影响. 动物学研究, 2013, 34(6): 631–635. |
| [6] | 舒树森, 杨君兴, 崔桂华, 李原. 滇池东岸湿地回植海菜花技术初探. 安徽农业科学, 2007, 35(29): 9240–9241. DOI:10.3969/j.issn.0517-6611.2007.29.054 |
| [7] | 王锦旗, 郑有飞, 薛艳. 紫外辐射对菹草成株生理特性的影响. 生态学报, 2015, 35(18): 5975–5983. |
| [8] | 陈小峰, 陈开宁, 肖月娥, 张守栋, 王庆亚. 光和基质对菹草石芽萌发、幼苗生长及叶片光合效率的影响. 应用生态学报, 2006, 17(8): 1413–1418. |
| [9] | 杨飞, 林超, 张毅敏, 王晋. 水体浊度对马来眼子菜和菹草生长的影响. 环境工程学报, 2015, 9(2): 506–512. DOI:10.12030/j.cjee.20150202 |
| [10] | 马婷, 王国祥, 李强, 潘国权, 王文林. 富营养化水体中菹草光合荧光特性研究. 生态环境, 2007, 16(3): 758–761. |
| [11] | 潘琦, 宋祥甫, 邹国燕, 叶春, 付子轼, 刘福兴, 范洁群. 不同温度对沉水植物保护酶活性的影响. 生态环境, 2009, 18(5): 1881–1886. |
| [12] | 谷巍, 施国新, 张超英, 王文, 徐勤松, 徐楠, 曾晓敏, 张小兰, 周红卫. Hg2+、Cd2+和Cu2+对菹草光合系统及保护酶系统的毒害作用. 植物生理与分子生物学学报, 2002, 28(1): 69–74. |
| [13] | 陈开宁, 陈小峰, 陈伟民, 刘恩生, 兰策介, 许海. 不同基质对四种沉水植物生长的影响. 应用生态学报, 2006, 17(8): 1511–1516. |
| [14] | 雷泽湘, 谢贻发, 刘正文. 太湖梅梁湾不同沉积物对3种沉水植物生长的影响. 华中师范大学学报:自然科学版, 2006, 40(2): 260–264. |
| [15] | 蒋金辉, 周长芳, 安树青, 关保华, 蔡颖. 轮叶黑藻对不同底质和密度的可塑性响应. 南京林业大学学报:自然科学版, 2008, 32(4): 76–80. |
| [16] | 杨娇, 王智, 厉恩华, 宋辛辛, 王学雷. 滇池不同底泥条件下黑藻和金鱼藻的生长生理特征. 湿地科学, 2015, 13(4): 430–436. |
| [17] | 尹延震. 洱海湖滨带环境特征与海菜花恢复研究. 北京: 中国环境科学研究院, 2011. |
| [18] | 邵毅, 叶文文, 徐凯. 温度胁迫对杨梅光合作用的影响. 中国农学通报, 2009, 25(16): 161-166. |
| [19] | 李鹏民, 高辉远, StrasserR J. 快速叶绿素荧光诱导动力学分析在光合作用研究中的应用. 植物生理与分子生物学学报, 2005, 31(6): 559–566. |
| [20] | Strasser R J, Tsimilli-Michael M, Srivastava A. Analysis of the chlorophyll a fluorescence transient//Papageorgiou G C, Govindjee, eds. Advances in Photosynthesis and Respiration: Chlorophyll a Fluorescence. Amsterdam: Springer, 2004: 321-362. |
| [21] | 张守仁. 叶绿素荧光动力学参数的意义及讨论. 植物学通报, 1999, 16(4): 444–448. |
| [22] | Appenroth K J, Stöckel J, Srivastava A, Strasser R J. Multiple effects of chromate on the photosynthetic apparatus of Spirodela polyrhiza as probed by OJIP chlorophyll a fluorescence measurements. Environmental Pollution, 2001, 115(1): 49–64. DOI:10.1016/S0269-7491(01)00091-4 |
| [23] | Van Heerden P D R, Strasser R J, Krüger G H J. Reduction of dark chilling stress in N2-fixing soybean by nitrate as indicated by chlorophyll a fluorescence kinetics. Physiologia Plantarum, 2004, 121(2): 239–249. DOI:10.1111/ppl.2004.121.issue-2 |
| [24] | Van Heerden P D R, Tsimilli-Michael M, Krüger G H J, Strasser R J. Dark chilling effects on soybean genotypes during vegetative development: parallel studies of CO2 assimilation, chlorophyll a fluorescence kinetics O-J-I-P and nitrogen fixation. Physiologia Plantarum, 2003, 117(4): 476–491. DOI:10.1034/j.1399-3054.2003.00056.x |
| [25] | Schansker G, Srivastava A, Govindjee, Strasser R J. Characterization of the 820-nm transmission signal paralleling the chlorophyll a fluorescence rise (OJIP) in pea leaves. Functional Plant Biology, 2003, 30(7): 785–796. DOI:10.1071/FP03032 |
| [26] | Strasser R J, Srivastava A, Govindjee. Polyphasic chlorophyll a fluorescence transient in plants and cyanobacteria. Photochemistry and Photobiology, 1995, 61(1): 32–42. DOI:10.1111/php.1995.61.issue-1 |
| [27] | 王利, 杨洪强, 张召, 范伟国, 姜倩倩, 冉昆. 根区酸化对平邑甜茶叶片光系统Ⅱ活性及光合速率的影响. 林业科学, 2011, 47(10): 167–171. DOI:10.11707/j.1001-7488.20111026 |
| [28] | Ögren E. Prediction of photoinhibition of photosynthesis from measurements of fluorescence quenching components. Planta, 1991, 184(4): 538–544. |
| [29] | 许大全. 光合作用学. 北京: 科学出版社, 2013: 306–306. |
| [30] | 武维华. 植物生理学 (第二版). 北京: 科学出版社, 2008: 164–165. |
| [31] | 葛顺峰, 季萌萌, 许海港, 郝文强, 魏绍冲, 姜远茂. 土壤pH对富士苹果生长及碳氮利用特性的影响. 园艺学报, 2013, 40(10): 1969–1975. DOI:10.3969/j.issn.0513-353X.2013.10.012 |
| [32] | 黄昌勇. 土壤学. 北京: 中国农业出版社, 2000: 179–179. |
 2017, Vol. 37
2017, Vol. 37