文章信息
- 刘发林
- LIU Falin.
- 模拟火干扰对森林土壤微生物活性及氮矿化的影响
- Simulating the effects of fire disturbance on microbial activity and nitrogen mineralization in forest soil
- 生态学报. 2017, 37(7): 2188-2196
- Acta Ecologica Sinica. 2017, 37(7): 2188-2196
- http://dx.doi.org/10.5846/stxb201512142483
-
文章历史
- 收稿日期: 2015-12-14
- 网络出版日期: 2016-08-30
火干扰对森林生态系统的影响错综复杂。众所周知, 森林火灾促进土壤有机质的氧化从而改变其化学成分, 但有机物氧化的程度取决于火干扰温度、持续时间和土壤热渗透性[1-2], 温度高于508℃时导致热敏性微生物死亡, 超过708℃直接烧毁植被[3-4], 随后, 被烧死的植物和微生物迅速氧化为无机氮[5], 然而, 有机物在极高的温度下燃烧会导致氮挥发[6]。土壤温度增加会导致土壤水的比热和导热特性发生变化[2, 7]。土壤含水量是影响评估火干扰对土壤生物和理化性质的主要因素[8]。潮湿土壤中热传导速度更快, 热穿透更深, 汽化潜热可以防止土壤温度超过958℃, 直到水完全蒸发, 这种潜热效应不会保护热敏感微生物, 一旦水蒸发后对大多数耐高温微生物将是致命的[9-11]。许多学者研究表明, 通过计划烧除短期内可提高林地质量和土壤养分浓度[12], 但为了避免火灾风险, 计划烧除一般在相对潮湿的季节进行, 如冬季和春季末[13], 相反, 大多数森林火灾一般发生在土壤水分和有机层水分枯竭的旱季, 如秋季。近年来火干扰导致土壤受热从而影响森林矿质土壤中碳和氮动态变化成为研究热点[14-15], 分析土壤含水率、火强度、火灾历史对火干扰后土壤生态系统的影响, 为土壤恢复提供理论依据。本研究的目的是研究火干扰后土壤水分和温度的变化对土壤微生物活性和氮矿化的影响, 来模拟湿润和干燥的季节中、低强度火干扰对土壤的影响。
1 材料与方法 1.1 研究区概况研究试验选取湖南省攸县高枧林场马尾松 (Pinus massoniana) 次生林。南方丘陵地貌, 成土母岩以紫砂页岩、板页岩及第四纪红色粘土为主, 土壤肥沃, 年平均气温为17.8℃和年降水量为1410 mm。样方及剖面设置在东北坡, 坡度为 (25±5)°, 海拔约800 m, 土壤样品特征如表 1。试验土壤均取自高枧林场马尾松次生林, 一套土壤样品收集于近80 a未过火的林地, 一套土壤样品收集于2014年8月29日经中强度火干扰林地, 两套土壤取样点海拔、土壤种类及地上林分的年龄、树种组成基本相似。
| 土壤 Soil |
pH | 总碳 Total C/ (g/kg) |
总氮 Total N/ (g/kg) |
生物量碳 Biomass C/ (μg/g) |
潜在可矿化氮 Potentially mineralized nitrogen (PMN)/(μg/g) |
| 未受火干扰No fire disturbance | 5.5 | 31 | 1.2 | 127.2 | 15.1 |
| 火干扰Fire disturbance | 5.8 | 49 | 2.5 | 105.3 | 0.3 |
实验样本采用完全随机抽取并培养, 按2×3×3方式设计, 代表两种土壤 (近80a未过火的林地和2014年8月29日经中强度火干扰林地)、3个温度 (25℃、160℃和380℃) 和3种土壤水势 (-0.03 MPa、-1.0 MPa和-1.5 MPa), 每个处理重复3次。于2014年9月8日同时收集两套土壤样品, 先在未烧林分和中强度火烧迹地内各设置20 m×20 m的标准地, 在标准地内随机设置土壤剖面, 选取0—10 cm层土壤, 先移除其他碎片, 晾干, 并经土壤筛 (2 mm筛) 后储存供测试。随后从两套土壤样品中各取4个样本, 各样本分成3等份, 分别湿润到-0.03、-1.0、-1.5 MPa, 模拟土壤水势, 浸泡7d后在25℃恒温状态观测样品重量的变化。另各取60 g土壤样品放置于金属密封罐并置于一个预热30 min的马弗炉上, 分别控制温度25、160、380℃, 模拟中、低强度火表面温度。
1.3 实验室分析土壤样本提取后立即加热 (包括常温控制土壤) 和加热后处理。取25 g烘干土壤样本和50 mm的2 mol/L氯化钾摇动30 min, 通过42号滤纸。提取后分别通过贝特洛反应、水杨酸硝化测定铵态氮、硝态氮[16], 微生物生物量由熏蒸/提取和茚三酮反应[17-18], 微生物碳用烟熏样本茚三酮反应与未烟熏样本的差值乘21来计算。潜在可矿化氮 (PMN) 是经14 d厌氧孵化5 g的潮湿土壤放置在一个盛有12.5 mm蒸馏水并充满N2气的离心管中, 25℃条件下孵化14 d后, 向每个离心管中添加12.5 mm的4 mol/L氯化钾并放置30 min, 再分析土壤铵态氮。潜在可矿化氮 (PMN) 值反映了孵化与孵化土壤样品之间的铵态氮的差异。可溶性己糖浓度用蒽酮反应碳测定, 采用0.5 M的硫酸钾分析25 g新鲜土壤。微生物呼吸经三维好氧培养后通过碱性圈闭测定[19], 取50 g新鲜土壤样品保持60%的持水量并放置于1L的玻璃瓶中, 将20 mL的1 mol/L的氢氧化钠溶液放入土壤样品, 并密封在25℃条件下分别培养为3、7、14d, 随后转移到200 mm锥形瓶, 用24 mL的2 mol/L氯化钡和5滴指示剂溶液滴定, 用1 mol/L的盐酸溶液滴定终点。
1.4 统计分析通过三因素方差分析, 发现所有的数据都不违反方差分析假设检验, 使用统计分析系统 (SAS Institute) 进行分析[20]。
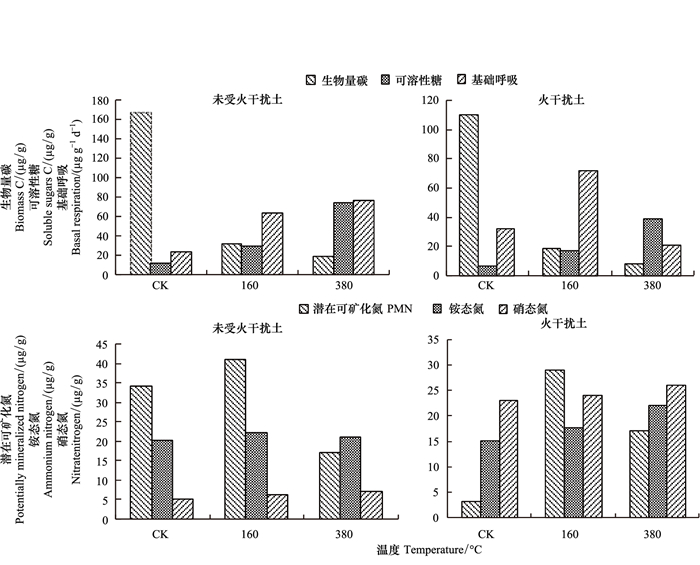
2 结果与分析 2.1 短期处理影响火干扰对土壤生物化学反应影响很大。经火干扰不久的土壤中碳、氮浓度较高, 微生物生物量碳和潜在可矿化氮较低 (表 1), 微生物生物量碳受火干扰后迅速下降, 土壤温度达380℃时下降最严重 (图 1), 火干扰历史和火干扰温度与微生物生物量碳之间的相互关系显著 (表 2)。未经火干扰的土壤微生物生物量碳浓度比火干扰温度达160、380℃的土壤高。当火干扰温度达160℃时土壤生物量碳均比对照样地减少, 当温度升高到380℃土壤生物量碳损失更大 (图 1)。
|
| 图 1 不同温度和湿度水平下土壤微生物生物量碳、水溶性糖、基础呼吸、PMN、铵态氮和硝态氮差异 Fig. 1 Difference of soil microbial biomass C, soluble sugars, basal respiration, PMN, ammonium nitrogen and nitrate nitrogen on different temperatures and moisture levels |
受热后土壤可溶性糖的浓度显著增加 (表 2), 160℃时土壤可溶性糖的含量增加近4倍, 380 ℃时增加近12倍 (图 1)。未受火干扰的土壤加热到380℃比曾经经历火干扰的土壤释放更多的可溶性糖。
| 项目 Project |
源 Source |
df | 均方 Mean square (MS) |
F | P>F | |
| 微生物量碳 | 土壤 | 1 | 13856 | 26.7 | 0.0001 | |
| Microbial biomass C | 温度 | 2 | 105548 | 202.6 | 0.0001 | |
| 土壤×温度 | 2 | 6511 | 12.5 | 0.0005 | ||
| 湿度 | 2 | 2649 | 5.1 | 0.0210 | ||
| 土壤×湿度 | 2 | 2058 | 3.9 | 0.0375 | ||
| 误差 | 16 | 515 | ||||
| 可溶性糖 | 土壤 | 1 | 3433 | 65.9 | 0.0001 | |
| Soluble sugars | 温度 | 2 | 12318 | 26.1 | 0.0001 | |
| 土壤×温度 | 2 | 1369 | 22.7 | 0.0001 | ||
| 湿度 | 2 | 589 | 11.4 | 0.0007 | ||
| 土壤×湿度 | 2 | 35 | 0.6 | 0.5089 | ||
| 误差 | 16 | 51 | ||||
| 基础呼吸 | 土壤 | 1 | 0.101 | 1.8 | 0.3044 | |
| Basal respiration | 温度 | 2 | 0.027 | 0.5 | 0.6638 | |
| 土壤×温度 | 2 | 0.079 | 3.9 | 0.3921 | ||
| 湿度 | 2 | 0.218 | 7.6 | 0.1983 | ||
| 土壤×湿度 | 2 | 0.417 | 3.7 | 0.1145 | ||
| 误差 | 16 | 0.096 | ||||
| 潜在可矿化氮 | 土壤 | 1 | 2661 | 58.4 | 0.0001 | |
| Potentially mineralized nitrogen | 温度 | 2 | 1763 | 38.4 | 0.0001 | |
| (PMN) | 土壤×温度 | 2 | 1056 | 23.1 | 0.0001 | |
| 湿度 | 2 | 164 | 3.5 | 0.0481 | ||
| 土壤×湿度 | 2 | 125 | 2.7 | 0.0901 | ||
| 误差 | 16 | 44 | ||||
| 铵态氮 | 土壤 | 1 | 109 | 24.7 | 0.0001 | |
| Ammonium nitrogen | 温度 | 2 | 64 | 14.5 | 0.0002 | |
| 土壤×温度 | 2 | 37 | 8.5 | 0.0025 | ||
| 湿度 | 2 | 612 | 138.9 | 0.0001 | ||
| 土壤×湿度 | 2 | 727 | 163.8 | 0.0001 | ||
| 误差 | 16 | 4.3 | ||||
| 硝态氮 | 土壤 | 1 | 4981 | 1239.7 | 0.0001 | |
| Nitrate nitrogen | 温度 | 2 | 11.4 | 2.8 | 0.0861 | |
| 土壤×温度 | 2 | 0.17 | 0.03 | 0.9587 | ||
| 湿度 | 2 | 384.8 | 95.8 | 0.0001 | ||
| 土壤×湿度 | 2 | 514.9 | 127.4 | 0.0001 | ||
| 误差 | 16 | 4 | ||||
| 在F检验中直接把概率P与显著水平α相比,如果P>α,则接受假设,如果P≤α,则拒绝 | ||||||
火干扰后短期内温度和土壤水势对基础呼吸速率的影响不显著, 因为土壤呼吸速率主要受水分和温度共同影响[21], 而本次研究控制的温度为25、160、380℃, 而森林地表火产生的高温可达400℃以上, 试验温度最高只有380℃, 热量向上辐射较多而向下热传导较少, 因此, 对土壤下层温度及土壤含水量的影响较小, 从而对土壤基础呼吸速率影响不显著。
如表 2和图 1, 加热到160℃两种土壤的潜在可矿化氮浓度是对照样地的两倍, 而380℃时潜在可矿化氮浓度比对照样地低。土壤受热导致铵态氮从氧化有机物中释放, 160℃时平均浓度增加10%和380℃增加22%, 相比之下, 受热对硝态氮浓度没有显著的影响, 与两种土壤火灾历史无关。
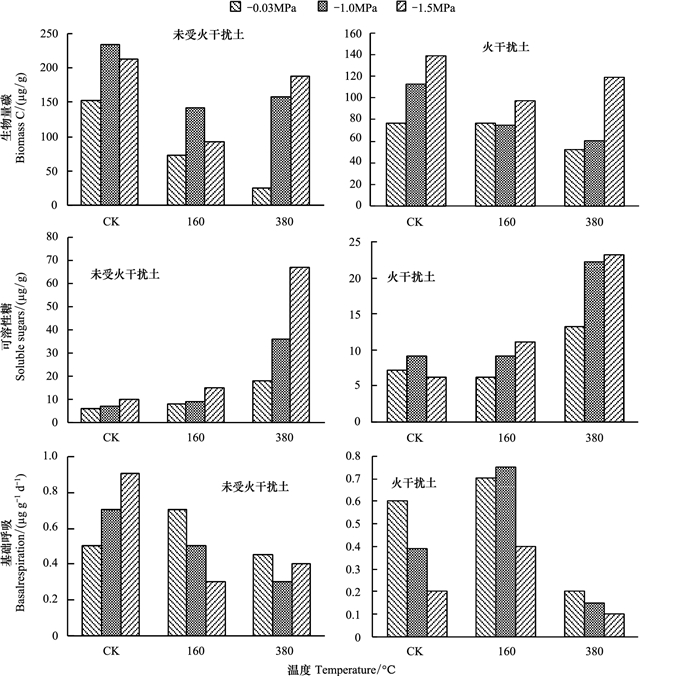
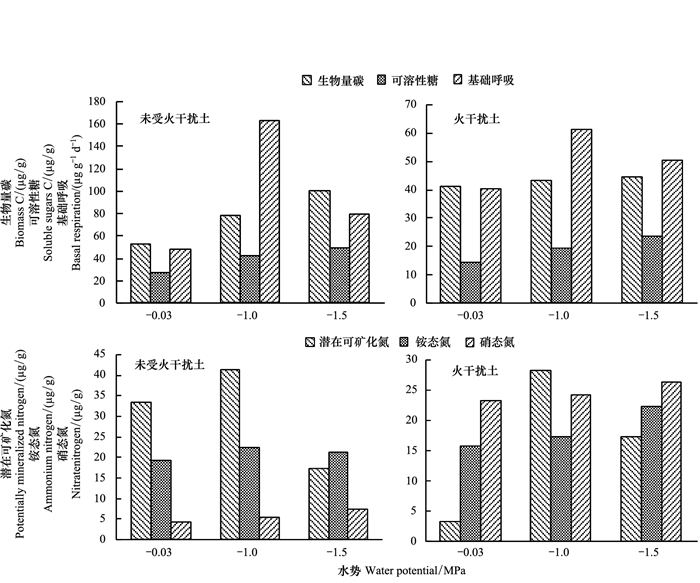
如表 2和图 3, 水势和土壤火干扰之间的交互作用显著影响微生物活动和氮转换, 低水势土壤中的微生物生物量碳、可溶性糖和潜在可矿化氮浓度高, 平均湿度条件下火干扰与受热温度对土壤铵态氮的相互作用影响显著。受热到160℃土壤铵态氮增加 (9%—13.3%), 受火干扰土壤升温到380℃时铵态氮增加42%, 而未受火干扰土壤仅增加6%。土壤历史与水势的相互作用对土壤氮矿化起重要作用, 未受火干扰土壤铵态氮浓度较高, 低水势土壤硝态氮浓度明显较高 (图 2)。
|
| 图 3 3种水势土壤受热14d后微生物生物量碳、可溶性糖和基础呼吸差异 Fig. 3 Difference of soil microbial biomass, soluble sugars and basal respiration at three soil water potentials after 14d exposure of three temperatures |
|
| 图 2 3种水势下土壤微生物生物量碳、水溶性糖、基础呼吸、PMN、铵态氮和硝态氮差异 Fig. 2 Difference of soil microbial biomass C, soluble sugars, basal respiration, PMN, ammonium nitrogen and nitrate nitrogen at three soil water potentials |
受火干扰土壤微生物生物量碳初始浓度较低与先前火干扰造成下层碳损耗和微生物死亡有关[19], 同时, 铵态氮与潜在可矿化氮减少, 较高的硝态氮会增强土壤硝化作用。相反, 硝态氮浓度低的未受火干扰土壤中硝化菌的初始种群受火影响较大, 研究表明大多数生物体在50—120℃被杀死, 且真菌比细菌对热更敏感[4]。潮湿土壤中微生物比干燥土壤死亡率更高, 因为其潜热渗透和热传播影响[7], 然而某种程度上干燥土壤微生物存活率更高可能与土壤预处理增强适应力有关。本次实验温度超过120℃, 因此, 微生物死亡也许是加热后可溶性糖增加的重要因素之一, 这与Diaz-Ravina等研究发现加热后70%的矿化碳来源于死微生物组织的观点一致[5]。此外, 研究发现, 当土壤温度达160℃时, 潜在可矿化氮浓度迅速不稳定增加, 归因于热破坏土壤有机质和热死亡微生物组织, 而未受火干扰土壤中潜在可矿化氮少量增加, 而近80a未受火干扰土壤中潜在可矿化氮显著增加[22], 当温度达350℃导致90%非微生物组织的破坏。
此外, 有机质蒸馏启动温度在200—315℃, 然而有机质燃烧产生的温度远远高于此温度, 导致可燃物完全氧化[23], 伴随氮的潜在挥发, 这与净矿化速度大和土壤铵态氮浓度较高相吻合, 归因于土壤中活的和死的有机物的热解。与Dunn等研究表明无机氮的浓度与火强和初始土壤有机质含量呈正相关关系的研究结果吻合[13]。
2.2 受热处理14d后的影响如图 3和4所示, 培养14d期间土壤火灾历史、热处理和土壤水势对微生物活性、碳和氮矿化有显著影响。-1.5 MPa水势下加热到380℃后两种土壤的微生物生物量碳含量最高, 而-0.03 MPa水势下加热到380℃后微生物生物量碳浓度最低。随着时间的推移, 两种土壤可溶性糖含量显著下降, 但比对照土壤高。培养14d并加热到380℃后可溶性糖浓度最高, 土壤水势和可溶性糖成负相关关系, 干燥土壤可溶性糖积累更多。-0.03 MPa水势下累积二氧化碳演化最激烈, 未受火干扰对照样品土壤的微生物生物量碳、可溶性糖含量最高, -1.5 MPa水势下火干扰土壤中二氧化碳演化较低。培养14d期间两种土壤的潜在可矿化氮都发生改变, 未受火干扰土壤仍保持较高, 高水势对照土壤潜在可矿化氮含量非常低, 受火干扰对照土壤中铵态氮浓度比培养前降低, 随后硝态氮浓度增加。
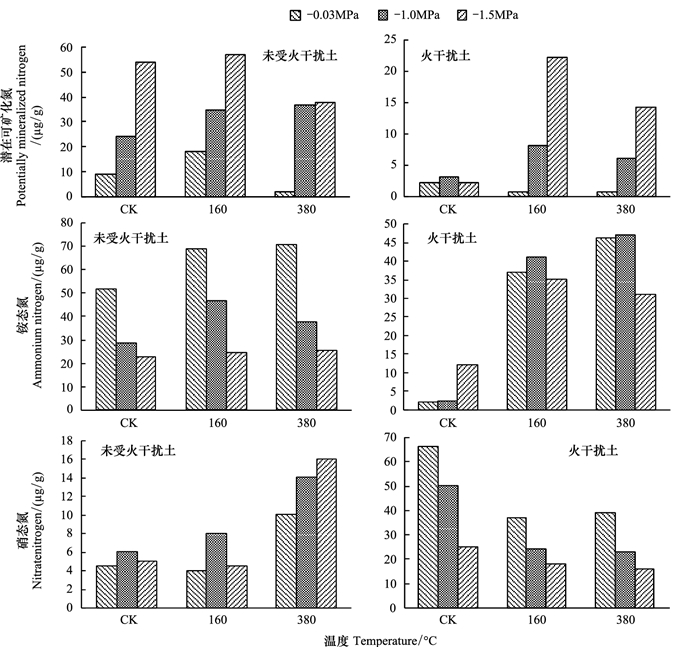
|
| 图 4 3种水势土壤受热14d后土壤潜在可矿化氮、铵态氮和硝态氮差异 Fig. 4 Difference of PMN, ammonium nitrogen and nitrate nitrogen at three soil water potentials after 14d exposure of three temperatures |
未烧对照土壤微生物生物量碳和可溶性糖含量与培养土壤样品相似, 加热后可溶性糖增加与有关学者研究结果一致, 表明干燥和再湿润导致可溶性糖释放, 随后逐渐恢复到火烧前水平[16]。
低水势条件下加热时释放碳和氮与微生物活动有关。两种土壤水溶性糖的浓度因加热而释放显著降低, 然而干燥土壤水溶性糖较高, 归因于碳矿化。加热后的土壤氮库的变化与初始火干扰后矿物与不稳定氮释放及潜在可矿化氮减少类似。火干扰土壤潜在可矿化氮比未受火干扰土壤损失多, 火干扰土壤潜在可矿化氮含量较低归因于热诱导后挥发和不稳定氮的矿化。此外, 试验研究表明, 低强度火干扰下不稳定氮显著比高强度火干扰损失少[19]。土壤加热后水势对氮矿化过程有显著影响, 水势越高, 潜在可矿化氮损失越大, 其次是无机氮净积累。火干扰土壤的含水量与硝态氮之间呈正相关关系, 表明有机物恢复受有效水分的影响比铵态氮更大。样地设置和火干扰状况对土壤含水量有潜在影响, 实验中使用的两种土壤生化成分显著不同与先前是否遭受火干扰关系紧密。之前受火干扰的土壤微生物生物量较低, 但氮矿化率较快, 这反映火干扰后土壤中生物量碳、潜在可矿化氮、可溶性糖和铵态氮浓度较低, 收集土壤样品时火灾后的氮化物已经基本恢复到火前水平, 相反, 未受火干扰土壤中微生物活性相对较高, 铵态氮浓度较低。低土壤水势可以保护新形成的不稳定氮, 干燥土壤比湿润土壤保持更长, 与火干扰历史无关。这种干燥的土壤条件发生在夏季森林火灾和秋季计划烧除, 而潮湿的土壤条件通常发生在春季计划烧除。
通过实验发现, 实验温度超过深层矿质土壤层温度, 火干扰时热量传递到土壤矿质层, 影响土壤多孔介质的绝缘效果和汽化潜热[24]。除可燃物载量特别大的区域, 此次实验控制温度影响最深为土壤表层3 cm。研究结果清楚地证明土壤水分和火灾历史对土壤生化特性的影响。
3 结论与讨论通过实验发现, 实验控制温度主要影响表层 (0—3 cm) 土壤, 火干扰时影响土壤多孔介质的绝缘效果和汽化潜热。研究结果表明火灾历史、土壤水势和火干扰对土壤生化特性产生很大的影响。
火干扰后短期内土壤碳和氮浓度较高, 微生物生物量碳和潜在可矿化氮较低, 火干扰历史和火干扰温度与微生物生物量碳之间的相互关系显著, 土壤生物量碳损失随火干扰温度的增加而增大。受火干扰土壤微生物生物量碳初始浓度较低与先前火干扰造成下层碳损耗和微生物死亡有关, 铵态氮与潜在可矿化氮减少。研究表明当土壤温度达160℃时, 潜在可矿化氮浓度迅速不稳定增加, 温度达350℃导致90%非微生物组织的破坏, 归因于火干扰破坏土壤有机质和导致微生物组织受热死亡。
火干扰林地土壤潜在可矿化氮比未受火干扰土壤损失多, 归因于热诱导后挥发和不稳定氮的矿化, 低强度火干扰下不稳定氮损失比中强度火干扰显著减少。土壤加热后水势对氮矿化过程有显著影响, 水势越高, 潜在可矿化氮损失越大。火干扰土壤的含水量与硝态氮之间呈正相关关系。火干扰后短期内温度和土壤水势对基础呼吸速率的影响不显著, 因为森林地表火产生的温度一般可达400℃以上, 而本研究的试验最高温度控制在380℃, 热量向上辐射较多而向下热传导较少, 因此, 对土壤下层温度及土壤含水量的影响较小, 从而对土壤基础呼吸速率影响不显著。受热后土壤可溶性糖和铵态氮的浓度显著增加, 而受热对硝态氮浓度没有显著的影响, 与两种土壤火灾历史无关。
培养14 d期间, 土壤火灾历史、热处理和土壤水势对微生物活性、碳和氮矿化有显著影响。水势和火干扰之间的交互作用显著影响微生物活动和氮转换, 低水势土壤中的微生物生物量碳、可溶性糖和潜在可矿化氮浓度高, 平均湿度条件下火干扰与受热温度对土壤铵态氮的相互作用影响显著。未受火干扰土壤潜在可矿化氮含量较高, 高水势对照土壤潜在可矿化氮含量非常低, 受火干扰对照土壤中铵态氮浓度比培养前降低, 硝态氮浓度增加。
| [1] | Fernández I, Cabaneiro A, Carballas T. Organic matter changes immediately after a wildfire in an Atlantic forest soil and comparison with laboratory soil heating. Soil Biology and Biochemistry, 1997, 29: 1–11. DOI:10.1016/S0038-0717(96)00289-1 |
| [2] | Hungerford R D, Harrington M G, Frandsen W H, Ryan K C, Niehoff G J. Influence of fire factors that affect site productivity//Harvey A E, Neuenschwande L F, eds. Proceeding of the Management and Productivity of Western Montane Forest Soils. Intermountain Research Station General Technical Report INT-280. USDA-FS, 1991:32-50. |
| [3] | Hernández T, García C, Reinhardt I. Short-term effect of wildfire on the chemical, biochemical and microbiological properties of Mediterranean pine forest soils. Biology and Fertility of Soils, 1997, 25: 109–116. DOI:10.1007/s003740050289 |
| [4] | Neary D G, Klopatek C C, DeBano L F, Folliott P F. Fire effects on belowground sustainability:a review and synthesis. Forest Ecology and Management, 1999, 122: 51–71. DOI:10.1016/S0378-1127(99)00032-8 |
| [5] | Díaz-Raviña M, Prieto A, Bååth E. Bacterial activity in a forest soil after soil heating and organic amendments measured by the thymidine and leucine incorporation technique. Soil Biology and Biochemistry, 1996, 28: 419–426. DOI:10.1016/0038-0717(95)00156-5 |
| [6] | Giovannini G, Lucchesi S, Giachetti M. Effects of heating on some chemical parameters related to soil fertility and plant growth. Soil Science, 1990, 149: 344–350. DOI:10.1097/00010694-199006000-00005 |
| [7] | Campbell G S, Jungbauer J D, Bidlake W R, Hungerford R D. Predicting the effect of temperature on soil thermal conductivity. Soil Science, 1994, 158: 307–313. DOI:10.1097/00010694-199411000-00001 |
| [8] | Albini F A, Reinhardt E D. Modeling ignition and burning rate of large woody natural fuels. International Journal of Wildland Fire, 1995, 5: 81–91. DOI:10.1071/WF9950081 |
| [9] | Baker K F. Selective killing of soil microorganisms by aerated steam//Toussoun T A, Bega R V, Nelson P E, Eds. Root Disease and Soil-Borne Pathogens. University of California Press, 1970:234-238. |
| [10] | 陶玉柱. 火对塔河森林土壤微生物及酶活性的干扰作用[D]. 哈尔滨: 东北林业大学, 2014. |
| [11] | 杨玉莲. 模拟增温对高山森林土壤微生物和酶活性的影响[D]. 雅安: 四川农业大学, 2012. |
| [12] | Arno S F, Harrington M G, Fiedler C F, Carlson C E. Restoring fire-dependent ponderosa pine forests in Western Montana. Restoration Management Notes, 1995, 13: 32–36. |
| [13] | Dunn P H, Barro S C, Poth M. Soil moisture affects survival of microorganisms in heated chaparral soil. Soil Biology and Biochemistry, 1985, 17: 143–148. DOI:10.1016/0038-0717(85)90105-1 |
| [14] | 吕爱锋, 田汉勤, 刘永强. 火干扰与生态系统的碳循环. 生态学报, 2005, 25(10): 2734–2743. DOI:10.3321/j.issn:1000-0933.2005.10.040 |
| [15] | 韩春兰, 邵帅, 王秋兵, 李甄, 孙仲秀, 毛伟伟. 兴安落叶松林火干扰后土壤有机碳含量变化. 生态学报, 2015, 35(9): 3023–3033. |
| [16] | Yang J E, Skogley E O, Schaff B E, Kim J J. A simple spectro-photometric determination of nitrate in water, resin, and soil extracts. Soil Science Society of America Journal, 1998, 62: 1108–1115. DOI:10.2136/sssaj1998.03615995006200040036x |
| [17] | Joergensen R G, Brookes P C. Ninhydrin-reactive N measurements of microbial biomass in 0.5 m K2SO4 soil extracts. Soil Biology and Biochemistry, 1990, 22(8): 1023–1027. DOI:10.1016/0038-0717(90)90027-W |
| [18] | DeLuca T H, Keeney D R. Ethanol stabilized chloroform as a fumigant for estimating microbial biomass by reaction with ninhydrin. Soil Biology and Biochemistry, 1993, 25: 1297–1298. DOI:10.1016/0038-0717(93)90229-5 |
| [19] | Zibilske L M. Carbon mineralization. Soil Science Society of America, 1994: 835–863. |
| [20] | SAS Institute. SAS user's guide.6th ed. Cary, NC: SAS Institute, 1995. |
| [21] | Raich JW, Potter CS. Global pat terns of carbon dioxide emissions from soils. Global Biogeochem Cycles, 1995, 9: 23–36. DOI:10.1029/94GB02723 |
| [22] | Choromanska U, DeLuca T H. Prescribed fire alters the impact of wildfire on soil biochemical properties in a ponderosa pine forest. Soil Science Society of America Journal, 2001, 65: 232–238. DOI:10.2136/sssaj2001.651232x |
| [23] | Pietikäinen J, Hiukka R, Fritze H. Does short-term heating of forest humus change its properties as a substrate for microbes?. Soil Biology and Biochemistry, 2000, 32: 277–288. DOI:10.1016/S0038-0717(99)00164-9 |
| [24] | 刘发林, 张思玉. 火干扰下马尾松林物种多样性和土壤养分特征. 西北林学院学报, 2009, 24(5): 36–40. |
 2017, Vol. 37
2017, Vol. 37