文章信息
- 韩永强, 弓少龙, 文礼章, 侯茂林
- HAN Yongqiang, GONG Shaolong, WEN Lizhang, HOU Maolin.
- 水稻施用硅肥对稻纵卷叶螟幼虫取食和成虫产卵选择性的影响
- Effect of silicon addition to rice plants on Cnaphalocrocis medinalis feeding and oviposition preference
- 生态学报. 2017, 37(5): 1623-1629
- Acta Ecologica Sinica. 2017, 37(5): 1623-1629
- http://dx.doi.org/10.5846/stxb201510092034
-
文章历史
- 收稿日期: 2015-10-09
- 网络出版日期: 2016-07-13
2. 湖南农业大学植物保护学院, 长沙 410128
2. College of Plant Protection, Hunan Agricultural University, Changsha 410128, China
稻纵卷叶螟Cnaphalocrocis medinalis (Guenée) 属鳞翅目螟蛾科, 是水稻上重要的迁飞性害虫, 主要分布在亚洲、大洋洲、东非等国家和地区[1]。在我国, 东起台湾, 西至西藏, 南至海南, 北到黑龙江, 28个省 (市、区) 均有发生危害[1]。近年来, 耕作制度改革、水稻品种更新及适宜的气候条件等诸多因素在一定程度上加剧了稻纵卷叶螟的发生和为害。该虫在2003年出现全国性特大暴发, 此后连年猖獗为害, 2007年再次出现全国性大暴发, 发生面积高达2530万hm2, 给我国水稻生产造成严重的经济损失[2]。此外, 稻纵卷叶螟对常用杀虫剂的抗药性有所增强, 这增大了其防治难度和成本。面对这种发生态势, 增强水稻对稻纵卷叶螟的抗性成为其综合治理的重要组分。除遗传途经外, 栽培管理也有望调节水稻对稻纵卷叶螟的抗性, 如增施硅肥。
硅是地壳中含量最丰富的元素之一, 仅次于氧, 居第二位。虽然硅不是植物的必需营养元素, 但硅在增强植物抗病性和抗虫性方面都具有重要作用。多数研究表明施用硅肥能提高植株硅含量, 从而增强植物对植食性昆虫的抗性[3-8]。如施用硅肥提高禾本科杂草的叶片粗糙度、阻碍食叶昆虫取食、延缓发育、降低食物同化效率[3];改变植物叶表面特性[9];促进植物挥发性次生物质的合成和释放, 进而影响植食性昆虫的产卵和取食选择[10]。抗稻纵卷叶螟水稻品种的一个显著特征是叶片硅含量高或硅细胞密度高[11-12]。水稻是典型的喜硅作物, 有“硅酸植物”之称, 具有主动吸收和富集硅的能力[13]。因此, 有望通过施用硅肥来提高水稻植株的硅含量, 进而增强其抗虫性。本文对盆栽水稻施用硅肥, 研究施硅对稻纵卷叶螟产卵和取食选择性的影响, 以期为通过施用硅肥来调控稻纵卷叶螟种群及其综合防治提供理论基础。
1 材料与方法 1.1 水稻及硅处理供试水稻品种为TN1(感虫品种)。水稻种子在50℃温水中浸种24 h后置于人工气候箱催芽72 h。以塑料育秧盒 (长×宽×高:75 cm×45 cm×15 cm) 作苗床播种, 第25日移栽。秧苗双本移栽到10 L的塑料桶 (直径×高:24.5 cm×20 cm) 中, 每桶移栽2穴。塑料桶内装同一批同质烘干的砂质壤土 (有机质含量2.19%, 全氮含量1.58 g/kg, 速效磷含量3.22 mg/kg, 速效钾含量98.16 mg/kg, 有效硅含量0.21 g/kg), 每桶装4.2 kg干土。
根据土壤有效硅含量和水稻对硅的需求量, 硅钙钾肥 (山西富邦肥业有限公司, 可溶性硅含量≥11.7%, CaO≥25.0, K2O≥4.0%, MgO≥2.0) 按照g Si/kg土壤的比例施用, 共设置3个水平 (按有效成分Si计算):(1)0 g/kg (对照);(2)0.16 g/kg (低硅处理);(3)0.32 g/kg (高硅处理)。
各处理均按每千克土壤施用纯氮0.37 g (包括磷酸二铵中纯氮的量和尿素中纯氮的量;尿素, 含N≥46.4%)、五氧化二磷0.25 g (磷酸二铵, 含N 16%、P2O5 44%)、氧化钾0.35 g (包括硅钙钾肥中K2O的量和氯化钾中K2O的量;氯化钾, K2O≥60%)。施硅处理和不施硅处理的氮、磷、钾肥施用量相同。尿素分4次施用:移栽前 (4/10)、分蘖期 (3/10)、抽穗期 (2/10)、乳熟期 (1/10), 磷酸二铵移栽前一次施用, 氯化钾分两次施用:移栽前 (2/3)、抽穗期 (1/3)。硅钙钾肥于移栽前72 h与基肥混合一次施用, 肥料施用后搅拌。
盆栽稻苗共分为两部分, 一部分置于室外自然感虫, 各处理盆栽稻苗完全随机排列;另一部分置于温室内, 防止自然发生害虫的为害。盆栽稻苗不施用杀虫剂, 按照水稻各生育期的需水规律浇水, 浇水量最多以不漫过桶沿为限。
1.2 供试虫源于2013年6月下旬成虫盛发时, 在农业部桂林有害生物野外科学观测实验站 (广西桂林市兴安县) 稻田内用捕虫网捕捉成虫, 然后将其置于圆柱形纱网笼罩 (纱网直径×高=123 cm×103 cm;内衬圆柱形铁丝框架, 直径×高=120 cm×100 cm) 中集体交配, 选取移栽后40 d的对照盆栽稻株, 放入笼罩内, 供稻纵卷叶螟卷成虫产卵, 产卵后, 剪取带有卵粒的水稻叶片, 一端用脱脂棉保湿, 置于铺有湿润滤纸的培养皿 (直径×高=9 cm×2 cm) 中。培养皿置于人工气候箱中 ((28±1)℃, RH (70±5)%, L : D=16 : 8 h), 逐日观察虫卵孵化情况, 选取部分初孵或3龄幼虫供试。其余的幼虫用对照水稻叶片饲养至化蛹, 取羽化后的雌雄成虫备用。
1.3 硅处理对土壤硅含量的影响于移栽前和移栽后60 d采集土壤用于测定硅含量。移栽后取样时, 每处理随机挑选5盆盆栽稻株用于土壤取样, 取样后将相同处理不同盆栽的土壤进行合并, 共4种土壤样品。土壤样品在105℃下烘干至恒重, 粉碎后过80目筛的样品备用, 采用醋酸缓冲液浸提法测定土壤硅含量[14]。
1.4 硅处理对水稻叶片硅含量和碳氮比的影响从移栽后40日龄TN1盆栽水稻上剪取相同叶位的叶片 (即40日龄稻苗包括心叶在内的倒数第2片完全叶, 叶片分化完成后的倒四叶) 各50片左右。叶片在110℃下杀青15 min, 后在80℃下烘干至恒重, 叶片干样用于硅含量、总氮含量和可溶性糖含量测定。将烘干后的叶片用食物粉碎机粉碎, 过60目筛的粉末用于测定硅含量[15]。叶片总氮含量和可溶性糖含量分别采用凯氏定氮法和蒽酮比色法测定[16], 根据总氮含量和可溶性糖含量计算叶片碳氮比 (C/N)。不同处理每个指标采用不同样品重复测定3次。
1.5 稻纵卷叶螟初孵和3龄幼虫对硅处理水稻的选择性选取移栽后40日龄不同硅处理TN1盆栽稻株, 每处理剪取倒四叶2片, 3个处理共6片叶, 每片叶长约6 cm, 一端用脱脂棉保湿, 将上述6片叶等距离排列在1个底部铺有湿润滤纸的白色圆盘 (半径30 cm) 中, 在圆心处接入30头初孵幼虫, 5 h后计数各叶片上的幼虫数。重复15次。针对3龄幼虫的实验方法类似, 不同的是在圆心处接入2头饥饿2 h (保持在有湿润滤纸的培养皿中) 的3龄幼虫, 持续观察直至幼虫停留在某一水稻叶片并开始取食后, 或者持续观察至30 min后停止实验。重复35次。
1.6 稻纵卷叶螟成虫对硅处理水稻的产卵选择性采用笼罩法测定稻纵卷叶螟成虫的产卵选择性。选取移栽后40日龄不同硅处理TN1盆栽稻株各2盆, 3个硅处理共6盆, 去除枯黄叶片及叶鞘, 每盆保留10株健壮分蘖, 将不同硅处理的6盆稻株等距离顺序排列在一个圆上 (盆外缘在直径120 cm内)。仔细清除稻苗上的其他任何昆虫后, 用圆柱形尼龙纱笼 (纱网直径×高=123 cm×103 cm;内衬圆柱形铁丝框架, 直径×高=120 cm×100 cm) 罩住。每笼罩接入12对稻纵卷叶螟雌雄成虫, 并饲以15%蜂蜜水, 任其自由产卵。72 h后计数各处理水稻上的卵粒数, 计算产卵量和着卵率。着卵率=(每处理水稻上的卵粒数/笼罩内所有处理水稻上的卵粒数)×100%。1个笼罩为1次重复, 设9次重复, 重复之间轮换笼罩内各处理稻苗的相对位置。产卵选择性试验在室外自然温度和光照下进行。
1.7 硅处理水稻对稻纵卷叶螟为害的影响盆栽稻苗室外自然感虫, 随机选择移栽后40日龄不同硅处理TN1盆栽稻株各15盆, 计数每盆稻株的分蘖数、叶片总数、卷叶株数和卷叶数, 计算卷叶株率和卷叶率。卷叶株率 (%)=(卷叶株数/分蘖数)×100;卷叶率 (%)=(卷叶数/叶片总数)×100。
1.8 数据分析试验所得数据采用SPSS 16.0统计软件进行单因素方差分析 (ANOVA), 用Tukey测验法比较不同处理间的差异显著性。百分数数据在方差分析前进行平方根反正弦转换, 以满足方差分析要求。
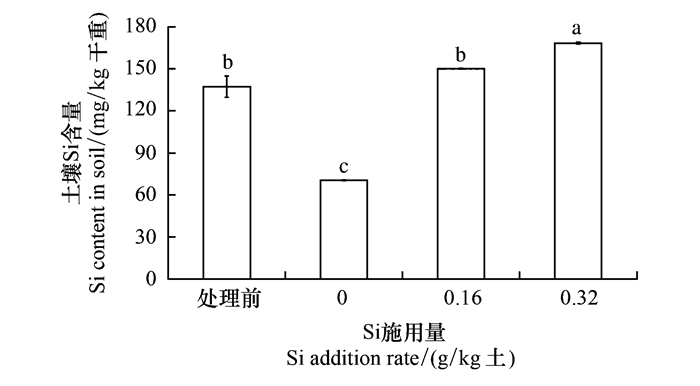
2 结果与分析 2.1 硅处理对土壤硅含量的影响施用硅肥或不施硅肥盆栽60 d后, 盆栽土壤Si含量与盆栽前土壤Si含量之间存在显著差异 (F=124.532, df=3, 11, P<0.001)(图 1)。相对于处理前的土壤, 高硅和低硅处理盆栽土壤的Si含量在60 d后分别上升了22.7%和9.3%, 而不施硅肥盆栽土壤的Si含量却下降了48.6%(图 1)。
|
| 图 1 施硅前和施硅60 d后土壤硅含量 Fig. 1 Soil silicon contents before and 60 d after Si addition |
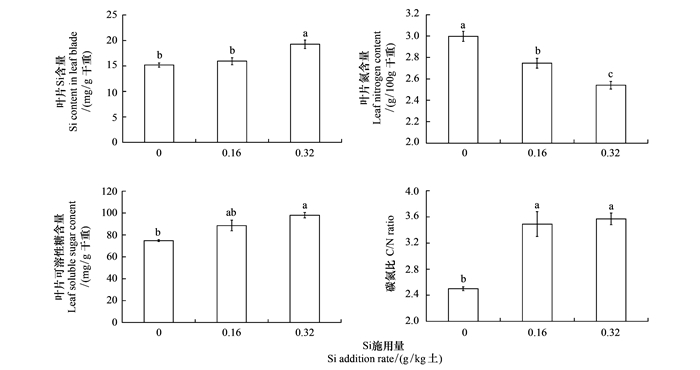
硅处理显著影响水稻叶片Si含量 (F=10.185, df=2, 8, P=0.012) 和可溶性糖含量 (F=13.255, df=2, 8, P=0.006;图 2)。高硅处理水稻叶片的Si和可溶性糖含量分别比对照显著增加26.7%和30.9%。
|
| 图 2 硅处理对水稻对叶片硅含量、可溶性糖含量、氮含量和碳氮比的影响 Fig. 2 Effects of silicon addition to rice plants on contents of silicon, soluble sugar, nitrogen and C : N ratio in rice leaves |
水稻叶片的氮含量 (F=27.257, df=2, 8, P=0.001) 随硅施用量的增加而逐渐降低, 在不同处理间存在显著差异 (图 2)。高硅和低硅处理水稻叶片的氮含量分别比对照显著降低15.2%和8.3%。施用硅肥显著增大水稻叶片的碳氮比 (F=23.703, df=2, 8, P=0.001)(图 2), 高硅和低硅处理水稻叶片的碳氮比分别比对照显著增加42.8%和39.6%。
2.3 稻纵卷叶螟幼虫对不同硅处理水稻的选择性稻纵卷叶螟初孵和3龄幼虫对不同硅处理水稻叶片的选择性随硅施用量的增加而逐渐降低, 在不同处理间存在显著差异 (初孵幼虫, F=89.16, df=2, 47, P<0.001, 图 3;3龄幼虫, F=64.866, df=2, 50, P<0.001, 图 3)。稻纵卷叶螟初孵幼虫对高硅和低硅处理水稻叶片的选择比例分别比对照低33.1%和26.7%;3龄幼虫对高硅和低硅处理水稻叶片的选择比例分别比对照低30.9%和20.8%。

|
| 图 3 稻纵卷叶螟幼虫对不同硅处理水稻的选择性 Fig. 3 Preference of C. medinalis larvae for rice leaves from plants with or without Si addition |
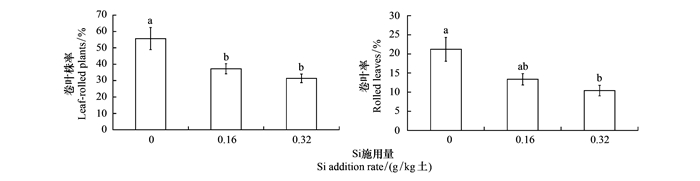
硅处理水稻上稻纵卷叶螟的着卵量 (F=7.137, df=2, 26, P=0.004;图 4) 和着卵率 (F=17.936, df=2, 26, P<0.001;图 4) 均显著降低。稻纵卷叶螟成虫在高硅和低硅处理水稻上的着卵量分别比对照减少45.3%和27.6%;着卵率分别比对照降低18.6%和11.0%。2.5硅处理水稻对稻纵卷叶螟为害的影响硅处理显著影响水稻的卷叶株率 (F=7.716, df=2, 44, P=0.001) 和卷叶率 (F=6.215, df=2, 44, P=0.004)(图 5)。高硅处理水稻的卷叶株率和卷叶率分别比对照显著降低24.3%和10.8%。

|
| 图 4 稻纵卷叶螟成虫对不同硅处理水稻的产卵选择性 Fig. 4 C. medinalis oviposition preference for silicon-treated and control rice plants |
|
| 图 5 不同硅处理水稻对稻纵卷叶螟为害的影响 Fig. 5 Effects of silicon addition to rice plants on percentage of leaf-rolled plants and rolled leaves |
植物抗虫性, 是害虫与植物之间在一定条件下相互作用的表现。植物抗虫机制表现为抗生性、耐害性和不选择性3个方面。不选择性是指昆虫不趋向植物栖息、产卵或取食的一些特性。植物的表面形态、生理生化特性和分泌的挥发性次生物质可以阻止昆虫趋向植物产卵或取食, 从而避免或减轻害虫的为害。结果表明, 稻纵卷叶螟初孵和3龄幼虫对硅处理水稻叶片的选择比例显著低于对照, 同时硅处理显著降低水稻的卷叶株率和卷叶率以及稻纵卷叶螟的着卵量和着卵率。水稻是典型的硅酸植物, 可以主动吸收和富集硅[13]。硅富集在水稻茎秆、叶鞘和叶片的表皮细胞, 增加植物组织的硬度和粗糙度, 降低植物可消化性[3, 17], 这可能有助于降低施硅水稻的卷叶率。前人就不同抗性水稻品种对稻纵卷叶螟的选择行为进行了研究。稻纵卷叶螟1龄和3龄幼虫对感虫品种水稻叶片的选择性显著高于抗虫品种[12, 18], 稻纵卷叶螟成虫在感虫水稻品种上的着卵量显著高于抗虫品种[18]。施用硅肥增强稻纵卷叶螟对水稻不选择性的机制尚不清楚, 有研究表明硅在植物叶表面的绒毛、毛状体和刺等附属物沉积, 改变叶表面形态特性[9], 增加植物挥发性次生物质的释放[10], 本研究中施硅增大叶片硅含量, 从而可能改变叶片的表明形态特性和挥发性次生物质的释放, 导致稻纵卷叶螟不选择施硅水稻, 这也可能是施硅水稻受害率下降的原因之一。此外, 也有一些研究表明, 植物体内硅的排列方式和沉积位点对植食性昆虫取食为害的阻抗作用比植物硅含量本身更为重要。如野生稻叶表皮硅细胞排列紧密, 杂交稻叶表皮硅细胞排列疏松, 相比较而言, 野生稻对稻纵卷叶螟的抗性更高[19]。
硅处理显著提高叶片可溶性糖含量。可溶性糖是高等植物的主要光合产物, 也是碳水化合物代谢和暂时储藏的主要形式, 在植物代谢中具有重要作用, 是植物体内重要的抗逆调节物质, 与植物抗虫性密切相关[20-21]。植物组织中的糖含量过高或过低均不利于昆虫的生长发育, 可溶性糖含量高可以提高植物自身的抗性水平[22]。施用硅肥可以促进水稻叶片光合产物运输, 显著提高叶片可溶性糖含量, 在一定程度上可能对害虫的取食危害具有补偿作用, 进而增强其耐害性。
硅处理显著降低叶片氮含量、提高叶片碳氮比。一般而言, 植物组织中高的C/N比和低的含氮量, 降低了植物对植食性昆虫取食的营养价值, 进而导致植食性昆虫取食增加、发育延缓、繁殖力下降等一系列反应, 对大多数植食性昆虫的种群发展是不利的[23]。硅通过什么途径改变植物对植食性昆虫的营养价值, 这还有待于深入研究。
施硅通过降低稻纵卷叶螟幼虫的食物转化效率而增强施硅水稻对其抗生性[8]。硅处理水稻叶片的硅含量、可溶性糖含量和碳氮比升高, 而氮含量降低;施硅导致稻纵卷叶螟幼虫对水稻叶片的取食选择性和成虫的着卵量及着卵率下降, 并进而降低水稻的卷叶株率和卷叶率。因此, 施用硅肥还可以通过降低稻纵卷叶螟幼虫和成虫对施硅水稻的选择性来增强水稻的抗虫性。
施用硅肥对土壤和水稻具有多种良好的生理效应, 如增强水稻的抗病性[24]、抗倒性[25]、对极端温度的抗性[26]和抗紫外线辐射能力[27], 提高水分利用效率[28], 促进稻穗发育和提高稻米产量和品质[17, 29]。因此, 可以通过施用硅肥来综合调控水稻的生长发育和水稻对稻纵卷叶螟的抗虫性。
| [1] | 张孝羲, 陆自强, 耿济国, 李国柱, 陈学礼, 吴学文. 稻纵卷叶螟迁飞途径的研究. 昆虫学报, 1980, 23(2): 130–140. |
| [2] | 刘宇, 王建强, 冯晓东, 蒋学辉. 2007年全国稻纵卷叶螟发生实况分析与2008年发生趋势预测. 中国植保导刊, 2008, 28(7): 33–35. |
| [3] | Massey F P, Ennos A R, Hartley S E. Silica in grasses as a defence against insect herbivores:contrasting effects on folivores and a phloem feeder. Journal of Animal Ecology, 2006, 75(2): 595–603. DOI:10.1111/jae.2006.75.issue-2 |
| [4] | 韩永强, 刘川, 侯茂林. 硅介导的水稻对二化螟幼虫钻蛀行为的影响. 生态学报, 2010, 30(21): 5967–5974. |
| [5] | Hou M L, Han Y Q. Silicon-mediated rice plant resistance to the Asiatic rice borer (Lepidoptera:Crambidae):effects of silicon amendment and rice varietal resistance. Journal of Economic Entomology, 2010, 103(4): 1412–1419. DOI:10.1603/EC09341 |
| [6] | Ye M, Song Y Y, Long J, Wang R L, Baerson S R, Pan Z Q, Zhu-Salzman K, Xie J F, Cai K Z, Luo S M, Zeng R S. Priming of jasmonate-mediated antiherbivore defense responses in rice by silicon. Proceedings of the National Academy of Sciences of the United States of America, 2013, 110(38): E3631–E3639.. DOI:10.1073/pnas.1305848110 |
| [7] | Sidhu J K, Stout M J, Blouin D C, Datnoff L E. Effect of silicon soil amendment on performance of sugarcane borer, Diatraea saccharalis (Lepidoptera:Crambidae) on rice. Bulletin of Entomological Research, 2013, 103(6): 656–664. DOI:10.1017/S0007485313000369 |
| [8] | Han Y Q, Lei W B, Wen L Z, Hou M L. Silicon-mediated resistance in a susceptible rice variety to the rice leaf folder, Cnaphalocrocis medinalis Guenée (Lepidoptera:Pyralidae). PLoS One, 2015, 10(4): e0120557. DOI:10.1371/journal.pone.0120557 |
| [9] | Hartley S E, Fitt R N, McLarnon E L, Wade R N. Defending the leaf surface:intra-and inter-specific differences in silicon deposition in grasses in response to damage and silicon supply. Frontiers in Plant Science, 2015, 6(1): 35–35. |
| [10] | Kvedaras O L, An M, Choi Y S, Gurr G M. Silicon enhances natural enemy attraction and biological control through induced plant defences. Bulletin of Entomological Research, 2010, 100(3): 367–371. DOI:10.1017/S0007485309990265 |
| [11] | Sudhakar G K, Sudhakar S, Mishra S B. Susceptibility of rice varieties of different durations to rice leaf folder, Cnaphalocrocis medinalisGuen. evaluated under varied land situations. Journal of Entomological Research, 1991, 15(2): 79–87. |
| [12] | 王亓翔.水稻抗稻纵卷叶螟鉴定方法及抗性机制研究[D].扬州:扬州大学, 2009. |
| [13] | Ma J F, Tamai K, Yamaji N, Mitani N, Konishi S, Katsuhara M, Ishiguro M, Murata Y, Yano M. A silicon transporter in rice. Nature, 2006, 440(7084): 688–691. DOI:10.1038/nature04590 |
| [14] | 鲍士旦. 土壤农化分析.第三版. 北京: 中国农业出版社, 2000. |
| [15] | 戴伟民, 张克勤, 段彬伍, 孙成效, 郑康乐, 蔡润, 庄杰云. 测定水稻硅含量的一种简易方法. 中国水稻科学, 2005, 19(5): 460–462. |
| [16] | 王学奎. 植物生理生化实验原理和技术.第二版. 北京: 高等教育出版社, 2006. |
| [17] | Ma J F, Miyake Y, Takahashi E. Silicon as a beneficial element for crop plants//Datnoff L E, Snyder G H, Korndorfer G H, eds. Silicon in Agriculture. Amsterdam: Elsevier Science, 2001: 17-39. |
| [18] | 田卉.重庆稻区主栽水稻品种对稻纵卷叶螟的抗性评价及防治指标研究[D].重庆:西南大学, 2013. |
| [19] | Ramachandran R, Khan Z R. Mechanisms of resistance in wild rice Oryza brachyantha to rice leaffolder Cnaphalocrocis medinalis (Guenée) (Lepidoptera:Pyralidae). Journal of Chemical Ecology, 1991, 17(1): 41–65. DOI:10.1007/BF00994421 |
| [20] | 覃光球, 严重玲, 韦莉莉. 秋茄幼苗叶片单宁、可溶性糖和脯氨酸含量对Cd胁迫的响应. 生态学报, 2006, 26(10): 3366–3371. |
| [21] | Koyama K, Mitsuhashi J. Rearing of the white-backed planthopper, Sogatella furcifera Horvath (Hemiptera:Delphacidae) on a synthetic diet. Japanese Journal of Applied Entomology and Zoology, 1980, 24(2): 117–119. DOI:10.1303/jjaez.24.117 |
| [22] | 李进步, 方丽平, 吕昭智, 张铮. 棉花抗蚜性与可溶性糖含量的关系. 植物保护, 2008, 34(2): 26–30. |
| [23] | Watt A D, Whittaker J B, Docherty M, Brooks G, Lindsay E, Salt D T. The impact of elevated atmospheric CO2 on insect herbivores//Harrington R, Stork N E, eds. Insects in a Changing Environment: Symposium of the Royal Entomological Society. New York: Academic Press, 1993: 198-217. |
| [24] | Cai K Z, Gao D, Luo S M, Zeng R S, Yang J Y, Zhu X Y. Physiological and cytological mechanisms of silicon-induced resistance in rice against blast disease. Physiologia Plantarum, 2008, 134(2): 324–333. DOI:10.1111/ppl.2008.134.issue-2 |
| [25] | Epstein E. Silicon. Annual Review of Plant Physiology and Plant Molecular Biology, 1999, 50: 641–664. DOI:10.1146/annurev.arplant.50.1.641 |
| [26] | 吴晨阳, 姚仪敏, 邵平, 王燚, 汪志威, 田小海. 外源硅减轻高温引起的杂交水稻结实降低. 中国水稻科学, 2014, 28(1): 71–77. |
| [27] | Goto M, Ehara H, Karita S, Takabe K, Ogawa N, Yamada Y, Ogawa S, Yahaya M S, Morita O. Protective effect of silicon on phenolic biosynthesis and ultraviolet spectral stress in rice crop. Plant Science, 2003, 164(3): 349–356. DOI:10.1016/S0168-9452(02)00419-3 |
| [28] | Gao X P, Zou C Q, Wang L J, Zhang F S. Silicon improves water use efficiency in maize plants. Journal of Plant Nutrition, 2005, 27(8): 1457–1470. DOI:10.1081/PLN-200025865 |
| [29] | Alvarez J, Datnoff L E. The economic potential of silicon for integrated management and sustainable rice production. Crop Protection, 2001, 20(1): 43–48. DOI:10.1016/S0261-2194(00)00051-X |
 2017, Vol. 37
2017, Vol. 37




