文章信息
- 冯建新, 熊德成, 邓飞, 史顺增, 许辰森, 钟波元, 陈云玉, 陈光水
- FENG Jianxin, XIONG Decheng, DENG Fei, SHI Shunzeng, XU Chensen, ZHONG Boyuan, CHEN Yunyu, CHEN Gunagshui.
- 土壤增温、隔离降水及其交互作用对杉木幼苗细根生产的影响
- Effects of soil warming and precipitation exclusion and their interaction on fine roots production of Chinese fir (Cunninghamia lanceolata) seedlings
- 生态学报. 2017, 37(4): 1119-1127
- Acta Ecologica Sinica. 2017, 37(4): 1119-1127
- http://dx.doi.org/10.5846/stxb201606211207
-
文章历史
- 收稿日期: 2016-06-21
- 修订日期: 2016-08-24
2. 湿润亚热带山地生态国家重点实验室培育基地, 福州 350007
2. State Key Laboratory of Subtropical Mountain Ecology (Funded by Ministry of Science and Technology and Fujian Province), Fujian Normal University, Fuzhou 350007, China
据IPCC (2013) 报告, 最近130年 (1880-2012) 全球海陆表面平均温度呈线性上升趋势, 升高了0.85 ℃; 在许多中纬度和亚热带干旱地区平均降水可能会减少, 而在许多中纬度湿润地区平均降水可能会增加[1]。在全球变暖背景下, 全球平均呈干旱化的趋势, 未来30至90年, 降水量的减少和土壤蒸发量增加导致未来多数地区将面对严重和大面积的干旱[2], 同时全球变暖及降水格局的改变将显著影响陆地生态系统的结构与功能[3-4]。因此研究土壤增温和降水减少对森林生态系统的响应对维持生态系统生产力和森林碳汇储量等方面具有一定的作用。
细根 (≤2 mm) 一般是根系最重要的部分[5], 其生产力占森林净初级生产力的3%-84%[6]。虽然细根生产在生态系统碳、养分和水循环过程中起着重要的作用, 但是至今, 我们还是不能科学解释细根生产如何响应多变的环境因子[7]。目前, 有关土壤增温对细根生产的影响不一, 很难发现一致的规律。Wan等[8]通过增加温室空气温度的方法提升了土壤在10 cm深度的温度 (+1.2 ℃), 发现与对照相比, 增温促进红枫 (Acer rubrum) 和糖枫 (Acer saccharum) 幼苗细根生产; Bai等[9]对中国北方半干旱温带草原研究发现土壤增温降低了年均根生产量; 此外, 有研究显示在氮贫瘠的土壤, 土壤增温对花旗松细根生产没有影响[10]。而大多数研究发现隔离降水试验会促进细根生产, 例如Joslin等[11]对美国南部成熟阔叶林进行隔离降水试验发现与对照相比, 隔离33%降水量的样地会促进细根生产。但迄今为止, 关于土壤增温与隔离降水交互试验对细根生产的影响鲜有报道, 因此开展土壤增温和隔离降水对细根生产的影响研究是十分重要的, 亦为全球变化下研究森林生态系统生产力提供科学依据。
我国湿润亚热带区域是全球同纬度少有的绿洲。该区是我国最重要的人工商品林基地, 其中杉木林是我国最重要的人工林之一, 面积占世界人工林面积的6%(我国人工林面积占世界1/3), 在我国林业生产和森林碳吸存中发挥着重要的作用[12]。相比其它气候带, 热带亚热带森林的增温和降水隔离的研究只有少数几例[13-14], 因此, 在我国亚热带区域开展相关研究是十分有意义的。为此本文以福建省三明市陈大国有林场杉木幼苗为研究对象, 通过模拟增温和隔离降水试验来研究土壤增温与降水减少对杉木幼苗细根生产的影响, 对我国湿润亚热带人工林生产力的科学预测和适应全球环境变化等有重要的指导意义。
1 试验区概况与研究方法 1.1 试验区概况试验地位于福建三明森林生态系统与全球变化研究站陈大观测点, 金丝湾森林公园陈大林业国有林场内 (26°19′N, 117°36′E)。平均海拔300 m, 属中亚热带季风气候, 年均气温19.1 ℃, 年均降水量1749 mm (主要集中在3-8月份), 年均蒸发量1585 mm, 相对湿度81%。
1.2 试验设计试验采用完全随机设计, 设置土壤增温×隔离降水双因子, 共4个处理, 即1) 对照 (CK):不增温, 不隔离降水; 2) 增温:增温5 ℃, 不隔离降水; 3) 隔离降水 (WP):不增温, 隔离降水50%;4) 增温+隔离降水 (WP):增温5 ℃, 隔离降水50%, 小区面积2 m×2 m, 每个处理5个重复。试验小区四周采用4块PVC板 (200 cm×70 cm深) 焊接而成, 与周围土壤隔开, 防止小区之间相互干扰。小区土壤取自附近的杉木林土壤, 分层 (0-10、10-20、20-70 cm) 取回, 剔除粗根、石块和其他杂物后, 土壤分层混合均匀, 并按20-70、10-20 cm和0-10 cm重填回2 m×2 m实验小区内, 同时采用压实法调整土壤容重与原位土壤容重接近 (表 1)。于2013年10月安装加热电缆 (所有小区都布设相同电缆), 平行布设, 深度为10 cm, 间距20 cm, 并在最外围环绕1圈, 保证样地增温的均匀性。2013年11月, 每个2 m×2 m小区均匀种植4棵1年生2代半短侧枝杉木幼苗, 平均高度为 (25.7±2.52) cm, 平均主干基径为 (3.35±0.48) cm, 杉木位置均处于两条电缆线之间。在每个小区中的两棵杉木幼苗正下方以45°斜角布两根长90 cm的微根管用以监测杉木细根生长和死亡动态。2014年3月在样地小区高处每隔0.05 m安放0.05 m×5 m的透明U型管, 均匀铺满隔离试验小区, 以隔离50%的降水 (试验期间总降水量为1994.2 mm)。样地布设完成后开始通电增温 (2014年3月)。
| 项目Item | 土层Soil layer/cm | |||||
| 0-10 | 10-20 | 20-30 | 30-40 | 40-50 | 50-60 | |
| 原位土壤In situ soil/(g/cm3) | 1.04 | 1.21 | 1.23 | 1.28 | 1.29 | 1.40 |
| 回填后土壤Backfilling soil/(g/cm3) | 1.05 | 1.13 | 1.29 | 1.40 | 1.41 | 1.31 |
本研究从2014年3月起至2015年3月对细根进行了为期1年的连续性观测。于每月上旬和下旬 (间隔大约15d) 使用微根管影像成像系统 (美国Bartz技术公司生产) 对细根生长过程进行影像收集, 在1d内完成每次影像的收集工作。图片收集后带回实验室使用Rootfly图像分析软件对其进行处理, 并获得各影像中细根直径、细根长度以及每张影像细根数量等数据。同时鉴别活根与死根:白色根和棕色根定义为活根, 黑色、皮层脱落或表皮褶皱的根定义为死根[15]。细根生产量用影像中细根出生数量作为指标。
1.4 数据处理与分析试验观测期从2014年3月至2015年3月, 依据亚热带气候条件, 将3、4、5月份划分为春季; 将6、7、8月份划分为夏季; 将9、10、11月份划分为秋季; 将12、1、2月份划分为冬季。
采用双因素ANOVA检验土壤增温、隔离降水对每根管细根1年出生数量的影响; 采用重复测量ANOVA检验土壤增温、隔离降水、季节对每根管细根出生数量的影响; 采用三因素ANOVA检验土壤增温、隔离降水、径级或土层对每根管细根出生数量的影响。采用单因素方差分析和LSD检验各处理间的每根管细根出生数量差异。所有的统计分析均在SPSS 19.0软件上进行, 显著性水平设定为P=0.05。
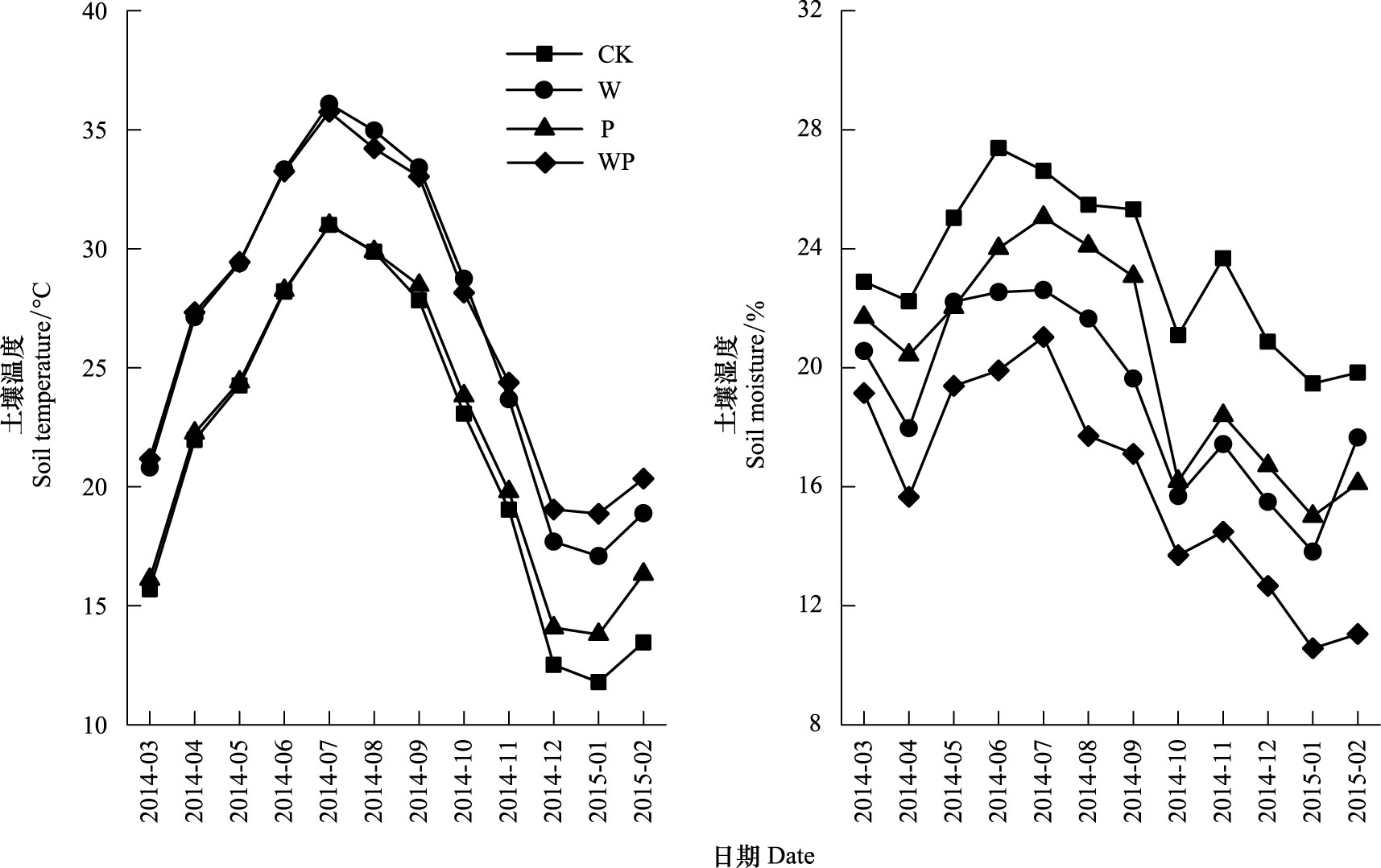
2 结果 2.1 土壤温度和水分增温对土壤温度和水分的影响达到极显著水平 (P<0.01), 增温与隔离降水的交互作用对土壤温度和水分没有影响 (P>0.05), 而隔离降水对土壤水分的影响达到极显著水平 (P<0.01), 对土壤温度没有影响 (P>0.05)(表 2)。试验处理一年期间, CK、W、P、WP的土壤平均温度和含水量分别为 (21.56±6.74)℃、(23.33±3.23)%, (26.77±6.75)℃、(18.96±3.54)%, (22.35±6.10)℃、(20.02±4.09)%, (26.93±6.01)℃、(16.05±3.85)%。与CK相比, W和WP的土壤温度显著增加 (P<0.05), P的土壤温度没有差异 (P>0.05);W、P和WP的土壤含水量则显著下降 (P<0.05)(图 1)。
| 因子Factors | P | ||
| 土壤温度 Soil temperature/℃ | 土壤湿度 Soil moisture/% | 每根管细根1年总出生数量/条 Total number of fine roots produced/(条管-1 a-1) | |
| W | <0.001 | <0.001 | 0.639 |
| P | 0.563 | <0.001 | 0.341 |
| W×P | 0.706 | 0.685 | 0.002 |
| W, 土壤增温Soil warming; P, 隔离降水Precipitation exclusion; W×P, 土壤增温与隔离降水的交互作用Interaction of soil warming and precipitation exclusion | |||
|
| 图 1 不同处理土壤温度和含水量的年变化 (0-10 cm) Fig. 1 Annual changes of soil (0-10 cm) temperature and moisture under different treatments CK, 对照control; W, 土壤增温; P, 隔离降水; WP, 土壤增温+隔离降水 |
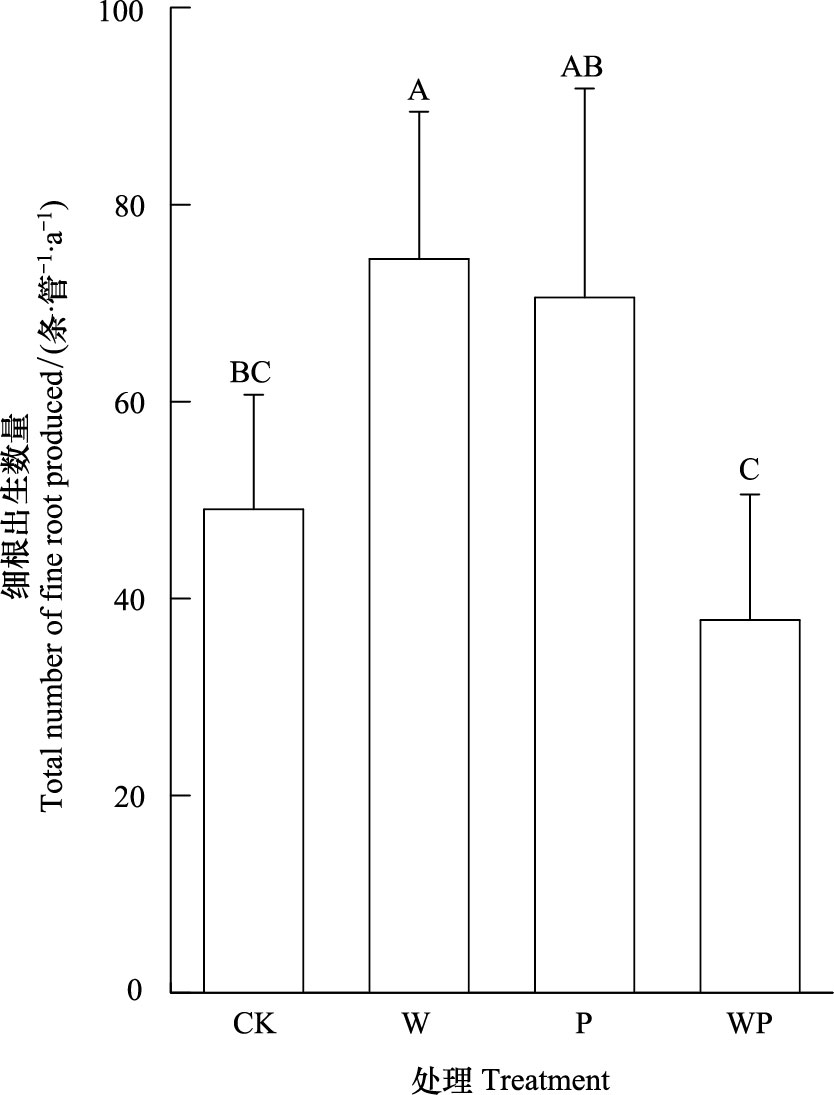
增温和隔离降水对细根总出生数量没有影响 (P>0.05), 而增温与隔离降水的交互作用对细根总出生数量的影响达到极显著水平 (P<0.01)(表 2)。在没有增温情况下, P处理与CK的细根总出生数量没有显著差异 (P>0.05);而在增温情况下, WP处理的细根总出生数量显著低于W处理 (P<0.05)。在没有隔离降水情况下, W处理比CK的细根总出生数量显著增加 (P<0.05);在隔离降水情况下, WP处理的细根总出生数量显著低于P处理 (P>0.05)(图 2)。
|
| 图 2 不同处理每根管细根一年总出生数量 Fig. 2 Total number of fine roots produced per tube one year under different treatments CK:对照control; W:土壤增温soil warming; P:隔离降水precipitation exclusion; WP:土壤增温+隔离降水soil warming plus precipitation exclusion; 不同大写字母表示不同处理差异显著, 图中数据为平均值±标准差 |
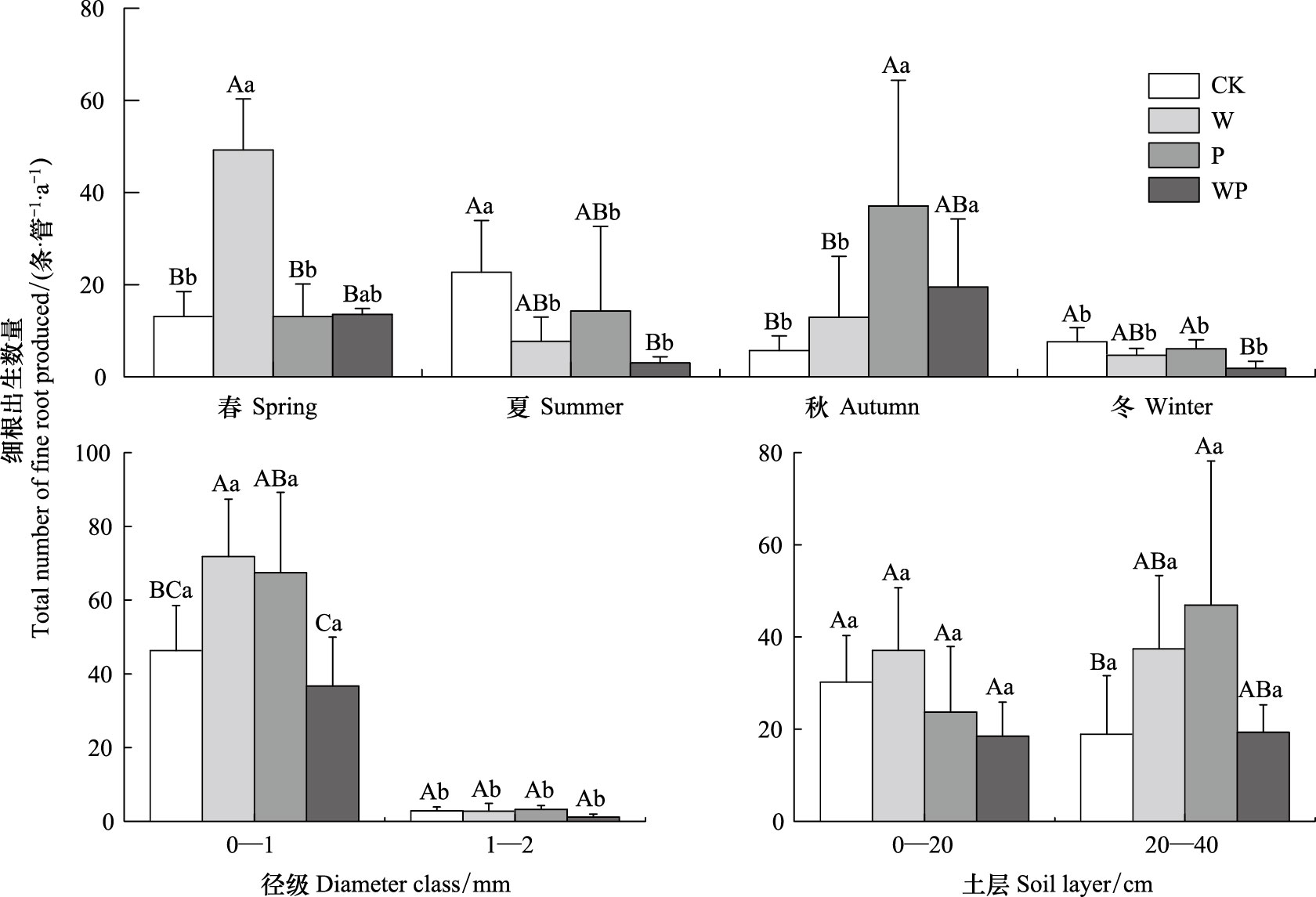
季节、增温与季节的交互作用、隔离降水与季节的交互作用对细根出生数量的影响达到极显著水平 (P<0.01);而土壤增温、隔离降水、季节三者的交互作用对细根出生数量没有影响 (P>0.05)(表 3)。在春季, W处理的细根出生数量显著高于CK和其它处理的细根出生数量 (P<0.05), 而其它处理之间则无显著差异 (P>0.05);在夏季, WP处理的细根出生数量显著低于CK (P<0.05), 而其他处理之间的细根出生数量没有显著差异 (P>0.05);在秋季, P处理的细根出生数量显著高于CK和W处理 (P<0.05), 而其它处理之间则无显著差异 (P>0.05);在冬季, WP处理的细根出生数量显著低于CK和P处理 (P<0.05), 而其它处理之间无显著差异 (P>0.05)(图 3)。不同处理细根出生的季节模式有一定差异。CK夏季的细根出生数量显著高于其他季节 (P<0.05);W处理春季的细根出生数量显著高于其他季节 (P<0.05);P处理秋季细根出生数量显著高于其他季节 (P<0.05);WP处理秋季的细根出生数量则显著高于夏季和冬季 (P<0.05)(图 3)。
| 因子Factors | |||||||
| W | P | S | W×P | W×S | P×S | W×P×S | |
| 每根管细根1年出生数量/条 Total number of fine roots produced/ (条管-1 a-1) | 0.639 | 0.341 | 0.001 | 0.002 | 0.005 | 0.001 | 0.074 |
| S:季节Season; W×S:土壤增温与季节的交互作用Interaction of soil warming and season; P×S:隔离降水与季节的交互作用Interaction of precipitation exclusion and season; W×P×S:土壤增温、隔离降水和季节三者的交互作用Interaction of soil warming, precipitation exclusion and season | |||||||
|
| 图 3 不同季节、径级、土层每根管细根出生数量 Fig. 3 Total number of fine roots produced per tube under different season, diameter class and soil layer 不同大写字母表示不同处理差异显著, 不同小写字母表示同一处理不同季节、径级、土层差异显著; 图中数据为平均值±标准差 |
径级以及土壤增温、隔离降水、径级三者的交互作用对细根出生数量的影响达到极显著水平 (P<0.01), 土壤增温与径级的交互作用、隔离降水与径级的交互作用对细根出生数量没有影响 (P>0.05)(表 4)。在0-1 mm径级, W处理细根出生数量显著高于CK, WP处理的细根出生数量则显著低于W处理和P处理。而1-2 mm径级的细根出生数量在各处理间均无显著差异 (图 3)。各处理的0-1 mm径级细根出生数量仅占总细根出生数量的绝大部分 (CK为94%, W为96%, P为95%, WP为97%)(图 3)。
| 因子Factors | |||||||
| W | P | D | W×P | W×D | P×D | W×P×D | |
| 每根管细根1年出生数量/条 Total number of fine roots produced/ (条管-1 a-1) | 0.649 | 0.352 | 0.000 | 0.001 | 0.848 | 0.428 | 0.002 |
| D:径级Diameter class; W×D:土壤增温与径级的交互作用Interaction of soil warming and diameter class; P×D:隔离降水与径级的交互作用Interaction of precipitation exclusion and diameter class; W×P×D:土壤增温、隔离降水和径级三者的交互作用Interaction of soil warming, precipitation exclusion and diameter class | |||||||
土层、土壤增温与土层的交互作用、隔离降水与土层的交互作用以及土壤增温和隔离降水与土层三者的交互作用均对细根出生数量没有影响 (P>0.05)(表 5), 表明土壤增温、隔离降水的影响及两者之间的交互作用不因土层而异。在0-20 cm土层, 各处理之间则无显著差异。而在20-40 cm土层, P处理的细根出生数量显著高于CK, 而其他处理之间均无显著差异 (图 3C)。
| 因子Factors | |||||||
| W | P | L | W×P | W×L | P×L | W×P×L | |
| 每根管细根1年出生数量/条 Total number of fine roots produced/ (条管-1 a-1) | 0.748 | 0.509 | 0.570 | 0.016 | 0.639 | 0.134 | 0.145 |
| L, 土层Soil layer; W×L, 土壤增温与土层的交互作用Interaction of soil warming and diameter class; P×L, 隔离降水与土层的交互作用Interaction of precipitation exclusion and diameter class; W×P×L, 土壤增温、隔离降水和土层三者的交互作用Interaction of soil warming, precipitation exclusion and diameter class | |||||||
与CK相比, W细根总出生数量显著增加, 说明土壤增温促进细根生产, 这与许多研究结果一致[16-19]。例如, Majdj等[20]对瑞典北部的云杉 (Norway spruce) 进行增温和施肥交互试验, 发现1996年10月至1997年6月增温样地和增温+施肥样地的细根生产量显著高于对照样地和施肥样地。造成土壤增温细根生产增加的主要原因是土壤增温能促进土壤氮矿化[21], 增加土壤氮有效性, 从而有利于细根生产。虽然P处理比CK细根总出生数量更多, 但未达到显著影响, 可能是因为隔离降水试验时间才1a, 受到影响的持续时间短, 而且本地区降水量丰富, 即使隔离50%降水量也可能遭受干旱的强度不大。然而根据最优分配理论, 当水分成为植物生长的限制因素时, 相对于植物地上部分的生长, 应分配更多的碳水化合物和养分用于细根生长[22], 之前相关研究也表明减少降水会促进细根生产, 例如Gaul等[23]通过对德国东南的挪威云杉6周隔离降水试验发现在6周轻度干旱期间细根生产增加, 主要原因是为了弥补干旱期间细根死亡量增加导致的细根生物量损失。本研究还显示与W处理和P处理相比, WP处理细根总出生数量显著降低。造成这种现象的原因是同时土壤增温和隔离降水时加剧了土壤的干旱程度, 可能会影响植物光合作用导致减少地下根系生长碳的供应, 进而减少细根生产[24]。
3.2 细根出生数量的季节动态本研究发现, CK的杉木幼苗细根出生数量在夏季和春季最多, 秋季最少, 这与前人的研究结果一致, 如Hendrick等[25]通过微根管技术对美国北方硬阔叶林研究表明, 细根生产在春末和夏初最多、秋季最少; 胡双成等[26]通过微根管技术对福建三明人促更新幼林研究发现人促更新幼林初期春季和夏季细根生产力比重大, 秋季比重小。造成这种季节动态的原因可能是是早春土温回升快, 降水量较多, 土壤含水量增加以及之前储存的碳水化合物供给均有利于根系的大量生长[27], 夏季树木固定的光合产物相对更多, 有大量的光合产物分配到地下, 满足了细根生长对碳的需求[28], 秋季细根开始减少与降水量减少、温度的下降, 以及分配给细根的碳水化合物减少有关[25]。与CK相比, W处理春季细根出生数量显著增加, 主要与W处理土壤温度较高, 养分矿化增强以及春季土壤水分有效性较高有关 (图 1)。P处理与CK相比, 秋季细根出生数量显著增加。这可能是由于与秋季P处理的土壤含水量与CK相比下降比较明显 (图 1), 从而诱发了P处理的杉木幼苗增加细根生产以获取土壤水分。WP处理与CK相比夏季细根出生数量显著降低的原因主要与土壤温度过高, 土壤含水量低有关; 而WP处理与CK相比冬季细根出生数量显著降低, 主要原因是因为, 与CK相比, WP处理冬季的土壤含水量极低, 降低了苗木的光合作用, 分配给地下的碳水化合物减少, 同时冬季土壤温度仍然较高, 细根呼吸消耗增加, 从而综合导致可用以细根生产的碳水化合物很少。
3.3 细根出生数量的径级分配和垂直分布研究结果显示, 土壤增温、隔离降水与径级的交互作用对细根出生数量的影响达到显著水平, 而且表明土壤增温与隔离降水的交互作用对细根出生数量的影响主要发生在0-1 mm径级。这是因为0-1 mm细根是吸收水分和养分的主要器官, 是最幼嫩 (未木质化) 的部分, 同时维持成本高, 因而其对土壤环境因子变化 (如土壤养分、水分、温度) 和光合产物的变化最为敏感。而1-2 mm细根主要起到运输作用, 已较充分木质化, 维持成本低, 因而对土壤环境因子和植物生理生态的变化敏感性较小。各处理的0-1 mm细根出生数量占细根总出生数量都达到90%以上, 表明0-1 mm细根对细根生产的贡献最大。这与前人的研究一致[26, 29], 如黄锦学等[30]研究发现细柄阿丁枫和米槠天然林0-1 mm细根占总生产力的比重达到90%以上。
本研究结果还显示, 土壤增温与土层、隔离降水与土层, 以及土壤增温、隔离降水与土层的交互作用均对细根出生数量没有影响。这表明在不同土层, 土壤增温、隔离降水及其交互作用对细根出生数量的均有相似的影响。不同处理的比较中, 只发现20-40 cm土层中P处理细根出生数量显著高于CK。这可能20-40cm土层的土壤环境因子影响有关。土壤表层土壤直接暴露于空气中, 土壤水分蒸发快, 不易受地下水分的补充, 同时隔离降水进一步限制了水分的补充, 从而诱发P处理的杉木幼苗细根向深层迁移以获取土壤水分。
4 结论本研究结果显示:1) 土壤增温和隔离降水对细根生产没有影响, 但两者的交互作用则极显著; 与CK相比, W处理细根总出生数量显著增加, 而WP处理细根总出生数量则显著低于W处理和P处理; 2) 土壤增温×季节、隔离降水×季节对细根出生数量均有显著影响, 说明土壤增温和隔离降水因改变土壤水热条件而改变了细根生产的季节; 3) 土壤增温×隔离降水×径级对细根出生数量存在显著影响, 土壤增温与隔离降水的交互作用主要发生在0-1 mm径级; 4) 土壤增温、隔离降水与土层之间不存在显著的交互作用, 这表明各处理对细根出生数量的影响不随土层而异。可见细根生产对土壤增温与隔离降水的交互作用的响应更多地通过改变细根生产季节和径级分配, 从而对杉木幼苗生长产生影响。
| [1] | IPCC.Climate change 2013:The physical science basis. Working Group I Contribution to the Fifth Assessment Report of the Intergovernmental Panel on Climate Change. Cambridge: Cambridge University Press, 2013. |
| [2] | Dai A G. Increasing drought under global warming in observations and models. Nature Climate Change, 2013, 3(1): 52–58. |
| [3] | Aronson E L, McNulty S G. Appropriate experimental ecosystem warming methods by ecosystem, objective, and practicality. Agricultural and Forest Meteorology, 2009, 149(11): 1791–1799. DOI:10.1016/j.agrformet.2009.06.007 |
| [4] | Melillo J M, Steudler P A, Aber J D, Newkirk K, Lux H, Bowles F P, Catricala C, Magill A, Ahrens T, Morrisseau S. Soil warming and carbon-cycle feedbacks to the climate system. Science, 2002, 298(5601): 2173–2176. DOI:10.1126/science.1074153 |
| [5] | Liu C, Xiang W H, Lei P F, Deng X W, Tian D L, Fang X, Peng C H. Standing fine root mass and production in four Chinese subtropical forests along a succession and species diversity gradient. Plant and soil, 2014, 376(1-2): 445–459. DOI:10.1007/s11104-013-1998-0 |
| [6] | 王瑞丽, 程瑞梅, 肖文发, 封晓辉, 刘泽彬, 王晓荣. 森林细根生产和周转的影响因素. 世界林业研究, 2012, 25(1): 19–24. |
| [7] | Pritchard S G, Rogers H H. Spatial and temporal deployment of crop roots in CO2-enriched environments. New Phytologist, 2000, 147(1): 55–71. DOI:10.1046/j.1469-8137.2000.00678.x |
| [8] | Wan S Q, Norby R J, Pregitzer K S, Ledford J, O'Neill E G. CO2 enrichment and warming of the atmosphere enhance both productivity and mortality of maple tree fine roots. New Phytologist, 2004, 162(2): 437–446. DOI:10.1111/nph.2004.162.issue-2 |
| [9] | Bai W M, Wan S Q, Niu S L, Liu W X, Chen Q S, Wang Q B, Zhang W H, Han X G, Li L H. Increased temperature and precipitation interact to affect root production, mortality, and turnover in a temperate steppe:implications for ecosystem C cycling. Global change biology, 2010, 16(4): 1306–1316. DOI:10.1111/gcb.2010.16.issue-4 |
| [10] | Johnson M G, Rygiewicz P T, Tingey D T, Phillips D L. Elevated CO2 and elevated temperature have no effect on Douglas-fir fine-root dynamics in nitrogen-poor soil. New Phytologist, 2006, 170(2): 345–356. DOI:10.1111/nph.2006.170.issue-2 |
| [11] | Joslin J D, Wolfe M H. Impacts of water input manipulations on fine root production and mortality in a mature hardwood forest. Plant and Soil, 1998, 204(2): 165–174. DOI:10.1023/A:1004352008490 |
| [12] | Chen G S, Yang Z J, Gao R, Xie J S, Guo J F, Huang Z Q, Yang Y S. Carbon storage in a chronosequence of Chinese fir plantations in southern China. Forest Ecology and Management, 2013, 300: 68–76. DOI:10.1016/j.foreco.2012.07.046 |
| [13] | Wu Z T, Dijkstra P, Koch G W, Peñuelas J, Hungate B A. Responses of terrestrial ecosystems to temperature and precipitation change:a meta-analysis of experimental manipulation. Global Change Biology, 2011, 17(2): 927–942. DOI:10.1111/gcb.2010.17.issue-2 |
| [14] | 陈云玉, 熊德成, 邓飞, 许辰森, 冯建新, 史顺增, 钟波元, 陈光水. 土壤增温与氮添加对杉木幼苗细根径级根长分布的影响. 应用生态学报, 2016, 27(4): 1009–1014. |
| [15] | Wells C E, Glenn D M, Eissenstat D M. Changes in the risk of fine-root mortality with age:a case study in peach, Prunus persica (Rosaceae). American Journal of Botany, 2002, 89(1): 79–87. DOI:10.3732/ajb.89.1.79 |
| [16] | Forbes P J, Black K E, Hooker J E. Temperature-induced alteration to root longevity in Lolium perenne. Plant and Soil, 1997, 190(1): 87–90. DOI:10.1023/A:1004298804353 |
| [17] | Fitter A H, Self G K, Brown T K, Bogie D S, Graves J D, Benham D, Ineson P. Root production and turnover in an upland grassland subjected to artificial soil warming respond to radiation flux and nutrients, not temperature. Oecologia, 1999, 120(4): 575–581. DOI:10.1007/s004420050892 |
| [18] | King J S, Pregitzer K S, Zak D R. Clonal variation in above-and below-ground growth responses of Populus tremuloides Michaux:influence of soil warming and nutrient availability. Plant and Soil, 1999, 217(1-2): 119–130. |
| [19] | Tierney G L, Fahey T J, Groffman P M, Hardy J P, Fitzhugh R D, Driscoll C T, Yavitt J B. Environmental control of fine root dynamics in a northern hardwood forest. Global Change Biology, 2003, 9(5): 670–679. DOI:10.1046/j.1365-2486.2003.00622.x |
| [20] | Majdi H, Öhrvik J. Interactive effects of soil warming and fertilization on root production, mortality, and longevity in a Norway spruce stand in Northern Sweden. Global Change Biology, 2004, 10(2): 182–188. DOI:10.1111/gcb.2004.10.issue-2 |
| [21] | Rustad L E, Campbell J L, Marion G M, Norby R J, Mitchell M J, Hartley A E, Cornelissen J H C, Gurevitch J. A meta-analysis of the response of soil respiration, net nitrogen mineralization, and aboveground plant growth to experimental ecosystem warming. Oecologia, 2001, 126(4): 543–562. DOI:10.1007/s004420000544 |
| [22] | Bloom A J, Chapin F S, Mooney H A. Resource limitation in plants-an economic analogy. Annual review of Ecology and Systematics, 1985, 16: 363–392. DOI:10.1146/annurev.es.16.110185.002051 |
| [23] | Gaul D, Hertel D, Borken W, Matzner E, Leuschner C. Effects of experimental drought on the fine root system of mature Norway spruce. Forest Ecology and Management, 2008, 256(5): 1151–1159. DOI:10.1016/j.foreco.2008.06.016 |
| [24] | Niu S L, Wu M Y, Han Y, Xia J Y, Li L H, Wan S Q. Water-mediated responses of ecosystem carbon fluxes to climatic change in a temperate steppe. New Phytologist, 2008, 177(1): 209–219. |
| [25] | Hendrick R L, Pregitzer K S. The dynamics of fine root length, biomass, and nitrogen content in two northern hardwood ecosystems. Canadian Journal of Forest Research, 1993, 23(12): 2507–2520. DOI:10.1139/x93-312 |
| [26] | 胡双成, 熊德成, 黄锦学, 邓飞, 陈云玉, 刘小飞, 陈光水. 福建三明米槠次生林在不同更新方式下的初期细根产量. 应用生态学报, 2015, 26(11): 3259–3267. |
| [27] | López B, Sabaté S, Gracia C A. Fine-root longevity of Quercus ilex. New Phytologist, 2001, 151(2): 437–441. DOI:10.1046/j.0028-646x.2001.00189.x |
| [28] | Withington J M, Reich P B, Oleksyn J, Eissenstat D M. Comparisons of structure and life span in roots and leaves among temperate trees. Ecological Monographs, 2006, 76(3): 381–397. DOI:10.1890/0012-9615(2006)076[0381:COSALS]2.0.CO;2 |
| [29] | 黄锦学, 凌华, 杨智杰, 卢正立, 熊德成, 陈光水, 杨玉盛, 谢锦升. 中亚热带细柄阿丁枫和米槠群落细根的生产和死亡动态. 生态学报, 2012, 32(14): 4472–4480. |
 2017, Vol. 37
2017, Vol. 37