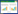文章信息
- 唐显江, 陶双伦, 马静, 章力, 吴帅玲, 李俊年
- TANG Xianjiang, TAO Shuanglun, MA Jing, ZHANG Li, WU Shuailing, LI Junnian.
- 视野受阻对东方田鼠觅食行为的影响
- Effects of vision obstruction on the foraging behavior in voles (Microtus fortis)
- 生态学报. 2017, 37(3): 1035-1042
- Acta Ecologica Sinica. 2017, 37(3): 1035-1042
- http://dx.doi.org/10.5846/stxb201508281792
-
文章历史
- 收稿日期: 2015-08-28
- 网络出版日期: 2016-06-13
2. 马格德堡大学医学心理学研究所, 马格德堡 39120
2. Institute of Medical Psychology, Otto-von-Guericke University, Magdeburg 39120, Germany
自然界, 植食性哺乳动物的觅食环境复杂多变, 捕食者的捕食及同种和异种个体的竞争等各种压力并存[1]。动物与环境长期相互作用的适应性进化过程中, 发展出各种警觉行为动作以应对和规避风险压力, 使其适合度最大化[2]。植食性哺乳动物的觅食活动作为其生命活动的重要组成成分之一, 其生命大部分时间都用于觅食, 且觅食活动伴随着警觉[3-4]。一些警觉行为动作可引起觅食活动出现短暂中断, 会潜在地影响觅食效率[4]。食物摄入率作为衡量动物觅食效率的关键性指标, 在一定程度上反映了动物对环境的适应性[5-6]。因此, 探讨不同环境条件下动物的摄入率动态对于阐明其觅食策略的进化适应性意义具有重要的生态学价值。
动物觅食活动中的警觉行为动作及强度随觅食环境而变化, 如在捕食者频繁出没的区域, 美洲野牛(Bison bison) 抬头监视环境的频次明显增加[3];随植被高度的增加, 穴兔(Spermophilus townsendii) 显著增大站立扫视周围环境的频次[7];捕食者在场时, 东方田鼠(Microtus fortis) 的觅食决定时间明显增加, 进食时盯视时间显著增大, 静听及嗅闻时间则明显减少[8]。尽管这些研究的旨趣在于探讨觅食活动中警觉行为动作特征与环境复杂性的相互关系, 但在不同环境条件下, 警觉行为变异究竟能在多大程度上影响摄入率, 目前仍无定论。有关复杂环境对动物觅食行为影响的研究众多[9-15], 但大多仅限于定性研究, 如一些研究将动物觅食活动中的警觉分为一般警觉和明显警觉两种类型[7, 11], 而另有一些研究则根据种内竞争及种间捕食关系, 将动物觅食活动中的警觉分为社会性警觉和反捕食警觉[14]。在未测定此类警觉行为所引致的觅食中断对摄入率的影响的条件下, 就定义一般警觉和社会性警觉为低代价行为, 明显警觉和反捕食警觉为高代价行为, 势必难以阐明植食性哺乳动物觅食行为的进化适应性意义。Lima等[16]认为, 动物各种警觉行为动作在警觉强度和代价上可能存在差异, 探讨动物的警觉代价时, 定义警觉动作应充分考虑其是否引起觅食中断。
动物对觅食环境各种风险因子的评估依赖于对环境各种信息的感知和判断。食物斑块周围植被高度作为环境复杂性因子之一, 对植食性哺乳动物尤其是中、小型动物的觅食行为有着重要的影响[7, 11]。植被低矮时, 动物视野开阔, 尽管能收集到较多相对稳定的环境信息, 但易被捕食者发现;而植被茂密时动物视野受限, 尽管收集周围信息相对困难, 须通过调节觅食活动中的警觉行为动作如增大直立扫视和静听动作频次等来收集信息[7, 11], 但有利于风险躲避和隐藏。由于植被高度对动物觅食行为影响的复杂性, 觅食活动中的警觉行为动作变化是否会影响觅食效率, 目前仍无定论。
植食性小哺乳动物觅食行为过程典型地由搜寻与采食和处理(咀嚼和吞咽) 食物动作组成, 期间伴有各种警觉行为动作如一般扫视、直立扫视、静听及嗅闻[4, 7-8, 11, 14, 16]。动物处理食物时能用一般扫视搜寻新的食物项目和监视周围环境, 不会导致觅食活动出现短暂中断。但直立扫视、静听和嗅闻动作与处理食物动作相互抑制不相重叠, 能使觅食活动出现短暂中断[4, 8]。自然界, 植食性小型哺乳动物觅食行为极易受到植被高度的影响[11]。植被低矮即植被高度低于动物身高时, 动物的警觉行为动作通常表现为一般扫视、静听和嗅闻几种类型, 偶尔也会出现直立扫视动作;植被高度大于身高时, 动物除了采用上述一般警觉行为动作监视环境外, 会明显增加直立扫视动作频次[11]。由此可以想见, 动物警觉行为动作组成模式因环境而异, 其构成了动物应对特定环境的觅食适应性策略[11]。
本文以栖息于洞庭湖区的东方田鼠(Microtus fortis) 为研究对象。在实验室条件下, 以田鼠喜食的新鲜白三叶(Trifolium repens) 为食物, 采用相等的叶片间距配置叶片大小一致的均质密集性食物斑块。在食物斑块周边覆以牛皮纸模拟食物斑块周围植被高度, 设置3种植被高度梯度, 进行实验动物视野阻挡。测定实验个体于不同程度的视野受阻条件下在食物斑块上的各觅食行为和警觉行为动作组成模式、发生频次及持续时间;分析不同程度的视野受阻所引起的警觉动作组成模式变异, 以及引起在觅食中断时间上的差异, 所导致的摄入率的变化, 以阐明视野受阻条件下东方田鼠觅食行为的进化适应性策略。
1 材料与方法 1.1 实验动物以栖息于湖南省洞庭湖区的东方田鼠为实验动物。野外捕捉后带回室内饲养, 达2个月后, 选取健康成体40只, 雌、雄各20只, 平均体重(52.4±8.9) g, 作为预实验动物。在实验室条件下, 以干木屑为巢垫, 兔颗粒饲料为主要食物, 附加一定量的胡萝卜, 供给充足的饮水, 驯养于透明饲养笼内。实验室温度为(20±1)℃, 光照周期12L:12D。实验期, 以新鲜白三叶叶片饲喂动物。
1.2 食物斑块配制采用木质纤维板构建80 cm×30 cm的个体觅食活动空间。前期的研究表明, 随叶片大小增加, 东方田鼠的摄入率显著增大, 当叶片大小达到6 mg左右时, 摄入率不再增大, 稳定于一定的水平[4]。因此, 以白三叶叶片大小为(6.06±0.83) mg (干重) 设置斑块, 通过控制其食物大小, 消除食物大小对摄入率的影响。以3.0 cm的空间距离在斑块上钻孔, 孔口直径约0.5 cm, 以小型塑胶软塞固定叶片于孔口处, 构成实验个体食物密集均质斑块。
1.3 行为观测装置为了有效控制实验个体, 便于准确地测定个体的觅食行为及过程, 在食物斑块上部周边设立观测箱。观测箱由透明玻璃构成, 底部面积与食物斑块大小一致, 高度为60 cm。观测箱由投放区(R) 和觅食区(F) 两部分构成(图 1)。在投放区周边玻璃上覆以牛皮纸, 作为觅食个体规避风险的隐藏区。两区间以底部带孔的隔板相隔, 此孔可作为实验个体在两区间自由活动的通路。投放区面积30 cm×20 cm, 觅食区面积80 cm×30 cm。觅食区覆以牛皮纸模拟食物斑块周围植被高度, 借以阻挡实验个体视野。设置3种视野遮挡高度(O), 分别为5、10 cm和15 cm。设置依据是, 在低遮挡条件下, 东方田鼠视野开阔, 能以一般扫视观察到周围环境;在中遮挡条件下, 个体只能以抬头和直立抬头扫视方式观察到周围环境;而在高遮挡条件下, 个体观察食物斑块周围的视野完全受阻, 即使采用直立抬头扫视方式亦不能观察到周围环境。
|
| 图 1 东方田鼠觅食行为观测装置示意图 Fig. 1 Sample of behavioral observing equipment in reed voles foraging R:投放区releasing area; F:觅食区foraging area; O:视野遮挡vision obstruction area |
参照Spalinger和Hobbs[17]、Hobbs和Gross等[18]、陶双伦等[4]等对植食性哺乳动物觅食及警觉行为参数的定义, 测定如下行为参数:采食时间(h),口鼻部接触到食物, 至分离食物的时间(min);处理时间(TT),咀嚼和吞咽食物的时间(min);采食回合时间(TBB),开始采食至下1次采食活动开始持续的时间(min);口量(S),通过一次或多次采食动作, 经连续咀嚼, 1次吞咽的食物量(g);觅食回合时间(TFB),1次连续采食活动所持续的时间, 在2个采食回合间无四处行走观察和企图逃跑等非觅食行为活动(min);一般扫视时间(Sc),包括平视和抬头扫视时间, 其中平视时间(HSc), 以头部转动方式观察周围环境所持续的时间(min);抬头扫视时间(RSc), 以前肢离地身体向上未完全伸展方式观察周围环境所持续的时间(min);直立扫视时间(USc),以前肢离地, 背部与地面几近垂直方式观察周围环境所持续的时间(min)。静听时间(L),停留于原地或站立抬头, 一动不动, 短暂停止一切觅食活动所持续的时间(min);嗅闻时间(Sn),口鼻部前升, 鼻孔部周围肌肉及毛发发生明显颤动所持续的时间(min);觅食中断时间(TFI),停止咀嚼, 直立抬头扫视、监听、及嗅闻等所持续的时间(min);警觉行为动作频次,觅食回合内, 警觉行为动作一般扫视、抬头扫视、静听及嗅闻动作的发生次数。摄入率(I),单位时间, 动物摄入的食物量(mg/min)。
1.5 实验程序及觅食行为参数估计行为测定前2周, 以新鲜白三叶叶片饲喂实验动物。行为观测装置置于吉首大学基础生物学动物行为学实验室特定位置, 上方悬挂1只60 W节能灯。为使个体充分适应观测装置, 将单只个体投放于观测箱, 使其适应15 min, 每天重复2次。测定时, 从预实验群体中选择20只觅食活跃、毛色光亮的健康雌、雄各10只作为实验个体。依据遮挡程度由低到高将实验分为对照组、处理组1和处理组2, 各组实验均采用所选择的20只个体作为实验动物进行测试。测试过程为先进行对照组实验, 然后进行处理组1和处理组2实验。测定时, 从观测箱投放区释放单只个体, 观测者位于观测箱一侧中部, 以录像机录像和人工计数测定个体上述觅食行为参数及其行为过程序列, 同时观测者记录实验个体每口消费的叶片占单个叶片大小比例[6]。每只个体每隔两天测定一次, 每个个体至少重复测定2次。每次行为测定结束后, 分离、称重每个被食叶片的剩余部分, 以自来水彻底冲洗斑块, 去掉遗留气味, 避免影响后续实验。待斑块阴干后, 重新配置叶片, 重复上述试验。实验测定期内, 行为测定均由同一观测者完成。
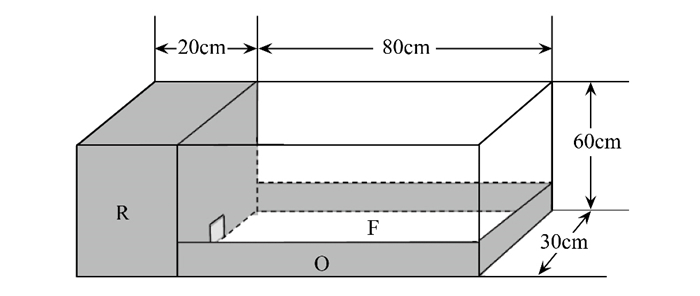
采用警觉-功能反应模型[4]计算个体的摄入率:
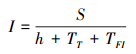
|
式中,h为采食时间, S为口量, TT为处理时间, TFI为觅食中断时间, I为摄入率。
1.6 统计分析测定处理组个体的觅食行为时, 部分个体在一些区域的觅食行为因牛皮纸遮挡而未能摄录完整, 统计分析时, 只统计觅食回合完整的个体的行为数据。这样, 可能会影响处理组个体觅食行为参数的样本数。因此, 测试期内, 采集每一个体至少一次完整的觅食活动。由于搜集到的觅食行为参数的样本数已足够大--样本数大于100, 基于统计学理论, 组间样本数差异不会对分析结果产生较大的影响。
实验动物体重、警觉行为参数、觅食行为参数均以平均值±标准误(M±SE) 表示;独立样本t检验及Mann-Whitney检验分析结果发现, 组内即对照组、处理组1及处理组2内雌雄个体的摄入率及觅食行为参数均无显著差异(P>0.05)。因此, 本文重点探讨各组间实验个体摄入率及觅食行为参数的差异。
采用独立样本t检验分析法, 检验东方田鼠摄入率;采用Mann-Whitney检验分析法, 检验警觉行为动作频次在视野受阻程度不同条件下的差异显著性;采用独立样本t检验分析法, 检验东方田鼠觅食回合中各种警觉行为动作时间及觅食中断时间在视野受阻程度不同条件下的差异显著性。
2 结果 2.1 摄入率实验个体在3种视野受阻条件下的摄入率极为相近, 其中对照组, n=252, I=(68.28±14.17)(mg/min);处理组1, n=220, I=(66.62±16.23)(mg/min);处理组2, n=114, I=(67.90±15.45)(mg/min)。独立样本t检验分析结果显示, 实验个体摄入率在3种视野受阻条件下差异均不显著(处理组1 vs对照组:t(469)=1.419, P=0.157>0.05;处理组2 vs对照组:t(363)=0.039, P=0.969>0.05;处理组1 vs处理组2:t(332)=-1.068, P=0.286>0.05)。表明, 在3种视野受阻条件下, 个体均能维持摄入率。
2.2 警觉行为参数东方田鼠各警觉行为动作频次在3种视野受阻条件下呈现不同的分配格局(图 2)。Mann-Whitney分析检验结果显示, 处理组1(n=18, 33; Z=-1.944, P=0.042 < 0.05) 和处理组2(n=17, 33; Z=-2.080, P=0.038 < 0.05) 个体的一般扫视动作频次显著低于对照组个体的, 而处理组1与处理组2个体的一般扫视动作频次差异则不显著(n=18, 17; Z=-1.082, P=0.279>0.05)。实验个体直立扫视动作频次在3种视野受阻条件下均无显著差异(处理组1 vs对照组:n=18, 33; Z=-1.079, P=0.281>0.05;处理组2 vs对照组:n=33, 17; Z=-0.318, P=0.751>0.05;处理组1 vs处理组2:n=18, 17; Z=-0.691, P=0.490>0.05);实验个体静听动作频次随视野受阻程度的增大而明显增高(图 2), 三者间差异均显著或极显著(处理组1 vs对照组:n=18, 33; Z=-2.578, P=0.04 < 0.05;处理组2 vs对照组:n=17, 33; Z=-2.689, P=0.007 < 0.01;处理组1 vs处理组2:n=18, 17; Z=-2.174, P=0.024 < 0.05)。处理组1个体的嗅闻动作频次显著低于对照组(n=18, 33; Z=-2.468, P=0.014 < 0.05) 和处理组2(n=18, 17; Z=-2.174, P=0.024 < 0.05) 个体的, 处理组2个体的嗅闻动作与对照组个体的差异不显著(n=33, 17; Z=-0.185, P=0.853>0.05)。检验结果说明, 视野受阻能明显改变东方田鼠的警觉动作频次。

|
| 图 2 3种视野受阻条件下东方田鼠警觉行为动作频次 Fig. 2 Vigilance frequencies of reed voles foragingin three levels of vision obstruction Sc:一般扫视Scanning; USc:站立扫视Upright & Scanning; L:静听Listening; Sn:嗅闻Sniffing |
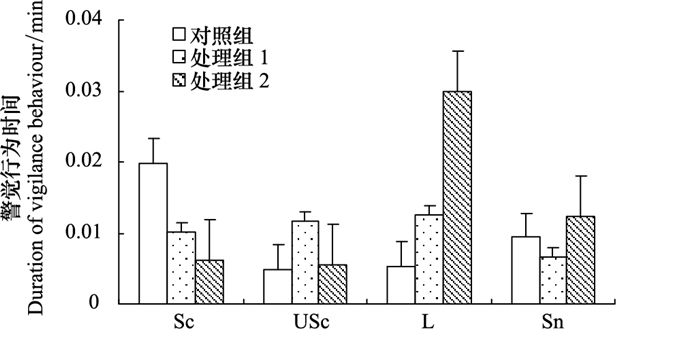
实验个体的各警觉行为动作持续时间在3种视野受阻条件下亦呈现明显地变异(图 3)。独立样本t检验结果显示, 处理组1(t(470)=2.572, P=0.010 < 0.05) 和处理组2(t(364)=2.933, P=0.004 < 0.01) 个体的一般扫视时间显著或极显著地低于对照组个体的, 处理组1与处理组2个体的一般扫视时间差异不显著(t(332)=1.216, P=0.225>0.05);处理组1个体的直立扫视时间显著地高于对照组(t(470)=-2.435, P=0.015 < 0.05) 和处理组2(t(332)=-2.216, P=0.023 < 0.05) 个体的, 而处理组2个体的直立扫视时间与对照组个体的差异不显著(t(364)=-0.342, P=0.733>0.05);个体的静听时间随视野受阻程度的增大而增高(图 3)。处理组2个体的静听时间显著或极显著地高于对照组(t(364)=-5.077, P=0.000 < 0.01) 和处理组1个体的(t(332)=-2.625, P=0.009 < 0.01), 处理组1个体的静听时间显著地高于对照组个体的(t(470)=-2.057, P=0.040 < 0.05);3种视野受阻条件下实验个体间的嗅闻时间无显著差异(处理组1 vs对照组:t(470)=1.303, P=0.193>0.05;处理组2 vs对照组:t(364)=-1.958, P=0.200>0.051;处理组1 vs处理组2:t(332)=-0.984, P=0.326>0.05)。说明, 视野受阻对东方田鼠嗅闻时间无显著性影响。
|
| 图 3 3种视野受阻条件下东方田鼠警觉行为时间 Fig. 3 Vigilance duration of reed voles in three levels vision obstruction |
3种视野受阻条件下, 实验个体分配于各采食回合的觅食中断时间较为一致, 其中对照组, n=252, TFI=(0.030±0.010)(min);处理组1, n=220, TFI=(0.032±0.008)(min);处理组2, n=114, TFI=(0.031±0.011)(min)。独立样本t检验结果显示, 处理组1(t(470)=-0.161, P=0.872>0.05) 及处理组2(t(364)=-1.285, P=0.200>0.05) 个体的觅食中断时间与对照组个体的差异不显著, 处理组1个体的觅食中断时间与处理组2的差异亦不显著(t(332)=-0.984, P=0.326>0.05)。说明, 视野受阻对东方田鼠觅食中断时间无影响。
上述检验结果充分说明, 食物斑块周边的植被高度通过影响东方田鼠觅食活动中的警觉行为, 能使其警觉动作的发生频次和时间产生变异, 进而影响其觅食行为, 但该种作用并未波及至对分配于各采食回合的觅食中断时间的影响, 因而个体摄入率依然保持稳定。从而揭示东方田鼠在植被高度引起的视野受阻条件下, 能通过调节觅食活动中各警觉行为动作的发生频次和持续时间, 使摄入率维持稳定。
3 讨论实验室条件下模拟东方田鼠在视野受到周围环境植被高度遮挡下的觅食行为, 结果发现, 实验个体在3种视野受阻条件下均能维持摄入率, 说明视野受阻对东方田鼠摄入率无影响。
从觅食活动中实验个体警觉发生的强度即频次来看, 与其他相关研究相类似[8, 11], 食物斑块周围植被高度能明显改变东方田鼠觅食活动中的警觉行为动作频次(图 2)。在视野不受制约的条件下, 对照组实验个体主要采用一般扫视和嗅闻来监测和评估环境风险。相较于对照组, 处理组1个体的视野不完全受阻, 而静听和嗅闻不受视野阻挡物的限制, 个体能通过直立扫视及静听和嗅闻动作监测周围环境, 因此一般扫视频次和嗅闻频次明显减少, 相应地直立扫视频次和静听频次显著增大;而处理组2个体的视野完全受阻即直立亦不能观察到周围环境, 因此, 其一般扫视及直立扫视频次上的变动规律与处理组1个体的较为一致, 但静听频次明显加强。与处理组1个体的嗅闻频次变化不同, 处理组2个体的同对照组个体的, 基本保持稳定。说明, 在不同程度的视野阻挡条件下, 实验个体觅食活动中的各警觉动作发生频次不同。动物各警觉动作强度变化是与其收集环境信息的难易程度紧密相关[3, 8, 11, 14-15]。眼睛作为植食性哺乳动物最为重要的感知外界环境的器官, 其大部分活动都与眼睛感官的活动密切相关[3, 13-14]。在视野不受阻碍的情况下, 个体能通过一般扫视动作监视周围环境;而视野受到不同程度的阻碍时, 则需通过调整视野监视动作频次如增大直立扫视动作频次或(和) 加强静听动作频次来弥补一般扫视感知外界环境信息的不足[7, 11, 14]。然而, 个体嗅闻频次与直立扫视频次和静听频次的变动格局不同(图 2)。相较于对照组个体的嗅闻频次, 处理组1个体的显著降低, 而处理组2个体的则保持稳定, 这可能与处理组1个体为观察和收集环境信息, 增大了直立扫视频次进而减少嗅闻频次有关。嗅觉的主要任务是通过检测同种及异种竞争者和捕食者身体在空气中散布的化学气味分子或粪便及尿迹气味来评估环境风险, 所检测的风险性质与扫视和静听不同, 前者属潜在的非紧迫性风险, 后者则为潜在的紧迫性风险[8]。视野不完全受阻时, 处理组1个体能充分利用视觉和听觉感官监测周围环境潜在的紧迫性风险, 因而降低了嗅闻对潜在的非紧迫性风险的监测。视野完全受阻时, 处理组2个体由于仅能采用静听和嗅闻两种警觉动作来监测环境风险, 故而增大了静听频次和维持嗅闻频次的稳定。
尽管, 视野受阻能影响东方田鼠觅食活动中各警觉行为动作的发生频次, 但这些行为动作在发生频次上的差异并不一定能引起觅食中断时间的相应变化[2]。植食性哺乳动物的觅食活动模式典型地表现为, 在处理口腔中食物的同时能搜寻新的食物项目[17]。动物的警觉行为贯穿于其觅食活动的始终, 而觅食活动中的各警觉行为动作对食物摄入过程的作用不同[4, 8]。动物处理(咀嚼和吞咽) 口腔中的食物时能同时搜寻新的食物项目和进行一般扫视动作监测环境, 而以直立扫视、静听及嗅闻动作监测环境时, 这些动作与处理食物动作相互抑制不相重叠, 须短暂停止食物处理, 因而能引起觅食活动的短暂中断[4, 8]。行为测定结果发现, 对照组个体分配于一般扫视动作的时间较多, 而分配于直立扫视、静听和嗅闻动作的时间则较少(图 3)。这与视觉感官作为监视周围环境最为重要的感觉器官之一, 动物大部分觅食活动如搜寻食物和监视周围环境都与其有关[3, 14-15]。然而,视野受阻时,处理组个体分配于各警觉行为动作的时间格局有别于对照组个体的,其警觉时间格局发生了明显的变异(图 3)。处理组1个体显著降低一般扫视时间, 增大直立扫视时间(图 3)。尽管嗅闻频次显著降低, 但分配于嗅闻的时间却依然维持稳定。说明视野不完全受阻时, 个体以直立扫视方式作为监测环境的主要手段。处理组2个体因视野完全受阻, 分配于一般扫视的时间同处理组1个体的, 亦明显减少。尽管处理组2个体直立扫视亦不能观察到周围环境, 但依然发生直立扫视, 分配于直立扫视动作的时间与对照组个体的无明显差异。我们认为, 动物觅食活动中的各种警觉行为动作是长期与环境相互作用进化形成的适应性产物, 为觅食活动中一种习惯化的有效行为模式[3-4]。为弥补视野监测的不足, 个体分配于静听的时间明显增大。说明视野完全受阻后, 静听则成为东方田鼠监视周围环境的主要手段。而分配于嗅闻的时间与对照组及处理组1个体的无明显差异。与对照组相比, 处理组1和处理组2个体监视周围环境投入的嗅闻时间无显著差异。如上所述, 出现这种结果与嗅闻的主要任务在于监测潜在的非紧迫性风险而其他警觉行为动作的目的则在于监测潜在的紧迫性风险有关[8]。虽然视野受阻影响了东方田鼠觅食活动中的警觉行为动作频次及时间分配, 但该种作用并未影响个体分配于各采食回合的觅食中断时间。与对照组个体相比较, 处理组1和2个体分配于各采食回合的觅食中断时间一致。说明视野受阻对个体觅食中断时间无影响。
根据植食性哺乳动物警觉-功能反应理论模型[4]预测, 动物在各采食回合的瞬时摄入率(I) 由食物大小(S) 决定, 且受采食和处理食物动作相互抑制及觅食中断时间的影响。由于我们是在食物大小相同的均质密集食物斑块上测定东方田鼠的觅食行为, 设定食物大小为实验个体经一次采食活动且一口所能获取的口量(S)。因口量稳定, 所以个体投入处理每口食物的时间恒定, 加之个体采食收获每口食物的时间基本恒定, 那么, 影响东方田鼠摄入率的参数则为觅食中断时间。由于在不同程度的视野受阻条件下, 东方田鼠分配于各采食回合的觅食中断时间无明显差异, 故而能维持摄入率的稳定。
以往的研究是以个体对外界环境响应的警觉行为动作性质特征如明显警觉和一般警觉[7, 11], 抑或是根据社群成员个体间的竞争或干扰以及群内个体对捕食者的警觉反映动作的功能性特征如社会性警觉和反捕食警觉来区分和定义警觉动作及其代价的[14], 忽视了这些警觉行为动作本身均含有的能引起觅食中断的静听和嗅闻动作[4, 8]。由此可知, 此类研究在探讨动物的警觉代价时, 未能充分考虑这些警觉是否能引起觅食中断, 因而难以评价这些不同警觉类型所引起的食物摄入损失的代价[4, 8, 16]。本项研究通过仔细观察植食性小型哺乳动物东方田鼠的觅食行为过程及序列, 对其觅食过程中警觉动作特征以及是否能引起觅食中断进行了细致的分类和定义, 能充分地反映动物觅食活动中普遍具有的警觉行为动作及特征, 并依据警觉-功能反应模型理论定量分析了个体的觅食代价, 因而能够很好地阐明视野受阻条件下东方田鼠觅食行为的适应性策略。
综上所述, 尽管视野受阻能影响东方田鼠觅食活动中各警觉行为动作的发生频次及持续时间, 实验个体各警觉动作发生频次格局却与分配于各警觉动作的时间格局迥然不同, 但觅食中断时间保持稳定。说明, 在视野受阻程度不同的食物斑块上, 东方田鼠能够通过觅食活动中的警觉行为动作调节, 使摄入率保持稳定。
致谢: 邓凯东教授帮助英文写作,特此致谢。| [1] | Brown J S, Kotler B P. Hazardous duty pay and the foraging cost of predation. Ecology Letters, 2004, 7(10): 999–1014. DOI:10.1111/ele.2004.7.issue-10 |
| [2] | Lima S L, Dill L M. Behavioral decisions made under the risk of predation:a review and prospectus. Canadian Journal of Zoology, 1990, 68(4): 619–640. DOI:10.1139/z90-092 |
| [3] | Fortin D, Boyce M S, Merrill E H, Fryxell J M. Foraging costs of vigilance in large mammalian herbivores. Oikos, 2004, 107(1): 172–180. DOI:10.1111/oik.2004.107.issue-1 |
| [4] | 陶双伦, 杨锡福, 邓凯东, 张良军, 李俊年, 刘季科. 东方田鼠警觉对其功能反应的作用格局. 生态学报, 2011, 31(2): 410–420. |
| [5] | Searle K R, Hobbs N T, Shipley L A. Should I stay or should I go? Patch departure decisions by herbivores at multiple scales. Oikos, 2005, 111(3): 417–424. DOI:10.1111/oik.2005.111.issue-3 |
| [6] | 陶双伦, 张伟华, 李俊年, 何岚, 杨锡福. 植食性哺乳动物能量收益增长减速机制的检验. 生态学报, 2010, 30(18): 4839–4847. |
| [7] | Monclús R, Rödel H G. Different forms of vigilance in response to the presence of predators and conspecifics in a group-living mammal, the European rabbit. Ethology, 2008, 114(3): 287–297. DOI:10.1111/eth.2008.114.issue-3 |
| [8] | 马静, 陶双伦, 杨锡福, 姚小燕, 王璐, 李俊年. 捕食风险对东方田鼠功能反应格局的作用. 生态学报, 2013, 33(9): 2734–2743. |
| [9] | Elgar M A. Predator vigilance and group size in mammals and birds:a critical review of the empirical evidence. Biological Reviews, 1989, 64(1): 13–33. DOI:10.1111/brv.1989.64.issue-1 |
| [10] | Lima S L. Vigilance and foraging substrate:anti-predatory considerations in a non-standard environment. Behavioral Ecology and Sociobiology, 1992, 30(3/4): 283–289. |
| [11] | Tchabovsky A V, Krasnov B, Khokhlova I S, Shenbrot G I. The effect of vegetation cover on vigilance and foraging tactics in the fat sand rat Psammomys obesus. Journal of Ethology, 2001, 19(2): 105–113. DOI:10.1007/s101640170006 |
| [12] | Beauchamp G. How does food density influence vigilance in birds and mammals?. Animal Behaviour, 2009, 78(2): 223–231. DOI:10.1016/j.anbehav.2009.04.029 |
| [13] | Powolny T, Eraud C, Masson, J D, Bretagnolle V. Vegetation structure and inter-individual distance affect intake rate and foraging efficiency in a granivorous forager, the Eurasian Skylark Alauda arvensis. Journal of Ornithology, 2015, 156(3): 569–578. DOI:10.1007/s10336-015-1161-1 |
| [14] | Favreau F R, Pays O, Fritz H, Goulard M, Best E C, Goldizen A W. Predators, food and social context shape the types of vigilance exhibited by kangaroos. Animal Behaviour, 2015, 99: 109–121. DOI:10.1016/j.anbehav.2014.11.001 |
| [15] | Berger-Tal O, Embar K, Kotler B P, Saltz D. Everybody loses:intraspecific competition induces tragedy of the commons in Allenby's gerbils. Ecology, 2015, 96(1): 54–61. DOI:10.1890/14-0130.1 |
| [16] | Lima S L, Bednekoff P A. Back to the basics of antipredatory vigilance:can nonvigilant animals detect attack?. Animal Behaviour, 1999, 58(3): 537–543. DOI:10.1006/anbe.1999.1182 |
| [17] | Spalinger D E, Hobbs N T. Mechanisms of foraging in mammalian herbivores:new models of functional response. The American Naturalist, 1992, 140(2): 325–348. DOI:10.1086/285415 |
| [18] | Hobbs N T, Gross J E, Shipley L A, Spalinger D E, Wunder B A. Herbivore functional response in heterogeneous environments:a contest among models. Ecology, 2003, 84(3): 666–681. DOI:10.1890/0012-9658(2003)084[0666:HFRIHE]2.0.CO;2 |
 2017, Vol. 37
2017, Vol. 37