文章信息
- 郑雨婷, 王梦馨, 崔林, 韩善捷, 俞鹏飞, 韩宝瑜.
- ZHENG Yuting, WANG Mengxin, CUI Lin, HAN Shanjie, YU Pengfei, HAN Baoyu.
- 基于EPG技术分析茶树品种对茶小绿叶蝉的抗性及其相关的抗性物质
- Resistance of tea cultivars to the tea green leafhopper analyzed by EPG technique and their resistance-related substances
- 生态学报. 2017, 37(23): 8015-8028
- Acta Ecologica Sinica. 2017, 37(23): 8015-8028
- http://dx.doi.org/10.5846/stxb201704270770
-
文章历史
- 收稿日期: 2017-04-27
- 网络出版日期: 2017-09-09
假眼小绿叶蝉Empoasca vitis (Göthe)(半翅目, 叶蝉科)是我国大陆茶园最重要的害虫, 成、若虫刺吸茶树嫩芽、嫩叶和嫩茎的汁液, 雌成虫产卵于嫩茎皮层, 注入酶类于茶树茎叶, 影响芽叶生理生化代谢以及营养物质的正常运输, 致芽叶失水凋萎、叶脉暗红、叶缘叶尖卷曲、叶片红褐焦枯, 以至于脱落。常年致茶叶减产10%左右, 严重时可达30%以上或超过50%[1]。几十年来主要依靠化学防治, 虽有效控制假眼小绿叶蝉的发生和为害, 但其已对吡虫啉、联苯菊酯和啶虫脒等化学农药产生显著抗性[2]。业界估测, 约有40%的茶园施药量是用于防治假眼小绿叶蝉的。大量的施药时常造成茶叶农残超标, 影响健康饮用。为减少化学农药施用量, 可充分利用茶树自身所具有的形态抗性、抗生性和耐害性等御虫机制。我国茶树种质资源丰富, 不乏抗性品种, 曾莉等[3]鉴定了西双版纳国家茶树种质资源圃30份茶树种质对假眼小绿叶蝉的抗性, 发现茶树抗性与叶片叶肉厚度、上表皮细胞数、栅栏组织厚度和海绵组织厚度皆呈负相关。黄亚辉等[4]也报道, 茶梢上假眼小绿叶蝉虫口密度与茶树叶片栅栏组织厚度、海绵组织厚度、主脉下方表皮厚度和主脉下方厚角组织厚度呈极显著负相关。即茶树形态具有抗叶蝉性能, 而抗生性也是植物抗虫性重要性能, 涉及的机理更为复杂, 需进一步深入探讨。
刺探电位技术(electrical penetration graph, EPG)是一项用于研究刺吸式口器害虫在寄主植物上取食行为的电生理技术, 它能够将昆虫口针在抗、感性植物组织内的取食活动转化为可视电信号, 准确记录昆虫口针在植物组织中的刺探行为和位置[5-6]。EPG作为抗虫性的辅助研究手段, 近20—30年在国际植保领域取得了长足进展, 研究对象已从蚜虫扩展到粉虱、蓟马、叶蝉和盲蝽等大多数刺吸式昆虫[7-9]。研究内涵不断拓展, 从基础波形的定义、生物学意义鉴定直至应用, Miranda等[10]、Zeng等[11]、Cameron等[12]利用EPG探究了各种杀虫剂对各类昆虫在其寄主植物取食上的影响, 发现杀虫剂皆能减弱昆虫的取食行为, 但不同杀虫剂减少昆虫取食程度存在差异。Lei等[13]、Zhao等[14]利用EPG技术研究了携带病毒植物对刺吸式昆虫取食的影响。而1970年Crane则最早应用EPG技术研究了叶蝉Hordnia circellata Baker的取食行为, 随后研究者们相继对叶蝉科昆虫取食行为进行了细致的探究[15-18]。苗进等[19-20]参考叶蝉等其他刺吸式取食昆虫的波形, 首次探讨了假眼小绿叶蝉在茶树新梢上刺探电位波形的类型及其与刺探取食行为之间的对应关系, 明确其取食波为A、E、C、F、R、S和非刺探波NP等7种波形。金珊等[21-22]利用EPG技术结合体视显微镜和口针切片技术, 鉴定得到的假眼小绿叶蝉取食波形为E1、E2、E3、E4、E5和E6波, 分别对应A、E、C、F、R和S波。
在假眼小绿叶蝉波形特征和生物学意义鉴定的基础上, 苗进等[19-20]、金珊等[21-22]和刘丽芳等[23]基于EPG技术评判了数种茶树品种对假眼小绿叶蝉感、抗性, 其结果与田间叶蝉虫口密度大小基本一致, 支持了EPG技术检测茶树抗虫性的可信性。然而, 我国茶树种植资源已记载3000多份, 已有的少量茶树品种(系)的抗虫性报道主要是调研了品种之间虫口密度差异, 很少涉及茶叶化学组成, 关于茶树抗虫性与EPG波形的相关性未见报道。本研究以现阶段全国广泛推广的11个国家级茶树良种和特色良种为试验材料, 利用EPG技术解读假眼小绿叶蝉在这些品种上的取食行为, 进而评定茶树品种抗、感性差异, 再检测茶叶化学组成, 探析抗感性与化学组成的关系, 为深入研究茶树抗虫性提供参考。
1 材料与方法 1.1 供试虫源将假眼小绿叶蝉雌、雄成虫配对接种于中国计量大学实验茶园的盆栽茶树上, 罩上60目养虫笼以防其逃逸。叶蝉产卵于茶树嫩枝上, 遂剪取1芽7叶茶枝水培于人工气候箱, 箱内温度(25±2)℃, 相对湿度75%±5%, 光照L:D=14:10。待茶枝上卵孵化为若虫, 继续观测其发育, 选择生长一致的3龄若虫用于EPG试验。
1.2 供试茶树品种选用单行条植于中国计量大学试验茶园中的铁观音、金观音、黄观音、紫牡丹、黄牡丹、龙井43、安吉白茶、宁波黄金芽、紫鹃、中茶108和乌牛早等11个茶树良种, 试验时剪取健壮的1芽4叶茶枝, 插入培养钵中, 引入供试的3龄叶蝉于其上。
1.3 EPG技术记录和各种波形的统计分析 1.3.1 EPG记录采用Tjallingii设计的DC-EPG Giga-8型EPG记录仪。将假眼小绿叶蝉3龄若虫和供试茶树嫩枝分别与生物电流放大器的昆虫电极和植物电极相连。昆虫电极是一段长3—4cm、直径18.5μm的金丝。粘连昆虫时, 先将培养皿放在冰袋上, 放入假眼小绿叶蝉3龄若虫, 迅速盖上皿盖, 待叶蝉不动时用毛笔轻轻调整叶蝉位置, 使其背部朝上。金丝端部蘸少量银胶, 形成银胶滴, 粘接叶蝉中胸背板。粘接之后, 让叶蝉在叶片上自由活动, 饥饿1h, 再小心地将连有叶蝉若虫的昆虫电极插入放大器的输入探头, 轻轻地将假眼小绿叶蝉接到芽下第二叶背面。由于金丝柔软, 叶蝉可在一定范围内自由活动。将植物电极插入栽有1芽4叶鲜嫩茶梢的盆钵基质中。当昆虫口针刺入植物组织时, 则回路闭合, 回路电流经AD转换器放大、转换为数字信号保存于电脑内, 经Probe 3.0软件转化为波形图谱输出, 显示在电脑屏幕上, 供研读并转换为可供统计的数字文件。
1.3.2 统计分析叶蝉在每个品种上的取食行为连续记录5h, 每次同时测试8头, 试验皆在室温(25±2)℃下进行。参照前人研究, 确定与假眼小绿叶蝉取食相关波形。统计分析时选其中10头供试叶蝉EPG图谱, 分析供试叶蝉在每个品种上的每种波形历期、刺探次数。对品种之间取食相关波形(E、F、A、S、C和R波)历期、非取食波(Np波)历期、以及刺探次数分别作差异性检验;以E波历期、F波历期和刺探次数作为参数, 将11个品种作为实体进行聚类分析, 先评判“类”之间抗感性差异, 再基于取食相关波形(E波、F波)历期、刺探次数评判“类”内的品种之间抗感性差异, 进而对11个品种的抗感性排序。
1.4 茶叶理化成分检测及其与抗性的相关性分析 1.4.1 仪器及试剂HPLC由美国Agilent公司制造, 型号为Agilent1260。所用乙腈、甲醇为色谱纯, 醋酸钠、三乙胺、乙醇、氧化镁和盐酸为分析纯;PITC购自Aladdin公司, 纯度标示量为98.0%;纯净水为Milli-Q纯水。
咖啡碱、儿茶素、茶氨酸和17种氨基酸标样购自Agilent公司, 17种氨基酸混合标准品包括天冬氨酸(Asp)、谷氨酸(Glu)、丝氨酸(Ser)、甘氨酸(Gly)、组氨酸(His)、精氨酸(Arg)、苏氨酸(Thr)、丙氨酸(Ala)、脯氨酸(Pro)、胱氨酸(Cys)、酪氨酸(Tyr)、缬氨酸(Val)、甲硫氨酸(Met)、异亮氨酸(Ile)、亮氨酸(Leu)、苯丙氨酸(Phe)和赖氨酸(Lys)。儿茶素标样包括:儿茶素(C)、表儿茶素(EC)、表没食子儿茶素(EGC)、表儿茶素没食子酸酯(ECG)、没食子儿茶素没食子酸酯(GCG)和表没食子儿茶素没食子酸酯(EGCG)。
1.4.2 茶叶主要理化成分检测5月上旬假眼小绿叶蝉盛发时采摘供试茶树品种的1芽2叶, 制成蒸青茶样, 装入塑封袋置于-20 ℃冰箱备用。测定生化成分时根据具体分析方法取出适量样品进行相应的前处理。
可溶性糖测定:称取0.2g茶粉放入试管中, 注入10mL蒸馏水, 在沸水浴上加热提取可溶性糖类。提取液冷却后在3000r/min下离心30min, 将上清液即粗提液稀释10倍后以蒽酮比色法测定可溶性糖含量。重复5次, 计算平均值。
氨基酸测定:称取2.0g茶粉置于具磨口塞的锥形瓶中, 加入75mL去离子水, 盖好瓶盖, 沸水浴浸提1h。吸取6mL提取液, 在2000r/min下离心5min。吸取2mL上清液用0.45μm滤膜过滤。吸取600μL滤液于2.0mL的EP管中, 加入0.2mol/L PITC-乙腈溶液以及1mol/L三乙胺-乙腈溶液各200μL, 轻摇, 再用涡旋器振荡1min以便混匀。室温下静置lh, 加入400μL正己烷, 涡旋震荡1min后静止30min, 取下层溶液进HPLC测定氨基酸含量。重复5次, 计算平均值。
分析氨基酸的色谱条件:色谱柱为PhenomenexLuna C18色谱柱(4.6mm×250mm, 5μm), 柱温为43℃。流动相A:V[0.1 mol/L醋酸钠缓冲液(以醋酸调pH6.5)]:V(乙腈)=93:7;流动相B:V(乙腈):V(水)=4:1。流动相经0.45μm滤膜过滤。梯度洗脱:0—20min, 0—4%B;20—21min, 4%—20%B;21—40min, 20%—22%B; 40—41min, 22%—30%B;41—46min, 30%—100%B; 46—48min, 100% B; 48—53min, 100%—0B;53—60min, 0%B。流速:1.0mL/min。检测波长为254nm;进样量20μL。
儿茶素含量测定:称取0.2g茶粉, 放入试管中, 加入50%甲醇溶液9mL, 30s涡旋混匀后, 常温下超声10min, 3000r/min下离心10min, 取上清液用EDTA溶液稀释10倍后经0.45μm滤膜过滤, 滤液用于HPLC测定儿茶素含量。重复5次, 计算平均值。
检测儿茶素的色谱条件:色谱柱为PhenomenexLuna C18色谱柱(4.6mm×250mm, 5μm), 柱温为30℃。流动相A:V(乙酸):V(乙腈)=1:999;流动相B:乙腈。流动相经0.45μm滤膜过滤。梯度洗脱:0—30min, 0%B—15%B;30—40min, 15%—25%B;40—50min, 40%—60%B。流速:0.5mL/min。检测波长为278nm;进样量为20μL。
咖啡碱按照国标8312—2013方法测定[24]。
1.4.3 茶叶主要理化成分与抗性的相关性分析可溶性糖、氨基酸、儿茶素和咖啡碱是茶叶主要成分, 分析这4类物质的含量分别与供试叶蝉若虫在不同品种上刺探次数、韧皮部取食波(E波)平均历期和韧皮部困难波(F波)平均历期的相关性。用DPS软件完成相关计算[25]。
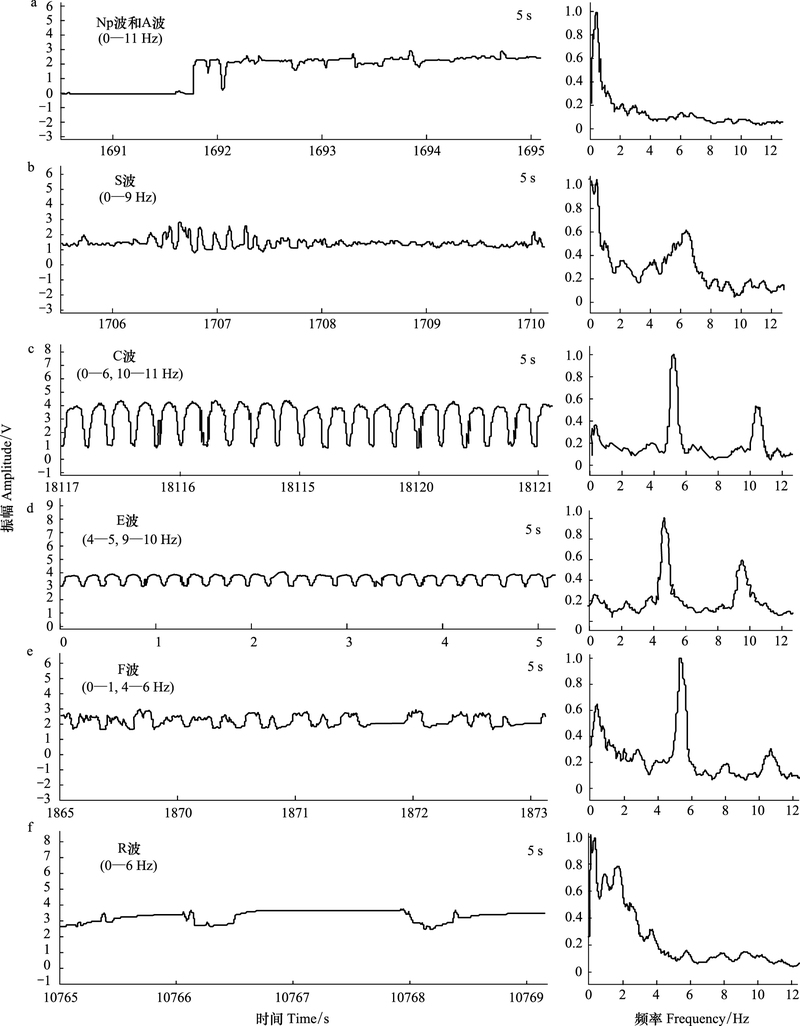
2 结果和分析 2.1 假眼小绿叶蝉刺吸波形的特征及其出现规则本研究得到7种主要波形及特征如图 1, 与苗进等[19-20]金珊等[21-22]鉴定的相似。本研究参照苗进等的方法命名波形(图 1、图 2), 并详细地观察了各种波形出现的规则:
|
| 图 1 假眼小绿叶蝉在茶树上取食波形及其频率 Fig. 1 EPG waveforms and frequency of E.vitis feeding on tea cultivars Np波:非刺探波;A波:路径波;S波:口针向韧皮部刺探和进入韧皮部的唾液分泌波;C波:口针到达韧皮部前的主动取食波;E波:韧皮部取食波;F波:取食困难波;R波:休息波 |
|
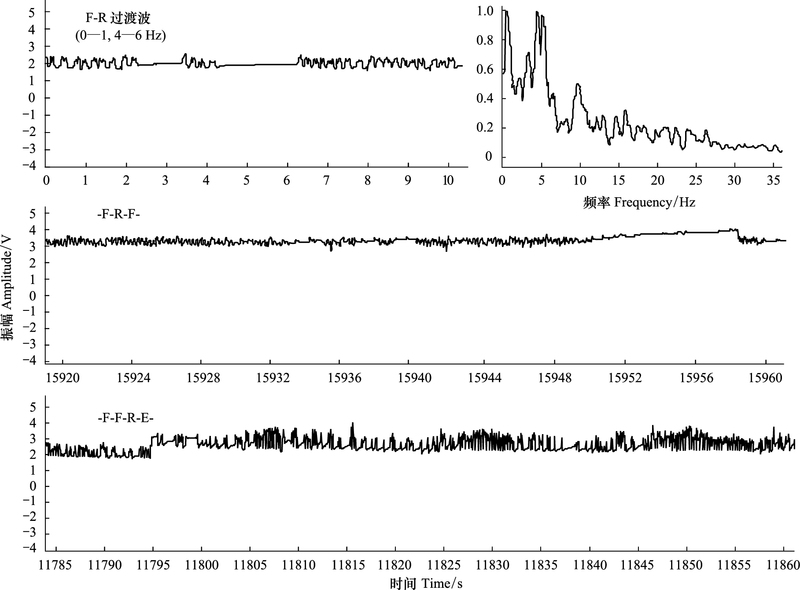
| 图 2 F-R过渡波及其频率和E、F、R波转换 Fig. 2 F-R Transition waveform with its frequency and transition among waveforms E, F and R |
(1) Np波:非刺探波;A波:路径波;S波:口针向韧皮部刺探和进入韧皮部的唾液分泌波;C波:口针到达韧皮部前的主动取食波;E波:韧皮部取食波;F波:取食困难波;R波:休息波。Np波是叶蝉口针刺探叶片前的一段平直波, 在电压为0的基准线上, 此时叶蝉若虫在叶片表面走动但不引起电压变化(图 1)。
(2) 分析发现, 在叶蝉口针刺透叶片之前, 许多茶树品种上叶蝉刺吸的EPG图谱只是振幅很低的杂乱波形, 持续时间通常少于30s。在叶蝉每次取食过程中, 通常以A波开始和结束, 其频率范围为0—1Hz, 主频为0.5Hz。S波紧随A波之后或出现在E波和F波之间, 频率范围0—9Hz, 主频为0—1Hz。C波在E波之前出现, 持续时间短, 主频为5—6Hz, 次频为10—11Hz, 振幅大, 波形有规律。E波每次持续时间长短不一, 主频为4—5Hz, 次频为9—10Hz, 振幅和频率皆低于C波, 波形成锯齿状。F波通常出现在E波之后, 频率混杂, 主频为4—5Hz, 次频为0—1Hz, F波的波形在不同茶树品种上略有差异。R波则在F波之后出现, 频率混杂, 主频为0—1Hz, 波形多样, 通常是平缓的线条。在本研究中, F波经常与E波或R波交错出现。而R波随F波出现, 主要以两种模式出现:一是与F波交错出现(图 2), 二是保持一条平直的波形缓慢下降到口针拨出。此外, 在F波与R波交错过程中还观察到F-R的过渡波形(图 1), 波形似F波与R波的结合, 频率混杂, 主频为0-5Hz。假眼小绿叶蝉一次完整刺探波形基本模式为:Np-A-S-C-E-F-(E-F)R-(F-R)A-Np, 非完整取食波形基本模式有:Np-A-Np, Np-A-S-C-E-A-Np, Np-A-E-S-F-R-Np, Np-A-E-F-E-F-R-A-Np等。
2.2 假眼小绿叶蝉在不同茶树品种上取食行为的差异供试叶蝉在11个茶树品种上各种波形历期占总记录时间百分率如图 3, 刺探次数和各种波形历期如表 1。黄观音和龙井43上的刺探次数最多;紫鹃、宁波黄金芽和金观音上的次之;铁观音和安吉白茶上刺探次数最少, 皆少于30次。铁观音和黄牡丹上E波的平均持续时间最长, 皆超过50min, 分别占整个测试时间的17.29%和17.01%, 乌牛早和安吉白茶的次之, 紫鹃的最短、仅占6.30%。黄观音上F波平均持续时间最长, 占整个测试时间的17.66%, 紫鹃、龙井43和宁波黄金芽上F波平均持续时间次之, 金观音上F波平均持续时间最短、只占6.06%。Np波在11个供试品种上的历时最长, 金观音品种上的非刺探波(Np波)历时最长, 黄观音的最短, 分别占总记录时间的65.38%和40.62%, 两者间差异达到显著水平(P<0.05)。路径波A波占整个测试时间的百分率:黄观音和紫鹃上的最大, 分别是15.86%和15.80%, 龙井43(13.00%)和金观音(11.7%)次之, 皆显著高于黄牡丹(6.98%)和铁观音(5.36%)。R波占整个测试时间的百分率:宁波黄金芽和中茶108上分别为21.37%和19.03%, 显著大于金观音(3.81%)和黄牡丹(3.55%)。比较发现:(1)黄观音、龙井43、金观音和紫鹃刺探次数多、路径刺探波时间长;(2)非韧皮部取食总的刺探时间(路径波、唾液分泌波和休息波之和)以紫鹃(34.13%)、黄观音(33.91%)和宁波黄金芽(33.26%)最长, 铁观音(13.64%)和黄牡丹(11.74%)最短;(3)韧皮部取食时间(取食波E波和取食困难波F波之和)以黄牡丹、黄观音和铁观音最长, 分别占25.09%、24.90%和24.88%, 金观音最短, 只占13.29%, 方差分析显示四者间差异达到显著水平(P<0.05)。

|
| 图 3 假眼小绿叶蝉7种EPG波形历期在11个茶树品种上占5h测试时间百分率 Fig. 3 The percentage of 7 EPG waveforms′ average duration of E.vitis on each of 11 tea plant cultivars during 5 hours a:紫鹃;b:龙井43;c:宁波黄金芽;d:黄观音;e:金观音;f:中茶108;g:紫牡丹;h:安吉白茶;i:乌牛早;j:黄牡丹;k:铁观音 |
| 品种 Cultivar |
刺探次数 Probe number |
A波 Waveform A/min |
S波 Waveform S/min |
C波 Waveform C/min |
E波 Waveform E/min |
F波 Waveform F/min |
R波 Waveform R/min |
Np波 Waveform Np/min |
| 紫鹃 Camellia sinensis (L.) ‘Zijuan’ |
63.3±19.57ab | 47.4±10.7a | 6.14±1.16c | 0.05±0.03b | 18.9±2.94c | 48.8±8.53a | 48.84±14.13abc | 133.08±13.86de |
| 龙井43 Camellia sinensis (L.) ‘Longjing 43’ |
78.5±17.98a | 38.99±5.87ab | 7.5±2.76bc | 0.23±0.09b | 21.12±4.31bc | 43.52±7.03a | 47.54±11.25abc | 141.07±15.74bcde |
| 宁波黄金芽 Camellia sinensis (L.) ‘Ningbohuangjinya’ |
64.5±13.33ab | 32.45±7.81ab | 3.22±0.73c | 0.1±0.07b | 21.64±4.06bc | 41.79±7.52ab | 64.11±20.24a | 136.65±20.58cde |
| 黄观音 Camellia sinensis (L.) ‘Huangguanyin’ |
77.2±21.6a | 47.59±14.35a | 15.44±3.79ab | 1.72±0.78b | 21.71±3.51bc | 52.98±4.8a | 38.69±8.74abc | 121.85±10.15e |
| 金观音 Camellia sinensis (L.) ‘Jinguanyin’ |
64.6±10.09ab | 35.13±6.03ab | 10.31±3.06abc | 7.07±2.7a | 21.71±6.04bc | 18.17±4.25c | 11.44±5.49c | 196.13±13.12a |
| 中茶 Camellia sinensis (L.) ‘Zhoingcha 108’ |
32.6±2.79b | 32.1±7.89ab | 5.49±1.73c | 2.91±1.07ab | 26.31±5.96bc | 19.32±3.14c | 57.09±14.27ab | 156.76±16.81abcde |
| 紫牡丹 Camellia sinensis (L.) ‘Zimudan’ |
42.3±13.18ab | 27.89±10.14ab | 3.88±1.14c | 7.17±4.13a | 32.74±4.37bc | 21.54±6c | 33.31±14.48abc | 173.45±13.63abcd |
| 安吉白茶 Camellia sinensis (L.) ‘Anjibaicha’ |
29.7±2.58b | 22.56±3.25ab | 16.88±5.94a | 0.84±0.52b | 37.37±6.78abc | 20.74±4.89c | 29.9±11.63abc | 171.68±13.88abcd |
| 乌牛早 Camellia sinensis (L.) ‘Wuniuzao’ |
46.66±6.84ab | 24.89±4.7ab | 10.86±2.84abc | 1.37±0.52b | 40.06±11.49ab | 26.66±5.58bc | 48.88±18.65abc | 147.26±22.13bcde |
| 黄牡丹 Camellia sinensis (L.) ‘Huangmudan’ |
30.1±7.37b | 20.95±4.62b | 3.61±1.18c | 1.38±0.51b | 51.04±3.76a | 24.22±3.64c | 10.65±2.52c | 188.12±3.77ab |
| 铁观音 Camellia sinensis (L.) ‘Tieguanyin’ |
29.54±6.11b | 16.09±2.99b | 3.89±1.28c | 1.86±1.03b | 51.88±7.48a | 22.75±2.99c | 20.93±4.94bc | 182.58±7.53abc |
| 标有不同字母的同一列数据(平均差±标准误)之间的差异达显著水平(P<0.05);采用了Duncan′s多重比较Np波:非刺探波;A波:路径波;S波:口针向韧皮部刺探和进入韧皮部的唾液分泌波;C波:口针到达韧皮部前的主动取食波;E波:韧皮部取食波;F波:取食困难波;R波:休息波 | ||||||||
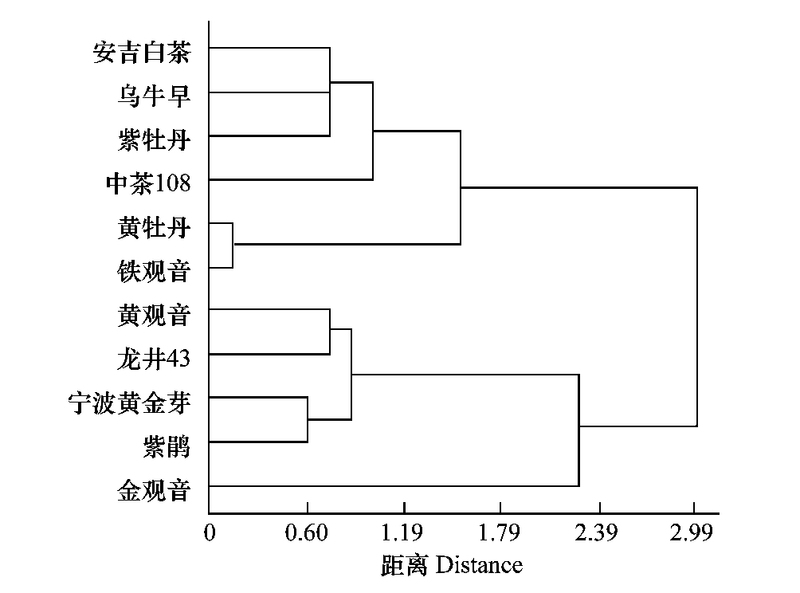
假眼小绿叶蝉主要以口针刺透叶肉细胞和吸取汁液而危害茶树, 研究发现以取食波的历期长短作为主要指标衡量茶树抗感性与田间调查结果基本一致[19, 21-22]。本研究选用假眼小绿叶蝉口针在茶叶上的刺探次数、在韧皮部取食波E波历期和韧皮部取食困难波F波历期等3个参数, 先进行标准化转换, 消除量纲, 再使用类平均法进行系统聚类, 将11个品种归纳为2大类(图 4)。第Ⅰ类:安吉白茶、乌牛早、紫牡丹、中茶108、黄牡丹和铁观音等6个品种;第Ⅱ类:黄观音、龙井43、紫鹃、宁波黄金芽和金观音等。对这2种类型品种上的EPG相关参数进行统计分析(表 2)发现:(1)第Ⅰ类上的叶蝉平均刺探次数、A波和F波平均历期均显著低于第Ⅱ类(P<0.05);(2)第Ⅰ类上E波历期和NP波历期则显著高于第Ⅱ类;(3)S波、C波和R波在2种类型之间均未达到显著性差异。可见, 叶蝉在两类品种之间的取食行为有显著差异, 以第Ⅱ类抗性较强。
|
| 图 4 假眼小绿叶蝉在11个茶树品种上取食行为的类平均法聚类图 Fig. 4 Cluster analysis diagram for feeding behavior of E.vitis on 11 tea plant cultivars based on average-linkage cluster method |
| 类别 Type |
刺探次数 Probe number |
A波 Waveform A /min |
S波 Waveform S /min |
C波 Waveform E /min |
E 波Waveform E /min |
F波 Waveform F /min |
R波 Waveform R /min |
Np波 Waveform Np /min |
| 第Ⅰ类抗性品种 Type Ⅰ resistant cultivar |
34.08±2.96b | 24.08±2.49b | 7.44±1.3a | 2.59±0.76a | 39.9±3.02a | 22.54±1.79b | 33.46±5.27a | 169.97±5.86a |
| 第Ⅱ类抗性品种 Type Ⅱ resistant cultivar |
69.62±7.36a | 40.31±4.17a | 8.52±1.25a | 1.83±0.66a | 21.02±1.85b | 41.05±3.32a | 42.12±6.09a | 145.75±7.45b |
若以韧皮部取食波E波历期和刺探次数为指标, 则11个茶树品种对叶蝉抗性排序为:紫鹃>龙井43>宁波黄金芽>金观音、黄观音>中茶108>紫牡丹>安吉白茶>乌牛早>黄牡丹>铁观音。
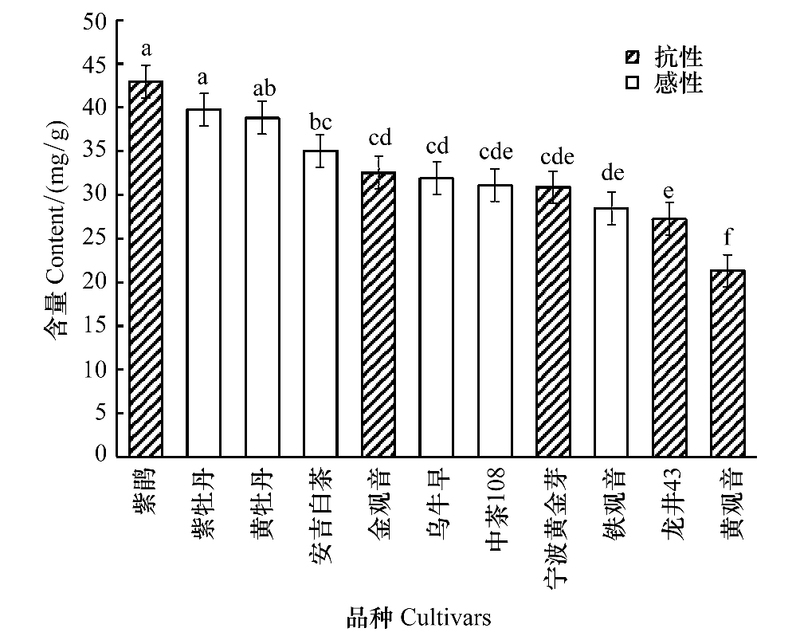
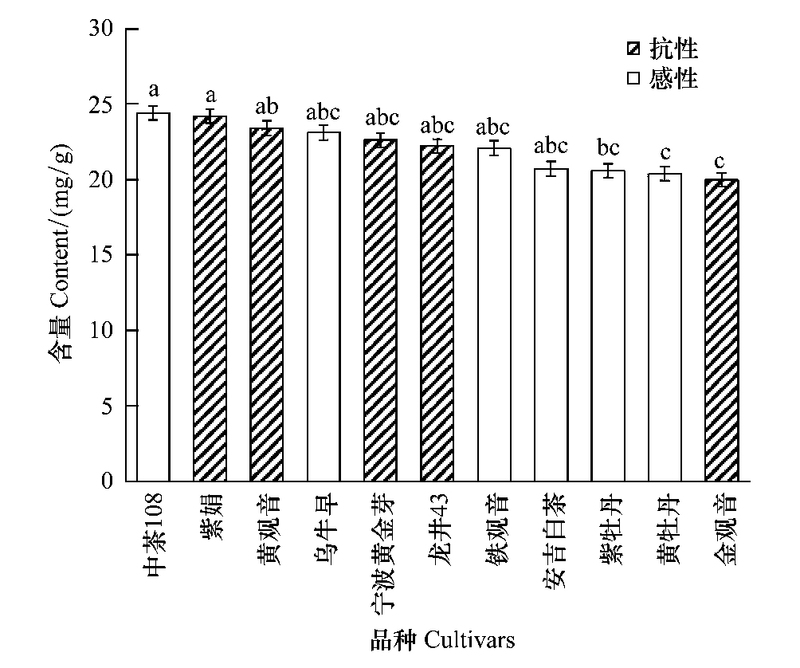
2.4 供试茶树品种主要化学成分含量及其与抗性的相关性本研究检测了11个茶树品种芽梢的儿茶素、咖啡碱、氨基酸和可溶性糖含量(表 3), 可见每个茶树品种中EGC和EGCG单体含量高于其他成分, 二者之和占总量50%以上;紫鹃、宁波黄金芽和龙井43的儿茶素总量较高, 显著高于紫牡丹的和安吉白茶的(P<0.05);抗性品种的儿茶素总量高于感性品种的。紫鹃和紫牡丹的咖啡碱含量最高, 金观音、乌牛早等品种的次之, 显著高于龙井43和黄观音的(P<0.05)(图 5)。中茶108、紫鹃的可溶性糖含量显著高于紫牡丹的、黄牡丹的和金观音的(P<0.05);其他茶树品种之间可溶性糖含量差异不明显(图 6)。本研究的11个茶树品种氨基酸总量占干重2.8%—4.5%(表 4), 茶氨酸含量最高, 脯氨酸次之;比较不同茶树品种氨基酸含量差异, 发现安吉白茶的氨基酸总量最高, 中茶108和乌牛早的次之, 皆显著高于黄牡丹的(P<0.05)。
| 品种Cultivar | EGC | EC | C | EGCG | GCG | ECG | 总量Total |
| 紫鹃Camellia sinensis (L.) ‘Zijuan’ | 36.97±1.54a | 0.53±0.09c | 1.44±0.04g | 19.48±0.51d | 75.11±4.66a | 2.51±0.51efg | 136.06±6.22a |
| 龙井43 Camellia sinensis (L.)‘Longjing 43’ | 21.12±3.15cd | 0.35±0.02c | 4.97±0.88de | 47.3±0.75a | 7.26±2.5b | 11.53±0.29def | 92.56±3.97b |
| 宁波黄金 Camellia sinensis (L.) ‘Ningbohuangjinya’ |
26.53±0.57bc | 0.61±0.08c | 8.05±0.09b | 40.16±1.87ab | 2.58±0.39bcd | 9.17±0.75bcd | 87.12±2.76b |
| 金观音 Camellia sinensis (L.)‘Jinguanyin’ | 19.86±1.71cde | 2.98±1.4b | 4.8±1.2de | 47.6±3.7a | 2.96±0.93bcd | 8.28±1.43a | 86.49±7.31b |
| 黄观音 Camellia sinensis (L.)‘Huangguanyin’ | 30.79±5.57ab | 5.65±1.07a | 5.95±1.35cd | 35.98±1.62bc | 0.17±0.11d | 4.54±0.34abc | 83.11±6.26bc |
| 中茶108 Camellia sinensis (L.)‘Zhongcha 108’ | 14.33±0.24def | 3.3±0.58b | 2.96±0.12efg | 43.53±3.43ab | 6.72±1.23bc | 7.81±1.41bcd | 78.66±5.43bcd |
| 紫牡丹 Camellia sinensis (L.)‘Zimudan’ | 27.91±0.46bc | 0.85±0.03c | 10.8±0.06a | 23.04±0.49d | 0.14±0.14d | 10.34±0.31g | 73.1±0.3bcd |
| 安吉白茶 Camellia sinensis (L.)‘Anjibaicha’ | 21.34±0.6cd | 7.33±0.51a | 7.24±0.85bc | 21.75±0.41d | 0.12±0.12d | 4.09±0.07fg | 61.88±1.37de |
| 乌牛早 Camellia sinensis (L.)‘Wuniuzao’ | 12.32±2.66ef | 0.4±0.03c | 1.47±0.22g | 42.98±7.02ab | 1.8±1.08bcd | 7.16±1.8g | 66.14±11.93cd |
| 黄牡丹 Camellia sinensis (L.)‘Huangmudan’ | 11.48±1.77f | 0.34±0.01c | 2.57±0.35fg | 28.76±2.93cd | 0.26±0.26d | 2.75±0.73ab | 46.17±6.04d |
| 铁观音 Camellia sinensis (L.)‘Tieguanyin’ | 24.91±3.32bc | 0.31±0c | 4.31±0.31def | 36.32±2.36bc | 1.42±0.5cd | 5.92±0.56cde | 73.21±4.1bcd |
|
| 图 5 11个茶树品种咖啡碱含量(按含量从高到低排列) Fig. 5 Content of caffeine from each of eleven tea cultivars (the order from high low to content) |
|
| 图 6 11个茶树品种中可溶性糖含量(按含量从高到低排列) Fig. 6 Content of soluble sugar from each of eleven tea cultivars (the order from high to low content) |
| 成分Component | 安吉白茶 Camellia sinensis (L.) ‘Anjibaicha’ |
黄观音 Camellia sinensis (L.) ‘Huangguanyin’ |
黄牡丹 Camellia sinensis (L.) ‘Huangmudan’ |
金观音 Camellia sinensis (L.) ‘Jinguanyin’ |
龙井43 Camellia sinensis (L.) ‘Longjing 43’ |
宁波黄金芽 Camellia sinensis (L.) ‘Ningbo- huangjinya’ |
铁观音 Camellia sinensis (L.) ‘Tieguanyin’ |
乌牛早 Camellia sinensis (L.) ‘Wuniuzao’ |
中茶108 Camellia sinensis (L.) ‘Zhongcha 108’ |
紫鹃 Camellia sinensis (L.) ‘Zijuan’ |
紫牡丹 Camellia sinensis (L.) ‘Zijuan’ |
| 天冬氨酸Asp | 1.59±0.36bcd | 1.12±0.64cd | 0.25±0d | 3.00±0.48ab | 3.72±1.34a | 1.59±0.2bcd | 0.25±0d | 2.61±0.44abc | 3.8±0.77a | 0.84±0.27cd | 1.28±0.22bcd |
| 谷氨酸Glu | 1.57±0.15bc | 2.02±1.47abc | 4.75±0.42ab | 1.86±0.56bc | 1.98±0.39abc | 3.00±0.4abc | 5.97±2.89a | 2.03±1.03abc | 1.6±0.31bc | 0.00±0c | 1.32±0.09bc |
| 丝氨酸Ser | 1.02±0.04bc | 0.39±0.14cd | 1.24±0.04ab | 1.3±0.09ab | 0.84±0.2bcd | 3.00±0.07cd | 0.27±0.01d | 0.65±0.57bcd | 1.8±0.19a | 1.18±0.01ab | 0.83±0.06bcd |
| 甘氨酸Gly | 0.25±0.01abcd | 0.34±0.27abc | 0.02±0cd | 0.14±0.05abcd | 0.38±0.05ab | 0.05±0.01cd | 0.27±0.09abcd | 0.44±0.08a | 0.1±0.07bcd | 0.00±0d | 0.07±0.03bcd |
| 组氨酸His | 0.25±0de | 1.44±0.52a | 1.14±0.05ab | 1.00±0.08abc | 0.63±0.09bcd | 0.92±0.07abc | 0.91±0.05abc | 0.47±0.25cde | 1.09±0.2abc | 0.00±0e | 1.16±0.1ab |
| 精氨酸Arg | 0.54±0.01ab | 0.55±0.07ab | 0.32±0.01bc | 0.82±0.02a | 0.57±0.03ab | 0.56±0.03ab | 0.07±0cd | 0.32±0.13bc | 0.32±0.24bc | 0.00±0d | 0.69±0.1a |
| 苏氨酸Thr | 0.15±0.01d | 0.23±0.11cd | 0.07±0d | 0.19±0d | 0.12±0.02d | 0.11±0d | 0.41±0.01b | 0.19±0.06d | 0.39±0.12bc | 0.69±0a | 0.11±0.02d |
| 丙氨酸Ala | 0.25±0bcd | 0.1±0.01f | 0.13±0def | 0.23±0.01cde | 0.27±0.08bc | 0.36±0.03b | 0.12±0ef | 0.22±0.05cdef | 0.18±0.05cdef | 2.21±0.03a | 0.21±0cdef |
| 脯氨酸Pro | 12.42±0.03a | 7.93±0.01c | 6.59±0.07c | 7.59±0.43c | 6.76±1.05c | 11.34±0.09ab | 7.46±0.08c | 9.8±0.44b | 11.11±0.27ab | 7.5±1.52c | 6.81±0.08c |
| 茶氨酸L-The | 20.73±0.55a | 14.46±0.83cd | 9.66±0.33f | 17.15±1.07b | 14.53±0.76cd | 16.26±0.21bc | 10.79±0.22ef | 19.68±1.33a | 16.68±1.1bc | 12.16±0.57de | 13.39±0.51d |
| 酪氨酸Cys | 1.47±0.05abc | 2.99±0.36a | 2.04±0.34abc | 1.4±0.05abc | 2.87±0.23ab | 1.39±0abc | 2.09±1.11abc | 1.79±1.35abc | 0.19±0c | 0.98±0.29bc | 0.81±0.18c |
| 缬氨酸Tyr | 2.06±0.02a | 0.74±0.45ab | 0.52±0.01ab | 0.59±0.37ab | 0.12±0.06b | 0.15±0.03b | 1.86±1.58ab | 0.4±0.3ab | 0.25±0.13b | 1.01±0.02ab | 0.3±0.19ab |
| 甲硫氨酸Val | 0.18±0.06bc | 0.36±0.25bc | 0.05±0c | 0.19±0.06bc | 1.59±0.01a | 0.32±0.01bc | 0.05±0c | 0.11±0bc | 0.68±0.5b | 0.61±0.05bc | 0.15±0bc |
| 胱氨酸Met | 0.18±0.02cd | 0.09±0.01d | 0.16±0cd | 0.12±0.03cd | 0.24±0.09bc | 0.07±0d | 0.12±0.01cd | 0.17±0cd | 0.34±0.02b | 2.29±0.04a | 0.23±0.05bc |
| 异亮氨酸Ile | 0.52±0.01b | 0.17±0.03c | 0.11±0c | 0.12±0.01c | 0.22±0.1c | 0.14±0c | 0.15±0.03c | 0.16±0.03c | 0.09±0c | 0.86±0.27a | 0.16±0.01c |
| 亮氨酸Leu | 0.12±0b | 0.11±0b | 0.2±0.01b | 0.12±0.01b | 0.11±0.01b | 0.12±0b | 0.11±0.01b | 0.16±0.03b | 0.17±0.03b | 0.66±0.18a | 0.14±0b |
| 苯丙氨酸Phe | 1.13±0.02cd | 1.34±0.37c | 0.69±0.07d | 2.57±0.2b | 0.66±0.21d | 1.11±0cd | 0.83±0.02cd | 0.11±0e | 0.87±0.05cd | 0.17±0.04e | 3.21±0.25a |
| 赖氨酸Lys | 0.34±0.04bc | 0.32±0.05bcd | 0.23±0.02ef | 0.35±0b | 0.24±0.02def | 0.23±0ef | 0.2±0f | 0.29±0.02bcde | 0.25±0cdef | 0.6±0.02a | 0.24±0.01ef |
| 总量Total | 44.85±0.56a | 34.8±1.91cde | 28.25±1.14f | 38.82±0.78bc | 35.95±1.3bcd | 37.6±0.68bc | 31.99±2.29def | 39.69±0.7b | 40±1.11b | 31.84±1.76def | 31.21±0.64ef |
分析各个茶树品种的化学成分与EPG抗性指标的相关性(表 5), 发现儿茶素总量与韧皮部取食波(E波)平均历期呈显著负相关(P < 0.05)。儿茶素总量与刺探次数和韧皮部取食困难波(F波)历期皆呈正相关, 但未达到显著水平。氨基酸、可溶性糖和咖啡碱含量与EPG韧皮部抗性指标(E、F波历期)都没有相关性。
| EPG参数 EPG parameter |
相关系数R Correlation coefficient R | |||
| 咖啡碱Caffeine | 儿茶素Catechin | 可溶性糖Soluble sugar | 氨基酸Amino acid | |
| 刺探次数Probe number | -0.389 | 0.611* | 0.056 | -0.013 |
| E波Waveform E | 0.154 | -0.731* | -0.204 | -0.262 |
| F波Waveform F | -0.284 | 0.617* | 0.308 | -0.225 |
| “**”表示相关性极显著(P < 0.01), “*”表示相关性显著(P < 0.05) | ||||
不同种类的刺吸式害虫取食策略存有差异, Backus等[26]发现叶蝉属取食策略为破损细胞取食, 金珊等[21-22]利用连续切片和TEM技术观察了人工饲料中、以及叶片组织中假眼小绿叶蝉口针取食活动, 判定假眼小绿叶蝉取食策略也为破损细胞取食, 叶蝉的破损细胞取食策略区别于蚜虫的胞间取食策略, 其对植物损伤更为严重。
在解析假眼小绿叶蝉取食波形的生物学意义时, 本研究主要参考苗进等[19-20]鉴定的7种波形特征及其生物学意义, 并结合金珊等[21-22]的研究, 对假眼小绿叶蝉取食波形进行鉴定, 还补充了新出现波形的特征。我们在分析过程中发现:多数茶树品种上, 在口针刺探前, EPG图谱呈振幅很低的杂乱波形;金珊等也在Np波中观察到不规则的小波;这是假眼小绿叶蝉在取食前对叶片表面的清扫行为。A波频率和波形特征与苗进等(A波)、金珊等(E1波)相似, 金珊等又将E1波细分为E1-A、E1-B和E1-C 3个亚波, 履行了1次刺探取食的开始和结束;A波有时出现在取食中间, A波是假眼小绿叶蝉刺透叶片、开通渠道和破损多细胞的过程。S波为唾液分泌波, 频率和波形特征与苗进等(S波)一致[19-20], 对应金珊等E6波[21-22], 通常出现在刺透叶片和韧皮部取食过程中。C波为口针到达韧皮部前的主动取食波;E波为韧皮部被动取食波;通过EPG分析比较, 发现C波持续时间仅占总测试时间的0.02%—2.39%, 远小于E波的持续时间和所占比例, 与刺吸式昆虫获得食物主要通过被动取食, 即韧皮部内的压强将汁液推入昆虫口针结论一致[27-28]。F波在已有研究报道中出现不多, 其频率与苗进等F波[19]、金珊等鉴定的E4波描述相似[21], 但其波形、持续时间和出现模式上稍有差异, 即本研究F波紧随E波出现, 波形复杂、总持续时间显著长于苗进等的F波、金珊等E4波的总持续时间。Njihia等[29]在组织学中演示推断与F波相似的Ib波, Ib波与缓慢移动口针刺透和吸取叶肉细胞浆液行为相关。Backus等[26]猜测F波代表单细胞刺透, 是一种破裂细胞取食行为。由此推测F波产生时口针仍位于韧皮部吸取汁液, 但韧皮部中可能存在某种物质阻碍假眼小绿叶蝉正常取食, 又不至于无法取食。
R波频率特征与苗进等R波[20]、金珊等E5波[22]相似, 在金珊等研究中E5波不易被观察到, 持续时间短, 出现在E4波(F波)之后;在苗进等研究中R波出现频率低, 持续时间从几分钟到几小时不等[20, 22]。本研究R波出现频率较高, 跟随在F波之后, 通常以两种模式跟随F波出现:一是与F波交错出现, 二是保持一条平直的波形缓慢下降到口针拨出;数据比对发现, F波总持续时间长, R波总持续时间普遍也相对较长, 最高可占总测试时间的20%。而且。本研究中还发现“F-R”过渡波形, 由此推测R波也是取食相关的波形, 可在一定程度上能反应茶树抗性情况, 但之前发现R波出现频率低, 没有被重视, 具体的生物学意义没有被明确定义。本研究推测, R波刚发生时假眼小绿叶蝉口针仍位于韧皮部, 是取食受阻时的缓冲休息, 或是长时间受阻取食后缓慢移动口针直至口针离开叶片的过程。金珊等研究假眼小绿叶蝉在人工饲料上的取食行为时, 只观察到E1(A)、E2(E)和E3(C), 说明S、E和F波只能在取食植物时被观察到, 推测S波、F波和R波的产生与植物体内的生化成分密切相关[22]。
3.2 基于EPG技术而评估茶树对叶蝉的抗性本研究以11个茶树良种为目标。龙井43、中茶108、乌牛早和安吉白茶是江浙地区传统制作绿茶的良种, 宁波黄金芽是加工黄茶的良种, 黄观音、金观音、铁观音、黄牡丹和紫牡丹则是福建推广制作乌龙茶的良种, 紫鹃则是云南省制作普洱茶的良种。解析EPG技术记录的刺吸式昆虫取食行为可以获取许多植物抗虫性的信息。本研究采用数个EPG参数为变量、对实体(11个品种)聚类分析, 分为2类:第Ⅰ类包括安吉白茶、乌牛早、紫牡丹、中茶108、黄牡丹和铁观音;第Ⅱ类含有黄观音、龙井43、紫鹃、宁波黄金芽和金观音。分析这2类的各项EPG波形指标, 发现第Ⅰ类的每个品种上叶蝉平均刺探次数、A波和F波平均历期皆显著小于第Ⅱ类的(P<0.05)。第Ⅰ类的E波和NP波平均历期显著大于第Ⅱ类。这两种类型的S波、C波和R波历期之间差异皆未达到显著水平。由于第Ⅰ类刺探次数少、A波、F波和R波平均持续时间短、以及E波平均持续时间长, 说明该类型茶树品种在叶蝉口针刺破叶片表面、达到韧皮部之前及其在韧皮部取食的整个过程所受阻碍少, 为感性品种;第Ⅱ类品种上叶蝉刺探次数多, A波、F波和R波平均持续时间最长, 均显著高于第Ⅰ类, 说明该类型茶树品种在叶蝉口针刺破叶片表面、达到韧皮部之前及其在韧皮部取食的整个过程所受阻碍大, 为抗性品种。其抗性强弱为:第Ⅱ类>第Ⅰ类。
若以E波历期为指标, 再比较每类茶树品种的抗感性:则在第Ⅱ类中发现紫鹃上E波持续时间最短, 抗性最强, 抗性由强到弱排序为紫鹃>龙井43>宁波黄金芽>金观音>黄观音;第Ⅰ类中铁观音和黄牡丹持续时间最长, 更易受叶蝉危害, 感性抗性由强到弱为:铁观音>黄牡丹>乌牛早>安吉白茶>紫牡丹>中茶108。与刘丽芳等[23]认为茶树抗叶蝉取食能力由强至弱为龙井43>中茶108>安吉白茶结果一致。在第Ⅱ类中, 金观音上F波持续时间显著短于其他4个抗性品种上F波, 或许金观音品种可能拥有某类未被鉴定的物质或缺乏叶蝉适口的营养物质, 从而有效地阻抑叶蝉持续取食。而且金观音和黄观音是铁观音与黄旦的人工杂交后代中选育而成的无性系新良种, 抗性、适应性和成活率皆超过双亲[30], 并且金观音和黄观音抗叶蝉性能超过亲本(铁观音、黄旦)。本研究中叶蝉在抗性茶树品种上的Np历期短于感性品种、R波历期也较长, 这与其他研究[20, 22]略有差异, 由于叶蝉在抗性品种上取食过程中E波、A波、F波和R波历期较长, 试验时间5h是固定的, Np历期就短了。
3.3 茶树抗感性与茶叶化学成分的相关性借助于EPG技术快速有效鉴定不同茶树品种抗感性等级, 检测了构成茶叶滋味的4类物质, 期望揭示抗感性与呈味物质之间的相关性。儿茶素类是茶多酚的主要成分, 但具有苦涩味, 占茶叶干重12%—24%。咖啡碱可刺激神经系统产生兴奋、消减疲乏, 占茶叶干重的2%—4%。茶叶可溶性糖类包括单糖和双糖、以及少量三糖等寡聚糖, 具有水溶性, 占干重0.4%—4%。氨基酸具有鲜爽口感, 通常占干重1%—4%。本研究比较了11个茶树品种咖啡碱、儿茶素、可溶性糖和氨基酸的含量差异, 只有儿茶素总量在抗性品种和感性品种之间存在差异, 以抗性品种的儿茶素总量高于感性品种的, 发现儿茶素含量与韧皮部取食波(E波)持续时间呈显著负相关, 与刺探次数和韧皮部取食困难波呈正相关但未达到显著性, 首次将茶树理化成分与EPG指标做关联分析。
前人也较多地探讨茶叶理化成分与抗虫性, 张贻礼等[31]发现虫口密度与咖啡碱含量呈显著负相关, 与氨基酸和茶多酚含量没有显著相关性。邹武等[32]的研究表明, 假眼小绿叶蝉在茶树品种上的种群数量与茶多酚、水溶性糖、儿茶素含量相关关系不明显, 但与咖啡碱含量呈负相关、与游离氨基酸呈正相关。金珊等[33]则发现, γ-氨基丁酸的含量在抗虫品种中普遍高于感虫品种, 而绿原酸和茶多酚则相反, 推测γ-氨基丁酸可能是影响假眼小绿叶蝉取食行为的关键因素。
可见, 关于茶树抗叶蝉性能与茶叶化学成分之间的说法不一致, 还需要进一步求证。EPG技术的推广使用可以快速观察到昆虫在植物上的取食特点, 对植物抗性进行初步定性, 但如果深入解析茶树抗虫性机理, 还需要与切片技术、生化与分子生物学手段和田间观测等相结合, 才能建立比较完善的抗性评价体系。
| [1] | 徐金汉, 王念武, 张灵玲, 关雄. 假眼小绿叶蝉防治指标的研究. 茶叶科学, 2005, 25(2): 131–135. |
| [2] | 庄家祥, 傅建炜, 苏庆泉, 李建宇, 占志雄. 福建省茶小绿叶蝉抗药性的地区差异. 茶叶科学, 2009, 29(2): 154–158. |
| [3] | 曾莉, 玉平盛, 许玫. 茶树对假眼小绿叶蝉的抗性研究. 茶叶科学, 2001, 21(2): 90–93. |
| [4] | 黄亚辉, 张觉晚, 张贻礼, 杨阳, 王沅江. 茶树抗假眼小绿叶蝉的叶片解剖特征. 茶叶科学, 1998, 18(1): 35–38. |
| [5] | Tjallingii W F. Electronic recording of penetration behaviour by aphids. Entomologia Experimentalis et Applicata, 1978, 24(3): 721–730. DOI:10.1111/eea.1978.24.issue-3 |
| [6] | Tjallingii W F. Electrical nature of recorded signals during stylet penetration by aphids. Entomologia Experimentaliset Applicata, 1985, 38(2): 177–186. DOI:10.1111/eea.1985.38.issue-2 |
| [7] | Jiang Y X, Lei H, Collar J L, Martin B, MuñizM, Ferers A. Probing and feeding behavior of two distinct biotypes of Bemisia tabaci (Homoptera:Aleyrodidae) on tomato plants. Journal of Economic Entomology, 1999, 92(2): 357–366. DOI:10.1093/jee/92.2.357 |
| [8] | Kindt F, Joosten N N, Peters D, Tjallingii W F. Characterisation of the feeding behaviour of western flower thrips in terms of electrical penetration graph (EPG)waveforms. Journal of Insect Physiology, 2003, 49(3): 183–191. DOI:10.1016/S0022-1910(02)00255-X |
| [9] | Cline A R, Backus E A. Correlations among AC electronic monitoring waveforms, body postures, and stylet penetration behaviors of Lygus hesperus (Hemiptera:Miridae). Environmental Entomology, 2002, 31(3): 538–549. DOI:10.1603/0046-225X-31.3.538 |
| [10] | Miranda M P, Yamamoto P T, Garcia R B, Lopes J P, Lopes J R. Thiamethoxam and imidacloprid drench applications on sweet orange nursery trees disrupt the feeding and settling behaviour of Diaphorina citri (Hemiptera:Liviidae). Pest Management Science, 2016, 72(9): 1785–1793. DOI:10.1002/ps.2016.72.issue-9 |
| [11] | Zeng X Y, He Y Q, Wu J X, Tang Y M, Gu J T, Ding W, Zhang Y Q. Sublethal effects of cyantraniliprole and imidacloprid on feeding behavior and life table parameters of Myzus persicae (Hemiptera:Aphididae). Journal of Economic Entomology, 2016, 109(4): 1595–1602. DOI:10.1093/jee/tow104 |
| [12] | Cameron R, Hopper L, Alvarez J M. Use of fluorescence to determine reduction in Bemisia tabaci (Hemiptera:Aleyrodidae) nymph feeding when exposed to cyantraniliprole and imidacloprid through systemic applications. Crop Protection, 2016, 84: 21–26. DOI:10.1016/j.cropro.2016.02.003 |
| [13] | Lei W B, Li P, Han Y Q, Gong S L, Yang L, Hou M L. EPG recordings reveal differential feeding behaviors in Sogatella furcifera in response to plant virus Infection and transmission success. Scientific Reports, 2016, 6: 30240. DOI:10.1038/srep30240 |
| [14] | Zhao W W, Wan Y R, Xie W, Xu B Y, Zhang Y J, Wang S L, Wei G S, Zhou X M, Wu Q J. Effect of spinosad resistance on transmission of tomato spotted wilt virus by the western flower thrips (Thysanoptera:Thripidae). Journal of Economic Entomology, 2016, 109(1): 62–69. DOI:10.1093/jee/tov278 |
| [15] | Crane P S. The feeding behavior of the blue-green sharpshooter, Hordnia circellata (Baker) (Homoptera:Cicadellidae). Davis: University of California, 1970. |
| [16] | Triplehorn B W, Nault L R, Horn D J. Feeding behavior of Graminella nigrifrons (Forbes). Annals of the Entomological Society of America, 1984, 77(1): 102–107. DOI:10.1093/aesa/77.1.102 |
| [17] | Kawabe S, McLean D L. Electronically recorded waveforms associated with salivatonand ingestion behavior of the aster leafhopper, Macrosteles fascifrons Stal (Homoptera:Cicadellidae). Applied Entomology and Zoology, 1978, 13(3): 143–148. DOI:10.1303/aez.13.143 |
| [18] | Rapusas H R, Heinrichs E A. Feeding behavior of Nephotettix virescens (Homoptera:Cicadellidae) on rice varieties with different levels of resistance. Environmental Entomology, 1990, 19(3): 594–602. DOI:10.1093/ee/19.3.594 |
| [19] | 苗进, 韩宝瑜. 假眼小绿叶蝉(Empoasca vitis Göthe)在不同品种茶树上的取食行为. 生态学报, 2007, 27(10): 3973–3982. DOI:10.3321/j.issn:1000-0933.2007.10.004 |
| [20] | Miao J, Han B Y, Zhang Q H. Probing behavior of Empoasca vitis (Homoptera:Cicadellidae) on resistant and susceptible cultivars of tea plants. Journal of Insect Science, 2014, 14: 223. |
| [21] | Jin S, Chen Z M, Backus E A, Sun X L, Xiao B. Characterization of EPG waveforms for the tea green leafhopper, Empoasca vitis Göthe (Hemiptera:Cicadellidae), on tea plants and their correlation with stylet activities. Journal of Insect Physiology, 2012, 58(9): 1235–1244. DOI:10.1016/j.jinsphys.2012.06.008 |
| [22] | 金珊, 孙晓玲, 陈宗懋, 肖斌. 不同茶树品种对假眼小绿叶蝉的抗性. 中国农业科学, 2012, 45(2): 255–265. |
| [23] | 刘丽芳, 徐德良, 穆丹, 韩宝瑜. EPG技术分析不同品种茶树抗假眼小绿叶蝉取食行为的差异. 安徽农业大学学报, 2011, 38(2): 281–286. |
| [24] | 中华人民共和国国家质量监督检验检疫总局, 中国国家标准化管理委员会. GB/T 8312-2013茶咖啡碱测定. 北京: 中国标准出版社, 2014. |
| [25] | 唐启义, 冯明光. DPS数据处理系统——实验设计、统计分析及数据挖掘. 北京: 科学出版社, 2007. |
| [26] | Backus E A, Serrano M S, Ranger C M. Mechanisms of hopperburn:an overview of insect taxonomy, behavior, and physiology. Annual Review of Entomology, 2005, 50: 125–151. DOI:10.1146/annurev.ento.49.061802.123310 |
| [27] | Mittler T E. Studies on the feeding and nutrition of tuberolachnus salignus (Gmelin)(Homoptera, Aphididae):Ⅰ. The uptake of Phloem Sap. Journal of Experimental Biology, 1957, 34(3): 334–341. |
| [28] | 雷宏, 徐汝梅. EPG——一种研究植食性刺吸式昆虫刺探行为的有效方法. 昆虫知识, 1996, 33(2): 116–120. |
| [29] | Njihia S N. Cellular Responses of Phaselous Beans to Specific Probing Behaviors of Empoasca kraemeri (Ross & Moore) (Homoptera:Cicadellidae)[D]. USA:University of Missouri-Columbia, 1996. |
| [30] | 郭吉春, 杨如兴, 张文锦, 陈志辉, 陈键. 茶树杂交种金观音与黄观音的选育及应用. 贵州科学, 2008, 26(2): 20–24. |
| [31] | 张贻礼, 张觉晚, 杨阳, 黄亚辉, 王沅江. 茶树抗虫品种资源调查及抗性机制研究——Ⅱ.不同品种茶树特征特性对假眼小绿叶蝉抗性的相关分析. 茶叶通讯, 1994(2): 4–6. |
| [32] | 邹武, 林乃铨, 王庆森. 福建主要茶树品种理化特性与假眼小绿叶蝉种群数量的相关性分析. 华东昆虫学报, 2006, 15(2): 129–134. |
| [33] | 金珊, 孙晓玲, 张新忠, 叶乃兴, 陈宗懋. 8个茶树品种生化成分分析及抗性成分的初步鉴定. 应用昆虫学报, 2016, 53(3): 516–527. DOI:10.7679/j.issn.2095-1353.2016.067 |
 2017, Vol. 37
2017, Vol. 37