文章信息
- 牛素贞, 宋勤飞, 樊卫国, 陈正武
- NIU Suzhen, SONG Qinfei, FAN Weiguo, CHEN Zhengwu.
- 干旱胁迫对喀斯特地区野生茶树幼苗生理特性及根系生长的影响
- Effects of drought stress on leaf physiological characteristics and root growth of the clone seedlings of wild tea plants
- 生态学报. 2017, 37(21): 7333-7341
- Acta Ecologica Sinica. 2017, 37(21): 7333-7341
- http://dx.doi.org/10.5846/stxb201608161674
-
文章历史
- 收稿日期: 2016-08-16
- 网络出版日期: 2017-07-11
2. 贵州大学茶叶工程技术研究中心, 贵阳 550025;
3. 贵州省果树工程技术研究中心, 贵阳 550025;
4. 贵州省茶叶研究所, 贵阳 550025
2. Tea Engineer and Technology Research Center of Guizhou, Guiyang 550025, China;
3. Fruits Engineer and Technology Research Center of Guizhou, Guiyang 550025, China;
4. Guizhou Tea Research Institute, Guiyang 550025, China
中国西南喀斯特地区分布着大量的野生茶树资源[1], 长期以来这些资源被当地人们作为饮料利用。近年来, 野生茶树植物资源在贵州等西南部地区受到重视, 但在喀斯特山区因土壤浅薄、保水能力弱, 生长中局部和临时性干旱频繁[2], 导致野生茶树种质资源的科学开发和利用受到影响。
干旱胁迫条件下, 木本植物的生理反应主要表现在叶片含水量的下降及渗透调节物质的改变以及抗氧化酶活性、光合调节、激素含量的变化等方面[3-5]。研究显示, 茶树对干旱胁迫反应敏感, 干旱条件下, 植株光合作用、气孔特性及叶片抗氧化系统物质均受到不同程度的影响, 使茶树受到伤害[6-7]。郭春芳等[8]通过对铁观音和福鼎大白茶的抗旱性研究得出, 茶树叶片活性氧的产生速率加快, 细胞膜透性增大, MDA含量上升, 铁观音SOD、POD的活性在轻度、中度水分胁迫下上升, 在重度水分胁迫下下降;而福鼎大白茶的保护酶活性和抗氧化剂含量在轻度水分胁迫下上升, 在中度、重度水分胁迫下下降。这与梁建萍等[9]认为生理指标与水分处理之间有很强的相关性的观点一致。由此可知, 茶树干旱胁迫生理与其他木本植物具有一定共性。根系作为植物水分吸收主要器官, 干旱来临时最先感知, 并迅速产生化学信号向上传递以促使气孔关闭, 减少水分散失[10];同时根系还可通过自身形态和生理特征的调整来适应变化后的水分环境[11]。如将根系与叶片生理指标相联系, 能更好地研究植物对干旱胁迫的适应性。为此, 本文立足于贵州喀斯特地区丰富的野生茶树资源, 选取4种野生茶树无性系幼苗通过盆栽控水法设置不同程度的水分处理, 比较这些资源在土壤干旱胁迫下的生理生化特性、根系生长特征和生物量的变化, 并用隶属函数加权平均值进行抗旱性综合评价, 同时通过田间模拟持续干旱试验对其加以验证, 以期为喀斯特地区野生茶树种质资源的保护、利用以及抗旱育种提供理论依据。
1 材料与方法 1.1 材料材料(表 1)来自于贵州喀斯特地区4种野生茶树种质资源。参考陈亮等[12]的分类方法, 4种资源分别为大理茶Camellia taliensis(W. W. Smish)、大厂茶Camellia tachangensis F. C. Zhang、茶Camellia sinensis(L.)-O.Kuntze、秃房茶Camellia gymnogyna Chang。
| 资源Germplasms | 来源Origin | 海拔Altitude/m | 年降雨量 Average annual precipitation/mm |
| 大理茶Camellia taliensis(W. W. Smish) | 黔西南州 | 1616.3 | 1229.2 |
| 大厂茶Camellia tachangensis F. C. Zhang | 黔西南州 | 1755.3 | 1398.7 |
| 茶Camellia sinensis (L.) O. Kuntze | 遵义 | 878.2 | 1079.3 |
| 秃房茶Camellia gymnogyna Chang | 毕节 | 1015.6 | 1038.4 |
水分胁迫设4个水分梯度。CK:对照组(相对含水量为75%±2.5%);T1:轻度胁迫(相对含水量为55%±2.5%);T2:中度胁迫(相对含水量为40%±2.5%);T3:重度胁迫(相对含水量为25%±2.5%)[8], 每个处理5个重复。
试验土壤取自贵州大学茶学试验茶园。黄壤, pH4.53、有效磷6.6 mg/kg、有机质10.68 g/kg、碱解氮22.63 mg/kg、速效钾140 mg/kg、有效铁1.99 mg/kg、交换钙40.51 mg/kg、交换镁21.8 mg/kg、有效锰12.73 mg/kg、有效铜0.19 mg/kg、有效锌0.54 mg/kg、有效硫30 mg/kg。
2011年11月, 选取在贵州大学茶学试验基地长势一致的1年生野生茶树扦插苗, 移栽至黑色塑料桶中, 每桶5株。于露天环境中常规管理。移栽时, 选取重量均为0.88 kg、容积36 L的黑色塑料桶, 向桶内移栽茶苗时共装土26 kg, 并在桶内打孔处用细棉布隔挡, 防止浇水时土壤流失。同时参考齐曼·尤努斯等[13]的方法, 另取一定量的土装入密封袋带回实验室, 检测并计算土壤含水量、土壤相对含水量、饱和水土壤重量。根据土壤含水量、相对含水量、饱和水土壤重量、装湿土重量、桶重以及移栽5棵茶苗的重量计算出每个处理每个重复达到所设定的相对含水量时的桶重。
2012年7月27日, 将材料置于遮雨棚中, 对各桶进行充分灌水使桶内土壤含水量基本达到饱和, 之后不浇水, 让桶内水分自然消耗至所设定的相对水分含量, 于2012年8月1日各处理均达到设定的土壤相对含水量, 此时开始水分胁迫处理。采用每日称重法控水[13], 于每天8:00称桶重并记录(忽略不同盆间生物量的变化), 根据各处理达到相对含水量时计算出的桶重减去当天所称桶重, 得出每天蒸发失水重量, 进行补水, 使土壤含水量控制在设定的范围内。其他管理按常规进行。于2012年9月15日取样进行生理指标的测定, 2012年10月1日进行生长指标的测定。
1.3 测定方法 1.3.1 生理生化指标随机采集足够量的茶树幼苗上第4—5片成熟叶(幼苗中部), 立即测定叶片相对含水量、相对电导率、丙二醛(MDA)、脯氨酸(Pro)、可溶性糖含量以及SOD、POD活性。叶片相对含水量、相对电导率和MDA含量参考陈文荣等[14]的方法;可溶性糖含量参考刘立军等[15]方法;SOD活性和POD活性参考史小玲等[16]的方法;根系活力参考齐曼·尤努斯等[13]的方法。每个材料重复3次。
1.3.2 生长指标生物量及根系指标参考何跃军和钟章成[17]的方法:处理结束后, 浇透水, 破桶后取出完整植株, 用流水小心冲洗根系, 待冲洗干净后, 从基部第一侧根处截取根系, 用EPSON4990扫描仪记录根系形态, 然后用Epson Express1000XL1.0分析根系总表面积、根系总体积、根系平均直径及根系总长。扫描完成后, 将各处理根系及地上部分在105℃杀青30 min, 然后在80℃下烘48 h, 称量根系生物量干重和地上部分生物量干重, 计算总生物量干重和根冠比。
1.4 抗旱性的隶属函数分析隶属函数计算方法:与抗逆性呈正相关的参数叶片相对含水量、SOD活性、POD活性、脯氨酸含量、可溶性糖含量、根冠比、根系活力和比叶面积采用公式:Uij=(Xij-Xjmin)/(Xjmax-Xjmin), 与抗逆性呈负相关的参数电导率、MDA含量采用公式:Uij=1-(Xij-Xjmin)/(Xjmax-Xjmin)[18-19]。式中Uij表示i种类j指标的抗旱隶属函数值;Xij表示i种类j指标的测定值;Xjmin表示所有种类j指标的最小值;Xjmax表示所有种类j指标的最大值;i表示某个品种;j表示某项指标。
权重应用客观赋权法进行计算:Ij=Cj/Sj, 其中, Ij是一个无量纲数, 表示某评价指标在干旱胁迫下的测定值相对于对照组的比值。Cj是第j个指标对照组的测定值, Sj表示第j个指标在某个胁迫处理下所测定的平均值。如果是负相关, 则计算式为Ij=Sj/Cj。最后通过归一化, 计算出每个评价指标的权重:Wj=Ij/∑Ij[20]。综合评价值:D=(Uij×Wj), D值越大, 抗旱性越强;反之越弱。
1.5 田间模拟干旱试验 1.5.1 田间模拟干旱试验设计选取位于贵州大学试验茶园作为试验地。于2011年11月将上述4种野生茶树1年生的扦插苗(苗高约15 cm)按随机区组设计进行宽窄双行种植, 株行距为1.5 m×0.3 m×0.3 m, 每小区种植20株, 每个种设置3个重复, 正常除草施肥, 待根系长稳后, 于2012年3月进行遮雨处理, 当土壤含水量低于25%田间持水量时进行补水至25%—35%之间, 共补水8次。于2012年11月统计植株死亡率、株高增长量等指标。于2013年11月重复2011年移栽试验, 并在2014年3月重复进行2012年遮雨处理试验。
1.5.2 土壤含水量测定及补水量计算方法土壤含水量测定及补水量计算参考霍治国等[21]的方法:采用TZS-1K土壤水分测定仪测定土壤含水量, 测定深度为0—60 cm。测定土层厚度间距为10 cm;测定时间是在水分控制时段内每7 d测定1次。
补水量计算:
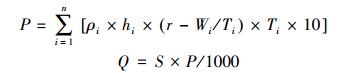
|
式中, P为补水量(mm);可折算成立方米进行补灌。ρ为试验基地地段实测土壤容重(g/cm3);h为测定土层厚度(cm);r是2个土壤水分处理等级, 分别为25%、35%;W为土壤重量含水率(%);T为试验基地地段实测田间持水量(%);n为土壤补水量计算层数, n=6;Q为小区灌溉需水量(mm);S为小区面积(m2)。
2 结果与分析 2.1 干旱胁迫对野生茶树幼苗叶片生理的影响随着水分胁迫程度的加强, 4种野生茶树叶片的相对含水量也逐渐降低。在轻度、中度和重度干旱胁迫条件(相对含水量分别为田间持水量的55%、40%和25%)下, 4种野生茶树幼苗的叶片相对含水量与对照组相比均显著下降(P < 0.05)。在重度干旱胁迫下, 4种野生茶树幼苗叶片含水量的差异进一步扩大, 秃房茶叶片相对含水量最高, 大理茶的叶片相对含水量最低, 分别为76.3%、55.1% (表 2)。随着水分胁迫程度的加强, 4种野生茶树幼苗叶片细胞质膜透性和MDA含量均呈显著上升趋势(P < 0.05) (表 2), 大理茶和茶的细胞质膜透性和MDA含量增加幅度较大, 说明其膜系统伤害较大;秃房茶和大厂茶细胞质膜透性和MDA含量增加幅度较小, 说明其膜系统伤害较小。
| 资源 Germplasm | 处理 Treatment | 叶片相对含水量 Relative water content/% | 电导率Relative conductivity/% | MDA含量 MDA content/ (μmol/kg) | 脯氨酸含量 Content of proline/(μg/g) | 可溶性糖含量 Content of soluble sugars/(mg/g) | SOD activity /(U/g) | POD activity/ (U g-1 min-1) |
| 大理茶 | CK | 93.02±0.98b | 7.82±0.09j | 5.35±0.10j | 68.91±1.39h | 5.28±0.03k | 378.56±0.47j | 20.73±0.34h |
| Camellia taliensis | T1 | 81.26±0.94e | 28.19±0.61e | 25.87±0.65e | 106.19±0.67c | 6.27±0.03i | 415.53±2.28de | 36.72±0.92g |
| (W. W. Smish) | T2 | 63.07±0.76i | 39.06±0.50c | 42.14±0.92c | 99.12±1.30de | 7.48±0.10g | 395.93±3.36i | 17.44±0.35i |
| T3 | 55.08±0.68j | 75.09±0.63a | 73.03±1.17a | 72.59±0.59g | 14.06±0.07a | 368.37±0.55k | 14.03±0.29j | |
| 大厂茶 | CK | 95.97±0.59a | 14.43±0.56i | 10.01±0.60i | 63.19±0.50i | 5.91±0.19j | 408.44±2.68fg | 38.02±0.51g |
| Camellia tachangensis | T1 | 85.67±0.39d | 20.37±0.49h | 12.46±0.08h | 108.72±0.81c | 6.67±0.03h | 417.37±3.23cd | 66.53±0.31e |
| F. C. Zhang | T2 | 79.70±0.76e | 25.22±0.50f | 15.89±0.13g | 136.08±2.59a | 7.52±0.08g | 429.84±1.90b | 80.57±1.00cd |
| T3 | 74.26±0.58fg | 40.98±0.67c | 27.72±0.72e | 102.2±1.66d | 12.64±0.11c | 405.37±1.59gh | 51.73±0.27f | |
| 茶 | CK | 92.76±1.04b | 15.24±0.41i | 8.92±0.38i | 62.35±0.78i | 6.25±0.06ij | 412.10±1.90ef | 81.15±0.94cd |
| Camellia sinensis (L.) | T1 | 85.19±0.66d | 22.43±0.51g | 15.49±0.27g | 73.07±0.74g | 7.51±0.08g | 425.40±0.84b | 101.56±1.83b |
| -O. Kuntze | T2 | 72.02±0.57g | 40.91±0.67c | 31.50±0.96d | 96.15±0.54ef | 8.75±0.06e | 420.39±1.08c | 127.02±0.56a |
| T3 | 69.30±1.19h | 54.55±0.96b | 62.80±0.88b | 74.85±1.45g | 13.13±0.09b | 381.02±2.73j | 99.15±1.30b | |
| 秃房茶 | CK | 96.15±0.54a | 7.97±0.17j | 5.14±0.15j | 49.76±0.28j | 5.99±0.07i | 392.38±1.22i | 37.52±0.59g |
| Camellia gymnogyna | T1 | 88.53±1.17c | 13.58±0.75i | 12.95±0.43h | 95.28±0.86f | 8.46±0.10f | 428.33±1.73b | 63.72±0.83 |
| Chang | T2 | 81.57±0.97e | 18.98±0.33h | 18.57±0.42f | 120.21±1.77b | 9.01±0.07e | 435.50±1.27a | 79.59±1.31d |
| T3 | 76.30±0.71f | 32.78±0.84d | 32.79±0.85d | 95.57±0.74ef | 11.03±0.11d | 401.59±2.01h | 82.95±0.58c | |
| 同列相同字母者表示无显著差异 | ||||||||
随着干旱胁迫程度的加重, 4种野生茶树幼苗叶片的游离脯氨酸含量存在先升后降的趋势, 且均显著高于对照(P < 0.05)。茶、大厂茶和秃房茶游离脯氨酸含量在中度胁迫下达到最大值, 大理茶游离脯氨酸含量在轻度胁迫下达到最大值。在轻度、中度、重度胁迫下, 大理茶游离脯氨酸含量分别是对照的1.54、1.44、1.05倍, 大厂茶分别是对照的1.72、2.15、1.62倍, 茶分别是对照的1.17、1.54、1.20倍, 秃房茶分别是对照的1.91、2.42、1.92倍。在重度干旱胁迫下种间的游离脯氨酸含量差异达显著水平(P < 0.05)。
可溶性糖含量随着干早胁迫程度的加强呈上升趋势, 均显著大于对照(P < 0.05)。在轻度、中度和重度干早胁迫下, 大理茶叶片可溶性糖含量分别是对照的1.19、1.42、2.66倍, 大厂茶分别是对照的1.13、1.27、2.14倍, 茶分别是对照的1.20、1.40、2.10倍, 秃房茶分别是对照的1.41、1.51、1.84倍。在轻度、中度干旱胁迫下4种野生茶树幼苗可溶性糖含量增幅均较小, 在重度干旱胁迫下, 除秃房茶外, 其他3个种可溶性糖含量增幅较大, 均是对照的2倍以上。
SOD活性随着干旱胁迫程度的加重呈先升后降趋势;大理茶和茶SOD活性的峰值出现在轻度胁迫下, 分别比对照增加了5.24%和9.77%;大厂茶和秃房茶SOD活性的峰值出现在中度胁迫下, 分别比对照增加了3.23%和10.99%;其后随着胁迫程度的加重, SOD活性降低, 在重度胁迫下仅秃房茶SOD活性显著高于对照外, 其他3个种SOD活性显著低于对照。说明一定程度干旱胁迫可诱导茶树叶片SOD活性增强, 有效清除氧自由基, 阻止膜的过氧化;但当超过一定胁迫强度后, SOD活性降低并导致氧自由基积累, 膜的完整性遭到破坏;并且不同的茶树种类, 在同一水平干旱胁迫下的受害程度存在显著差异(P < 0.05)。
与对照相比, 除秃房茶POD活性随胁迫程度的加大呈上升趋势外, 其他野生茶树幼苗叶片中POD活性均为先升高后降低趋势。大理茶POD活性的变化幅度较小, 其峰值出现在轻度胁迫下, 比对照增加了77.15%, 差异显著(P < 0.05), 在中度和重度胁迫下大理茶POD活性显著低于对照(P < 0.05);大厂茶和茶POD活性在中度胁迫下最高, 显著高于对照(P < 0.05), 分别是对照的2.12、1.57倍, 在重度胁迫下大厂茶和茶POD活性开始下降, 但仍显著高于对照(P < 0.05)。4种野生茶树幼苗叶片POD活性变化显示, 茶最高, 大理茶最低。
2.2 水分胁迫对野生茶幼苗生物量和根系指标的影响表 3结果表明, 大理茶对照组生物量显著高于其他3个种, 在轻度、中度和重度水分胁迫下, 大理茶干物质积累量分别比对照降低了24.69%、36.33%、51.61%;随着干旱胁迫的加强, 大理茶根系总表面积、根系总体积、根系总长和根系活力呈显著下降趋势;比叶面积在轻度干旱胁迫下的变化差异不显著, 在中度和重度干旱胁迫下显著低于对照;根系平均直径均显著高于对照, 根冠比与对照的差异不显著。表明轻度、中度和重度干旱胁迫均阻碍了大理茶的地上部分和地下部分正常生长。
| 资源 Germplasms | 处理 Treatments | 总生物量干重 Total dry biomass/g | 比叶面积 Specific leaf area/ (cm2/g) | 根冠比 Root-shoot ratio | 根系总表面积 Root total surface area/cm2 | 根系总体积 Root total volume/cm3 | 根系平均直径 Average diameter/mm | 根系总长 Root total surface length/cm | 根系活力 Root activity/ (mg g-1 h-1) |
| 大理茶 | CK | 12.11±0.03a | 238.37±3.24de | 0.53±0.02bc | 355.50±2.03a | 6.41±0.06a | 0.73±0.01g | 1553.98±6.23a | 5.45±0.02f |
| Camellia taliensis | T1 | 9.12±0.04d | 250.96±3.03cd | 0.54±0.02b | 273.73±1.56c | 5.20±0.05c | 0.76±0.01f | 1147.94±5.23b | 5.23±0.02g |
| (W. W. Smish) | T2 | 7.71±0.07e | 184.63±4.23f | 0.54±0.02b | 238.73±1.45c | 4.60±0.02e | 0.76±0.01f | 1098.16±1.89c | 4.15±0.06j |
| T3 | 5.86±0.03g | 180.71±3.46f | 0.53±0.01bc | 134.82±1.67h | 2.53±0.03j | 0.78±0.01f | 557.24±2.12g | 3.66±0.01l | |
| 大厂茶 | CK | 4.21±0.01i | 273.16±8.17bc | 0.45±0.01f | 107.86±1.81i | 2.27±0.03k | 0.84±0.01d | 403.32±1.98i | 6.24±0.03c |
| Camellia tachangensis | T1 | 3.21±0.02j | 251.89±2.37cd | 0.68±0.02a | 133.95±2.57h | 2.5±0.01j | 0.89±0.01c | 413.44±2.18h | 6.78±0.02a |
| F. C. Zhang | T2 | 2.93±0.01jk | 236.11±1.73de | 0.56±0.01b | 63.07±0.62j | 1.06±0.03l | 0.94±0.01b | 305.±1.23j | 6.69±0.04a |
| T3 | 2.50±0.01k | 231.15±3.42de | 0.45±0.01f | 38.77±0.98k | 0.93±0.03m | 0.66±0.00h | 134.77±0.15k | 4.29±0.01i | |
| 茶Camellia sinensis | CK | 11.32±0.04b | 173.86±5.74f | 0.26±0.00h | 294.04±1.15b | 5.75±0.09b | 0.78±0.01f | 895.66±3.12d | 6.08±0.01d |
| (L.)-O. Kuntze | T1 | 9.23±0.01d | 216.12±6.31e | 0.36±0.01g | 169.14±1.71f | 4.11±0.01f | 0.85±0.02d | 596.71±1.13f | 6.37±0.03b |
| T2 | 6.27±0.03fg | 224.28±9.81de | 0.25±0.01h | 156.81±1.70g | 3.92±0.07g | 0.91±0.02c | 598.06±1.56f | 5.71±0.02e | |
| T3 | 5.12±0.04h | 212.67±1.23e | 0.24±0.00h | 143.08±1.37h | 3.37±0.07i | 1.04±0.02a | 402.46±1.67i | 4.03±0.02k | |
| 秃房茶 | CK | 10.25±0.05c | 117.82±7.26g | 0.46±0.01ef | 173.72±1.95f | 3.74±0.09h | 0.81±0.01e | 816.5±3.34e | 5.26±0.01g |
| Camellia gymnogyna | T1 | 10.14±0.06c | 281.13±6.78b | 0.49±0.01de | 244.32±2.24d | 5.06±0.02d | 0.78±0.01f | 1024.51±2.34c | 6.13±0.01c |
| Chang | T2 | 9.83±0.03cd | 309.33±1.68a | 0.50±0.02cd | 204.73±2.70e | 4.18±0.09f | 0.73±0.01g | 1137.66±3.67b | 6.71±0.02a |
| T3 | 6.71±0.03f | 267.69±9.37bc | 0.48±0.01def | 180.41±1.01f | 3.86±0.04g | 0.71±0.00g | 913.95±5.76d | 4.73±0.03h | |
| 同列相同字母者表示无显著差异 | |||||||||
大厂茶对照组总生物量显著低于其他3个种, 在轻度、中度和重度胁迫下, 大厂茶分别比对照降低了23.75%、30.40%、40.62%;在轻度胁迫下, 大厂茶根冠比、根系总长、根系平均直径、根系总体积以及根系活力均显著高于对照, 表明大厂茶对轻度干旱胁迫有较强的适应性, 并通过优先满足根系生长和增加根系活力适应干旱胁迫;在中度胁迫下大厂茶根冠比、根系平均直径和根系活力显著高于对照, 表明在中度胁迫下也可以通过加快根系物质的运输, 从而保持一定的根系吸水能力, 缓解干旱伤害;重度胁迫下, 大厂茶根冠比、根系活力、比叶面积及根系形态指标均显著低于对照, 严重受害。
在轻度、中度和重度胁迫下, 茶生物量分别比对照降低了18.46%、44.61%、54.77%;在轻度胁迫下茶的比叶面积、根冠比、根系平均直径和根系活力显著高于对照;中度和重度干旱胁迫下比叶面积显著高于对照, 总生物量干重、根系各指标均显著低于对照。
在轻度、中度和重度水分胁迫下, 秃房茶总生物量干重分别比对照降低了1.07%、4.09%、34.54%;在轻度和中度胁迫下, 干物质积累量均与对照差异不显著, 比叶面积、根系总表面积、根系总体积、根系总长和根系活力显著高于对照, 根系平均直径显著低于对照;在重度胁迫下比叶面积、根系总体积、根系总长显著高于对照, 根系平均直径和根系活力显著低于对照, 根冠比和根系总表面积与对照差异不显著, 表明秃房茶在轻度、中度干旱胁迫下均能通过根系形态的变化保持较高的根系吸水能力, 保证在干旱状态下的正常生长。在重度干旱胁迫下可以通过比叶面积、根系总体积、根系总长的增加保持一定的根系吸水能力, 减少伤害。
2.3 野生茶树幼苗抗旱性的综合评价以10个指标的隶属函数加权平均值对4种野生茶树种质资源抗旱性进行综合评价(表 4)。从权重Wj方面测算出的与野生茶树抗旱性最为密切的2个指标依次为:MDA、电导率(平均权重均大于0.1)。抗旱性顺序分别为秃房茶>大厂茶>茶>大理茶。其中, 4种野生茶树种质资源中秃房茶的隶属函数加权平均值为0.936, 为具有强抗旱特性的野生茶树种质资源;其次是大厂茶, 其隶属函数值为0.801, 属于较强抗旱的野生茶树种质资源;大理茶的隶属函数加权平均值仅为0.032, 为耐旱性最差的材料。
| 资源 Germplasm | 指标Index | 相对含 水量 Relative water content | 电导率 Relative conductivity | MDA | 脯氨酸 Contenst of proline | 可溶性糖 Contents of soluble sugar | SOD | POD | 比叶面积 Specific leaf area | 根冠比 Root- shoot ratio | 根系活力 Root activity | 综合 评价值 Compre- hensive value |
| 大理茶 | 隶属函数值(Uij) | 0.000 | 0.000 | 0.000 | 0.000 | 0.000 | 0.000 | 0.000 | 0.000 | 1.000 | 0.000 | 0.032 |
| Camellia taliensis (W. W. Smish) | 权重(Wj) | 0.056 | 0.316 | 0.449 | 0.035 | 0.088 | 0.034 | 0.022 | 0.024 | 0.032 | 0.022 | |
| 大厂茶 | 隶属函数值Uij) | 0.904 | 0.806 | 1.000 | 1.007 | 0.025 | 1.010 | 0.443 | 0.580 | 0.724 | 0.589 | 0.801 |
| Camellia tachangensis F. C. Zhang | 权重(Wj) | 0.099 | 0.218 | 0.213 | 0.124 | 0.164 | 0.077 | 0.104 | 0.069 | 0.082 | 0.056 | |
| 茶Camellia sinensis | 隶属函数值Uij) | 0.670 | 0.485 | 0.226 | 0.077 | 0.831 | 0.345 | 1.000 | 0.367 | 0.000 | 0.346 | 0.365 |
| (L.)-O. Kuntze | 权重(Wj) | 0.076 | 0.204 | 0.401 | 0.068 | 0.120 | 0.062 | 0.070 | 0.068 | 0.051 | 0.037 | |
| 秃房茶 | 隶属函数值Uij) | 1.000 | 1.000 | 0.888 | 0.781 | 1.000 | 0.907 | 0.810 | 1.000 | 0.828 | 1.000 | 0.936 |
| Camellia gymnogyna Chang | 权重(Wj) | 0.067 | 0.220 | 0.341 | 0.103 | 0.099 | 0.052 | 0.118 | 0.123 | 0.057 | 0.049 |
两年的田间持续干旱试验结果表明, 干旱对4种野生茶树幼苗均有不同程度的伤害(表 5)。秃房茶的伤害程度最小, 死亡率最低, 株高净增量显著高于其他种;其次是大厂茶和茶, 其旱死率较低。干旱对大理茶伤害最大, 2012年旱死率为59.17%±6.09%, 2014年旱死率为55.00%±1.53%, 株高净增量均小于4 cm。田间模拟持续干旱试验结果与各指标综合评价结果(表 4)基本一致, 进一步印证了4种野生茶树种质资源抗旱性是秃房茶>大厂茶>茶>大理茶。
| 资源Germplasm 试验时间Trial time | 旱死率Death rate of drougth/% | 株高净增量Rise of plant height/cm | ||
| 2012年 | 2014年 | 2012年 | 2014年 | |
| 大理茶Camellia taliensis (W. W. Smish) | 59.17±6.09a | 55.00±1.53a | 3.00±0.08d | 1.67±0.33c |
| 大厂茶Camellia tachangensis F. C. Zhang | 28.27±2.13c | 26.67±1.76b | 5.47±0.18b | 5.33±0.67b |
| 茶Camellia sinensis (L.) -O. Kuntze | 36.01±1.45b | 29.17±1.20b | 4.17±0.33c | 4.01±0.58b |
| 秃房茶Camellia gymnogyna Chang | 11.43±1.05d | 14.17±1.21c | 11.10±0.54a | 9.67±0.88a |
| 同列相同字母者表示无显著差异 | ||||
在干旱条件下, 植株的叶片持水力越强, 细胞膜受到的伤害程度越小, 抗旱性越强[22-23]。本研究中4种野生茶树幼苗的相对含水量随干旱胁迫程度的加强而逐渐降低, 在中度和重度干旱胁迫下秃房茶和大厂茶细胞膜受害较小, 大理茶和茶细胞膜受害较大。细胞膜受到伤害后, 会引起膜上激发能的上升而发生能量过剩, 产生过量的活性氧, 若不及时清除会造成氧化胁迫, 引起膜脂过氧化产物(MDA)和质膜透性增加, 导致膜系统受到破坏[24]。随着叶片相对含水量下降, 细胞膜受损产生活性氧的同时, 植物细胞也会启动清除活性氧的保护酶系统[25]。SOD、POD是活性氧防御系统的关键酶, 担负着清除自由基的重要功能, 避免膜伤害[26]。干旱条件下, 酶活性越高, 植物的抗旱性越强[11, 27]。同时植物还会通过积累一些可溶性物质进行渗透调节适应干旱胁迫[28]。可溶性糖和游离脯氨酸是植物体内重要的渗透调节物质[10], 当植物遭受干旱胁迫时, 植物细胞通过脯氨酸和可溶性糖的积累进行渗透调节, 从而阻止细胞膜解离, 增强细胞保水能力, 稳定细胞结构, 防止细胞脱水[29]。本研究结果显示, 随着干旱胁迫程度的加强, 4种野生茶树幼苗叶片质膜透性、MDA含量和可溶性糖含量逐渐升高, 脯氨酸含量、SOD活性先升后降, POD活性除秃房茶逐渐显著升高外, 其他3个种先升高后降。说明4种野生茶树均诱导启动了渗透调节机制和保护酶系统适应干旱胁迫。但是随着干旱胁迫程度的加强, 渗透调节机制和保护酶系统逐渐会受到抑制。秃房茶、大厂茶的质膜透性和MDA含量提高的幅度较小, 在中度干旱胁迫下均达到最大值, 随后降低。大理茶和茶的质膜透性和MDA含量提高的幅度较大, 在轻度干旱胁迫下达到最大值, 随后逐渐降低。表明大理茶和茶对干旱胁迫敏感, 秃房茶和大厂茶对干旱胁迫不敏感, 尤其是秃房茶, 其POD活性随着胁迫程度的加强而逐渐增加, 在重度干旱胁迫下POD的活性没有受到抑制, 说明适应干旱胁迫能力比其他三个种强。
3.2 干旱胁迫对根系指标、比叶面积及总生物量的影响根系是植物吸收水分的主要器官, 干旱来临时最先感知, 并通过自身形态特征的调整来适应变化后的水分环境[30];而根、冠关系是植物受遗传和环境因素表现出的互作综合效应。Magnani等[31]指出, 当根、冠结构与功能处于均衡状态时, 二者生长比例协调, 资源利用效率较高。本研究表明, 干旱胁迫抑制了野生茶树幼苗的干物质积累和根系生长, 但4个种表现出明显的差异。其中, 大理茶的地上部分和根系生长均受到显著抑制, 在轻度干旱时的抗旱调节能力较弱, 干旱极易对其造成危害。大厂茶在轻度胁迫下, 通过增加根系形态指标、地下部分物质的量的运输以及根系活力来适应土壤水分的降低, 在中度胁迫下是通过显著增加根系平均直径、根系活力来补偿根系吸收面积的减小, 从而保持一定量的根系吸水能力, 缓解干旱对生长的抑制。茶仅在轻度胁迫下通过增加根系平均直径和根系活力的途径缓解干旱带来的伤害, 对中度和重度水分胁迫应对能力较差, 以致于生长受到严重抑制。秃房茶在轻度、中度干旱胁迫下均能通过根系形态的变化维持较高的根系吸水能力, 保证在干旱状态下的正常生长。在重度干旱胁迫下通过根系形态的变化保持一定的根系吸水能力, 从而避免地上部生长过度受抑, 减轻干旱的危害。
表明秃房茶在轻度、中度干旱胁迫下均能通过根系形态的变化保持较高的根系吸水能力, 保证在干旱状态下的正常生长。在重度干旱胁迫下可以通过比叶面积、根系总体积、根系总长的增加保持一定的根系吸水能力, 减少伤害。
3.3 野生茶树幼苗的抗旱性综合评价Michael[32]、Pucholt[33]的研究认为树木抗旱性是受复杂的多种因素综合的影响, 是通过多个途径来实现, 目前尚未有一个合适的、统一的评价方法[34]。对于农作物的抗旱评价, 应用较多的有抗旱系数、伤害指数和敏感指数[34-35], 但这些方法均以产量性状为主, 须收获后才能进行评价, 而茶树作为木本植物, 测定成龄茶园产量周期较长, 以上方法不宜应用于这类多年生木本植物的筛选。因此本研究中选用苗期作为试验材料, 相对于其他生长周期, 苗期鉴定耐旱性具有时间短、可重复性强等优点[10]。本研究中, 4种野生茶树幼苗叶片的几个指标间变化趋势呈现出不一致性, 可见, 仅从单一因素来评价植物的抗旱性, 存在一定程度的局限性。而隶属函数分析可以在一定程度上提高鉴定的准确性[23, 36]。考虑到干旱胁迫对各个指标的影响程度存在差异, 本研究中选用了客观赋权法来评价各指标的权重并通过隶属函数结合权重计算出综合抗旱值。结果显示4种野生茶树幼苗抗旱性的综合评价结果与田间持续干旱试验结果是一致的, 可见, 基于生理指标的隶属函数评价方法使得评价结果更为全面, 具有较好的可靠性及应用价值。
综上所述:4种野生茶树幼苗的抗旱性差异较大, 抗旱顺序是秃房茶>大厂茶>茶>大理茶。基于生长生理指标的隶属函数评价植物抗旱性的方法准确可行。干旱胁迫降低了野生茶树幼苗总生物量干重, 耐旱性的秃房茶可以通过诱导增加渗透调节物质、启动保护酶系统、提高根系活力、保持较高的根系生长量来保持较高的根系吸水能力, 进而维持较高的叶片含水量和比叶面积, 来保证茶树的正常生长, 缓解干旱对生长的抑制。
| [1] | 庄晚芳. 茶树原产于我国何地. 浙江大学学报:农业与生命科学版, 1981, 7(3): 111–115. |
| [2] | 杨瑞, 莫红林, 李光容, 喻理飞, 戴全厚. 贵州喀斯特高原区几种灌木对土壤水分和物理性质的影响. 中南林业科技大学学报, 2015, 35(4): 78–82. |
| [3] | Liu C C, Liu Y G, Guo K, Fan D Y, Li G Q, Zheng Y R, Yu L F, Yang R. Effect of drought on pigments, osmotic adjustment and antioxidant enzymes in six woody plant species in Karst habitats of southwestern China. Environmental and Experimental Botany, 2011, 71(2): 174–183. DOI:10.1016/j.envexpbot.2010.11.012 |
| [4] | Habermann G, Ellsworth P F V, Cazotoc J L, Simão E, Bieras A C. Comparative gas exchange performance during the wet season of three Brazilian Styrax species under habitat conditions of cerrado vegetation types differing in soil water availability and crown density. Flora-Morphology, Distribution, Functional Ecology of Plants, 2011, 206(4): 351–359. DOI:10.1016/j.flora.2010.05.009 |
| [5] | Muthusamy M, Uma S, Backiyarani S, Saraswathi M S. Genome-wide screening for novel, drought stress-responsive long non-coding RNAs in drought-stressed leaf transcriptome of drought-tolerant and-susceptible banana (Musa spp) cultivars using Illumina high-throughput sequencing. Plant Biotechnology Reports, 2015, 9(5): 279–286. DOI:10.1007/s11816-015-0363-6 |
| [6] | Netto L A, Jayaram K M, Puthur J T. Clonal variation of tea [Camellia sinensis (L.)O. Kuntze] in countering water deficiency. Physiology and Molecular Biology of Plants, 2010, 16(4): 359–367. DOI:10.1007/s12298-010-0040-8 |
| [7] | 牛素贞, 樊卫国. 喀斯特地区古茶树幼苗对干旱胁迫的生理响应及其抗旱性综合评价. 园艺学报, 2013, 40(8): 1541–1552. |
| [8] | 郭春芳, 孙云, 张木清. 不同土壤水分对茶树光合作用与水分利用效率的影响. 福建林学院学报, 2008, 28(4): 333–337. |
| [9] | 梁建萍, 贾小云, 刘亚令, 吴云, 周然, 冯前进. 干旱胁迫对蒙古黄芪生长及根部次生代谢物含量的影响. 生态学报, 2016, 36(14): 4415–4422. |
| [10] | 吴敏, 张文辉, 周建云, 马闯, 韩文娟. 干旱胁迫对栓皮栎幼苗细根的生长与生理生化指标的影响. 生态学报, 2014, 34(15): 4223–4233. |
| [11] | 丁红, 张智猛, 戴良香, 慈敦伟, 秦斐斐, 宋文武, 刘孟娟, 付晓. 水分胁迫和氮肥对花生根系形态发育及叶片生理活性的影响. 应用生态学报, 2015, 26(2): 450–456. |
| [12] | 陈亮, 虞富莲, 杨亚军. 茶树种质资源与遗传改良. 北京: 中国农业科学技术出版社, 2006: 28–35. |
| [13] | 齐曼·尤努斯, 木合塔尔·扎热, 塔衣尔·艾合买提. 干旱胁迫下尖果沙枣幼苗的根系活力和光合特性. 应用生态学报, 2011, 22(7): 1789–1795. |
| [14] | 陈文荣, 曾玮玮, 李云霞, 李永强, 郭卫东. 高丛蓝莓对干旱胁迫的生理响应及其抗旱性综合评价. 园艺学报, 2012, 39(4): 637–646. |
| [15] | 刘立军, 陈为峰, 王凯, 张呈祥. 不同灌水量下限对高羊茅绿期及抗寒性生理指标的影响. 应用生态学报, 2012, 23(1): 38–44. |
| [16] | 史小玲, 薛立, 任向荣, 冯慧芳, 郑卫国, 傅静丹. 华南地区4种阔叶幼苗水分胁迫条件下的抗旱性初探. 林业科学研究, 2011, 24(6): 760–767. |
| [17] | 何跃军, 钟章成. 水分胁迫和接种丛枝菌根对香樟幼苗根系形态特征的影响. 西南大学学报:自然科学版, 2012, 34(4): 33–39. |
| [18] | 徐莲珍. 三个树种抗旱生理生态特性的研究[D]. 杨凌: 西北农林科技大学, 2008. http://d.wanfangdata.com.cn/Thesis/Y1284904 |
| [19] | 田青. 内蒙古典型草原植物性状对模拟降雨的响应及其对生态系统功能的影响[D]. 兰州: 甘肃农业大学, 2009. http://cdmd.cnki.com.cn/Article/CDMD-10733-2009253244.htm |
| [20] | 程启月. 评测指标权重确定的结构熵权法. 系统工程理论与实践, 2010, 30(7): 1225–1228. DOI:10.12011/1000-6788(2010)7-1225 |
| [21] | 霍治国, 白月明, 温民, 陈林, 胡延龙, 叶彩玲. 水分胁迫效应对冬小麦生长发育影响的试验研究. 生态学报, 2001, 21(9): 1527–1535. |
| [22] | Liu B H, Li M J, Cheng L, Liang D, Zou Y J, Ma F W. Influence of rootstock on antioxidant system in leaves and roots of young apple trees in response to drought stress. Plant Growth Regulation, 2012, 67(3): 247–256. DOI:10.1007/s10725-012-9683-5 |
| [23] | 刘登望, 王建国, 李林, 谭红姣, 马杰, 卢山. 不同花生品种对旱涝胁迫的响应及生理机制. 生态学报, 2015, 35(11): 3817–3824. |
| [24] | 周珩, 郭世荣, 邵慧娟, 陈新斌, 魏摇斌, 胡摇荣, 姜冬晨, 郑智航, 孙摇锦. 渗NaCl和Ca(NO3)2胁迫对黄瓜幼苗生长和生理特性的影响. 生态学报, 2014, 34(7): 1880–1890. |
| [25] | 刘声传, 陈亮. 茶树耐旱机理及抗旱节水研究进展. 茶叶科学, 2014, 34(2): 111–121. |
| [26] | 张仁和, 郑友军, 马国胜, 张兴华, 路海东, 史俊通, 薛吉全. 干旱胁迫对玉米苗期叶片光合作用和保护酶的影响. 生态学报, 2014, 31(5): 1303–1311. |
| [27] | 刘声传. 茶树对干旱胁迫和复水响应的生理、分子机理[D]. 杭州: 中国农业科学院茶叶研究所, 2015. http://cdmd.cnki.com.cn/Article/CDMD-82101-1015378863.htm |
| [28] | 谢小玉, 马仲炼, 白鹏, 刘晓健. 辣椒开花结果期对干旱胁迫的形态与生理响应. 生态学报, 2014, 34(13): 3797–3805. |
| [29] | 刘承, 李佐同, 杨克军, 徐晶宇, 王玉凤, 赵长江, 张翼飞, 李竹, 孙少慧, 富士江, 赵莹, 谷英楠, 付健, 方永江, 刘瑀, 张发明, 马丽峰, 石新新. 水分胁迫及复水对不同耐旱性玉米生理特性的影响. 植物生理学报, 2015, 51(5): 702–708. |
| [30] | 杨再强, 邱译萱, 刘朝霞, 陈艳秋, 谭文. 土壤水分胁迫对设施番茄根系及地上部生长的影响. 生态学报, 2016, 36(3): 748–757. |
| [31] | Magnani F, Mencuccini M, Grace J. Age-related decline in stand productivity: The role of structural Acclimation under hydraulic constraints. Plant, Cell, & Environment, 2000, 23(3): 251–263. |
| [32] | Ryan M G, Way D. Tree responses to drought. Tree Physiology, 2011, 31(3): 237–239. DOI:10.1093/treephys/tpr022 |
| [33] | Pucholt P, Sjödin P, Weih M, Rönnberg-Wästljung A C, Berlin S. Erratum to: Genome-wide transcriptional and physiological responses to drought stress in leaves and roots of two willow genotypes. BMC Plant Biology, 2015, 15: 285–285. DOI:10.1186/s12870-015-0665-4 |
| [34] | 魏秀俭. 玉米自交系耐旱性的模糊隶属函数法分析. 山东农业科学, 2005(2): 25–27. |
| [35] | 祁旭升, 刘章雄, 关荣霞, 王兴荣, 苟作旺, 常汝镇, 邱丽娟. 大豆成株期抗旱性鉴定评价方法研究. 作物学报, 2012, 38(4): 665–674. |
| [36] | 吴俊文, 刘珊, 李吉跃, 何茜, 苏艳, 邱权, 白晶晶, 王燕, 贾朋. 干旱胁迫下广东石漠化地区造林树种光合和耗水特性. 生态学报, 2016, 36(11): 3429–3440. |
 2017, Vol. 37
2017, Vol. 37




