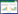文章信息
- 徐英德, 丁雪丽, 李双异, 孙良杰, 高晓丹, 谢柠桧, 金鑫鑫, 白树彬, 孙海岩, 汪景宽
- XU Yingde, DING Xueli, LI Shuangyi, SUN Liangjie, GAO Xiaodan, XIE Ninghui, JIN Xinxin, BAI Shubin, SUN Haiyan, WANG Jingkuan.
- 不同肥力棕壤全氮和微生物量氮对外源玉米残体氮的响应
- Effect of maize-derived nitrogen supplementation on the total and microbial biomass nitrogen of brown earths with different fertility levels
- 生态学报. 2017, 37(20): 6818-6826
- Acta Ecologica Sinica. 2017, 37(20): 6818-6826
- http://dx.doi.org/10.5846/stxb201608031602
-
文章历史
- 收稿日期: 2016-08-03
- 网络出版日期: 2017-06-01
氮素是土壤肥力中最为活跃、最为关键的因素之一[1], 也是农业生产中重要的限制因子, 因此氮肥施用一直是提高作物产量最重要的措施[2]。作物残体是农田生态系统中土壤有机碳的主要来源, 同时也是氮素重要的“源”和“库”[3], 因此作物残体还田对促进土壤氮循环、减少化肥施用、维持农田地力具有非常重要的作用[4]。已有研究表明秸秆还田对土壤养分和土壤生物学特性的影响是一个十分复杂的过程[5]。还田后秸秆的腐解是在土壤微生物驱动下的生物化学过程, 促进氮的微生物固持也是减少氮素损失的有效途径之一[6]。微生物在外源氮的同化和有机质的转化过程中起主导作用[7], 因此明确微生物量氮的相应变化对了解作物残体氮素的生物有效性至关重要。作物残体各部分(根、茎、叶)因成分间存在显著的差异性[8], 导致不同部位有机成分组成、尤其是有机碳与氮含量的不同[9], 影响了其在土壤中腐解的进程[10]。有研究发现水稻秸秆来源氮素会随着分解过程的进行进入不同的土壤氮库[11], 还有报道指出秸秆腐解期间等量秸秆较根茬更有利于补充土壤活性碳与氮的数量[12]。谢柠桧等[13]则证明玉米不同部位残体在土壤中的残留与分配对土壤有机碳的固定起到关键作用。然而关于作物残体不同部位来源氮素在不同肥力水平土壤中的分配及其对土壤氮库的贡献尚鲜见报道。本研究以长期玉米连作体系下两种不同施肥水平棕壤为基础, 利用15N稳定同位素示踪技术, 通过室内培养方法, 研究添加不同部位玉米残体(根、茎、叶)后不同肥力棕壤中“新”“老”全氮的动态变化及微生物量氮的响应, 探索秸秆腐解过程中在不同土壤肥力水平下外源新氮分配与贡献机制, 以期为构建合理的秸秆还田与施肥措施提供理论依据。
1 材料与方法 1.1 供试材料 1.1.1 供试土壤供试土壤采自沈阳农业大学棕壤长期定位试验站。该试验站始建于1987年春天, 位于41°49′N, 123°34′E, 土壤为发育在黄土性母质上的壤质棕壤。试验站长期种植作物为玉米, 每年4月中下旬播种, 9月中下旬收获, 具体试验布置与施肥处理详见安婷婷等[14]。本研究所采用的低肥棕壤为连续27a未施用任何肥料的处理(LF), 高肥棕壤为多年施用高量有机肥的处理(折合年施用有机肥中含纯N 270 kg/hm2, HF)。于2014年秋季玉米收获后采集耕层(0—20 cm)土壤。样品采回后在室温条件下自然风干, 挑出土壤样品中根系、石块等杂质, 过2 mm筛后备用。供试土壤样品主要理化性质详见表 1。
| 肥力水平 Fertility level |
有机碳/(g/kg)Soil organic carbon | 全氮/(g/kg)Total nitrogen | δ15N/‰ δ15N value | 碳氮比C/N |
| 低肥力水平Low fertility(LF) | 10.10±0.12 | 1.10±0.03 | 8.08±0.21 | 8.78±0.14 |
| 高肥力水平High fertility(HF) | 17.80±0.15 | 2.20±0.06 | 1.48±0.12 | 8.08±0.19 |
供试有机物料为氮稳定同位素(15N)标记的玉米残体。标记的主要过程为:待标记玉米于2014年4月25日播种, 在玉米生长进入拔节期开始标记, 用丰度为98%的(15NH4)2SO4配成0.2 mol/L溶液后分2次注入根部[15]。玉米残体收获后, 在105℃下杀青30 min, 然后在60℃下烘8 h。将根、茎和叶分开, 并剪成2 cm小段, 用秸秆粉碎机粉碎, 过40目筛后备用。试验所需玉米残体主要理化性质详见表 2。
| 玉米残体Maize plant residue | 有机碳Soil organic carbon/(g/kg) | 全氮Total nitrogen/(g/kg) | δ15Nδ15N value/‰ | 碳氮比C/N |
| 根Root | 400.76±0.20 | 12.55±0.30 | 19522.82±15.85 | 31.94±0.77 |
| 茎Stem | 440.08±0.02 | 14.45±0.25 | 19268.75±12.04 | 30.46±0.54 |
| 叶Leaf | 420.80±0.07 | 12.70±0.24 | 16787.05±23.26 | 33.14±0.65 |
本试验采用室内恒温培养法, 共设8个处理:① 低肥力土壤添加玉米根(低肥+根);② 低肥力土壤添加玉米茎(低肥+茎);③ 低肥力土壤添加玉米叶(低肥+叶);④ 高肥力土壤添加玉米根(高肥+根);⑤ 高肥力土壤添加玉米茎(高肥+茎);⑥ 高肥力土壤添加玉米叶(高肥+叶), 同时以不添加秸秆的2种肥力土壤作为对照(低肥、高肥), 每个处理3次重复。按照试验设计称取相当于120 g烘干土重的风干土样, 加蒸馏水调节含水量至7%左右, 在25℃下预培养7 d。之后将土样分别与玉米根、茎、叶充分混匀, 有机物料加入比例为烘干土重量的1%。调节土壤含水量至田间持水量的60%, 放入25℃恒温培养箱中继续培养, 每5 d补充1次水分。分别于培养后1、7、28、56、180 d和360 d进行取样, 然后将一部分鲜样进行微生物量氮的测定, 另一部分风干, 用研钵研磨并过100目筛, 进行全氮及其δ15N值的测定。
1.3 测定方法微生物量氮的测定:采用氯仿熏蒸浸提的方法[16]。称取相当于10 g烘干土重的新鲜土样放入培养皿中, 将培养皿置于真空干燥器中, 同时将已经提纯的氯仿放入真空干燥器中, 之后用真空泵抽氯仿至沸腾, 并保持5 min, 之后将抽真空的干燥器放入25℃恒温培养箱中24 h。熏蒸结束后, 将土壤转移到100 mL震荡瓶, 加入0.5 mol/L K2SO4溶液(水土比为1:4), 在25℃下恒温震荡30 min, 之后将上清液用0.45 μm滤膜过滤。在氯仿熏蒸的同时做不熏蒸的对照处理。提取液的全氮含量采用High-TOC II(Elementar II, Germany)分析仪测定。
微生物量氮的计算公式[17]:
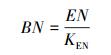
|
式中, EN为熏蒸土样与未熏蒸土样全氮之差, KEN=0.54。
全氮及其δ15N值的测定:利用元素分析-稳定同位素质谱联用仪(EA-IRMS, IsoPrime100, Germany)测定。其基本原理和测定过程为:样品经高温燃烧后(燃烧管温度为920℃, 还原管温度为600℃), 通过TCD(Thermal Conductivity Detecor)检测器测定全氮含量, 剩余气体经CO2/N2排出口(Vent)通过稀释器进入质谱仪, 在质谱仪上测定δ15N值[14]。
1.4 计算方法δ15N值的计算公式[18](标准物质为纯净大气氮):
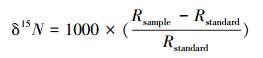
|
式中,Rsample为样品15N/14N原子比值;Rstandard=0.0036765。
土壤全氮中外源新氮贡献率(外源新氮所占比例)计算公式:
|
式中,δ15Nsample为添加玉米根、茎、叶处理土壤全氮的δ15N值;δ15Nbackground为裸土对照处理土壤全氮的δ15N值;δ15Nmaize为玉米根、茎、叶的δ15N值。
1.5 数据处理及结果分析应用Origin 8软件对试验数据进行处理和绘图, 用SPSS 19.0软件对试验结果进行方差分析, 不同处理间的差异显著性水平采用Duncan法进行多重比较, 显著水平为P<0.05。
2 结果分析 2.1 土壤全氮含量的变化不同肥力棕壤添加玉米残体后全氮含量发生显著变化。由表 3可以看出, 未添加玉米残体的低肥力和高肥力棕壤全氮平均含量分别为(1.16±0.03) g/kg和(1.85±0.02) g/kg。添加玉米残体后全氮含量显著提升(P<0.05)。而且, 添加残体对低肥力棕壤全氮含量的提升效果更显著, 其中低肥+根、低肥+茎、低肥+叶提升幅度分别为9.88%、10.21%和9.56%, 而高肥+根、高肥+茎、高肥+叶分别提升4.13%、5.44%和5.81%。在秸秆腐解过程中, 各处理随培养时间的延长未发生明显规律性的变化, 且不同部位间整体上没有明显差异。
| 培养时间Incubation time/d | 低肥力棕壤Low fertility brown earth /(g/kg) | 高肥力棕壤High fertility brown earth /(g/kg) | ||||||
| 对照 Control |
根 Root |
茎 Stem |
叶 Leaf |
对照 Control |
根 Root |
茎 Stem |
叶 Leaf |
|
| 1 | 1.15±0.02ABd | 1.28±0.01ABc | 1.30±0.03ABc | 1.29±0.03Ac | 1.86±0.03Ab | 1.91±0.02Bb | 2.00±0.08Aa | 2.00±0.09Aa |
| 7 | 1.20±0.03Ad | 1.28±0.00ABc | 1.26±0.04ABc | 1.29±0.02Ac | 1.86±0.05Ab | 1.93±0.02ABa | 1.97±0.04ABa | 1.97±0.03ABa |
| 28 | 1.18±0.03Ad | 1.31±0.03Ac | 1.30±0.04ABc | 1.29±0.01Ac | 1.85±0.02Ab | 1.96±0.06ABa | 1.98±0.03ABa | 1.98±0.00ABa |
| 56 | 1.15±0.06ABe | 1.29±0.06ABd | 1.31±0.05Ad | 1.30±0.04Ad | 1.82±0.03Ac | 2.01±0.07Ab | 1.92±0.06ABc | 2.09±0.03Aa |
| 180 | 1.18±0.01ABb | 1.24±0.01Bb | 1.23±0.05Bb | 1.23±0.04Bb | 1.85±0.04Aa | 1.91±0.01Ba | 1.90±0.02Ba | 1.84±0.15Ba |
| 360 | 1.12±0.01Be | 1.25±0.01ABcd | 1.28±0.08ABc | 1.23±0.02Bd | 1.85±0.01Ab | 1.82±0.04Cb | 1.92±0.01ABa | 1.84±0.05Bb |
| 表中的值为平均值±SD, 大写字母表示同一处理不同培养时期差异显著性(P<0.05), 小写字母表示同一时期不同处理组合(肥力水平(低肥力、高肥力)×添加玉米残体部位(不添加、根、茎、叶))差异显著性(P<0.05). | ||||||||
低肥力棕壤和高肥力棕壤对照处理在整个培养过程中土壤全氮δ15N值平均为(10.48±1.39)‰和(8.90±0.35)‰, 波动较小(数据未列出)。2种肥力棕壤添加不同部位玉米残体后全氮δ15N值随培养时间延长的变化情况如图 1所示。从图 1可以看出, 添加玉米残体后, 土壤全氮δ15N值显著升高(P<0.05)。在培养前期添加根的处理δ15N值较添加茎和叶的处理波动大, 之后均较为平稳, 在两种肥力棕壤中δ15N值表现为低肥>高肥(P<0.05)。对于玉米残体不同部位, 土壤全氮δ15N值在两种肥力棕壤整体表现为茎高于根和叶, 到培养360 d时, 低肥力棕壤中添加茎处理的土壤全氮δ15N值分别是添加根和叶的1.12倍和1.58倍, 而高肥土壤中三者差异不显著(P>0.05)。
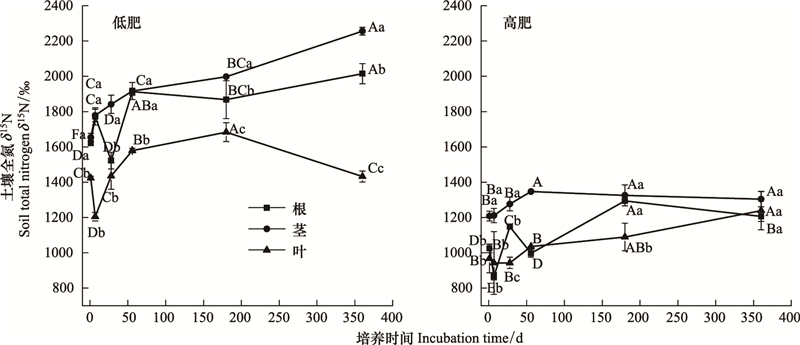
|
| 图 1 不同肥力棕壤添加15N标记玉米残体后土壤全氮δ15N值变化 Fig. 1 Dynamic changes of δ15N values in total nitrogen in different fertility brown earth added with 15N-labeled maize resdiues 大写字母表示同一处理不同培养时期差异显著性(P<0.05), 小写字母表示同一时期不同残体部位差异显著性(P<0.05) |
两种肥力棕壤添加不同部位玉米残体后, 外源新氮贡献率随培养时间和土壤全氮δ15N值变化趋势总体一致(图 2)。在整个培养过程中, 低肥+根、低肥+茎、低肥+叶、高肥+根、高肥+茎、高肥+叶处理外源新氮贡献率的均值分别为9.09%、9.87%、8.62%、5.55%、6.59%和6.13%。外源新氮贡献率同样表现出培养前期添加根的处理, 较添加茎和叶的处理波动大, 之后均较为平稳。在不同肥力水平下, 低肥力棕壤外源新氮贡献率显著高于高肥力棕壤(P<0.05)。培养到360 d时, 低肥力棕壤中添加根、茎、叶后土壤外源新氮贡献率分别为10.26%、11.29%和8.49%, 高肥力棕壤外源新氮贡献率分别为6.13%、6.74%和7.34%。
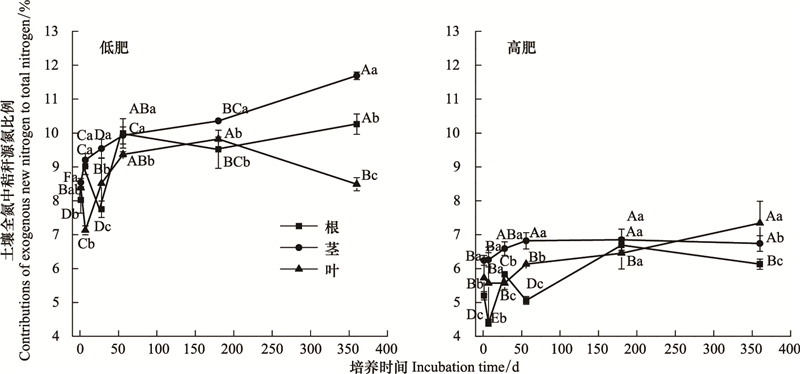
|
| 图 2 不同肥力棕壤添加15N标记玉米残体后土壤全氮中外源新氮贡献率的变化 Fig. 2 Dynamic changes of contributions of exogenous new nitrogen to total nitrogen in different fertility soils added with 15N-labeled maize residues 大写字母表示同一处理不同培养时期差异显著性(P<0.05), 小写字母表示同一时期不同残体部位差异显著性(P<0.05) |
在培养初期, 土壤微生物量氮逐渐上升, 第7天达到最大值, 以后逐渐降低(图 3)。两种肥力棕壤添加玉米残体后土壤微生物量氮较对照处理含量明显增加(P<0.05), 在56 d的培养时间内, 低肥力棕壤微生物量氮平均增加0.83—0.98倍, 高肥力棕壤微生物量氮平均增加0.87—1.56倍。添加秸秆后, 除第1天和第56天添加根的处理外, 其余各时期, 土壤微生物量氮含量均为高肥力水平>低肥力水平。低肥力水平各处理中, 第1天土壤微生物量氮含量为低肥+根>低肥+叶>低肥+茎, 以后的各培养时期三者无显著差异。在培养的1—56 d, 高肥力水平各处理中微生物量氮含量均为高肥+茎、高肥+叶高于高肥+根处理。添加秸秆各处理均在培养的初期微生物量氮含量迅速增加, 低肥中, 在培养的前28 d, 低肥+根、低肥+茎、低肥+叶均出现了不同程度的下降, 下降幅度分别为32.98%、11.75%和16.64%;在28—56 d微生物氮含量有所上升, 上升幅度分别为22.26%、23.13%和16.81%。高肥力水平各处理均表现为前7 d迅速上升并达到峰值, 7—28 d下降, 28—56 d趋于稳定的趋势。培养56 d时与开始时相比, 低肥+根、高肥+茎、高肥+叶出现了明显的下降, 低肥+茎略有上升, 其他处理则差异不明显。
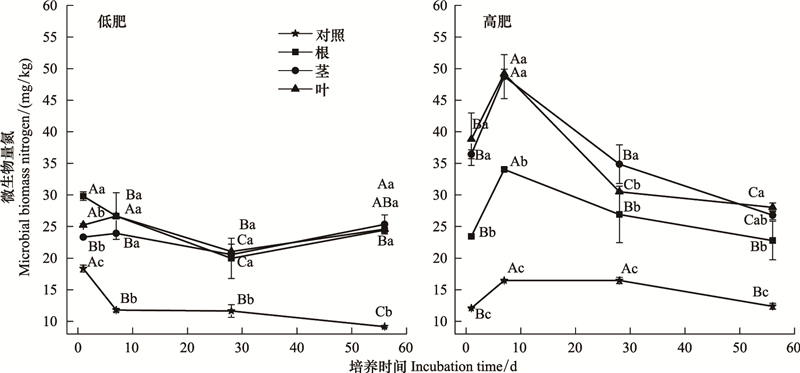
|
| 图 3 不同肥力土壤添加15N标记玉米残体后土壤微生物量氮含量的变化 Fig. 3 Dynamic changes of microbial biomass nitrogen in different fertility level soils added with 15N-labeled maize residues 大写字母表示同一处理不同培养时期差异显著性(P<0.05), 小写字母表示同一时期不同残体部位差异显著性(P<0.05) |
δ15N标记玉米残体加入土壤后明显提高了土壤全氮含量及其δ15N值, 这与王淑平[19]和Chaves[20]的研究结果一致, 本研究在此基础上进一步突出了肥力水平及残体部位的影响。在低肥力棕壤中, 玉米残体对土壤全氮的提升效果更明显, 表明秸秆在两种肥力棕壤中腐解有差异, 从而影响了秸秆氮对土壤氮的补充。在本研究中δ15N值波动的幅度表明进入土壤的外源新氮整体在前56 d周转较快, 这一阶段可能处于作物残体中易分解化合物的快速分解阶段[21]。一些研究[13, 22]发现外源新碳在土壤中的分配呈现土壤初始有机碳含量越低, 分配越多的趋势。本试验通过δ15N值的变化进一步表明外源新氮在不同肥力棕壤的分配呈现出初始土壤全氮含量越低贡献率越大的相似规律。Aita等也指出15N与13C两种外源同位素在土壤中的分布和动力学过程相似[23]。低肥力水平各处理的δ15N值均明显高于高肥力水平各处理, 表明低肥力棕壤对残体氮的固定能力要高于高肥力棕壤。在本试验站低肥力棕壤较高肥力棕壤含有更多的粘粒含量[24], 很多无机胶体没有与有机胶体结合, 当有机物加入时, 这些无机胶体(粘粒)与有机物紧密结合, 形成比较稳定的有机-无机复合体, 从而固定更多的有机碳, 使土壤有机质含量提高, 与此同时也就提高了土壤全氮含量。王佳佳等[25]和吴景贵等[9]分别研究表明作物残体叶片的腐解速率和氮素释放速率大于茎秆, 而本研究中添加不同部位玉米残体后δ15N值在不同肥力棕壤中的总体表现为茎>叶>根, 主要是因为根含有较多的木质素等难分解物质, 而茎和叶中含有更多的糖类、纤维素和半纤维素等易分解物质[26], 并且在试验材料中茎的碳氮比最低而全氮含量最高, 尤其是在低肥力水平处理的培养后期, 茎的低碳氮比优势发挥明显。在培养结束时(360 d), 低肥力水平处理较高肥力水平处理不同部位残体间的差异更明显。这主要是由于秸秆中氮素的分解受到土壤结构和秸秆自身组成特性的影响[27]。研究表明作物残体各部分性质的差异主要取决于是否是支撑组织(茎), 传导组织(叶)或保护组织(根)[28], 且残体各个部位化学组成存在很大的差异[9], 低肥力土壤较高的粘粒含量以及较少的有机-无机复合体含量扩大了秸秆自身组成及碳氮比所导致的与粘粒结合成稳定结构的差异性。而在髙肥力水平处理中, 培养前期和中期(1 d—180 d)不同残体氮的固定存在差异, 而在培养一年后差异不明显, 可见随培养时间的延长, 高肥力棕壤的肥力背景和趋于饱和的高有机质含量掩盖了不同部位玉米残体之间的差异。由此结果可见, 秸秆自身组成和碳氮比的差异以及土壤肥力水平的差异会共同导致培养的各个时期不同残体氮的固定出现差异。
3.2 土壤外源新氮贡献率的变化添加玉米残体后外源新氮占土壤全氮的比例反映出了外源新氮贡献率的大小。在本试验中残体氮对低肥力棕壤全氮的贡献率高于高肥力棕壤, 低肥力棕壤中全氮含量较低, 新加入的玉米残体进入到土壤里, 含有15N的物质增多, 使15N比例增大, 随着秸秆的腐解, 秸秆氮的贡献比有不同程度的增加, 在低肥力棕壤中贡献率增加幅度茎>根>叶, 高肥力棕壤中叶>根>茎, 呈现完全相反的趋势, 因为高低肥力棕壤之间存在着微生物种群和生物多样性的较大差异[29], 并且不同部位玉米残体在不同肥力土壤会产生不同程度的激发效应[30-31], 致使土壤的碳氮比[23]以及土壤中微生物的区系发生变化, 从而使不同部位氮素的分解产生差异。培养到360 d时, 从不同部位玉米残体在棕壤贡献率的差异可以看出, 茎的氮素贡献率在高低两种肥力土壤中差异更大, 这表明棕壤中微生物群落对茎的外源氮加入反应最敏感。
3.3 土壤微生物量氮的变化作物残体的腐解是微生物主导的生化过程, 向土壤中添加植物残体能够改变土壤微环境以及微生物所利用的碳源, 进而影响土壤中微生物的数量和活性[3, 32]。
通过本试验可以看出, 添加玉米残体不同部位均能刺激土壤微生物的生长, 增加微生物对氮素的同化, 有利于土壤氮的协调供应。促进土壤微生物量增加的原因主要是原有土壤有机质的进一步分解引起(利用土壤腐殖质所含能源和养分)[33]以及秸秆添加增加环境可利用氮素含量[11]。微生物量的大小通常与土壤的肥力水平呈正相关[34], 本试验结果表明土壤肥力水平也会影响不同部位玉米残体添加后微生物量氮的动态变化。两种肥力棕壤均在培养前期微生物氮含量较对照有显著的增加。秸秆还田后只有当氮素充足时微生物才更容易繁殖[35], 高肥力棕壤含有更多的微生物可利用氮源, 从长远来看更有利于微生物的繁殖。本试验中土壤微生物氮含量一般为高肥力水平>低肥力水平, 不仅因为高肥力棕壤的土壤微生物量氮本底值高[29], 而且高肥力棕壤微生物量氮对玉米残体加入后的响应更明显。高肥力水平处理表现为前7 d显著上升并达到峰值, 之后下降并趋于稳定, 而闫德智等[11]研究发现乌栅土添加水稻秸秆后微生物量氮在14 d时才达到最大值, 这可能是因为本试验所用玉米秸秆(C/N 31.85)相对于水稻秸秆(C/N 55.64)较低的碳氮比所导致。在低肥力水平处理中, 土壤微生物量氮总体上呈现前28 d下降, 28 d后上升的趋势。这主要是由于低肥力棕壤较高肥力棕壤有机质含量低, 微生物本身活性较弱, 玉米残体施入土壤后激发效应会更强烈, 氮素在培养前期就很快被固持在微生物体, 之后随着微生物的死亡被固定的氮被重新释放到土壤中。由于前两次取样的时间相隔7 d, 不排除在这7 d之间出现峰值的情况, 而高低肥力水平处理微生物量氮达到最大峰值的时间不一致, 可能是由于土壤肥力和秸秆加入引起的土壤微环境的变化综合作用的结果。低肥+根处理在第1天微生物量氮就达到很高水平, 原因比较复杂, 不溶性化合物含量多的作物残体更易引起激发效应[31]。在培养的后期, 低肥力水平处理稳中有升, 而高肥力水平处理稳中有降, 可能受棕壤不同施肥模式的影响, 也可能是因为随着培养时间的延长, 秸秆腐解后成分发生变化, 微生物群落也会发生更替, 微生物量氮可能会出现周期性的变化[36]。综合来看玉米残体施入土壤后的1个月是土壤微生物量氮动态变化的高峰期。综上, 土壤肥力水平和残体部位化学组分的差异性均会导致土壤微生物量氮含量对残体氮添加后的反馈机制的差异性。
4 结论(1) 外源新氮对土壤氮库的贡献受初始土壤肥力水平的显著影响, 低肥力棕壤全氮对外源新氮施入后的响应更敏感。外源氮素对土壤氮库的贡献与土壤的肥力水平及不同残体部位自身的组成特性密切相关。
(2) 高肥力棕壤微生物量氮对作物残体输入后的响应更敏感, 且相对于低肥力棕壤更能扩大微生物氮含量在施入不同部位残体后的差异性。玉米茎叶还田更有利于增加土壤微生物量氮含量。
(3) 本研究只探讨了外源新氮在棕壤全土中的分配与固定, 而关于不同部位玉米残体氮在土壤不同团聚体组分中的去向与分配机制还有待进一步研究。
| [1] | 陆景陵. 植物营养学(第二版). 北京:中国农业大学出版社, 2003: 23–23. |
| [2] | 张文, 周广威, 闵伟, 马丽娟, 侯振安. 应用15N示踪法研究咸水滴灌棉田氮肥去向. 土壤学报, 2015, 52(2): 372–380. |
| [3] | Dinnes D L, Karlen D L, Jaynes D B, Kaspar T C, Hatfield J L, Colvin T S, Cambardella C A. Nitrogen management strategies to reduce nitrate leaching in tile-drained midwestern soils. Agronomy Journal, 2002, 94(1): 153–171. DOI:10.2134/agronj2002.1530 |
| [4] | 潘剑玲, 代万安, 尚占环, 郭瑞英. 秸秆还田对土壤有机质和氮素有效性影响及机制研究进展. 中国生态农业学报, 2013, 21(5): 526–535. |
| [5] | 李娟, 赵秉强, 李秀英, HwatB S. 长期有机无机肥料配施对土壤微生物学特性及土壤肥力的影响. 中国农业科学, 2008, 41(1): 144–152. |
| [6] | 艾娜. 不同处理土壤微生物量对氮素的固持及其调控研究[D]. 杨凌: 西北农林科技大学, 2008. |
| [7] | Burger M, Jackson L E. Microbial immobilization of ammonium and nitrate in relation to ammonification and nitrification rates in organic and conventional cropping systems. Soil Biology and Biochemistry, 2003, 35(1): 29–36. DOI:10.1016/S0038-0717(02)00233-X |
| [8] | Abiven S, Recous S, Reyes V, Oliver R. Mineralisation of C and N from root, stem and leaf residues in soil and role of their biochemical quality. Biology and Fertility of Soils, 2005, 42(2): 119–128. DOI:10.1007/s00374-005-0006-0 |
| [9] | 吴景贵, 陈丽荣, 王明辉, 姜亦梅, 耿玉晖. 玉米植株残体腐解过程的化学分析. 吉林农业大学学报, 2000, 22(3): 61–66. |
| [10] | Nicolardot B, Recous S, Mary B. Simulation of C and N mineralisation during crop residue decomposition: A simple dynamic model based on the C: N ratio of the residues. Plant and Soil, 2001, 228(1): 83–103. DOI:10.1023/A:1004813801728 |
| [11] | 闫德智, 王德建, 张刚, 查书平. 15N标记秸秆在太湖地区水稻土上的氮素矿化特征研究. 土壤学报, 2012, 49(1): 77–85. DOI:10.11766/trxb201101260044 |
| [12] | 把余玲, 田霄鸿, 万丹, 李锦, 王淑娟. 玉米植株不同部位还田土壤活性碳、氮的动态变化. 植物营养与肥料学报, 2013, 19(5): 1166–1173. DOI:10.11674/zwyf.2013.0516 |
| [13] | 谢柠桧, 安婷婷, 李双异, 孙良杰, 裴久渤, 丁凡, 徐英德, 付时丰, 高晓丹, 汪景宽. 外源新碳在不同肥力土壤中的分配与固定. 土壤学报, 2016, 53(4): 942–950. |
| [14] | 安婷婷, 汪景宽, 李双异, 付时丰, 裴久渤, 李慧. 用13C脉冲标记方法研究施肥与地膜覆盖对玉米光合碳分配的影响. 土壤学报, 2013, 50(5): 948–955. |
| [15] | An T T, Schaeffer S, Li S Y, Fu S F, Pei J B, Li H, Zhuang J, Radosevich M, Wang J K. Carbon fluxes from plants to soil and dynamics of microbial immobilization under plastic film mulching and fertilizer application using 13 C pulse-labeling. Soil Biology and Biochemistry, 2015, 80: 63–61. |
| [16] | Brookes P C, Landman A, Pruden G, Jenkinson D S. Chloroform fumigation and the release of soil nitrogen: a rapid direct extraction method to measure microbial biomass nitrogen in soil. Soil Biology and Biochemistry, 1985, 17(6): 837–842. DOI:10.1016/0038-0717(85)90144-0 |
| [17] | 薛菁芳, 高艳梅, 汪景宽. 长期施肥与地膜覆盖对土壤微生物量碳氮的影响. 中国土壤与肥料, 2007(3): 55–58. DOI:10.11838/sfsc.20070314 |
| [18] | Robinson D. δ 15N as an integrator of the nitrogen cycle. Trends in Ecology & Evolution, 2001, 16(3): 152–162. |
| [19] | 王淑平, 周广胜, 姜岩, 刘孝义. 添加玉米残体对土壤——植物系统中氮素转化的影响. 应用生态学报, 2004, 15(3): 449–452. |
| [20] | Chaves B, De Neve S, Boeckx P, Berko C, Van Cleemput O, Hofman G. Manipulating the N release from 15N labelled celery residues by using straw and vinasses. Soil Biology and Biochemistry, 2006, 38(8): 2244–2254. DOI:10.1016/j.soilbio.2006.01.023 |
| [21] | Wang W J, Baldock J A, Dalal R C, Moody P W. Decomposition dynamics of plant materials in relation to nitrogen availability and biochemistry determined by NMR and wet-chemical analysis. Soil Biology and Biochemistry, 2004, 36(12): 2045–2058. DOI:10.1016/j.soilbio.2004.05.023 |
| [22] | 吕元春, 薛丽佳, 尹云锋, 高人, 马红亮, 杨玉盛. 外源新碳在不同类型土壤团聚体中的分配规律. 土壤学报, 2013, 50(3): 534–539. |
| [23] | Aita C, Recous S, Angers D A. Short-term kinetics of residual wheat straw C and N under field conditions: characterization by 13C 15N tracing and soil particle size fractionation. European Journal of Soil Science, 1997, 48(2): 283–294. DOI:10.1111/ejs.1997.48.issue-2 |
| [24] | Pei J B, Li H, Li S Y, An T T, Farmer J, Fu S F, Wang J K. Dynamics of maize carbon contribution to soil organic carbon in association with soil type and fertility level. PLoS One, 10(3): e0120825–10.1371/journal.pone.0120825. DOI:10.1371/journal.pone.0120825 |
| [25] | 王佳佳, 奚永兰, 常志州, 王暝琰, 张荣. 麦秸不同部位生物降解速率差异. 农业资源与环境学报, 2015, 32(1): 74–80. |
| [26] | Clemente J S, Simpson M J, Simpson A J, Yanni S F, Whalen J K. Comparison of soil organic matter composition after incubation with maize leaves, roots, and stems. Geoderma, 2013, 192(1): 86–96. |
| [27] | Chivenge P, Vanlauwe B, Gentile R, Six J. Comparison of organic versus mineral resource effects on short-term aggregate carbon and nitrogen dynamics in a sandy soil versus a fine textured soil. Agriculture, Ecosystems & Environment, 2011, 140(3/4): 361–371. |
| [28] | Machinet G E, Bertrand I, Chabbert B, Recous S. Decomposition in soil and chemical changes of maize roots with genetic variations affecting cell wall quality. European Journal of Soil Science, 2009, 60(2): 176–185. DOI:10.1111/ejs.2009.60.issue-2 |
| [29] | 李世朋, 蔡祖聪, 杨浩, 汪景宽. 长期定位施肥与地膜覆盖对土壤肥力和生物学性质的影响. 生态学报, 2009, 29(5): 2489–2498. |
| [30] | Asmar F, Eiland F, Nielsen N E. Interrelationship between extracellular enzyme activity, ATP content, total counts of bacteria and CO2 evolution. Biology and Fertility of Soils, 1992, 14(4): 288–292. DOI:10.1007/BF00395465 |
| [31] | Fontaine S, Mariotti A, Abbadie L. The priming effect of organic matter: A question of microbial competition?. Soil Biology and Biochemistry, 2003, 35(6): 837–843. DOI:10.1016/S0038-0717(03)00123-8 |
| [32] | Tu C, Ristaino J, Hu S J. Soil microbial biomass and activity in organic tomato farming systems: Effects of organic inputs and straw mulching. Soil Biology and Biochemistry, 2006, 38(2): 247–255. DOI:10.1016/j.soilbio.2005.05.002 |
| [33] | 王志明, 朱培立, 黄东迈. 14 C、15 N双标记秸秆对土壤微生物量碳、氮动态变化的影响. 江苏农业学报, 1999, 15(3): 173–176. |
| [34] | Witter E, Mårtensson A M, Garcia F V. Size of the soil microbial biomass in a long-term field experiment as affected by different N-fertilizers and organic manures. Soil Biology and Biochemistry, 1993, 25(6): 659–669. DOI:10.1016/0038-0717(93)90105-K |
| [35] | 刘骁蒨, 涂仕华, 孙锡发, 辜运富, 张先琴, 张小平. 秸秆还田与施肥对稻田土壤微生物生物量及固氮菌群落结构的影响. 生态学报, 2013, 33(17): 5210–5218. |
| [36] | 张成娥, 王栓全. 作物秸秆腐解过程中土壤微生物量的研究. 水土保持学报, 2000, 14(3): 96–99. |
 2017, Vol. 37
2017, Vol. 37