文章信息
- 韩路, 王海珍, 牛建龙, 王家强, 柳维扬
- HAN Lu, WANG Haizhen, NIU Jianlong, WANG Jiaqiang, LIU Weiyang.
- 荒漠河岸林胡杨群落特征对地下水位梯度的响应
- Response of Populus euphratica communities in a desert riparian forest to the groundwater level gradient in the Tarim Basin
- 生态学报. 2017, 37(20): 6836-6846
- Acta Ecologica Sinica. 2017, 37(20): 6836-6846
- http://dx.doi.org/10.5846/stxb201607281547
-
文章历史
- 收稿日期: 2016-07-28
- 网络出版日期: 2017-06-01
中国西部干旱区气候干旱、降水稀少、植被稀疏, 生态环境极其脆弱, 水资源开发过程中生态与经济的矛盾十分突出。水作为干旱区最关键的生态环境因子, 不仅是干旱区绿洲生态系统发展和稳定的基础, 而且决定着干旱区绿洲化过程与荒漠化过程这两类极具对立与冲突性的生态环境演化过程[1]。众多研究表明, 地表水日益减少甚至断流的干旱区内陆河流域, 地下水是维系荒漠植被生长发育与生存的唯一水源[1-5]。地下水位时空变化直接影响着自然植被生长和衰败, 控制着植物群落结构与功能动态[1-3], 影响干旱区荒漠植被生态服务功能的提升。因此, 干旱区地下水位成为制约荒漠植被恢复与绿洲稳定的首要关键因素。然而, 干旱区地下水位变化与植被之间具有复杂的关系, 它涉及到地下水、土壤和植被等相互之间的动态平衡[1]。为此, 许多学者开展了针对地下水与天然植被的关系研究, 提出了地下水生态平衡埋深、生态地下水位和合理地下水位、生态水位线以及适宜水位、胁迫水位和生态警戒水位等概念[2, 5-8], 这些研究为进一步认识荒漠植被和土壤水分、地下水埋深的关系及合理生态水位的确定奠定了基础。
塔里木盆地地处欧亚大陆腹地, 它以鲜明地域特色和环境问题著称于世。沿塔里木河两岸分布并经长期自然演替形成的独特荒漠河岸林, 成为防风固沙、遏制荒漠化、维护区域经济发展与生态安全、保护生物多样性和保障绿洲农牧业生产的天然屏障。但近50 a来, 塔里木河流域大规模的水土资源开发致使河流断流、地下水位持续降低;原有荒漠植被的生态过程与自然景观格局被改变, 植被退化、沙尘暴剧增、生物多样性锐减[3]、耕地撩荒, 严重危及荒漠绿洲生态服务功能与区域社会经济的持续发展。塔里木荒漠河岸林沿环境梯度的生态响应是荒漠河岸林植被恢复与生态需水机理研究中的重要方向, 是确定荒漠河岸林合理生态水位和推演适宜生态需水量的基础。诸多学者从不同角度分析了塔里木河水资源开发利用与生态关系, 研究内容主要涉及塔里木河中、下游植被与地下水埋深动态关系、植被生理生态响应机理、地下水化学性质与合理生态地下水位等方面[1-6, 9], 但不同学者的研究结果存在差异且针对塔里木河上游植被格局、优势种群特征沿环境梯度的变化及与地下水埋深的相互关系研究十分有限。因此, 研究塔里木荒漠河岸林物种多样性与胡杨种群特征对地下水位梯度的响应是实施流域科学生态输水工程的前提。本文结合近5年对塔里木河上游各断面植被样地调查和土壤水分、地下水位的监测资料, 探讨胡杨群落生态特征沿地下水位梯度的响应与浅层地下水位变化对胡杨种群的影响, 揭示极端干旱区天然植被与地下水位的关系及荒漠河岸林植被的合理生态水位与生态阈值, 为塔里木河流域荒漠植被恢复、生物多样性保护和生态输水提供理论依据。
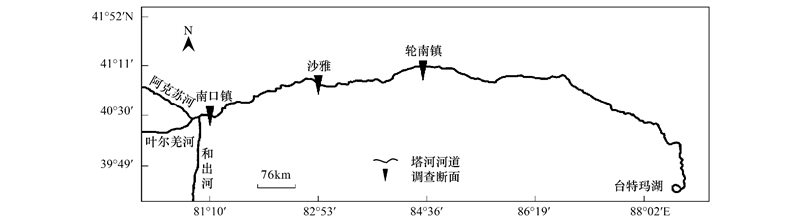
1 研究区自然概况塔里木河上游指从阿克苏河、叶尔羌河、和田河三河交汇的肖夹克至轮台县的英巴扎, 全长495 km(图 1)。该区(40°28′N, 80°56′E至41°10′N, 84°36′E)属典型暖温带大陆性干旱气候, 区内光热资源丰富, 年均日照时数2 729.0 h, 太阳总辐射能5 796 MJ m-2 a-1;年均气温10.4 ℃, 平均气温≥10℃的持续日数为201 d, ≥10℃年积温4 340 ℃;极端最高温度39.4℃, 极端最低温度-25.0℃。年均降水量50.4 mm, 年均蒸发量>2 500 mm, 干燥度12—19[10]。该区春、夏季多大风天气, 风沙灾害频繁, 是该区常见自然灾害。经实地考察, 该区植物群落结构简单、乔灌草三层结构明显, 物种多样性低, 植被稀疏。优势种为胡杨(Populus euphratica)、灰胡杨(Populus pruinosa), 林下主要分布多枝柽柳(Tamarix ramosissima)、铃铛刺(Halimodendron halodendron)、黑果枸杞(Lycium ruthenwum)、骆驼刺(Alhagi sparsifolia)、芦苇(Phragmites australis)、甘草(Glycyrrhiza uralensis)等植物[10]。土壤类型为林灌草甸土。
|
| 图 1 塔里木河上游荒漠河岸林群落调查断面示意图 Fig. 1 Investigation sections of desert riparian forest at the upper reaches of Tarim river |
经野外实地踏查于塔里木河上游(肖夹克—英巴扎)荒漠河岸林内选择林分具有代表性、人为干扰较小的上段南口镇(U1)、中段沙雅(M1)与下段轮南镇(L1)设置研究断面(图 1), 分别垂直河岸设置3条样带(50 m宽), 样带间隔100 m, 依据植被长势与地下水位在每条样带上每隔100—500 m设置50 m × 50 m样地1块(表 1), 每块样地以25 m为间隔分成4个25 m×25 m的小样方, 采用相邻格子法以5 m × 5 m为基本单元进行每木检尺, 记录胸径(DBH)≥2.0 cm的全部乔木及灌木种名、胸径(灌木为地径)、树高、冠幅[10]、树冠疏失度[11]、活立木和枯立木等指标;乔木幼苗统计时以基株为单位, 记录其中径级最大一株的高度、地径、冠幅。草本层采用对角线以1 m × 1 m小样方对植物种类、高度、盖度、多度等进行详细调查。同时, 各样方采用GPS定位, 记录其经度、纬度、海拔高度、郁闭度等生态因子。每块样地采用对角线法(5点)采集土样, 深度定为1.0 m, 分5层用土钻每隔20 cm取土样, 用铝盒和塑料袋封装, 土壤含水量采用烘干法测定, 地下水位采用人工打井(PVC管, 10 m)、电导法测定[12], 用于长期监测样地地下水位。
| 序号 No. |
地下水位/m Groundwater level |
参数Paramaters | ||||||
| 密度/(株/hm2) Density |
平均胸径/cm Average diameter at breast height |
冠幅/m Canopy diameter |
盖度/% Coverage |
树冠疏失度/% Crown loss |
物种丰富度 Species richness |
|||
| 上段 Upper section |
1 | 2.3 | 340 | 14.72 | 4.59 | 37.79 | <10 | 7 |
| 2 | 2.6 | 280 | 17.82 | 3.39 | 32.88 | <10 | 3 | |
| 3 | 3.0 | 144 | 22.31 | 4.64 | 30.27 | 10—15 | 3 | |
| 4 | 4.0 | 104 | 18.31 | 3.60 | 15.05 | 15—25 | 2 | |
| 中段 Middle section |
5 | 1.2 | 29352 | 1.00 | 0.48 | 66.17 | <10 | 9 |
| 6 | 1.5 | 27884 | 1.23 | 0.54 | 46.28 | <10 | 6 | |
| 7 | 2.0 | 4816 | 3.78 | 1.72 | 55.29 | <10 | 4 | |
| 8 | 2.4 | 752 | 8.37 | 2.13 | 50.23 | <10 | 4 | |
| 9 | 3.5 | 1096 | 17.93 | 3.16 | 38.31 | 10—15 | 3 | |
| 10 | 4.8 | 205 | 21.97 | 4.33 | 31.02 | 50 | 2 | |
| 下段 Low section |
11 | 1.4 | 8800 | 3.12 | 0.68 | 81.43 | <10 | 23 |
| 12 | 2.2 | 2207 | 6.28 | 2.28 | 67.81 | <10 | 18 | |
| 13 | 3.1 | 1290 | 13.56 | 2.55 | 50.12 | 10—15 | 10 | |
| 14 | 4.2 | 413 | 21.32 | 4.11 | 29.77 | 25—50 | 4 | |
| 15 | 5.5 | 297 | 17.78 | 2.44 | 22.75 | 75—100 | 2 | |
应用生态学中大小结构分析法[13]来研究种群年龄结构特征。虽然种群龄级和径级有所不同, 但在同一环境下, 同一树种的龄级和径级对环境的反应规律具有一致性[14]。按照2003年森林资源规划设计调查主要技术规定并结合胡杨生活史与生境异质性的特点, 将种群划分为12个径级, 第1径级胸径为0—2 cm, 第2径级胸径为2—4 cm, 之后每级间隔4 cm, 把直径大于40 cm都归为第12级;第1径级对应Ⅰ龄级, 第2径级对应第Ⅱ龄级, 依此类推。统计各龄级株数及其占总体的百分比, 以龄级为纵轴, 各龄级所占%为横轴, 绘制胡杨种群年龄结构图。乔木冠幅以树冠(d东西+d南北)/2来表示, 树冠疏失度调查方法与评判标准[11]。
2.2.2 Hill与β多样性沿地下水位梯度的变化含参数的多样性指数有利于揭示环境的变化或时空尺度的变化对多样性的影响, 也有利于多样性大小的生态解释[2]。鉴于此, 引入含参数的Hill多样性指数[2, 15]:
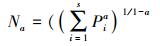
|
式中, α≥0, α≠1, 规定α=1时, Nα=eH, H为Shannon-Weiner指数;α=0时, Na=S;α=2时, Na=1/D, D为Simpson多样性指数。Pi表示第i个种的多度比例; S表示样方内的物种数。
β多样性可直观地反映不同生境物种组成的差异性, 揭示不同环境梯度下生境被物种分割的程度或不同地段的生境多样性及物种替代速率与变化速率。本文选用Sorensen指数、Cody指数和Whittaker指数作为β 多样性的测度方法[16-17]:
Sorensen指数 βs=2c/(a+b)
Whittaker指数 βw=S/ma-1
Cody指数 βc=[g(H)+t(H)]/2
式中, S为物种总数;ma为平均物种数;c为两群落共有的物种数, a、b为两群落的物种数;g(H)为沿环境梯度增加的物种数;t(H)为沿环境梯度失去的物种数, 即在上一个梯度中存在的而在下一个梯度中没有的物种数目。
2.2.3 统计分析方法离差平方和法是分类效果较好, 在生态科学领域应用较广泛的聚类方法。依据塔里木河上游3个断面45块样地胡杨群落物种组成、种群数量指标(胸径、冠幅、密度等)、地下水位等调查资料, 采用离差平方和法进行聚类分析。同时, 利用不同生境胡杨种群数量指标与地下水位进行回归分析, 并对拟合曲线进行一阶求导得出种群适宜生存水位及地下水位阈值。应用SPSS 19.0统计软件进行数据分析和Origin 8.0作图。
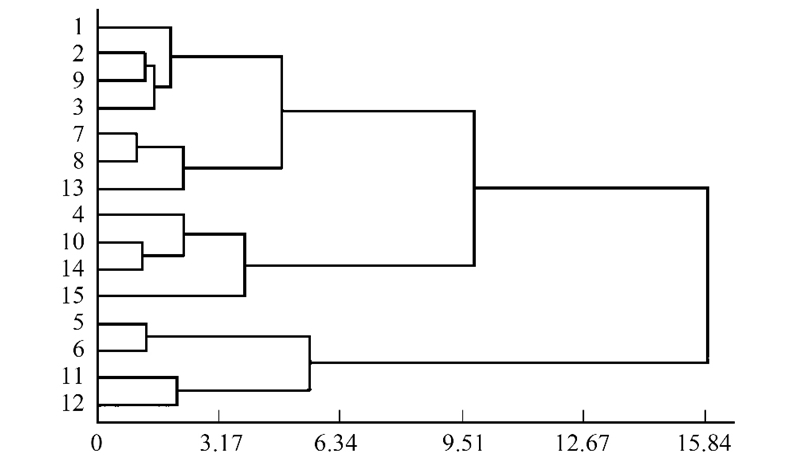
3 结果与分析 3.1 荒漠河岸林胡杨群落生态特征对地下水位梯度的响应 3.1.1 胡杨群落特征对地下水位梯度的响应优势种群作为环境梯度的一个相当可靠的指示者, 其动态变化是生态环境变化的可见标志[18]。聚类分析显示(图 2), 调查样地5、6、11、12归为一类(H1), 地下水位<2 m, 主要分布在近河道、经常洪水漫溢区域(<200 m), 群落物种组成多样, 优势种为胡杨与铃铛刺, 伴生种以浅根系中生草本植物为主;优势种与伴生种种子随洪水飘落河漫滩在充足土壤水分下萌发、生长形成物种多样性高与密度大的幼龄林。样地1、2、3、7、8、9、13归为一类(H2), 地下水位2—4 m。随远离河道和地下水位下降、土壤水分降低, 一些浅根系和中生性草本植物逐渐消失, 群落主要以胡杨、柽柳、黑果枸杞、甘草、芦苇、骆驼刺等组成, 群落乔、灌、草分层明显, 种群密度降低, 个体长势良好, 植被主要依靠浅层地下水维系生存。但因地表丧失洪水漫溢补给, 优势种胡杨种子难以萌发而缺乏更新及难以满足胡杨幼苗的生长, 形成青壮林与成熟林并存格局。样地4、10、14、15归为一类(H3), 地下水位4—6 m。由于距离河道较远, 一些中生耐旱性差的灌草植物及多年生深根性的草本植物逐渐适应不了日益旱化环境而退出群落及小径级优势种难以吸收地下水而立枯, 保留深根耐旱的胡杨、柽柳, 形成群落结构简单、物种多样性低的过熟林。分类后的胡杨群落与优势种群特征见表 2。
|
| 图 2 不同生境胡杨群落的聚类分析结果(Ward法) Fig. 2 The results of P.euphratica community under different habitats with Wards methods of cluster analysis |
| 地下水位/m Groundwater level |
参数Parameters | ||||||||
| 密度 Density/ (株/hm2) |
平均胸径 Average diameter at breast height/cm |
冠幅 Canopy diameter/m |
盖度 Coverage/% |
树冠疏失度/% Crown loss |
物种丰富度 Species richness |
死亡率 Mortality rate/% |
林分郁闭度 Stand canopy density |
||
| H1 | <2 | 17061.75±13628.06 | 2.90±2.45 | 0.99±0.86 | 65.42±14.48 | <10 | 14.00±7.87 | 0.03±0.06 | 0.79±0.07 |
| H2 | 2—4 | 1245.43±1632.06 | 14.07±6.27 | 3.17±114 | 42.48±9.17 | 10—25 | 4.86±2.67 | 1.43±1.52 | 0.42±0.12 |
| H3 | 4—6 | 254.75±131.69 | 19.85±2.11 | 3.62±0.84 | 24.65±7.36 | 44—69 | 2.50±1.0 | 24.01±19.41 | 0.23±0.07 |
| H1、H2、H3 表示地下水位分别为0—2 m、2—4 m、4—6 m的生境 | |||||||||
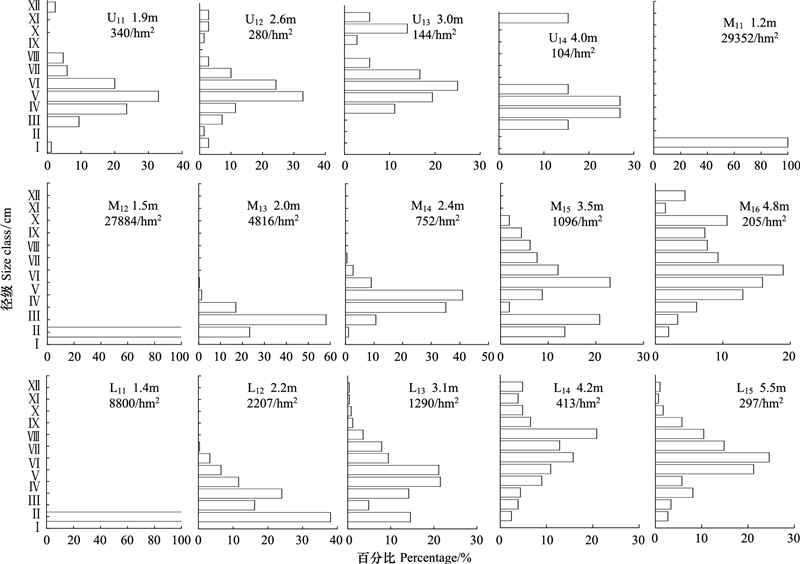
种群径级结构是揭示种群结构现状和更新策略的重要途径之一, 是探索种群动态的有效方法。U1、M1、L1断面胡杨种群径级结构沿地下水位梯度表现出相似的变化规律, 随远离河岸与地下水位降低, 种群均由增长型转变为稳定型, 然后退化为衰退型种群(图 3)。表 2可见, 地下水位<2 m生境(H1), 胡杨种群平均密度为17061株/hm2, 幼苗丰富;平均盖度为65.4%, 个体平均胸径<4 cm, 处于幼龄阶段。随地下水位下降与远离河岸, 地下水位在2—4 m生境(H2)胡杨种群幼苗(DBH<2 cm)显著降低, 降幅达78.98%(与H1相比);胸径明显增大, 最大胸径达60 cm, >4 cm个体数增多46.47%。种群结构呈金字塔型, 但Ⅰ级幼苗比例仅为21.02%, 而Ⅱ级个体比例占32.33%, 表明种群属暂时稳定型。随未来水资源持续减少与地下水位持续降低, 胡杨种群因更新资源不足而趋于衰退。随离河岸距离不断增大, 地下水位在4—6 m生境(H3)胡杨种群幼龄比例(DBH<4 cm)降低至5.38%, 减少48.15%(与H2相比), 同时这些幼龄个体均是根萌蘖产生, 生长势极差。胡杨种群密度、冠幅、盖度与林分郁闭度降低, 但平均胸径、树冠疏失度与立枯死亡率增大, 尤其树冠2/3以上干枯(疏失度达70%)和立枯比率最高达50.3%。种群最大胸径达82 cm, >32 cm个体数增多15.67%, 种群结构呈倒金字塔型, Ⅰ、Ⅱ级幼苗严重匮乏(图 3), 属衰退型种群。可见, 随地下水位的下降, 种群结构由更新资源丰富、增长型逐渐转变为更新匮乏、立枯增多的衰退型种群, 林分由幼龄林演化为成过熟林。地下水位降低是导致优势种群衰退的直接因子。
|
| 图 3 塔里木河上游3个断面胡杨种群径级结构沿地下水位梯度的动态 Fig. 3 The DBH distribution of P.euphratica under different habitats in the upper reaches of Tarim river U11—U14为上段南口镇;M11—M16为中断沙雅;L11—L15为下段轮南镇 |
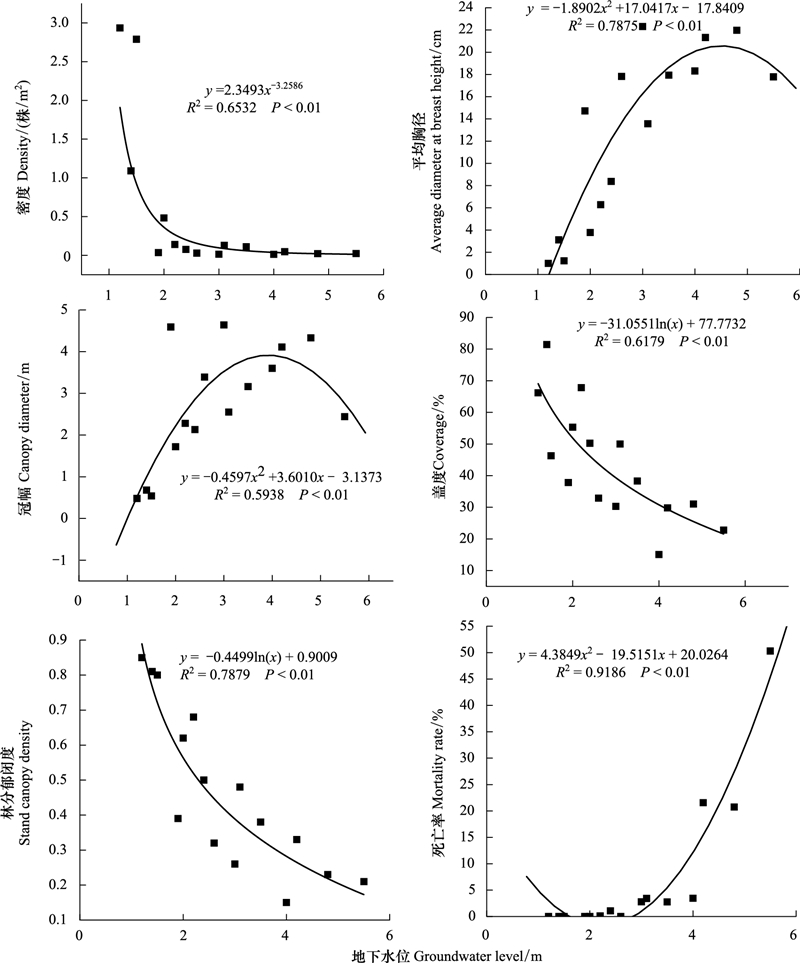
地下水是干旱荒漠区植被赖以生存的重要水分来源, 尤其地下水是胡杨生存与生长的先决条件[19]。图 4可见, 胡杨种群密度、盖度与林分郁闭度均随地下水位下降而降低, 死亡率则增加;密度、盖度、死亡率、林分郁闭度与地下水位的拟合曲线均达极显著水平(P<0.01)(图 4);平均胸径、冠幅与地下水位呈二次曲线关系(P<0.01)(图 4), 表明地下水位直接影响优势种群结构、密度、长势与存亡动态。冠幅间接反映树冠的饱满程度和树木长势状况的好坏[11], 冠幅变化是衡量环境梯度下种群生长状态的重要生态指标之一。对胡杨种群冠幅与地下水位的二次曲线进行一阶求导(图 4), 当地下水位为3.95m时, 胡杨个体冠幅最大, 随地下水位降低而下降。表明地下水位<4 m, 胡杨种群树冠伸展与生长势强, 光合面积大, 此为胡杨种群的适宜生存水位, 这与徐海量等[20]、樊自立等[21]研究结果相似。对胡杨种群密度、死亡率、林分郁闭度与地下水位的数量关系分析, 当地下水位分别为8.0、7.05 m和7.42 m时, 种群密度与林分郁闭度为0及死亡率达100%, 表明地下水位在7—8 m, 是胡杨种群生存的地下水位阈值。
|
| 图 4 塔里木河上游胡杨种群数量特征与地下水位的关系 Fig. 4 The relationship of quantitative characteristics of P.euphratica population and groundwater levels in the upper reaches of Tarim river |
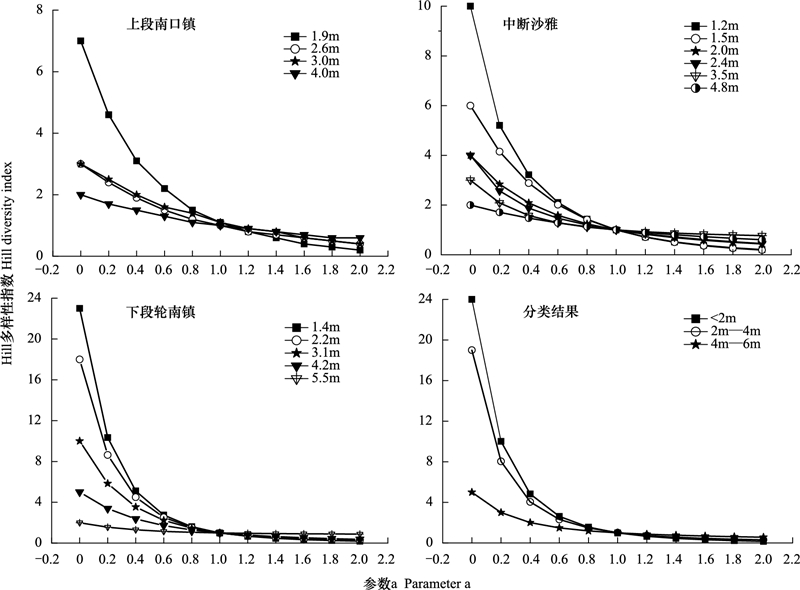
图 5可见, 胡杨群落物种多样性随着地下水位下降表现出逐步降低趋势, 地下水位越深, 多样性指数越小。这是因随着地下水位下降, 乔木多样性无变化, 而灌木和草本的生存资源不断减少, 物种丰富度和均匀度逐步降低所致。同时, 图 5显示出塔里木河上游物种多样性随地下水位梯度呈现出3个明显不同的变化特征。① 地下水位<2 m, 3个断面不同地下水位生境的物种多样性指数走势相似, 均呈迅速降低趋势, 并随参数α增大多样性指数变幅明显, α=0.8、2.0时多样性指数比α=0时分别降低了9.5倍、68.1倍。② 地下水位2—4 m范围内, 不同地下水位生境的多样性指数下降减速、曲线弯曲度与高差缩小;并随着参数α增大多样性指数变幅缩小, α=0.8、2.0时多样性指数比α=0时分别降低了3.7倍、11.6倍。③ 地下水位4—6 m范围内, 不同地下水位生境的多样性曲线走势趋于平直化, 几乎成一条直线;并随着参数α增大多样性指数变化较小, α=0.8、2.0时多样性指数比α=0时分别降低了2.4倍、4.6倍。3个断面胡杨群落Hill多样性指数随地下水位梯度的变化趋势与聚类分析后Hill指数变化趋势基本一致(图 5)。可见, 地下水位在4—6 m范围内, 塔里木河上游物种多样性明显锐减。此阶段由于地下水位较深且长年缺乏洪水的补给而逐年降低, 地下水位超过了草本植物的耐受限度造成草本植物死亡;继而致使耐旱性差的半灌木和灌木逐渐衰退并消失, 使胡杨群落物种种类和数量骤减、多样性降低。可以预见地下水位>6 m, 塔里木河上游植物群落退化为稀疏衰败的胡杨+柽柳或单优柽柳群落, 这与野外调查结果一致。
|
| 图 5 塔里木河上游Hill多样性对地下水位梯度的响应 Fig. 5 The response of Hill species diversity to groundwater level in the upper reaches of Tarim river |
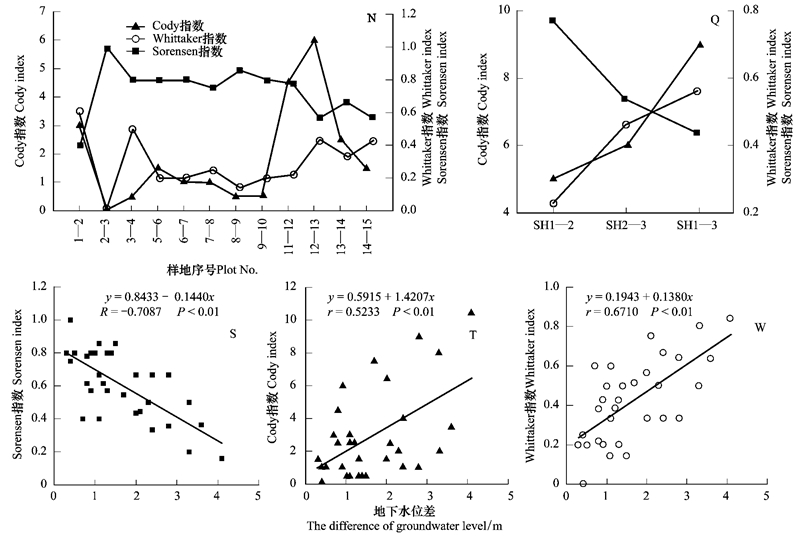
图 6可见, 胡杨群落Cody(βc)和Whittaker(βw)指数随相邻样地间生境异质性增大而增大, Sorensen(βs)指数则随之降低(图 6)。聚类后的相邻样地间βs值均大于非相邻样地间βs值, βs最大值出现在样地H1与H2(SH1-2)之间(图 6), 说明地下水位<4 m胡杨群落结构与物种组成相似, 共有种较多;随地下水位降低, βs值随之下降, 样地H2与H3(SH2-3)、H1与H3(SH1-3)间的βs值分别比SH1-2降低了30.31%、43.38%, 表明地下水位>4 m, H3样地物种多样性与共有种明显降低, 群落层次结构简单化, 胡杨种群特征变化较大(表 1);此水位正是中生浅根系灌、草植物迅速退出群落的临界区域, 也是由中生植物向中旱生-旱生植物演化的区域。聚类后的βc、βw均随着地下水位梯度递增呈逐渐增大趋势, 且非相邻样地间βc、βw值大于相邻样地间, βc、βw最大值均出现在样地H1与H3(SH1-3), SH2-3与SH1-3的βc、βw值分别比SH1-2增大了20%、80%和103.04%、147.47%(图 6), 不同生境间物种变化速率较快, 生境异质性显著增强。βs、βc、βw与地下水位高差之间均呈极显著相关(P<0.01) (图 6S、T、W), 表明随地下水位降低, 胡杨群落层次结构与种类组成差异性增大, 共有种和物种多样性显著减少, 物种旱生化, 植株稀疏, 群落逆行演替至以生态幅宽、抗旱性强的深根性乔灌物种(胡杨/柽柳), 这与刘加珍等[22]研究结果相似。
|
| 图 6 胡杨群落β多样性指数沿地下水位梯度的变化 Fig. 6 The dynamics of β diversity index of P.euphratica along the groundwater level gradients SH1-2表示样地H1与样地H2间的指数计算, 其它类推 |
塔里木河流域两岸分布着经长期自然演替形成以胡杨为优势种的荒漠河岸林, 其依水而生, 无水而亡是植被发生发展的典型特征。受全球气候变暖、径流量逐年减少和人类社会经济活动对流域水资源时空分布的改变, 使植物群落发展长期停留在演替早期阶段, 由于乔灌草物种之间的依存性较弱, 胡杨种群在群落中的优势地位未发生动摇。随地下水位持续降低, 胡杨群落结构简化、物种多样性降低、优势种群稀疏与长势衰败, 反映出极端干旱区地下水位是限制荒漠植被分布与生存的关键生态因子。学者研究指出地下水位持续降低和立地条件干化是引起塔里木河流域优势种群衰败与植被退化的主导因子[1-5, 20-23]。然而, 干旱区植被演变与地下水位变化之间存在着复杂的关系, 植物群落、物种多样性变化与地下水位的定量关系及合理地下水位的确定均涉及到地下水、土壤、植被等相互之间的动态平衡[1-2, 4, 23]。因此, 学者分别从荒漠植被数量特征、植物生理生态、地下水水质对地下水位的响应;物种生态位与分布频率、潜水蒸发与土壤盐渍化及荒漠化的关系等方面[2-4, 6, 9, 20-26]来探索研究干旱荒漠区植被合理生态水位。陈亚宁等指出胡杨、柽柳生存的合理生态水位应<4 m, 临界地下水位为9 m左右[3]。郝兴明等[2, 4, 23]、庄丽等[24]、张丽等[25]、袁素芬等[26]指出塔里木河下游地下水埋深>6 m植被盖度小于20%, 柽柳生物量最大值在地下水埋深4.52 m以内, >7 m其生物量较小;植物生长和维持较高物种多样性的适宜地下水位在2—4 m, 植被正常生长开始受到胁迫和物种多样性受损的临界地下水位为6 m。陈永金等[9]指出塔里木河下游能维持较好水质并抑制荒漠化发展的合理生态水位为5 m。樊自立等[21]研究指出地下水埋深大于2 m时, 土壤积盐微弱;埋深4—6m时植被生长受抑, 确定荒漠植被生存适宜生态水位在2—4 m。徐海量等[20]把既能减少地下水强烈蒸发返盐, 又不造成土壤干旱而影响植物生长的合理生态水位作为评价标准, 确定塔里木河下游合理生态水位为3.5—5 m。Lamontagne等[27]指出澳大利亚Daly河流域的河岸林植被适宜生态水位 < 5 m。综上所述, 塔里木荒漠河岸林植被合理生态地下水位应保持在2—4 m, 利于植被生长和生态环境恢复[25]。这一结果与流域生态输水工程实施后发现地下水埋深2—5 m时植被恢复状况良好[9, 20]基本一致。本文从植物群落物种多样性、优势种群数量特征与地下水位的定量分析, 表明塔里木河上游不同地下水位的胡杨群落大致可划分为3类, 随地下水位降低, 胡杨群落结构简化、物种多样性下降, 当地下水位在4—6 m时, 物种多样性锐减, β多样性急剧增大, 物种变化速率加快, 生境异质性显著增大;地下水位在2—4 m时, 群落相似性与共有种较高。可见, 4 m是物种多样性开始受损与群落结构简化的地下水位。同时优势种胡杨种群密度、冠幅、盖度与生长势下降, 死亡率增大, 种群结构由增长型演化为衰退型, 林分由幼龄林逐渐转变为成过熟林。当地下水位4—4.5m时, 优势种胡杨种群冠幅、平均胸径最大;此时群落盖度>30%, 林分郁闭度>0.25, 远大于20%的荒漠化临界盖度。而当地下水位在6—6.5m, 群落盖度<20%与林分郁闭度<0.1, 此时林相衰败、群落退化与荒漠化突显, 这与徐海量等[20]报道塔里木河下游地下水位在5.83—7.46 m时, 植被大片衰败与盖度<15%相似。进一步分析胡杨数量特征与地下水位的关系, 发现胡杨种群生存的地下水位阈值为7—8 m。徐海量等[20]曾报道塔里木河下游地下水位在7.35—8.57 m时, 植被大片枯死与活植被盖度仅为2%;且这一水位仅能满足尚存的个别深根系植被救命之用, 无法实现自然植被的生态恢复。因此, 塔里木河上游胡杨群落维持较高物种多样性和优势种正常生长的合理生态水位在4 m左右, 地下水位>6 m胡杨群落衰败、物种多样性锐减, 优势种长势衰弱, 此地下水位可视为维持荒漠河岸林稳定的临界水位。从区域植被恢复与生态环境改善角度出发, 塔里木荒漠河岸林植被恢复的合理生态地下水位在4 m左右, 保持荒漠河岸林稳定的地下水位应 < 6 m, 这与学者研究结果[2, 3, 4, 6, 20-21, 23-26]基本一致。
5 结论(1) 塔里木河上游不同地下水位的胡杨群落划归为地下水位<2 m, 2—4 m和4—6 m的3类群落。随地下水位梯度降低, 荒漠河岸林群落层次结构简单化与物种组成差异性增大, 物种多样性降低, 优势种胡杨密度、冠幅、盖度与长势下降, 死亡率增大, 种群结构由增长型演化为衰退型, 林分由幼龄林逐渐转变为成过熟林。地下水位降低是导致优势种群衰退和群落衰败的主导因子。
(2) 塔里木河上游荒漠河岸林物种多样性开始受损的地下水位为4.0 m;地下水位6 m左右, 植物群落明显退化, 优势种群稀疏衰败。胡杨种群适宜生存地下水位<4 m, 地下水位阈值在7—8 m。
(3) 塔里木荒漠河岸林植被恢复的合理生态地下水位在4 m左右。
| [1] | 陈亚宁, 李卫红, 徐海量, 刘加珍, 张宏峰, 陈亚鹏. 塔里木河下游地下水位对植被的影响. 地理学报, 2003, 58(4): 542–549. DOI:10.11821/xb200304008 |
| [2] | 郝兴明, 李卫红, 陈亚宁. 新疆塔里木河下游荒漠河岸(林)植被合理生态水位. 植物生态学报, 2008, 32(4): 838–847. |
| [3] | 陈亚宁, 王强, 李卫红, 阮晓, 陈亚鹏, 张丽华. 植被生理生态学数据表征的合理地下水位研究——以塔里木河下游生态恢复过程为例. 科学通报, 2006, 51(S1): 7–13. |
| [4] | 郝兴明, 陈亚宁, 李卫红. 新疆塔里木河下游物种多样性与地下水位的关系. 生态学报, 2007, 27(10): 4106–4112. DOI:10.3321/j.issn:1000-0933.2007.10.018 |
| [5] | 宋郁东, 樊自立, 雷志栋, 张发旺. 中国塔里木河水资源与生态问题研究. 乌鲁木齐: 新疆人民出版社, 2000. |
| [6] | 陈亚宁, 陈亚鹏, 李卫红, 张宏锋. 塔里木河下游胡杨脯氨酸累积对地下水位变化的响应. 科学通报, 2003, 48(9): 958–961. |
| [7] | 张惠昌. 干旱区地下水生态平衡埋深. 勘察科学技术, 1992(6): 9–13. |
| [8] | 杨泽元, 王文科. 干旱半干旱区地下水引起的生态效应的研究现状与发展趋势. 干旱区地理, 2009, 32(5): 739–745. |
| [9] | 陈永金, 陈亚宁, 李卫红, 刘加珍. 塔里木河下游输水条件下浅层地下水化学特征变化与合理生态水位探讨. 自然科学进展, 2006, 16(9): 1130–1137. |
| [10] | 韩路, 王家强, 王海珍, 宇振荣. 塔里木河上游胡杨种群结构与动态. 生态学报, 2014, 34(16): 4640–4651. |
| [11] | 古丽加米拉木·买买提, 玉米提·哈力克, 塔依尔江·艾山, 王金山. 胡杨树冠疏失度对塔里木河下游应急生态输水的响应. 新疆农业科学, 2010, 47(2): 241–245. DOI:10.6048/j.issn.1001-4330.2010.02.006 |
| [12] | 马建新, 陈亚宁, 李卫红, 黄湘, 朱成刚, 马晓东. 胡杨液流对地下水埋深变化的响应. 植物生态学报, 2010, 34(8): 915–923. |
| [13] | 李先琨, 苏宗明, 向悟生, 宁世江, 唐润琴, 欧祖兰, 李瑞棠. 濒危植物元宝山冷杉种群结构与分布格局. 生态学报, 2002, 22(12): 2246–2253. DOI:10.3321/j.issn:1000-0933.2002.12.031 |
| [14] | Frost I, Rydin H. Spatial pattern and size distribution of the animal-dispersed tree Quercus robur in two spruce-dominated forests. Ecoscience, 2000, 7(1): 38–44. DOI:10.1080/11956860.2000.11682569 |
| [15] | 张金屯. 数量生态学. 北京: 科学出版社, 2004. |
| [16] | 马克平, 刘灿然, 刘玉明. 生物群落多样性的测度方法Ⅱ. β多样性的测度方法. 生物多样性, 1995, 3(1): 38–43. |
| [17] | 赵淑清, 方精云, 宗占江, 朱彪, 沈海花. 长白山北坡植物群落组成、结构及物种多样性的垂直分布. 生物多样性, 2004, 12(1): 164–173. |
| [18] | Gregory S V, Swanson F J, McKee W A, Cummins K W. An ecosystem perspective of riparian zones. BioScience, 1991, 41(8): 540–551. DOI:10.2307/1311607 |
| [19] | Gries D, Zeng F, Foetzki A, Arndt S K, Bruelheide H, Thomas F M, Zhang X, Runge M. Growth and water relations of Tamarix ramosissima and Populus euphratica on Taklamakan desert dunes in relation to depth to a permanent water table. Plant, Cell & Environment, 2003, 26(5): 725–736. |
| [20] | 徐海量, 宋郁东, 陈亚宁. 生态输水后塔里木河下游合理水位探讨. 水土保持通报, 2003, 23(5): 22–25. |
| [21] | 樊自立, 马英杰, 张宏, 王让会, 赵元杰, 周宏飞. 塔里木河流域生态地下水位及其合理深度确定. 干旱区地理, 2004, 27(1): 8–13. |
| [22] | 刘加珍, 陈亚宁, 李卫红, 陈亚鹏. 塔里木河下游植物群落分布与衰退演替趋势分析. 生态学报, 2004, 24(2): 379–383. |
| [23] | 郝兴明, 陈亚宁, 李卫红, 赵锐锋, 朱成刚. 塔里木河中下游荒漠河岸林植被对地下水埋深变化的响应. 地理学报, 2008, 63(11): 1123–1130. DOI:10.3321/j.issn:0375-5444.2008.11.001 |
| [24] | 庄丽, 陈亚宁. 塔里木河下游干旱胁迫条件下柽柳生理代谢的响应. 科学通报, 2006, 51(4): 442–447. |
| [25] | 张丽, 董增川, 黄晓玲. 干旱区典型植物生长与地下水位关系的模型研究. 中国沙漠, 2004, 24(1): 110–113. |
| [26] | 袁素芬, 陈亚宁, 李卫红, 刘加珍, 孟丽红, 张丽华. 新疆塔里木河下游灌丛地上生物量及其空间分布. 生态学报, 2006, 26(6): 1818–1824. |
| [27] | Lamontagne S, Cook P G, O′Grady A, Eamus D. Groundwater use by vegetation in a tropical savanna riparian zone (Daly River, Australia). Journal of Hydrology, 2005, 310(1/4): 280–293. |
 2017, Vol. 37
2017, Vol. 37