文章信息
- 张舒怡, 何雪宝, 王建军, 林和山, 黄雅琴, 林俊辉, 牟剑锋, 刘坤, 郑成兴
- ZHANG Shuyi, HE Xuebao, WANG Jianjun, LIN Heshan, HUANG Yaqin, LIN Junhui, MOU Jianfeng, LIU Kun, ZHENG Chengxing.
- 福建洛阳河口潮间带大型底栖甲壳动物群落及其功能群研究
- Characteristics of the benthic crustacean community structures and functional groups around the Luoyang Estuary in Fujian
- 生态学报. 2017, 37(18): 5961-5972
- Acta Ecologica Sinica. 2017, 37(18): 5961-5972
- http://dx.doi.org/10.5846/stxb201607011353
-
文章历史
- 收稿日期: 2016-07-01
- 网络出版日期: 2017-04-25
河口潮间带的湿地生态系统作为一种典型的群落交错区, 是由生活于其中的动物、植物、微生物以及非生物环境构成, 在支撑着与其临近的陆域和海域生命系统的平衡起着特殊作用[1]。大型底栖动物是生态系统物质循环、能量流动的消费者和转移者[2], 它们通过摄食、掘穴以及排泄等活动与周围环境相互影响[3]。其群落结构和功能群组成能综合反映与环境的关系, 有利于从整体上对河口生态系统的结构和功能进行评估。根据食物来源、摄食结构等可将底栖动物分为多种不同的摄食功能群;根据运动能力及栖息方式等可分为多种生活型功能群。功能群的组成及其间相互作用对群落生产力及其稳定性具有重要作用, 是生境梯度及环境质量的综合反映[4-5]。
底栖甲壳动物是河口潮间带生态系统的重要组成部分, 往往被作为优势类群进行讨论分析, 底栖甲壳动物自由活动能力强, 广泛分布在各个潮区。泉州洛阳河口潮间带湿地生态系统存在多种不同类型的生境, 如红树林、林缘光滩、光滩等生境, 栖息着丰富的底栖甲壳动物。各种类型生境相互交错, 不同生境转换区往往存在明显的生境过渡带, 栖息在该区域的生物常存在边缘效应, 使得该过渡带区域群落结构特征具有明显的特殊性[6], 其在研究生物多样性保护和管理方面具有特殊地位和重要意义。目前有关泉州洛阳河口潮间带湿地生态系统底栖动物研究主要关注于红树林生境(包括不同年份间)[7-10]、米草生境和光滩生境底栖动物群落结构及物种多样性[11-15], 多忽略不同生境间的过渡带。
因此本文选择在洛阳河口潮间带湿地生态系统的人工种植红树林生境、光滩生境和生境过渡带林缘光滩等区域开展底栖甲壳动物群落结构和功能群组成特征的生境间对比、季节对比研究, 分析生境间的边缘效应及季节变化, 探讨红树林湿地生态系统中种植红树林对底栖动物群落恢复作用, 以期为红树林生态系统的修复、生物多样性保护和管理提供数据支撑。
1 材料与方法 1.1 样品采集2013年夏季(8月)、2013年秋季(10月)、2014年冬季(1月)和2014年春季(4月)在洛阳河口潮间带湿地生态系统的中潮区选择5种生境(Q1—Q5) 开展甲壳动物定量调查。生境Q1、Q2、Q3均位于人工种植红树林区内, 但有明显区别, 其中Q1为2002年人工种植秋茄红树林生境;生境Q2种植年限与Q1相同, 但采样站位附近为养虾池和水闸淡水汇入的潮沟;Q3生境是靠近米草区的秋茄与桐花树混合生长的红树林, 平均林高明显低于Q1和Q2, 林间间隙较大。Q4生境位于无植被覆盖的光滩。Q5生境为红树林边缘的林缘光滩, 采样站位位于生境Q1、Q2、Q3人工种植红树林区外光滩, 距红树林边缘5—10 m。各生境均设置3个采样站, 分别位于中潮区3个潮层中, 但各潮层潮高差别不大;每个站设置3个平行样, 每个平行样采样面积为25 cm×25 cm, 采样深度30 cm, 平行样间距控制在3 m范围以内。
将样品放入“WSB1”型底栖生物涡旋分选器淘洗, 再经网目孔径为0.5 mm的过筛器分选, 将筛网内残渣一起装入标本瓶中, 贴上标签。样品用7%的中性福尔马林溶液进行固定, 带回实验室进行分类鉴定、计数和称量。样品的取样、保存、分离、鉴定和分析按《海洋调查规范》(GB/T12763.6—2007) 执行。
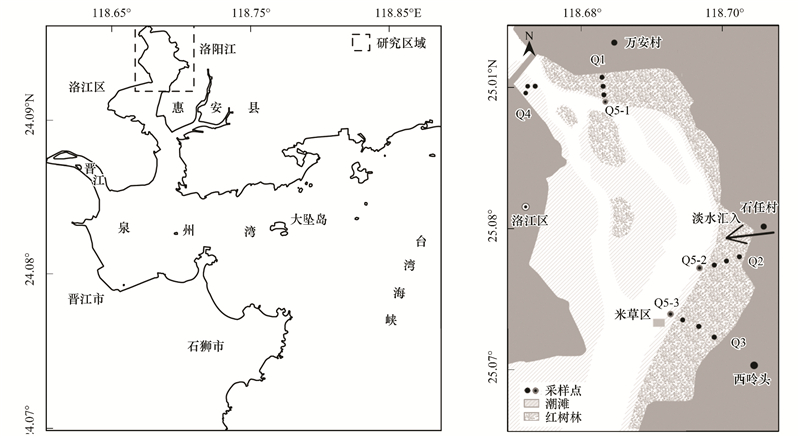
|
| 图 1 研究区域及采样生境示意图 Fig. 1 Study area and sampling sites |
根据大型底栖动物的栖息空间和活动方式, 生活型功能群可分为底上游泳型(Swimming form, Sf)、潜穴型(Infaunal form, If)、穴居型(Caving form, Cf)[16]。
根据底栖动物功能群的食性分类方法文献[17-18], 将底栖动物功能群分为5类:浮游生物食者(Planktophagous group, Pl)、植食者(Phytophagous group, Ph)、肉食者(Camivorous group, C)、杂食者(Omnivorous group, O)、碎屑食者(Detritivorous group, D)。
1.3 数据分析应用PRIMER软件包计算Shannon-Wiener物种多样性指数(H′)、Pielou物种均匀度指数(J′)和Margalef物种丰富度指数(D)。
指数具体计算公式如下:
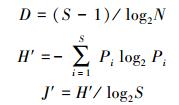
|
式中,S为样品中的种类总数, N为总个体数, Pi为第i种的个体数与总个体数的比值。
优势种选用Pinkas(1971) 提出的相对重要指数IRI[19], 其中IRI值>1000为优势种;IRI值介于100—1000为重要种;IRI值介于10—100为常见种, IRI值 < 10为少见种[20]。
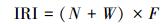
|
式中,N为某一种类的个数占总个数的百分比(%), W为某一种类的生物量占总生物量的百分比(%), F为某一种类出现的频率(%)。
运用SPSS19.0软件进行重复双因素方差分析不同生境和不同季节物种数、栖息密度和生物量、多样性指数间的差异。
利用组平均连接法构建基于Bray-Curtis相似系数的相似性矩阵进行非度量多维度标序nMDS(non-metric Multi-Dimensional Scaling)分析群落结构相似性。
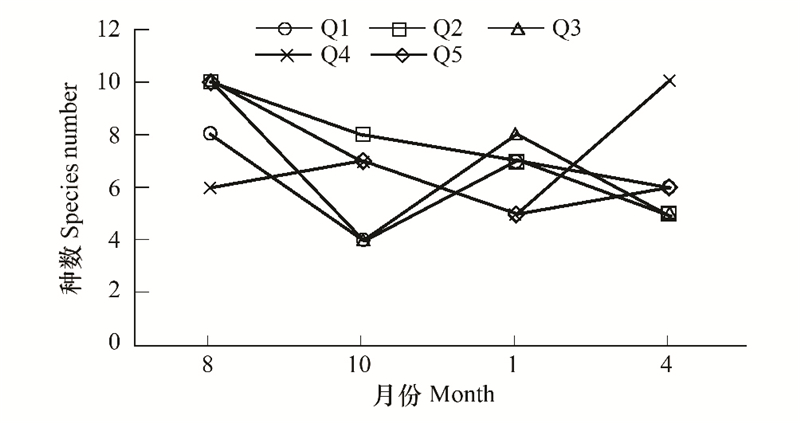
2 结果分析 2.1 不同生境间底栖甲壳动物种类组成变化及优势种分布调查共获得底栖甲壳动物18科35种(附表 1, 图 2)。双因素方差分析表明, 底栖甲壳动物的物种数在不同季节间存在显著差异(F=4.19, P < 0.05), 不同生境间存在极显著差异(F=8.77, P < 0.01), 但在不同季节不同生境间差异不显著(P>0.05), 各生境不同潮层站位间差异不显著(P>0.05), 红树林生境Q1、Q2、Q3的物种数在不同季节不同潮层站位间差异不显著(P>0.05)。
| 种名Species | 相对重要指数 Index of relative importance (IRI) |
摄食功能群 (Functional feeding group) |
生活型功能群 (Life form-functional group) |
||||
| Q1 | Q2 | Q3 | Q4 | Q5 | |||
| 弧边招潮Uca arcuata | 2623.95** | 531.89* | 2111.56** | 787.52* | 4594.48** | Ph | Cf |
| 薄片蜾蠃蜚Sinocorophium lamellatum | 24.18 | 13.75 | 11.87 | 964.91* | 143.23* | Pl | Cf |
| 宁波泥蟹Ilyoplax ningpoensis | 0 | 0 | 0.872 | 1950.89** | 16.39 | Ph | Cf |
| 秀丽长方蟹Metaplax elegans | 297.64* | 238.42* | 2196.19** | 27.18 | 459.37* | Ph | Cf |
| 褶痕拟相手蟹 Parasesarma plicata | 389.39* | 977.80* | 42.89 | 0 | 6.52 | O | Cf |
| 长足长方蟹Metaplax longipes | 2.57 | 155.83* | 11.84 | 48.75 | 84.74 | Ph | Cf |
| 上野蜾蠃蜚Monocorophium uenoi | 0 | 0 | 7.88 | 79.06 | 0 | Pl | Cf |
| 秉氏厚蟹Helice pingi | 55.10 | 103.36* | 0 | 0 | 72.35 | Ph | Cf |
| 细巧仿对虾Parapenaeopsis tenella | 16.70 | 60.93 | 24.51 | 4.95 | 0 | Pl | Sf |
| 日本美人虾Nihonotrypaea japonica | 79.63 | 19.96 | 21.59 | 0 | 0 | D | Sf |
| 巨指长臂虾Palaemon macrodacttylus | 22.85 | 3.79 | 69.28 | 0 | 0 | O | Sf |
| 双齿近相手蟹Perisesarma bidens | 0 | 19.07 | 10.26 | 0 | 9.31 | O | Cf |
| 日本鼓虾Alpheus japonicus | 10.29 | 8.20 | 0 | 0 | 0 | C | Sf |
| 刺螯鼓虾 Alpheus hoplocheles | 0 | 0 | 12.79 | 0 | 0 | C | Sf |
| 少疣长方蟹Metaplax takahashii | 16.16 | 0 | 0 | 0 | 0 | Ph | Cf |
| **为优势种, *为重要种; 食性功能群:Pl:浮游生物食者;Ph:植食者;C:肉食者;O:杂食者;D:碎屑食者;栖息方式:Sf:游泳型;Cf:穴居型; ; IRI>10 | |||||||
|
| 图 2 甲壳动物物种分布与季节变化 Fig. 2 Distribution and seasonal variation of crustaceans species number at different habitats |
计算35种底栖甲壳动物的IRI值(表 1)显示5种生境的优势种存在变化。穴居型植食者弧边招潮为生境Q1、Q3和Q5的共同优势种, 是生境Q2和Q4的重要种。生境Q4优势种为穴居型植食者宁波泥蟹, 该种类在其它生境优势度低或未采集到。生境Q1、Q2和Q3具有部分相同的重要种, 均以蟹类为主;常见种大部分相同, 主要为游泳型的虾类。Q4和Q5的重要种和常见种与红树林3种生境相差较大, 如薄片蜾蠃蜚、上野蜾蠃蜚等穴居型浮游生物食者主要集中在生境Q4及Q5。
以上分析得出, 光滩Q4优势种、重要种以及常见种有别于其它4种生境, 尤其是优势种分布差异较大。常见种游泳型虾类的摄食功能群包括浮游生物食者、碎屑食者以及杂食者等, 在5种生境中分布明显, 主要分布于红树林3种生境Q1、Q2和Q3中, 在生境Q4、Q5中优势度低或未采集到。端足类等浮游生物食者则在光滩Q4和林缘光滩Q5的优势度较高。
2.2 生物量与栖息密度分布调查区域甲壳动物平均生物量为154.8 g/m2, 平均密度为824个体/m2。双因素方差分析表明, 甲壳动物生物量在不同生境间差异不显著(F=1.84, P>0.05), 但不同季节间差异显著(F=3.16, P < 0.05)。栖息密度在不同生境和不同季节间差异极显著(F=5.51, P < 0.001)。红树林生境Q1、Q2、Q3的生物量和栖息密度在不同季节不同潮层站位间均差异不显著(P>0.05)。
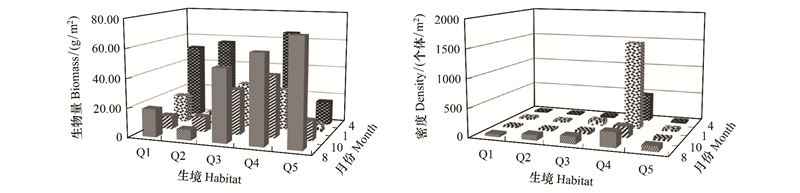
调查区域不同生境甲壳动物平均生物量排序为Q4(49.06 g/m2)>Q3(33.69 g/m2)>Q5(26.87 g/m2)>Q1(24.66 g/m2)>Q2(20.52 g/m2), 平均栖息密度排序为Q4(612个体/m2)>Q3(79个体/m2)>Q5(51个体/m2)>Q2(48个体/m2)>Q1(34个体/m2)。甲壳动物平均生物量季节变化为春季(214.52 g/m2)>夏季(208.04 g/m2)>秋季(105.71 g/m2)>冬季(90.92 g/m2);Q4生物量普遍高于红树林生境Q1、Q2、Q3, 季节变化趋势为春季最高。平均栖息密度季节变化为冬季(1733个体/m2)>夏季(619个体/m2)>春季(590个体/m2)>秋季(356个体/m2);Q4冬季甲壳动物的栖息密度高于其它4种生境各季节栖息密度, 主要是受薄片蜾蠃蜚的栖息密度影响, 生境Q1、Q2、Q3和Q5密度季节变化趋势相近。
|
| 图 3 甲壳动物数量分布及季节变化 Fig. 3 Seasonal variation of crustaceans biomass and density at different habitats |
摄食功能群分析发现, 植食者种数与平均生物量高于其它功能群, 杂食者次之。浮游生物食者和植食者的平均密度高于其它功能群(表 2)。双因素方差分析表明, 甲壳动物各功能群物种数在季节间均差异显著(F=2.142, P < 0.05), 在不同生境间物种数差异极显著(F=7.845, P < 0.001), 其中植食者和浮游生物食者物种数在5种生境间均存在极显著差异(P < 0.001)。各功能群生物量与栖息密度在不同季节间和不同生境间均存在显著差异(P < 0.05), 但生物量在季节-生境双因素间差异不显著(P>0.05)。其中, 植食者和浮游生物食者的生物量和栖息密度在5种生境间均差异显著(P < 0.05)。
| 参数 Parameters |
植食者 Phytophagous group (Ph) |
杂食者 Omnivorous group (O) |
肉食者 Camivorous group (C) |
碎屑食者 Detritivorous group (D) |
浮游生物食者 Planktophagous group (Pl) |
| 种数Species number | 13 | 9 | 4 | 4 | 5 |
| 平均生物量Average biomass/(g/m2) | 132.78 | 12.52 | 2.04 | 4.44 | 3.01 |
| 平均密度Average density/(个体/m2) | 285 | 37 | 4 | 7 | 492 |
各功能群物种数在不同生境间和季节间存在差异, 生境Q1、Q2和Q3在各个季节中功能群组成结构相近, 在生境中季节变化以夏季最高。生境Q5功能群物种数季节变化与Q1、Q2和Q3趋势相近, 但功能群组成较少, 与Q4功能群组成相近。5种生境中甲壳动物摄食功能群均以植食者为主(附表 1, 图 4);不同生境摄食功能群物种数存在差异, 生境Q1、Q2和Q3以植食者为主, 杂食者次之, 3种生境功能群组成结构相近。林缘光滩Q5功能群缺少肉食者和碎屑食者。光滩(Q4) 主要功能群还有浮游生物食者。各功能群生物量和栖息密度在不同生境差异较大, 植食者在各生境的生物量高于其它功能群, 且最高在Q4。栖息密度以Q4浮游生物食者最高, 植食者次之, 其它功能群在各生境栖息密度均不高。

|
| 图 4 甲壳动物各功能群不同生境间物种数、生物量和密度比较 Fig. 4 Functional feeding groups composition, density and biomass of Crustaceans at different habitats |
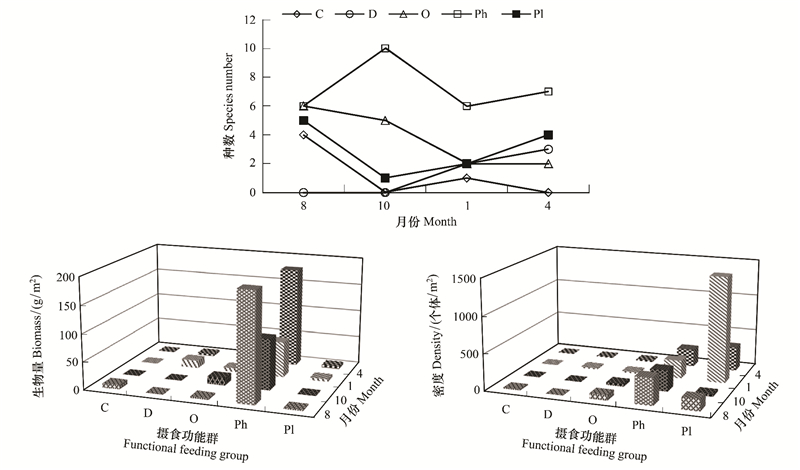
季节变化方面, 植食者在四季的物种数均高于其它四个类别, 除肉食者外, 其余各类别季节变化明显, 肉食者与植食者的季节变化趋势相反。各功能群在不同季节的生物量和栖息密度呈现季节变化规律(图 5), 植食者的生物量和栖息密度在夏季最高, 生物量在四个季节均高于其它功能群, 浮游生物食者栖息密度在冬季最高, 主要是受薄片蜾蠃蜚的影响。
|
| 图 5 甲壳动物各功能群种类数、生物量与密度季节变化 Fig. 5 Seasonal variation of functional feeding groups composition, biomass and density |
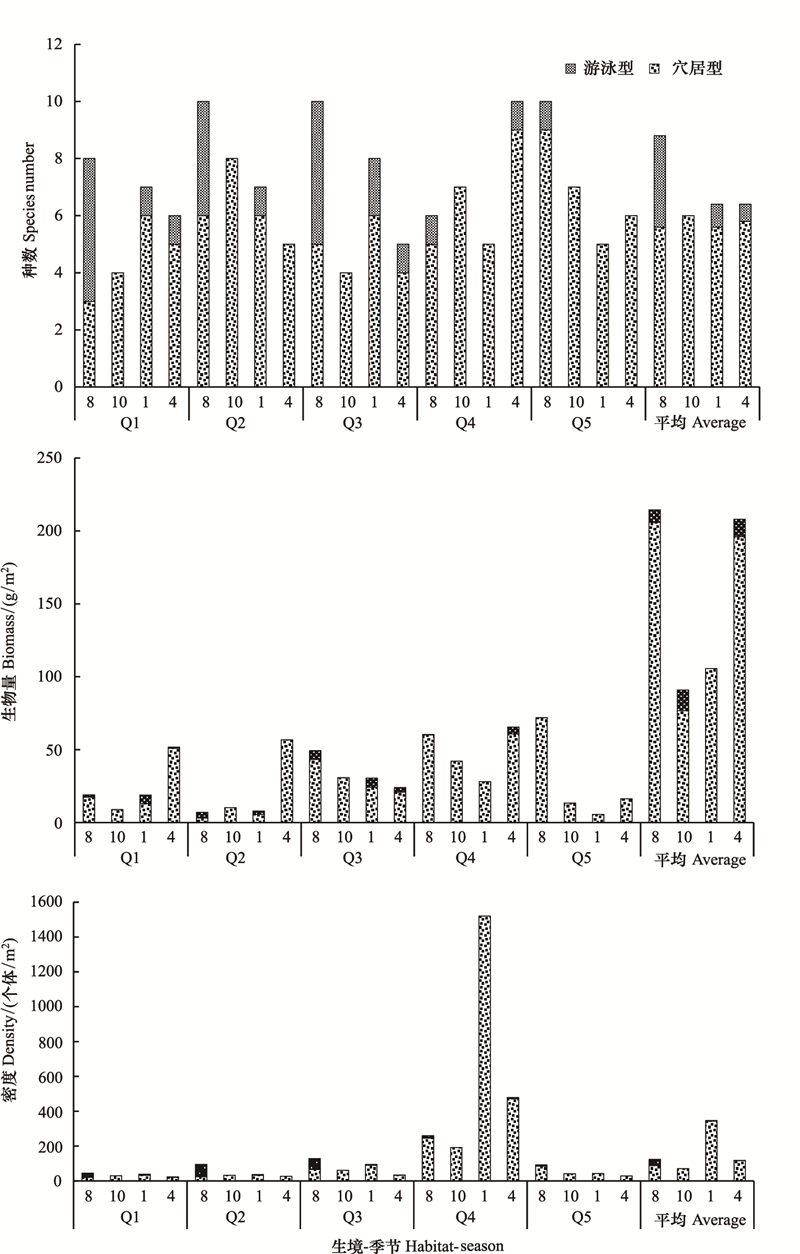
生活型功能群分析发现, 红树林甲壳动物仅存在穴居型和游泳型2种类型, 其中生境Q1—Q3生活型分布类似, 而生境Q4和Q5明显不同于前面3种生境, 主要为穴居型甲壳动物, 游泳型较少(表 3)。季节变化中, 生境Q1、Q2和Q3的生活型功能群除秋季外均有两种, 游泳型功能群在夏季最多, 其余季节物种数较少。秋季生活型功能群仅有穴居型。生境Q4游泳型生物主要分布在夏季和春季, Q5分布在夏季。生物量和栖息密度在不同生境中季节变化差异大, 但都以穴居型甲壳动物占优势图 6。
| 生活型功能群 Life form-functional group |
生境Habitat | ||||
| Q1 | Q2 | Q3 | Q4 | Q5 | |
| 游泳型Sf | 6 | 5 | 6 | 2 | 1 |
| 穴居型Cf | 9 | 13 | 9 | 12 | 12 |
|
| 图 6 甲壳动物各生活型功能群物种数、生物量和密度季节变化 Fig. 6 Seasonal variation of life form-functional groups composition, biomass and density |
底栖甲壳动物各生境物种多样性指数:Margalef种类丰富度(D)、Shannon-Wiener指数(H′)、Pielou均匀度指数(J′)如表 4所示, Q2生境的种类丰度最高。双因素方差分析表明, 不同生境间均匀度指数和多样性存在显著差异(P < 0.05), 季节间差异不显著。丰富度在不同季节不同生境间均差异不显著。
| 参数 Parameters |
月份 Month |
生境Habitat | ||||
| Q1 | Q2 | Q3 | Q4 | Q5 | ||
| Margalef(D)丰富度指数 | 8 | 1.85 | 1.98 | 1.86 | 0.90 | 1.99 |
| Margalef species richness index | 10 | 0.88 | 2.02 | 0.73 | 1.14 | 1.62 |
| 1 | 1.64 | 1.66 | 1.54 | 0.55 | 1.07 | |
| 4 | 1.59 | 1.22 | 1.14 | 1.46 | 1.49 | |
| 平均值 | 1.49 | 1.72 | 1.32 | 1.01 | 1.54 | |
| Shannon-Wiener(H′)多样性指数 | 8 | 2.79 | 1.86 | 2.51 | 1.61 | 2.57 |
| Shannon-wiener diversity index | 10 | 1.87 | 2.71 | 1.54 | 1.36 | 2.15 |
| 1 | 2.63 | 2.53 | 1.98 | 0.46 | 1.81 | |
| 4 | 2.04 | 2.04 | 1.97 | 1.96 | 2.53 | |
| 平均值 | 2.33 | 2.28 | 2.00 | 1.35 | 2.27 | |
| Pielou(J′)均匀度指数 | 1 | 0.93 | 0.56 | 0.76 | 0.62 | 0.77 |
| Pielou evenness index | 10 | 0.93 | 0.90 | 0.77 | 0.49 | 0.77 |
| 1 | 0.93 | 0.90 | 0.66 | 0.20 | 0.78 | |
| 4 | 0.79 | 0.88 | 0.85 | 0.59 | 0.98 | |
| 平均值 | 0.90 | 0.81 | 0.76 | 0.47 | 0.82 | |
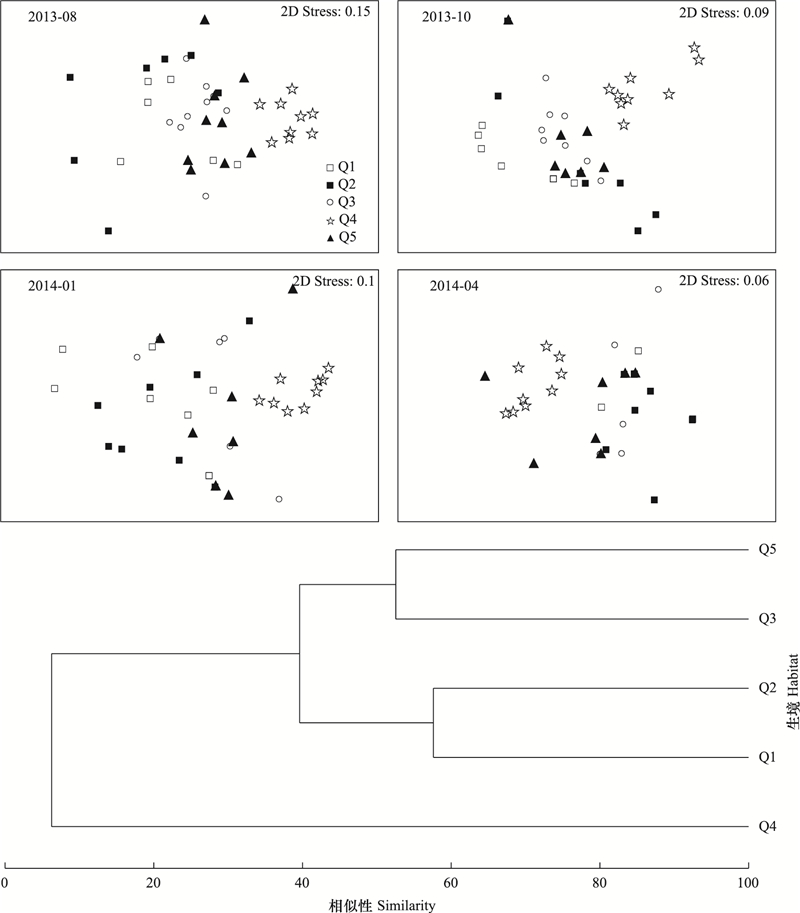
按季节分生境进行非度量多维度标序(MDS)分析显示光滩生境Q4在4个季节明显区别于其它生境, 林缘光滩Q5介于光滩Q4和红树林生境之间, 更靠近红树林区, 与红树林3种生境均存在部分重叠。Bray-Curtis相似系数生境聚类分析也显示Q4明显区别于其它生境, 红树林区Q1与Q2生境相似度高, 但红树林区Q3生境与Q5生境较为相似(图 7)。
|
| 图 7 各生境甲壳动物群落相似性分析和nMDS标序 Fig. 7 Bray-Curtis similarity analysis and Non-metric Multi-Dimensional Scaling of crustaceans community at different habitats |
将5种生境进行比较, 林缘光滩相比光滩生境与红树林生境的相似度更高, 光滩生境明显区分于其它生境。林缘光滩的物种多样性, 功能群组成等都比光滩高, 生物量与栖息密度低于光滩。底栖甲壳动物物种多样性及均匀度指数受生境影响显著, 红树林生境(Q1、Q2、Q3) 与林缘光滩(Q5) 高于光滩生境。生境过渡带林缘光滩在一定程度上会受到林区的影响, 介于红树林生境及光滩生境之间。目前研究讨论的红树林大型底栖动物在不同生境中的多样性水平在世界各地并不一致, 1983年Wells的研究表明, 在与红树林毗邻的泥滩的大型底栖动物种类与栖息密度高于红树林区[21], 国内2004年九龙江口红树林的调查[22]及2010年漩门湾[23]调查结果也显示, 光滩甲壳动物种类数高于红树林区。而本次调查则与1997年Sheridan[24]和2013年陈光程[25]的研究结果相一致, 结果显示红树林区3种生境的甲壳动物物种多样性高于林缘光滩和光滩等无植被覆盖的两种生境(Q2>Q1、Q3>Q4>Q5)
4.2 季节变化与底栖甲壳动物群落结构和功能群底栖甲壳动物的物种数和栖息密度在季节变化间差异显著, 物种数以夏季最高, 红树林生境物种数季节变化与林缘光滩生境变化趋势相似。栖息密度以冬季最高, 季节间优势种存在差异, 主要受优势种小型端足类薄片蜾蠃蜚栖息密度的影响。生物量季节变化间差异不显著, 以春季最高。底栖动物数量季节变化可能与环境参数季节变化以及底栖动物自身生理繁殖特性等因素相关, 季节间栖息密度和生物量的变动是各优势种类数量季节变动的叠加结果[26]。摄食功能群季节变化间差异显著, 以植食者为主, 肉食者与植食者季节变化趋势相反, 摄食功能群种类及栖息密度均以夏季最高, 冬季则以浮游生物食者为主。生活型功能群以穴居型为主, 游泳型功能群在秋季未出现, 种类数及栖息密度也以夏季最高。红树林凋落物直接或间接为红树林生态系统与邻近系统的底栖甲壳动物提供食物来源[27], 有关研究表明[28], 秋茄红树林的凋落物在夏季最高, 冬季最低, 这与本文研究的功能群的季节种类组成及变化趋势相符合, 表明季节变化从影响环境与食物来源等进而影响底栖甲壳动物的群落结构和功能群组成。
4.3 底栖甲壳动物群落和功能群的主要影响因素大型底栖甲壳动物群落分布与温度、盐度、底质和植被等因素密切相关[29], 种植红树林会改变林内的土壤性质, 如盐度、酸度和营养元素的含量[25], 复杂生境为大型底栖动物尤其是甲壳动物提供了适宜的栖息环境, 本文5种生境的主要差别在于植被覆盖、食物来源与类型、底质及周边环境等。相比林缘光滩和光滩两种生境, 红树林具有丰富的食物来源和较高的生产力, 但其植株间的间隙及发达的根系会影响潜穴型甲壳动物的栖息[16]。这一因素可能是形成红树林区3种生境内获得的甲壳动物生物量和栖息密度均低于光滩和林缘光滩两种生境, 且光滩高于林缘光滩的原因。穴居型甲壳动物在光滩及林缘光滩的优势度相对较高, 这与2010年黄雅琴[10]、2012年李海宏等[30]对红树林生境与光滩生境的研究结果一致。由此可见, 生境间的植被差异是造成大型底栖甲壳动物丰度及分布差异的原因之一。
有研究表明[31]生境与大型底栖动物功能群的组成结构存在一定的关系, 生境中底栖甲壳动物功能群的相似性与生境的相似性有关。植被类型、覆盖度以及初级生产力的高低将影响底栖动物功能群的分布。5种生境都以穴居型植食者为主要优势种, 红树林区生境Q1、Q2和Q3摄食功能群与生活型功能群类型多样化均高于光滩与林缘光滩, 可看出生境复杂程度影响功能群的组成结构, 生境越复杂, 功能群类型更趋于多样化。季节与生境双因素下会对底栖甲壳动物功能群组成造成差异, 在优势种比较中, 差异更为显著。因此生境的变换会导致优势种的改变进而影响底栖甲壳动物的群落结构和功能群组成。
结合上述观点,生境过渡带林缘光滩可作为红树林区底栖甲壳动物栖息的缓冲区间, 对修复红树林等具有重要作用, 红树林生境相较于光滩生境对底栖甲壳动物群落多样性的恢复作用高。生境差异性和季节变化是影响底栖甲壳动物分布及组成的重要因素。
| [1] | 陆健健, 王伟. 湿地生态恢复. 湿地科学与管理, 2007, 3(1): 34–35. |
| [2] | 王友绍. 红树林生态系统评价与修复技术. 北京: 科学出版社, 2013. |
| [3] | Dauer D M. Biological criteria, environmental health and estuarine macrobenthic community structure. Marine Pollution Bulletin, 1993, 26(5): 249–257. DOI:10.1016/0025-326X(93)90063-P |
| [4] | 尤仲杰, 陶磊, 焦海峰, 施慧雄, 楼丹. 象山港大型底栖动物功能群研究. 海洋与湖沼, 2011, 42(3): 431–435. DOI:10.11693/hyhz201103015015 |
| [5] | 魏德重, 项长友, 鲍毅新, 李良峰, 章书声. 红树林种植对大型底栖动物群落结构及功能群的影响. 浙江师范大学学报:自然科学版, 2012, 35(2): 195–202. |
| [6] | 邓文洪, 高玮. 温带次生林的岛屿化对鸟类物种多样性及密度的影响. 生物多样性, 2005, 13(3): 204–212. |
| [7] | 卓异, 蔡立哲, 郭涛, 傅素晶, 陈昕韡, 吴辰. 泉州湾蟳埔潮间带大型底栖动物群落的时空分布. 生态学报, 2014, 34(5): 1244–1252. |
| [8] | 李想, 蔡立哲, 卓异, 郭涛, 饶义勇, 颜露露, 傅素晶, 陈昕韡. 泉州湾蟳埔潮间带大型底栖动物功能群研究. 海洋通报, 2014, 33(5): 497–504. DOI:10.11840/j.issn.1001-6392.2014.05.003 |
| [9] | 郭涛, 蔡立哲, 卓异, 饶义勇, 李想, 陈昕韡, 傅素晶, 纪剑锋. 泉州湾洛阳江口2种红树林生境大型底栖动物群落多样性比较. 应用海洋学学报, 2014, 33(2): 204–211. |
| [10] | 黄雅琴. 洛阳江红树林自然保护区大型底栖动物多样性研究[D]. 厦门: 国家海洋局第三海洋研究所, 2010: 90. |
| [11] | 郭涛. 泉州湾红树林和盐沼湿地大型底栖动物群落生态环境效应研究[D]. 厦门: 厦门大学, 2014: 136. |
| [12] | 李伟, 崔丽娟, 王义飞, 张曼胤. 福建洛阳江口红树林湿地恢复对蟹类密度的影响. 生态环境学报, 2010, 19(12): 2929–2933. DOI:10.3969/j.issn.1674-5906.2010.12.028 |
| [13] | 谢进金. 福建泉州湾河口湿地潮间带贝类调查. 泉州师范学院学报, 2002, 20(6): 66–70. |
| [14] | 张雅芝, 陈灿忠, 王渊源, 陈品健, 杨瑞琼. 福建红树林区底栖生物生态研究. 生态学报, 1999, 19(6): 896–901. |
| [15] | Alfaro A C. Benthic macro-invertebrate community composition within a mangrove/seagrass estuary in northern New Zealand. Estuarine, Coastal and Shelf Science, 2006, 66(1/2): 97–110. |
| [16] | 胡成业, 水玉跃, 田阔, 张春草, 覃胡林, 冀萌萌, 水柏年. 瓯江口树排沙湿地不同生境大型底栖动物群落多样性研究. 海洋与湖沼, 2016, 47(2): 422–428. |
| [17] | Grémare A. Feeding, tube-building and particle-size selection in the terebellid polychaete Eupolymnia nebulosa. Marine Biology, 1988, 97(2): 243–252. DOI:10.1007/BF00391309 |
| [18] | Navarro-Barranco C, Tierno-de-Figueroa J M, Guerra-García J M, Sánchez-Tocino L, García-Gómez J C. Feeding habits of amphipods (Crustacea: Malacostraca) from shallow soft bottom communities: comparison between marine caves and open habitats. Journal of Sea Research, 2013, 78: 1–7. DOI:10.1016/j.seares.2012.12.011 |
| [19] | Pinkas L, Oliphant M S, Iverson I L K. Food habits of albacore, bluefin tuna, and bonito in California waters. California Department of Fish and Game Fish Bulletin, 1971, 152: 1–105. |
| [20] | 徐开达, 张洪亮, 谢汉阳, 梁君, 张龙, 朱文斌. 中街山列岛水域甲壳类资源及其群落多样性. 海洋渔业, 2012, 34(3): 308–315. |
| [21] | Wells F E. An analysis of marine invertebrate distributions in a mangrove swamp in northwestern Australia. Bulletin of Marine Science, 1983, 33(3): 736–744. |
| [22] | 洪荣标, 吕小梅, 陈岚, 方少华. 九龙江口红树林湿地与米草湿地的底栖生物. 台湾海峡, 2005, 24(2): 189–194. |
| [23] | 龚堃, 鲍毅新, 任鹏, 方平福, 李海宏, 王华. 漩门湾围垦区外滩涂不同生境大型底栖动物功能群及其变化. 生态学报, 2016, 36(24): 1–10. |
| [24] | Sheridan P. Benthos of adjacent mangrove, seagrass and non-vegetated habitats in Rookery Bay, Florida, U.S.A.. Estuarine, Coastal and Shelf Science, 1997, 44(4): 455–469. DOI:10.1006/ecss.1996.0125 |
| [25] | 陈光程, 余丹, 叶勇, 陈彬. 红树林植被对大型底栖动物群落的影响. 生态学报, 2013, 33(2): 327–336. |
| [26] | 林俊辉, 何雪宝, 王建军, 林和山, 黄雅琴, 刘坤, 牟剑锋, 张舒怡, 江锦祥. 福建洛阳江口红树林湿地大型底栖动物多样性及季节变化. 生物多样性, 2016, 24(7): 791–801. DOI:10.17520/biods.2015328 |
| [27] | 陈光程. 九龙江口秋茄红树植被与主要大型底栖动物某些生态关系的研究[D]. 厦门: 厦门大学, 2009: 153. |
| [28] | 卢昌义, 郑逢中, 林鹏. 九龙江口秋茄红树林群落的掉落物量研究. 厦门大学学报:自然科学版, 1988(4): 459–463. |
| [29] | 寿鹿, 高爱根, 曾江宁, 陈全振, 廖一波, 徐晓群. 底质环境对浙江衢山岛潮间带大型底栖动物分布的影响. 动物学杂志, 2007, 42(3): 79–83. |
| [30] | 李海宏, 江旷, 鲍毅新, 王华, 任鹏. 茅埏岛不同生境大型底栖动物生物多样性. 生态学杂志, 2015, 34(3): 765–772. |
| [31] | 朱晓君, 陆健健. 长江口九段沙潮间带底栖动物的功能群. 动物学研究, 2003, 24(5): 355–361. |
 2017, Vol. 37
2017, Vol. 37