文章信息
- 景涛, 谢会成, 孙居文, 刘浩栋, 李辉
- JING Tao, XIE Huicheng, SUN Juwen, LIU Haodong, LI Hui.
- 向日葵对苯胺废水的光合生理响应及净化效果
- Tolerance and phytoremediation capacity of sunflower exposed to aniline wastewater
- 生态学报. 2017, 37(18): 6091-6098
- Acta Ecologica Sinica. 2017, 37(18): 6091-6098
- http://dx.doi.org/10.5846/stxb201606271259
-
文章历史
- 收稿日期: 2016-06-27
- 网络出版日期: 2017-04-25
苯胺是芳香胺类最具代表性的物质, 是我国水污染中常见的工业污染物, 是印染业、制药业、农业等行业的主要污染物之一。随着这些行业的发展, 排入环境的苯胺逐年增多。排入水中苯胺具有强烈的毒性并抑制水生动植物的生长。苯胺主要通过皮肤、呼吸道和消化道进入人体, 从而破坏血液造成溶血性贫血, 损害肝脏引起中毒性肝炎。为此, 我国将苯胺列入“中国环境优先污染物黑名单”中, 美国EPA也将苯胺列为优先控制的129种污染物之一[1-2]。
相对净化环境中的苯胺常用的物理方法、化学方法和微生物修复方法而言, 植物修复方法不但可以去除污染物, 而且还可以促进污水中营养物质的循环和再利用, 同时还能绿化土地, 改善区域气候, 促进生态环境的良性循环[3]。刘振龙[4]利用冰草(Agropyron cristatum (L.) Gaertn.)对苯胺污染的土壤进行植物修复试验发现, 冰草根系可吸收苯胺, 经过茎秆向叶片和穗中转运;王忠全和温琰茂[5]研究了六种水生植物对含苯胺废水的修复效果, 研究发现, 植物对水体苯胺的修复效率为50.7%—97.3%, 其中以蕹菜(Ipomoea aquatica Forsk)的修复效果最好。
向日葵(Helianthus annuus), 属菊科向日葵属植物, 是一种耐盐碱、耐瘠、耐旱、适应性广的油料作物[6-8]。赵鲁雪等[9]比较了五种植物的土壤铀污染修复效果, 发现向日葵和四季豆(Phaseolus vulgaris L)可以作为铀污染土壤的固持修复植物;美国一些场地使用向日葵来修复放射性核素污染的地下水[10];Xie等[11]的研究揭示, 向日葵对不同种类的偶氮染料废水的耐受性和脱色率差异很大。因此, 向日葵在苯胺废水净化方面有很好的环境适应性基础和修复潜力。向日葵对苯胺的修复及光合生理响应方面的研究还未见报道。本研究以向日葵(美国油葵1号)为材料, 分析了不同浓度的苯胺胁迫对向日葵的生长状态、光合作用和叶绿素荧光参数的影响以及苯胺在向日葵体内的积累情况。试图揭示向日葵对苯胺胁迫的耐受能力和适应机制, 为水体苯胺的植物修复提供科学依据。
1 材料与方法 1.1 试验设计水培试验以美国油葵(Helianthus annuus Linn.)1号为试验材料。选取饱满且大小一致的种子, 经24小时浸泡后, 将种子埋入灭菌的石英砂中, 用去离子水浇灌, 自然条件下发芽。选择生长一致的健壮幼苗, 放于250 mL三角瓶中, 用50%浓度的霍格兰培养液培养五周后, 选择生长一致的植株进行苯胺胁迫处理。
苯胺胁迫处理浓度分别为100、200、300、400、500 mg/L, 对照不含苯胺, 每处理8个重复。自然环境条件下处理7天后, 测定叶片光合参数和植物体内苯胺含量及水体中苯胺含量。
1.2 测定项目与方法 1.2.1 向日葵生物量的测定(鲜重)将向日葵用去离子水洗净, 然后用吸水纸擦干, 称重。
1.2.2 光合生理参数测定在晴朗天气, 选取每一试验植株中部生长健壮成熟叶片3片, 应用英国PPS公司生产的CIRAS-2型光和作用系统, 测定净光合速率(Pn)、蒸腾速率(Tr)、气孔导度(Gs)、胞间二氧化碳浓度(Ci)等光合作用参数, 叶片水分利用效率(WUE)和气孔限制值(Ls)分别用公式计算:WUE=Pn/Tr[12], Ls=1-Ci/Ca[13], 式中Ca为空气CO2浓度。
1.2.3 叶绿素荧光参数测定在自然光下活化30 min后, 使用脉冲调制式荧光系统(FMS 2.02型, 英国Hansatech公司)测定不同苯胺浓度梯度下向日葵叶片初始荧光(Fo)、最大荧光(Fm)、光下最小荧光(Fo′)、光下最大荧光(Fm′)、实际荧光产量(Fs), 按照公式[14-15]计算PSⅡ的最大光化学效率Fv/Fm=(Fm-Fo)/Fm;PSⅡ实际光化学效率ΦPSⅡ=(Fm′-Fs)/Fm′;光化学淬灭系数qP=(Fm′-Fs)/(Fm′-Fo′);非光化学淬灭NPQ=(Fm-Fm′) /Fm′。
1.2.4 苯胺的测定试验结束后, 采取向日葵根、茎、叶样品, 每一器官混合取样, 用蒸馏水洗净, 吸水纸擦干表面水分, 称取样品3 g, 粉碎后放入50 mL离心管中, 加入27 mL甲醇振荡提取24h, 用0.22 μm有机滤膜过滤3次, 得待测样品。水样经过0.22 μm膜进行过滤后得到待测液。使用高效液相色谱仪(water 515, 美国)2478双波长紫外检测器进行样品中的苯胺测定。色谱条件:波长为240 nm, 流动相为甲醇:水(35:65 (体积比)), 流动相pH=3.0, 流速为0.8 mL/min, 进样量为10 μL [16]。每个样品测定3次。
1.3 数据分析采用SPSS 17.0和Excel 2010软件进行数据分析, 平均数采用单因素方差分析(one-way ANOVA), 用DUNCAN进行差异显著性比较。采用Origin 7.5作图。去除率用公式[17]计算:去除率(%)=((初始苯胺浓度-最终苯胺浓度)/初始苯胺浓度)×100。
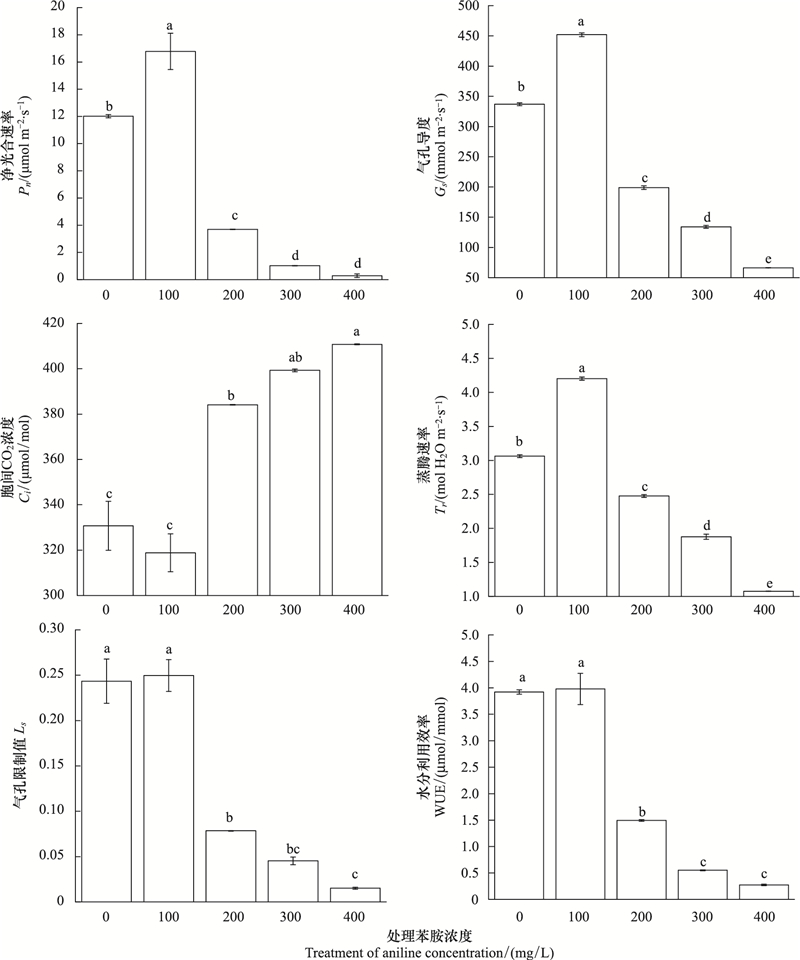
2 结果与分析 2.1 苯胺胁迫对向日葵光合参数的影响随着苯胺浓度的增高, 向日葵叶片的净光合速率(Pn)先升高后下降, 以苯胺浓度为100 mg/L的Pn最高(16.78 μmol CO2m-2s-1), 是对照组的1.40倍(P<0.05)(图 1);当苯胺浓度达到200 mg/L, 向日葵的Pn显著下降(P<0.05);当苯胺浓度达到400 mg/L, Pn仅为对照组的2.41%。表明低浓度苯胺促进向日葵的光合作用, 高浓度苯胺抑制光合作用, 且随着浓度的增高抑制作用增强。利用韦布尔函数模拟了向日葵的净光合速率(Pn)与苯胺浓度(c)的关系, 得到模型: Pn=14.3893×(1-EXP(-((c+63.1496)/220.3939)^-6.5830))。计算得到光合速率减半时的苯胺浓度为182 mg/L。随着苯胺浓度的增高, 向日葵叶片的气孔导度(Gs)、蒸腾速率(Tr)、水分利用效率(WUE)及气孔限制值(Ls)的变化趋势与Pn相同, 均呈现先升高后下降的变化趋势, 且在苯胺浓度为100 mg/L达到最大值。而Ci的变化趋势与Pn相反, 当苯胺浓度大于100 mg/L时, 随着苯胺浓度的增高Ls显著下降而Ci显著上升(P<0.05), 说明向日葵叶片Pn下降的主要原因发生了由气孔因素向非气孔因素的转变。此外, 当苯胺浓度大于100 mg/L时, 向日葵WUE显著低于对照组(P<0.05), 当苯胺浓度达到400 mg/L, WUE仅为对照组的7.01%。
|
| 图 1 苯胺胁迫下向日葵的光合参数(平均值±标准误) Fig. 1 Photosynthetic parameters of sunflowers under aniline stress (means±SE) 不同小写字母表示处理间在0.05水平上差异显著; Pn:净光合速率Net photosynthetic rate; Tr蒸腾速率Transpiration rate; Gs:气孔导度Stomatal conductance; Ci:胞间CO2浓度Intercellular CO2concentration; Ls:气孔限制值Stomatal limitation; WUE:水分利用效率Water use efficiency |
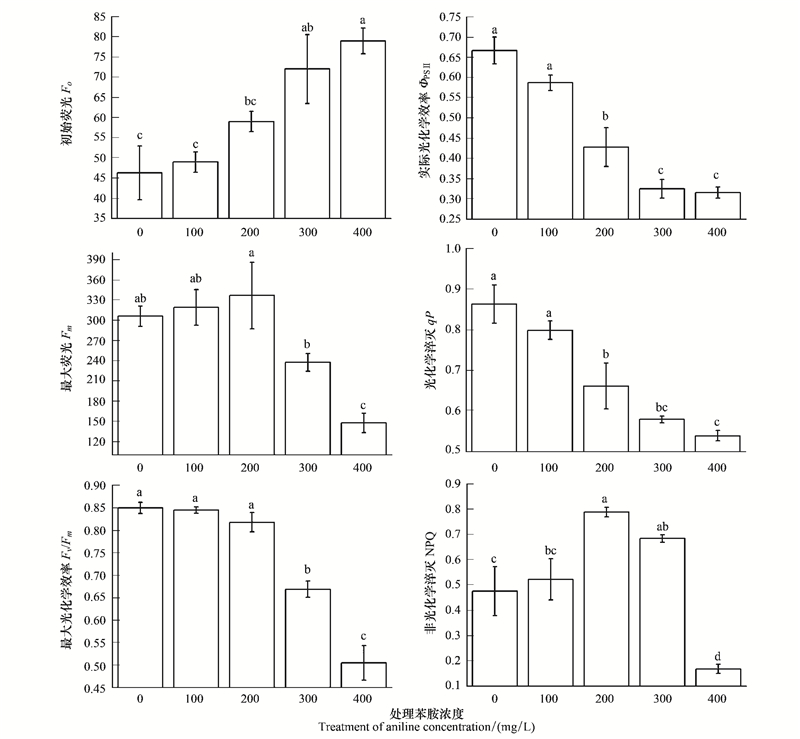
由图 2可以看出, 随着苯胺浓度的升高, 初始荧光(Fo)呈上升趋势, 当苯胺浓度高于200 mg/L后, 试验组Fo显著高于对照组(P<0.05), 表明高浓度苯胺胁迫使PSⅡ反应中心发生破坏或可逆失活[18]。相反地, 随着苯胺浓度的升高, 向日葵PSⅡ最大光化学效率(Fv/Fm)、实际光化学效率(ΦPSⅡ)及光化学淬灭系数(qP)都明显下降, 而非光化学淬灭系数(NPQ)呈现出先升高后下降的趋势, 即在苯胺浓度低于200 mg/L时, 随着苯胺浓度的增加而升高, 在苯胺浓度大于200 mg/L时, 随着苯胺浓度的升高而降低。其中Fv/Fm和ΦPSⅡ降低表明PSⅡ的潜在活性下降, qP的降低说明PSⅡ反应中心的活性降低[19], 表明苯胺胁迫会明显抑制或者降低向日葵叶片的PSⅡ光化学活性和光化学效率。
|
| 图 2 苯胺胁迫下向日葵的荧光参数(平均值±标准误) Fig. 2 Fluorescence parameters of sunflowers under aniline stress (means±SE) 不同小写字母表示处理间在0.05水平差异显著; Fo:初始荧光Minimal fluorescence; Fm:最大荧光Maximal fluorescence; Fv/Fm: PSⅡ最大光化学效率Maximal quantum yield of PSⅡ photochemistry; qP:光化学猝灭系数Photochemical quenching coefficient; NPQ:非光化学猝灭系数Non photochemical quenching; ΦPSⅡ:实际光化学效率Effective quantum yield of PSⅡ photochemistry |
随着苯胺处理浓度的增高, 向日葵生物量显著降低(表 1)。当苯胺处理浓度为200 mg/L时, 向日葵生物量显著低于对照组(P<0.05);当苯胺浓度为400 mg/L时, 生物量降低幅度达28.04%;当苯胺浓度达到500 mg/L时, 向日葵植株死亡, 表明在一周的培养期中, 500 mg/L已达到向日葵最大耐受浓度。
| 水体中的苯胺浓度/(mg/L) Aniline concentration in water |
鲜重差值/g The difference in fresh weight |
去除率/% Removal rate |
植物体中的苯胺浓度/(mg/g) Aniline concentration in plant |
|||
| 试验前 Before the test |
试验后 After the test |
叶 Leaf |
茎 Stem |
根 Root |
||
| 0 | 0 | 2.057 | 0.000 | 0.000 | 0.000 | |
| 100 | 19.032 | 2.680 | 80.968 | 0.027±0.003d | 5.182±0.232a | 0.945±0.098a |
| 200 | 51.617 | -2.530 | 74.192 | 2.750±0.351c | 3.213±0.192b | 0.210±0.048c |
| 300 | 83.283 | -2.867 | 72.239 | 3.953±0.655b | 3.023±0.257b | 0.260±0.020bc |
| 400 | 141.177 | -2.893 | 64.706 | 4.623±0.214b | 3.759±0.366b | 0.385±0.008b |
| 500 | 239.517 | death | 52.097 | 7.092±0.103a | 3.483±0.159b | 0.390±0.008b |
| a, b, c, d分别表示向日葵相同部位不同处理的苯胺含量的差异性比较 | ||||||
向日葵不同器官对苯胺处理的积累具有显著差异(表 1), 在苯胺浓度较低时, 苯胺主要积累在向日葵的茎中;当苯胺浓度为300 mg/L时, 苯胺主要积累在叶中, 积累量随着苯胺浓度的增大而增大。随着苯胺浓度的升高, 向日葵对苯胺的去除率呈现降低趋势, 当苯胺浓度为100 mg/L时, 去除率最高, 达到80.968%。
3 讨论与结论光合作用是植物生长的基础, 而逆境胁迫对植物的光合生理影响较明显。张志刚和尚庆茂[20]研究发现低温、弱光及盐胁迫均能降低辣椒的净光合作用, 且复合逆境的抑制效果大于单一逆境。通常影响植物光合作用的因素可分为气孔因素和非气孔因素, 前者指水分胁迫导致气孔导度下降, CO2进入叶片受阻而使光合下降, 后者指叶肉细胞的光合活性下降[21]。本研究表明(图 1), 当苯胺浓度为100 mg/L时, 向日葵的净光合速率相比于对照组显著升高(P<0.05), 而且其水分利用效率与对照组没有显著差异(P>0.05), 暗示低浓度苯胺对于向日葵正常的生理活动有一定的促进作用。而当苯胺浓度达到或大于200 mg/L时, 苯胺会明显抑制向日葵的光合作用, 其浓度越大抑制能力越强;而且Pn的下降伴随着Ci的上升和Ls的下降, 表明此时光合作用的主要限制因素是非气孔因素[22], 向日葵的光合机构受到损害。李辉等[23]研究发现, 在苯酚浓度较低(50 mg/L)的情况下, 垂柳的净光合作用即出现下降趋势;Xie等[11]表明, 向日葵的净光合作用速率在三种偶氮染料(俾斯麦棕、伊文思蓝、橙黄)浓度为100 mg/L时显著降低。王泽港[24]的研究表明土壤中低浓度的萘(10 mg/kg)提高了水稻的净光合速率, 高浓度则明显抑制, 而相同浓度的1, 2, 4-三氯苯则均能明显抑制水稻的净光合速率。上述研究表明, 有机物对植物的毒性差异很大, 而植物对有机污染胁迫的光合生理响应也表现出了差异性。植物在受到外界胁迫作用时, 其光合作用的限制作用会在气孔限制与非气孔限制之间进行转换, 由此我们推测:在苯胺浓度为100—200 mg/L之间, 可能存在一个临界浓度, 具体临界浓度还待于进一步试验研究。
叶绿素荧光参数在测定植物光合作用过程中光系统对光能的吸收、传递、耗散、分配等方面具有独特的作用[21]。Fo是PSⅡ反应中心全部开放时的荧光水平, PSⅡ反应中心的破坏或可逆性失活则引起Fo的增加[25], 本研究中随着苯胺浓度的增加, Fo也不断增加, 特别是苯胺浓度大于200 mg/L时其与对照的差异达到显著水平, 说明高浓度苯胺可引起PSⅡ反应中心的破坏或可逆性失活(图 2)。Fv/Fm是PSⅡ最大光化学量子产量, 反映了PSⅡ反应中心的光能转化效率[26], 非胁迫条件下该参数变化极小, 不受物种和生长条件的影响, 胁迫条件下明显下降, 在苯胺浓度大于200 mg/L时Fv/Fm与对照的差异达到显著水平(图 2), 说明此时向日葵叶片的光合作用发生了光抑制或PSⅡ系统遭到破坏。ΦPSⅡ反映光下光合机构所吸收的光能用于光化学反应的比例[27]。qP表示PSⅡ反应中心对激发能利用的情况, 其值越高, 说明PSⅡ的电子传递活性越高[28]。本试验显示(图 2), 随着苯胺浓度的上升, qP和ΦPSⅡ均呈现下降趋势, 表明苯胺胁迫会增大PSⅡ反应中心的关闭程度, 光合电子传递速率下降, 用于PSⅡ实际化学反应的光能降低[28]。随着苯胺浓度的升高, NPQ呈现出先升高后降低的趋势, 即在苯胺浓度低于200 mg/L时, 随着苯胺浓度的增加而升高, 但Fo并没有发生显著变化, 表明此时向日葵的光破坏防御机制启动, PSⅡ所吸收的光能用于天线色素热耗散的能量增加, 从而起到了缓解苯胺胁迫对PSⅡ反应中心机构的破坏作用[29];在苯胺浓度大于200 mg/L时, NPQ随着苯胺浓度的升高而降低, 此时Fo显著升高, 表明此时用于天线色素热耗散的能量也降低, 说明高浓度的苯胺可能对紫黄质脱环氧化酶产生了影响, 造成依赖于叶黄素循环的热耗散降低[27], 向日葵的PSⅡ光合系统受到强光明显的损伤。王泽港[24]的研究表明随着土壤中萘和1, 2, 4-三氯苯浓度的升高, NPQ迅速降低, 水稻通过热耗散方式的自我保护机制遭到严重破坏。
试验中通常以植物的死亡率作为有害物质检测的重要指标。本试验中, 虽然苯胺导致的植物死亡率不是很明显, 但是它对向日葵的生长指标和生物量都产生了显著的影响。当水体中苯胺浓度低于100 mg/L时, 向日葵的生物量与对照无显著差异, 表明低浓度苯胺对向日葵的生长影响不大。当苯胺的浓度达到200 mg/L后, 向日葵的生物量显著下降, 但当苯胺浓度继续增大时, 向日葵的生物量不再有明显的变化, 这一试验结果与柏伟荣[30]及温广军[31]的试验结果相似, 表明较高浓度的苯胺(≥200 mg/L)抑制向日葵生长(表 1), 当苯胺浓度达到500 mg/L时, 向日葵死亡, 表明在1周的培养期中, 500 mg/L已达到向日葵最大耐受浓度。水体中的污染物残留可以直观的表现出植物对污染物的富集及去除效果, 而借助植物体中的污染物残留可推测出植物对污染物的降解能力。向日葵对苯胺的去除率与苯胺的浓度有关, 随着苯胺浓度的升高, 向日葵对苯胺的去除率呈现降低趋势, 当苯胺浓度为100 mg/L时, 向日葵对苯胺的去除率最高, 达80.968%, 这与王忠全和温琰茂[5]报道的美人蕉(Canna indica L.)对30 mg/L苯胺的去除效果相似, 但低于蕹菜等植物;Xie等[11]的研究表明, 当偶氮染料浓度为100 mg/L时, 向日葵对其的平均去除率为62.64%, 暗示向日葵对苯胺的去除效果要优于偶氮染料。当苯胺浓度为200 mg/L时, 苯胺主要积累在日葵的茎中;而当苯胺浓度大于200 mg/L时, 苯胺主要积累叶中, 根的苯胺积累量相对较少。而当苯胺浓度为100 mg/L时, 叶片中苯胺含量很低, 根中的含量相比于其他处理反而较高。结合植物的光合及荧光参数, 推测苯胺主要在叶片中进行降解, 水体中苯胺含量越低, 降解能力越强, 而叶片中苯胺的降解又会促进根部对苯胺的吸收。苯胺主要积累在向日葵的地上部分, 因此可以通过收割地上部分而将苯胺从环境中移除。
总之, 低浓度的苯胺胁迫(<100 mg/L)对向日葵的正常生长有一定的促进作用, 向日葵对低浓度苯胺具有较强的富集及降解能力。当苯胺浓度逐渐提高后, 向日葵的光合速率降低, 干物质积累能力下降, 影响向日葵的正常生长。模拟研究显示, 苯胺浓度为182 mg/L时, 净光合速率下降一半, 可以作为利用向日葵净化废水中苯胺浓度的上限。
| [1] | Larry H K, William A T. Priority pollutants: Ⅰ. A perspective view. Environmental Science & Technology, 1979, 13(4): 416–423. |
| [2] | 王孝华. 苯胺废水处理的新进展. 工业水处理, 2010, 30(2): 11–14. DOI:10.11894/1005-829x.2010.30(2).11 |
| [3] | 张晓斌. 植物修复在水环境污染治理中的研究[D]. 浙江: 浙江师范大学, 2007. http://cdmd.cnki.com.cn/Article/CDMD-10345-2007184805.htm |
| [4] | 刘振龙. 硝基苯类和苯胺类污染土壤的植物修复研究[D]. 兰州: 兰州大学, 2012. http://cdmd.cnki.com.cn/Article/CDMD-10730-1014302370.htm |
| [5] | 王忠全, 温琰茂. 水体苯胺、N和P生物修复研究. 农业环境科学学报, 2009, 28(3): 570–574. |
| [6] | 李庆文. 向日葵及其栽培. 北京: 农业出版社, 1991. |
| [7] | 郑青松, 陈刚, 刘玲, 刘兆普, 徐文君. 盐胁迫对油葵种子萌发和幼苗生长及离子吸收、分布的效应. 中国油料作物学报, 2005, 27(1): 60–64. |
| [8] | 唐奇志, 刘兆普, 刘玲, 郑青松, 陈铭达. 海侵地区不同降雨条件下海水灌溉'油葵G101'的研究. 植物生态学报, 2005, 29(6): 1000–1006. |
| [9] | 赵鲁雪, 罗学刚, 唐永金, 彭芳芳, 王丽超. 铀污染环境下植物的光合生理变化及对铀的吸收转移. 安全与环境学报, 2014, 14(2): 299–304. |
| [10] | 蓝俊康. 植物修复技术在污染治理中的应用现状. 地质灾害与环境保护, 2004, 15(1): 46–51. |
| [11] | Xie H C, Li C R, Li J H, Wang L. Phytoremediatgion of wastewater containing azo dye by sunflowers and their photosynthetic response. Acta Ecologica Sinica, 2012, 32(5): 240–243. DOI:10.1016/j.chnaes.2012.07.001 |
| [12] | Nijs I, Ferris R, Blum H, Hendrey G, Impens I. Stomatal regulation in a changing climate: a field study using free air temperature increase (FATI) and free air CO2 enrichment (FACE). Plant, Cell & Environment, 1997, 20(8): 1041–1050. |
| [13] | Berry J A, Downton W J S. Environmental regulation of photosynthesis//Govindjeed. Photosynthesis. Vol. Ⅱ: Development, Carbon Metabolism, and Plant Productivity. New York: Academic Press, 1982. |
| [14] | Krause G H, Weis E. Chlorophyll fluorescence and photosynthesis: the basics. Annual Review of Plant Physiology and Plant Molecular Biology, 1991, 42(1): 313–349. DOI:10.1146/annurev.pp.42.060191.001525 |
| [15] | Roháček K. Chlorophyll fluorescence parameters: the definitions, photosynthetic meaning and mutual relationships. Photosynthetica, 2002, 40(1): 13–29. DOI:10.1023/A:1020125719386 |
| [16] | Qiong J, Hu Z C, Jin Z F, Qiu L Q, Zhong W H, Pan Z Y. Biodegradation of aniline in an alkaline environment by a novel strain of the halophilic bacterium, Dietzia natronolimnaea JQ-AN. Bioresource Technology, 2012, 117: 148–154. DOI:10.1016/j.biortech.2012.04.068 |
| [17] | Khandare R V, Govindwar S P. Phytoremediation of textile dyes and effluents: Current scenario and future prospects. Biotechnology Advance, 2015, 33(8): 1697–1714. DOI:10.1016/j.biotechadv.2015.09.003 |
| [18] | Yamane Y, Kashion Y, Koike H, Satoh K. Increases in the fluorescence Fo level and reversible inhibition of photosystem Ⅱ reaction center by high-temperature treatments in higher plants. Photosynthesis Research, 1997, 52(1): 57–64. DOI:10.1023/A:1005884717655 |
| [19] | Piñol R, Simón E. Effect of 24-epibrassinolide on chlorophyll fluorescence and photosynthetic CO2 assimilation in Vicia faba plants treated with the photosynthesis-inhibiting herbicide terbutryn. Journal of Plant Growth Regulation, 2009, 28(2): 97–105. DOI:10.1007/s00344-008-9077-0 |
| [20] | 张志刚, 尚庆茂. 低温、弱光及盐胁迫下辣椒叶片的光合特性. 中国农业科学, 2010, 43(1): 123–131. |
| [21] | 裴斌, 张光灿, 张淑勇, 吴芹, 徐志强, 徐萍. 土壤干旱胁迫对沙棘叶片光合作用和抗氧化酶活性的影响. 生态学报, 2013, 33(5): 1386–1396. |
| [22] | Farquhar G D, Sharkey T D. Stomatal conductance and photosynthesis. Annual Review of Plant Physiology, 1982, 33(1): 317–345. DOI:10.1146/annurev.pp.33.060182.001533 |
| [23] | 李辉, 张光灿, 谢会成, 许景伟, 李传荣, 孙居文. 苯酚废水对垂柳叶片光合生理参数的影响. 植物学报, 2016, 51(1): 31–39. DOI:10.11983/CBB15028 |
| [24] | 王泽港, 骆剑峰, 高红明, 万定珍, 葛才林, 罗时石, 杨建昌. 1, 2, 4-三氯苯和萘对水稻抽穗期叶片光合特性的影响. 中国农业科学, 2005, 38(6): 1113–1119. |
| [25] | Krause G H. Photoinhibition Fo photosynthesis: an evaluation of damaging and protective mechanisms. Physiologia Plantarum, 1988, 74(3): 566–574. DOI:10.1111/ppl.1988.74.issue-3 |
| [26] | 刘建锋, 杨文娟, 江泽平, 郭泉水, 金江群, 薛亮. 遮荫对濒危植物崖柏光合作用和叶绿素荧光参数的影响. 生态学报, 2011, 31(20): 5999–6004. |
| [27] | 陈华新, 陈玮, 姜闯道, 高辉远, 邹琦. 光温交叉处理对小麦紫黄质脱环氧化酶活性及其热耗散能力的影响. 植物生态学报, 2008, 32(5): 1015–1022. |
| [28] | 韩刚, 赵忠. 不同土壤水分下4种沙生灌木的光合光响应特性. 生态学报, 2010, 30(15): 4019–4026. |
| [29] | Brack W, Frank H. Chlorophyll a fluorescence: a tool for the investigation of toxic effects in the photosynthetic apparatus. Ecotoxicology and Environmental Safety, 1998, 40(1/2): 34–41. |
| [30] | 柏伟荣. 苯胺对紫萍营养生长、光合色素及抗氧化酶系统的影响[D]. 扬州: 扬州大学, 2012. http://cdmd.cnki.com.cn/Article/CDMD-11117-1013181678.htm |
| [31] | 温广军. 苯胺对浮萍营养生长和部分生理指标的毒性效应[D]. 扬州: 扬州大学, 2012. http://cdmd.cnki.com.cn/Article/CDMD-11117-1013180757.htm |
 2017, Vol. 37
2017, Vol. 37