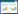文章信息
- 安申群, 贡璐, 朱美玲, 李红林, 解丽娜, 罗艳
- AN Shenqun, GONG Lu, ZHU Meiling, LI Honglin, XIE Li'na, LUO Yan.
- 塔里木盆地北缘典型荒漠植物根系化学计量特征及其与土壤理化因子的关系
- Root stoichiometric characteristics of desert plants and their correlation with soil physicochemical factors in the northern Tarim Basin
- 生态学报. 2017, 37(16): 5444-5450
- Acta Ecologica Sinica. 2017, 37(16): 5444-5450
- http://dx.doi.org/10.5846/stxb201605241003
-
文章历史
- 收稿日期: 2016-05-24
- 网络出版日期: 2017-03-26
2. 绿洲生态教育部重点实验室, 乌鲁木齐 830046
2. Key Laboratory of Oasis Ecology, Ministry of Education, Urumqi 830046, China
化学计量学是研究生态过程和生态作用的重要工具, 主要用于探索各元素动态平衡及其相互作用[1]。作为植物体内的重要生源元素, C、N、P为研究植物生长发育、生态系统物质与能量交换提供有效途径;同时, 不同的元素含量及其比值关系对生态系统中养分的限制与有机质的分解速率有较好的指示性[2-3]。植物根系是植物吸收土壤中水分与矿质元素的器官, 对营养元素的运移与固定有重要作用。应用化学计量学方法对植物根系及其与土壤理化因子关系的研究有助于揭示在特定的环境内植物的生态策略[4-5], 对物质的循环与平衡机制有重要意义。
自19世纪80年代化学计量学首次被应用于生态学中以来, 国内外科学家取得了瞩目的成就。其研究主要集中于草原、森林、湿地等生态系统[6-7], 较少关注荒漠生态系统。研究内容则聚焦于植物地上部分, 得出C、N、P含量及不同比例关系对植物生长有显著影响[8]。但在不同生态系统中的影响程度不同、各器官化学计量特征存在差异[9-10]。由于植物根系分布复杂、不易获取, 对根系化学计量特征的研究鲜有报道[11]。
塔里木盆地北缘荒漠属我国极干旱地区, 生态系统脆弱, 生物多样性低下[12], 荒漠植物通过调整生理-生态方式以适应缺水、土地贫瘠、土壤盐渍化的生境[9, 13], 植物功能性状也发生相应变化, 如广泛分布于研究区的多年生草本植物甘草、花花柴、骆驼刺有较强的抗旱能力、发达的根系, 其中骆驼刺地下根系深度可达3m;另外, 芦苇为多年生禾草本植物, 生态位宽、盐碱适应力极强, 在不同环境中所表现出的特征差异较大[14];柽柳、盐爪爪是生长在干旱盐渍地的多年生灌木, 其针状与圆柱状的叶片可减少水分的蒸发。但是, 荒漠植物如何调整根系的化学计量特征以适应干旱区环境?根系的化学计量特征与土壤理化因子的关系如何?
为此, 本研究植物采集于塔里木河北缘荒漠区, 选取具有代表性的甘草(Glycyrrhiza)、芦苇(Phragmites australis)、花花柴(Karelinia caspica)、骆驼刺(Alhagi sparsifolia)、柽柳(Tamarix chinensis)、盐爪爪(Kalidiumfoliatum)6种植物, 分析根系C、N、P含量及比值特征, 探索其与土壤理化因子的相关性, 旨在揭示荒漠植物生存策略及生态化学计量的生态指示性, 为荒漠区植物生态化学计量特征的探究及地球生物化学循环提供参考。
1 材料和方法 1.1 研究区概况研究区位于天山南麓, 塔克拉玛干沙漠北缘, 塔里木河上游阿拉尔垦区, 跨81°15′—81°38′E, 40°30′—40°43′N。海拔最高1012 m, 最低996 m, 东高西低。属暖温带干旱气候, 年均气温12.4℃, 大于10℃的有效积温为4201℃, 无霜期200 d, 年均降水量44.7 mm, 年均蒸发量2498 mm, 年平均日照时数为2729.0 h。主要土壤类型为灌漠土、棕漠土、盐土和风沙土。主要植物为甘草、芦苇、花花柴、骆驼刺、柽柳、盐爪爪、胡杨(Populus euphratica Oliv.)。
1.2 研究方法样品采集于2014年8月塔里木河上游荒漠区, 设置3条垂直于塔里木河的样带, 每条样带上设置6个样地, 相邻样地间隔1 km, 每个样地3个重复, 并将3个重复样地获取的相同植物根系进行混合。在设置样方时, 草本样方为5 m×5 m, 灌木为15 m×15 m, 确定每个样方的优势种, 对长势良好的植物随机选取, 用挖掘法挖1.5 m深壕沟, 取其主根和侧根, 剥落杂质后混合, 其中草本根系混合后称取50 g, 灌木根系100 g, 将根系样品进行密封保存。采集样方内0—20 cm表层土样, 并用四分法取土样500 g, 同步测出根系附近土壤电导率、含水量。
室内所测生态化学计量指标为根系与土壤的有机碳、全氮、全磷含量。有机碳用重铬酸钾容量法-外加热法测定, 全氮用高氯酸-硫酸消化法测定, 全磷用酸溶-钼锑抗比色法测定。
1.3 数据分析实验所得数据用Excel 2007进行整理, 用SPSS 17.0进行统计学分析。对植物的C、N、P、C/N、C/P、N/P采用One-Sample Kolmogorov-Smirnov Test (K-S检验)进行正态性检验, 计算出其平均值与标准差。用单因素方差分析检验根系和土壤理化因子的差异, 先进行方差齐性检验(F检验), 若结果为齐性, 则用LSD方法进行显著性多重比较;若为非齐性, 用Tamhane′s T2法进行多重比较, 显著性水平为α=0.05。
本研究将根系的化学计量特征作为研究对象, 以土壤含水量、土壤电导率及土壤C、N、P含量为环境变量, 用冗余分析(Redundancy Analysis, RDA)分析根系C、N、P与环境变量的关系。其中, 土壤化学计量特征、土壤含水量与电导率的变异膨胀系数均为4, 小于作为环境变量的临界值20, 即可将其作为环境变量进行比较。排序轴梯度长度LGA<3, 即根系对环境变量的响应为线性, 符合线性排序法, 可用RDA对其进行分析。
2 结果与分析 2.1 植物根系C、N、P元素的基本特征由表 1可知, 在研究区6种典型荒漠植物根系中, C、N、P含量均值分别为443.62、7.44、1.06 mg/g, C/N、C/P、N/P值依次为59.64、418.91、7.02。变异系数是描述空间变量稳定性的主要指标, 研究区植物根系C、N、P及其比值变异较大, 具体变异程度见表 1。研究表明(图 1), 植物根系N元素与P元素(R2= 0.339, P < 0.05)、P元素与N/P(R2=0.266, P < 0.05) 呈显著相关关系, C元素与其他根系生态化学计量特征未表现出显著相关性。
| 指标 Index |
样本数 Number of samples |
均值 Mean |
标准差 SD |
变异系数 CV |
| C/(mg/g) | 18 | 443.62 | 70.84 | 0.16 |
| N/(mg/g) | 18 | 7.44 | 3.59 | 0.48 |
| P/(mg/g) | 18 | 0.46 | 1.92 | 0.82 |
| C/N | 18 | 59.64 | 40.67 | 0.53 |
| C/P | 18 | 418.91 | 991.88 | 0.84 |
| N/P | 18 | 7.02 | 10.46 | 0.67 |

|
| 图 1 根系C、N、P化学计量特征的相关性 Fig. 1 The relationship of stoichiometric characteristics among root C, N and P |
C、N、P含量在不同植物类型间的变化趋势分别为盐爪爪>芦苇>甘草>柽柳>花花柴>骆驼刺、甘草>盐爪爪>骆驼刺>花花柴>柽柳>芦苇、盐爪爪>花花柴>骆驼刺>甘草>柽柳>芦苇。C含量在不同植物间未表现出显著差异性, N含量在甘草与芦苇、柽柳间存在显著差异(P < 0.05), P元素在盐爪爪与其他类型植物间存在显著差异(P < 0.05), 在花花柴和柽柳与其他类型植物间也存在显著差异(P < 0.005)(表 2)。
| 指标 Index |
甘草 Glycyrrhiza |
芦苇 Phragmites australis |
花花柴 Karelinia caspica |
骆驼刺 Alhagi sparsifolia |
柽柳 Tamarix chinensis |
盐爪爪 Kalidium foliatum |
| C/(mg/g) | 472.45±31.09a | 506.78±74.08a | 438.62±56.54a | 433.32±38.21a | 456.62±10.91 a | 510.30±55.56a |
| N/(mg/g) | 10.91±1.47a | 4.09±0.49c | 5.58±0.54ac | 7.76±0.72abc | 4.89±1.28bc | 10.62±3.37ac |
| P/(mg/g) | 0.37±0.11c | 0.24±0.07c | 0.99±0.17b | 0.37±0.05c | 0.30±0.13bc | 1.52±0.39a |
| C/N | 43.64±3.92bc | 124.31±17.13a | 78.63±5.90bc | 55.86±1.30c | 103.16±37.73ab | 49.33±5.79c |
| C/P | 1325.92±246.10b | 2348.99±1040.41a | 451.57±86.52b | 117.76±200.59b | 644.42±611.23b | 350.45±53.41b |
| N/P | 30.36±4.99a | 19.18±8.99b | 5.71±0.72a | 21.11±3.88a | 17.59±17.45a | 7.07±0.25a |
| 不同小写字母代表植物根系C、N、P含量及化学计量比在不同类型植物之间存在显著差异( P<0.05) | ||||||
进一步分析不同植物类型C、N、P比的差异性可知, C/N、C/P、N/P在不同植物类型间的变化趋势为芦苇>柽柳>花花柴>骆驼刺>盐爪爪>甘草, 芦苇>甘草>柽柳>花花柴>盐爪爪>骆驼刺, 甘草>骆驼刺>芦苇>柽柳>盐爪爪>花花柴。C/N在盐爪爪与柽柳、芦苇中表现出显著差异(P < 0.05), C/P与N/P在芦苇与其他类型植物中均表现出显著性差异(P < 0.05)(表 2)。
2.3 植物根系生态化学计量特征与土壤理化因子的RDA 2.3.1 植物根系生态化学计量特征与土壤理化因子的RDA排序对6种植物的生态化学计量特征与土壤理化因子进行RDA后, 可得出土壤含水量、电导率、C、N、P含量这些土壤理化特征对植物根系生态化学计量特征的解释量。植物根系生态化学计量特征在第Ⅰ轴、第Ⅱ轴的解释量分别为85.0%和3.7%, 第Ⅲ轴与第Ⅳ轴的解释量之和仅为1.6%, 且前两轴累计解释根系生态化学计量特征量为88.7%, 对植物根系和土壤理化关系的累计解释量为91.2%, 由此可知, 前两轴能够很好地反映植物根系与土壤理化因子的关系, 且主要由第Ⅰ轴决定。
图 2为对根系生态化学计量特征与土壤理化因子关系的二维排序图。实心箭头代表植物根系生态化学计量特征, 空心箭头代表土壤理化因子;箭头连线的长短表示根系生态化学计量特征与土壤理化的关系大小, 箭头连线越长表示相关性越大, 反之越小;箭头与排序轴的夹角表示相关性的大小, 夹角越小, 相关性越大。从图中可以看出, 在所有土壤理化因子中, 土壤含水量与电导率的箭头连线最长, 可知土壤含水量与电导率对植物根系生态化学计量特征变异起到了很好的解释。土壤含水量和植物根系C含量、N含量、N/P成反比与根系的C/N、C/P、P含量成正比, 其中含水量和C/P的相关性最大;电导率和N、P含量呈正相关。土壤C、N含量皆与根系C、N含量、N/P成正比;土壤P含量与根系P含量成正比, 且相关性明显大于与其他根系生态化学计量特征的相关性。
|
| 图 2 根系C、N、P化学计量特征与理化因子关系的冗余分析二维排序图 Fig. 2 Bidimensional ordering chart of the RDA of relationships of stoichiometric characteristics of root C, N and P with physicochemical factors A:根系碳含量Root C;B:根系氮含量Root N;C:根系磷含量Root P;D:根系C/N Root C/N;E:根系C/P Root C/P;F:根系N/P Root N/P;a:土壤碳含量Soil C;b:土壤氮含量Soil N;c:土壤磷含量Soil P;d:土壤含水量Soil moisture;e:土壤电导率EC |
表 3为土壤理化因子影响程度大小排序, 其重要性由大到小排序依次为:土壤含水量、土壤电导率、土壤P含量、土壤C含量、土壤N含量。其中, 土壤含水量与土壤电导率对根系的影响显著(P < 0.05), 土壤含水量与电导率占所有土壤理化因子解释量的63%与57%, 说明含水量与电导率是影响根系生态化学计量特征的主要因子;土壤C、N、P含量对其影响未达到显著水平。
| 指标 Index |
重要性排序 Importance sequencing |
理化因子解释量 Ecplained variation of various physicochemical |
F | P |
| 土壤含水量Soil moisture | 1 | 63 | 49.75 | 0.008 |
| 土壤电导率EC | 2 | 57 | 11.55 | 0.026 |
| 土壤磷含量Soil P | 3 | 7 | 11.38 | 0.311 |
| 土壤碳含量Soil C | 4 | 4 | 1.92 | 0.856 |
| 土壤氮含量Soil N | 5 | 1 | 1.08 | 0.950 |
在长期自然选择过程中, 植物通过优化自身资源配置以应对不同环境带来的胁迫, 造成在不同环境中根系所含营养元素存在差异[15]。通过与Jackson[16]基于全球水平上的研究对比得出, 塔里木河上游典型荒漠植物根系C、N、P含量均低于全球植物根系平均水平(表 4), 这是由于塔里木河上游荒漠区土地贫瘠, 土壤营养元素含量低下, 植物通过自身调节将C、N、P含量维持在一个较低水平以达到元素的优势地位和利用效率[17-18]。C元素在植物中起到骨架作用, 其含量与全球植物根系含量基本一致, 且具有最小的变异系数, P含量的变异系数最大, N含量次之。C元素在植物生命活动中表现出了较高的稳定性, 可能由于C元素不直接参与植物的生产活动;其次是N元素, N元素具有较高的内稳态系数, 对外界环境变化的响应不敏感[19];P元素则表现出了最低的稳定性, 因为土壤P含量差异性大, 造成根系P含量稳定性较低。
| 研究区域Study area | C/(mg/g) | N/(mg/g) | P/(mg/g) | C/N | C/P | N/P |
| 全球Global | 535.58 | 11.10 | 0.77 | 48.25 | 1158.00 | 24.00 |
| 本研究This research | 443.62 | 7.44 | 0.46 | 63.37 | 964.39 | 15.22 |
C/N、C/P反映了N、P利用效率和植物生长速率, N/P值则反映植物受N或P的限制情况。如表 5所示, 本研究C/N值远大于全球平均水平[16]、藏北高寒区的值[20], 表明研究区荒漠生态系统具有较高的元素利用效率。C/P、N/P值则远小于全球平均水平;另外, 本研究得出的N/P值(15.22) 与Han[21]有关全国平均水平(13.5) 的说法有所差异, 说明在区域尺度上根系生态化学计量特征变异较大。
植物根系C与N、C与P含量无显著相关性, N和P含量呈显著正相关关系, 与基于全球尺度的研究结果一致[22], 但较于叶片N、P的相关性有所降低[23-26]。表明即使在干旱缺水的荒漠区N与P元素仍然保持着较强的内在联系性, 这对植物维持其内稳性有重要意义。另一方面, P与N/P也表现出了显著相关性, 张文彦[26]、He[27]等人也得出了相同的研究结果, 说明干旱区植物根系的N/P也受到P元素的限制。
不同类型的荒漠植物对干旱区生态系统功能的影响存在差异, 主要体现在植物生理生态等方面, 而这些差异性则被认为是遗传与适应机制的体现[28-29]。C元素在各类型植物中未体现显著差异性, 再次验证了其在植物体内的骨架作用;N元素在甘草与芦苇、柽柳间存在显著差异(P < 0.05);P元素在盐爪爪与其他类型植物间存在显著差异(P < 0.05), 在花花柴和柽柳与其他类型植物间也存在显著差异(P < 0.05);表明不同植物对营养元素的吸收有选择性。C/N在盐爪爪与柽柳、芦苇间存在显著差异(P < 0.05);C/P N/P在芦苇与其他类型植物间存在显著差异(P < 0.05);说明不同荒漠植物对养分适应策略不同, 即对营养元素的利用效率及对环境的适应能力存在差异[30]。
3.2 根系生态化学计量与土壤理化因子的关系土壤与根系直接接触, 是植物生命活动的重要场所, 土壤理化特性对根系生态化学计量特征产生重大影响。研究区土壤含水量与根系N含量、C/P、C/N、N/P均呈显著相关关系, 与土壤C、P含量无显著相关关系, 随土壤含水量的增加, 根系N含量减少、N/P值降低, C/P、C/N均有不同程度的增加。水是干旱区限制因子, 植物对水敏感, 高的土壤含水量加快植物根系生物量的积累, 对N元素有稀释作用[31];C元素作为植物结构元素, 具有较小的变异系数, 不随土壤因子变化而产生大的变异。这与有关学者对塔里木盆地荒漠区植物与水分关系的研究结论一致[32]。贡璐[14]认为荒漠植物根系特征与土壤含水量密切相关;李玉霖[5]、丁小慧[33]对中国北方植物叶片生态化学计量的研究得出相同结论。虽然以往研究多集中于植物地上部分, 但本研究证实此结论在植物根系上也呈现类似规律。
土壤电导率与土壤含盐量之间存在显著正相关关系且常用于表示土壤含盐量的高低[34]。研究区土壤电导率与植物根系N、P含量呈显著正相关关系, 与C/N呈显著负相关关系, 说明高的土壤含盐量促进根系对N、P元素的吸收, 这与李修仓[35]对干旱区植物研究得出的结论一致。已有学者对荒漠区植物与盐分的关系进行研究, 得出植物生长受全盐、钠吸附比[32]、pH[36]不同程度的影响。但Thevs等[37]在塔里木河中游对芦苇与含盐量的研究发现其与含盐量并无显著相关性, 说明在区域尺度上植物所受环境因子的影响有差异。
本文应用冗余技术研究土壤含水量、电导率及土壤C、N、P含量对根系生态化学计量的影响, 并根据其程度进行排序, 这种方法的应用是对干旱区研究的有益尝试。但单独分析水、盐或营养元素对根系生态化学计量的影响是存在缺陷的, 根系的生态化学计量特征受土壤理化因子的双重或多重影响的, 且土壤理化因子之间也存在相互制约。研究是基于单次采样分析, 使化学计量特征值有所波动, 表明单次的研究不能精确地反映研究结果, 多次的采样研究更为合理、科学。
| [1] | Amatangelo K L, Vitousek P M. Stoichiometry of ferns in Hawaii:implications for nutrient cycling. Oecologia, 2008, 157(4): 619–627. DOI:10.1007/s00442-008-1108-9 |
| [2] | Ågren G I. The C:N:P stoichiometry of autotrophs-theory and observations. Ecology Letters, 2004, 7(3): 185–191. DOI:10.1111/ele.2004.7.issue-3 |
| [3] | Knecht M F, Göransson A. Terrestrial plants require nutrients in similar proportions. Tree Physiology, 2004, 24(4): 447–460. DOI:10.1093/treephys/24.4.447 |
| [4] | 牛得草, 李茜, 江世高, 常佩静, 傅华. 阿拉善荒漠区6种主要灌木植物叶片C:N:P化学计量比的季节变化. 植物生态学报, 2013, 37(4): 317–325. |
| [5] | 李玉霖, 毛伟, 赵学勇, 张铜会. 北方典型荒漠及荒漠化地区植物叶片氮磷化学计量特征研究. 环境科学, 2010, 31(8): 1716–1725. |
| [6] | 邬畏, 何兴东, 周启星. 生态系统氮磷比化学计量特征研究进展. 中国沙漠, 2010, 30(2): 296–302. |
| [7] | Elser J J, Sterner R W, Gorokhova E, Fagan W F, Markow T A, Cotner J B, Harrison J F, Hobbie S E, Odell G M, Weider L J. Biological stoichiometry from genes to ecosystems. Ecology Letters, 2000, 3(6): 540–550. DOI:10.1046/j.1461-0248.2000.00185.x |
| [8] | 肖遥, 陶冶, 张元明. 古尔班通古特沙漠4种荒漠草本植物不同生长期的生物量分配与叶片化学计量特征. 植物生态学报, 2014, 38(9): 929–940. |
| [9] | 李从娟, 雷加强, 徐新文, 唐清亮, 高培, 王永东. 塔克拉玛干沙漠腹地人工植被及土壤C N P的化学计量特征. 生态学报, 2013, 33(18): 5760–5767. |
| [10] | 许振柱, 周广胜. 全球变化下植物的碳氮关系及其环境调节研究进展——从分子到生态系统. 植物生态学报, 2007, 31(4): 738–747. |
| [11] | 徐露燕, 田大伦, 王光军, 罗赵慧, 叶生晶, 梁贵. 湘潭锰矿栾树叶片和土壤N、P化学计量特征. 生态学报, 2014, 34(9): 2316–2322. |
| [12] | 朱秋莲, 邢肖毅, 张宏, 安韶山. 黄土丘陵沟壑区不同植被区土壤生态化学计量特征. 生态学报, 2013, 33(15): 4674–4682. |
| [13] | Niklas K J. Plant allometry, leaf nitrogen and phosphorus stoichiometry, and interspecific trends in annual growth rates. Annals of Botany, 2006, 97(2): 155–163. |
| [14] | 贡璐, 朱美玲, 塔西甫拉提·特依拜, 张雪妮, 韩丽, 解丽娜. 塔里木盆地南缘旱生芦苇生态特征与水盐因子关系. 生态学报, 2014, 34(10): 2509–2518. |
| [15] | Cao Y B, Wang B T, Wei T T, Ma H. Ecological stoichiometric characteristics and element reserves of three stands in a closed forest on the Chinese loess plateau. Environmental Monitoring and Assessment, 2016, 188: 80. DOI:10.1007/s10661-015-5057-6 |
| [16] | Jackson R B, Mooney H A, Schulze E D. A global budget for fine root biomass, surface area, and nutrient contents. Proceedings of the National Academy of Sciences of the United States of America, 1997, 94(14): 7362–7366. DOI:10.1073/pnas.94.14.7362 |
| [17] | Helton A M, Ardón M, Bernhardt E S. Thermodynamic constraints on the utility of ecological stoichiometry for explaining global biogeochemical patterns. Ecology Letters, 2015, 18(10): 1049–1056. DOI:10.1111/ele.12487 |
| [18] | Yamamichi M, Meunier C L, Peace A, Prater C, Rúa M A. Rapid evolution of a consumer stoichiometric trait destabilizes consumer-producer dynamics. Oikos, 2015, 124(7): 960–969. DOI:10.1111/oik.2015.v124.i7 |
| [19] | Yu Q, Elser J J, He N P, Wu H H, Chen Q S, Zhang G M, Han X G. Stoichiometric homeostasis of vascular plants in the Inner Mongolia grassland. Oecologia, 2011, 166(1): 1–10. DOI:10.1007/s00442-010-1902-z |
| [20] | 洪江涛, 吴建波, 王小丹. 藏北高寒草原紫花针茅根系碳氮磷生态化学计量学特征. 山地学报, 2014, 32(4): 467–474. |
| [21] | Han W X, Fang J Y, Guo D L, Zhang Y. Leaf nitrogen and phosphorus stoichiometry across 753 terrestrial plant species in China. New Phytologist, 2005, 168(2): 377–385. DOI:10.1111/j.1469-8137.2005.01530.x |
| [22] | Yuan Z Y, Chen H Y H, Reich P B. Global-scale latitudinal patterns of plant fine-root nitrogen and phosphorus. Nature Communications, 2011, 2: 344. DOI:10.1038/ncomms1346 |
| [23] | 樊江文, 张良侠, 张文彦, 钟华平. 中国草地样带植物根系N、P元素特征及其与地理气候因子的关系. 草业学报, 2014, 23(5): 69–76. DOI:10.11686/cyxb20140508 |
| [24] | Corman J R, Moody E K, Elser J J. Stoichiometric impact of calcium carbonate deposition on nitrogen and phosphorus supplies in three montane streams. Biogeochemistry, 2015, 126(3): 285–300. DOI:10.1007/s10533-015-0156-6 |
| [25] | Danger M, Gessner M O, Bärlocher F. Ecological stoichiometry of aquatic fungi:current knowledge and perspectives. Fungal Ecology, 2016, 19: 100–111. DOI:10.1016/j.funeco.2015.09.004 |
| [26] | 张文彦, 樊江文, 钟华平, 胡中民, 宋璐璐, 王宁. 中国典型草原优势植物功能群氮磷化学计量学特征研究. 草地学报, 2010, 18(4): 503–509. DOI:10.11733/j.issn.1007-0435.2010.04.005 |
| [27] | He J S, Wang L, Flynn D F B, Wang X P, Ma W H, Fang J Y. Leaf nitrogen:phosphorus stoichiometry across Chinese grassland biomes. Oecologia, 2008, 155(2): 301–310. DOI:10.1007/s00442-007-0912-y |
| [28] | 汪涛, 杨元合, 马文红. 中国土壤磷库的大小、分布及其影响因素. 北京大学学报(自然科学版), 2008, 44(6): 945–952. |
| [29] | Sterck F J, Poorter L, Schieving F. Leaf traits determine the growth-survival trade-off across rain forest tree species. The American Naturalist, 2006, 167(5): 758–765. |
| [30] | Wright I J, Reich P B, Westoby M, Ackerly D D, Baruch Z, Bongers F, Cavender-Bares J, Chapin T, Cornelissen J H C, Diemer M, Flexas J, Garnier E, Groom P K, Gulias J, Hikosaka K, Lamont B B, Lee T, Lee W, Lusk C, Midgley J J, Navas M L, Niinemets V, Oleksyn J, Osada N, Poorter H, Poot P, Prior L, Pyankov V I, Roumet C, Thomas S C, Tjoelker M G, Veneklaas E J, Villar R. The worldwide leaf economics spectrum. Nature, 2004, 428(6985): 821–827. DOI:10.1038/nature02403 |
| [31] | Reich P B, Oleksyn J. Global patterns of plant leaf N and P in relation to temperature and latitude. Proceedings of the National Academy of Sciences of the United States of America, 2004, 101(30): 11001–11006. DOI:10.1073/pnas.0403588101 |
| [32] | Hao X M, Li W H, Huang X, Zhu C G, Ma J X. Assessment of the groundwater threshold of desert riparian forest vegetation along the middle and lower reaches of the Tarim River, China. Hydrological Processes, 2010, 24(2): 178–186. |
| [33] | 丁小慧, 罗淑政, 刘金巍, 李魁, 刘国华. 呼伦贝尔草地植物群落与土壤化学计量学特征沿经度梯度变化. 生态学报, 2012, 32(11): 3467–3476. |
| [34] | 彭杰, 王家强, 向红英, 腾洪芬, 柳维扬, 迟春明, 牛建龙, 郭燕, 史舟. 土壤含盐量与电导率的高光谱反演精度对比研究. 光谱学与光谱分析, 2014, 34(2): 510–514. |
| [35] | 李修仓, 胡顺军, 李岳坦, 李雪梅. 干旱区旱生芦苇根系分布及土壤水分动态. 草业报, 2008, 17(2): 97–101. |
| [36] | 赛迪古丽·哈西木, 海米提·依米提. 于田绿洲土壤pH值的空间异质性及其对芦苇生长的影响研究——以喀尔克乡为例. 新疆师范大学学报:自然科学版, 2012, 31(2): 9–15. |
| [37] | Thevs N, Zerbe S, Gahlert F, Mijit M, Succow M. Productivity of reed (Phragmites australis Trin. ex Steud.) in continental-arid NW China in relation tosoil, groundwater, and land-use. Journal of Applied Botany and Food Quality, 2007, 81(1): 62–68. |
 2017, Vol. 37
2017, Vol. 37