文章信息
- 李超然, 温仲明, 李鸣雷, 朱朵菊, 曾鸿文, 史海静
- LI Chaoran, WEN Zhongming, LI Minglei, ZHU Duoju, ZENG Hongwen, SHI Haijing.
- 黄土丘陵沟壑区地形变化对土壤微生物群落功能多样性的影响
- Impact of terrain changes on the functional diversity of soil microbial community in the loess hilly-gully region of China
- 生态学报. 2017, 37(16): 5436-5443
- Acta Ecologica Sinica. 2017, 37(16): 5436-5443
- http://dx.doi.org/10.5846/stxb201605160944
-
文章历史
- 收稿日期: 2016-05-16
- 网络出版日期: 2017-03-27
2. 中国科学院大学, 北京 100049;
3. 西北农林科技大学水土保持研究所, 杨凌 712100;
4. 西北农林科技大学林学院, 杨凌 712100
2. University of Chinese Academy of Sciences, Beijing 100049, China;
3. Institute of Soil and Water Conservation, Northwest Agriculture and Forestry University, Yangling 712100, China;
4. College of Forestry, Northwest Agriculture and Forestry University, Yangling 712100, China
黄土高原丘陵沟壑区地形破碎, 复杂地形对土壤理化性质及地表植被均有显著影响。不同地形、土壤性质以及植被覆盖下发育不同的土壤微生物群落。土壤微生物群落是陆地生态系统的重要生物成分, 其结构和功能多样性与土壤功能关系密切, 直接影响到系统的碳、氮等生态过程, 所以土壤微生物群落既是土壤功能的保证, 也是恢复土壤功能的基础[1]。微生物结构相对简单, 对环境变化能产生快速、灵敏的应答, 土壤微生物功能多样性能够综合反映土壤质量指标信息[2], 可以看作是评价土壤质量变化的敏感参数[3]。土壤生物化学过程、有机质的分解转化以及菌根的形成均离不开土壤微生物的参与, 作为分解者, 土壤微生物通过营养元素的周转, 调节养分的供应, 作用植物的生长、资源分配和化学组成, 影响植物的生长、植被发育、群落结构演替和土壤发育[4-5]。
土壤微生物群落功能多样性是土壤微生物群落状态与功能的指标, 能够反映土壤中微生物的生态特征[6]。研究表明, 微生物群落功能多样性与地上植被类型变化密切相关[7], 如李刚[8]等人通过研究呼伦贝尔沙地不同植被恢复模式下土壤固氮微生物多样性发现不同植被恢复模式间的土壤固氮微生物群落组成差异显著;胡雷[9]和张于光[10]等人研究了三江源地区不同退化演替阶段高寒草甸和不同植被的土壤微生物群落结构发现地上植被与地下微生物之间存在明显的关联性, 植物种类容易影响土壤微生物群落的活性。
黄土丘陵区地形破碎, 形成了千沟万壑、不计其数的微小地形, 丰富的坡面结构会引起局部环境的较大变化, 如张宏芝[11]研究发现微地形会改善原状坡的土壤化学性质, 而邝高明[12]提出微地形对土壤水分和生物量有显著影响。目前较多的研究还分析了地形变化对植被分布或生物多样性的影响, 如卢纪元[13]与王晶[14]对陕北黄土区植被特征对微地形的响应进行了研究, 张丽娟[15]和白红梅[16]研究了沙地植被功能群及其多样性对微地形变化的响应, 马宝霞[17]研究了乔木群落的多样性与微地形的关系, 但少有研究分析地形变化对微生物群落结构的影响。由于微生物对于群落生态过程与系统功能的重要性, 本文在现有研究的基础上, 进一步分析地形变化对土壤微生物群落功能多样性的影响, 有助于深入认识黄土丘陵区复杂地形区的主要生态过程与格局变化。
本文利用Biolog微平板培养法对黄土丘陵沟壑区同一坡面的不同坡位土壤微生物群落功能多样性进行研究, 探究地形变化对土壤微生物功能多样性的影响, 以为理解该区主要生态过程与系统功能的空间变化提供依据, 并为该区植被恢复重建提供依据。
1 材料与方法 1.1 研究区概况研究区位于陕西省延安市安塞县陈家洼小流域(36°49′—36°50′N, 109°15′—109°19′E), 海拔1148—1222 m, 属于典型的黄土高原丘陵沟壑区, 为暖温带半湿润向半干旱过渡区;气候属大陆性季风气候, 年平均气温8.8 ℃, 年平均降水量505.3 mm, 无霜期157 d;土壤为黄绵土与沙黄土交错分布;植被区划属于暖温带落叶阔叶林向干草原过渡的森林草原区, 受地形影响, 乔木多分布于沟谷中, 坡面分布有矮乔木伴生的疏林草原群落[18], 是典型受人类活动影响的水土流失严重区。研究样地信息及群落组成见表 1, 群落优势种主要有草木樨状黄耆(Astragalus melilotoides)、铁杆蒿(Artemisia sacrorum)、达乌里胡枝子(Lespedeza davurica)、异叶败酱(Patrinia heterophylla )和菊叶委陵菜(Potentilla tanacetifolia), 在不同坡位还分布有白羊草(Bothriochloa ischaemum)和旱生芦苇(Phragmites australis), 群落盖度在63%—75%之间。
| 坡位 Position |
海拔/m Elevation |
坡向 Aspect |
盖度/% Coverage |
坡度/(°) Slope |
群落优势种 Dominant species |
| 坡上部Upslope | 1222 | 东北 | 63 | 18 | 草木樨、达乌里胡枝子、铁杆蒿、长芒草 |
| 坡中部Mid-slope | 1185 | 东北 | 75 | 28 | 甘草、披针叶野决明、达乌里胡枝子、铁杆蒿 |
| 坡下部Downslope | 1148 | 东北 | 70 | 30 | 旱生芦苇、野豌豆、菊叶委陵菜、大针茅、异叶败酱 |
依据地形变化, 选择坡上部(PS)、坡中部(PZ)和坡下部(PX) 3个坡位进行采样。样品于2015年8月6日在研究样地选定坡面采用土钻采集, 在坡上部、坡中部和坡下部0—10 cm和10—20 cm分层取样, 每个坡位采用“S”型路线选择5个点进行多点混合采样作为一个样品, 过2 mm筛, 去除可见动植物残体, 一部分用铝盒密封, 用作土壤含水率的测定;一部分冰盒冷藏带回实验室, 供测土壤微生物群落功能多样性;剩余部分风干, 留测土壤理化性质。
1.2.1 土壤理化指标及其测定土壤含水率采用烘干法测定;土壤pH使用梅特勒-托利多pH计测定(土水比1:2.5);土壤有机质含量使用重铬酸钾氧化法;全氮使用全自动凯氏定氮仪(FOSS全自动凯氏定氮仪KJELTEC 2300) 测定;全磷含量采用硫酸高氯酸氧化法。测定结果见表 2。
| 坡位 Position |
土层/cm Depth |
含水率/% Water Content |
全碳/(g/kg) Total C |
全氮/(g/kg) Total N |
全磷/(g/kg) Total P |
pH |
| 坡上部Upslope | 0—10 | 4.01a | 5.36a | 0.60a | 0.55a | 8.61a |
| 10—20 | 3.43a | 0.48b | 0.51b | 8.68a | ||
| 坡中部Mid-slope | 0—10 | 3.49a | 4.49a | 0.60a | 0.56a | 8.71a |
| 10—20 | 4.21a | 0.41c | 0.52b | 8.73a | ||
| 坡下部Downslope | 0—10 | 15.79b | 4.24a | 0.48b | 0.56a | 8.66a |
| 10—20 | 3.26a | 0.41c | 0.55a | 8.70a | ||
| 同列不同字母表示P < 0.05水平差异显著 | ||||||
试验采用的Biolog EcoPlate是美国Biolog公司生产的微平板培养基, 用于测定微生物群落水平多样性, 每块平板有8×12共计96个微孔, 为3个重复, 各包含有31种碳源和1个水空白。接种土壤微生物溶液后, 在一定温度下培养, 微生物代谢底物产生的电子会使微孔内的氧化还原染料变色, 通过比对颜色变化的差异可以分析土壤微生物群落对底物的代谢情况。此方法操作简便, 培养时间短, 是研究土壤微生物群落功能多样性的主流方法之一[19]。
称取相当于5.0 g风干质量的新鲜土壤, 加入装有45 mL无菌生理盐水(0.85% NaCl)的三角瓶中, 摇床(200 r/min)振荡30 min, 获得土壤样品表面和内部的微生物悬浮液。静置片刻后取上清液, 采用10倍稀释法, 用无菌生理盐水将其稀释至浓度为10-3的悬浮液接种于ECO微平板中, 每孔150 μL。将接种的ECO板装入聚乙烯盒中置于25 ℃暗箱培养, 连续培养13 d, 在此培养过程中每隔24 h在ELISA反应微平板读数器上590 nm处读数1次。本试验供试土样来自黄土高原丘陵沟壑区, 为pH值在8.6—8.7的强碱性黄绵土, 土壤养分含量低, 微生物量本底值小, 因此需要较长时间来达到使微孔发生稳定颜色变化。观察图 1和图 2发现AWCD培养曲线趋于稳定时间为第10天前后, 所以选择第11天数据进行群落多样性指数的计算和主成分分析。多样性指数包括碳源利用丰富度指数(S)、Shannon丰富度指数(H)、Simpson优势度指数(D)和McIntosh均一度指数(U)。
|
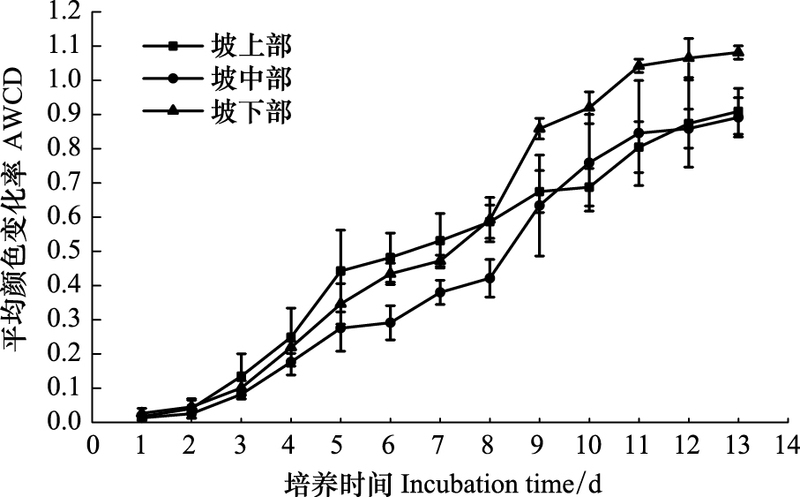
| 图 1 不同坡位0—10 cm土壤微生物AWCD随培养时间的变化 Fig. 1 AWCD changes with incubation time of different positions at 0—10cm PS:坡上部Upslope;PZ:坡中部Mid-slope;PX:坡下部Downslope |
|
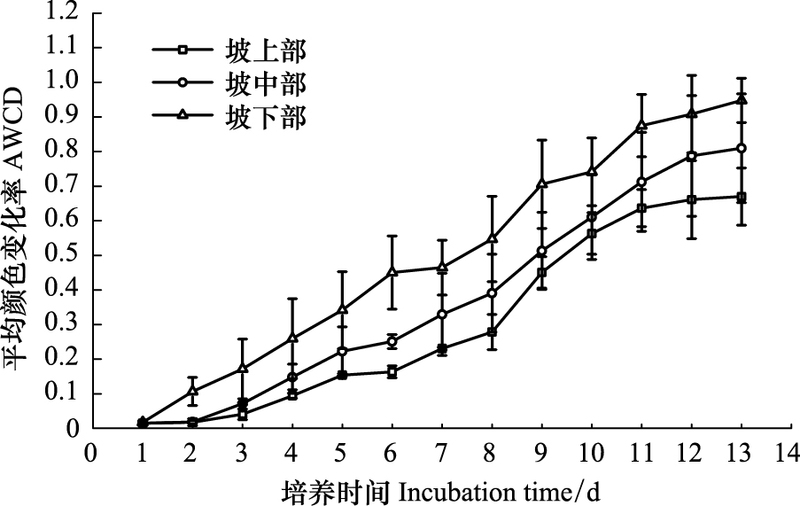
| 图 2 不同坡位10—20 cm土壤微生物AWCD随培养时间的变化 Fig. 2 AWCD changes with incubation time of different positions at 10—20 cm |
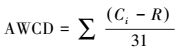
|
AWCD值可用于评判群落对31种碳源利用的总能力, 式中, Ci为各反应孔在590 nm处的吸光值;R为ECO板对照孔A1在590 nm处的吸光值。(Ci-R)小于零的孔, 计算时记(Ci-R)为零, 即:(Ci-R)≥0。
1.3.2 群落多样性指数碳源利用丰富度指数(S):

|
Shannon指数(H)用于评估群落丰富度, 式中Pi为第i孔相对吸光值与整板平均相对吸光值总和之比, 即: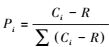

|
Simpson指数(D)用于评估群落常见种优势度, 式中Pi为第i孔相对吸光值与整板平均相对吸光值总和之比, 计算公式如下:

|
McIntosh指数(U)用于评估群落均一度, ni为第i孔相对吸光值(Ci-R), 计算公式如下:
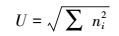
|
使用Biolog EcoPlate培养第11天AWCD值用于主成分分析。采用SPSS 22.0和Origin 9.0软件进行主成分分析, 数据处理和制图采用Excel 2013与Origin 9.0进行。
2 结果与分析 2.1 Biolog EcoPlate每孔平均颜色变化率(AWCD)平均颜色变化率(AWCD)反映了土壤微生物在群落水平上利用单一碳源的能力, 从图 1和图 2可以看出, 随着培养时间的变化, 所有EcoPlate的AWCD值均呈现不断上升的趋势, 从第11天逐渐趋于稳定, 且不同样品稳定值之间差异很明显, 在第13天时极差已经达到0.41, 占最小值坡上部10—20 cm土层土壤AWCD的61.4%。对于表层0—10 cm土壤, 样品培养前期各坡位差异不大, 中期第4天至第8天坡上部的AWCD值最大且呈现相互交叉的变化过程, 在此后的培养过程中坡下部AWCD快速上升, 最终保持在三者最大, 而坡中部和坡下部之间差异不明显。对于10—20 cm土层样品, 随着培养时间的延长, AWCD始终保持着坡下部>坡中部>坡上部的规律, 且各坡位差异较为明显。图 1和图 2 AWCD值增长曲线总的呈现出坡下部>坡中部>坡上部的规律, 且坡下部AWCD值与坡中部、坡上部间差异显著。
2.2 土壤微生物群落功能多样性分析根据AWCD值随培养时间的变化曲线, 选取第11天的AWCD值用于计算土壤微生物群落的各项多样性指数, 可以在简单的数字特征上对土壤微生物群落的功能多样性进行比较。如表 3所示, 坡下部在不同土层深度间碳源利用丰富度指数(S)和各指数均无显著性差异, 坡上部与坡中部的McIntosh指数(U)、坡中部Simpson指数(D)在不同土壤深度之间也无显著性差异;坡上部与坡中部碳源利用丰富度指数(S)和Shannon指数(H)、坡上部的Simpson指数(D)在不同土壤深度均有显著性差异。
| 坡位 Position |
深度/cm Depth |
碳源利用丰富度 指数(S) Substrate utilization |
丰富度指数(H) Shannon Index |
优势度指数(D) Simpson Index |
均一度指数(U) McIntosh Index |
| 坡上部Upslope | 0—10 | 22.33±0.58bc | 3.077±0.003bc | .950±0.000bc | 5.556±0.499a |
| 10—20 | 18.00±1.73a | 2.915±0.092a | .936±0.006a | 4.974±0.173a | |
| 坡中部Mid-slope | 0—10 | 23.00±2.65c | 3.130±0.124c | .951±0.007bc | 5.734±0.641ab |
| 10—20 | 19.00±1.73ab | 2.970±0.059ab | .943±0.005ab | 5.260±1.029a | |
| 坡下部Downslope | 0—10 | 25.00±2.65c | 3.175±0.056c | .955±0.003c | 6.872±0.115b |
| 10—20 | 21.67±1.16bc | 3.052±0.075abc | .949±0.004bc | 6.147±0.697ab |
综合比较, 坡下部不论是碳源利用丰富度指数(S)、Shannon指数(H)、Simpson指数(D)还是McIntosh指数(U)均比坡上部和坡中部高, 而坡下部0—10 cm层有25个孔发生颜色反应, Shannon指数(H)为3.175, Simpson指数(D)为0.955, McIntosh指数(U)为6.872均为所有培养样品中的最大值, 与AWCD值随培养时间的变化曲线表现结果一致。
2.3 土壤微生物群落碳源利用分析坡面地形会影响土壤和环境间的物质交换与能量流动, 对光照、温度、水分、养分等环境因子具有再分配作用。不同坡位土壤养分剖面分布的差异主要是由于坡面土壤性质和坡面养分在降雨侵蚀过程中的再分配所造成的。在坡面上, 地形部位是决定土壤性质变化的重要因素, 沿坡面不同位置土壤的成土过程导致了坡面土壤性质的差异[20], 不同坡位微生境不论是温湿度还是养分含量都有较大差异, 这使得土壤微生物群落的结构和功能也有所不同, 表现在本试验中则是各样品对碳源的利用各有差异。
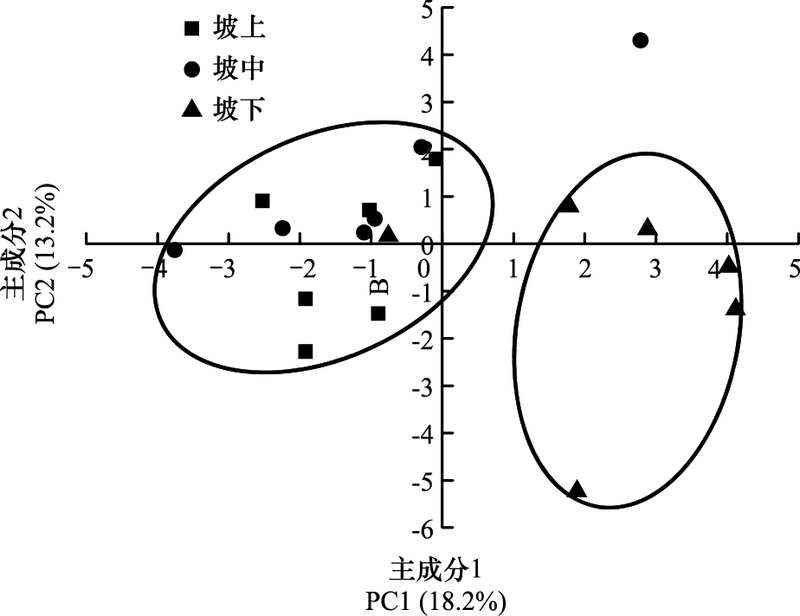
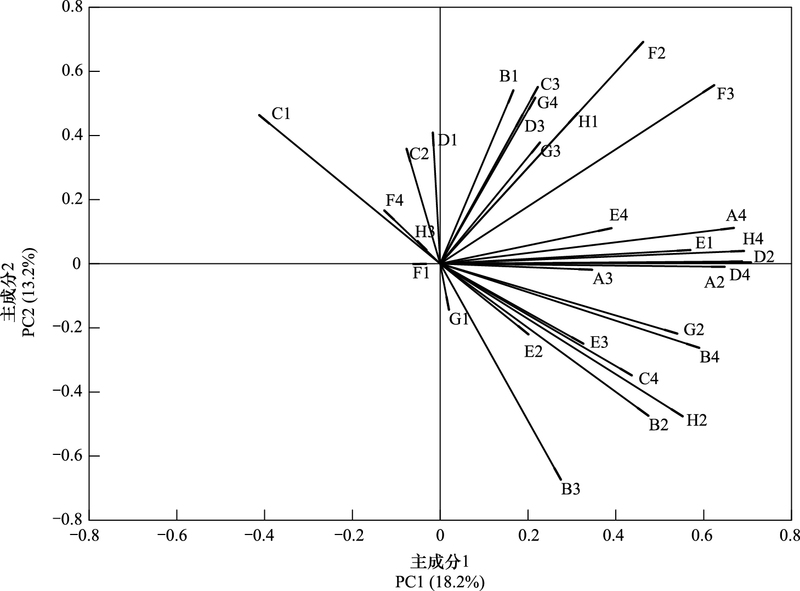
采用第11天的AWCD值进行主成分分析, 将31个因子降维得到9个主成分(PC), 它们的特征值分别是5.63、4.10、3.67、3.26、2.62、2.45、2.12、1.64和1.300, 累积方差贡献率达到了86.40%, 因此认为这9个主成分可以表征不同坡位土壤微生物对单一碳源的代谢能力。如图 3所示, 坡下部与坡上部和坡中部在PC1发生明显分离聚集, 这表明坡位的不同的确对表层土壤微生物群落的碳源利用有较大影响。分析前2个主成分(PC1和PC2) 的因子载荷, 其中单一碳源对PC1贡献较大(因子载荷>0.5) 的碳源共有10种, 对PC2贡献较大的碳源共6种。结合因子载荷图(图 4)可以直观地发现糖类碳源(β-甲基D-葡萄糖苷、D-甘露醇、葡萄糖-1-磷酸盐和D, L-a-甘油等)和氨基酸类碳源(L-精氨酸、L-天冬酰胺酸和L-丝氨酸等)对PC1起主要分异作用;而羧酸类碳源(丙酮酸甲脂、D-半乳糖醛酸、D-葡萄胺酸和衣康酸等)、多酚化合物类碳源(2-羟苯甲酸)和多胺类碳源(苯乙基胺)则对PC2贡献较大。因此可以认为对于本试验样品, 对土壤微生物群落功能多样性差异贡献较大的碳源是糖类、羧酸类和多酚化合物类碳源。
|
| 图 3 土壤微生物群落主成分分析 Fig. 3 Principal component analysis of soil microbial community |
|
| 图 4 31种碳源(A2-H4) 对PC1和PC2的因子载荷 Fig. 4 Factor loadings of 31 carbon sources(A2-H4) for PC1 and PC2 |
微生物群落功能多样性受温度、湿度、生物等环境因子的影响。本研究中, 土壤微生物群落培养的平均吸光度值(AWCD)增长曲线总的呈现坡下部>坡中部>坡上部的规律, 且坡下部AWCD值与坡中部、坡上部间差异显著, 表明不同坡位的土壤微生物群落功能多样性存在差异。下坡位土壤微生物群落多样性明显高于坡中部和坡上部, 微生物群落丰富度和均一度与土壤全氮含量正相关, 优势度反之, 这与杨云锋的研究结果[21]青藏高原微生物功能多样性与环境条件, 特别是土壤氮循环之间强烈相关相似。但本文的供试土样全碳、全磷和pH在各坡位间无显著性差异, 没有显示出微生物群落结构和功能多样性与全碳、全磷和pH的显著相关性。一方面可能与黄土母质发育的土壤本身碱性强, 磷含量高, 地面植被发育较差有关, 坡面地形对这些元素的迁移和累积没有达到显著性差异;但另一方面也说明微生物功能多样性对环境变化的响应较碳、磷等土壤元素更为敏感, 能更好地反映地形变化对生态过程的影响[2]。因此将微生物功能多样性作为衡量黄土高原丘陵沟壑区土壤质量与立地条件的一个间接指标, 可能能更好地区分不同立地环境质量, 对于评估立地环境质量的空间变化, 进而为植被恢复规划与布局提供更好的支持。
不同坡位的土壤微生物群落功能多样性存在显著差异, 可能与不同地形条件下的土壤环境及生物组成密切相关。地形变化会影响土壤的一系列重要指标[22]如密度、孔隙度、含水率、养分、pH和Eh等, 同时也深刻影响着土壤微生物群落[23]。本研究中地形变化对土壤微生物群落生境的影响主要体现在土壤含水率的高低, 土壤水分可以通过影响土壤有机碳、全氮含量等理化性质, 对土壤微生物群落结构产生影响。下坡位土壤水分含量远高于上坡位和中坡位, 土壤水分的增加可导致土壤通气性变差, 减缓有机质分解速率, 使有机质及其他一些营养元素更易于累积[24], 同时影响地面植被组成和分布;地面植被的发育对土壤理化性质亦有作用, 植物根系分泌物作用于土壤, 可为微生物群落提供丰富的资源以及差异性的理化环境[25], 促成微生物群落的结构和功能变迁改变土壤微生物群落多样性。在下坡位地面植物群落主要由旱生芦苇、铁杆蒿、异叶败酱和草木樨构建, 群落多样性和生物量均高于坡上部和坡中部, 这使得在坡下部表层土壤凋落物含量和组成均与坡上部和坡中部有较大差异。同时, 主成分分析发现对土壤微生物群落功能多样性差异贡献较大的碳源是糖类、羧酸类和多酚化合物类碳源, 这表明在不同坡位土壤微生物群落组成的差异是底物筛选作用的结果。
土壤微生物群落的结构和功能多样性能够快速响应环境变化, 对于监测和评价环境生态过程具有重要实用价值, 继续深入研究地形变化对土壤微生物群落功能多样性的影响对于黄土高原丘陵沟壑区生态环境恢复和保护具有重要意义, 可以加深对该区主要生态过程与系统功能的空间变化的理解, 为该区植被恢复重建提供依据。
致谢: 感谢西北农林科技大学资源环境学院钱勋博士、孙薇博士、殷亚楠博士和张雅君硕士对本研究的帮助。| [1] | 林先贵, 胡君利. 土壤微生物多样性的科学内涵及其生态服务功能. 土壤学报, 2008, 45(5): 892–900. |
| [2] | Zelles L. Fatty acid patterns of phospholipids and lipopolysaccharides in the characterisation of microbial communities in soil:a review. Biology and Fertility of Soils, 1999, 29(2): 111–129. DOI:10.1007/s003740050533 |
| [3] | 闫晗, 吴祥云, 黄静, 何志明. 评价土壤质量的微生物指标及其研究方法. 山西农业科学, 2010, 38(10): 78–81. DOI:10.3969/j.issn.1002-2481.2010.10.22 |
| [4] | 毕江涛, 贺达汉. 植物对土壤微生物多样性的影响研究进展. 中国农学通报, 2009, 25(9): 244–250. |
| [5] | Harris J A. Measurements of the soil microbial community for estimating the success of restoration. European Journal of Soil Science, 2003, 54(4): 801–808. DOI:10.1046/j.1351-0754.2003.0559.x |
| [6] | 曹永昌, 谭向平, 和文祥, 耿增超, 刘帅, 佘雕, 侯林. 秦岭地区不同林分土壤微生物群落代谢特征. 生态学报, 2016, 36(10): 2978–2986. |
| [7] | 陈颖. 典型草原植物功能群及物种对土壤微生物多样性的影响[D]. 呼和浩特: 内蒙古大学, 2012. http://cdmd.cnki.com.cn/Article/CDMD-10126-1012439893.htm |
| [8] | 李刚, 王丽娟, 李玉洁, 乔江, 张海芳, 宋晓龙, 杨殿林. 呼伦贝尔沙地不同植被恢复模式对土壤固氮微生物多样性的影响. 应用生态学报, 2013, 24(6): 1639–1646. |
| [9] | 胡雷, 王长庭, 王根绪, 马力, 刘伟, 向泽宇. 三江源区不同退化演替阶段高寒草甸土壤酶活性和微生物群落结构的变化. 草业学报, 2014, 23(3): 8–19. DOI:10.11686/cyxb20140302 |
| [10] | 张于光, 王慧敏, 李迪强, 肖启明, 刘学端. 三江源地区不同植被土壤固氮微生物的群落结构研究. 微生物学报, 2005, 45(3): 420–425. |
| [11] | 张宏芝, 朱清科, 赵磊磊, 邝高明, 谢静, 李镇. 陕北黄土坡面微地形土壤化学性质. 中国水土保持科学, 2011, 9(5): 20–25. |
| [12] | 邝高明, 朱清科, 刘中奇, 赵荟, 王晶. 黄土丘陵沟壑区微地形对土壤水分及生物量的影响. 水土保持研究, 2012, 19(3): 74–77. |
| [13] | 卢纪元, 朱清科, 陈文思, 王瑜. 陕北黄土区植被特征对坡面微地形的响应. 中国水土保持科学, 2016, 14(1): 53–60. |
| [14] | 王晶, 朱清科, 秦伟, 张宏芝, 云雷, 谢静, 邝高明. 陕北黄土区封禁流域坡面微地形植被特征分异. 应用生态学报, 2012, 23(3): 694–700. |
| [15] | 张丽娟, 于永奇, 高凯. 沙地植物功能群及其多样性对微地形变化的响应. 草地学报, 2015, 23(1): 41–46. DOI:10.11733/j.issn.1007-0435.2015.01.007 |
| [16] | 白红梅, 李钢铁, 马骏骥, 李亚杰, 梁田雨. 浑善达克沙地微地形植被特征分析. 北方园艺, 2015(17): 53–57. |
| [17] | 马宝霞, 李景侠. 东灵山植物群落(乔木)物种多样性与微地形关系的研究. 西北林学院学报, 2006, 21(6): 47–49. |
| [18] | 朱志诚. 黄土高原森林草原的基本特征. 地理科学, 1994, 14(2): 152-156, 200-200. |
| [19] | 张燕燕, 曲来叶, 陈利顶. Biolog EcoPlate-TM实验信息提取方法改进. 微生物学通报, 2009, 36(7): 1083–1091. |
| [20] | Brubaker S C, Jones A J, Lewis D T, Frank K. Soil properties associated with landscape position. Soil Science Society of America Journal, 1993, 57(1): 235–239. DOI:10.2136/sssaj1993.03615995005700010041x |
| [21] | Yang Y F, Gao Y, Wang S P, Xu D P, Yu H, Wu L W, Lin Q Y, Hu Y G, Li X Z, He Z L, Deng Y, Zhou J Z. The microbial gene diversity along an elevation gradient of the Tibetan grassland. The ISME Journal, 2014, 8(2): 430–440. DOI:10.1038/ismej.2013.146 |
| [22] | 刘占锋, 傅伯杰, 刘国华, 朱永官. 土壤质量与土壤质量指标及其评价. 生态学报, 2006, 26(3): 901–913. |
| [23] | 周桔, 雷霆. 土壤微生物多样性影响因素及研究方法的现状与展望. 生物多样性, 2007, 15(3): 306–311. |
| [24] | 牛佳, 周小奇, 蒋娜, 王艳芬. 若尔盖高寒湿地干湿土壤条件下微生物群落结构特征. 生态学报, 2011, 31(2): 474–482. |
| [25] | 夏北成, ZhouJ Z, JamesM T. 植被对土壤微生物群落结构的影响. 应用生态学报, 1998, 9(3): 296–300. |
 2017, Vol. 37
2017, Vol. 37