文章信息
- 曾成城, 陈锦平, 魏虹, 刘媛, 马文超, 王婷, 周翠
- ZENG Chengcheng, CHEN Jinping, WEI Hong, LIU Yuan, MA Wenchao, WANG Ting, ZHOU Cui.
- 水淹生境下秋华柳对Cd污染土壤微生物数量及酶活性的影响
- Effects of Salix variegata on soil microorganisms and enzymatic activity in contaminated soils under flooding conditions
- 生态学报. 2017, 37(13): 4327-4334
- Acta Ecologica Sinica. 2017, 37(13): 4327-4334
- http://dx.doi.org/10.5846/stxb201606011054
-
文章历史
- 收稿日期: 2016-06-01
- 修订日期: 2017-01-03
2. 四川省彭州市敖平中学, 彭州 611931;
3. 广西农业科学院农业资源与环境研究所, 南宁 530007
2. Aoping middle school of pengzghou Sichuan, Pengzhou 611931, China;
3. Agricultural Resources and Environment Research Institute, Guangxi Academy of Agricultural Sciences, Nanning 530007, China
三峡库区完成蓄水后, 在周边形成反复经历“淹没-干旱-淹没”的消落带。消落带原有生态系统受损, 环境不稳定, 其生物组成和群落结构简单、生态调节功能弱, 新的湿地生态系统尚未发育完善, 截留和吸收污染物的能力较小[1]。调查发现, 三峡库区表层土壤中污染最严重的重金属元素为Cd, 清洁区仅占52.12%[2]。植物修复是通过种植植物将土壤中的重金属提取, 富集并转移到地上部分储存, 以达到降低土壤污染物浓度, 进而提高土壤安全性的一种廉价、绿色的重金属修复技术[3]。前期研究结果表明, 水淹条件下, 作为耐水淹的杨柳科(Salicaceae)柳属(Salix L.)植物秋华柳(Salix variegate)对重金属Cd污染土壤有较好的修复能力[4]。
由于重金属在土壤中的难降解、强毒性, 有积累效应等特性, 对土壤微生物也会产生不良影响。主要表现在影响土壤微生物区系、改变微生物群落、降低生物量, 以及影响微生物活性等方面[5]。与动植物相比, 土壤微生物种类、数量和生理活性对重金属污染的响应更为敏感[6], 能更及时准确地预测环境质量的变化, 反应土壤污染状况, 是最具潜力的土壤环境质量评价指标[7]。土壤酶指土壤中的聚积酶, 来源于土壤微生物、动植物活体或残体, 是土壤生化过程的产物[8], 与矿质营养元素循环、有机物质矿化分解、能量转移以及环境质量等均密切相关, 故其活性的变化对植物生长起着重要的作用[9]。前人研究表明, 当土壤受到重金属污染后, 土壤酶将受到抑制, 其途径大致有两方面, 一方面重金属可络合土壤基质、螯合土壤蛋白基质或与酶基质产生络合反应, 直接影响酶活性;另一方面, 重金属离子通过影响土壤微生物及土壤动物的代谢活动, 并影响植物的生长发育, 影响土壤酶来源, 间接影响土壤酶活[10]。因此, 土壤微生物指标和酶活性常作为检测土壤重金属污染状况及修复成效的重要指标之一[11]。
水淹条件下, 兼性厌氧微生物和厌氧微生物可将土壤中氧化物作为呼吸作用的电子受体, 形成各种还原性物质, 导致土壤氧化还原电位降低[12], 土壤中的SO42-被还原成S2-, S2-易与Cd2+结合成难溶于水的CdS[13]。在此过程中, 随氧化铁溶解、聚合, 再至沉淀等活化作用的快递完成, 可交换态Cd将更易被土壤表面吸持[14], 导致土壤中Cd的生物有效性降低, 使更多的Cd以活性低的形态沉淀在土壤中, 从而降低重金属对植物根际土壤的负面影响。在水淹环境下, 秋华柳种植对Cd污染土壤的微生物数量和酶活特征具有怎样的影响?为了对三峡库区消落带Cd污染土壤的植物修复提供理论和实践依据, 值得对这一问题进行进一步探究。
1 材料与方法 1.1 试验材料于2014年10月于嘉陵江边采集当年生的秋华柳枝条, 剪成长约15 cm, 直径0.8—1.0 cm的插条进行扦插。2015年5月29日选取生长旺盛, 且大小均匀一致的秋华柳扦插苗作为试验材料。种植后将所有盆栽试验用苗置西南大学生态试验园(海拔249 m)的遮雨棚下(棚顶透明, 四面敞开)进行相同条件的适应生长, 并给与除草除虫等常规管理。试验用土壤基本理化性质见表 1。
| pH | 有机质 Organic matter/ (g/kg) | 全氮 Total N/ (g/kg) | 全磷 Total P/ (g/kg) | 全钾 Total K/ (g/kg) | 碱解氮 Alkali hydrolysable N/ (mg/kg) | 有效磷 Available P/ (mg/kg) | 速效钾 Available K/ (mg/kg) | 总Cd Total Cd/ (mg/kg) |
| 7.83 | 15.23 | 0.99 | 0.78 | 12.21 | 81.27 | 11.83 | 186.27 | 0.53 |
试验采用三因素完全随机试验设计, 共16个处理(表 2)。根据三峡库区消落带Cd污染状况[2, 15], 设置4个Cd处理浓度:0、0.5、2、10 mg/kg(Cd2+/土壤), 分别代表对照组、低浓度组、中浓度组和高浓度组, 以CdCl2·2.5H2O溶液形式加入经风干后过1 mm筛的紫色土壤, 充分搅拌混匀, 陈化1个月后, 将其装入盆高15 cm, 盆底直径13 cm, 盆口直径18 cm的花盆, 每盆土重2 kg。水分处理有2种:正常供水组CK及水淹组FL(土壤表面以上5 cm积水), 水淹组将花盆放入水桶(上径26 cm×下径19.5 cm×高17 cm)进行水淹处理。所有处理组均包括秋华柳种植组和无植物组。试验期间, 每天对试验材料进行观察, 并确保各处理组保持设定的土壤含水量。分别对处理60 d和120 d的土壤进行取样, 每个处理3个重复。
| Cd浓度处理 Cd treatment | 植物与水分处理Plant and water treatment | |||
| 无植物正常供水CK | 无植物水淹FL | 有植物正常供水PCK | 有植物水淹PFL | |
| T0(0 mg/kg) | CK0 | FL0 | PCK0 | PFL0 |
| T1(0.5 mg/kg) | CK1 | FL1 | PCK1 | PFL1 |
| T2 (2 mg/kg) | CK2 | FL2 | PCK2 | PFL2 |
| T3 (10 mg/kg) | CK3 | FL3 | PCK3 | PFL3 |
| CK: control check(正常供水组); FL: flooding(水淹组); PCK: plant control check(种植秋华柳正常供水组); PFL: plant flooding(种植秋华柳水淹组) | ||||
取约0.5 kg新鲜土壤, 放置于消毒后的聚乙烯自封袋, 带回实验室进行测定。土壤细菌采用牛肉膏蛋白胨培养基, 放线菌采用改良高氏一号合成培养基, 真菌用马丁培养基进行培养, 均采用稀释平板法进行测定。
1.3.2 土壤酶活性取约0.5 kg鲜土用信封取回实验室后放入4 ℃冰箱, 参照文献[16]的方法对土壤酶活进行测定:脲酶活性采用苯酚钠比色法, 碱性磷酸酶活性采用磷酸苯二钠比色法, 蔗糖酶活性采用3, 5-二硝基水杨酸比色法。
1.4 数据处理及分析利用SPSS 20.0软件采用三因素方差分析(Three factors variance analysis)来揭示不同水分、秋华柳种植以及Cd浓度梯度处理对土壤微生物数量以及酶活的影响, 并运用Duncan(Duncan′s multiple range test)检验法检验不同处理的各个指标差异显著性;采用Pearson相关系数评价土壤微生物数量及酶活性之间的相关关系。
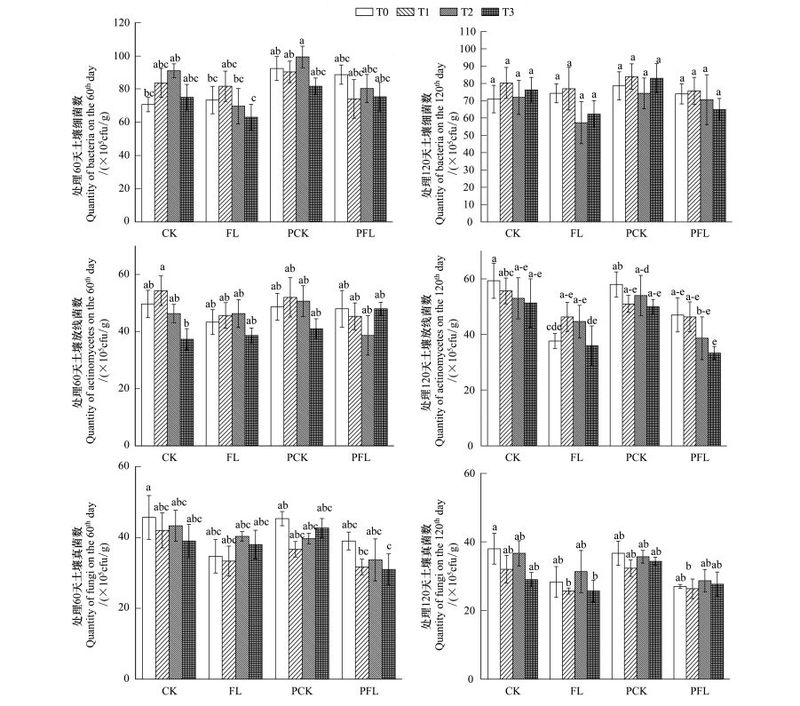
2 结果与分析 2.1 微生物数量植物及水分处理显著影响处理60 d土壤细菌数(P<0.05), 种植秋华柳显著提高了土壤细菌数量(图 1);处理120 d土壤放线菌数量中, 水淹组显著低于正常供水组(P<0.05)(图 1);处理60 d和120 d土壤真菌数均表现出水淹组极显著低于正常供水组的趋势(P<0.01)(图 1)。高浓度的Cd浓度处理降低土壤细菌、放线菌和真菌数量, 但未达到差异显著水平(P>0.05), 各级交互作用对土壤微生物数量的影响均未不显著(P>0.05)。
|
| 图 1 各处理组土壤微生物数量 Fig. 1 Quantities of microorganisms in the soil of each treatment CK: control check(正常供水组); FL: flooding(水淹组); PCK: plant control check(种植秋华柳正常供水组); PFL: plant flooding(种植秋华柳水淹组); 不同小写字母分别表示各处理之间有显著差异(P<0.05); a—e表示abcde, a—d表示abcd, b—e表示bcde |
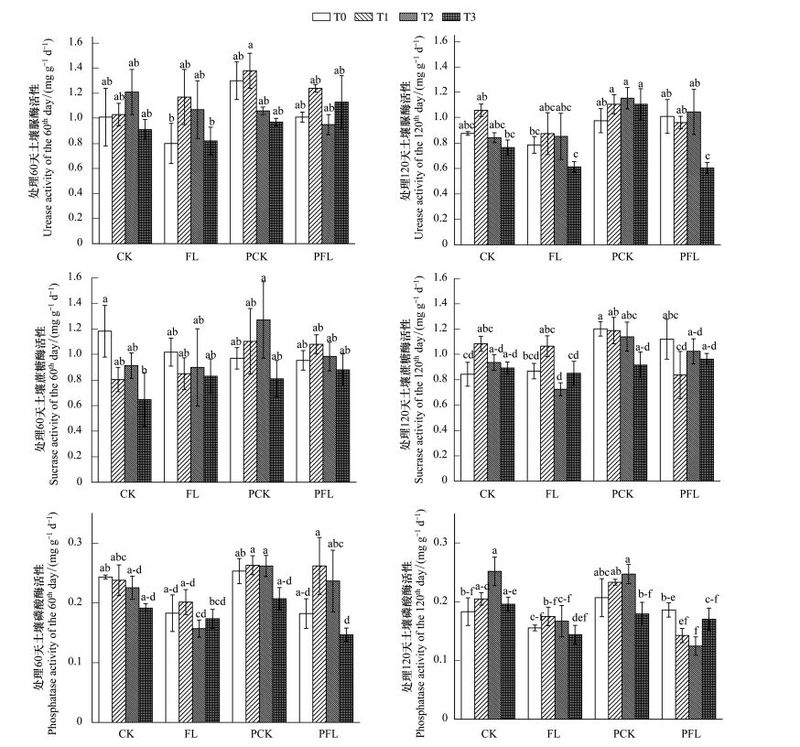
植物、水分及Cd浓度处理显著影响处理120 d土壤脲酶和蔗糖酶活性(P<0.05), 种植秋华柳显著提高了处理120 d土壤脲酶和蔗糖酶活性(图 2), 植物、水分和Cd浓度处理均显著影响处理60 d土壤磷酸酶活性(P<0.05)。除水淹高浓度处理组外, 种植秋华柳显著提高了处理60 d土壤磷酸酶活性(图 2)。与正常供水处理组相比, 水淹组土壤磷酸酶活性表现出下降的趋势(图 2), 水分处理和水分与Cd浓度处理交互作用显著影响处理120 d土壤磷酸酶活性(P<0.05)。
|
| 图 2 不同处理土壤中酶活性 Fig. 2 Soil enzymatic activities of each treatment CK: control check(正常供水组); FL: flooding(水淹组); PCK: plant control check(种植秋华柳正常供水组); PFL: plant flooding(种植秋华柳水淹组); 不同小写字母分别表示各处理之间有显著差异(P<0.05) |
对土壤微生物数量及酶活性的相关性分析得出:处理60 d, 土壤中细菌数与放线菌数、蔗糖酶活性、脲酶活性显著正相关(P<0.05), 放线菌数与真菌数及蔗糖酶显著正相关(P<0.05);处理120 d, 土壤放线菌数与真菌数和磷酸酶活性呈极显著正相关(P<0.01), 真菌数与磷酸酶活呈显著正相关(P<0.05), 脲酶与磷酸酶活性显著正相关(P<0.05)(表 3)。
| 处理时间 Treatment time | 磷酸酶活性 Phosphatase activity | 蔗糖酶活性 Invertase activity | 脲酶活性 Urease activityactivity | 真菌数 Quantities of fungi | 放线菌数 Quantities of actinomycetes | |
| 处理60 d | 细菌数Quantities of bacteria | 0.258 | 0.274* | 0.317* | 0.261 | 0.317* |
| 放线菌数Quantities of actinomycetes | 0.264 | 0.382** | 0.151 | 0.322* | ||
| 真菌数Quantities of fungi | 0.152 | 0.035 | 0.065 | |||
| 脲酶活性Urease activityactivity | 0.163 | 0.101 | ||||
| 蔗糖酶活性Invertase activity | 0.265 | |||||
| 处理120 d | 细菌数Quantities of bacteria | 0.128 | 0.014 | -0.077 | 0.096 | 0.077 |
| 放线菌数Quantities of actinomycetes | 0.455** | 0.236 | 0.163 | 0.524** | ||
| 真菌数Quantities of fungi | 0.412** | -0.028 | 0.017 | |||
| 脲酶活性Urease activityactivity | 0.273* | 0.218 | ||||
| 蔗糖酶活性Invertase activity | 0.245 | |||||
| *和**分别表示在0.05与0.01水平上差异显著 | ||||||
土壤微生物是影响土壤生态过程的重要因素之一, 它在推动土壤能量流动、地球化学循环、污染物降解以及净化地下水质量等方面都具有重要作用[17-18]。土壤酶则是土壤中一切生物化学反应的催化剂[16], 在土壤有机质及养分循环过程中有重要的作用[19], 是土壤生物学活性的总体现[20]。作为土壤环境的重要组分, 大部分土壤酶来自于微生物, 故土壤微生物和酶之间存在着不可分割的关系[21]。本研究结果显示, 三大微生物间存在较好相关性, 其消长具有一定的同步性。细菌是土壤微生物中数量最多、繁殖最快的微生物, 在新陈代谢中产生大量的过氧化氢酶、脲酶、蔗糖酶及蛋白酶等[22]。综合两次取样结果来看, 细菌和放线菌与三大酶活相关性较明显, 真菌最次。鉴于土壤微生物数量与酶活性相关性较大, 并且该二者均易受到土壤环境因素的影响, 对土壤污染物反应敏感, 故把这两类指标结合起来作为判断土壤Cd污染程度和治理成效指标更为合理。
本研究结果表明, 无论是否种植秋华柳, 水淹处理组的土壤微生物数量均低于正常供水组, 这与水淹导致土壤氧气含量大量减少有关。其次, 水淹环境下, 土壤营养元素大量溶出, 降低了土壤微生物的营养来源, 特别是氮的供应, 这也可能是导致土壤微生物数量下降的一个原因。水淹条件下, 土壤微生物群落改变, 影响土壤酶的释放, 同时在还原条件下土壤酶活性会受到增大的Fe2+离子浓度的明显抑制[23-24]。本研究表明, 随淹水时间的延长, 3种土壤酶活性显著降低, 可能是长时间水淹下土壤呼吸强度、微生物数量降低, 土壤酶来源减少导致的。水淹造成磷素向水中释放, 使土壤中磷酸酶作用的底物减少, 也会导致其活性的下降[25], 本研究结果中, 水淹组碱性磷酸酶活性降幅较之脲酶和蔗糖酶更大与该结论一致。
由于重金属在土壤中的难降解性, 导致其对土壤微生物活性产生明显的负面影响[26]。作为非必需元素, Cd具有致突变效应, 导致脱氧核糖核酸链断裂。本研究中, 高浓度的Cd处理组对细菌和放线菌有一定的抑制作用, 而真菌的耐受能力相对较强。多数情况下, 低浓度的重金属污染土壤利于CO2的释放, 刺激微生物的生长, 增加微生物生物量。故本研究结果表明, 外源Cd的施加, 对土壤微生物数量也表现出不同程度的刺激作用。
重金属对土壤酶活的影响很大程度上受到污染程度的影响, 一般表现为随着重金属浓度的增加, 土壤酶活逐渐增强, 达到一定浓度时又逐渐下降[27], 其拐点浓度随土壤类型及酶种类以及污染元素而异[28]。除少数处理组外, 本研究结果表明较低浓度Cd处理(0.5, 2 mg/kg)对土壤酶活性有一定促进作用, 高浓度(10 mg/kg)Cd处理则表现出一定的抑制作用。值得注意的是, 本研究中脲酶、蔗糖酶及磷酸酶均表现出水淹组的高浓度处理组(PFL3、FL3)的酶活性要强于对照组(PCK3、CK3), 有可能是在水淹或者水淹与植物双重影响下, 土壤Cd浓度降低, 使其更加接近拐点浓度。
植物对土壤微生物生理生态过程能产生重要的影响, 能促使其产生微生物区系。在植物的参与下, 土壤微生物能从根系分泌物中获取更多C、N等营养物质, 促进根际土壤微生物生物量的增多[29]。前人研究结果表明, 植物根际土壤微生物数量明显高于非根际土壤[30-31]。Zn的超富集植物Thlaspi caerulescens与非超富集植物Trifolium pratense根际微生物差异很大, 超富集植物根际具有更多的耐重金属细菌和真菌[32]。前期研究结果表明, 秋华柳对Cd污染土壤有较好的耐受和富集能力[33], 本研究中种植秋华柳显著提高了处理60 d土壤细菌数。当外源Cd处理浓度为10 mg/kg时, 处理60 d土壤中PCK、PFL的细菌和放线菌和PFL组真菌数以及处理120 d土壤中的PCK组的细菌数和真菌数均大于无植物组土壤, 虽未达到统计分析的显著水平, 但在一定程度上显现了秋华柳种植对土壤微生物特性的影响。酶活方面, 受植物根系活动的影响, 根系分泌物及残体在土壤分解过程中可刺激微生物活动, 进而使根际土壤酶活性得以增强[34]。李伟的研究结果表明, 吊兰根际土壤的脲酶活性、磷酸酶活性以及蔗糖酶活性分别比无植物组土壤高59.37%、78.58%及41.99%[30]。本研究中, 秋华柳对两次土样中酶活性均有一定程度的提高。由于植物-土壤-微生物构成的土壤微生态系统非常复杂, 植物不同, 其根系分泌物种类和数量各异, 故不同植物对土壤根际的酶活也会有不同影响[35]。秋华柳对水淹组的酶活性的提高效果要略弱于正常供水组, 其主要原因可能是水淹胁迫导致植物根系缺氧, 减少了酶来源, 导致酶减少, 其活性降低[36]。
综上所述, 在水淹胁迫和Cd污染胁迫共存的三峡库区消落带区域, 土壤微生物和酶活性可较为敏锐地反映环境质量特征。秋华柳种植可改善土壤微生物数量和酶活性, 综合前期研究结果, 即秋华柳在水淹和正常供水条件下对土壤Cd均有一定的富集能力, 笔者认为, 秋华柳在三峡库区消落带Cd污染土壤的修复治理方面具有一定的应用前景。
| [1] | 储立民, 常超, 谢宗强, 熊高明. 三峡水库蓄水对消落带土壤重金属的影响. 土壤学报, 2011, 48(1): 192–196. DOI:10.11766/trxb200904250188 |
| [2] | 唐将. 三峡库区镉等重金属元素迁移富集及转化规律[D]. 成都理工大学, 2005. |
| [3] | David E. S, Blaylock M, Kumar N P. B. A., Dushenkov V, Ensley B D, Chet I, Raskln I. Phytoremediation:a novel strategy for the removal of toxic metals from the environment using plants. Biotechnology, 1995, 13: 468–474. |
| [4] | 曾成城, 陈锦平, 马文超, 刘媛, 贾中民, 魏虹, 王婷. 水淹生境下秋华柳对镉污染土壤修复能力的研究. 生态学报, 2016, 36(12): 3978–3986. |
| [5] | 王嘉, 王仁卿, 郭卫华. 重金属对土壤微生物影响的研究进展. 山东农业科学, 2006(1): 101–105. |
| [6] | Giller K E, Witter E, Mcgrath S P. Toxicity of Heavy Metals to Microorganisms and Microbial Processes in Agricultural Soils:A Review. Soil Biology & Biochemistry, 1998, 30(10/11): 1389–1414. |
| [7] | 张妍, 崔骁勇, 罗维. 重金属污染对土壤微生物生态功能的影响. 生态毒理学报, 2010, 05(3): 305–313. |
| [8] | 雷明, 李昌晓, 马朋, 马骏. 岸坡坡耕地不同耕地类型下土壤酶与土壤微生物的研究. 北方园艺, 2013(11): 175–181. |
| [9] | Yao X H, Min H, Lü Z H, Yuan H P. Influence of acetamiprid on soil enzymatic activities and respiration. European Journal of Soil Biology, 2006, 42(2): 120–126. DOI:10.1016/j.ejsobi.2005.12.001 |
| [10] | Yang G, Zhou P, Liang M, Zhi Y E, Shi W J. Assessment of effects of heavy metals combined pollution on soil enzyme activities and microbial community structure:modified ecological dose-response model and PCR-RAPD. Environmental Earth Sciences, 2010, 60(3): 603–612. DOI:10.1007/s12665-009-0200-8 |
| [11] | 王涛, 李惠民, 史晓燕. 重金属污染农田土壤修复效果评价指标体系分析. 土壤通报, 2016(3): 725–729. |
| [12] | Pezeshki S R, Delaune R D. Soil oxidation-reduction in wetlands and its impact on plant functioning. Biology, 2012, 1(2): 196–221. |
| [13] | Plekhanova I O. Effect of wetting conditions on the fractional composition of heavy metal compounds in agrosoddy-podzolic soils contaminated with sewage sludge. Eurasian Soil Science, 2012, 45(45): 657–664. |
| [14] | 胡宁静, 李泽琴, 黄朋, 陶成. 贵溪市污灌水田重金属元素的化学形态分布. 农业环境科学学报, 2004, 23(4): 683–686. |
| [15] | 刘意章, 肖唐付, 宁增平, 贾彦龙, 黎华军, 杨菲, 姜涛, 孙曼. 三峡库区巫山建坪地区土壤镉等重金属分布特征及来源研究. 环境科学, 2013, 34(6): 2390–2398. |
| [16] | 关松荫. 土壤酶及其研究法. 北京: 农业出版社, 1986. |
| [17] | Balser T, Kinzig A, Firestone M. The Functional Consequences of Biodiversity. In:Kinzig A, Paeala S, Tilman D eds, The Functional Consequences of Biodiversity. Princeton:Princeton University Press, 2002:265-239. |
| [18] | Noah F, Joshua P S, Patrieia A H. Variations in Mierobial Community Composition Through two Soil Denth Profiles. Soils Biology & Biochemistry, 2003, 35(1): 167–176. |
| [19] | Ciarkowska K, Sołek-Podwika K, Wieczorek J. Enzyme activity as an indicator of soil-rehabilitation processes at a zinc and lead ore mining and processing area. Journal of Environmental Management, 2014, 132(132C): 250–256. |
| [20] | 杨文浩. 镉污染/镉-锌-铅复合污染土壤植物提取修复的根际微生态效应研究[D]. 浙江大学, 2014. |
| [21] | 王启兰, 曹广民, 王长庭. 高寒草甸不同植被土壤微生物数量及微生物生物量的特征. 生态学杂志, 2007, 26(7): 1002–1008. |
| [22] | Trasar-Cepeda C, Leirós M C, Seoane S, Gil-Sotres F. Limitations of soil enzymes as indicators of soil pollution. Soil Biology & Biochemistry, 2000, 32(13): 1867–1875. |
| [23] | Freeman C, Liska G, Ostle N J. Microbial activity and enzymic decomposition processes following peatland water table drawdown. Plant & Soil, 1996, 180(180): 121–127. |
| [24] | Kang H, Freeman C. Phosphatase and arylsulphatase activities in wetland soils:annual variation and controlling factors. Soil Biology & Biochemistry, 1999, 31(3): 449–454. |
| [25] | 马朋, 任庆水, 李昌晓, 杨予静, 马骏. 模拟水淹干旱胁迫对2年生水杉(Metasequoia gly ptostroboides)幼树盆栽土壤酶活性的影响. 西南大学学报:自然科学版, 2015, 37(2): 24–31. |
| [26] | 高焕梅, 孙燕, 和林涛. 重金属污染对土壤微生物种群数量及活性的影响. 江西农业学报, 2007, 19(8): 83–85. |
| [27] | 陆文龙, 徐松巍, 李英华. 重金属镉对土壤呼吸和土壤微生物群落的影响研究. 吉林化工学院学报, 2013, 30(7): 65–67. |
| [28] | 罗虹, 刘鹏, 宋小敏. 重金属镉、铜、镍复合污染对土壤酶活性的影响. 水土保持学报, 2006, 20(2): 94–96. |
| [29] | 李廷强, 舒钦红, 杨肖娥. 不同程度重金属污染土壤对东南景天根际土壤微生物特征的影响. 浙江大学学报:农业与生命科学版, 2008, 34(6): 692–698. |
| [30] | 李伟, 韦晶晶, 刘爱民, 王友保, 朱志鹏, 王兴飞. 吊兰生长对锌污染土壤微生物数量及土壤酶活性的影响. 水土保持学报, 2013, 27(2): 276–281. |
| [31] | Abou-Shanab R I, Delorme T A, Angle J S, Chaney R L, Ghanem K, Moawad H, Ghozlan H A. Phenotypic Characterization of Microbes in the Rhizosphere of Alyssum murale. International Journal of Phytoremediation, 2003, 5(4): 367–379. DOI:10.1080/15226510309359043 |
| [32] | Delorme T A, Gagliardi J V, Angle J S, Chaney R L. Influence of the zinc hyperaccumulator Thlaspi caerulescens J. & C. Presl. and the nonmetal accumulator Trifolium pratense L. on soil microbial populations. Canadian Journal of Microbiology, 2001, 47(47): 773–776. |
| [33] | 贾中民, 魏虹, 孙晓灿, 李昌晓, 孟翔飞, 谢小红. 秋华柳和枫杨幼苗对镉的积累和耐受性. 生态学报, 2011, 31(1): 107–114. |
| [34] | 朱姗姗. 水稻根际土壤重金属形态分布及其对酶活性的影响[D]. 中南林业科技大学, 2013. |
| [35] | 胡开辉, 罗庆国, 汪世华, 林旋, 林文雄. 化感水稻根际微生物类群及酶活性变化. 应用生态学报, 2006, 17(6): 1060–1064. |
| [36] | 杜琳倩, 何钢, 王静, 王蕾. 水淹胁迫下新型氧肥对土壤脲酶活性的影响. 中南林业科技大学学报, 2013, 33(4): 66–69. |
 2017, Vol. 37
2017, Vol. 37