文章信息
- 辜晨, 贾晓红, 吴波, 成龙, 杨占武, 杨德福, 赵雪彬
- GU Chen, JIA Xiaohong, WU Bo, CHENG Long, YANG Zhanwu, YANG Defu, ZHAO Xuebin.
- 高寒沙区生物土壤结皮覆盖土壤碳通量对模拟降水的响应
- Effect of simulated precipitation on the carbon flux in biological-soil crusted soil in alpine sandy habitats
- 生态学报. 2017, 37(13): 4423-4433
- Acta Ecologica Sinica. 2017, 37(13): 4423-4433
- http://dx.doi.org/10.5846/stxb201603220510
-
文章历史
- 收稿日期: 2016-03-22
- 网络出版日期: 2017-02-23
2. 青海省农林科学院, 西宁 810016;
3. 青海共和荒漠生态系统国家定位观测研究站, 共和 813000
2. Qinghai Academiy of Agriculture and f Forestry Science, Xining 810016, China;
3. Qinghai Gonghe Desert Ecosystem Research Station, Gonghe 813000, China
生物土壤结皮广泛分布于干旱半干旱地区, 结构上主要由两个部分组成, 上层为微生物和隐花植物例如藻类、藓类、地衣等, 下层为覆盖的土壤颗粒, 二者通过菌丝、假根和分泌物等的紧密胶结成为一个整体, 是具有代谢活性的特殊地表覆盖层。在受非生物因素调控和胁迫的荒漠生态系统中, 生物土壤结皮作为荒漠生态系统常见的地表覆被类型, 是荒漠生态系统重要的组成部分和景观特征之一, 广泛分布于干旱、半干旱区, 地表覆盖度到达60%以上甚至更高[1-2]。在荒漠景观地区有机和无机成分的循环与交流中, 生物土壤结皮扮演着联系、指示和影响的角色, 对许多生态过程产生直接或间接的影响。作为具有光合固碳活性的土壤与大气系统界面层, 生物土壤结皮中的藻类和藓类植物以及下层土壤能够通过呼吸作用释放CO2, 同时在有光条件下开始光合固碳过程, 固定空气中的CO2, 释放出氧气。因此生物土壤结皮是干旱、半干旱地区荒漠系统碳通量的重要影响因素[2-4]。
在干旱半干旱区荒漠生态系统中, 水分是主要的调控和限制因子, 能够直接影响生物土壤结皮的生理活动[5]。生物土壤结皮的重要组分藻类、地衣及藓类植物作为变水植物对水分的变化尤其敏感, 在频繁多变的水分条件下有着很强的适应能力, 缺水时自身开始脱水进入休眠状态, 而在水分条件适宜的情况下其生理活性才会逐渐恢复并显现。因此生物土壤结皮的碳通量和碳释放量受水分影响较为明显。受全球气候变化影响, 未来干旱半干旱地区的降水格局将产生变化, 降水频率和幅度都将增加, 这将导致许多自然资源和地表覆盖类型产生巨大的空间异质性, 地表植被的分布不均和自然资源的时空变异使我们在评估生物土壤结皮的碳源汇角色时增加了不确定性[6-9]。
目前国外有关研究集中在极地和苔原、科罗拉多高原、热带荒漠、亚热带草原、地中海中欧草原等, 国内主要集中在黄土高原、腾格里沙漠、古尔班通古特沙漠、毛乌素沙地、科尔沁沙地等地。生物土壤结皮在降水影响下的碳通量交换规律的研究相对较少[4, 10], 在高寒沙区条件下进行的相关研究更是略显不足。本研究在青海省共和盆地中西部典型高寒沙区人工植被恢复区, 进行不同水平模拟降水下生物土壤结皮覆盖土壤的净碳通量(NCF)、呼吸速率(DR)、光合速率(Pn)以及相关环境因子进行动态监测, 探寻生物土壤结皮覆盖土壤碳通量对不同水平降水的响应规律, 揭示了土壤碳通量与降水、土壤水分之间的关系, 以期能够为该地区生物土壤结皮的碳交换研究做出参考, 也为整个高寒干旱半干旱地区的生物研究提供有益的背景资料。
1 材料与方法 1.1 研究区自然概况研究区位于青海省林业厅下属沙珠玉乡治沙实验站(98°45′—101°30′E, 35°03′—35°40′N)。该实验站地处共和盆地中西部, 位于青海南山以南, 是青海省荒漠化土地集中分布区之一, 研究区总面积为5.28×102 km2, 沙地面积为1.74×102 km2, 海拔为2600—3400m。年均气温为2.4 ℃, 1月平均气温为-12.5℃, 7月平均气温为14.6 ℃。年均降水量仅为246.3mm, 主要集中生长季, 年内分配不均。降水多发生在夜间, 历时短且降水量少。年均潜在蒸发量为1716.7mm。
沙珠玉地区海拔较高, 气温度较低, 太阳辐射较强, 水资源稀缺, 生态环境脆弱;近几年来, 草场和林地被破坏的情况增多, 使得该区域环境更加恶化, 土地沙漠化程度逐年提高。从上世纪下半叶开始, 沙珠玉地区逐渐开始对荒漠化土地进行有效治理, 通过人工植被培育, 减缓甚至遏制了沙漠化发展趋势, 稳固了沙丘, 形成了具有一定规模的人工植被恢复区。本研究选择1977年的植被恢复区为实验样地, 该样地位于固定沙丘的顶部, 样地内生物结皮发育良好, 且分布广泛, 主要有藻结皮、藓类结皮2种类型。土壤为棕钙土和栗钙土, 非地带性土壤为草甸土、盐土和风沙土。研究区内的植被种类较少, 群落结构简单。自然植被中多为草本群落, 如短花针茅(Stipa breviflora Griseb)和芨芨草(Achnatherum splendens (Trin.) Nevski)。人工植被中, 乔木主要有青杨(Populus cathayana Rehd.)、河北杨(Populus hopeiensis Hu et Chow)和小叶杨(Populus simonii Carr.), 灌木主要有柠条锦鸡儿(Caragana korshinskii Kom.)、沙棘(Hippophae rhamnoides Linn.)、柽柳(Tamarix chinensis Lour.)等。藻结皮主要包含4类藻种, 分别为漂浮克里藻(Klebsormidium fluitans)、微小色球藻(Chroococcus minutus)、窝形席藻(Phormidicum foveolarum)和溪生须藻(Homoeothrix fluviatillis)[11]。对该样地内的结皮盖度、厚度、结皮生物量等指标进行调查。由于结皮无法用烘干法测干物质的生物量, 因此在本研究中藻结皮、藓结皮的生物量均测定叶绿素a含量, 用来表示其生物量。测定方法参照苏延桂等的方法[12]。采集生物土壤结皮样本放于土壤盒中(直径4.5cm, 表面积约15.9cm2), 在实验室中测定生物结皮叶绿素a含量。
用蒸馏水冲洗结皮样本后放入研钵中同1.5mL乙醇(浓度98%)和少量石英砂、碳酸钙进行研磨。完全研磨后, 再加入7mL相同浓度乙醇进行2次各30min的离心(4℃, 14000r/min)。完成后把提取液转移至25mL容量瓶中, 利用相同浓度的乙醇定容, 之后将样品放于25mL试管中。叶绿素a用紫外分光光度计(UV-2450; Shimadzu, Kyoto, Japan)测定, 测定使用波长为649nm、665nm。计算使用的公式如下:
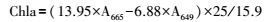
|
(1) |
式中, Chla为叶绿素a含量(mg/cm2), A665、A649分别表示波长为649nm、665nm时吸光值A, 25表示稀释体积(mL), 15.9表示结皮的垂直投影面积(cm2)。为了防止叶绿素a的降解, 样品研磨、提取、测定均在相对黑暗的环境中进行。
实验使用生物结皮样品的特征如表 1所示。
| 结皮类型 Type of Biological-soil Crusts | 结皮盖度/% Crust coverage | 结皮厚度/cm Crust thickness | 结皮生物量/(mg/cm2) Crust biomass |
| 藻结皮Algea crust | >95 | 1.01±0.01 | 3.69±0.21 |
| 藓类结皮Moss crust | >95 | 1.49±0.06 | 4.65±0.25 |
| 生物结皮生物量用叶绿素a含量表示 | |||
在研究区内坡度小于5°的丛间地上选择发育良好的以藓类结皮、藻类结皮为主的生物土壤结皮覆盖土壤为研究样地, 保证结皮覆盖度达到90%, 结构完整, 种类统一。
对于藓类、藻类结皮, 分别设置4个10m×10m的样方, 每个样方之间相距5m以上。在4个大样方中随机选择3个, 设置4个50cm×50cm的小样方, 每个小样方内分别放置1个直径为20cm的土壤环, 进行1mm、2mm、5mm、10mm的模拟降水处理, 即P1、P2、P5、P10, 剩余一个大样方设置3个小样方, 进行0mm (对照, CK)降水。土壤环使用PVC材料自制, 在测定之前3d设置于样地内, 以便内外充分平衡, 放置时保证样环内结皮完整。整个样方设置分为2种结皮处理, 5种降水处理, 3个重复, 共30个测定基座。
1.2.2 土壤碳通量测定参考当地多年降水资料, 雨季集中在每年6月—9月, 降水基本在10mm以下以小降水事件为主。因此实验于2015年9月进行, 设置1、2、5、10mm4种降水处理。在晴朗的天气条件下, 每天日出之后, 约7点左右开始人工模拟降水, 使用喷壶喷洒, 保证水流速度, 使水滴均匀撒在地表, 并保证不能形成地表径流, 控制整个降雨过程在3min之内, 对不同的降水量使用完全相同的操作方法。在降水后的0、1、2、4、6、8、12、24、48h进行净碳通量(NCF)和呼吸速率(DR)的测定。测定时间分别为第一日07:00、08:00、09:00、11:00、13:00、15:00、19:00、第2日07:00、第3日07:00, 每次测定都在天亮时进行。碳通量的测定使用Li-8100土壤碳通量系统, 配以便携测量室8100-103以及长期监测室8100-104C。净碳通量即为在光照条件下(使用长期检测室8100-104C, 该气室使用透明材料制作, 透光率>99%), 测定通过空气-土壤界面层的CO2通量值, 为生物土壤结皮的光合作用、呼吸作用与下层土壤的呼吸作用的总和。呼吸速率即为在遮光条件下(使用便携测量室8100-103, 该气室外罩使用金属材质, 保证测定在完全黑暗条件下进行), 测定通过界面的CO2通量值, 为生物土壤结皮呼吸作用与亚表层土壤的呼吸作用的总和。使用Li-8100测定碳通量时, 设定每次测定90s, 仪器自动对变化曲线进行拟合得出斜率, 即为通量值。根据NCF和DR即可计算得到光合速率(Pn)。
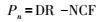
|
(1) |
式中, Pn为正并且数值越大时, 表示光合速率越高, 碳吸收能力越强。
土壤体积含水量(SVWC)采用辅助传感器测定, 测量土壤深度为5cm, 与土壤碳通量测定同时进行。
1.2.3 数据处理与分析对模拟降水后的藓类覆盖土壤和藻类覆盖土壤的净碳通量、呼吸速率和光合速率进行了分析, 同时对模拟降水后48h内的碳通量值进行了平均得到平均碳通量, 并且对两种不同结皮覆盖土壤48h内的碳通量变化规律曲线进行了积分, 得到累积碳量。
数据分析和图表绘制分别在SPSS、Origin和Excel中进行。使用重复测量方差分析进行土壤覆盖类型对碳通量影响效果的分析。双因素方差分析用来对比不同降水处理之间的碳通量规律间的区别。回归方程用来模拟碳通量和土壤水分温度之间的关系。回归方程的显著性检验通过方差分析检验。
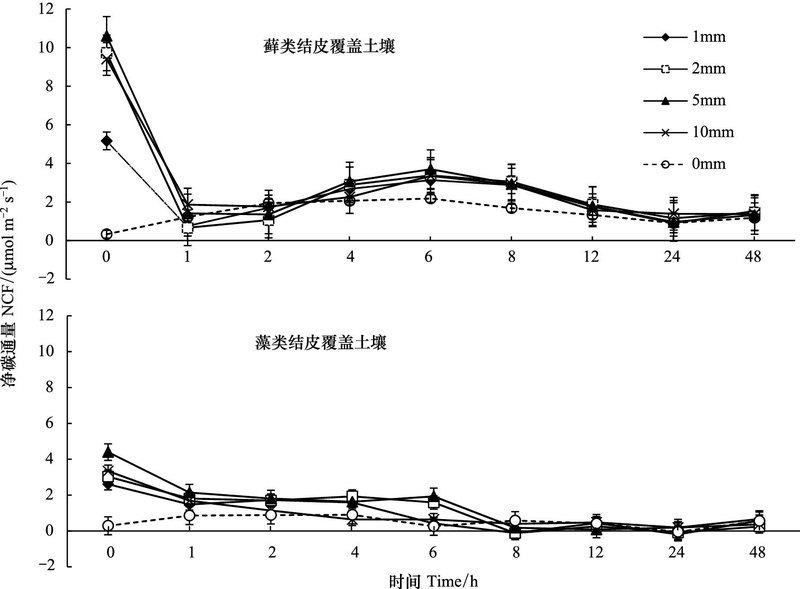
2 结果与分析 2.1 生物土壤结皮覆盖土壤碳通量对模拟降水的响应 2.1.1 生物土壤结皮覆盖土壤净碳通量的动态变化降水量对生物土壤结皮覆盖土壤的NCF有极显著影响(P<0.01)。降雨前两种生物土壤结皮覆盖土壤的NCF分别是1.17, 2.51μmol m-2 s-1。降水后二者均表现出大量的碳释放, 其NCF在短时间内到达峰值, 然后随时间逐渐下降, 在1h左右重新上升, 并在6h时到达又一峰值后再次开始下降, 呈现出先快后慢, 先上升后下降的趋势(图 1)。藓类结皮在24h左右回到原始水平, 而藻类结皮在12h左右基本回到原始水平。
|
| 图 1 生物土壤结皮覆盖土壤净碳通量对模拟降水的响应 Fig. 1 Response of net carbon flux in biological-soil crusted soil to simulated precipitation |
对于藓类结皮, 五种处理下的NCF的最大值分别为0.33、5.16、9.72、10.61、9.41μmol m-2 s-1, 即P5> P2 >P10>P1>CK。藻类结皮覆盖土壤的NCF最大值分别为0.29、2.61、3.03、4.40、3.34μmol m-2 s-1。NCF在两种结皮类型中差异显著(P<0.01), 而4种降水处理与CK对比差异显著(P<0.01), 降水量之间对比不显著(P>0.01) (表 2)。
| 误差来源 Source of variance | 净碳通量NCF | 呼吸速率DR | 光合速率Pn | ||||||
| df | F | p | df | F | p | df | F | p | |
| 结皮种类 Type of biological soil crusts | 1.000 | 42.285 | 0.000 | 1.000 | 51.393 | 0.000 | 1.000 | 0.946 | 0.333 |
| 降水量Precipitation | 4.000 | 6.509 | 0.029 | 4.000 | 3.928 | 0.006 | 4.000 | 1.265 | 0.290 |
| 结皮种类×降水量 Type×Precipitation | 4.000 | 2.139 | 0.044 | 4.000 | 0.329 | 0.858 | 4.000 | 0.940 | 0.940 |
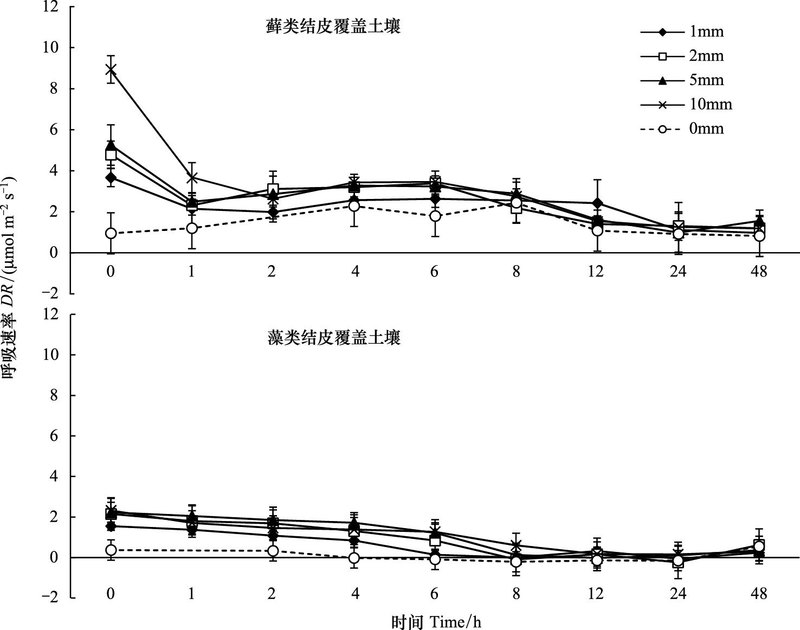
降水量对生物土壤结皮覆盖土壤的DR也有着显著影响(P<0.01)。降雨前两种生物土壤结皮覆盖土壤的DR分别是1.16, 0.79μmol m-2 s-1。降水后两种生物土壤结皮覆盖土壤的DR十分迅速的达到最高值, 然后随时间逐渐下降。在峰值时藓类结皮DR分别为0.95、3.66、4.78、5.25、8.93μmol m-2 s-1, 表现为P10 >P5 >P2>P1>CK, P10显著高于其他处理, P5、P2和P1显著高于CK。藓类结皮的DR在24h后回到正常水平。
|
| 图 2 生物土壤结皮覆盖土壤呼吸速率对模拟降水的响应 Fig. 2 Response of respiration rate in biological-soil crusted soil to simulated precipitation |
|
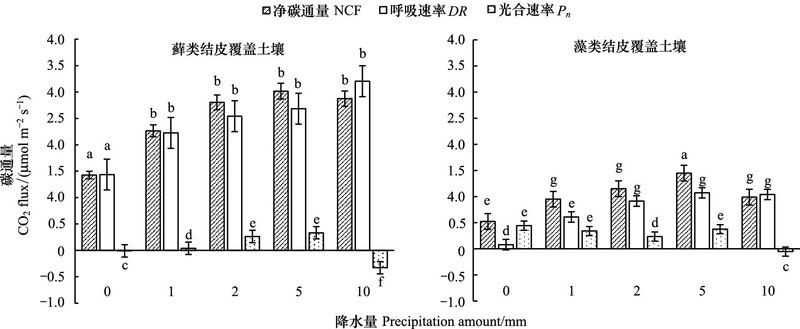
| 图 3 48h内平均碳通量和降水的关系 Fig. 3 The relationships between the average CO2 flux and simulated rainfall amount over the first 48 h (AVR) a, b, c, d, e, f代表不同的显著性水平 |
藻类结皮覆盖土壤的DR最大值分别为0.37、1.55、2.15、2.23、2.32μmol m-2 s-1, 表现为P5 > P10> P2> P1, 均显著高于CK, 不同降水处理间有显著差异(P<0.01)。对于藻结皮, 除P10外其他降水处理均在24h左右回到正常水平。两种结皮相对比, 藓类结皮覆盖土壤的DR受到模拟降水的影响较明显, 且藓类结皮的DR最大值高于藻类结皮。
随着降水量的增大, 两种结皮覆盖土壤的48h内平均碳通量也随之增加, 藓类结皮覆盖土壤的NCF分别为1.42、2.66、2.80、3.01、2.87μmol m-2 s-1, DR分别为1.43、2.22、2.54、2.68、3.20μmol m-2 s-1。
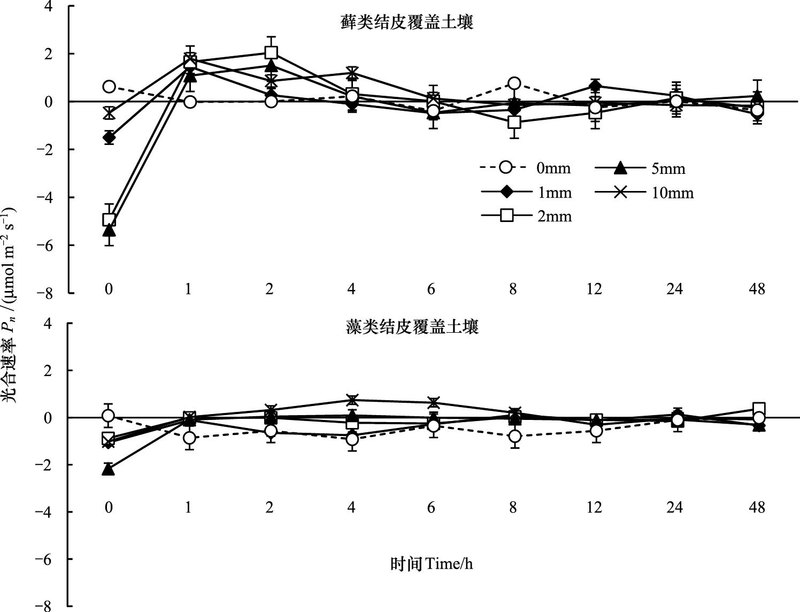
2.1.3 生物土壤结皮光合速率的动态变化根据图 4所示, 降水后藓类结皮的Pn在降水后总体呈现出逐渐上升的趋势。初始值分别为-1.50、-4.94、-5.35、-0.47、0.62μmol m-2 s-1, 在2h左右到达光合速率最大值, 此时为0.26、2.04、1.50、0.86、0μmol m-2 s-1, 并在12h之后基本保持平稳。在整个测定过程中, 藓类结皮的4种降水处理与对照之间差异显著(P<0.01), 而每个降水量之间的差异不显著(P>0.01)。
|
| 图 4 光合速率对模拟降水的响应 Fig. 4 Response of photosynthetic rate in biological-soil crusts to simulated precipitation |
藻类结皮Pn的变化趋势较之藓类表现的并不明显。藻类结皮在开始时分别为-1.06、-0.88、-2.17、-1.02、0.08μmol m-2 s-1, 其中P10随着时间其Pn逐渐提高并在4h至6h左右到达最大值, 并在降水后24h后恢复正常值。其他降水处理并没有表现出明显的光合速率增加趋势。藓类结皮光合速率表现出的最高值为藻类结皮的2.76倍, 而藻类结皮的光合速率也比藓类结皮更早回到正常水平。
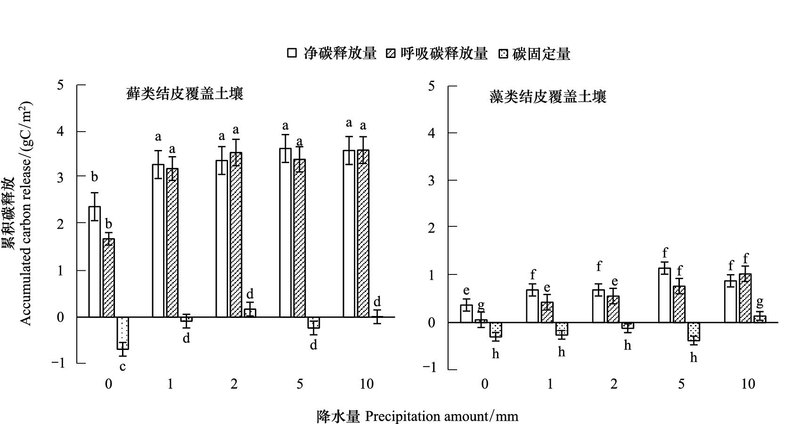
2.2 模拟降水对生物土壤结皮碳累积释放量的影响如图 5所示, 降水后, 藓类结皮48h内累计碳净释放量(有光条件下NCF累计量)随降雨量变化相对于CK明显增加, 分别为1.68、3.19、3.54、3.39、3.59 gC/m2。表现为P10 > P2> P5> P1, 各降水处理之间差异不显著(P>0.01)。藻类结皮分别为0.37、0.69、0.69、1.15、0.88 gC/m2。各个降水处理之间差异不显著(P>0.01), 但是与CK之间差异显著(P<0.01)。藓类结皮覆盖土壤净累积碳释放明显多于藻类结皮, 分别为藻类结皮的3.78、4.58、5.13、2.93、4.05倍。藓类呼吸累积碳释放量(DR累计量)同样随降雨量的增大而增大, 分别为1.68、3.20、3.54、3.40、3.59 gC/m2, 表现为P5 > P10 > P2 > P1, 差异不显著(表 3)。藻类呼吸累积释放量分别为0.06, 0.43, 0.56, 0.77, 1.03 gC/m2, 随着降雨量的增加而增加。
|
| 图 5 模拟降水与累积碳释放量的关系 Fig. 5 The relationships between the total accumulated carbon relaease and simulated rainfall amount a, b, c, d, e, f代表不同的显著性水平 |
| 误差来源 Source of variance | 净碳释放量(有光条件下) Carbon releases in light | 呼吸碳释放量(遮光条件下) Carbon releases in dark | 碳固定量 Carbon fixation | ||||||
| df | F | p | df | F | p | df | F | p | |
| 结皮种类 Type of biological soil crusts | 1.000 | 72.714 | 0.001 | 1.000 | 2.747 | 0.173 | 1.000 | 1445.647 | 0.000 |
| 降水量 Precipitation | 4.000 | 2.874 | 0.166 | 4.000 | 0.342 | 0.838 | 4.000 | 8.265 | 0.058 |
| 结皮种类×降水量 Type×Precipitation | 4.000 | 3.432 | 0.025 | 4.000 | 0.700 | 0.598 | 1.000 | 56.650 | 0.012 |
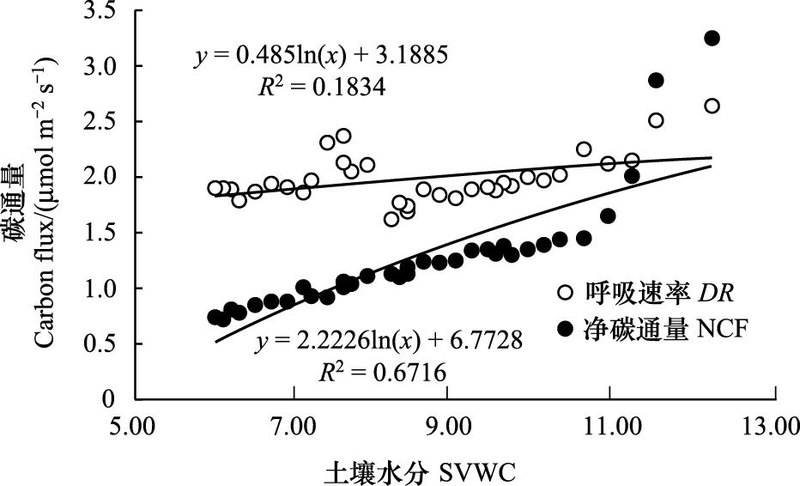
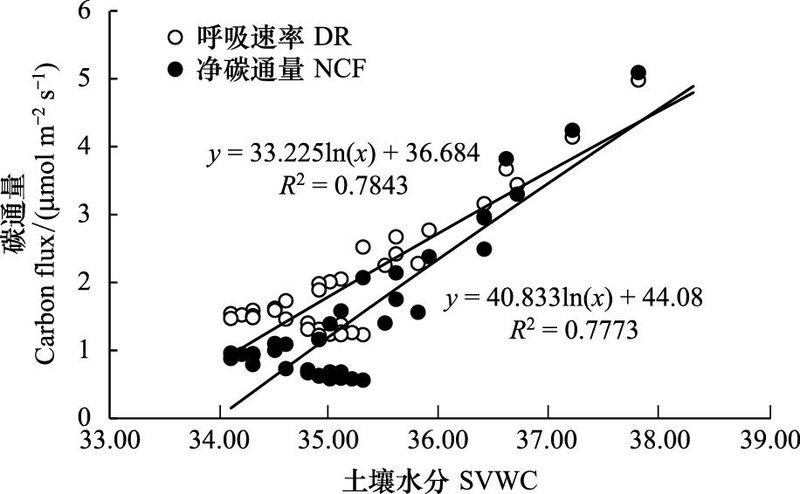
为了分析土壤水分与碳通量的关系, 使用对数方程分别对藓类结皮P5和藻结皮P10降水处理下的NCF与DR进行拟合。拟合方程分别为y=0.485ln (x) + 3.1885(藓类结皮覆盖土壤呼吸速率, P<0.01), y=2.2226ln (x)+6.7728(藓类结皮覆盖土壤净碳通量, P<0.01), y=33.225ln (x) + 36.684(藻类结皮覆盖土壤呼吸速率, P<0.01) 以及y=40.833ln (x) + 44.08(藻类结皮覆盖土壤净碳通量, P<0.01)。两种结皮覆盖土壤的NCF和DR均表现出了随水分增大的趋势(图 6, 图 7)。
|
| 图 6 5mm降水处理下藓类结皮覆盖土壤净碳通量和呼吸速率与土壤水分的关系 Fig. 6 The relationships between the NCF, DR and SVWC in moss-crusted soil under 5mm precipitation |
|
| 图 7 10mm降水处理下藻类结皮覆盖土壤净碳通量和呼吸速率与土壤水分的关系 Fig. 7 The relationships between the NCF, DR and SVWC in algea-crusted soil |
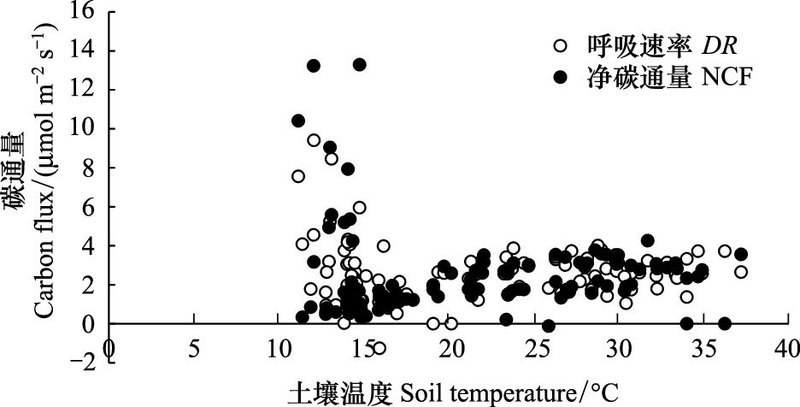
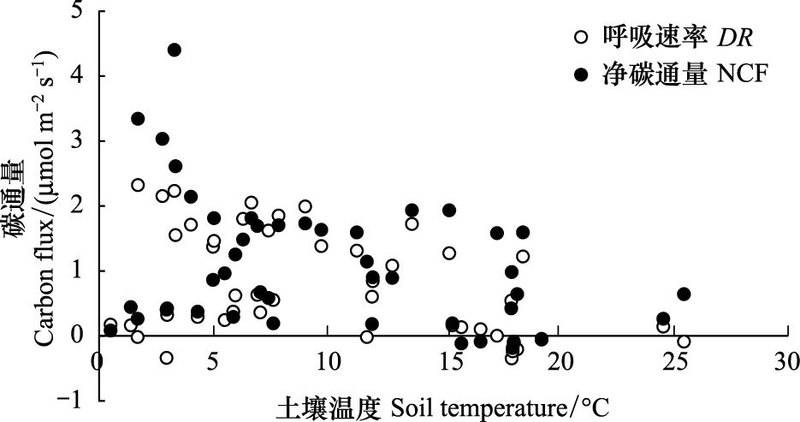
对藓类和藻类为主结皮覆盖土壤的NCF和DR与土壤温度的相关分析表明, 两类结皮覆盖土壤的NCF和DR均与温度无明显的相关关系(图 8, 图 9)。
|
| 图 8 土壤温度与藓类结皮覆盖土壤碳通量的关系 Fig. 8 The relationships between the CO2 flux and the soil temperatures in moss-crusted soil |
|
| 图 9 土壤温度与藻类结皮覆盖土壤碳通量的关系 Fig. 9 The relationships between the CO2 flux and the soil temperatures in algea-crusted Soil |
在沙漠中, 土壤有效水分是决定植被种类, 植物生理活性和其他相关生理过程的关键因素[13-14]。对于生物土壤结皮, 水分能够直接影响其光合与呼吸作用。而土壤水分与降水直接相关, 在干旱半干旱地区土壤中的水分绝大多数来自于降水。本研究表明降水会刺激藓类结皮和藻类结皮的碳释放, 并且随着降水量的增加, 碳释放量也有一定程度的增加, 这与前人的研究一致[15-17]。
研究中, 生物土壤结皮覆盖土壤的净碳通量在模拟降水后迅速到达峰值然后下降, 1h至2h后再次上升, 之后随着时间的推移逐渐下降至自然水平。对于这种现象, 可能有以下几个原因。首先, 降水前土壤水分处于干旱状态, 土壤空隙较大, 降雨后水分渗入土壤空隙将土壤空隙中的CO2排出, 这就增加了土壤碳排放[18-19];其次, 在干燥条件下土壤中可能累积一定的活性碳和呼吸底物, 水分的增加可能影响了土壤微生物活性从而增加了土壤碳排放[20]。随着时间推移这一部分的碳排放会迅速减少, 生物土壤结皮因为之前处于干燥状态而对水分的响应存在一定的延迟与滞后, 在一段时间后才能增加呼吸速率和光合速率, 所以在图中表现出了降水一段时间后碳通量的二次上升现象。两种结皮的净碳通量、呼吸速率、光合速率以及累积碳释放量在降水后均有明显的增加, 但在数值上有较大差异, 藓类结皮的净碳通量、呼吸速率和光合速率更高。这不仅是因为两种结皮自身存在着生理活性的差异, 藓类结皮拥有着比藻类结皮更强的呼吸与光合能力, 除此之外还存在其他影响因素。一方面, 藓类结皮能够保持较长时间的水分有效性, 因此能够在降水后长时间内保持湿润, 减缓水分蒸发和下渗, 保持自身活性。藻类结皮的保水持水能力较差, 在降水事件, 尤其是小降水事件后的20h之内回到原始水平。另一方面, 两种结皮覆盖土壤的性状也有所区别, 藓类结皮覆盖土壤孔隙度较大, 养分含量相对较高, 而藻类结皮覆盖土壤的土壤稳定性较差、粘粒含量很少。两种结皮的覆盖对水分小循环的影响和对土壤性状的改变所表现出的差异也符合生物土壤结皮从藻类到藓类、从低级到高级的演替规律[21]。
虽然有研究认为生物土壤结皮能够通过光合作用固定大气中的CO2, 是干旱半干旱区潜在的碳汇, 但本次研究结果表明模拟降水后生物土壤结皮覆盖土壤扮演着碳源的角色。两种生物土壤结皮覆盖土壤在模拟降水后的净碳通量都表现为碳释放, 这个过程中没有观测到生物土壤结皮的碳吸收, 说明结皮覆盖土壤在模拟降水的刺激下始终保持着碳源效应。这与前人的研究具有相同之处[22, 23]。这可能是由于生物土壤结皮的光合速率较低, 不能抵消土壤呼吸所导致的。研究中发现藓类结皮的光合速率最大达到2.04μmol m-2 s-1, 下降后基本在0至-1.5μmol m-2 s-1之间波动。藻类为优势种的结皮中光合速率通常为1 μmol m-2 s-1或更少[24-26]。研究地区频繁的干旱胁迫导致生物土壤结皮经常保持在休眠状态, 而在干旱休眠状态时的生物土壤结皮基本不具备光合能力。休眠中的生物土壤结皮在有了适当的水分时并不能立即完全表现出其光合生理活性, 需要一定时间响应。所以这有可能是实验选择的小降雨量引起的生物土壤结皮光合速率尤其是藻类结皮覆盖土壤光合速率较低且变化不明显的原因。
本研究中虽然根据自然降水情况设置了模拟降水, 但是没有连续长时间的在自然条件下监测, 同时也没有考虑某些特殊环境条件, 例如冰雪融水、极端降水等, 生物土壤结皮在干旱区碳循环中的功能以及碳循环中的碳源汇角色有待深入研究。
4 结论(1) 降水对生物土壤结皮覆盖土壤的净碳通量和呼吸有极显著激发作用。两种生物土壤结皮覆盖土壤的净碳通量、呼吸、平均碳通量和累积碳释放均随着降水的增加而增加, 各降水处理相比于对照差异显著。两种结皮覆盖土壤的光合速率在降水后也有增加的趋势, 其中藓类结皮覆盖土壤的光合速率增加趋势较明显, 各降水处理与对照差异显著。藻类结皮覆盖土壤的光合速率变化不明显, 只有在高降水量处理下才有较明显的增加。
(2) 两种生物土壤结皮覆盖土壤在模拟降水后的净碳通量、呼吸和光合速率变化规律差异显著。藓类结皮覆盖土壤在模拟降水后的净碳通量、呼吸和光合速率的极值显著高于藻类结皮, 同时藓类结皮覆盖土壤碳通量受降水激发的有效时间也高于藻类结皮覆盖土壤。两种生物土壤结皮覆盖土壤在模拟降水后48h内的累积碳释放随着降水量的增加而增加, 相对于对照差异显著, 且藓类结皮覆盖土壤的48h累计碳释放显著高于藻类结皮。
(3) 两种生物土壤结皮的净碳通量和呼吸速率与土壤水分有着较明显的相关性, 表现出随土壤水分增大而增大的趋势, 但与土壤温度没有明显的相关关系。
| [1] | Su Y G, Wu L, Zhou Z B, Liu Y B, Zhang Y M. Carbon flux in deserts depends on soil cover type:a case study in the Gurbantunggute Desert, North China. Soil Biology and Biochemistry, 2013, 58: 332–340. DOI:10.1016/j.soilbio.2012.12.006 |
| [2] | Belnap J, Lange O L. Biological Soil Crusts:Structure, Function, and Management. Berlin:Springer-Verlag, 2001: 239–257. |
| [3] | Wassmann R, Neue H U, Lantin R S, Aduna J B, Alberto M C R, Andales M J, Tan M J, van der Gon H A C D, Hoffmann H, Papen H, Rennenberg H, Seiler W. Temporal patterns of methane emissions from wetland rice fields treated by different modes of N application. Journal of Geophysical Research-Atmospheres, 1994, 991(D8): 16457–16462. |
| [4] | 李新荣, 贾玉奎, 龙利群, 王新平, 张景光. 干旱半干旱地区土壤微生物结皮的生态学意义及若干研究进展. 中国沙漠, 2001, 21(1): 4–11. |
| [5] | Grote E E, Belnap J, Housman D C, Sparks J P. Carbon exchange in biological soil crust communities under differential temperatures and soil water contents:implications for global change. Global Change Biology, 2010, 16(10): 2763–2774. DOI:10.1111/gcb.2010.16.issue-10 |
| [6] | Schlesinger W H, Raikes J A, Hartley A E, Cross A F. On the spatial pattern of soil nutrients in desert ecosystems. Ecology, 1996, 77(2): 364–374. |
| [7] | Jasoni R L, Smith S D, Arnone J A Ⅲ. Net ecosystem CO2 exchange in Mojave Desert shrub lands during the eighth year of exposure to elevated CO2. Global Change Biology, 2005, 11(5): 749–756. DOI:10.1111/gcb.2005.11.issue-5 |
| [8] | Wohlfahrt G, Fenstermaker L F, Arnone J A Ⅲ. Large annual net ecosystem CO2 uptake of a Mojave Desert ecosystem. Global Change Biology, 2008, 14(7): 1475–1487. DOI:10.1111/j.1365-2486.2008.01593.x |
| [9] | Xie J X, Li Y, Zhai C X, Li C H, Lan Z D. CO2 absorption by alkaline soils and its implication to the global carbon cycle. Environmental Geology, 2009, 56(5): 953–961. DOI:10.1007/s00254-008-1197-0 |
| [10] | José J J S, Bravo C R. CO2 exchange in soil algal crusts occurring in the trachypogon savannas of the Orinoco Llanos, Venezuela. Plant and Soil, 1991, 135(2): 233–244. DOI:10.1007/BF00010911 |
| [11] | 陈正宏. 高寒草甸沙化过程中生物结皮藻类组成及分布的变化[D]. 兰州: 兰州理工大学, 2009. |
| [12] | 苏延桂, 李新荣, 陈应武, 崔艳, 鲁艳. 温度和CO2浓度升高对荒漠藻结皮光合作用的影响. 应用生态学报, 2010, 21(9): 2217–2222. |
| [13] | Song W M, Chen S P, Wu B, Zhu Y J, Zhou Y D, Li Y H, Cao Y L, Lu Q, Lin G H. Vegetation cover and rain timing co-regulate the responses of soil CO2 efflux to rain increase in an arid desert ecosystem. Soil Biology and Biochemistry, 2012, 49: 114–123. DOI:10.1016/j.soilbio.2012.01.028 |
| [14] | Sponseller R A. Precipitation pulses and soil CO2flux in a Sonoran Desert ecosystem. Global Change Biology, 2007, 13(2): 426–436. DOI:10.1111/gcb.2007.13.issue-2 |
| [15] | Housman D C, Grote E E, Belnap J. Annual CO2 flux from a biological soil crust system on the Colorado Plateau:effects of increased temperature and summer precipitation//Ecological Society of America Annual Meeting Abstracts. 2007. |
| [16] | 赵蓉, 李小军, 赵洋, 杨昊天, 陈栋. 固沙植被区两类结皮斑块土壤呼吸对不同频率干湿交替的响应. 生态学杂志, 2015, 34(1): 138–144. |
| [17] | 赵洋, 齐欣林, 陈永乐, 张志山, 贾荣亮, 胡宜刚, 张鹏. 极端降雨事件对不同类型生物土壤结皮覆盖土壤碳释放的影响. 中国沙漠, 2013, 33(2): 543–548. DOI:10.7522/j.issn.1000-694X.2013.00074 |
| [18] | Anderson J M. Carbon dioxide evolution from two temperate, deciduous woodland soils. Journal of Applied Ecology, 1973, 10(2): 361–378. DOI:10.2307/2402287 |
| [19] | Birch H F. The effect of soil drying on humus decomposition and nitrogen availability. Plant and Soil, 1958, 10(1): 9–31. DOI:10.1007/BF01343734 |
| [20] | Gordon H, Haygarth P M, Bardgett R D. Drying and rewetting effects on soil microbial community composition and nutrient leaching. Soil Biology and Biochemistry, 2008, 40(2): 302–311. DOI:10.1016/j.soilbio.2007.08.008 |
| [21] | Zaady E, Kuhn U, Wilske B, Sandoval-Soto L, Kesselmeier J. Patterns of CO2 Exchange in biological soil crusts of successional age. Soil Biology and Biochemistry, 2000, 32(7): 959–966. DOI:10.1016/S0038-0717(00)00004-3 |
| [22] | 吴林, 苏延桂, 张元明. 模拟降水对古尔班通古特沙漠生物结皮表观土壤碳通量的影响. 生态学报, 2012, 32(13): 4103–4113. |
| [23] | 贾晓红, 辜晨, 吴波, 李元寿, 成龙, 李新荣. 干旱沙区生物土壤结皮覆盖土壤CO2通量对脉冲式降雨的响应. 中国沙漠, 2016(02): 423–432. |
| [24] | Lange O L, Belnap J, Reichenberge H. Photosynthesis of the cyanobacterial soil-crust lichen Collema tenax from arid lands in southern Utah, USA:role of water content on light and temperature responses of CO2 exchange. Functional Ecology, 1998, 12(2): 195–202. DOI:10.1046/j.1365-2435.1998.00192.x |
| [25] | Brostoff W N, Sharifi M R, Rundel P W. Photosynthesis of cryptobiotic soil crusts in a seasonally inundated system of pans and dunes in the western Mojave Desert, CA:field studies. Flora-Morphology, Distribution, Functional Ecology of Plants, 2005, 200(6): 592–600. DOI:10.1016/j.flora.2005.06.008 |
| [26] | Li X R, Zhou H Y, Wang X P, Zhu Y G, O'Conner P J. The effects of sand stabilization and revegetation on cryptogam species diversity and soil fertility in the Tengger Desert, Northern China. Plant and Soil, 2003, 251(2): 237–245. DOI:10.1023/A:1023023702248 |
 2017, Vol. 37
2017, Vol. 37