文章信息
- 彭阿辉, 王根绪, 杨阳, 肖瑶, 张莉, 杨燕
- PENG Ahui, WANG Genxu, YANG Yang, XIAO Yao, ZHANG Li, YANG Yan.
- 青藏高原高寒草甸两种优势植物的生长及其CNP化学计量特征对模拟增温的响应
- Effects of experimental warming on the growth and stoichiometrical characteristics of two dominant species (Kobresia pygmaea and Kobresia tibetica) in alpine meadow of the Tibetan Plateau
- 生态学报. 2017, 37(12): 4118-4127
- Acta Ecologica Sinica. 2017, 37(12): 4118-4127
- http://dx.doi.org/10.5846/stxb201606161173
-
文章历史
- 收稿日期: 2016-06-16
- 修订日期: 2016-11-04
2. 中国科学院大学, 北京 100049
2. University of Chinese Academy of Sciences, Beijing 100049, China
以全球变暖和大气CO2浓度升高为主要特征的全球气候变化正在改变着陆地生态系统的结构和功能, 威胁着人类的生存与健康, 因而受到世界各国政府和科学家的关注[1]。据联合国气候变化专门委员会(IPCC, 2013) 第五次气候变化评估报告[2], 2003—2013年大气平均温度比1900—1950年上升了0.78 ℃。作为全球气候变化的敏感区, 青藏高原平均海拔4000m以上, 气温增加幅度明显高于北半球及全球增温幅度[3], 成为研究气候变化对高寒生态系统影响模式和效应的理想场所。
气候变暖导致气温和土壤温度升高, 将直接或间接地影响植物的光合作用和生长速率[4-5]、植物体内元素含量[6-8]和生物量分配格局[7, 9-10], 进而引起群落结构和物种多样性的强烈变化。植物叶片的形态结构及解剖特征是由植物的生长发育状况、植物的遗传特征和环境因素等多因素共同决定的[11]。根系活力是根系生命力的综合指标, 根系活力强, 植物代谢旺盛, 则根系吸收能力强, 从而保证了逆境胁迫下植物对营养元素的吸收[12]。碳(C)、氮(N)和磷(P)作为植物生长所必需的营养元素, 虽然其含量在特定植物的特定生长阶段具有一定的变异性, 但C、N、P三者之间的化学计量比却是相对稳定的[13]。然而, 植物体内的C、N、P含量易受到气候变暖的强烈作用而发生变化, 从而影响植物的生长、C积累动态和N、P养分限制格局, 并将成为植物生长、生理过程发生紊乱的内在驱动因素之一[13]。
全球气候变化深刻影响着陆地生态系统的结构和功能, 尤其在高寒高海拔地区表现强烈[14]。在高原和高山极端环境影响下所形成的高寒草甸生态系统极其脆弱, 对全球变化和环境变化的响应更为迅速。高寒草甸和高寒沼泽是青藏高原腹地典型的植被类型, 其在生境上和物种组成上有很大差异。小嵩草(Kobresia pygmaea)和藏嵩草(Kobresia tibetica)分别作为青藏高原风火山地区高寒草甸和高寒沼泽的优势种, 对群落的组成和结构有明显的控制作用。目前, 基于增温对高寒草甸的研究多集中在植物群落组成、物种多样性和生物量等[5-6, 9-10, 13, 15], 关于增温对小嵩草和藏嵩草形态特征及其化学计量学特征研究较少, 尤其关于两种优势植物对温度增加的响应对比研究更为匮乏。因此本研究以青藏高原高寒草甸小嵩草和高寒沼泽藏嵩草为研究对象, 探讨气候变暖对青藏高原风火山地区小嵩草和藏嵩草的形态特征、养分分配策略和化学计量学特征的影响, 揭示二者对气候变暖的响应模式及差异, 为预测未来气候变暖情景下该区域植被群落结构和功能演变的可能格局提供理论基础。
1 材料与方法 1.1 研究区概况及试验设计实验区位于青藏高原腹地长江源区的风火山地区(92°50′—93°30′E, 34°40′—34°48′N), 气候属青藏高原干旱气候区, 年均气温-5.3 ℃, 降雨量270 mm, 且80%的降水发生在植物生长季(5—9月), 蒸发量1478 mm, 冻结期为9月至次年4月[16]。主要植被类型为高寒草甸和沼泽草甸[16], 其中高寒草甸主要分布于山地的阳坡、阴坡、圆顶山、滩地和河谷阶地, 分布上限可达5200 m左右;高寒沼泽主要分布在海拔3200—4800 m的河畔、湖滨、排水不畅的平缓滩地、山间盆地、蝶形洼地、高山鞍部、山麓潜水溢出带和高山冰雪带下缘等部位[16]。
采用国际冻原计划(International Tundra Experiment, ITEX)所采用的被动式增温法——开顶式气室法(OTCs), 建造开顶式小暖室, 温室采用有机玻璃纤维建造, 加工成正六边形圆台状开顶式小室, 小室的高度为40cm, 并保证圆台的上开口为60cm, 圆台的斜边与地面的夹角均为60°。2012年8月, 在研究区域选择植被分布相对均匀一致的高寒草甸和高寒沼泽样地作为研究对象, 随机布设6个1m×1m的样方, 每个样方的距离为3—5m。随机选取其中3个样方作为对照, 另外3个样方作为OTC增温处理。通过在OTC内和对照样地内设置传感器, 以测定OTC内与对照样地上气温和地下20cm土壤相对含水量, 每隔30min测定1次。试验地周围用网围栏封育, 禁止放牧。
1.2 样品的采集和分析2014年8月初, 在每个样方中, 随机选择10株植物, 测量其株高、叶长后, 将采集的叶片在野外立即用FAA固定液(福尔马林-冰醋酸-酒精)固定。采用常规石蜡切片法制片, 测量其解剖特征。根系总吸收面积和活跃吸收面积采用甲烯蓝吸附法测定, 单位重量总吸收面积和单位重量活跃吸收面积采用根系总吸收面积和活跃吸收面积除以鲜重重量[17]。土钻分层在各样方中取地下部分, 与地上部分样品一起经烘干、粉碎, 测定其C、N、P含量。植物叶片的C、N含量采用元素分析仪法(Elementar, VarioMacrocube, Germany), P含量测定采用酸溶-钼锑抗比色法, 于700nm处自外分光比色, 测定结果均用单位质量的养分含量表示, 并以此计算地上部分和地下部分的C/N、C/P和N/P。
1.3 数据处理用Microsoft Excel对各项测量数据进行描述性统计, 采用Origin 9.2统计软件进行单因素方差分析(One-Way ANOVA), 并作图。文中实验数值以平均值±标准误差表示, 以P < 0.05作为差异显著的标准。
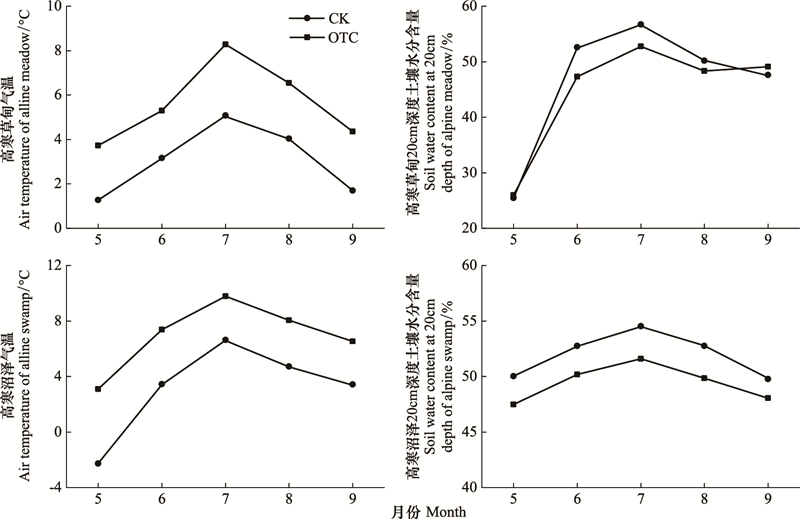
2 结果与分析 2.1 气温和土壤水分变化由图 1可知, 在植物生长季(5—9月)内OTC温室增温作用明显, 与对照相比高寒草甸月平均气温提高了2.59 ℃, 高寒沼泽提高3.10 ℃。在OTC增温作用下, 温室内0—20cm土层水分散失明显, 其中高寒草甸降低了1.83%, 高寒沼泽降低了2.53%(图 1)。
|
| 图 1 高寒草甸和沼泽草甸OTC内外的生长季内月平均气温及20cm土层含水量 Fig. 1 Monthly mean air temperature and soil water content inside and outside the OTCs in two meadows |
增温处理下小嵩草的叶长和叶片数量的均值与对照相比分别增加40%、73%, 统计检验显著;藏嵩草的株高和叶长均值与对照相比分别增加了12%、19%, 统计检验显著(P < 0.05)。
| 物种 Species |
处理 Treatment |
株高 Height/mm |
叶长 Length of leaf/mm |
叶片数量 Number of leaf |
| 小嵩草 | CK | 53.83±7.98a | 36.03±3.96b | 3.67±0.58b |
| Kobresia pygmaea | OTC | 65.66±3.09a | 50.45±5.17a | 6.33±1.53a |
| 藏嵩草 | CK | 123.74±4.96b | 77.26±2.71b | 3.67±0.58a |
| Kobresia tibetica | OTC | 138.50±7.18a | 92.16±6.75a | 5.33±1.53a |
| 不同小写字母代表不同处理间的差异显著 | ||||
从表 2中可看出模拟增温对小嵩草和藏嵩草的上表皮厚度、下表皮厚度、下表皮细胞角质层、叶肉细胞长和叶肉细胞宽均没有显著影响。
| 物种 Species |
处理 Treatment |
上表皮厚度 Thickness of upper cuticle/μm |
下表皮厚度 Thickness of low cuticle/μm |
下表皮细胞厚度 Thickness of lower epidermis cell/μm |
叶肉细胞长 length of mesophyll cell/μm |
叶肉细胞宽 Width of mesophyll cell/μm |
| 小嵩草 | CK | 22.16+7.7a | 19.88+3.27a | 6.04+2.57a | 24.01+1.84a | 15.5+2.08a |
| OTC | 19.28+3.91a | 13.79+4.45a | 3.4+0.31a | 19.95+3.49a | 13.42+2.86a | |
| 藏嵩草 | CK | 14.29+0.62a | 9.17+0.73a | 2.93+0.13a | 14.77+1.18a | 10.64+1.44a |
| OTC | 14.91+1.27a | 9.93+1.43a | 2.88+0.41a | 16.22+1.1a | 10.01+2.27a |
| 物种 Species |
处理 Treatment |
总吸收面积 Total absorption area/m2 |
活跃吸收面积 Active absorption area/m2 |
单位重量总吸收面积 Total absorption area per weight/(m2/g鲜重) |
单位重量活跃吸收面积 Active absorption area per weight/(m2/g鲜重) |
| 小嵩草 | CK | 0.59+0.09a | 0.21+0.03b | 1.2+0.16a | 0.43+0.07a |
| OTC | 0.67+0.14a | 0.31+0.08a | 1.23+0.17a | 0.58+0.16a | |
| 藏嵩草 | CK | 0.79+0.18a | 0.3+0.14a | 1.33+0.26a | 0.51+0.26a |
| OTC | 0.68+0.22a | 0.24+0.07a | 1.24+0.4a | 0.44+0.15a |
增温显著增加了小嵩草根系的活跃吸收面积, 对小嵩草的总吸收面积、单位重量总吸收面积和单位重量活跃吸收面积均没有显著影响;增温对藏嵩草根系活性指标均没有显著影响。
2.5 增温对地上部分C、N、P含量的影响小嵩草和藏嵩草C、N和P的化学计量特征对增温具有不同的响应特征。其中, 增温显著降低了小嵩草地上部分N含量, 对其C、P含量影响不显著。增温导致藏嵩草地上部分C、N含量分别降低了31%、44%, 统计检验显著;而对P含量影响不显著(图 2)。

|
| 图 2 增温对小嵩草和藏嵩草地上部分碳(C)、氮(N)、磷(P)含量的影响 Fig. 2 Effects of experimental warming on total carbon, nitrogen and phosphorus content in the above-ground of plant of Kobresia pygmaea and Kobresia tibetica 平均值±标准差, 6个重复; 不同小写字母表示在对照和OTC内差异显著 |
模拟增温后小嵩草地下部分C含量增加了2%, N、P含量分别降低了2%、16%, 统计检验不显著。增温引起藏嵩草地下部分C含量降低了10%, 统计检验显著;P含量降低了2%, 而N含量增加2%, 且统计检验不显著(图 3)。

|
| 图 3 增温对小嵩草和藏嵩草地下部分碳(C)、氮(N)、磷(P)含量的影响 Fig. 3 Effects of warming on the total carbon, nitrogen and phosphorus content in the under-ground of Kobresia pygmaea and Kobresia tibetica |
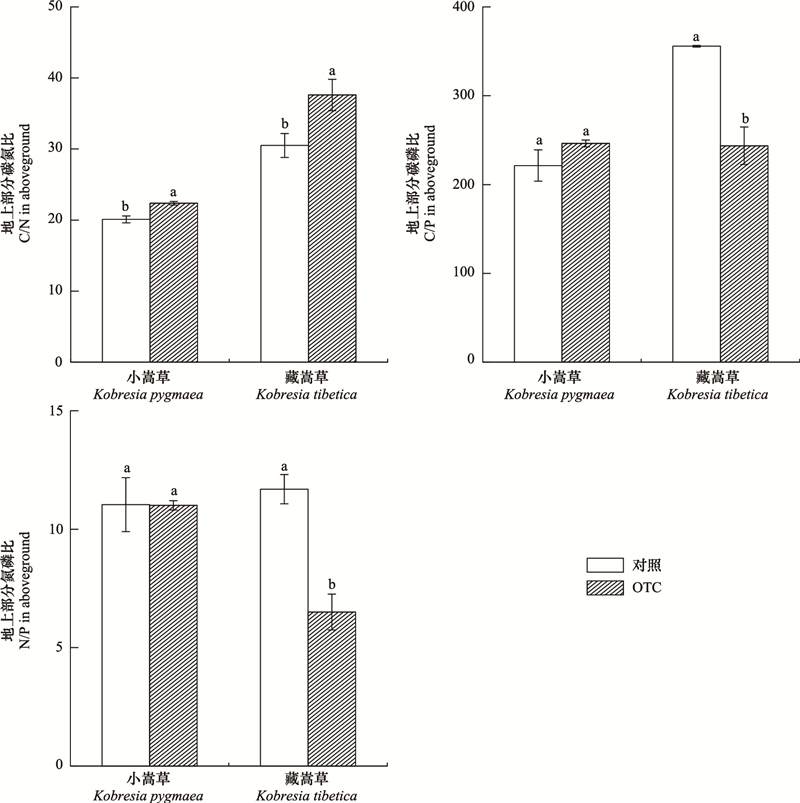
与对照相比, 模拟增温后小嵩草地上部分C/N增加了11%, 且统计检验显著。藏嵩草地上部分C/N增加了23%, 而C/P、N/P分别降低了31%、44%, 且统计检验均显著(图 4)。
|
| 图 4 增温对小嵩草和藏嵩草地上部分碳氮比、碳磷比、氮磷比的影响 Fig. 4 Effects of warming on the C/N, C/P, N/P of the aboveground of Kobresia pygmaea and Kobresia tibetica |
增温对小嵩草地下部分C/N、C/P、N/P没有影响;藏嵩草地下部分C/N、C/P比与对照相比降低了29%、10%, 且统计检验显著(图 5)。

|
| 图 5 增温对小嵩草和藏嵩草地下部分碳氮比、碳磷比、氮磷比的影响 Fig. 5 Effects of experimental warming on the C/N, C/P, N/P in the below-ground of Kobresia pygmaea and Kobresia tibetica |
温度是限制高寒地区植物生长的关键因素之一[18], 温度升高在一定程度上满足了植物对热量的需求, 从而有利于植物的生长和发育[19]。植物叶片株高、叶长和叶片数量是表征植物生长的重要指标, 也是对增温最直观的响应。Sarah等[20]对苔原158个植物群落的研究显示温度升高增加了植株高度, 本研究结果表明增温增加了小嵩草和藏嵩草的叶片长度和数量, 增加了生长高度, 促进了其形态生长, 这与周华坤[19]在青藏高原的矮嵩草草甸模拟增温试验中, 发现增温能促进植物群落的形态生长结果相一致。这可能是因为增温提高了高寒植物的光合能力和生长速率[4], 使生长季延长[21], 从而促进植物的生长。
较厚的叶片表皮和表皮附属物可以有效的抵抗强烈的紫外辐射和水分散失, 以维持叶片的正常生理代谢[22]。在本研究中, 由于藏嵩草发育区土壤水分条件较好, 因此相对于小嵩草来说, 具有表皮细胞较薄。而模拟增温后, 小嵩草的上表皮厚度、下表皮厚度角质层的厚度均发生降低, 但不显著。这似乎与增温处理下土壤含水量减少叶片应增大表皮厚度以提高水分利用效率相矛盾, 这可能由于在高寒草地中, 低温使水分常以固态的形式存在, 增温处理后, 土壤水分以液态存在, 小嵩草可通过根系吸收更多水分改变了水分亏损状态, 因此降低了其各组织厚度[23]。由于高寒沼泽中含水量较高, 虽然增温后高寒沼泽土壤含水量降低, 对于藏嵩草来说, 不需通过改变其解剖特征以防止水分蒸腾, 因此其解剖特征数据未发生明显改变。
3.3 增温对两种植物根系活性的影响根系活力是植物根系吸收、合成、氧化和还原能力的综合体现。根系活力的高低能反映植物的生长发育状况, 是其生命力的综合指标, 能够从本质上反映植物根系生长与土壤水分及其环境之间的动态关系[24]。单立山等[25]研究指出随干旱胁迫的增加红砂幼苗根系活力呈增加的趋势, 石岩等[26]研究指出:在土壤水分胁迫下小麦根系活力持续增加。本研究在小嵩草也得到相同的结论, 随增温引起土壤含水量含量降低, 小嵩草根系活跃吸收面积呈增加的趋势, 表明小嵩草为适应水分胁迫, 增强了根系呼吸作用, 释放大量的ATP从而使根系活力呈增强的趋势。本研究中增温后藏嵩草的根系活性呈降低趋势, 但不显著, 这可能是因为藏嵩草适应土壤水分饱和的生境, 模拟增温后, 虽然土壤含水量降低了, 但其值并未低于藏嵩草根系活性的阈值, 因此其根系活性并未改变。
3.3 增温对两种植物养分含量及养分利用效率的影响温度变化能影响植物的新陈代谢及自身养分元素的分配, 从而改变各元素在植物器官中的转移和再分配。由于物种之间存在差异性, 因此不同物种对增温的响应模式不同, 其分配方式也存在差异[27]。增温后小嵩草和藏嵩草叶片氮元素含量呈降低趋势, 而P元素含量变化不明显。本研究N元素含量变化的结果与Reich等[28]在全球尺度上、Han等[29]在全国尺度上及杨阔等[30]在青藏高原草地冠层尺度上得出的随年均温度的升高, N含量降低的结果相同。这可能是因为增温使温室内小气候趋于暖干化发展, 较为干旱的土壤阻碍了根系的生长, 引起了根系死亡率的增加, 因此降低了植物对干旱土壤中氮素的吸收, 且植物分解速率加快, 使得植物体内氮素向土壤中释放。另一个原因可能是增温改变植物群落的结构和组成, 破坏了植物群落原有的种间关系, 从而影响了小嵩草和藏嵩草的对N素的竞争。然而在本文中小嵩草和藏嵩草的地上部分P含量却没有受增温的影响, 这与Reich等[28]、Han等[29]和杨阔等[30]得出的随着年均温度的升高, P含量降低的结果不同。这可能是由于植物对养分的吸收具有选择性, 土壤中P含量可能处于过剩状态[31], 土壤中的P含量能满足植物的生长的需求, 因此其P含量没有下降。
C/N大小表示植物吸收单位养分元素含量所同化C的能力, 在一定程度上可以反映植物体养分元素的利用率[32]。增温提高了小嵩草和藏嵩草地上部分碳氮比, 这表明增温条件下, 小嵩草和藏嵩草能够更有效地利用N素, 增加其对氮素的利用效率。温度升高导致土壤中有机物质的降解速率增加, 提高氮矿化速率[33], 引起土壤中无机态氮含量增加[34, 35]。但藏嵩草对土壤氮的依赖性较低, 适宜于低氮环境, 当模拟增温后藏嵩草对氮素的竞争能力不如高寒沼泽的次优势种和伴生种[36], 因此藏嵩草叶片氮含量显著降低。当养分有效性越低, 植物提高养分利用效率以适应贫瘠的环境[37], 与此类似, 小嵩草和藏嵩草形成了以提高氮素利用效率以减缓N素限制的一种竞争性策略。
3.4 增温对两种植物地下部分C、N、P的影响在环境压力或资源有限的条件下, 植物通过自身调控分配地下和矿质元素的吸收, 以提高植物对资源的利用和吸收[38]。藏嵩草根系碳含量发生显著降低, 而小嵩草根系碳含量却变化不明显, 造成这两种优势物种根系碳含量变化趋势不一致的原因可能是由于高寒草甸和沼泽草甸生态系统的自然条件和增温后土壤水热状况不一致[39]。增温后高寒草甸土壤水分的减少限制了小嵩草的生长, 在一定程度上不利于根系的生长, 为了更好的适应OTC内暖干的环境, 小嵩草分配更多的碳水化合物用于植物的根系的生长以吸收更多矿质元素和水分供给地上部分生长, 使得碳水化合物的积累与根系生长速率一致, 抵消掉了根系生长带来的“稀释作用”[40], 因此小嵩草地下部分碳含量变化不明显。藏嵩草处于沼泽草甸于植物群落的最上层, 光照、水分和温度条件充足的条件下, 藏嵩草为了最大化的利用资源和促进植物生长, 将更多的有机碳和全氮等营养物质分配到叶片中, 且表层干热的环境不利于藏嵩草地下部分的生长, 使藏嵩草为优势物种的地下生物量分配比例减少, 因此藏嵩草地下部分碳含量明显下降。
在全球变暖背景下, 增温能在一定程度上促进小嵩草和藏嵩草的形态生长, 但对其叶片解剖特征影响不显著, 并且其能通过调节自身不同组分间C、N、P元素含量来应对未来的气候变化。本文仅对优势物种进行分析, 今后可对群落中不同物种进行扩展研究, 以便全面真实地揭示高寒生态系统对气候变暖的响应机制, 为高寒草甸生态系统应对气候变化, 进行适应性管理方面提供科学依据。
致谢: 感谢中铁西北科学研究院对野外实验工作的帮助。| [1] | Vitousek P M. Beyond global warming:ecology and global change. Ecology, 1994, 75(7): 1861–1876. DOI:10.2307/1941591 |
| [2] | IP CC. 2013. Climate change:The Physical science basis//The Fifth Assessment Report of Working Group I (WGI). |
| [3] | Liu X D, Chen B D. Climatic warming in the Tibetan Plateau during recent decades. International Journal of Climatology, 2000, 20(14): 1729–1742. DOI:10.1002/(ISSN)1097-0088 |
| [4] | Ya ng, Y an, Wa ng, Genxu, Klanderud, Ka ri, Ya ng, Liudong. Responses in leaf functional traits and resource allocation of a dominant alpine sedge (Kobresia pygmaea) to climate warming in the Qinghai-Tibetan Plateau permafrost region. Plant & Soil, 2011, 349(1/2): 377–387. |
| [5] | 石福孙, 吴宁, 吴彦, 王乾. 模拟增温对川西北高寒草甸两种典型植物生长和光合特征的影响. 应用与环境生物学报, 2009, 15(6): 750–755. |
| [6] | Klanderud, K. and Ø. Totland, Simulated climate change altered dominance hierarchies and diversity of an alpine biodiversity hotspot. Ecology, 2005. 86(8):p. 2047-2054. |
| [7] | 余欣超, 姚步青, 周华坤, 金艳霞, 杨月娟, 王文颖, 董世魁, 赵新全. 青藏高原两种高寒草甸地下生物量及其碳分配对长期增温的响应差异. 科学通报, 2015(4): 379–388. |
| [8] | 江肖洁, 胡艳玲, 韩建秋, 周玉梅. 增温对苔原土壤和典型植物叶片碳、氮、磷化学计量学特征的影响. 植物生态学报, 2014, 38(9): 941–948. |
| [9] | 李娜, 王根绪, 杨燕, 高永恒, 柳林安, 刘光生. 短期增温对青藏高原高寒草甸植物群落结构和生物量的影响. 生态学报, 2011, 31(4): 895–905. |
| [10] | 周华坤, 周兴民, 赵新全. 模拟增温效应对矮嵩草草甸影响的初步研究. 植物生态学报, 2000, 24(5): 547–553. |
| [11] | Lake J A, Quick W P, Beerling D J, Woodward F I. Plant development:signals from mature to new leaves. Nature, 2001, 411(6834): 154–154. DOI:10.1038/35075660 |
| [12] | 齐曼·尤努斯, 木合塔尔·扎热, 塔衣尔·艾合买提. 干旱胁迫下尖果沙枣幼苗的根系活力和光合特性. 应用生态学报, 2011, 22(7): 1789–1795. |
| [13] | 羊留冬, 杨燕, 王根绪, 郭剑英, 杨阳. 短期增温对贡嘎山峨眉冷杉幼苗生长及其CNP化学计量学特征的影响. 生态学报, 2011, 31(13): 3668–3676. |
| [14] | Grabherr G, Gottfried M, Pauli H. Climate effects on mountain plants. Nature, 1994, 369(6480): 448–448. |
| [15] | Yang Y, Wang G X, Yang L D, Guo J, Li N. Physiological responses of Kobresia pygmaea to warming in Qinghai-Tibetan Plateau permafrost region. Acta Oecologica, 2012, 39(2): 109–116. |
| [16] | 李娜, 王根绪, 高永恒, 王俊峰, 柳林安. 模拟增温对长江源区高寒草甸土壤养分状况和生物学特性的影响研究. 土壤学报, 2010, 47(6): 1214–1224. DOI:10.11766/trxb200904170177 |
| [17] | 张志良. 植物生理学实验指导. 北京: 高等教育出版社, 1990. |
| [18] | Ma W H, He J S, Yang Y H, Wang X P, Liang C Z, Anwar M, Zeng H, Fang J Y, Schmid B. Environmental factors covary with plant diversity-productivity relationships among Chinese grassland sites. Global Ecology & Biogeography, 2010, 19(2): 233–243. |
| [19] | 周华坤, 周兴民, 赵新全. 模拟增温效应对矮嵩草草甸影响的初步研究. 植物生态学报, 2000, 24(5): 547–553. |
| [20] | Elmendorf S C, Henry G H R, Hollister R D, Bj rk R G, Bjorkman A D, Callaghan T V, Collier L S, Cooper E J, Cornelissen J H C, Day T A, Fosaa A M, Gould W A, Grétarsdóttir J, Harte J, Hermanutz L, Hik D S, Hofgaard A, Jarrad F, Jónsdóttir I S, Keuper F, Klanderud K, Klein J A, Koh S, Kudo G, Lang S I, Loewen V, May J L, Mercado J, Michelsen A, Molau U, Myers-Smith I H, Oberbauer S F, Pieper S, Post E, Rixen C, Robinson C H, Schmidt N M, Shaver G R, Stenstr m A, Tolvanen A, Totland O, Troxler T, Wahren C H, Webber P J, Welker J M, Wookey P A. Global assessment of experimental climate warming on tundra vegetation:heterogeneity over space and time. Ecology Letters, 2012, 15(2): 164–175. DOI:10.1111/ele.2011.15.issue-2 |
| [21] | Walther, G.R., S. Beißner, and C.A. Burga, Trends in the upward shift of Alpine plants. Journal of Vegetation Science, 2009. 16(5):p. 541-548. |
| [22] | Kostina E, Wulff A, Julkunen-Tiitto R. Growth, structure, stomatal responses and secondary metabolites of birch seedlings (Betula pendula) under elevated UV-B radiation in the field. Trees, 2001, 15(8): 483–491. DOI:10.1007/s00468-001-0129-3 |
| [23] | 何涛, 吴学明, 贾敬芬. 青藏高原高山植物的形态和解剖结构及其对环境的适应性研究进展. 生态学报, 2007, 27(6): 2574–2583. |
| [24] | 斯琴巴特尔, 吴红英. 不同逆境对玉米幼苗根系活力及硝酸还原酶活性的影响. 干旱地区农业研究, 2004, 19(2): 67–70. |
| [25] | Shan L S, Yi L, Geng D M, Dong Q L. Ecological adaptation of reaumuria soongorica root system architecture to arid environments. Journal of Desert Research, 2012, 32(5): 1283–1290. |
| [26] | 石岩, 于振文, 位东斌, 余松烈. 土壤水分胁迫对小麦根系与旗叶衰老的影响. 西北植物学报, 1998, 18(2): 196–201. |
| [27] | Kimball B A. Theory and performance of an infrared heater for ecosystem warming. Global Change Biology, 2005, 11(11): 2041–2056. |
| [28] | Reich P B, Oleksyn J. Global patterns of plant leaf N and P in relation to temperature and latitude. Proceedings of the National Academy of Sciences of the United States of America, 2004, 101(30): 11001–11006. DOI:10.1073/pnas.0403588101 |
| [29] | Han W X, Fang J Y, Guo D L, Zhang Y. Leaf nitrogen and phosphorus stoichiometry across 753 terrestrial plant species in China. New Phytologist, 2005, 168(2): 377–385. DOI:10.1111/j.1469-8137.2005.01530.x |
| [30] | 杨阔, 黄建辉, 董丹, 马文红, 贺金生. 青藏高原草地植物群落冠层叶片氮磷化学计量学分析. 植物生态学报, 2010, 34(1): 17–22. |
| [31] | Marion G M, Hastings S J, Oberbauer S F, Oechel WC. Soil-plant element relationships in a tundra ecosystem. Ecography, 1989, 12(3): 296–303. DOI:10.1111/eco.1989.12.issue-3 |
| [32] | Farquhar G D, Ehleringer J R, Hubick K T. Carbon isotope discrimination and photosynthesis. Annual Review of Plant Physiology and Plant Molecular Biology, 2003, 40: 503–537. |
| [33] | Rustad L E, Campbell J, Marion G M, Norby R, Mitchell M, Hartley A, Cornelissen J, Gurevitch J. A meta-analysis of the response of soil respiration, net nitrogen mineralization, and aboveground plant growth to experimental ecosystem warming. Oecologia, 2001, 126(4): 543–562. DOI:10.1007/s004420000544 |
| [34] | 王其兵, 李凌浩, 白永飞, 邢雪荣. 气候变化对草甸草原土壤氮素矿化作用影响的实验研究. 植物生态学报, 2000, 24(6): 687–692. |
| [35] | Hart S C, Perry D A. Transferring soils from high-to low-elevation forests increases nitrogen cycling rates:climate change implications. Global Change Biology, 1999, 5(1): 23–32. DOI:10.1046/j.1365-2486.1998.00196.x |
| [36] | 王文颖, 周华坤, 杨莉, 李锦萍, 汪新川. 高寒藏嵩草(Kobresia tibetica)草甸植物对土壤氮素利用的多元化特征. 自然资源学报, 2014, 29(2): 249–255. DOI:10.11849/zrzyxb.2014.02.006 |
| [37] | Kost J A, Boerner R E J. Foliar nutrient dynamics and nutrient use efficiency in Cornus florida. Oecologia, 1985, 66(4): 602–606. DOI:10.1007/BF00379355 |
| [38] | Edwards E J, Benham D G, Marland L A, Fitter A H. Root production is determined by radiation flux in a temperate grassland community. Global Change Biology, 2004, 10(2): 209–227. DOI:10.1111/gcb.2004.10.issue-2 |
| [39] | 王根绪. 江河源区的生态环境变化及其综合保护研究. 兰州: 兰州大学出版社, 2000. |
| [40] | Körner C. The nutritional status of plants from high altitudes a worldwide comparison. Oecologia, 1989, 81(3): 379–391. DOI:10.1007/BF00377088 |
 2017, Vol. 37
2017, Vol. 37