文章信息
- 李迎春, 陈双林, 岳永德, 刘玉芳, 郭子武, 杨清平
- LI Yingchun, CHEN Shuanglin, YUE Yongde, LIU Yufang, GUO Ziwu, YANG Qingping.
- 持续淹水对河竹器官养分元素分配格局的影响
- Effect of continuous flooding stress on nutrient element distribution patterns in Phyllostachys rivalis modules
- 生态学报. 2017, 37(10): 3482-3493
- Acta Ecologica Sinica. 2017, 37(10): 3482-3493
- http://dx.doi.org/10.5846/stxb201602150282
-
文章历史
- 收稿日期: 2016-02-15
- 网络出版日期: 2017-02-17
2. 中国林业科学研究院亚热带林业研究所, 富阳 311400
2. Research Institute of Subtropical Forestry, Chinese Academy of Forestry, Fuyang 311400, China
江河洲滩、湖库、湿地等多种生境, 会长期或定期淹水, 形成消落带生境, 造成土壤缺氧环境, 导致植物根系生长发育受到抑制, 乃至死亡, 对植被覆盖及局部生态环境造成不良影响[1-2]。针对消落带的特点, 国内外从不同的水位梯度与水淹模式等角度, 开展了淹水区域植物存活率、生物量等方面的研究[3-5], 并筛选出耐淹性较强的枫杨 (Pterocarya stenoptera)[6-8]、秋华柳 (Salix variegata)[9-10]、柳树 (Salix sp.)[11]、池杉 (Taxodium ascendens)[12]、湿地松 (Pinus elliottii)[13]等木本植物和双穗雀稗 (Paspalum distichum)、香附子 (Cyperus rotundus) 等多年生草本植物用于该生境的植被恢复材料与重建[14]。筛选具有耐水淹能力且能够自我更新维持种群稳定的物种是消落带生态恢复的关键问题之一[15], 而在该生境下植物养分元素获取与C的同化则是限制生物量积累和种群更新的限制因子[16]。竹子是以根状茎无性繁殖为主的禾本科多年生大型植物, 集经济、生态和社会效益于一体, 具有强烈的生理整合能力, 能够集团抵御不良环境的胁迫。竹子一次造林后, 通过地下系统的延伸生长能形成纵横交错, 具有强大锚固土壤能力的系统, 是区域经济社会发展和生态环境治理上应用的重要植物类型。因此, 筛选耐水湿竹种为自然消落带生境植被恢复提供更为丰富的备选植物材料是非常必要的。
河竹 (Phyllostachys rivalis H. R. Zhao) 隶属禾本科倭竹族 (Shibataeeae) 刚竹属 (Phyllostachys Shieb. et Zucc.) 水竹组 (Sect. Heterocladae Z. P. Wang), 主要分布于浙江、福建及广东等地, 生于溪涧边、山沟旁, 性喜水湿, 其鞭根极为发达, 竹鞭韧皮部密生一圈肉眼可见的气孔, 具有耐淹植物的特征[3, 17]。前期研究发现河竹能够通过改变根系的形态可塑性和生理塑性以适应水淹胁迫, 能在长期淹水环境下自然生长更新[18], 有应用于岸带滩地生态重建的潜力。但长期淹水胁迫下河竹器官养分元素分配格局尚无研究报道, 限制了人们对竹类植物淹水环境下养分适应机制与化学计量特征的认识。植物养分元素的积累量是植物在一定生境条件下吸收营养元素的能力, 它能揭示植物物种的特性, 同时还能反映植物与环境之间的相互关系[19]。研究表明淹水胁迫促进桐花树 (Aegiceras corniculatum) 叶片N、K及根系P、K、Na、Fe的积累, 但抑制了叶片P、Ca、Fe、Mn、Cu和根系N、Ca、Mg、Mn、Cu的积累[20]。随着淹水时间的延长尖瓣海莲(Bruguiera sexangula var. rhynochopetala)幼苗叶片N、Mg、Al、P和Fe含量上升, 而K含量下降;茎干内Mg和根系Ca、Mg、Al、Mn和Fe含量下降;并导致幼苗各器官的化学计量特征的变化, 尤其以叶片的变化最明显, 茎干和根部变化较小[21]。不同植物基因型或同种植物不同器官养分元素的分布格局对水淹环境的响应与适应存在差异[17]。例如, 对不同耐渍基因型芝麻的研究表明, 水淹增加了根系Ca、P元素, 其中尤以耐渍品种根系P的增量最为突出, 而非耐渍品种根系K含量下降最多[22]。因此, 本文研究了不同淹水深度对河竹器官营养元素分配格局的影响, 旨在探讨:1) 养分元素含量对水淹梯度的差异性响应规律;2) 养分元素分配格局对水淹胁迫的响应特征;3) 水淹胁迫下元素化学计量特征与限制格局变化规律。通过上述问题的阐释, 可以了解河竹适应水淹的养分元素积累特征与调控规律, 为河竹淹水环境的营养生理适应机制研究提供理论参考。
1 材料与方法 1.1 试验材料与处理试验地位于浙江省临安市 (29°56′—30°23′N, 118°51′—119°52′E) 太湖源观赏竹种园。该地属中亚热带湿润季风气候, 年均气温15.4℃, 极端低温-10.3℃(2014年1月份), 极端高温44.5℃(2013年8月份), 年日照时数1850—1950 h, 日均高于10℃活动积温约5100℃左右, 年均无霜期235 d, 年降水量1250—1600 mm, 年均空气相对湿度80%以上。
2012年2月在种苗林中挖取2年生小丛状河竹苗, 竹苗规格为:地径 (1.0±0.2) cm, 全高 (1.03±0.38) m, 保留5—6盘枝, 选择规格基本一致的竹苗移栽到加仑盆中 (上端直径32 cm、下端直径23 cm、高度27 cm), 每盆栽植10株立竹。栽培基质为细沙与红壤体积比1:3均匀混合而成, 每盆填充基质约15 kg, 占容器体积的4/5。基质水解氮、速效磷、速效钾分别为198.47、67.25、74.16 mg/kg, pH值为5.8。通过定期喷灌保持盆栽苗水分供应, 并及时清除竹笋和杂草。2013年4月15日对盆栽苗进行淹水处理。试验设3个水淹梯度处理, 即对照 (CK), 淹水Ⅰ和淹水Ⅱ。对照实行定期人工喷灌供水使基质相对含水率保持在85%左右;淹水Ⅰ水位高于土壤表面5 cm, 植物地上部分相对淹水深度约5%;淹水Ⅱ水位高于土壤表面10 cm, 植物地上部分相对淹水深度约10%。试验盆栽苗置于方形水泥池 (长度4.3 m、宽度3.3 m和深度0.5 m) 中进行淹水处理, 试验期间保持设定水位。每个处理设置40个重复, 即盆栽苗40盆。
1.2 立竹器官取样与养分含量测定根据已有报道, 自然消落带淹水时间平均3个月左右, 最长时间可达6个月[7], 而前期试验表明, 淹水360 d后, 河竹仍能正常生长, 且表现出一定的更新能力。为探讨长期淹水对河竹营养元素积累和分配格局的影响, 故本研究设置淹水处理的时间分别为90、180 d和360 d时, 在设定时间, 随机选取各处理河竹盆栽苗各3盆, 将竹苗从盆中挖出, 冲洗干净鞭、根部的泥土, 然后将根、鞭、茎、枝、叶分离, 分别装袋带回实验室, 于烘箱内105 ℃杀青30 min, 在80℃烘干48 h至恒重。植物样品粉碎后过40目筛, 装袋储存于真空干燥器中以备化学分析。植物C含量采用重铬酸钾容量法测定, N含量采用凯氏定氮法测定, P含量采用钼锑抗比色法测定, K含量采用火焰光度法测定[23], Fe、Mg和Ca含量采用原子分光光度法测定[24]。
1.3 数据处理采用SPSS 20.0软件对试验数据进行单因素 (one-way ANOVA) 和重复测量 (repeated measures ANOVA) 方差分析方法, 用Duncan方法进行多重比较。用Excel 2010软件绘制图表。河竹器官C、N、P化学计量比用质量比表示。
2 结果与分析 2.1 淹水对河竹器官C含量的影响淹水对河竹各器官C含量的影响显著, 淹水时间、淹水深度和河竹器官间存在显著的交互作用 (P < 0.001)(表 1)。由图 1可知, 淹水90 d时, 与对照比较, 淹水Ⅰ和Ⅱ中叶、枝和根的C含量均显著增加 (P < 0.05), 而秆和鞭的C含量变化不显著 (P>0.05);淹水Ⅰ和Ⅱ比较, 仅有根C含量差异显著。淹水180 d, 与对照相比, 除淹水Ⅱ叶片中C含量显著升高 (P < 0.05) 外, 淹水Ⅰ和Ⅱ其它各器官的C含量差异不显著 (P>0.05)。淹水360 d, 除Ⅰ叶和枝的C含量与对照无显著差异外, 淹水Ⅱ各器官的C含量均显著降低。同一淹水深度, 随着淹水时间的延长, 河竹各器官C含量的变化趋势不同, 淹水Ⅰ的叶、枝为先降后升, 根为先升后降, 淹水Ⅱ的叶、枝、鞭和根均为显著降低, 淹水Ⅰ、Ⅱ处理秆的C含量变化不显著。

|
| 图 1 淹水环境下河竹叶、枝、秆、鞭和根的C相对含量 Fig. 1 Effect of flooding stress on C contents in the leaf, branch, stem and root of Ph.rivalis 试验设3个水淹梯度处理, 即对照 (CK), 淹水Ⅰ和淹水Ⅱ; 对照实行定期人工喷灌供水使基质相对含水率保持在85%左右;淹水Ⅰ水位高于土壤表面5 cm, 植物地上部分相对淹水深度约5%;淹水Ⅱ水位高于土壤表面10 cm, 植物地上部分相对淹水深度约10%;小写字母为相同器官相同处理时间不同处理间比较, 大写字母为相同器官相同处理不同处理时间间比较; 不同字母表示差异显著 (P < 0.05) |
| 变异来源 Variation source |
测定指标 Determined indexes |
df | F | P |
| 处理时间 (T) | C | 2 | 16.945 | < 0.001 |
| Treatment time | N | 2 | 47.521 | < 0.001 |
| P | 2 | 570.380 | < 0.001 | |
| K | 2 | 29.111 | < 0.001 | |
| Ca | 2 | 94.227 | < 0.001 | |
| Fe | 2 | 41.840 | < 0.001 | |
| Mg | 2 | 41.866 | < 0.001 | |
| 处理水平 (L) | C | 2 | 0.833 | 0.445 |
| Treatment level | N | 2 | 461.680 | < 0.001 |
| P | 2 | 766.377 | < 0.001 | |
| K | 2 | 320.532 | < 0.001 | |
| Ca | 2 | 335.462 | < 0.001 | |
| Fe | 2 | 91.845 | < 0.001 | |
| Mg | 2 | 82.060 | < 0.001 | |
| 器官 (O) | C | 4 | 12.931 | < 0.001 |
| Organ | N | 4 | 4168.701 | < 0.001 |
| P | 4 | 830.647 | < 0.001 | |
| K | 4 | 403.056 | < 0.001 | |
| Ca | 4 | 4324.254 | < 0.001 | |
| Fe | 4 | 578.365 | < 0.001 | |
| Mg | 4 | 476.118 | < 0.001 | |
| T×L | C | 4 | 16.1653 | < 0.001 |
| N | 4 | 8.302 | < 0.001 | |
| P | 4 | 67.951 | < 0.001 | |
| K | 4 | 14.869 | < 0.001 | |
| Ca | 4 | 16.817 | < 0.001 | |
| Fe | 4 | 4.627 | < 0.001 | |
| Mg | 4 | 20.015 | < 0.001 | |
| T×O | C | 8 | 9.831 | < 0.001 |
| N | 8 | 371.510 | < 0.001 | |
| P | 8 | 316.751 | < 0.001 | |
| K | 8 | 23.612 | < 0.001 | |
| Ca | 8 | 18.831 | < 0.001 | |
| Fe | 8 | 42.976 | < 0.001 | |
| Mg | 8 | 14.998 | < 0.001 | |
| L×O | C | 8 | 6.626 | < 0.001 |
| N | 8 | 21.155 | < 0.001 | |
| P | 8 | 57.719 | < 0.001 | |
| K | 8 | 15.231 | < 0.001 | |
| Ca | 8 | 42.545 | < 0.001 | |
| Fe | 8 | 17.505 | < 0.001 | |
| Mg | 8 | 6.100 | < 0.001 | |
| T×L×O | C | 16 | 6.061 | < 0.001 |
| N | 16 | 13.507 | < 0.001 | |
| P | 16 | 34.189 | < 0.001 | |
| K | 16 | 14.303 | < 0.001 | |
| Ca | 16 | 40.563 | < 0.001 | |
| Fe | 16 | 5.929 | < 0.001 | |
| Mg | 16 | 9.340 | < 0.001 |
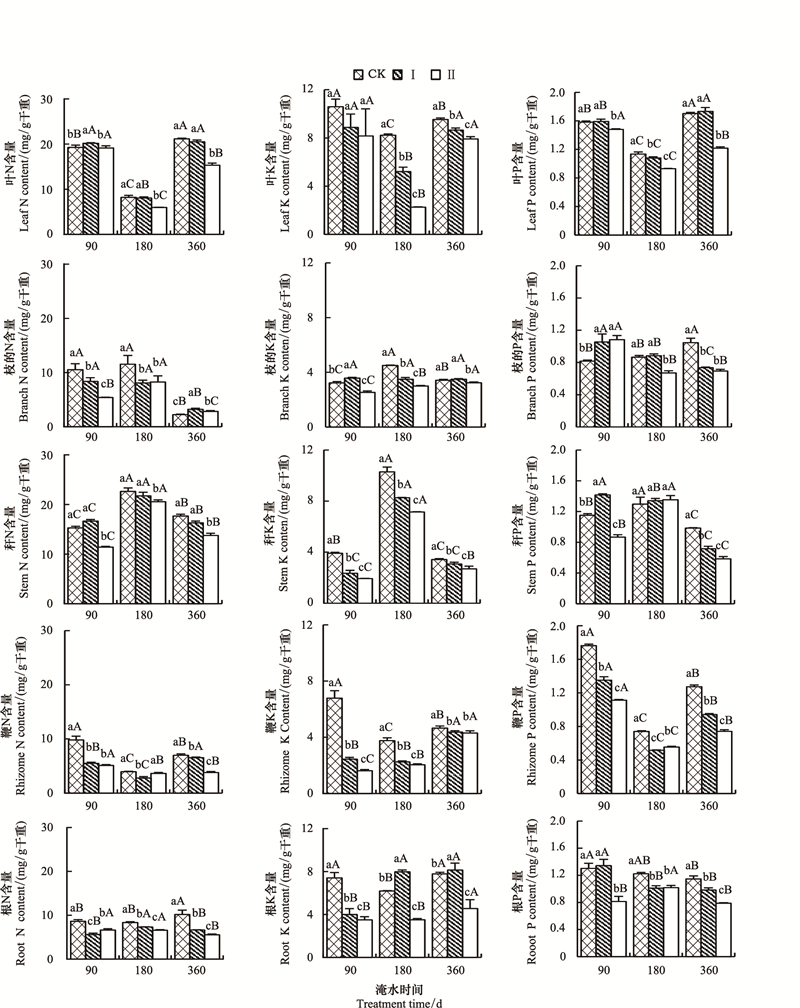
淹水处理对河竹各器官N、P、K含量影响显著, 但各器官之间不同元素的变化并不一致 (图 2)。不同处理时间、处理水平下, 各器官的N、P和K含量差异显著 (P < 0.001), 且处理时间、处理水平和器官间存在显著的交互作用 (P < 0.001)(表 1)。淹水90 d时, 与对照比较, 淹水Ⅰ中叶片N含量显著升高 (P < 0.05), 而秆N含量变化不显著, 枝、鞭和根均显著降低;枝、秆P含量显著增加而鞭中P含量则显著降低 (P < 0.05), 叶和根的P含量变化不显著;秆、鞭和根中K含量显著降低。随着淹水深度的增加, 各器官中的元素含量变化略有不同, 枝、秆、鞭和根N含量与对照比较显著降低 (P < 0.05);淹水Ⅱ枝中P含量显著升高 (P < 0.05), 与淹水Ⅰ无显著差别, 而叶、秆、鞭和根中P含量显著降低 (P < 0.05)。随着淹水时间的延长, 淹水Ⅰ、Ⅱ处理的叶和鞭中N含量先降后升, 而根中N含量变化则相反, 枝中N含量变化则呈降低趋势, 淹水180 d时秆中N含量达到最高;淹水Ⅰ、Ⅱ的叶和鞭P含量先降后升, 淹水Ⅰ枝、秆和根的P含量呈下降趋势, 而淹水Ⅱ秆和根P含量则先升后降;淹水Ⅰ、Ⅱ叶的K含量为先降后升, 淹水Ⅰ枝的K含量变化不显著, 淹水Ⅱ枝的K含量升高, 淹水Ⅰ、Ⅱ秆的K含量均先升后降, 鞭根的K含量均升高。
|
| 图 2 淹水环境下河竹叶、枝、秆、鞭和根的N、P和K含量 Fig. 2 Effect of flooding stress on N, P and K contents in the leaf, branch, stem and root of Ph.rivalis |
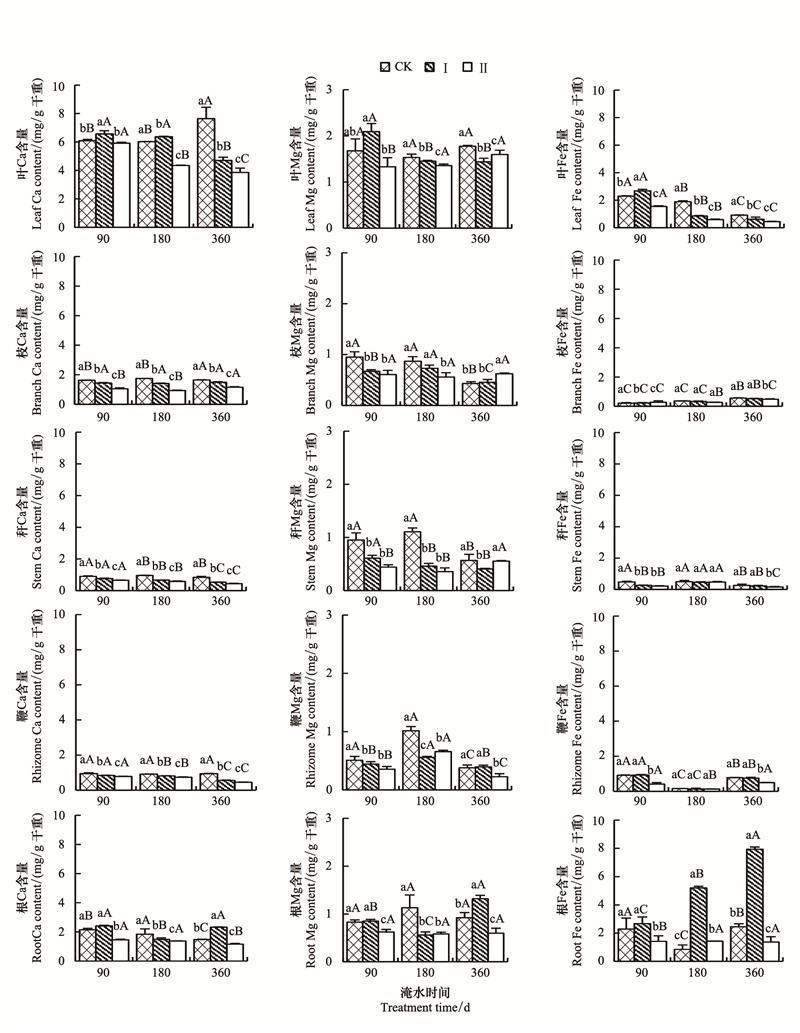
不同处理时间、处理水平下, 各器官的Ca、Fe和Mg含量差异显著 (P < 0.001), 且处理时间、处理水平和器官间存在显著的交互作用 (P < 0.001)(表 1)。如图 3所示, 淹水90 d时, 与对照比较, 枝、秆、鞭和根的Ca和Mg含量均显著降低, Fe含量也降低但未达显著差异。Ca、Mg和Fe含量基本保持显著降低的趋势, 唯一例外的是根中的Fe含量, 在淹水Ⅰ显著增加而淹水Ⅱ时急剧减少。随着淹水时间的延长, Ca含量, 在淹水Ⅰ、Ⅱ的叶、秆、鞭和根中均降低, 而枝为先降后升;Fe含量, 在淹水Ⅰ、Ⅱ处理的叶片中均显著降低, 而在枝中则升高, 秆和根中均为先升后降, 鞭为先降后升;Mg含量在淹水Ⅰ的叶和秆中均降低, 在枝和鞭中的含量在淹水180 d达到最高, 而根则相反, 在淹水Ⅱ处理处理的叶、枝和根中无显著差异, 秆中为先降后升, 鞭中为先升后降。
|
| 图 3 淹水环境下河竹叶、枝、秆、鞭和根的Ca、Fe和Mg含量 Fig. 3 Effect of flooding stress on Ca、Fe and Mg contents in the leaf, branch, stem and root of Ph.rivalis |
由表 2可知, 淹水对河竹器官中养分元素间的相关性有一定的影响, 但对不同淹水处理、不同器官中各元素的影响不同。淹水Ⅰ叶片的C、N、P和K相互之间的相关系数均高于对照, 说明元素间协同性增强;淹水Ⅱ叶片的C与N、P和K三者间的协同性减弱, 而Fe与C、P和Ca间的协同性增强。淹水Ⅰ和Ⅱ中枝的N与P相关性减弱, 淹水Ⅱ的C与P相关性增强;淹水Ⅱ秆的C与P、Ca、Fe呈极显著正相关, 与Mg呈极显著负相关, 而淹水Ⅰ秆的C与其它元素相关不显著, 淹水Ⅱ秆的N与P、K和Fe呈显著或极显著正相关, Mg与其它元素均呈负相关;除淹水Ⅱ鞭的C与N显著正相关外, 淹水Ⅰ和Ⅱ的C与其它元素均无相关性, 淹水Ⅰ鞭的N与P、K和Fe呈显著正相关, Mg与N、K、Fe呈显著负相关, 淹水Ⅱ鞭的N与P正相关, K与Ca、Fe与Mg均呈负相关, 其它元素无相关性;淹水Ⅰ根的N与P、Ca呈显著负相关, P与Ca、K与Mg呈正相关, 淹水Ⅱ根的C、N、Fe间呈极显著正相关, K与C、N、Fe呈极显著负相关。
| 器官 Organ |
处理 Treatment |
元素 Element |
N | P | K | Ca | Fe | Mg |
| 叶Leaf | CK | C | 0.695* | 0.733* | 0.261 | 0.830** | -0.822** | 0.581 |
| N | 0.995** | 0.792* | 0.724* | -0.362 | 0.585 | |||
| P | 0.749* | 0.577 | 0.227 | 0.634 | ||||
| K | 0.603 | 0.227 | 0.440 | |||||
| Ca | -0.837** | 0.456 | ||||||
| Fe | -0.377 | |||||||
| Ⅰ | C | 0.924** | 0.881** | 0.865** | -0.272 | 0.496 | 0.547 | |
| N | 0.974** | 0.951** | -0.426 | 0.385 | 0.450 | |||
| P | 0.903** | -0.587 | 0.197 | 0.297 | ||||
| K | -0.315 | 0.440 | 0.531 | |||||
| Ca | 0.654 | 0.582 | ||||||
| Ⅱ | Fe | 0.941** | ||||||
| C | 0.248 | 0.424 | -0.054 | 0.829** | 0.831** | -0.553 | ||
| N | 0.977** | 0.894** | 0.538 | 0.633 | 0.102 | |||
| P | 0.829** | 0.699** | 0.782** | -0.048 | ||||
| K | 0.315 | 0.396 | 0.076 | |||||
| Ca | 0.973** | -0.612 | ||||||
| Fe | -0.491 | |||||||
| 枝Branch | CK | C | -0.575 | 0.782* | 0.291 | 0.411 | 0.849** | -0.662 |
| N | 0.887** | 0.440 | 0.423 | -0.834** | 0.943** | |||
| P | -0.171 | -0.109 | 0.937** | -0.884** | ||||
| K | 0.959** | 0.074 | 0.209 | |||||
| Ca | 0.111 | 0.217 | ||||||
| Fe | -0.923** | |||||||
| Ⅰ | C | 0.258 | 0.612 | 0.488 | -0.077 | -0.340 | 0.299 | |
| N | 0.832** | 0.366 | -0.748* | -0.936** | 0.819** | |||
| P | 0.438 | -0.465 | -0.875** | 0.427 | ||||
| K | -0.027 | -0.373 | 0.173 | |||||
| Ca | 0.566 | -0.732* | ||||||
| Fe | -0.668* | |||||||
| Ⅱ | C | -0.048 | 0.988** | -0.874** | 0.118 | -0.321 | 0.678* | |
| N | -0.065 | -0.274 | -0.874** | -0.743* | -0.302 | |||
| P | -0.890** | 0.112 | -0.355 | 0.629 | ||||
| K | 0.273 | 0.723* | -0.328 | |||||
| Ca | 0.731* | 0.443 | ||||||
| Fe | 0.269 | |||||||
| 秆Stem | CK | C | 0.054 | 0.484 | 0.214 | 0.444 | 0.296 | 0.520 |
| N | 0.612 | 0.918** | 0.174 | 0.253 | 0.426 | |||
| P | 0.811** | 0.758* | 0.810** | 0.859** | ||||
| K | 0.483 | 0.563 | 0.708* | |||||
| Ca | 0.827** | 0.862** | ||||||
| Fe | 0.852** | |||||||
| Ⅰ | C | 0.259 | 0.002 | 0.210 | 0.075 | 0.201 | 0.027 | |
| N | 0.434 | 0.934** | 0.472 | 0.789* | -0.195 | |||
| P | 0.305 | 0.982** | 0.489 | 0.705* | ||||
| K | 0.389 | 0.873** | -0.341 | |||||
| Ca | 0.613 | 0.651 | ||||||
| Fe | -0.119 | |||||||
| Ⅱ | C | 0.490 | 0.889** | 0.572 | 0.892** | 0.802** | -0.904** | |
| N | 0.787* | 0.967** | 0.233 | 0.890** | -0.582 | |||
| P | 0.868** | 0.758* | 0.957** | -0.843** | ||||
| K | 0.365 | 0.937** | -0.662 | |||||
| Ca | 0.571 | -0.684* | ||||||
| Fe | -0.858** | |||||||
| 鞭Rhizome | CK | C | -0.228 | -0.207 | -0.393 | 0.001 | 0.114 | -0.430 |
| N | 0.987** | 0.920** | 0.440 | 0.931** | -0.740* | |||
| P | 0.948** | 0.523 | 0.945** | -0.757* | ||||
| K | 0.435 | 0.815** | -0.553 | |||||
| Ca | 0.520 | -0.583 | ||||||
| Fe | -0.915** | |||||||
| Ⅰ | C | 0.364 | -0.073 | 0.446 | -0.484 | 0.102 | -0.550 | |
| N | 0.699* | 0.762* | -0.642 | 0.875** | -0.937** | |||
| P | 0.097 | 0.076 | 0.949** | -0.639 | ||||
| K | -0.979** | 0.386 | -0.707* | |||||
| Ca | -0.230 | 0.620 | ||||||
| Fe | -0.818** | |||||||
| Ⅱ | C | 0.742* | 0.634 | -0.551 | 0.578 | 0.085 | -0.101 | |
| N | 0.947** | -0.513 | 0.494 | 0.368 | -0.307 | |||
| P | -0.329 | 0.304 | 0.569 | -0.522 | ||||
| K | -0.990** | 0.542 | -0.604 | |||||
| Ca | -0.560 | 0.623 | ||||||
| Fe | -0.950** | |||||||
| 根Root | CK | C | -0.456 | 0.044 | -0.951** | 0.526 | -0.562 | 0.504 |
| N | -0.490 | 0.600 | -0.774* | 0.439 | -0.169 | |||
| P | -0.007 | 0.750* | 0.165 | -0.171 | ||||
| K | -0.529 | 0.728* | -0.502 | |||||
| Ca | -0.159 | 0.184 | ||||||
| Fe | -0.485 | |||||||
| Ⅰ | C | 0.212 | 0.049 | -0.644 | 0.250 | -0.288 | -0.504 | |
| N | -0.875** | 0.042 | -0.771* | -0.452 | -0.265 | |||
| P | -0.482 | 0.938** | 0.205 | -0.144 | ||||
| K | -0.653 | 0.175 | 0.868** | |||||
| Ca | 0.289 | -0.361 | ||||||
| Fe | 0.231 | |||||||
| Ⅱ | C | 0.892** | 0.203 | -0.867** | 0.900** | 0.066 | 0.049 | |
| N | 0.569 | -0.952** | 0.903** | 0.155 | -0.246 | |||
| P | -0.527 | 0.326 | 0.007 | -0.341 | ||||
| K | -0.937** | -0.154 | 0.061 | |||||
| Ca | 0.150 | -0.039 | ||||||
| Fe | -0.337 | |||||||
| 试验设3个水淹梯度处理, 即对照 (CK), 淹水Ⅰ和淹水Ⅱ; 对照实行定期人工喷灌供水使基质相对含水率保持在85%左右;淹水Ⅰ水位高于土壤表面5 cm, 植物地上部分相对淹水深度约5%;淹水Ⅱ水位高于土壤表面10 cm, 植物地上部分相对淹水深度约10%; *为P < 0.05, **P < 0.01, N=9 | ||||||||
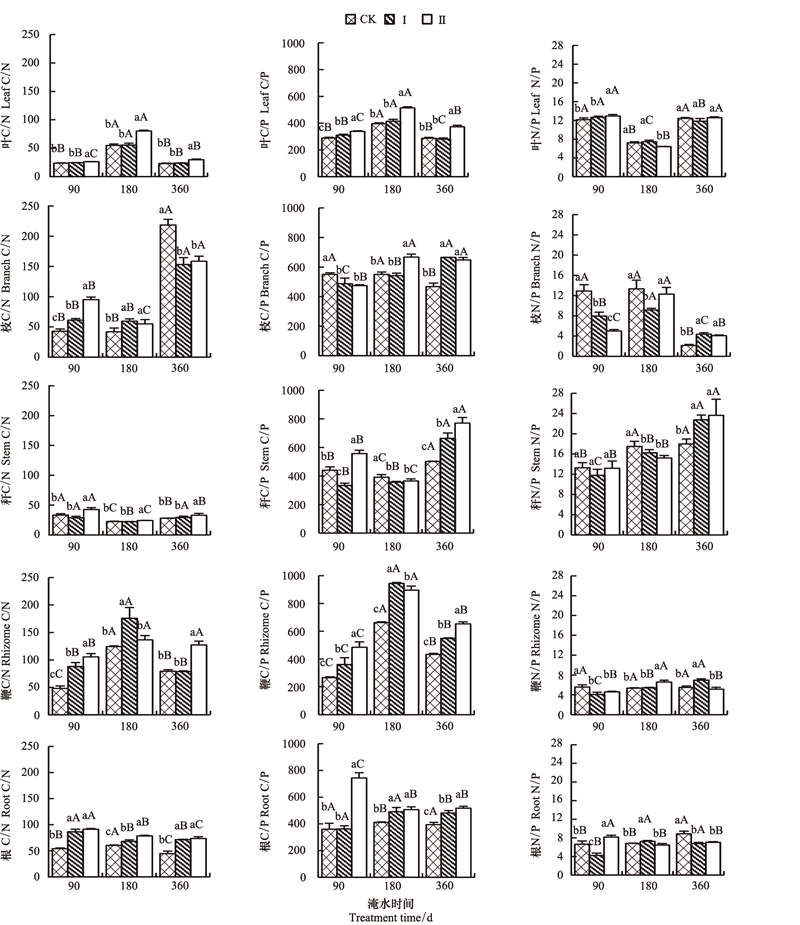
从图 4可知, 淹水对河竹器官的C/N、C/P和N/P有显著影响, 但各构件的变化趋势不同。淹水90d时, 淹水Ⅰ各构件的C/N除鞭根显著高于对照 (P < 0.05) 外, 叶、枝、秆的与对照无显著差异 (P>0.05)。淹水Ⅱ河竹各构件C/N均显著高于对照 (P < 0.05);淹水Ⅰ和Ⅱ叶、鞭和根的C/P均显著高于对照 (P < 0.05);淹水Ⅰ和Ⅱ秆的N/P与对照差异不显著, 而枝、鞭均显著降低。随着淹水时间的延长, 同一处理C/N、C/P和N/P的变化趋势不同, 叶片和鞭的C/N各处理均呈倒“V”变化, 而枝和秆呈“V”型, 淹水Ⅰ、Ⅱ根变化与对照相反, 呈先降后升的趋势;C/P叶和鞭各处理均呈倒“V”变化, 淹水Ⅰ、Ⅱ枝呈升高趋势, 秆呈“V”型变化, 淹水Ⅰ根与对照变化一致, 先升高后平稳, 而淹水Ⅱ相反;淹水Ⅰ、Ⅱ中叶片N/P与对照均呈“V”变化, 但淹水Ⅰ叶片的N/P与对照差异不显著 (P<0.05), 枝和秆呈倒“V”变化, 淹水Ⅰ鞭呈升高趋势, 而淹水Ⅱ鞭先升高后降低, 淹水Ⅱ根和对照为先降后升, 而淹水Ⅰ根呈倒“V”。
|
| 图 4 淹水环境下河竹器官C、N、P化学计量比 Fig. 4 The stoichiometric ratio of C, N and P in organs of Ph. rivalis under flooding stress |
C元素是构成植物体内干物质的主要元素, 并为植物的新陈代谢、生长发育和繁殖等提供能源物质[25]。河竹短时间淹水 (90 d), 植株叶片的C含量增加, 这是河竹植株适应水淹环境的应激反应, 促进光合等生理反应, 从而有利于有机物质的合成积累, 增加河竹植株生命活性和抗逆能力。随着淹水时间的延长 (180 d), C含量维持稳定状态, 至淹水360 d, 植株C含量降低, 尤其淹水10 cm处理显著降低, 这与淹水胁迫下秋茄 (Kandelia candel) 叶片的C含量变化一致[26], 可能是河竹光合作用变弱, CO2同化能力降低, 导致干物质合成减少, 从而减低植株体内C含量。木本植物的根、茎中C元素浓度高于叶, 是由于这些器官主要是由木质素和纤维素等富含C元素的多糖物质组成, 起输导和支撑作用[25, 27], 这些多糖物质是植物体的骨架性物质。本研究中持续淹水后河竹鞭中的C含量最高, 竹鞭为竹的繁殖与输导组织器官, 说明河竹竹鞭在淹水条件下仍具有很强的生长势。
3.2 持续淹水对河竹各器官矿质元素分配格局的影响淹水造成根系周围土壤缺氧, 影响根系的呼吸, 从而影响营养元素在植物体内的运输和分布。持续性淹水严重阻碍小麦对N、P和K的吸收, 降低地上部分N素含量和累积量[28]。本研究中持续淹水对河竹器官矿质元素含量的影响达到显著或极显著水平, 尤其对叶和根的矿质元素影响更显著, 淹水5 cm, 处理90 d时, 河竹叶片N、P、Ca、Fe和Mg含量均显著升高, K含量变化不显著, 而根的N、P含量则显著降低, K、Ca、Fe和Mg含量略有升高, 未达显著水平。Ca对细胞膜稳定性有重要作用, P为蛋白质的成份和能量梭子ATP的组成元素, K是活跃的生命元素, 叶片是进行光合作用的主要场所, 其代谢过程需要各种必需的矿质元素, 以上元素的变化是河竹植株适应淹水的主动反应, 是生理代谢加强的一种表现。持续淹水90 d, 影响河竹根系吸收养分能力, 减少了对N、P的吸收和积累, 但叶片中的N、P、Ca、Fe和Mg含量升高, 表明淹水促进河竹矿质元素向地上部分运输, 以增强叶片的生理代谢, 来适应淹水环境。淹水90 d对河竹吸收Ca、Mg等的影响较小, 这是因为根系对这些离子的吸收不需要消耗能量, 可在吸收水分的同时摄入, 所以植物体内含量的变化不大[29]。但持续淹水180 d和360 d时, 河竹各构件的矿质元素除根部的K、Fe和Mg含量外, 其它元素均显著降低, 这是可能是由于河竹自身机能下降, 导致对离子的吸收能力也下降。Fe元素在河竹根部随着淹水持续时间的延长而大量积累, 这可能是河竹在淹水条件下的一种普通适应机制, 通过根表面形成铁氧化合物保护膜来维持正常的生理代谢[30]。
3.3 持续淹水对河竹器官养分元素之间关系的影响植物组织中的C/N和C/P比反映了植物的生长速度, 代表着植物吸收养分所同化C的能力, 能在一定程度上表示植物的养分利用效率[31], 并与植物的N和P利用效率有关, N/P则能反映N或P的丰缺程度[32]。本研究中, 持续淹水10 cm河竹叶片中C/N、C/P较对照显著增加, 而N/P较对照差异不显著, 说明河竹在淹水条件下具有较高内稳定性, 通过提高C同化能力来提高养分利用效率来适应养分吸收抑制的不利影响。植物器官尤其是叶片的N/P被广泛用来诊断植物个体、群落和生态系统的氮磷养分限制格局[33-36]。本试验淹水及对照组的河竹叶片N/P均小于14, N/P值比值较小的原因, 可能与河竹的生物学特性有关, 说明河竹的生长主要受N素限制。K、Ca、Mg和Fe是植物生长所必需的大量矿质元素, 具有重要的生理功能, 但这些离子只有处于相对平衡时才能发挥正常的生理作用, 而平衡关系的破坏将对其生理作用产生不利影响[36]。本研究结果显示, 淹水5 cm, 水位深度对元素关系产生明显影响, 淹水5cm叶片的C-K、N-K、P-K、Fe-Ca和Fe-Mg相关系数升高, 元素间协同性增强;淹水10cm时, 相关系数明显下降, 元素间的协同性减弱。叶片的CK、N-K、P-K、Fe-Ca和Fe-Mg相关系数间升高, 说明持续淹水后河竹器官元素间协同性增强, 有利于河竹适应淹水环境。
| [1] | 曹福亮, 蔡金峰, 汪贵斌, 张往祥. 淹水胁迫对乌桕生长及光合作用的影响. 林业科学, 2010, 46(10): 57–61. DOI:10.11707/j.1001-7488.20101009 |
| [2] | 赵竑绯, 赵阳, 张驰, 徐小牛. 模拟淹水对杞柳生长和光合特性的影响. 生态学报, 2013, 33(3): 898–906. |
| [3] | Robertson A I, Bacon P, Heagney G. The responses of floodplain primary production to flood frequency and timing. Journal of Applied Ecology, 2001, 38(1): 126–136. DOI:10.1046/j.1365-2664.2001.00568.x |
| [4] | 何斌源, 赖廷和, 陈剑锋, 邱广龙. 两种红树植物白骨壤 (Avicennia marina) 和桐花树 (Aegiceras corniculatum) 的耐淹性. 生态学报, 2007, 27(3): 1130–1138. |
| [5] | 衣英华, 樊大勇, 谢宗强, 陈芳清. 模拟淹水对枫杨和栓皮栎气体交换、叶绿素荧光和水势的影响. 植物生态学报, 2006, 30(6): 960–968. |
| [6] | 衣英华, 樊大勇, 谢宗强, 陈芳清. 模拟淹水对池杉和栓皮栎光合生理生态过程的影响. 生态学报, 2008, 28(12): 6025–6033. DOI:10.3321/j.issn:1000-0933.2008.12.030 |
| [7] | 贾中民, 魏虹, 田晓峰, 李昌晓. 长期水淹对枫杨幼苗光合生理和叶绿素荧光特性的影响. 西南大学学报:自然科学版, 2009, 31(5): 124–129. |
| [8] | 吕茜. 三峡库区两种适生树种幼苗对土壤水分含量变化的光合与生长响应[D]. 重庆: 西南大学, 2010. |
| [9] | 陈芳清, 郭成圆, 王传华, 许文年, 樊大勇, 谢宗强. 水淹对秋华柳幼苗生理生态特征的影响. 应用生态学报, 2008, 19(6): 1229–1233. |
| [10] | 秦洪文, 刘云峰, 刘正学, 周大祥, 李彦杰, 刘仁华, 杨俊年, 石汝杰, 甘丽萍, 胡莲, 万成炎, 王敬. 三峡水库消落区模拟水淹对2种木本植物秋华柳Salix variegata和地果Ficus tikoua生长的影响. 西南师范大学学报:自然科学版, 2012, 37(10): 77–81. |
| [11] | 钟彦, 刘正学, 秦洪文, 熊瑛, 向丽霞, 刘锐, 杨艳, 马睿. 冬季淹水对柳树生长及恢复生长的影响. 南方农业学报, 2013, 44(2): 275–279. |
| [12] | 李昌晓, 钟章成. 三峡库区消落带土壤水分变化条件下池杉幼苗光合生理响应的模拟研究. 水生生物学报, 2005, 29(6): 712–716. |
| [13] | 张晔, 李昌晓. 水淹与干旱交替胁迫对湿地松幼苗光合与生长的影响. 林业科学, 2011, 47(12): 158–164. |
| [14] | 樊大勇, 熊高明, 张爱英, 刘曦, 谢宗强, 李兆佳. 三峡库区水位调度对消落带生态修复中物种筛选实践的影响. 植物生态学报, 2015, 39(4): 416–432. DOI:10.17521/cjpe.2015.0041 |
| [15] | 戴方喜, 许文年, 刘德富, 陈方清. 对构建三峡库区消落带梯度生态修复模式的思考. 中国水土保持, 2006(1): 34–36. |
| [16] | 孙崇玉, 刘景双, 王洋, 郑娜, 窦晶鑫, 赵光影. 三江平原湿地小叶章各器官主要营养元素特征. 湿地科学, 2011, 9(2): 157–162. |
| [17] | Kozlowski T T. Responses of woody plants to flooding and salinity. Tree Physiology, 1997, 17(17): 490–490. |
| [18] | 刘玉芳, 陈双林, 李迎春, 陈珊, 郭子武. 河竹鞭根对长期淹水环境的生理响应. 林业科学研究, 2014, 27(5): 621–625. |
| [19] | 金茜, 王瑞, 周向睿, 周志宇, 卢鑫, 赵萍, 李金辉, 周媛媛. 水淹胁迫对紫穗槐生长及营养元素积累的影响. 草业科学, 2013, 30(6): 904–909. |
| [20] | 罗美娟, 崔丽娟, 张守攻, 黄雍容, 何文广. 淹水胁迫对桐花树幼苗水分和矿质元素的影响. 福建林学院学报, 2012, 32(4): 336–340. |
| [21] | 刘滨尔, 廖宝文, 李玫, 陈玉军, 管伟. 不同潮汐淹浸程度下2种红树植物化学计量特征. 华南农业大学学报, 2014, 35(1): 86–92. |
| [22] | 王文泉, 张福锁, 郑永战, 梅鸿献. 厌氧胁迫下芝麻不同耐渍基因型形态、生理及矿质元素变化的比较研究. 应用生态学报, 2002, 13(4): 421–424. |
| [23] | 郑淑霞, 上官周平. 黄土高原地区植物叶片养分组成的空间分布格局. 自然科学进展, 2006, 16(8): 965–973. |
| [24] | Hunt J. Dilute hydrochloric acid extraction of plant material for routine cation analysis. Communications in Soil Science and Plant Analysis, 1982, 13(1): 49–55. DOI:10.1080/00103628209367243 |
| [25] | 李单凤, 于顺利, 王国勋, 方伟伟. 黄土高原优势灌丛营养器官化学计量特征的环境分异和机制. 植物生态学报, 2015, 39(5): 453–465. |
| [26] | 何缘, 张宜辉, 于俊义, 黄冠闽, 林鹏. 淹水胁迫对秋茄 (Kandelia candel) 幼苗叶片C、N及单宁含量的影响——一个关于碳素-营养平衡假说的实验. 生态学报, 2006, 28(10): 4725–4731. |
| [27] | Freudenberg K, Neish A C. Constitution and Biosynthesis of Lignin. Berlin: Springer-Verlag, 1968: 199–199. |
| [28] | 蒋丽娜, 徐姗, 常江, 郜红建, 章力干. 持续淹水对小麦养分吸收动态和产量的影响. 中国农学通报, 2012, 28(27): 113–117. |
| [29] | 陆景陵. 植物营养学-上册 (第二版). 北京: 中国农业大学出版社, 2003. |
| [30] | 刘玉芳, 陈双林, 李迎春, 陈珊, 郭子武, 杨清平. 长期淹水对河竹鞭根养分化学计量特征的影响. 西北植物学报, 2015, 35(2): 350–355. |
| [31] | Wardle D A, Walker L R, Bardgett R D. Ecosystem properties and forest decline in contrasting long-term chronosequences. Science, 2004, 305(5683): 509–513. DOI:10.1126/science.1098778 |
| [32] | 韩文轩, 吴漪, 汤璐瑛, 陈雅涵, 李利平, 贺金生, 方精云. 北京及周边地区植物叶的碳氮磷元素计量特征. 北京大学学报:自然科学版, 2009, 45(5): 855–860. |
| [33] | Aerts R, ChapinⅢ F S. The mineral nutrition of wild plants revisited: a re-evaluation of processes and patterns. Advances in Ecological Research, 1999, 30: 1–67. DOI:10.1016/S0065-2504(08)60016-1 |
| [34] | Güsewell S, Koerselman W, Verhoeven J T A. Biomass N:P ratios as indicators of nutrient limitation for plant populations in wetlands. Ecological Applications, 2003, 13(2): 372–384. DOI:10.1890/1051-0761(2003)013[0372:BNRAIO]2.0.CO;2 |
| [35] | Drenovsky R E, Richards J H. Critical N:P values: predicting nutrient deficiencies in desert shrublands. Plant and Soil, 2004, 259(1/2): 59–69. DOI:10.1023/B:PLSO.0000020945.09809.3d |
| [36] | Jeyasingh P D, Weider L J, Sterner R W. Genetically-based trade-offs in response to stoichiometric food quality influence competition in a keystone aquatic herbivore. Ecology Letters, 2009, 12(11): 1229–1237. DOI:10.1111/ele.2009.12.issue-11 |
 2017, Vol. 37
2017, Vol. 37