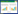文章信息
- 胡星云, 孙志高, 孙文广, 王苗苗, 王伟, 田莉萍
- HU Xingyun, SUN Zhigao, SUN Wenguang, WANG Miaomiao, WANG Wei, TIAN Liping.
- 黄河口新生湿地碱蓬生物量及氮累积与分配对外源氮输入的响应
- Biomass and nitrogen accumulation and allocation in Suaeda salsa in response to exogenous nitrogen enrichment in the newly created marshes of the Yellow River Estuary, China
- 生态学报[J]. 2017, 37(1): 226-237
- Acta Ecologica Sinica[J]. 2017, 37(1): 226-237
- http://dx.doi.org/10.5846/stxb201607261523
-
文章历史
- 收稿日期: 2016-07-26
- 修订日期: 2016-08-29
2. 路易斯安那州立大学植物、环境与土壤科学系, 巴图鲁日 70803;
3. 成都信息工程学院资源环境学院, 成都 610225;
4. 鲁东大学地理与规划学院, 烟台 264025
2. School of Plant, Environmental and Soil Sciences, Louisiana State University, Baton Rouge, 70803, US;
3. Department of Resources and Environment, College of Information and Engineering, Chengdu 610225, China;
4. Department of Geography and Planning, Ludong University, Yantai 264025, China
氮作为河口湿地营养水平的指示剂之一, 常常是最主要的限制性养分, 其含量直接影响湿地系统生产力[1]。氮沉降是河口湿地的一个重要氮输入源, 其对河口或海岸地区净初级生产的作用较之河流而言不可忽视[2], 是发生赤潮的一个诱因。河口湿地不仅受氮沉降的影响, 而且流域内人类生产、生活产生的大量含氮物质通过河流排放入海亦可对河口湿地产生严重影响[3]。据估计, 当前全球由河流排放入海的可溶性有机氮(DON)和无机氮(DIN)总量为30-36 Mt/a, 其中DON占31%-37%, 且未来仍有不断增加的趋势[4]。当前, 河口氮负荷增强已成为改变河口湿地最重要的因素之一[5], 其对于生源元素循环的影响已成为国际海岸带陆海相互作用计划(LOICZ)的研究热点[6]。
氮输入增加作为当前重要的全球性环境问题可对湿地中各种生态过程产生深刻影响[7]。目前, 国外已在氮沉降特征及其生态效应[8]、生物固氮贡献及其影响[9]、人为氮或径流氮输入及其生态影响[10], 以及氮输入生态效应模型表征与模拟[11]等方面开展了大量研究, 但以对森林生态系统的研究居多。与之相比, 国内在该领域也开展了较多工作并取得了许多重要成果, 但这些研究亦多集中于森林生态系统[12-13], 而对湿地生态系统的研究相对较弱。目前, 国内关于湿地生态过程对氮输入的响应研究已涉及三江平原湿地植被-土壤系统关键过程[14-15]、闽江河口湿地温室气体产生与释放[16]、江苏大丰滨海盐沼植被生态特征[17]、云南纳帕海高原湿地土壤氮转化过程[18]以及青藏高原高寒湿地土壤有机碳矿化[19]等, 但以对三江平原淡水沼泽湿地的研究居多, 而对其它类型或地区天然湿地, 特别是对滨海湿地(河口湿地或滨海盐沼)和高原湿地的相关研究还比较薄弱。另外, 现有研究多侧重于探讨氮输入对土壤碳氮转化过程的影响, 而对湿地植被氮累积与分配模式对不同氮输入梯度的响应研究还比较缺乏。
黄河口湿地作为渤海与黄河河口相互作用形成的重要湿地, 承接着来自上游带来的大量含氮物质。据中国海洋环境质量公报显示, 2010-2014年黄河口入海污染物达到1.90×105-5.70×105t, 其中氨氮、硝酸盐氮和亚硝酸盐氮含量占总污染物总量的4.02-16.17%。近年来, 黄河口营养盐入海通量已达1.41×104-4.22×104 t, 并始终保持较高水平[20], 另据报道, 黄河口地区的氮湿沉降量已从1980年的1-2g m-2 a-1增至2007年的3-4.5g m-2 a-1[21], 接近其氮沉降临界负荷(4.0g m-2 a-1)[22], 而这可能对湿地和近岸生态系统的植物生长和养分循环等产生深刻影响[23]。碱蓬(Suaeda salsa)作为黄河口新生湿地的典型盐生植被, 是黄河三角洲丹顶鹤(Grus japonensis)、白鹭(Egretta garzetta)和鹆形目鸟类等的主要栖息地, 同时还具有维持湿地系统正常演替、防风固堤、调节气候等重要功能, 其对环境变化有着重要的指示作用[24]。尽管很多学者已在碱蓬营养元素季节动态[25]、元素累积与分配特征[26]、盐分胁迫[27, 28]以及生态改良[29]等方面开展了大量工作, 但关于外源氮输入对碱蓬生态特征以及其对植被氮累积与分配模式的影响研究还鲜有报道。鉴于此, 本文以黄河入海口北部滨岸高潮滩的碱蓬湿地为研究对象, 基于野外原位氮输入模拟试验, 研究了不同氮输入梯度下碱蓬不同器官生物量以及氮累积与分配特征的差异, 研究结果有助于揭示黄河口新生湿地氮循环关键过程对外源氮输入的响应机制, 并可为该区退化湿地的恢复与重建提供重要的理论与实践依据。
1 研究区概况与研究方法 1.1 研究区概况研究区位于山东黄河三角洲国家级自然保护区(37°40′N-38°10′N, 118°41′E-119°16′E), 保护区总面积15.3万hm2, 其中陆地面积8.27万hm2, 潮间带面积3.83万hm2, 潮间带面积占整个保护区陆地面积的46.25%。研究区年降水量551.6mm, 年蒸发量1928.2mm, 年均温12.1℃, 无霜期196 d, 四季分明, 雨热同期, 属于暖温带季风型大陆性气候。保护区的土壤类型主要为隐域性潮土和盐土, 主要植被类型为碱蓬、芦苇(Phragmites australis)、柽柳(Tamatix chinensis)、白茅(Imperata cylindrica)及罗布麻(Apocynum venetum)等。
1.2 研究方法 1.2.1 植物样品采集与测定选择今黄河入海口北部滨岸高潮滩的碱蓬湿地为研究对象, 参照欧洲NITREX项目以及靳英华等在长白山地区类似研究的设计[30], 开展外源氮野外原位输入模拟试验。在碱蓬湿地试验区内布设相关装置通过人工喷氮方式模拟外源氮输入。试验设4个处理。N0, 对照处理:无额外氮输入, 其值为当前湿地实际氮输入量。结合该区现有资料, 考虑陆源氮输入(2.5-3.5gN m-2 a-1)和氮沉降(3-4.5 gN m-2 a-1)的综合影响, 将值确定为6.0 gN m-2 a-1\]; N1, 低氮处理:1.5倍N0(9.0 gN m-2 a-1), 模拟湿地未来较低的外源氮增加量; N2, 中氮处理:2.0倍N0(12.0 gN m-2 a-1), 模拟湿地未来较高的外源氮增加量; N3, 高氮处理:3.0倍N0(18.0 gN m-2 a-1), 模拟湿地未来更高的外源氮增加量。每个处理设3个样地, 每个样地面积为5 m×10 m。试验于2014年4-11月进行, 自4月下旬开始, 每隔20-30d以CO (NH2)2水溶液的形式对不同样地进行外源氮输入强度的模拟, 共喷氮8次。按照4种处理在不同阶段的氮输入要求, 将CO (NH2)2溶解在20L水中, 通过预布设装置均匀喷洒入各样地。对照样地喷洒等量的水以减少因外加水造成对湿地生态过程的影响。
地上生物量采用收获法, 自5月份按照植物生长特点每隔20-30d采样1次。在不同氮处理样地内选取3-4个25 cm×25 cm的样方, 沿地面剪下植物地上部分, 带回实验室将其分离为茎、叶。由于成熟期碱蓬的果实与小叶紧密相连, 难以准确区分, 所以实际为叶+果实。地下生物量采用挖掘法, 并在地上生物量测定样方内进行测定。采样时, 将样方内0-40cm的根挖出, 放在细纱网袋中将泥土冲洗干净至无。枯落物采样与生物量测定同步, 将样方割除植物地上部分, 摘除立枯物(实验室进行), 同时收集样方内散落在地面上的当年凋落物。所有植物样品置于80℃烘干箱中烘干至恒重后称量。将样品粉碎过0.25 mm筛后采用元素分析仪(Vario Micro cube)测定其TN含量。
1.2.2 数据处理与统计运用Origin 7.5软件对数据进行作图和计算, 并对不同氮输入处理间的生物量、枯落物量、氮含量和氮分配比数据进行方差分析, 显著性水平设定为P=0.05。运用SPSS 22.0软件对不同氮输入处理下的生物量和枯落物量进行数学模拟。
2 结果与分析 2.1 氮输入对植物生物量及枯落物量的影响 2.1.1 地上生物量结果表明, 潮滩湿地碱蓬的地上及不同器官生物量在不同氮输入处理下均具有明显季节变化特征(图 1), 且大多符合抛物线模型(表 1)。整体而言, 不同氮输入梯度下碱蓬的地上生物量自5月随着水热条件的改善均迅速增加, 至8月, 除高氮输入处理下的地上生物量继续增加外, 其他氮输入处理的地上生物量均存在小幅降低, 之后又呈增加趋势。不同氮输入梯度下(N1、N2和N3)碱蓬的地上生物量均于10月末达到最高值(N1, 945.65g/m2; N2, 956.75g/m2; N3, 1269.97g/m2), 其达到最大值的时间相对于无氮输入处理(N0)达到最大值(794.40g/m2)的时间延迟20 d左右, 说明不同氮输入处理均可延迟植物的生长高峰期。10月下旬以后, 随着气温的持续降低, 植物地上部分几乎完全枯死并呈立枯状或枯落归还地表, 此时四种处理下植物的地上生物量均于11月下旬降至最低值(N0, 123.89g/m2; N1, 181.28g/m2; N2, 187.52g/m2; N3, 278.72g/m2)。另外, 不同氮输入处理下茎和叶生物量的变化趋势整体与地上生物量一致, 且其达到最大生物量时间亦与地下生物量达到最大值的时间具有较好的同步性(图 1)。比较而言, 4种氮输入处理下碱蓬的地上及不同器官生物量整体均表现为N3>N2>N1>N0, 但其之间的差异均不显著(P>0.05)。
|
| 图 1 不同氮输入处理下碱蓬生物量季节动态 Fig. 1 Seasonal dynamics of the biomasses of different organs of Suaeda salsa as affected by different nitrogen import treatment N0, 123.89g/m2; N1, 181.28g/m2; N2, 187.52g/m2; N3, 278.72g/m2 |
| 项目 Items |
氮输入处理 Nitrogen import treatments |
模拟模型 Simulation models |
R2 | P |
| 茎Stem | N0 | y=-299.356-0.05t2+12.453t | 0.778 | 0.023 |
| N1 | y=-278.946-0.05t2+12.719t | 0.690 | 0.053 | |
| N2 | y=-376.603-0.063t2+15.715t | 0.835 | 0.011 | |
| N3 | y=-526.317-0.08t2+20.536t | 0.775 | 0.024 | |
| 叶Leaf | N0 | y=223.7+0.083t2-5.625t | 0.787 | 0.079 |
| N1 | y=210.185+0.067t2-4.239t | 0.599 | 0.257 | |
| N2 | y=232.914+0.103t2-6.584t | 0.654 | 0.197 | |
| N3 | y=247.437+0.099t2-6.039t | 0.739 | 0.116 | |
| 地上生物量 | N0 | y=-310.170-0.067t2+16.404t | 0.706 | 0.047 |
| Aboveground biomass | N1 | y=-263.815-0.065t2+16.423t | 0.622 | 0.088 |
| N2 | y=-433.387-0.084t2+20.96t | 0.742 | 0.034 | |
| N3 | y=-566.704-0.102t2+26.232t | 0.730 | 0.038 | |
| 枯落物Litter amount | N0 | y=0.00002×exp (t/11.374)+37.371 | 0.982 | < 0.05 |
| N1 | y=0.00009×exp (t/12.541)+43.716 | 0.992 | < 0.01 | |
| N2 | y=0.105×exp (t/22.118)-12.928 | 0.901 | < 0.05 | |
| N3 | y=0.084×exp (t/21.564)-0.345 | 0.901 | < 0.05 | |
| y:生物量, t:生长天数; N0, 无氮输入; N1, 低氮输入; N2, 中氮输入; N3, 高氮输入 | ||||
不同氮输入处理下植物地下生物量尽管亦具有明显季节变化特征, 但其变化幅度要低于地上生物量(图 1)。N0处理下的地下生物量在生长季呈“M”型变化, 其分别在8月中旬和10月上旬出现较高值(46.83g/m2和45.12g/m2)。尽管不同氮输入处理下的地下生物量均于生长初期增加迅速, 但之后则呈不同变化趋势。其中, N1地下生物量在于7月中旬达到最大值(49.65g/m2)后整体呈波动降低趋势; N2地下生物量在6月下旬达到最大值后(55.84g/m2)整体呈较大波动降低变化; N3地下生物量的变化与N0相似, 亦呈“M”型, 其分别于6月下旬和10月上旬出现较高值(64.12g/m2和70.67g/m2)。比较而言, N3处理下的地下生物量均高于N2、N1和N0处理, 但其差异并不显著(P>0.05)。尽管N1处理对碱蓬生长初期的地下生物量亦起到了明显促进作用, 但在8月中旬到10月下旬, N1处理下的地下生物量却略低于N0处理。
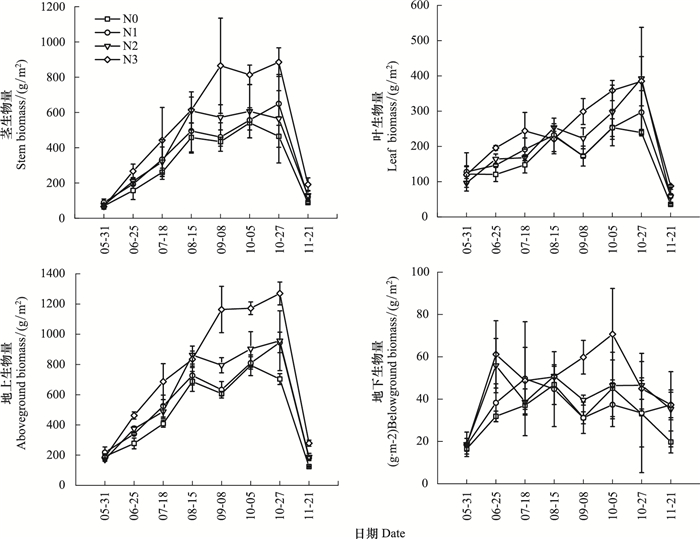
2.1.3 枯落物量不同氮输入处理下碱蓬的枯落物量整体均呈指数增长模型变化(y=Aexp (t/B)+C, 式中y为枯落物量, t为天数, A、B、C均为常数)(表 1)。7月中旬到10月末, 不同氮输入处理下的枯落物量均处于较低水平, 且其之间并无明显差异(P>0.05)。生长末期, 随着植物地上部分大量枯死, 不同处理下的枯落物量骤然增加并达到最大值(N0, 643.41g/m2; N1, 775.63g/m2; N2, 902.24g/m2; N3, 918.08g/m2), 其在10月末至11月下旬的增幅分别高达1171.12% (N0)、648.48%(N1)、1201.31%(N2)和1175.11%(N3)。尽管不同氮输入处理下的枯落物量在生长末期整体表现为N3>N2>N1>N0, 但其之间的差异并不显著(P>0.05)。
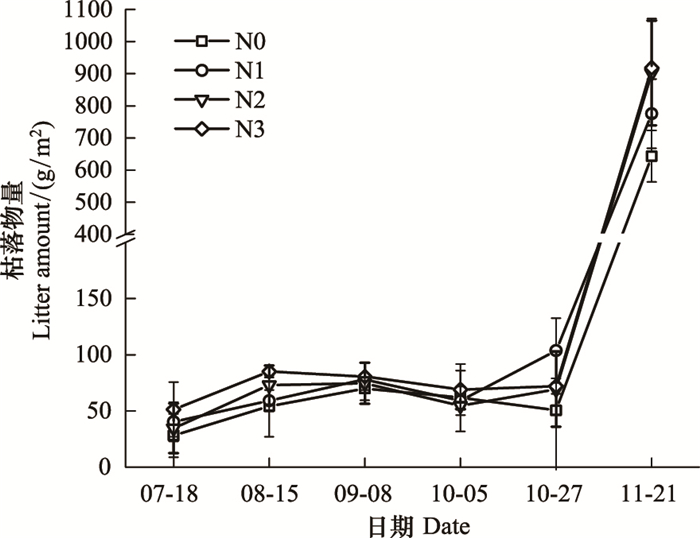
2.2 氮输入对植物氮累积特征的影响 2.2.1 不同器官氮累积特征不同氮输入处理下碱蓬各器官的TN含量在生长季均具有相似的变化模式(图 3), 但不同器官因生长阶段和自身组织结构的不同, 其TN含量变化模式亦存在一定差异。整体而言, 不同氮输入处理下植物各器官的TN含量表现为叶>根>茎, 说明叶是氮的主要累积器官, 而根作为养分供给器官亦具有很强的氮吸收能力。不同氮输入处理下根中TN含量均在生长初期最高, 之后整体呈波动降低趋势, 并均于10月下旬达到最低值后骤然增加。与根中TN含量变化模式相似, 不同氮输入处理下茎中TN含量整体呈波动降低变化, 并均于10月下旬取得最低值后又出现小幅增加。与根和茎相比, 不同氮输入处理下叶中TN含量的变化较为复杂, 其在5-6月显著降低, 之后则呈迅速增加趋势; 至生长末期, 除N2叶的TN含量在9月上旬骤然降低外, 其它处理的TN含量均于10月上旬后呈小幅降低变化。另外, N2处理下根和茎中TN含量在10月末的骤然增加与其在叶中的骤然降低亦存在较好的同步性。尽管不同氮输入处理下碱蓬根、茎和叶中TN含量均不存在显著差异(P>0.05), 但不同时期各器官的TN含量相对于N0处理均存在不同程度降低。
|
| 图 2 不同氮输入处理下碱蓬枯落物量季节动态 Fig. 2 Seasonal dynamics of litter amount of Suaeda salsa as affected by different nitrogen import treatments |
|
| 图 3 不同氮输入处理下碱蓬不同器官和枯落物TN含量季节变化 Fig. 3 Seasonal variations of TN content in different organs and litter of Suaeda salsa as affected by different nitrogen import treatments |
不同氮输入处理下碱蓬枯落物的TN含量季节变化模式较为相似(图 3)。N0、N1和N2处理下枯落物的TN含量均在产生初期较高, 之后迅速降低, 并于8月中旬后逐渐增加; 三者均于10月末达到最高值, 其值分别为7.02、6.53g/m2和6.41 mg/g。与之不同, N3处理下枯落物的TN含量自产生初期开始一直增加, 并亦于10月末达到最高值(8.73 mg/g)。生长末期, 4种处理下枯落物的TN含量均呈显著降低趋势。尽管不同氮输入处理下枯落物的TN含量不存在显著差异(P>0.05), 但N3处理的TN含量整体高于N0处理, 而N2和N1处理的TN含量大部分时期均低于N0处理。
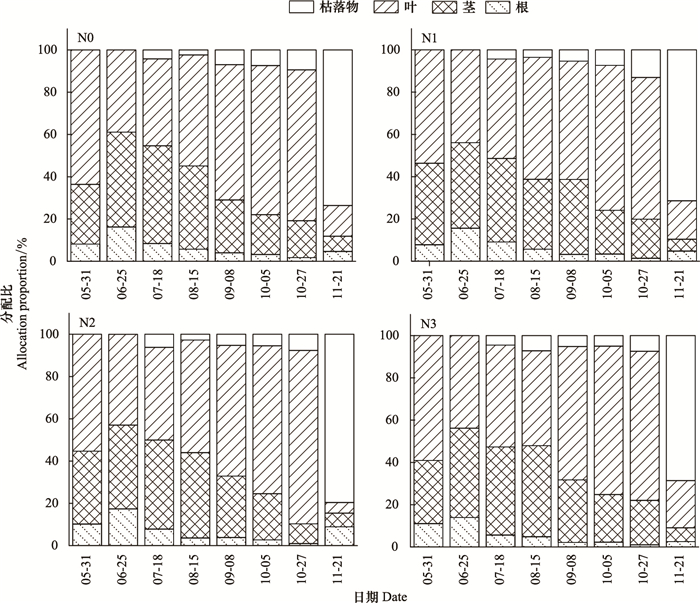
2.3 氮输入对植物氮分配特征的影响不同氮输入处理下碱蓬各部分的氮分配比在不同时期均存在较大差异(图 4)。不同处理下各部分的氮分配比整体以叶最高, 说明叶是碱蓬的主要氮累积器官。不同氮输入处理下叶的氮分配比在生长初期均表现为小幅降低, 生长旺期表现为迅速增加而生长末期则表现为骤然降低, 且均于10月末取得最大值(N0, 71.31%;N1, 68.60%;N2, 81.99%;N3, 70.49%)。与之相反, 4种氮输入处理下根的氮分配比在生长初期均表现为小幅增加, 生长旺期表现为迅速降低而生长末期则表现为骤然增加, 反映出地上与地下在养分供给方面的密切联系。除生长初期外, 不同氮输入处理下茎的氮分配比整体均呈降低趋势, 而枯落物的氮分配比整体均呈增加趋势。比较而言, N0、N1和N3处理下不同部分的氮分配比在5-6月整体均表现为叶>茎>根, 7-10月表现为叶>茎>枯>根, 11月则表现为枯>叶>茎>根。与之不同, N2处理下不同部分的氮分配比在11月下旬表现为叶最低, 根(8.95%)与叶、茎之和的比例(11.45%)相当, 而枯落物所占比例高达79.58%, 这与前面氮在此间不同器官中的氮含量变化特征正好吻合(图 3)。
|
| 图 4 不同氮输入处理下碱蓬不同部分氮分配比季节变化 Fig. 4 Seasonal variations of nitrogen allocation proportions of different parts of Suaeda salsa as affected by different nitrogen import treatments |
氮作为湿地植物生长所必须的大量营养元素, 其吸收与利用状况显著影响植物的净初级生产力。已有研究表明, 适量氮输入可促进植物生产力的提高[31], 并对一些生态指标(叶片可溶性蛋白、叶片可溶性糖、游离氨基酸、叶绿素等)产生促进作用[32-33], 但长期、持续氮输入超过植物和微生物氮需求时则会对植物生理生态特征产生不利影响[23]。本研究表明, 氮输入量的增加尽管提高了植物的净初级生产力, 但并未改变其地上生物量的季节变化模式, 并且不同处理之间的地上生物量差异并不显著(P>0.05), 原因可能与碱蓬湿地受氮限制程度较高[26], 而不同氮输入量并未完全满足碱蓬生长的氮需求有关。Mao等关于氮输入对三江平原沼泽湿地植物生态特征的研究亦得到类似结果[34], 即不同氮输入梯度尽管可提高植物的株高及地上生物量, 但因氮输入量并未达到植物需氮最大值, 从而导致不同氮输入处理对地上生物量的影响并不显著。本研究还表明, 8月中旬至10月末, 除高氮处理下的地上及不同器官生物量继续呈增长趋势外, 其它氮输入处理下的地上及不同器官生物量增加缓慢甚至于9月上旬出现较大幅度降低, 原因可能主要有两方面:一是与该时期黄河口地区温度较高、降水相对较少以及蒸发量大导致土壤盐分表聚, 进而对碱蓬生长产生盐分胁迫有关。已有研究表明, 盐分胁迫可对植物生长产生抑制作用[27, 35], 但较高的氮输入量可缓解盐分胁迫对碱蓬生长的抑制作用[28]。梁飞等对碱蓬盐碱地追加氮肥的研究表明, 追施氮肥可促进盐地碱蓬对盐渍土的生物修复[29]。亦有研究指出, 减少30%的降水可显著提高叶片的气孔导度, 而气孔导度增加引起的水分散失也就相对减少, 此时氮添加可显著地提高植物的光合能力[13]。据此可知, 该时期黄河口的较高蒸降比可促使碱蓬叶片提高水分的保持能力, 而高氮输入可明显促进植物的光合作用, 进而使得地上及不同器官生物量在高氮水平下一直呈增加趋势且其值最高。尽管低氮和中氮处理对植物的地上及不同器官生物量亦具有一定的促进作用, 但相对较低的氮输入水平在8-10月尚不足以缓解植被的盐分胁迫, 由此导致其地上及不同器官生物量出现较大幅度降低。二是与不同氮输入处理下植被的自疏作用有关。8-10月, 不同氮输入处理下的植物株高均明显增加, 而此间植物的密度却明显降低(图 5)。由于植物根系所提供的养分不足以满足每一株植物的生长, 由此可引发植株之间的竞争, 从而导致一部分弱势植株的死亡和地上生物量的缓慢下降。从图 2中亦可发现, 除N3处理外, 9月上旬N1和N2处理下的枯落物量较8月中旬而言增加明显, 这正好与此间两种处理下自疏效应导致部分植株死亡进而使得枯落物量增加的推测相吻合。本研究中, N3处理下的植物株高在生长季明显大于N2、N1和N0处理下的株高, 但其密度则明显低于其它处理(图 5), 说明N3处理下植物的自疏效应最强。尽管N3处理下的植物密度因自疏效应明显而有所下降, 但充足的氮养分明显促进了植物的生长(图 5), 进而可对植物的高度和径向生长产生一种补偿效应[36]。与N3处理相比, N1和N2处理虽然在一定程度上促进了植物的生长, 但因其密度下降明显(图 5), 使得二者地上及不同器官生物量整体呈降低趋势。本研究还表明, 氮输入量的增加不仅可促进地上生物量的增加, 而且还可延长植物的生长高峰期, 特别是N1、N2和N3处理下的地上生物量最大值取得时间相对于N0处理推迟20d左右。相关研究亦得到类似结论, 如Sun等的研究发现, 氮添加可使得三江平原小叶章(Calamagrostis angustifolia)茎和叶的最大生物量取得时间相对于无氮输入处理推迟了15-30d[14], 原因可能在于, 氮是叶绿素的重要组成部分, 不同程度的氮添加可促使植物体产生更多的叶绿素, 使得光合作用强度增加而延缓植物的生长发育期。另外, 氮也是许多酶的重要组成部分, 其对植物体的代谢机制具有重要影响, 而氮添加可促进细胞分裂素的合成, 使得叶绿素分解受到抑制, 进而可延缓和防止植物器官衰老[37]。据此可知, 本研究中的三种氮输入处理在一定程度上可能均促进了碱蓬叶绿素和酶的合成能力, 延缓了植物的生长高峰期, 提高其地上及不同器官的生物量。
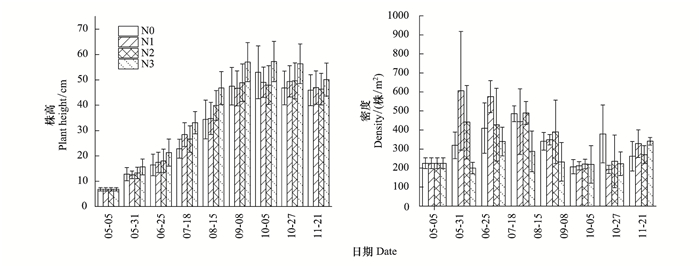
|
| 图 5 不同氮输入处理下潮滩湿地碱蓬株高及密度季节动态 Fig. 5 Seasonal variations of the plant height and density of Suaeda salsa as affected by different nitrogen import treatment |
与地上生物量不同, 不同氮输入处理下地下生物量的季节变化模式存在较大差异(图 1), 即不同氮输入处理改变了地下生物量的季节变化模式。特别是N2和N3处理均对植物生长初期的地下生物量产生明显促进作用, 且相对于N1和N0处理, 初期地下生物量较高值的取得要提前20-50d。原因在于, N2和N3处理下的养分供给相对于N0和N1处理更为充足, 在初期极大地促进了根系的生长, 而根系的生长极大地促进了其从环境中吸收和累积养分的能力, 从而更有利于根系的生长和发育, 而这就使得N2和N3处理下地下生物量的变化模式与N0和N1处理存在较大差异。另外, 与N2和N3处理下的地下生物量季节变化模式不同, N0或N1处理下的地下生物量整体呈波动递减变化, 而这正好与地上生物量增加存在一定的养分供给关系。生长初期, 植物根系因氮输入而快速发育与生长, 进而有利于其从环境中吸收更多养分而供给地上器官较快的生长; 当地上器官进入快速生长阶段而需大量养分来维持其生长时, 根系中氮养分大量向地上转移, 从而导致地下生物量的明显降低。研究还发现, N1处理下的地下生物量在8月中旬到10月下旬整体低于N0处理(图 1), 原因可能在于, N1处理对根系发育的刺激作用并不明显, 加之对地下生物量的测定误差可能较大而掩盖了其较弱的刺激作用。与N1相比, N2和N3处理对此间的地下生物量具有明显的促进作用(图 1), 这也与孙大成等在帕纳海湿地对茭草输氮的相关研究结果一致[18]。尽管不同氮输入处理下碱蓬枯落物量的变化趋势较为一致, 但其增幅在生长末期差异较大, 其值相对于产生初期分别增加22.94倍(N0)、19.23倍(N1)、26.07倍(N2)和17.89倍(N3)。比较而言, N2处理的枯落物量增长幅度较大, 原因主要与其产生初期的枯体量本身就少而生长末期的产生量非常大(与N3处理相当)有关(图 2)。总之, 氮输入不但对碱蓬的地上和地下生物量产生一定的促进作用(地上平均增幅:19.71-62.29%, 地下平均增幅:16.52%-51.95%), 而且亦可明显延迟植物的生长高峰期, 高氮输入更有利于植物生物量的增加。
3.2 氮输入对植物氮累积与分配的影响本研究表明, 不同氮输入处理下碱蓬根与茎的TN含量变化模式较为相似, 即均于生长初期取得最高值后波动下降, 并于10月下旬取得最低值后又出现小幅增加。生长初期较高的TN含量主要与根和茎的生物量较低(图 1)且碱蓬幼苗对氮养分需量求量大有关[26]; 生长中期TN含量的降低主要与根和茎中的氮营养不断供给叶生长发育以及促进光合作用有关(图 3); 生长末期(10月末以后), 植物开始大量死亡, 此时地上器官中的氮开始向地下转移。此间, 叶最先死亡, 氮营养整体呈现出先向茎而后再向根转移的特征, 由此导致根中的TN含量骤然增加, 而茎中的TN含量仅出现小幅增加。与根和茎不同, 不同氮输入处理下碱蓬叶中的TN含量变化模式整体均表现出初期下降中期增加末期又下降的变化特征, 而这主要与不同时期氮养分在植物各器官中的转移有关。生长初期, 植物根系较弱, 其吸收的有限氮营养主要供给地上器官生长发育的需要, 此间植物生长发育(特别是叶)较快, “稀释效应”明显, 由此使得叶中的TN含量迅速下降; 生长旺期, 植物根系较为发达(图 1), 尽管此间地上部分生长发育所需的养分增多, 但较为发达的根系可将吸收的大量养分不断转移至地上光合作用器官, 由此导致叶生物量迅速增加(图 1)所导致的“稀释效应”不明显(图 3), 使得叶中的TN含量呈增加趋势。值得注意的是, 叶+果实中的TN含量在10月份出现最大值, 原因主要与这一时期碱蓬果实(种子)的发育和成熟需从根与茎中转移大量的氮营养有关。本研究还发现, N2处理下根和茎中TN含量在10月末的骤然增加与其在叶中的骤然降低存在较好的同步性, 且N2处理下叶+果实的TN含量峰值取得的时间(9月上旬)相对于其它处理(10月上旬)提前约1个月。根据碱蓬生长节律以及不同氮处理下其各器官TN含量的变化规律, 我们推测N2处理下碱蓬种子的发育相对于其它氮输入处理可能会提前, 但其种子发育高峰时期可能依然集中于10月上旬。在实地采样中, 的确也观测到9月份N2处理下的碱蓬种子发育要早于其它氮输入处理, 而种子大量发育的时期则集中于10月份。原因可能主要有以下两方面:一是与供氮水平可影响植物体内的碳分配有关。有研究指出, 适量供氮可加速氮的代谢, 进而可使大量的碳参与蛋白质的合成, 但较高或过量供氮可使蛋白质的积累受到抑制[38]。德科加等对青藏高原燕麦的施氮试验也表明, 施氮水平与蛋白质合成之间存在极显著的线性相关关系, 一定限度的施肥可提高蛋白质的合成能力, 进而可促进种子的灌浆和增重[39]; 二是与植物对适量氮养分输入环境的适应对策有关。已有研究表明, 黄河口新生湿地的碱蓬生长主要受氮限制且其对贫养分环境具有特殊的适应对策, 当生长环境中的养分增加后, 碱蓬自身的生长特性亦可能发生一定的改变[29, 40]。王界平的研究表明, 增加氮肥可显著提高碱蓬体内的氮含量, 且种子中氮含量的变化对氮肥施用量最为敏感[41]。碱蓬进入成熟期, 叶+果实(种子)成为养分的主要积累库, 为了促进种子的发育, 植物根系会从环境中吸收大量氮养分并通过茎和叶不断转移到果实中而积累。与N0和N1处理相比, 此时N2处理下植物生长的养分条件本身较好, 植物根系极易从环境中获得较为充足的氮养分来满足地上果实发育的需要。尽管N3处理下的氮养分供给更为充足, 但由于碱蓬具有对贫养分环境的特殊适应特性使得其果实发育对高养分环境的敏感程度较低。也就是说, 碱蓬已适应了相对贫瘠的养分环境, 当养分供给增加时, 其极有可能提前蓄积和转移足够的氮养分至果实以供给种子发育的需要, 而这也是碱蓬通过改变自身生长特性而对湿地不同氮养分状况的一种特殊适应对策。
本研究发现, 枯落物中的TN含量变化模式与叶中的TN含量变化模式较为相似, 即除N3处理外, 其它氮输入处理均呈现出先降低后增加而后又降低的变化趋势。原因在于, 产生初期的枯落物量较低且主要为叶, 而此前叶中的TN含量又相对较高, 由此使得叶枯死后虽然存在部分氮转移, 但滞留于叶枯体中的氮含量依然较高。7-8月, 植物的茎开始枯死, 此间茎的生物量大于叶(图 1)而TN含量低于叶(图 3), 由此导致枯落物的TN含量亦下降。另外, 由于这一时期的降水充沛且热量条件较好, 枯落物更易受到雨水淋溶和微生物分解的影响, 由此使得枯落物中的氮在短期内流失明显。10月末至11月末, 枯落物中的氮含量降低主要与此间种子发育成熟而脱落以及地上器官大量枯死过程中伴随着氮养分大量向地下根系转移有关。比较而言, N3处理下的枯落物TN含量整体要高于N0处理, 充足的氮养分供给使得高氮处理下地上器官的氮累积量增大, “稀释效应”不明显, 由此使得其产生的枯落物TN含量也相对较高。不同的是, N1和N2处理下的枯落物TN含量在大部分时期均低于N0处理, 原因在于N1和N2处理下碱蓬对氮的吸收量尽管较N0多, 但因其地上生物量的增幅远高于N0处理, 进而使得“稀释效应”明显有关。正是由于“稀释效应”的存在, 使得两种处理产生的枯落物TN含量总体低于N0处理。本研究还表明, 尽管不同氮输入处理并未改变碱蓬不同器官的氮累积与分配格局以及地上与地下之间的养分供给关系, 但其为适应不同养分条件而调整自身养分供给与分配的特性在N2处理下表现的尤为明显。生长末期N2处理下根的氮分配比明显高于其它氮输入处理, 而叶的氮分配比明显低于其它氮输入处理, 原因可能与植物体为适应不同养分环境而对自身生长特性和养分分配状况的调节作用有关。Xie等指出, 在养分增加情况下, 植物体自身可适时调整养分的分配比[42]。据图 1可知, 生长末期N2与N1处理下的地上生物量相当, 但其地下生物量则与N3相当, 加之N2处理下植物的种子发育可能提前, 说明N2处理下植物地上器官的养分极有可能也会提前向地下转移, 并在一定程度上促进了根系的生长, 最终导致生长末期其根的氮分配比明显高于其它氮处理(图 4)。
上述研究表明, 碱蓬可在氮负荷增强条件下(特别是适度养分处理, N2)通过调整自身的生长特性以及不同器官的氮分配比来适应较好的养分供给环境。近年来, 黄河口的营养盐入海通量尽管年际变化较大, 但一直保持在较高水平[20]。当前, 黄河口的营养盐入海通量以及氮沉降量整体呈不断增加趋势[21], 而这就使得贫养分的新生湿地养分状况可能会不断被改善, 并在未来一段时期极有可能达到本研究的中氮输入水平。据本研究可知, 当未来碱蓬湿地的氮养分状况达到较高水平(特别是中等水平)时, 其生物量、生长节律(特别是种子发育时间)以及不同器官氮累积与分配状况可能将发生明显改变。
4 结论(1)尽管不同氮输入处理并未改变碱蓬地上生物量的季节变化模式, 但随着输氮量的增加其地上生物量亦呈增加趋势(N3>N2>N1>N0);输氮延长了植物的生长高峰期, 氮处理下地上生物量最大值取得时间相对于未输氮处理推迟20 d左右。
(2)不同氮输入处理改变了地下生物量的季节变化模式, 特别是中氮和高氮处理均对生长初期的地下生物量产生了明显促进作用, 且在生长季初期其地下生物量较高值的取得时间比低氮处理和未输氮处理早20-50d。
(3)不同氮输入处理下碱蓬各器官的TN含量总体上均表现为叶>茎>根, 叶是氮的主要累积器官。不同氮输入处理并未改变碱蓬不同器官的氮累积分配格局以及地上与地下之间的养分供给关系, 但其为适应不同养分条件而调整自身养分供给与分配的特性在中等氮输入处理下表现的尤为明显。
(4)随着黄河口新生湿地氮养分供给的不断增加, 当未来碱蓬湿地氮养分状况达到较高水平(特别是中等水平)时, 其生物量、生长节律(特别是种子发育时间)以及不同器官氮累积与分配状况可能将发生明显改变。
| [1] | Mitsch W J, Gosselin J G. Wetlands. New York:Van Nostrand Reinhold Company Inc , 2000 : 89–125. |
| [2] | 张金良, 于志刚, 张经. 大气的干湿沉降及其对海洋生态系统的影响. 海洋环境科学 , 1999, 18 (1) : 70–76. |
| [3] | Wade A J, Neal C, Whitehead P G, Flynn N J. Modelling nitrogen fluxes from the land to the coastal zone in European systems:a perspective from the INCA project. Journal of Hydrology , 2005, 304 (1-4) : 413–429. DOI:10.1016/j.jhydrol.2004.07.041 |
| [4] | Boyer E W, Howarth R W, Galloway J N, Dentener F J, Green P A, Vörösmarty C J. Riverine nitrogen export from the continents to the coasts. Global Biogeochemical Cycles , 2006, 20 (1) : GBIS91. |
| [5] | Bukaveckas P A, Isenberg W N. Loading, transformation, and retention of nitrogen and phosphorus in the Tidal Freshwater James River (Virginia). Estuaries and Coasts , 2013, 36 (6) : 1219–1236. DOI:10.1007/s12237-013-9644-x |
| [6] | Lunau M, Voss M, Erickson M, Dziallas C, Casciotti K, Ducklow H. Excess nitrate loads to coastal waters reduces nitrate removal efficiency:mechanism and implications for coastal eutrophication. Environmental Microbiology , 2013, 15 (5) : 1492–1504. DOI:10.1111/emi.2013.15.issue-5 |
| [7] | Vitousek P M, Aber J D, Howarth R W, Likens G E, Matson P A, Schindler D W, Schlesinger W H, Tilman D G. Human alteration of the global nitrogen cycle:sources and consequences. Ecological Applications , 1997, 7 (3) : 737–750. |
| [8] | Whitall D, Hendrickson B, Paerl H. Importance of atmospherically deposited nitrogen to the annual nitrogen budget of the Neuse River estuary, North Carolina. Environment International , 2003, 29 (2-3) : 393–399. DOI:10.1016/S0160-4120(02)00175-7 |
| [9] | Gathumbi S M, Cadisch G, Giller K E. 15N natural abundance as a tool for assessing N2-fixation of herbaceous, shrub and tree legumes in improved fallows. Soil Biology and Biochemistry , 2002, 34 (8) : 1059–1071. DOI:10.1016/S0038-0717(02)00038-X |
| [10] | Mckinney R A, Nelson W G, Charpentier M A, Wigand C. Ribbed mussel nitrogen isotope signatures reflect nitrogen sources in coastal salt marshes. Ecological Applications , 2001, 11 (1) : 203–214. DOI:10.1890/1051-0761(2001)011[0203:RMNISR]2.0.CO;2 |
| [11] | Carmichael R H, Annett B, Valiela I. Nitrogen loading to Pleasant Bay, Cape Cod:application of models and stable isotopes to detect incipient nutrient enrichment of estuaries. Marine Pollution Bulletin , 2004, 48 (1-2) : 137–143. DOI:10.1016/S0025-326X(03)00372-2 |
| [12] | 宋学贵, 胡庭兴, 鲜骏仁, 肖春莲. 川南天然常绿阔叶林土壤酶活性特征及其对模拟N沉降的响应. 生态学报 , 2009, 29 (3) : 1234–1240. |
| [13] | 闫慧, 吴茜, 丁佳, 张守仁. 不同降水及氮添加对浙江古田山4种树木幼苗光合生理生态特征与生物量的影响. 生态学报 , 2013, 33 (14) : 4226–4236. |
| [14] | Sun Z G, Liu J S. Distribution and fate of anthropogenic nitrogen in the Calamagrostis angustifolia wetland ecosystem of Sanjiang Plain, Northeast China. Journal of Integrative Plant Biology , 2008, 50 (4) : 402–414. DOI:10.1111/jipb.2008.50.issue-4 |
| [15] | 刘德燕, 宋长春. 湿地植物小叶章对外源氮输入的响应. 应用生态学报 , 2008, 19 (12) : 2599–2604. |
| [16] | 牟晓杰, 刘兴土, 仝川, 孙志高. 闽江河口短叶茳芏湿地CH4和N2O排放对氮输入的短期响应. 环境科学 , 2012, 33 (7) : 2482–2489. |
| [17] | 张耀鸿, 张富存, 李映雪, 谢晓金, 周晓冬, 李强, 雷俊. 外源氮输入对互花米草生长及叶特征的影响. 生态环境学报 , 2010, 19 (10) : 2297–2301. |
| [18] | 孙大成, 郭雪莲, 解成杰, 余磊朝, 许静. 氮输入对沼泽湿地植物生长和氮吸收的影响. 生态环境学报 , 2013, 22 (8) : 1317–1321. |
| [19] | 白洁冰, 徐兴良, 宋明华, 何永涛, 蒋婧, 石培礼. 温度和氮素输入对青藏高原三种高寒草地土壤碳矿化的影响. 生态环境学报 , 2001, 20 (5) : 855–859. |
| [20] | Sun Z G, Sun W G, Tong C, Zeng C S, Yu X, Mou X J. China's coastal wetlands:Conservation history, implementation efforts, existing issues and strategies for future improvement. Environment International , 2015, 79 : 25–41. DOI:10.1016/j.envint.2015.02.017 |
| [21] | 遆超普, 颜晓元. 基于氮排放数据的中国大陆大气氮素湿沉降量估算. 农业环境科学学报 , 2010, 29 (8) : 1606–1611. |
| [22] | 段雷, 郝吉明, 谢绍东, 周中平. 用稳态法确定中国土壤的硫沉降和氮沉降临界负荷. 环境科学 , 2002, 23 (2) : 7–12. |
| [23] | Aber J D, McDowell W, Nadelhoffer K, Magill A, Berntson G, Kamakea M, McNulty S, Currie W, Rustad L, Fernandez I. Nitrogen saturation in temperate forest ecosystems:Hypotheses revisited. BioScience , 1998, 48 (11) : 921–934. DOI:10.2307/1313296 |
| [24] | Bauer G A, Bazzaz F A, Minocha R, Long S, Magill A, Aber J D, Berntson G M. Effects of chronic N additions on tissue chemistry, photosynthetic capacity, and carbon sequestration potential of a red pine (Pinus resinosa Ait.) stand in the NE United States. Forest Ecology and Management , 2004, 196 (1) : 173–186. DOI:10.1016/j.foreco.2004.03.032 |
| [25] | 宋红丽, 孙志高, 牟晓杰, 王玲玲, 姜欢欢, 孙万龙, 孙文广. 黄河三角洲新生湿地不同生境下翅碱蓬锰和锌含量的季节变化. 湿地科学 , 2012, 10 (1) : 65–73. |
| [26] | 牟晓杰, 孙志高, 王玲玲, 董洪芳. 黄河口滨岸潮滩不同生境下翅碱蓬氮的累积与分配特征. 湿地科学 , 2010, 8 (1) : 57–66. |
| [27] | 崔保山, 贺强, 赵欣胜. 水盐环境梯度下翅碱蓬(Suaeda salsa)的生态阈值. 生态学报 , 2008, 28 (4) : 1408–1418. |
| [28] | 宋红丽, 孙志高, 孙景宽, 牟晓杰, 姜欢欢, 孙文广. 氮、磷输入对黄河口潮滩湿地不同生境下碱蓬种子萌发与幼苗生长的影响. 草业学报 , 2012, 21 (6) : 30–41. |
| [29] | 梁飞, 田长彦, 田明明, 梁笛, 张科. 追施氮肥对盐地碱蓬生长及其改良盐渍土效果研究. 草业学报 , 2013, 22 (3) : 234–240. |
| [30] | 靳英华, 许嘉巍, 宗盛伟, 王鹏. 氮沉降对长白山苔原植被影响的试验研究. 地理科学 , 2014, 34 (12) : 1526–1532. |
| [31] | Fang Y, Xun F, Bai W M, Zhang W H, Li L H. Long-term nitrogen addition leads to loss of species richness due to litter accumulation and soil acidification in a temperate steppe. PLoS One , 2012, 7 (10) : e47369. DOI:10.1371/journal.pone.0047369 |
| [32] | Zhang L H, Song C C, Wang D X, Wang Y Y. Effects of exogenous nitrogen on freshwater marsh plant growth and N2O fluxes in Sanjiang Plain, Northeast China. Atmospheric Environment , 2007, 41 (5) : 1080–1090. DOI:10.1016/j.atmosenv.2006.09.029 |
| [33] | 窦晶鑫, 刘景双, 王洋, 赵光影. 小叶章对氮沉降的生理生态响应. 湿地科学 , 2009, 7 (1) : 40–46. |
| [34] | Mao R, Zhang X H, Song C C. Effects of nitrogen addition on plant functional traits in freshwater wetland of Sanjiang Plain, Northeast China. Chinese Geographical Science , 2014, 24 (6) : 674–681. DOI:10.1007/s11769-014-0691-4 |
| [35] | 段德玉, 刘小京, 李存桢, 乔海龙. N素营养对NaCl胁迫下盐地碱蓬幼苗生长及渗透调节物质变化的影响. 草业学报 , 2005, 14 (1) : 63–68. |
| [36] | 邵成, 陈中林, 董厚德. 辽河河口湿地芦苇的生长及生物量研究. 辽宁大学学报:自然科学版 , 1995, 22 (1) : 89–94. |
| [37] | 陆景陵. 植物营养学(上). 北京:中国农业大学出版社 , 2003 : 24–25. |
| [38] | 周瑞莲, 赵哈林, 杨树德, MarkW E. 子叶供氮对不同基因型大豆种子组分的影响. 中国农业科学 , 2008, 41 (10) : 3033–3041. |
| [39] | 德科加, 王德利, 周青平, 刘文辉, 徐成体. 施肥对青藏高原燕麦种子生产的增产效应. 草业科学 , 2008, 25 (1) : 26–30. |
| [40] | Mou X J, Sun Z G, Wang L L, Wang C Y. Nitrogen cycle of a typical Suaeda salsa marsh ecosystem in the Yellow River estuary. Journal of Environmental Sciences , 2011, 23 (6) : 958–967. DOI:10.1016/S1001-0742(10)60530-X |
| [41] | 王界平, 田长彦. 施用氮磷肥对盐土中碱蓬生长及矿物质吸收累积特征的影响. 西北农林科技大学学报:自然科学版 , 2010, 38 (11) : 201–208. |
| [42] | Xie Y H, Wen M Z, Yu D, Li Y K. Growth and resource allocation of water hyacinth as affected by gradually increasing nutrient concentrations. Aquatic Botany , 2004, 79 (3) : 257–266. DOI:10.1016/j.aquabot.2004.04.002 |
 2017, Vol. 37
2017, Vol. 37