文章信息
- 张秋芳, 谢锦升, 陈奶寿, 陈坦, 吕茂奎, 张浩, 杨玉盛
- ZHANG Qiufang, XIE Jinsheng, CHEN Naishou, CHEN Tan, LÜ Maokui, ZHANG Hao, YANG Yusheng.
- 生态恢复对马尾松叶片化学计量及氮磷转移的影响
- Effects of ecological restoration on stoichiometric characteristics and nutrient resorption efficiency of Pinus massoniana foliage
- 生态学报[J]. 2017, 37(1): 267-276
- Acta Ecologica Sinica[J]. 2017, 37(1): 267-276
- http://dx.doi.org/10.5846/stxb201510182100
-
文章历史
- 收稿日期: 2015-10-18
- 修订日期: 2016-06-28
2. 福建师范大学湿润亚热带山地生态国家重点实验室培育基地, 福州 350007;
3. 福建师范大学地理研究所, 福州 350007
2. State Key Laboratory of Subtropical Mountain Ecology (Founded by Ministry of Science and Technology and Fujian Province), Fujian Normal University, Fuzhou 350007, China;
3. Institute of Geography, Fujian Normal University, Fuzhou 350007, China
碳(C)、氮(N)、磷(P)作为植物基本的化学元素, 在植物生长和各种生理调节机制中发挥着重要作用[1], 而生态化学计量学的提出为认识C、N、P耦合循环特征、驱动力及机制等提供了新手段和新方法[2]。C:N和C:P在一定程度上反映了植物的营养利用效率[3], 而植物叶片N:P是判断生产力受哪种元素限制的关键指标[4]。土壤的N、P有效性经常控制植物的生产力[5], 因此植物C:N、C:P和N:P的大小一定程度上受土壤N、P含量的调节[6]。另一方面, 在养分供应有限的环境中, 植物自身也通过养分转移满足生长的需要[7], 这是植物保持和重新利用养分的一种重要机制[8]。
目前, 国内外对森林生态系统的生态化学计量学及养分转移开展了大量的研究, 如对天童山常绿阔叶林的研究中发现:群落演替初期的生产力主要受到氮素的限制作用, 演替中期的针叶林主要受到氮磷的共同限制作用, 演替后期则主要受到磷限制[9];对世界范围内森林生态系统的叶片和凋落物的生态化学计量学的研究发现不同生物群(温带阔叶林、温带针叶林和热带森林)具有不同的生态化学计量学特征[10]。其中, 养分转移的研究则集中于常绿和落叶树种的比较, 如Aerts[11]认为常绿树种的养分转移率更高, 而薛立[12]等则发现落叶树种的N转移率更高。土壤肥力水平可对营养转移产生重要影响, 养分充足的林地的养分转移率通常较低, 而养分贫乏的林地则相反[13]。转移率较高的元素可能是限制林木生长的养分, 因为通过提高元素转移生产更多的生物量可能是植物适应贫瘠环境的一种重要竞争策略[14], 这对于生长在贫瘠土壤的植物尤为重要。
我国南方红壤是我国水土流失最严重的区域之一, 部分地区侵蚀退化土壤养分贫瘠[15]。自20世纪80年代以来, 当地开展了大量的水土保持与生态恢复实践, 恢复了大面积的马尾松林[16-17]。随着生态恢复年限的增加, 生态环境方面大有改善[15], 但这是否影响马尾松的化学计量比及养分转移, 目前尚不清楚。因此, 本研究以生长于侵蚀红壤上不同恢复年限的马尾松人工林为研究对象, 通过对马尾松叶片及凋落叶的C、N、P化学计量比和养分转移研究, 试图回答以下问题:侵蚀红壤生态恢复过程中, 1)马尾松叶片的C、N、P化学计量比与土壤养分含量、叶片养分转移的关系;2)马尾松叶片N、P养分转移受哪些因素控制。
1 材料和方法 1.1 研究地概况研究样地位于福建省长汀县河田镇(116° 18′ -116° 31′ E, 25° 33′ -25° 48′ N), 海拔300-500 m。该地区地貌为河谷盆地, 属中亚热带季风气候区, 年均降水量约1737 mm, 年均气温在17.5-18.8 ℃, 平均无霜期260 d, 平均日照时数1925 h, ≥10 ℃积温4100-5650 ℃, 地带性植被(常绿阔叶林)破坏殆尽, 现有植被主要以马尾松(Pinus massoniana)次生林和人工林为主。土壤为中粗粒花岗岩发育的红壤, 抗蚀能力低。
不同治理时间的马尾松林样地均位于河田镇。其中, 以来油坑未治理的严重侵蚀地(CK1)和大路口的次生林(CK2)为对照, 选择治理前立地条件基本类似且具代表性的恢复13、30、33a马尾松人工林, 各实验地类型及基本概况:1)来油坑未治理的严重侵蚀地(CK1), 土壤侵蚀度达强度以上, 即俗称的“光板地”, 地表植被以稀疏的“小老头”树--马尾松为主, 平均胸径2.8 cm, 平均树高1.9 m;2)石壁下(恢复13 a), 于2001年治理恢复, 马尾松平均胸径8.9 cm, 平均树高7.4 m;3)水东坊(恢复30 a), 于1984年治理, 水平沟整地, 林下套种胡枝子(Lespedeza bicolor), 补植黑荆(Acacia mearnsii), 而后进行封禁管护, 马尾松平均胸径16.9 cm, 平均树高14.3 m;4)罗地(恢复33 a), 于1981年治理, 全垦整地, 施肥并按一定比例播撒马唐(Digitaria sanguinalis)、金色狗尾草(Setaria glauca)等草种, 调查时播种的草种早已退化, 后期恢复生长的芒萁(Dicranopteris dichotoma)较高, 植被覆盖度约达90%以上, 马尾松平均胸径约7.8 cm, 平均树高6.7 m;5)大路口风水林(CK2), 马尾松平均胸径47.5 cm, 平均树高19.0 m, 该地是当地村民为保护本村风水而得以保存下来, 马尾松密度338株/hm2。土壤母岩均为粗晶花岗岩, 具体土壤理化性质见表 1。
| 样地地点 Plots location |
恢复年限 Restoration years/a |
总有机碳 Total organic carbon/ (g/kg) |
全氮 Total nitrogen/ (g/kg) |
全磷 Total phosphorus/ (g/kg) |
土壤容重 Soil bulk density/ (g/cm3) |
pH |
| 来油坑Laiyoukeng | CK1 | 1.69 | 0.20 | 0.04 | 1.30 | 4.55 |
| 石壁下Shibixia | 13 | 9.83 | 0.60 | 0.12 | 1.30 | 4.44 |
| 水东坊Shuidongfang | 30 | 11.44 | 0.68 | 0.09 | 1.32 | 4.63 |
| 罗地Luodi | 33 | 15.02 | 0.73 | 0.10 | 1.28 | 4.31 |
| 大路口Dalukou | CK2 | 21.32 | 1.38 | 0.12 | 1.21 | 4.28 |
于2013年8月, 对不同恢复年限的马尾松林进行样方调查, 即在每个试验样地设3个20 m×20 m样方, 在样方内对乔木层进行每木检尺, 记录种名、树高、胸径、冠幅;不同恢复年限的马尾松林均采集成熟的营养叶片, 随机在样方中选择乔木, 在树冠部位剪切东南西北四个方位和上中下不同部位的枝条, 分别采集1年龄、2年龄叶片(未发现3年龄叶片), 同时收集新鲜凋落的叶片, 采用四分法取样分别装入样品袋中并做好标记。在每个样方内按S形选取5个样点, 用直径为5 cm土钻取样, 取样深度为0-10 cm, 混合后用自封袋装好样品并做好标记。
1.3 室内测定取样后先于85 ℃下杀青15 min, 再在65 ℃下烘干至恒重。烘干植物样品粉碎、研磨过筛(孔径为0.149 mm), 装瓶保存用于测定植物总有机C、全N和全P含量。将土壤样品剔除石砾和草根等杂物, 自然风干后过2 mm土壤筛, 然后用四分法取部分样品过0.149 mm筛, 装瓶保存用于测定土壤全N和全P含量。用碳氮元素分析仪(Elementar Vario EL Ⅲ)测定植物总有机C与全N含量, 用碳氮元素分析仪(Elementar Vario MAX)测定土壤全N含量, 植物/土壤全P含量先采用HClO4-H2SO4法提取[18], 再用流动分析仪(Skalar san++)测定。
1.4 数据处理植物N、P养分转移率的计算方法[19]见公式(1):

|
(1) |
同时, 还分别计算了马尾松凋落叶和2年龄针叶、2年龄和1年龄叶片之间的养分转移, 分别见公式(2)和(3):

|
(2) |

|
(3) |
内稳性指数用内稳性模型通过回归分析计算[6], 公式见(4):
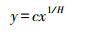
|
(4) |
式中, y是马尾松叶片N (P)的含量, x是土壤中的N (P)含量, H即为内稳性指数, H值高, 表示植物的内稳性强, 控制元素变化的能力强。
采用SPSS 20.0统计软件对数据进行统计分析, 选用单因素方差分析比较不同恢复年限马尾松叶片C、N、P含量、化学计量比及养分转移率的差异, 并用Origin 9.0制图。
2 结果和分析 2.1 马尾松叶片C、N、P含量马尾松2年龄叶片和凋落叶平均C含量分别为497.7 g/kg和506.0 g/kg, 分别比1年龄叶片C含量(481.4 g/kg)高3.4%和5.1%(P < 0.05), 表明马尾松叶片在衰老过程中C含量有增加趋势。恢复13 a的马尾松1年龄叶片C含量与CK1无显著差异, 而恢复30 a和33 a马尾松1年龄叶片C含量则显著低于CK1, 随马尾松恢复年限的增加, 马尾松叶片C含量总体有下降趋势(表 2)。
| 恢复年限 Restoration years/a |
1年龄叶片 One-year old foliage |
2年龄叶片 Two-year old foliage |
凋落叶 Litter foliage |
|
| 总有机碳 | CK1 | 487.58±3.62 a | 502.91±7.75 a | 492.83±0.77 d |
| Total organic carbon/(g/kg) | 13 | 484.87±0.16 ab | 503.30±0.25 a | 518.60±1.07 a |
| 30 | 477.56±2.88 cd | 498.72±3.98 ab | 504.58±0.35 c | |
| 33 | 481.03±1.31 bc | 493.08±1.77 bc | 509.10±2.78 b | |
| CK2 | 476.06±0.51 d | 490.59±0.53 c | 504.91±0.24 c | |
| 平均值 | 481.42±4.84 | 497.72±5.73 | 506.00±9.29 | |
| 全氮Total nitrogen/(g/kg) | CK1 | 9.00±1.25 b | 8.13±1.07 c | 5.58±1.16 a |
| 13 | 8.86±0.54 b | 7.55±0.32 c | 6.34±0.76 a | |
| 30 | 11.15±2.01 a | 9.47±0.77 b | 6.50±0.05 a | |
| 33 | 8.91±0.04 b | 8.56±0.05 bc | 6.64±0.07 a | |
| CK2 | 12.48±0.14 a | 11.13±0.90 a | 6.07±0.09 a | |
| 平均值Average | 10.08±1.65 | 8.97±1.40 | 6.23±0.42 | |
| 全磷Total phosphorus/(g/kg) | CK1 | 0.68±0.06 b | 0.59±0.01 b | 0.32±0.03 ab |
| 13 | 0.78±0.01 b | 0.62±0.04 a | 0.25±0.00 d | |
| 30 | 0.84±0.19 b | 0.59±0.06 a | 0.29±0.00 c | |
| 33 | 0.81±0.03 b | 0.62±0.01 a | 0.35±0.01 a | |
| CK2 | 1.08±0.03 a | 0.68±0.10 a | 0.32±0.00 bc | |
| 平均值Average | 0.84±0.15 | 0.60±0.08 | 0.31±0.04 | |
| 平均值±标准差, 不同小写字母表示不同恢复年限之间差异性显著(P < 0.05) | ||||
马尾松2年龄叶片和凋落叶平均N含量分别为9.0 g/kg和6.2 g/kg, 比1年龄叶片N含量(10.1 g/kg)低10.9%和38.6%(P < 0.05)。恢复13 a和33 a马尾松1年龄叶片N含量分别与CK1无显著性差异。恢复30 a马尾松1年龄叶片N含量相比CK1增加了23.9%(P < 0.05), 恢复30 a马尾松1年龄叶片N含量相比CK2无显著差异(表 2)。
马尾松2年龄叶片和凋落叶平均P含量分别为0.6 g/kg和0.3 g/kg, 分别比1年龄叶片P含量(0.8 g/kg)低25.0%和62.5%(P < 0.05)。恢复13-33 a马尾松1年龄叶片P含量与CK1相比无显著差异, 但显著低于CK2的1年龄叶片P含量(表 2)。总体而言, 在侵蚀退化红壤恢复过程中, 马尾松1年龄叶片N、P含量虽有增加趋势但总体变化不大, 但叶片在衰老过程中N、P含量变化较大(1年龄叶片、2年龄叶片N、P含量分别与凋落叶N、P含量差异显著), 养分发生了转移。
2.2 马尾松叶片C:N、C:P、N:P化学计量比马尾松1年龄、2年龄叶片和凋落叶C:N变化幅度分别为38.1-54.9、44.3-66.7和76.7-91.1。其中, 恢复13 a和33 a的马尾松1年龄叶片C:N与CK1相比均无显著差异, 而恢复30 a的马尾松1年龄叶片C:N比CK1的下降了20.4%(P < 0.05), 恢复30 a 1年龄叶片C:N与CK2相比无显著性差异(表 3)。
| 恢复年限 Restoration years (a) |
1年龄叶片 One-year old foliage |
2年龄叶片 Two-year old foliage |
凋落叶 Litter foliage |
|
| C:N | CK1 | 54.90±7.67 a | 62.61±8.33 a | 91.08±20.52 a |
| 13 | 54.89±3.26 a | 66.73±2.96 a | 82.64±9.69 a | |
| 30 | 43.71±7.30 b | 52.90±4.42 ab | 77.66±0.66 a | |
| 33 | 54.00±0.39 a | 57.61±0.50 ab | 76.66±0.92 a | |
| CK2 | 38.14±0.39 b | 44.28±3.62 b | 83.18±1.27 a | |
| 平均值Average | 49.13±7.75 | 56.83±8.73 | 82.24±5.73 | |
| C:P | CK1 | 716.46±67.14 a | 1058.75±37.74 a | 1528.13±141.63 cd |
| 13 | 621.90±6.99 ab | 786.07±44.65 b | 2054.23±13.91 a | |
| 30 | 589.04±122.53 b | 850.54±92.77 b | 1738.80±20.98 b | |
| 33 | 594.28±17.13 b | 789.21±14.25 b | 1443.19±94.37 d | |
| CK2 | 439.52±13.36 c | 729.79±105.67 b | 1588.86±7.96 c | |
| 平均值Average | 592.24±99.56 | 842.87±128.02 | 1670.64±240.06 | |
| N:P | CK1 | 13.12±0.92 a | 17.07±1.83 a | 17.27±3.56 c |
| 13 | 11.36±0.82 b | 11.81±1.53 a | 25.08±2.86 a | |
| 30 | 13.41±0.62 a | 16.10±1.62 a | 22.39±0.43 ab | |
| 33 | 11.01±0.40 b | 13.70±0.22 a | 18.82±1.01 bc | |
| CK2 | 11.53±0.47 b | 16.68±3.76 a | 19.10±0.35 bc | |
| 平均值Average | 12.08±1.10 | 15.02±2.24 | 20.53±3.15 | |
| 平均值±标准差, 不同小写字母表示不同恢复年限之间差异性显著(P < 0.05) | ||||
马尾松1年龄、2年龄叶片和凋落叶C:P变化幅度分别为439.5-716.5、729.8-1058.8和1443.2-2054.2。恢复13 a马尾松1年龄叶片C:P与CK1相比无显著差异, 而30 a和33 a马尾松1年龄叶片C:P与CK1相比分别下降了17.8%和17.1%(P < 0.05), 30 a和33 a马尾松1年龄叶片C:P均显著高于CK2(表 3)。
马尾松1年龄、2年龄叶片和凋落叶N:P变化幅度分别为11.0-13.4、11.8-17.1和17.3-25.1。恢复13 a和33 a1年龄叶片N:P相比CK1分别下降了13.3%和16.0%(P < 0.05), 恢复13 a和33 a1年龄叶片N:P与CK2无显著性差异, 但恢复30 a1年龄叶片N:P却显著高于CK2(表 3)。
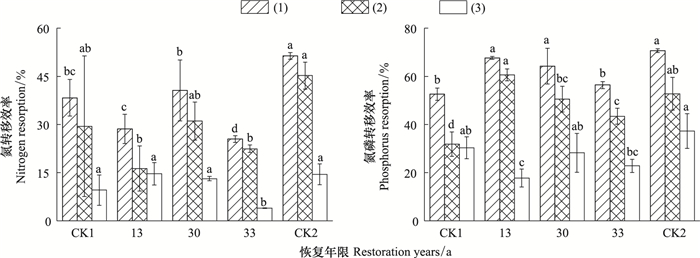
2.3 马尾松叶片的N、P转移特征凋落叶和1年龄叶片之间的N转移率均值为36.9%, 恢复13 a和30 a的N转移率与CK1相比无显著差异, 恢复13-33 a的N转移率相比CK2分别低44.6%、21.1%和50.8%(P < 0.05)(图 1)。随恢复年限的变化, 凋落叶和1年龄叶片之间的P转移率变化不大, 均值为62.3%, 恢复33 a的马尾松林的P转移率相比CK1无显著差异, 恢复13 a和30 a的P转移率相比CK1分别增加了28.6%和22.1%(P < 0.05)(图 1)。
|
| 图 1 马尾松叶片N、P转移率 Fig. 1 The N and P resorption efficiency of P. massoniana foliage 图例中(1)表示凋落叶和1年龄叶片之间的N (P)转移率, (2)表示凋落叶和2年龄叶片之间的N (P)转移率, (3)表示2年龄和1年龄叶片之间的N (P)转移率。不同小写字母表示不同恢复年限之间差异显著(P < 0.05) |
不同恢复年限的凋落叶和2年龄叶片之间的N转移率差异性较小(图 1)。凋落叶和2年龄叶片之间的P转移率波动趋势与凋落叶和1年龄叶片之间的P转移率接近(图 1)。
2年龄和1年龄叶片之间的N转移随恢复年限的增加变化不大, 比凋落叶和1年龄叶片之间的N转移率低69.8%(P < 0.05)。恢复13 a和30 a的2年龄和1年龄叶片之间的N转移率与CK1、CK2相比均无显著性差异, 恢复33 a的2年龄和1年龄叶片之间的N转移率显著最低, 这可能与植物在不同叶龄阶段自身养分转移快慢有关(图 1)。2年龄和1年龄叶片之间的P转移率比凋落叶和1年龄叶片之间的P转移率低56.2%(P < 0.05)。CK2 2年龄和1年龄叶片之间的P转移率显著最高(图 1)。
通过比较1年龄、2年龄、凋落叶彼此之间的N (P)转移率, 总体表明马尾松叶片在衰老前就开始发生养分转移, 但是大量的养分转移主要还是发生在凋落前。凋落叶和1年龄叶片之间的P转移率显著高于N转移率。随着1年龄叶片C:N、C:P的增加, 马尾松凋落叶和1年龄叶片之间的N、P转移率分别随之显著下降(P < 0.05), 说明C:N、C:P的大小可能控制着养分转移率的高低。治理后马尾松树高和胸径比未治理的对照(CK1)显著增加(样地概况中), 利用线性模拟发现, C:N和C:P比与树高、胸径成显著负相关关系(P < 0.05)(表 4)。
| 1年龄叶片C:N C:N of one-year old foliage |
1年龄叶片C:P C:P of one-year old foliage |
||||||
| 线性方程Linear | r | P | 线性方程Linear | r | P | ||
| 树高Tree height/m | y=-0.62x+40.337 | 0.824 | < 0.000 | y=-0.047x+37.548 | 0.796 | < 0.000 | |
| 胸径Diameter at breast height (DBH)/cm | y=-1.576x+94.195 | 0.790 | < 0.000 | y=-0.126x+91.417 | 0.810 | < 0.000 | |
| 氮转移率N resorption/% | y=-0.9047x+81.307 | 0.711 | 0.003 | - | - | - | |
| 磷转移率P resorption/% | - | - | - | y=-0.056x+95.467 | 0.778 | 0.001 | |
| 表中转移率表示凋落叶和1年龄叶片之间的N (P)转移率 | |||||||
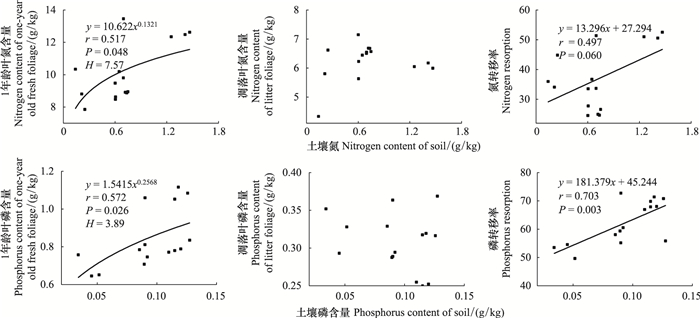
马尾松1年龄叶片N、P含量分别与土壤N、P含量呈显著正相关关系(图 2);凋落叶N、P含量分别与土壤N、P含量不相关(图 2);N、P转移率分别随土壤N、P含量的升高而升高(图 2), 即植物-土壤元素变化呈现一致性。按照内稳性模型y=cx1/H回归分析计算知, 1年龄叶片N、P的内稳性指数H分别为7.57(图 2)和3.89(图 2), 表明马尾松内稳性高, 而控制N元素变化的能力比P元素强。
|
| 图 2 叶片-土壤养分的关系(转移率表示凋落叶和1年龄叶片之间的N (P)转移率) Fig. 2 Relationship in foliage and soil nutrient of P. massoniana (Here expressed the N and P resorption that between litter foliage and one-year old fresh foliage) |
C、N、P含量是植物生长重要的生理指标[20], 也是对环境条件积极响应的结果。本研究中, 马尾松1年龄叶片C含量平均水平(476-588 g/kg)低于天童山马尾松叶片C含量(514 g/kg)[21]及珠江三角洲马尾松叶片C含量(537 g/kg)[22], 说明侵蚀红壤马尾松叶片有机化合物含量整体较低。马尾松1年龄叶片N、P含量均值分别为10.1 g/kg和0.8 g/kg, 均在中国东部南北样带102个优势种叶片N和P含量范围内(分别是8.4-30.5 g/kg和0.6-6.2 g/kg)[23], 高于天童山马尾松叶片N (5.8 g/kg)与P (0.5 g/kg)平均水平[21], 与珠江三角洲马尾松叶片N (9.6 g/kg)与P (0.6 g/kg)平均水平[23]更接近, 这可能主要受土壤养分含量和采样季节的影响, 另一方面反映了侵蚀地生长的马尾松的内部存在养分转移。本研究中, 尽管恢复30 a和33 a的恢复年限接近, 但在恢复30 a的实验地林下曾套种胡枝子, 补植黑荆等豆科植物, 土壤N恢复较快, 可供植物吸收的N素也增加, 而33 a的实验样地治理初期尽管草地覆盖和马尾松林生长恢复很快, 但其后因人畜破坏等原因导致实验地重新发生退化[24], 因此恢复30 a的马尾松1年龄叶片N含量显著较高, 这也是导致恢复33 a的马尾松生长较慢的原因。恢复13-33 a的马尾松叶片N、P含量仍显著低于CK2马尾松叶片N、P含量, 主要是因为其土壤养分含量仍较低(表 1)。
3.2 马尾松叶片C:N、C:P、N:P化学计量随恢复年限的变化和养分限制性本研究中, 马尾松1年龄叶片C:N均值为49.1, 与天童山及珠江三角洲马尾松叶片C:N均值接近(分别为51.5和55.9)[21-22];而C:P (592.2)则明显较低(天童山和珠江三角洲马尾松平均水平分别为702.4和839.1)[21-22], 这主要是因为马尾松1年龄叶片C含量相对较低导致的。另外, 马尾松1年龄叶片N:P均值为12.1, 略低于天童山马尾松叶平均N:P (13.9)[21]和全球平均水平(13.8)[25]。Koerselma[26]等认为, 虽然植物叶片化学计量比会因季节和树种不同, 但总体上在N:P < 10-14时, 说明受N限制, N:P>16-21时, 说明受P限制, 介于两者中间表明受到N、P元素的共同限制作用[27]。本研究中, CK1与恢复30 a马尾松1年龄叶片N:P无差异(P>0.05)(均值为13.3), 均显著高于恢复13 a、33 a及CK2马尾松1年龄叶片N:P (P < 0.05)(变化范围为11.0-11.5), 说明马尾松林仍受N素和P素共同限制。另一方面, 马尾松根系与外生菌根真菌形成的菌根能促进土壤P溶解, 增加寄主对P的吸收[28], 因此, 马尾松能适应贫瘠土壤生长。总体来说, 马尾松叶片C:N、C:P和N:P随恢复年限变化较小(表 3), 这与马尾松叶片N、P较高的内稳性指数有关(分别为7.57和3.89), 说明在受养分限制的情况下, 植物体具有保持自身化学元素组成相对稳定的能力[6], 而陆地植物器官中相对恒定的N:P是植物在地球生存的重要适应机制[29]。
3.3 马尾松叶片N、P转移率及其控制因素养分转移是森林生态系统保持养分的最重要机制之一, 是研究植物生态策略的一个重要生态学指标[30]。本研究中, 不同恢复年限马尾松凋落叶和1年龄叶片间的N转移率(均值为37%)低于全球常绿植物的N素转移率(47%)[31], 但CK2马尾松凋落叶和1年龄叶片间N转移率(51%)与天童山马尾松N转移率(53%)接近[32]。本研究除了CK2外, 其余样地的马尾松凋落叶和1年龄叶片间的N转移率较低, 原因可能包括两个方面, 一方面马尾松富含丰富的树脂、单宁酸、蜡等, 会抑制N素转移[10], 另一方面侵蚀土壤可利用P库较低[33], P含量不足也会影响N的转移[34]。同N素转移率的结果相比, 马尾松凋落叶和1年龄叶片间P转移率较高(均值为62%), 且高于全球常绿植物P素平均转移率(51%)[31]及天童山马尾松P转移率(41%), 生物的生长需要大量的核糖体, 核糖体是植物体内P的主要贮藏库[6], 因而导致植物P转移率高于N转移率, Tully等[13]也有类似结果。本研究中N:P表现出受土壤N、P共同限制的特征, N转移率显著低于P转移率, 说明转移率一方面可以反映马尾松对N、P的需求存在差异, 另一方面表明N、P在马尾松体内的吸收和转化机制不同[35], 因此, 养分转移效率高低有时并不等同于养分限制的高低。
本研究结果还表明, 植物养分的转移率受养分利用效率和植物生长的影响。本研究中1年龄叶片C:N、C:P分别与马尾松凋落叶和1年龄叶片间N、P转移率成负相关关系(r=0.711和r=0.778, P < 0.05)(表 4), 说明N、P利用效率是影响N、P养分转移的主要因素。当马尾松叶片C:N、C:P较低时, 表明N、P利用效率较低, 当叶片衰老时更多的N和P可以转移利用;而当马尾松叶片C:N和C:P较高时, N、P利用效率较高。Reed等[14]认为植物占据较贫瘠的生境时, 通常具有更高的养分转移效率, 而本研究中马尾松凋落叶和1年龄叶片间N、P转移率随土壤N、P含量的增加而增高(图 2), 这与Vourlitis等[36]结果相反, 一方面说明侵蚀红壤仍较贫瘠, 土壤中可供植物吸收利用的养分较低, 但受马尾松内稳性控制, 为让C:N、C:P保持一定的范围, 因此植物体内可供转移利用的养分含量较低, 其转移效率随之较低。另一方面, 利用线性模拟发现, C:N、C:P分别与树高、胸径成显著负相关关系(P < 0.05)(表 4), 即马尾松生长对N、P的需求会影响化学计量比的变化, 从而影响养分转移, 因此土壤养分并不能充分预测养分转移模式[13]。本研究还发现, 马尾松2年龄叶片也发生了N、P转移(图 1), 表明叶片更新过程养分转移是逐渐发生的, 为下一个生长季节叶片的生长提供充足的养分, 以满足自身生长的需要, 该机制有利于马尾松先锋群落的建立。
4 结论在侵蚀退化红壤生态恢复过程中, 1)马尾松叶片C、N、P含量及其C:N、C:P和N:P化学计量比变化较小, 这与马尾松较高的N、P内稳性指数有关(分别为7.57和3.89), 说明在受养分限制的情况下, 马尾松具有保持自身化学元素组成相对稳定的能力;2)马尾松叶片的养分转移率受养分利用效率和植物生长的影响, 养分利用效率较低、植物生长较快时, 转移率较高;3)红壤侵蚀地生态恢复缓慢, 土壤养分贫瘠, 叶片N:P和养分转移均表明马尾松生长仍受N、P养分共同限制。因此, 为了提高马尾松林的生产力, 下一步治理措施应考虑适当施加N肥和P肥。
致谢: 福建师范大学地理科学学院陈岳民研究员对本文写作给予帮助, 特此致谢。| [1] | Fan H B, Wu J P, Liu W F, Yuan Y H, Hu L, Cai Q K. Linkages of plant and soil C:N:P stoichiometry and their relationships to forest growth in subtropical plantations. Plant and Soil , 2015, 392 (1/2) : 127–138. |
| [2] | Moe S J, Stelzer R S, Forman M R, Harpole W S, Daufresne T, Yoshida T. Recent advances in ecological stoichiometry:insights for population and community ecology. Oikos , 2005, 109 (1) : 29–39. DOI:10.1111/oik.2005.109.issue-1 |
| [3] | Wang M, Murphy M T, Moore T R. Nutrient resorption of two evergreen shrubs in response to long-term fertilization in a bog. Oecologia , 2014, 174 (2) : 365–377. DOI:10.1007/s00442-013-2784-7 |
| [4] | Elser J J, Bracken M E S, Cleland E E, Gruner D S, Harpole W S, Hillebrand H, Ngai J T, Seabloom E W, Shurin J B, Smith J E. Global analysis of nitrogen and phosphorus limitation of primary producers in freshwater, marine and terrestrial ecosystems. Ecology Letters , 2007, 10 (12) : 1135–1142. DOI:10.1111/ele.2007.10.issue-12 |
| [5] | Pan F J, Zhang W, Liu S J, Li D J, Wang K L. Leaf N:P stoichiometry across plant functional groups in the karst region of southwestern China. Trees , 2015, 29 (3) : 883–892. DOI:10.1007/s00468-015-1170-y |
| [6] | Yu Q, Elser J J, He N P, Wu H H, Chen Q S, Zhang G M, Han X G. Stoichiometric homeostasis of vascular plants in the Inner Mongolia grassland. Oecologia , 2011, 166 (1) : 1–10. DOI:10.1007/s00442-010-1902-z |
| [7] | Farahat E, Linderholm H W. Nutrient resorption efficiency and proficiency in economic wood trees irrigated by treated wastewater in desert planted forests. Agricultural Water Management , 2015, 155 : 67–75. DOI:10.1016/j.agwat.2015.03.008 |
| [8] | Chen F S, Niklas K J, Liu Y, Fang X M, Wan S Z, Wang H M. Nitrogen and phosphorus additions alter nutrient dynamics but not resorption efficiencies of Chinese fir leaves and twigs differing in age. Tree Physiology , 2015, 35 (10) : 1106–1117. DOI:10.1093/treephys/tpv076 |
| [9] | 阎恩荣, 王希华, 周武. 天童常绿阔叶林演替系列植物群落的N:P化学计量特征. 植物生态学报 , 2008, 32 (1) : 13–22. |
| [10] | McGroddy M E, Daufresne T, Hedin L O. Scaling of C:N:P stoichiometry in forests worldwide:implications of terrestrial Redfield-type ratios. Ecology , 2004, 85 (9) : 2390–2401. DOI:10.1890/03-0351 |
| [11] | Aerts R. Nutrient use efficiency in evergreen and deciduous species from heathlands. Oecologia , 1990, 84 (3) : 391–397. DOI:10.1007/BF00329765 |
| [12] | 薛立, 徐燕, 吴敏, 李燕. 4种阔叶树种叶中氮和磷的季节动态及其转移. 生态学报 , 2005, 25 (3) : 520–526. |
| [13] | Tully K L, Wood T E, Schwantes A M, Lawrence D. Soil nutrient availability and reproductive effort drive patterns in nutrient resorption in Pentaclethra macroloba. Ecology , 2013, 94 (4) : 930–940. DOI:10.1890/12-0781.1 |
| [14] | Reed S C, Townsend A R, Davidson E A, Cleveland C C. Stoichiometric patterns in foliar nutrient resorption across multiple scales. New Phytologist , 2012, 196 (1) : 173–180. DOI:10.1111/j.1469-8137.2012.04249.x |
| [15] | 何圣嘉, 谢锦升, 曾宏达, 田浩, 周艳翔, 胥超, 吕茂奎, 杨玉盛. 红壤侵蚀地马尾松林恢复后土壤有机碳库动态. 生态学报 , 2013, 33 (10) : 2964–2973. |
| [16] | Xie J S, Guo J F, Yang Z J, Huang Z Q, Chen G S, Yang Y S. Rapid accumulation of carbon on severely eroded red soils through afforestation in subtropical China. Forest Ecology and Management , 2013, 300 (300) : 53–59. |
| [17] | 吕茂奎, 谢锦升, 周艳翔, 曾宏达, 江军, 陈细香, 胥超, 陈坦, 付林池. 红壤侵蚀地马尾松人工林恢复过程中土壤非保护性有机碳的变化. 应用生态学报 , 2014, 25 (1) : 37–54. |
| [18] | 鲍士旦. 土壤农化分析. 北京: 中国农业出版社, 200074–76. |
| [19] | Pugnaire F I, Chapin Ⅲ F S. Controls over nutrient resorption from leaves of evergreen Mediterranean species. Ecology , 1993, 74 (1) : 124–129. DOI:10.2307/1939507 |
| [20] | Peñuelas J, Poulter B, Sardans J, Ciais P, van der Velde M, Bopp L, Boucher O, Godderis Y, Hinsinger P, Llusia J, Nardin E, Vicca S, Obersteiner M, Janssens I A. Human-induced nitrogen-phosphorus imbalances alter natural and managed ecosystems across the globe. Nature Communications , 2013, 4 (1) : 2934. |
| [21] | 阎恩荣, 王希华, 郭明, 仲强, 周武. 浙江天童常绿阔叶林、常绿针叶林与落叶阔叶林的C:N:P化学计量特征. 植物生态学报 , 2010, 34 (1) : 48–57. |
| [22] | 吴统贵, 陈步峰, 肖以华, 潘勇军, 陈勇, 萧江华. 珠江三角洲3种典型森林类型乔木叶片生态化学计量学. 植物生态学报 , 2010, 34 (1) : 58–63. |
| [23] | 任书杰, 于贵瑞, 姜春明, 方华军, 孙晓敏. 中国东部南北样带森林生态系统102个优势种叶片碳氮磷化学计量学统计特征. 应用生态学报 , 2012, 23 (3) : 581–586. |
| [24] | 谢锦升, 陈光水, 何宗明, 杨玉盛, 吴大同. 退化红壤不同治理模式马尾松生长特点分析. 水土保持通报 , 2001, 21 (6) : 24–27. |
| [25] | Reich P B, Oleksyn J. Global patterns of plant leaf N and P in relation to temperature and latitude. Proceedings of the National Academy of Sciences of the United States of America , 2004, 101 (30) : 11001–11006. DOI:10.1073/pnas.0403588101 |
| [26] | Koerselman W, Meuleman A F M. The vegetation N:P ratio:a new tool to detect the nature of nutrient limitation. Journal of Applied Ecology , 1996, 33 (6) : 1441–1450. DOI:10.2307/2404783 |
| [27] | Wright I J, Reich P B, Westoby M, Ackerly D D, Baruch Z, Bongers F, Cavender-Bares J, Chapin T, Cornelissen J H C, Diemer M, Flexas J, Garnier E, Groom P K, Gulias J, Hikosaka K, Lamont B B, Lee T, Lee W, Lusk C, Midgley J J, Navas M L, Nilnemets V, Oleksyn J, Osada N, Poorter H, Poot P, Prior L, Pyankov V I, Roumet C, Thomas S C, Tjoelker M G, Veneklaas E J, Villar R. The worldwide leaf economics spectrum. Nature , 2004, 428 (6985) : 821–827. DOI:10.1038/nature02403 |
| [28] | 陈展, 王琳, 尚鹤. 接种彩色豆马勃对模拟酸沉降下马尾松幼苗生物量的影响. 生态学报 , 2013, 33 (20) : 6526–6533. |
| [29] | 曾昭霞, 王克林, 刘孝利, 曾馥平, 宋同清, 彭晚霞, 张浩, 杜虎. 桂西北喀斯特森林植物-凋落物-土壤生态化学计量特征. 植物生态学报 , 2015, 39 (7) : 682–693. |
| [30] | Wang X G, Lü X T, Han X G. Responses of nutrient concentrations and stoichiometry of senesced leaves in dominant plants to nitrogen addition and prescribed burning in a temperate steppe. Ecological Engineering , 2014, 70 (3) : 154–161. |
| [31] | Aerts R, Chapin Ⅲ F S. The mineral nutrition of wild plants revisited:a re-evaluation of processes and patterns. Advances in Ecological Research , 1999, 30 (08) : 1–67. |
| [32] | 王希华, 黄建军, 闫恩荣. 天童常绿阔叶林若干树种的叶片营养转移研究. 广西植物 , 2004, 24 (1) : 81–85. |
| [33] | 詹书侠, 陈伏生, 胡小飞, 甘露, 朱友林. 中亚热带丘陵红壤区森林演替典型阶段土壤氮磷有效性. 生态学报 , 2009, 29 (9) : 4673–5680. |
| [34] | Yan Z B, Kim N, Han W X, Guo Y L, Han T S, Du E Z, Fang J Y. Effects of nitrogen and phosphorus supply on growth rate, leaf stoichiometry, and nutrient resorption of Arabidopsis thaliana. Plant and Soil , 2015, 388 (1/2) : 147–155. |
| [35] | Bell C W, Asao S, Calderon F, Wolk B, Wallenstein M D. Plant nitrogen uptake drives rhizosphere bacterial community assembly during plant growth. Soil Biology and Biochemistry , 2015, 85 : 170–182. DOI:10.1016/j.soilbio.2015.03.006 |
| [36] | Vourlitis G L, de Almeida Lobo F, Lawrence S, Holt K, Zappia A, Pinto Jr O B, de Souza Nogueira J. Nutrient resorption in tropical savanna forests and woodlands of central Brazil. Plant Ecology , 2014, 215 (9) : 963–975. DOI:10.1007/s11258-014-0348-5 |
 2017, Vol. 37
2017, Vol. 37