文章信息
- 张鹏, 赵洋, 黄磊, 胡宜刚, 韩旭
- ZHANG Peng, ZHAO Yang, HUANG Lei, HU Yigang, HAN Xu
- 植被重建对露天煤矿排土场土壤酶活性的影响
- Effect of revegetation on soil extracellular enzyme activity in the dumping site of an open-pit coal mine in Heidaigou
- 生态学报, 2016, 36(9): 2715-2723
- Acta Ecologica Sinica, 2016, 36(9): 2715-2723
- http://dx.doi.org/10.5846/stxb201505231034
-
文章历史
- 收稿日期: 2015-05-23
- 修订日期: 2016-01-07
2. 甘肃农业大学 资源与环境学院, 兰州 730070
2. College of Resource and Environmental Sciences, Gansu Agricultural University, Lanzhou 730070, China
采矿业是我国国民经济的重要基础产业,在国民经济发展中具有重要地位。矿产资源的大规模开采在为国民经济发展做出重要贡献的同时,不可避免地破坏大量土地并引发一系列生态环境问题。据统计,目前煤矿开采造成年增沉陷地面积约2.7—4.2万hm2;年增煤矸石约3亿t,总占地达4万hm2,而传统的土地复垦率尚不到20%[1]。我国超过70%的煤炭产自西部,露天开采需要剥离上覆岩土层,对土地资源的破坏更加严重,露天开采每万吨煤,破坏土地面积0.22 hm2,其中直接挖掘破坏土地面积0.12 hm2,外排土场占用0.10 hm2,土地复垦率仅有2%。露天开采对土壤结构与肥力破坏性强,造成排土场水土流失严重、渗透性差、土壤贫瘠、生态修复难度大,排土场植被重建和土壤生境恢复是一项艰巨而又亟待解决的难题[2, 3]。
人工植被建设是受损生态系统恢复的重要途径,也是最有效的恢复方法之一。国内外大量以植被建设为主的生态恢复实践和研究表明,受损系统土壤生境的恢复是一个十分漫长的过程,如何恢复受损的土壤系统,促进生态系统功能的提高,是生态恢复的前沿难点问题,土壤生境的恢复是生态系统全面恢复的根本[4, 5, 6, 7, 8]。土壤酶是高分子有机物催化分解的一类具有蛋白性质的生物催化剂,主要来源于土壤微生物的活动、植物根系分泌物和腐解的动植物残体,参与土壤中各种有机质的分解、合成、转化及与无机物质的氧化还原等过程,其活性与土壤理化特性、微生物及土壤类型等关系密切,可以很好地指示土壤有机物分解、元素循环和微生物养分需求等土壤生态系统的变化,是评价土壤质量的一个重要指标[9, 10, 11]。近年来,有关煤矿区复垦适生先锋植物种的选育、土壤改良及生物复垦技术等生态恢复实践工作和研究有了长足发展,但也有部分人工植被因为植物种类单一、抗逆性差,仅表现出生态治理的短期行为;尤其在一些干旱缺水的地区,露天开采造成的扰动和破坏由于气候条件的影响而变得更为严重,矿区人工植被恢复的长期生态效应仍不明显[1, 12, 13]。本研究以黑岱沟露天煤矿排土场人工植被恢复区为研究对象,分析植被重建及恢复过程中土壤酶活性的演变过程,探讨土壤酶活性在评价煤矿区人工植被恢复过程中的生态意义,为黄土高原露天煤矿生态脆弱区植被恢复与生态重建提供科学依据。
1 材料与方法 1.1 研究区概况黑岱沟露天煤矿位于内蒙古自治区鄂尔多斯市准格尔旗东部,矿区地貌为典型的黄土丘陵沟壑区,面积约52.11 km2 (39°43′—39°49′ N,111°13′—111°20′ E),海拔1025—1302 m。该区气候属中温带半干旱大陆性气候,年均温7.2 ℃,≥10 ℃年积温3350 ℃。年均降水量401.6 mm,集中在7—9月,约占全年降水量的60%—70%。年蒸发量为1824.7—2896.1 mm。地带性土壤为以砒沙岩为母岩的栗褐土,矿区土壤主要为黄绵土,土质疏松,抗冲蚀性差,微碱性,肥力低下[14]。
矿区内地带性植被属暖温型草原带,植被稀疏低矮,盖度一般在30%以下。人工林以刺槐(Robinia pseudoacacia)、油松(Pinus tabulaeformis)、小叶杨(Populus simonii)、锦鸡儿(Caragana mirophylla)、沙棘(Hippophae rhamnoides)等植物为主;荒坡主要为铁杆蒿(Artemisia gmelinii)、本氏针茅(Stipa bungeana)、白草(Pennisetum centrasiaticum)、沙蒿(Artemisia arenaria)、狗尾草(Setaria viridis)、披针叶黄华(Thermopsis lanceolata)、赖草(Leymus secalinus)等组成的处于不同恢复阶段的草本植物群落[2]。
1.2 野外调查与样品采集2013年8月在黑岱沟露天煤矿北排土场(1995年建植)选择4种植被配置类型,即“草本”、“乔木”、“乔+草”、“乔+灌+草”;在东排土场(1998年建植)、西排土场(2003年建植)选择常见的“乔+灌+草”配置类型;同时选择内排土场裸地(2010年排土,未进行植被建设)、相邻的撂荒地(1998年撂荒)和天然植被区进行植被调查和取样(各样地基本情况见表 1)。在每样地随机设置3个10 m × 10 m的大样方用于木本植物的调查,同时在每个大样方内再随机设置3个1 m × 1 m的小样方用于草本植物的调查。在各样地大样方内按S型选取6点,每点用土钻采集0—20 cm土壤,3次重复。各样方多点采集土样混匀后带回实验室经处理后用于土壤理化指标和土壤酶活性的测定。
| 样地/代码Plots/Code | 植被类型Vegetation types | 建植年代Year revegetated | 建植年龄/aAge revegetated | 主要人工植被/天然植被Main artificial vegetation |
| 内排土场 /BLInner dump | 裸地 | — | — | 沙蒿 Artemisia desertorum、狗尾草 Setaria viridis、赖草 Leymus secalinus |
| 西排土场 /ASH10West dump | 乔木+灌木+草本 | 2003 | 10 | 毛白杨+小叶锦鸡儿+白羊草 Populus tomentosa+ Caragana microphylla+ Bothriochloa ischaemum |
| 东排土场 /ASH15East dump | 乔木+灌木+草本 | 1998 | 15 | 毛白杨+柠条+白羊草 Populus tomentosa+ Caragana korshinskii+ Bothriochloa ischaemum |
| 北排土场 /ASH18North dump | 乔木+灌木+草本 | 1995 | 18 | 毛白杨+沙棘+白羊草 Populus tomentosa+ Hippophae rhamnoides+ Bothriochloa ischaemum |
| 北排土场 /AH18North dump | 乔木+草本 | 1995 | 18 | 毛白杨+白羊草 Populus tomentosa+ Bothriochloa ischaemum |
| 北排土场 A18North dump | 乔木 | 1995 | 18 | 毛白杨+油松 Populus tomentosa+ Pinus tabulaeformis |
| 北排土场 H18North dump | 草本 | 1995 | 18 | 白羊草 Bothriochloa ischaemum |
| 撂荒地 /ALAbandoned land | 草本 | 1998撂荒 | 15 | 山杏 Armeniaca sibirica,狗尾草 Setaria viridis,赖草 Leymus secalinus,本氏针茅 Stipa capillata,白羊草 Bothriochloa ischaemum |
| 天然植被区 /NVNatural vegetation | 草本 | 茭蒿 Artemisia giraldii,本氏针茅 Stipa capillata,白羊草 Bothriochloa ischaemum,猪毛菜 Salsola collina,牛枝子 Lespedeza potaninii,苦豆子 Sophora alopecuroides |
土壤有机质(SOM)、铵态氮(NH4+-N)、硝态氮(NO3--N)、速效磷(AP)、速效钾(AK)、电导率(C)、pH值采用常规方法测定[15],不同植被类型及恢复阶段土壤基本理化性质见表 2。
| 样地代码Site code | 土壤有机质SOM/(g/kg) | 铵态氮NH4+-N/(mg/kg) | 硝态氮NO3--N/(mg/kg) | 速效磷Available P/(mg/kg) | 速效钾Available K/(mg/kg) | 电导率Conductivity/(μs/cm) | pH |
| BL | 3.9±0.34d | 6.7±0.11h | 4.7±0.08e | 6.7±0.09d | 77.4±1.06de | 0.64±0.001b | 7.97±0.02 |
| ASH10 | 4.4±0.06d | 7.6±0.08g | 5.0±0.42e | 7.4±0.13d | 82.9±1.50f | 0.71±0.003a | 8.91±0.02a |
| ASH15 | 5.3±0.18c | 10.4±0.08d | 6.9±0.05bc | 6.8±0.04b | 82.2±0.52e | 0.54±0.001f | 8.68±0.10b |
| ASH18 | 5.8±0.04b | 13.2±0.07b | 8.8±0.05a | 10.0±0.07a | 118.2±1.84a | 0.62±0.006c | 7.67±0.03e |
| AH18 | 5.6±0.14bc | 10.5±0.09cd | 7.0±0.06b | 8.8±0.10c | 98.0±1.13c | 0.58±0.003e | 8.12±0.06d |
| A18 | 5.3±0.11c | 9.7±0.20e | 6.5±0.14c | 9.5±0.10b | 105.2±0.72b | 0.57±0.003e | 7.79±0.05e |
| H18 | 3.9±0.26d | 8.5±0.07f | 5.6±0.04d | 9.5±0.10b | 107.2±0.48b | 0.60±0.001d | 7.73±0.03e |
| AL | 6.8±0.13a | 13.7±0.06a | 9.1±0.04a | 7.6±0.08d | 86.0±0.86d | 0.58±0.003e | 8.17±0.01d |
| NV | 6.4±0.06a | 10.7±0.07c | 7.1±0.05b | 7.7±0.12d | 84.4±1.30de | 0.54±0.010f | 8.44±0.03f |
| BL: 新排土场未进行植被建设的裸地;ASH10: 建植10a的乔+灌+草型植被;ASH15: 建植15a的乔+灌+草型植被;ASH18: 建植18a的乔+灌+草型植被;AH18: 建植18a的乔+草型植被;A18: 建植18a的乔木型植被;H18: 建植18a的草本型植被;AL: 撂荒15a的撂荒地;NV: 天然植被; 表中数据为平均值±标准误,同列不同小写字母表示不同样地土壤理化指标具有差异显著性( P < 0.05) | |||||||
过氧氢化酶(Catalase,CAT)采用高锰酸钾滴定法测定,多酚氧化酶(Polyphenol oxidase,POL)采用邻苯三酚比色法测定,脱氢酶(Dehydrogenase,DEH)采用TTC分光光度法测定,蔗糖酶(Sucrase,SUC)采用3,5-二硝基水杨酸比色法测定,脲酶(Urease,URE)采用苯酚钠-次氯酸钠比色法测定,磷酸酶(Phosphatase,PHO)采用磷酸苯二钠比色法测定,纤维素酶(Cellulase,CEL)采用3,5-二硝基水杨酸比色法测定[9, 16]。
1.4 土壤酶恢复速率综合评价采用土壤酶恢复速率[11]来评价植被重建对土壤酶活性的影响,计算公式如下:
式中,RRecovery指植被恢复区土壤酶相对天然植被区土壤酶活性的恢复速率,A指土壤酶活性,下标R指植被恢复区,D指未进行植被建设的新排土场,N指天然植被区。为评价植被重建后不同恢复阶段土壤酶活性的年均恢复速率,选择不同年份建植的同一人工植被类型(乔+灌+草)来计算各恢复阶段的土壤酶年均恢复速率[11]计算公式如下:
式中,RStage指不同恢复阶段土壤酶恢复速率(用%/a表示),Astart和Aend指植被建设开始(用新排土场未进行植被建设的裸地代替)和结束时的土壤酶活性,T指植被重建后恢复时间(a)。 1.5 数据处理与统计方法采用单因素方差分析(One-way ANOVA)中的最小显著差数法(LSD)分析不同植被类型、恢复阶段土壤酶活性的差异显著性;用二元变量相关(Pearson)分析土壤酶活性与土壤理化因子的相关性。所有统计分析在SPSS 11.5下完成。数据整理、计算与作图均采用Microsoft Excel 2013软件进行。
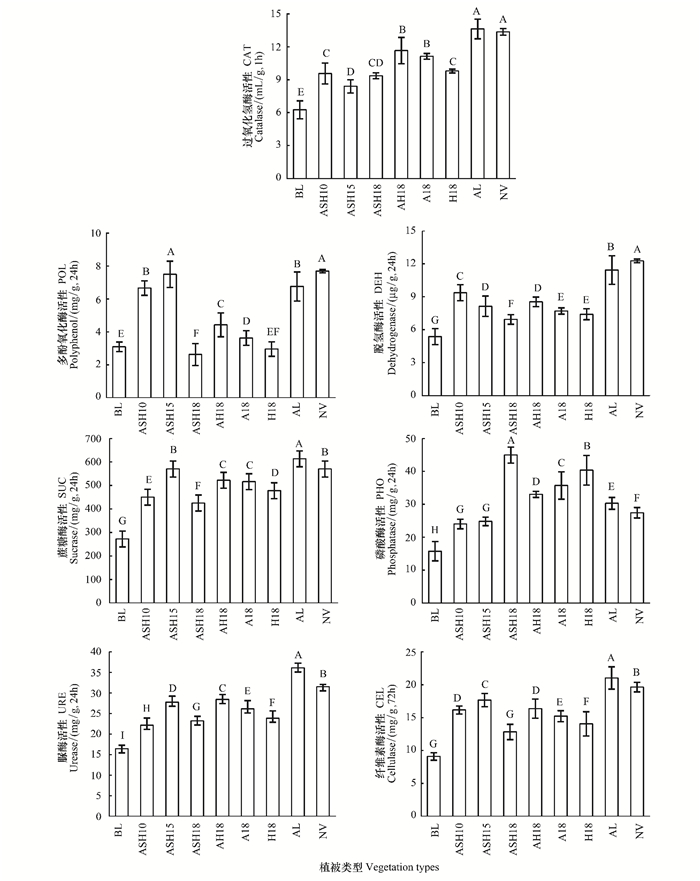
2 结果与分析 2.1 不同植被类型、恢复阶段土壤酶活性的变化方差分析显示7种土壤酶活性在9个样地间具有较高的差异显著性(图 1)。除磷酸酶外,其余6种土壤酶活性都表现为撂荒地和天然植被区显著高于人工植被区,未进行植被建设的裸地最低,差异显著。撂荒地和天然植被区过氧化氢酶活性平均为13.5 (mL/g,1h),是人工植被区(取平均值)和裸地的1.4和1.6倍;多酚氧化酶活性为7.2 (mg/kg,24h),是人工植被和裸地的1.5和1.6倍;脱氢酶活性为11.9 (μg/g,24h),是人工植被和裸地的1.5倍;蔗糖酶活性为591.9 (mg/kg,24h),是人工植被和裸地的1.2和1.8倍;脲酶活性平均为33.8 (mg/kg,24h),分别是人工植被和裸地的1.3和1.5倍;磷酸酶活性人工植被最高,为33.8 (mg/kg,24h),分别是天然植被和裸地的1.2倍和2.2倍;纤维素酶活性为20.3 (mg/kg,24h),是人工植被和裸地的1.3和1.7倍。
|
| 图 1 不同植被类型及恢复阶段土壤酶活性的变化 Fig. 1 Soil enzyme activities in different vegetation types and recovery stage 不同大写字母表示土壤酶活性在不同植被类型间具有差异显著性(P < 0.05),数据为平均值±标准误 |
人工植被配置类型对土壤酶活性影响显著,建植18a人工植被区土壤过氧化氢酶活性表现为乔+草型AH18、乔木型A18>草本型H18、乔+灌+草型ASH18,差异显著(P=0.005);多酚氧化酶活性为AH18> A18> H18、ASH18,差异显著(P < 0.001);脱氢酶活性为AH18>A18、H18>ASH18,差异显著(P < 0.001);蔗糖酶活性为AH18、A18>H18>ASH18,差异显著(P < 0.001);脲酶活性表现为(AH18)>(A18)>(H18)>(ASH18),差异显著(P < 0.001);磷酸酶活性为ASH18>H18>A18>AH18,差异显著(P < 0.001);纤维素酶活性为AH18>A18>H18>ASH18,差异显著(P < 0.001) (图 1)。
同一类型人工植被(乔+灌+草型,ASH)不同恢复阶段(建植10、15、18a)各土壤酶活性表现各异,过氧化氢酶活性差异不显著(P=0.061);多酚氧化酶活性表现为15a>10a>18a,差异显著(P < 0.001);脱氢酶活性表现为10a>15a>18a,差异显著(P < 0.001);蔗糖酶活性表现为15a>10a>18a,差异显著(P < 0.001);脲酶活性表现为15a>18a>10a,差异显著(P < 0.001);磷酸酶活性表现为18a>15a、10a,差异显著(P < 0.001);纤维素酶活性表现为15a>10a>18a,差异显著(P < 0.001)(图 1)。
2.2 土壤酶活性与土壤理化因子的相关性分析相关性分析表明(表 3),除磷酸酶外,土壤有机质与其余6种酶活性均显著正相关;铵态氮和硝态氮与过氧化氢酶、蔗糖酶、脲酶、磷酸酶、纤维素酶均显著正相关;速效磷与多酚氧化酶显著负相关,与磷酸酶显著正相关;速效钾与脱氢酶、多酚氧化酶显著负相关,与磷酸酶显著正相关;电导率与过氧化氢酶、蔗糖酶、脲酶均显著负相关;pH与脱氢酶、多酚氧化酶、纤维素酶显著正相关,与磷酸酶显著负相关。
| 变量Variables | 有机质SOM | 铵态氮NH4+-N | 硝态氮NO3--N | 速效磷Available P | 速效钾Available K | 电导率Conductivity | pH |
| 过氧化氢酶 CAT | 0.739** | 0.529** | 0.543** | 0.119 | 0.036 | -0.426* | 0.055 |
| 多酚氧化酶 POL | 0.457* | 0.100 | 0.114 | -0.76** | -0.748** | -0.254 | 0.841** |
| 脱氢酶 DEH | 0.695** | 0.359 | 0.372 | -0.344 | -0.390* | -0.310 | 0.478* |
| 蔗糖酶 SUC | 0.695** | 0.525** | 0.535** | -0.066 | -0.073 | -0.636** | 0.285 |
| 脲酶 URE | 0.833** | 0.677** | 0.679** | -0.069 | -0.104 | -0.631** | 0.179 |
| 磷酸酶 PHO | 0.222 | 0.490** | 0.489** | 0.867** | 0.902** | -0.199 | -0.605** |
| 纤维素酶 CEL | 0.726** | 0.456* | 0.468* | -0.301 | -0.318 | -0.464 | 0.475* |
| * P < 0.05, ** P < 0.01 | |||||||
撂荒地(AL)除多酚氧化酶和脱氢酶恢复速率达到天然植被的80%以上,其余5种酶恢复速率均已超过天然植被(>100%)(表 4)。人工植被区过氧化氢酶活性恢复速率在人工植被AH18、A18和H18下较快,分别是天然植被区的75.9%、68.2%和49.8%,其它植被配置下恢复速率均不到天然植被区的一半(< 50%);多酚氧化酶恢复速率在ASH15和ASH10下最快,分别为96.1%和78.4%,在其它植被配置下均低于50%;脱氢酶恢复速率仅在ASH10下超过50%,为57.8%,其余植被配置下均低于50%;蔗糖酶恢复速率在6种人工植被下均超过50%,其中ASH10最快,为99.8%;脲酶恢复速率在AH18、ASH15和A18较快,分别为79.7%、75.3%和64.4%;磷酸酶恢复速率在ASH10和ASH15下达到70.7%和77.3%,其它植被配置下均超过100%,在ASH18和H18下恢复速率最快,是天然植被区的250.1%和211.1%;纤维素酶恢复速率在ASH15、AH18、ASH10和A18下较快,分别为81.4%、69.4%、67.3%和58.6%,其余植被下均低于50%(表 4)。
| 恢复速率/%Recovery rate | ASH10 | ASH15 | ASH18 | AH18 | A18 | H18 | AL |
| 过氧化氢酶 CAT | 45.7±16.8c | 29.9±10.5d | 43.2±4.7cd | 75.9±15.9b | 68.2±5.1b | 49.8±4.1c | 103.0±25.6a |
| 多酚氧化酶POL | 78.4±5.7b | 96.1±19.5a | 6.5±8.5d | 29.3±8.5c | 12.2±3.9d | 4.5±0.6d | 80.1±10.8b |
| 脱氢酶DEH | 57.8±6.0b | 39.8±9.2c | 22.2±3.8e | 45.7±3.7c | 33.9±7.2dc | 29.2±6.1d | 87.5±14.1a |
| 蔗糖酶SUC | 59.7±10.3de | 99.8±8.8b | 51.4±5.7e | 83.9±9.3c | 81.9±10.4c | 69.0±10.6d | 114.6±17.3a |
| 脲酶URE | 38.0±6.3g | 75.3±12.9c | 44.7±10.5f | 79.7±5.6b | 64.4±10.1d | 49.3±8.4e | 130.6±11.6a |
| 磷酸酶PHO | 70.7±11.7f | 77.3±11.6f | 250.1±15.1a | 148.1±6.5d | 170.9±17.1c | 211.1±32.8b | 124.4±14.7e |
| 纤维素酶CEL | 67.3±8.7c | 81.4±11.7b | 35.4±5.2f | 69.4±13.1c | 58.6±9.3d | 47.4±14.3e | 114.0±15.2a |
| 表中数据为平均值±标准差,同行不同小写字母表示不同植被类型下土壤酶活性恢复速率具有差异显著性(P < 0.05) | |||||||
在人工植被“乔+灌+草”建植10a的恢复进程中,过氧化氢酶、多酚氧化酶、脱氢酶和纤维素酶活性年均恢复速率最快,分别为4.63%/a、7.87%/a、5.80%/a和6.70%/a;在建植15a的恢复中,蔗糖酶和脲酶的恢复速率最快,为6.70%/a和5.03%/a;建植18a的恢复中,磷酸酶恢复速率最快,为10.90%/a,其余6种酶活性恢复速率在该阶段最慢,均显著低于10a和15a恢复阶段(图 2)。

|
| 图 2 人工植被不同恢复阶段土壤酶活性恢复速率 Fig. 2 Stage recovery rates of activities of soil enzyme 不同小写字母表示土壤酶活性恢复速率在不同植被恢复阶段间具有差异显著性(P < 0.05),数据为平均值±标准差 |
在植被恢复的生态实践中,有关植被配置类型对土壤酶影响的研究在不同区域和受损生态系统中均有报道,几乎所有的研究都显示植被建设会促进土壤酶活性的恢复,但不同植被配置对不同酶类影响的报道差异较大[10, 11, 17, 18, 19, 20, 21, 22, 23]。由于土壤酶类对土壤理化性质及其他环境因子的变化反应敏感,能够较早指示土壤肥力和生物活性的变化,可将其作为反映土壤营养元素有效水平的一项生物指标[18]。本研究中,9个样地间7个土壤理化指标(表 2)和7个土壤酶指标(图 1)差异明显,植被重建显著改善了土壤理化性质和土壤酶活性。总体而言,相比未进行植被建设的新排土场裸地,人工植被建设显著提高了7种土壤酶活性;但除磷酸酶外,人工植被重建后即使经过18a的恢复,其他6种土壤酶活性都显著低于天然植被区,说明完全受损排土场土壤酶活性的恢复是一个漫长的过程。一般认为植被重建主要通过以下几个方面影响土壤酶活性:首先,植被重建促进了土壤有机质的积累,改善土壤理化状况,为酶类提供丰富的碳源;其次,植被恢复促进了土壤中植物根系的聚集,而根系代谢可释放大量酶类,从而提高土壤酶活性;最后,植被重建可影响土壤的团粒结构和通透性,改善土壤水分的渗透和运移状况,进而促进酶类物质的运动和活性。研究区排土场常见的4种人工植被配置类型在建植18a后其土壤酶活性变化不尽相同。其中6种土壤酶活性都表现为:乔-草型最高,其次为乔木型,再次为草本型,乔-灌-草型最低;人工植被区显著高于裸地,但均显著低于撂荒地和天然植被区(图 1)。矿区排土场是煤炭开采中上层剥离物经一定的工艺和层次堆积填压而成,原有的土体结构和层次被完全破坏,肥力较差,抗风蚀水蚀能力较低,且在堆排过程中经大型机械碾压,通透性较差,土壤酶活性低下。人工植被建设后改善了土壤理化性质(表 2),同时影响一年生草本定居[24]和生物土壤结皮的拓殖发育[2],进而促进了土壤酶活性的提高。
3.2 土壤理化性质与土壤酶活性的关系人工植被重建和恢复过程也是植物对土壤不断适应和改造的过程,不同的植物群落对土壤理化性质的影响不同,包括土壤酶在内的土壤性质的改变是植物改变的重要驱动力之一[25]。土壤有机质是土壤中酶促底物的主要供给源,土壤中有机物质的转化,几乎与所有的土壤酶活性有关[9]。本研究中除磷酸酶外,其他6种酶活性均与土壤有机质含量显著正相关。土壤有效氮水平直接调控植物生理过程,同时影响土壤有机质的分解过程,与土壤酶类关系密切[26, 27]。研究中除多酚氧化酶和脱氢酶外,过氧化氢酶、蔗糖酶、脲酶、磷酸酶与硝态氮和铵态氮均显著正相关。土壤速效磷和速效钾仅与多酚氧化酶、脱氢酶和磷酸酶具有较好的相关性,这或许是植被重建后改善了土壤浅层的磷钾状况,如研究区所有人工植被区土壤速效磷、速效钾含量都接近和超过了天然植被区水平,说明磷钾已不再是限制因子,其相关性降低[21, 22]。此外,电导率与土壤过氧化氢酶、蔗糖酶和脲酶活性显著负相关;pH值与多酚氧化酶、脱氢酶、纤维素酶活性显著正相关,与磷酸酶活性显著负相关。本研究中监测的7种酶活性与主要土壤养分因子相关性显著,说明土壤酶在植被重建恢复过程中对于改善土壤质量具有相当重要的作用,它们直接影响着土壤养分的循环和能量转化。因此,在进行煤矿区植被恢复的综合评价时,可将土壤酶作为评价土壤恢复效果的一个指示指标。
3.3 植被重建恢复中的土壤酶恢复速率由于缺少植被恢复中对土壤酶活性动态变化的长期监测,多数研究一般以空间代替时间的方法来评价恢复过程中土壤酶的变化,大部分研究结果显示土壤酶活性均随植被恢复进程而提高,但其恢复速率在不同植被类型下和恢复阶段具有较大差异[18, 20, 21, 22, 23, 28]。如在黄土丘陵人工刺槐林的研究显示,土壤蔗糖酶、纤维素酶、脲酶、碱性磷酸酶、过氧化氢酶和淀粉酶都在建植10 a后迅速提高,20—25 a趋于平稳,此后略有下降,到50 a时达到最大值,可恢复到天然林的70%左右[22]。对秦岭地区华北落叶松人工林的研究显示,浅层土壤(0—20 cm)磷酸酶、脲酶在建植5—20 a恢复缓慢,30—40 a时最高;过氧化氢酶则在20 a时恢复最快,此后逐渐降低;蔗糖酶在建植5 a即达到最大值,10 a后迅速下降[28]。安太堡露天矿植被恢复区的研究显示,不同植被配置对土壤酶恢复影响显著,且土壤酶活性都随恢复进程而提高[20, 21]。本研究中,7种土壤酶活性恢复速率在不同植被配置类型和恢复阶段差异较大(表 4),总体来看,人工植被区水解酶(蔗糖酶、脲酶、磷酸酶、纤维素酶)恢复速率较快,平均可恢复到天然植被区的86.9%,而氧化还原酶(过氧化氢酶、多酚氧化酶、脱氢酶)恢复速率较慢,是天然植被区的42.7%。这是因为人工植被建立后迅速改善了土壤理化性质,尤其是草本的入侵生长和生物土壤结皮的拓殖发育为土壤提供了易分解的活性碳[2, 24];同时,土壤孔隙结构和水分通气条件得到改善,进而促进了土壤水解酶的恢复[10, 29]。但也有相反的变化趋势被证实,如在沙坡头地区人工固沙植被区50 a恢复期土壤酶恢复的研究中则发现氧化还原酶恢复速率快于水解酶,研究认为偏碱性、低有机质和低含水量的沙漠土及人工植被恢复过程中植被类型的变化和生物土壤结皮的发育是主导因素[11]。此外,研究区相同类型人工植被不同恢复阶段土壤酶年均恢复速率差异较大(图 2),建植10、15、18 a乔-灌-草人工植被下土壤氧化还原酶和水解酶年均恢复速率分别为3.7%/a和5.6%/a;都表现为建植10 a后年均恢复速率最快,其次为15 a,建植18 a最慢。土壤酶恢复速率的变化与大部分研究一致,都显示为植被恢复初期的土壤酶恢复速率较快,尔后变缓,此后逐渐提高[20, 21, 22, 28]。这与植被恢复的一般规律相符,在植被恢复前期,植物生长较快,枯枝落叶和营养物质急剧增加,土壤酶活性迅速得到改善;此后随着植被恢复,乔灌生长旺盛、群落郁闭度增大,光照强度降低,土壤水分消耗剧烈,水肥竞争加剧,下层草本生长受到强烈抑制,根系微生物活性减弱,土壤酶活性变缓或下降;到恢复后期,在自然稀疏等因素的作用下,群落郁闭度降低,光照养分得到改善,草本多样性提高,生物土壤结皮盖度增大,土壤代谢途径更加多样,土壤酶活性增强[20,22-24,28,30-31]。
4 结论植被重建显著提高了露天煤矿排土场的土壤酶活性,但对于大部分土壤酶,18a的时间不足以使土壤酶活性恢复到天然植被区的水平,土壤酶活性的恢复需要一个漫长的过程。土壤酶活性与土壤主要理化指标具有较强的相关性,可将土壤酶活性作为评价植被恢复效果的一个指示指标。人工植被恢复进程中土壤水解酶恢复速率快于氧化还原酶,恢复初期快于恢复后期。
| [1] | 李文华. 中国当代生态学研究: 生态系统恢复卷. 北京: 科学出版社, 2013. |
| [2] | 赵洋, 张鹏, 胡宜刚, 黄磊, 虎瑞, 刘美玲. 黑岱沟露天煤矿排土场不同植被配置对生物土壤结皮拓殖和发育的影响. 生态学杂志, 2014, 33(2): 269-275. |
| [3] | 吴钢, 魏东, 周政达, 唐明方, 付晓. 我国大型煤炭基地建设的生态恢复技术研究综述. 生态学报, 2014, 34(11): 2812-2820. |
| [4] | Callaham M A Jr, Rhoades C C, Heneghan L. A striking profile: soil ecological knowledge in restoration management and science. Restoration Ecology, 2008, 16(4): 604-607. |
| [5] | Roberts L, Stone R, Sugden A. The rise of restoration ecology. Science, 2009, 325(5940): 555-555. |
| [6] | 李新荣. 荒漠生物土壤结皮生态与水文学研究. 北京: 高等教育出版社, 2012. |
| [7] | Li X R, Zhang Z S, Huang L, Wang X P. Review of the ecohydrological processes and feedback mechanisms controlling sand-binding vegetation systems in sandy desert regions of China. Chinese Science Bulletin, 2013, 58(13): 1483-1496. |
| [8] | Li X R, Zhang Z S, Tan H J, Gao Y H, Liu L C, Wang X P. Ecological restoration and recovery in the wind-blown sand hazard areas of Northern China: relationship between soil water and carrying capacity for vegetation in the Tengger Desert. Science China Life Sciences, 2014, 57(5): 539-548. |
| [9] | 关松荫. 土壤酶及其研究法. 北京: 农业出版社, 1986. |
| [10] | Sinsabaugh R L, Lauber C L, Weintraub M N, Ahmed B, Allison S D, Crenshaw C, Contosta A R, Cusack D, Frey S, Gallo M E, Gartner T B, Hobbie S E, Holland K, Keeler B L, Powers J S, Stursova M, Takacs-Vesbach C, Waldrop M P, Wallenstein M D, Zak D R, Zeglin L H. Stoichiometry of soil enzyme activity at global scale. Ecology Letters, 2008, 11(11): 1252-1264. |
| [11] | Zhang Z S, Dong X J, Liu Y B, Li X R, Jia R L, Hu Y G, He M Z, Huang L. Soil oxidases recovered faster than hydrolases in a 50-year chronosequence of desert revegetation. Plant and Soil, 2012, 358(1/2): 275-287. |
| [12] | 米文宝, 谢应忠. 生态恢复与重建研究综述. 水土保持研究, 2006, 13(2): 49-53. |
| [13] | 张成梁, Li B L. 美国煤矿废弃地的生态修复. 生态学报, 2011, 31(1): 276-285. |
| [14] | 李青丰, 曹江营, 张树礼, 薛玲, 李利平, 秦梅枝. 准格尔煤田露天矿植被恢复的研究-排土场植被自然恢复的观察研究. 中国草地, 1997, (2): 23-25, 66-66. |
| [15] | 劳家柽. 土壤农化分析手册. 北京: 农业出版社, 1988. |
| [16] | 林先贵. 土壤微生物研究原理与方法. 北京: 高等教育出版社, 2010. |
| [17] | 杨勤学, 赵冰清, 郭东罡. 中国北方露天煤矿区植被恢复研究进展. 生态学杂志, 2015, 34(4): 1152-1157. |
| [18] | An S S, Zheng F L, Zhang F, Van Pelt S, Hamer U, Makeschin F. Soil quality degradation processes along a deforestation chronosequence in the Ziwuling area, China. Catena, 2008, 75(3): 248-256. |
| [19] | 陈丹梅, 陈晓明, 梁永江, 霍新建, 张长华, 段玉琪, 杨宇虹, 袁玲. 种植模式对土壤酶活性和真菌群落的影响. 草业学报, 2015, 24(2): 77-84. |
| [20] | 李晋川, 王翔, 岳建英, 王宇宏, 郭春燕, 卢宁, 杨生权. 安太堡露天煤矿植被恢复过程中土壤生态肥力评价. 水土保持研究, 2015, 22(1): 66-71, 79-79. |
| [21] | 王翔, 李晋川, 岳建英, 周小梅, 郭春燕, 卢宁, 王宇宏, 杨生权. 安太堡露天矿复垦地不同人工植被恢复下的土壤酶活性和肥力比较. 环境科学, 2013, 34(9): 3601-3606. |
| [22] | 张超, 刘国彬, 薛萐, 宋籽霖, 樊良新. 黄土丘陵区不同林龄人工刺槐林土壤酶演变特征. 林业科学, 2010, 46(12): 23-29. |
| [23] | 杨宁, 邹冬生, 杨满元, 林仲桂, 宋光桃, 陈志阳, 赵林峰. 衡阳紫色土丘陵坡地植被恢复阶段土壤特性的演变. 生态学报, 2014, 34(10): 2693-2701. |
| [24] | 赵洋, 张鹏, 胡宜刚, 黄磊, 苏洁琼. 露天煤矿排土场不同配置人工植被对草本植物物种多样性的影响. 生态学杂志, 2015, 34(2): 387-392. |
| [25] | 曲国辉, 郭继勋. 松嫩平原不同演替阶段植物群落和土壤特性的关系. 草业学报, 2003, 12(1): 18-22. |
| [26] | Aber J, McDowell W, Nadelhoffer K, Magill A, Berntson G, Kamakea M, McNulty S, Currie W, Rustad L, Fernandez I. Nitrogen saturation in temperate forest ecosystems: hypotheses revisited. BioScience, 1998, 48(11): 921-934. |
| [27] | 吕超群, 田汉勤, 黄耀. 陆地生态系统氮沉降增加的生态效应. 植物生态学报, 2007, 31(2): 205-218. |
| [28] | 赵海燕, 徐福利, 王渭玲, 王伟东, 陈钦程, 赵亚芳, 马亚娟. 秦岭地区华北落叶松人工林地土壤养分和酶活性变化. 生态学报, 2015, 35(4): 1086-1094. |
| [29] | Yao H Y, Bowman D, Rufty T, Shi W. Interactions between N fertilization, grass clipping addition and pH in turf ecosystems: implications for soil enzyme activities and organic matter decomposition. Soil Biology and Biochemistry, 2009, 41(7): 1425-1432. |
| [30] | Kotroczó Z, Veres Z, Fekete I, Krakomperger Z, Tóth J A, Lajtha K, Tóthmérész B. Soil enzyme activity in response to long-term organic matter manipulation. Soil Biology and Biochemistry, 2014, 70: 237-243. |
| [31] | Stone M M, DeForest J L, Plante A F. Changes in extracellular enzyme activity and microbial community structure with soil depth at the Luquillo Critical Zone Observatory. Soil Biology and Biochemistry, 2014, 75: 237-247. |
 2016, Vol. 36
2016, Vol. 36






