文章信息
- 聂兰琴, 吴琴, 尧波, 付姗, 胡启武
- NIE Lanqin, WU Qin, YAO Bo, FU Shan, HU Qiwu
- 鄱阳湖湿地优势植物叶片-凋落物-土壤碳氮磷化学计量特征
- Leaf litter and soil carbon, nitrogen, and phosphorus stoichiometry of dominant plant species in the Poyang Lake wetland
- 生态学报, 2016, 36(7): 1898-1906
- Acta Ecologica Sinica, 2016, 36(7): 1898-1906
- http://dx.doi.org/10.5846/stxb201409301944
-
文章历史
- 收稿日期: 2014-09-30
- 网络出版日期: 2015-08-05
2. 江西师范大学科学技术学院, 南昌 330027
2. Science and Technology College, Jiangxi Normal University, Nanchang 330027, China
碳(C)、氮(N)、磷(P)化学计量关系反映元素的平衡与耦合,影响植物生长发育[1]、C、N养分循环[2]、食物营养关系[3]、物种组成与多样性[4],是生态系统结构、功能与稳定性维持的重要机制[5, 6]。当前,C:N:P化学计量格局及其驱动因素仍然是生态化学计量学的一个重要研究领域[7],不同学者先后在全球尺度上探讨了植物叶片[8]、凋落物[9]、土壤[10]、细根[11]及微生物[12]等C、N、P化学计量格局。近年来国内生态化学计量学亦发展迅速,相关研究跨越不同时空尺度,涉及不同生态系统类型[7]。以湿地为例,研究报道既包括不同湿地类型、不同湿地物种,还包括植物不同器官、湿地土壤等[13, 14, 15, 16, 17, 18, 19]。然而,这些研究往往聚焦于生态系统某一组分,缺乏生态系统的综合考虑。以植物叶片为核心的化学计量信息亟需拓展至植物其他部位乃至生态系统不同组分[2]。湿地处于水陆交界部位,土壤养分、水分等相对于陆地具有更大的波动性,对环境变化更加敏感[20]。受全球变化与人类活动的影响,一些湿地与水域的C、N、P化学计量关系正在发生变化,最终可能会改变生态系统的结构和功能[21, 22]。例如,Elser等[23]对挪威和瑞典2053个湖泊的研究表明大气氮沉降增加了湖泊的N:P值,从而导致湖泊浮游植物养分限制格局的变化,在氮沉降低的湖泊,浮游植物的生长总体受氮限制,而一些氮沉降高的湖泊则一致表现为磷受限。因此,加强从湿地植物地上植株到凋落物直至土壤的化学计量垂直分异的探讨,不仅有助于揭示生态系统不同组分化学计量的趋同与分异,同时对于理解或预测生态系统对全球变化的响应具有重要意义[2, 7]。
鄱阳湖 “丰水一片,枯水一线”存在剧烈的年内、年际水位波动,由此引起的频繁的湿地干湿交替势必造成土壤养分的极大波动。此外,鄱阳湖湿地沿水位梯度依次发育挺水、湿生与沉水植物群落,且群落中往往以某一物种占绝对优势,伴生物物种极少,结构简单,如挺水植物群落中的南荻(Triarrhena lutarioriparia)、菰(Zizania latifolia (Griseb.) Stapf),湿生植物群落中的灰化苔草(Carex cinerascens)等[24, 25]。因此,这些关键物种的养分化学计量特征很可能关系到鄱阳湖湿地生态系统结构、功能与稳定性的维持。本研究通过测定6种典型植物群落中优势植物叶片-凋落物-表层土壤C、N、P含量,分析C、N、P化学计量关系的垂直分异,探讨不同物种、不同生活型间化学计量差异,为进一步揭示鄱阳湖湿地植物群落对水位波动的响应与适应机制提供依据。
1 材料与方法 1.1 研究区概况研究区设置在鄱阳湖南矶湿地国家级自然保护区内,地理坐标为28°52′05″—29°06′50″ N,116°10′33″—116°25′05″ E。属亚热带暖湿季风气候,多年平均气温17.3℃,平均降水量为1358—1823mm,4—9月是洪水季,10月份进入枯水期。南矶湿地位于赣江北支、中支和南支汇入鄱阳湖开放水域冲积形成的赣江三角洲前缘,是赣江三大支流的河口与鄱阳湖水体之间的水陆过渡带,在南昌市新建县界内,区内除南山岛和矶山岛(乡行政机构所在地,面积仅4 km2) 外,其余为洲滩和水域,总面积约330 km2。湿地植被中挺水植物以芦苇( Phragmites australis)、南荻和菰等3种最为典型;湿生植物则以苔草最为典型,其中灰化苔草广泛分布于鄱阳湖洲滩,在湿生植物中占绝对优势[26]。
1.2 样品采集与分析2013年11月初在保护区挺水植物群落芦苇、南荻、菰及湿生植物群落灰化苔草、红穗苔草(Carex argyi)和水蓼(Polygonum hydropiper)等6个典型植物群落分布区设置取样地,为避免采样的假重复,每种群落类型设置5—6个样地,随机在其中的4个样地中,以多点混合的方式同时采集植物绿色叶片、凋落物以及表层土壤(0—15cm)样品。上述样品各4个重复,共计采集72个样品。将采集的样品分装于标记好的自封袋内带回实验室,叶片、凋落物75℃/48h烘干至恒重,研磨过60目筛,进行全C、全N、全P测定。植物全C、全N采用意大利欧维特元素分析仪测定(EA3000)测定,全P采用钼锑抗比色法测定。土壤经风干磨细后有机碳采用高锰酸钾氧化外加热法测定,全N、全P测定方法同上。
1.3 数据处理与分析采用Microsoft Excel 2003软件进行数据处理及制图。利用单因素方差分析方法(One-way ANOVA)分别对叶片、凋落物、表层土壤C、N、P含量及其化学计量比进行物种间差异的分析;利用单因素方差分析方法分析叶片-凋落物-表层土壤3个组分之间C、N、P含量及C:N、C:P、N:P化学计量比的差异。上述统计均用LSD法进行多重比较。此外,采用Pearson相关系数及一元线性回归方法分析了叶片-凋落物-土壤之间C、N、P含量及化学计量比的关系。文中显著性水平设置为α=0.05。
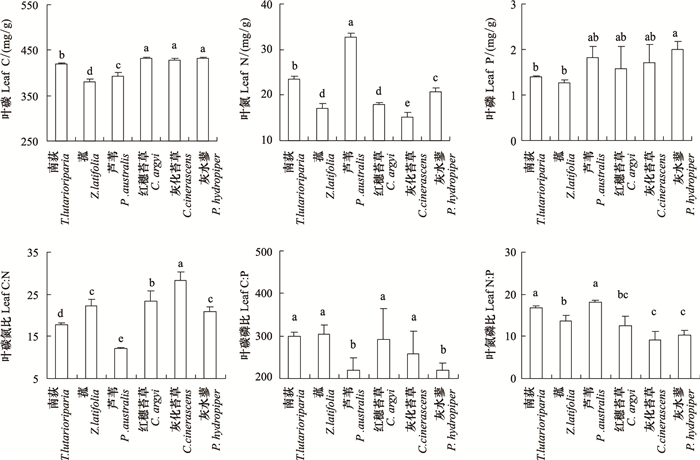
2 结果与分析 2.1 叶片C、N、P含量及化学计量比叶片C含量变化范围为380.6—432.2 mg/g,平均值为414.3 mg/g,不同物种间的C含量差异显著(F=111.09,P<0.001)(图 1)。叶片N含量在15.3—32.6 mg/g之间波动,物种间差异显著(F=201.97,P<0.001),最高值与最低值分别为芦苇与灰化苔草(图 1)。叶片P含量变化范围为1.3—2.0 mg/g,平均值为1.6 mg/g,方差分析显示叶片P含量在植物间差异显著(F=3.545,P<0.05)(图 1)。
|
| 图 1 鄱阳湖湿地6种优势植物叶片C、N、P含量及化学计量比 Fig.1 Leaf carbon, nitrogen and phosphorus concentrations and stoichiometry of six dominant plant species in Poyang Lake wetlands |
叶片C:N、C:P和N:P值变化范围分别为12.1—28.2、218.2—303.3和9.1—18.1,对应平均值分别为20.8、265.2、13.4。C:N、C:P和N:P值在物种间差异显著(P<0.05)(图 1)。
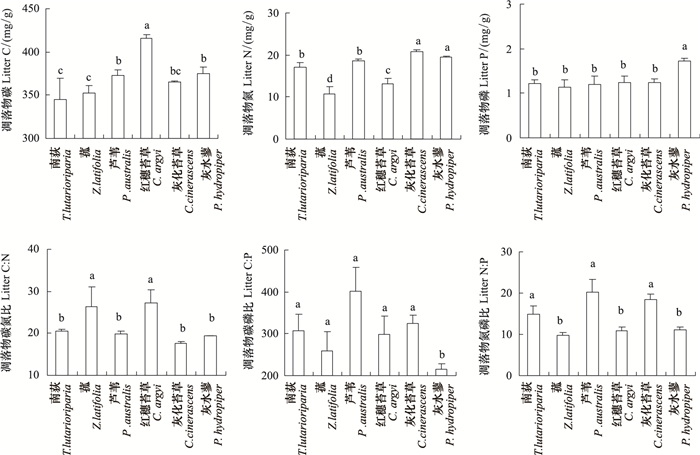
2.2 凋落物C、N、P含量及化学计量比凋落物C含量变化范围为345.4—416.1 mg/g,平均值为371.1 mg/g,最低值为南荻,最高值为红穗苔草。凋落物N含量在10.8—20.8 mg/g之间波动,平均值为16.6 mg/g。凋落物P含量变化范围为1.1—1.7 mg/g,平均值为1.3 mg/g,其中,水蓼凋落物P含量最高。方差分析显示不同物种间凋落物C、N、P含量差异性均达到显著性水平(P<0.01)(图 2)。
|
| 图 2 鄱阳湖湿地6种优势植物凋落物C、N、P含量及化学计量比 Fig.2 Litter carbon, nitrogen and phosphorus concentrations and stoichiometry of six dominant plant species in Poyang Lake wetlands |
凋落物C:N、C:P和N:P值变化范围分别为17.7—27.1、214.9—402.3、9.8—20.3,对应的平均值分别为21.8、300.8、14.2,方差分析显示不同物种间凋落物C、N、P的化学计量比差异极显著(P<0.01)(图 2)。
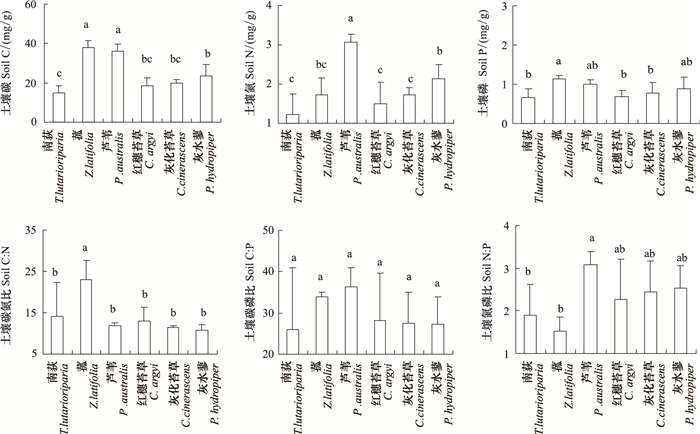
2.3 表层土壤C、N、P含量及化学计量关系土壤C、N、P含量整体上表现为挺水植物表层土壤高于湿生植物。方差分析显示不同物种下的表层土壤C、N、P含量均差异显著(P<0.05)(图 3)。其中,土壤有机C含量变化范围为15.0—38.1 mg/g,平均值为25.1 mg/g,最大值为菰对应下的土壤,最小值为南荻土壤。土壤N含量在1.2—3.1 mg/g之间波动,平均值为1.9mg/g,最高值为芦苇土壤,最低值为南荻土壤。土壤P含量变化范围为0.7—1.1mg/g,平均值为 0.9 mg/g,最高值为菰对应下的土壤,最低值为南荻土壤。
|
| 图 3 鄱阳湖湿地6种群落类型下表层0—15 cm土壤C、N、P含量及化学计量比 Fig.3 Soil carbon, nitrogen and phosphorus contents and stoichiometry at 0—15 cm depth under six plant communities in Poyang Lake wetlands |
土壤C:N、C:P和N:P值的变化范围分别为10.8—23.0、25.9—36.2和1.5—3.1,平均值分别为14.0、29.9和2.3。方差分析显示土壤C:N和N:P在不同群落间差异显著(P<0.05),而C:P没有显著差异(图 3)。
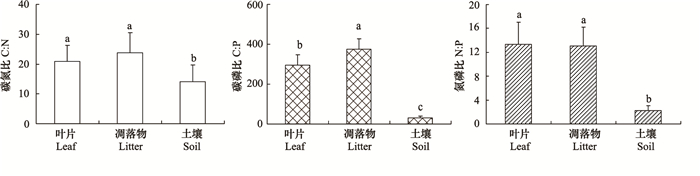
2.4 叶片、凋落物、土壤之间C、N、P含量及化学计量比关系方差分析显示叶片、凋落物与土壤间C、N、P含量差异显著(P<0.001),且叶片养分元素含量显著高于凋落物与土壤。叶片与凋落物间除C:P外差异不显著,土壤与植物叶片及凋落物间C:N、C:P和N:P均差异显著(图 4)。表 1显示了叶片、凋落物、土壤间C、N、P含量及化学计量比的相关关系。其中,叶片N含量与土壤N呈极显著正相关,凋落物与叶片之间除C:P比外,其它化学计量比之间相关性未达到显著性水准;土壤C:N、C:P及N:P与植物叶片之间的相应化学计量比相关性均不显著,而C:N、N:P与凋落物相应化学计量比呈显著正相关(表 1)。进一步的线性回归分析表明凋落物的C:N、N:P分别能解释土壤C:N、N:P变异的35%、18%。
|
| 图 4 叶片-凋落物-土壤间C:N、C:P及N:P差异 Fig.4 The discrepancy of C:N, C:P and N:P ratios between leaves, litters and soil |
| 叶片Leaf | 凋落Litter | 叶片Leaf | 凋落Litter | |||||||||||
| C | N | P | C | N | P | |||||||||
| 凋落 | C | 0.41 * | -0.09 | 0.24 | C:N | 0.21 | 0.48 * | 0.02 | ||||||
| Litter | N | 0.47 * | 0.27 | 0.56 ** | C:P | 0.06 | 0.51 * | 0.35 | ||||||
| P | 0.43 * | -0.01 | 0.58 ** | N:P | -0.12 | -0.13 | 0.20 | |||||||
| 土壤 | C | -0.83 ** | 0.30 | -0.11 | -0.14 | -0.29 | -0.17 | C:N | 0.08 | 0.27 | 0.05 | 0.59 ** | 0.23 | -0.41 * |
| Soil | N | -0.35 | 0.61 ** | -0.24 | 0.05 | 0.31 | 0.08 | C:P | -0.19 | 0.09 | 0.28 | 0.18 | 0.32 | 0.06 |
| P | -0.58 ** | 0.14 | 0.03 | -0.32 | -0.21 | 0.03 | N:P | -0.22 | -0.17 | 0.19 | -0.35 | 0.11 | 0.43 * | |
| * P<0.05, **表示P<0.01, n=24 | ||||||||||||||
研究表明北美地区湿地植物的N、P含量变化范围分别为0.8—42 mg/g、0.04—6.4 mg· g-1[27],欧洲湿地植物的N、P含量变化范围为6—20 mg/g和0.2—3.3 mg· g-1[28, 29]。与上述地区湿地相比较,本研究中6种植物叶片N(15.3—32.6 mg/g)、P (1.3—2.0 mg/g) 含量均在其范围内。与国内其它地区湿地相比较,叶片N平均含量(21.2 mg/g)明显高于杭州湾[13]、苏北潮滩[30]、九段沙上沙[31]、崇明东滩[32]、闽江口[15]、梁子湖[33]、洱海[14]等滨海、河口及内陆湖泊湿地海三棱藨草(Scirpus mariqueter)、互花米草(Spartina alterniflora)、糙叶苔草(Carex scabrifolia)、盐地碱蓬(Suaeda salsa)、盐蒿(Artemisia halodendron)、菰等优势植物。叶片P平均含量(1.6 mg/g)则介于上述湿地植物之间。由于芦苇耐盐碱、水湿,广泛分布于各种生境中,成为不同湿地类型的共有种。本研究中芦苇叶片N含量(32.6 mg/g)低于辽河口湿地[34](36.5 mg/g),与闽江口[15](30.4 mg/g)、乌梁素海[17](31.4 mg/g)相当,明显高于苏北潮滩[30](1.8 mg/g)、洱海[14](6.7 mg/g)、崇明东滩[32](11.5 mg/g) 、杭州湾[13](11.6 mg/g)和九段沙[31](19.7 mg/g)等湿地类型。叶片P(1.8 mg/g)则与闽江口、洱海、九段沙相当,明显高于上述湿地中的其它类型。因此,即使是同一物种,由于其所处湿地生境的差异,也会表现出极大的N、P养分含量差异。
本研究中叶片N含量与土壤全N含量显著正相关,表明土壤N含量的变化是引起地表植物叶片N含量差异的重要原因,这与以往在大尺度上的研究结果一致[8]。此外,6种植物中灰化苔草叶片N含量显著低于其它物种,还可能与灰化苔草快速生长过程中的N稀释作用有关[2],因为灰化苔草在10月底至11月初仍然处于秋季生长季(洪水过后的生长季)的旺盛时期,而其他5种植物已进入生长季的末期。本研究中芦苇、南荻、菰属于大型挺水植物,单位面积的生物量高于苔草、水蓼等湿生植物[26],因此,挺水植物N:P值显著高于湿生植物可能与不同生活型植物体型大小有关,因为小型植物往往拥有更低的N:P值[2]。此外,芦苇、南荻与灰化苔草及水蓼N:P值差异显著,这可能是鄱阳湖湿地除了大面积的单一物种占绝对优势的群落结构之外,在某些地段能形成以芦苇或南荻为群落的顶层优势植物,而灰化苔草或水蓼处于群落底层的一种群落结构的重要原因之一,因为N、P养分化学计量的差异可能引起不同层次上资源“供应-需求”之间的错配,从而使得不同物种能各自占有有利的生态位,有利于物种共存[1, 7]。对于相同生活型的植物,尽管叶片N含量差异显著,但N:P值保持了相对一致性。例如,3种湿生植物中灰化苔草、红穗苔草与水蓼N:P没有显著差异,挺水植物中南荻与芦苇之间也没有显著差异,在一定程度上反映了相同生活型的物种对养分利用及外界环境适应与进化方面的趋同性。
3.2 叶片-凋落物-表层土壤养分化学计量的垂直分异统计分析发现C、N、P元素及C:N、C:P与N:P在叶片-凋落物-表层土壤3个组分之间均存在显著的差异。凋落物C、N、P平均含量分别相当于叶片的90%、78%和81%,这与其他地区的湿地研究结果一致[15, 27]。研究表明植物地上活体,特别是植物叶片在衰老与凋落前普遍将其养分转移到其他部位,亦即发生养分重吸收的过程,是植物保持养分与提高利用效率的重要机制[35]。因此,新鲜叶片的N、P含量要比衰老叶片或凋落物的N、P含量高。同样,本研究中凋落物的C:N、C:P值均高于叶片亦是源于上述原因,这与Mcgroddy等[9]对全球森林叶片、凋落物C与N、P养分化学计量比的研究结果一致。鄱阳湖湿地地处中亚热带地区,与温带北美湿地相比较,本研究中凋落物的N含量明显偏高,P含量则相当[27]。进一步的比较发现本研究中凋落物C:N(23.7)、C:P(296.3)值远低于Aert[36]综述研究中的温带地区、密西西比地区及热带地区陆生植物凋落物的C:N、C:P值,表明湿地生态系统的凋落物化学计量关系与陆地生态系统可能有极大差异。
由于凋落物在进入土壤转为土壤有机质的过程中还经历了复杂的微生物分解过程,在这个过程中大量有机态的C、N、P被矿化分解,最终促成土壤的C、N、P含量及C:N、C:P、N:P值显著低于植物叶片及凋落物。本研究还发现土壤C:N、N:P与凋落物的关系更为密切,凋落物的C:N、N:P分别能解释土壤C:N、N:P变异的35%、18%。土壤C:N与凋落物C:N之间的相关性较土壤C:P与凋落物C:P之间的相关性更显著,主要是由于土壤中的P不仅来自于凋落物的输入,还与土壤成土母质中的矿物成分密切相关。Sardans 等[37]指出植物体C:N:P值要比水体或土壤更加保守与稳定,这在本研究中也得到了证实,6种植物叶片C:N、C:P与N:P的变异系数分别为25%,19%,27%,凋落物为28%,18%,24%,而土壤对应的化学计量比的变异系数则分别为40%,29%,33%。
3.3 C、N、P化学计量的指示意义叶片C:N、C:P代表植物吸收营养元素时所能同化碳的能力,反映了植物营养元素的利用效率,同时也代表着不同群落固碳效率的高低[7]。研究区不同植物叶片C:N值挺水植物(17.4)低于湿生植物(24.5),说明湿生植物N利用效率可能高于挺水植物。以灰化苔草、水蓼等为优势种的湿生植物带一年中经历频繁的干湿交替,土壤中的N、P等养分,特别是N处于极大的波动中。同时,由于地表径流与地下径流等影响极易造成土壤养分的流失。而以芦苇、南荻为代表的挺水植物区因为所处的湖底高程相对较高,一年中淹水时间及干湿交替的频率要低于湿生植物区,土壤中的养分相对比较稳定。因此,湿生植物表现出较高的C:N值很可能是对养分波动的一种适应。Koerselman和 Meuleman[28]对欧洲湿地植物的研究表明,在群落水平上,N:P>16意味着植物P受限,N:P <14说明N受限,N:P值介于二者之间可能受N、P的共同限制。由于鄱阳湖湿地植物群落结构的高度单一性,本研究中6种植物均是相应植物群落中的绝对优势种,以灰化苔草群丛为例,灰化苔草单一物种的生物量超过总群落生物量的98%。因此,这些绝对优势的物种特性基本上代表了群落的总体特征。以此来判断,灰化苔草(9.1)、水蓼(10.4)和红穗苔草(12.03)等3类湿生植物群落更多地表现为N受限。菰(14.0)群落则可能N与P共同受限,而芦苇(18.1)、南荻(16.9)则可能更受P的限制。菰虽为挺水植物但因为其生境常年淹水,N的波动相对较大,因而相对于芦苇、南荻更加受N的限制。总体上挺水植物群落可能更加受P的限制,而湿生植物群落更加受N的限制,这与C:N、C:P的指示意义相对一致,即在某种养分相对限制的生境中,植物对该养分保持相对较高的利用效率[8]。尽管N:P被广泛应用于养分限制的判断,但不同生态系统类型N、P限制的N:P比阈值可能存在较大差异,因而利用化学计量关系来判断养分的限制还需要进一步的野外施肥实验加以印证。
研究表明凋落物C:N比小于40,开始出现凋落物矿化分解净N释放[38],且凋落物分解速率与C:N、C:P值呈显著负相关,C:N、C:P值越低,其分解速率越快[39]。因此,根据凋落物的C:N化学计量比来判断,本研究中6种植物群落的凋落物理论上都具有快速分解周转的特征,这也在一定程度上解释了鄱阳湖湿地土壤碳储量远低于东北三江及青藏高原高寒湿地[40]。
4 结论鄱阳湖湿地不同优势植物种间叶片、凋落物及土壤C、N、P含量差异显著,且叶片C、N、P含量显著高于凋落物与土壤。叶片-凋落物-土壤间C、N、P化学计量关系差异显著,表现为土壤C:N、C:P及N:P值显著低于叶片与凋落物,且土壤C、N、P化学计量关系与凋落物更为密切,凋落物的C:N、N:P分别能解释土壤C:N、N:P变异的35%、18%。挺水植物与湿生植物之间叶片C:N、N:P值差异显著,C:P则差异不显著;凋落物C:N、C:P与N:P在挺水植物与湿生植物间均未达到显著性差异。
| [1] | Güsewell S. N: P ratios in terrestrial plants: variation and functional significance. New Phytologist, 2004, 164(2): 243-266. |
| [2] | Elser J J, Fagan W F, Kerkhoff A J, Swenson N G, Enquist B J. Biological stoichiometry of plant production: metabolism, scaling and ecological response to global change. New Phytologist, 2010, 186(3): 593-608. |
| [3] | Elser J J, Fagan W F, Denno R F, Dobberfuhl D R, Folarin A, Huberty A, Interlandi S, Kilham S S, McCauley E, Schulz K L, Siemann E H, Sterner R W. Nutritional constraints in terrestrial and freshwater food webs. Nature, 2000, 408(6812): 578-580. |
| [4] | Abbas M, Ebeling A, Oelmann Y, Ptacnik R, Roscher C, Weigelt A, Weisser W W, Wilcke W, Hillebrand H. Biodiversity effects on plant stoichiometry. PLOS ONE, 2013, 8(3): e58179, doi: 10.1371/journal.pone.0058179. |
| [5] | Sterner R W, Elser J J. Ecological Stoichiometry: The Biology of Elements from Molecules to the Biosphere. Princeton, NJ: Princeton University Press, 2002. |
| [6] | Yu Q, Chen Q S, Elser J J, He N P, Wu H H, Zhang G M, Wu J G, Bai Y F, Han X G. Linking stoichiometric homoeostasis with ecosystem structure, functioning and stability. Ecology Letters, 2010, 13(11): 1390-1399. |
| [7] | 贺金生, 韩兴国. 生态化学计量学: 探索从个体到生态系统的统一化理论. 植物生态学报, 2010, 34(1): 2-6. |
| [8] | Reich P B, Oleksyn J. Global patterns of plant leaf N and P in relation to temperature and latitude. Proceedings of the National Academy of Sciences of the United States of America, 2004, 101(30): 11001-11006. |
| [9] | McGroddy M E, Daufresne T, Hedin L O. Scaling of C: N: P stoichiometry in forests worldwide: implications of terrestrial Redfield-type ratios. Ecology, 2004, 85(9): 2390-2401. |
| [10] | Cleveland C C, Liptzin D. C: N: P stoichiometry in soil: is there a "Redfield ratio" for the microbial biomass?. Biogeochemistry, 2007, 85(3): 235-252. |
| [11] | Yuan Z Y, Chen H Y, Reich P B. Global-scale latitudinal patterns of plant fine-root nitrogen and phosphorus. Nature Communications, 2011, 2: 344-344. |
| [12] | Li P, Yang Y H, Han W X, Fang J Y. Global patterns of soil microbial nitrogen and phosphorus stoichiometry in forest ecosystems. Global Ecology and Biogeography, 2014, 23(9): 979-987. |
| [13] | 吴统贵, 吴明, 刘丽, 萧江华. 杭州湾滨海湿地3种草本植物叶片N、P化学计量学的季节变化. 植物生态学报, 2010, 34(1): 23-28. |
| [14] | 鲁静, 周虹霞, 田广宇, 刘贵华. 洱海流域44种湿地植物的氮磷含量特征. 生态学报, 2011, 31(3): 709-715. |
| [15] | 王维奇, 徐玲琳, 曾从盛, 仝川, 张林海. 河口湿地植物活体-枯落物-土壤的碳氮磷生态化学计量特征. 生态学报, 2011, 31(31): 7119-7124. |
| [16] | 李征, 韩琳, 刘玉虹, 安树青, 冷欣. 滨海盐地碱蓬不同生长阶段叶片C、N、P化学计量特征. 植物生态学报, 2012, 36(10): 1054-1061. |
| [17] | Li L P, Zerbe S, Han W X, Thevs N, Li W P, He P, Schmitt A O, Liu Y N, Ji C J. Nitrogen and phosphorus stoichiometry of common reed (Phragmites australis) and its relationship to nutrient availability in northern China. Aquatic Botany, 2014, 112: 84-90. |
| [18] | Zhang Z S, Lu X G, Song X L, Guo Y, Xue Z S. Soil C, N and P stoichiometry of Deyeuxia angustifolia and Carex lasiocarpa wetlands in Sanjiang Plain, Northeast China. Journal of Soils and Sediments, 2012, 12(9): 1309-1315. |
| [19] | Zhang Z S, Song X L, Lu X G, Xue Z S. Ecological stoichiometry of carbon, nitrogen, and phosphorus in estuarine wetland soils: influences of vegetation coverage, plant communities, geomorphology, and seawalls. Journal of Soils and Sediments, 2013, 13(6): 1043-1051. |
| [20] | Davidson E A, Janssens I A. Temperature sensitivity of soil carbon decomposition and feedbacks to climate change. Nature, 2006, 440(7081): 165-173. |
| [21] | Sardans J, Rivas-Ubach A, Peñuelas J. The C: N: P stoichiometry of organisms and ecosystems in a changing world: A review and perspectives. Perspectives in Plant Ecology, Evolution and Systematics, 2012, 14(1): 33-47. |
| [22] | Van de Waal D B, Verschoor A M, Verspagen J M H, van Donk E, Huisman J. Climate-driven changes in the ecological stoichiometry of aquatic ecosystems. Frontiers in Ecology and the Environment, 2010, 8(3): 145-152. |
| [23] | Elser J J, Andersen T, Baron J S, Bergström A K, Jansson M, Kyle M, Nydick K R, Steger L, Hessen D O. Shifts in lake N: P stoichiometry and nutrient limitation driven by atmospheric nitrogen deposition. Science, 2009, 326(5954): 835-837. |
| [24] | 胡振鹏, 葛刚, 刘成林, 陈伏生, 李述. 鄱阳湖湿地植物生态系统结构及湖水位对其影响研究. 长江流域资源与环境, 2010, 19(6): 597-605. |
| [25] | 葛刚, 赵安娜, 钟义勇, 吴志强. 鄱阳湖洲滩优势植物种群的分布格局. 湿地科学, 2011, 9(1): 19-25. |
| [26] | 刘信中, 樊三宝, 胡斌华. 江西南矶山湿地自然保护区综合科学考察. 北京: 中国林业出版社, 2006: 1-6. |
| [27] | Bedford B L, Walbridge M R, Aldous A. Patterns in nutrient availability and plant diversity of temperate North American wetlands. Ecology, 1999, 80(7): 2151-2169. |
| [28] | Koerselman W, Meuleman A F M. The vegetation N: P ratio: a new tool to detect the nature of nutrient limitation. Journal of Applied Ecology, 1996, 33(6): 1441-1450. |
| [29] | Güsewell S, Koerselman W. Variation in nitrogen and phosphorus concentrations of wetland plants. Perspectives in Plant Ecology, Evolution and Systematics, 2002, 5(1): 37-61. |
| [30] | 高建华, 白凤龙, 杨桂山, 欧维新. 苏北潮滩湿地不同生态带碳、氮、磷分布特征. 第四纪研究, 2007, 27(5): 756-765. |
| [31] | 刘长娥, 杨永兴, 杨杨. 九段沙上沙湿地植物N、P、K的分布特征与季节动态. 生态学杂志, 2008, 27(11): 1876-1882. |
| [32] | 赵美霞, 李德志, 潘宇, 吕媛媛, 高锦瑾, 程立丽. 崇明东滩湿地芦苇和互花米草N、P利用策略的生态化学计量学分析. 广西植物, 2012, 32(6): 715-722. |
| [33] | 熊汉锋, 黄世宽, 陈治平, 廖勤周, 谭启玲, 王运华. 梁子湖湿地植物的氮磷积累特征. 生态学杂志, 2007, 26(4): 466-470. |
| [34] | 罗先香, 张珊珊, 敦萌. 辽河口湿地碳、氮、磷空间分布及季节动态特征. 中国海洋大学学报: 自然科学版, 2010, 40(12): 97-104. |
| [35] | Vergutz L, Manzoni S, Porporato A, Novais R F, Jackson R B. Global resorption efficiencies and concentrations of carbon and nutrients in leaves of terrestrial plants. Ecological Monographs, 2012, 82(2): 205-220. |
| [36] | Aerts R. Climate, leaf litter chemistry and leaf litter decomposition in terrestrial ecosystems: a triangular relationship. Oikos, 1997, 79(Fasc. 3): 439-449. |
| [37] | Sardans J, Rivas-Ubach A, Peñuelas J. The elemental stoichiometry of aquatic and terrestrial ecosystems and its relationships with organismic lifestyle and ecosystem structure and function: a review and perspectives. Biogeochemistry, 2012, 111(1-3): 1-39. |
| [38] | Parton W, Silver W L, Burke I C, Grassens L, Harmon M E, Currie W S, King J Y, Adair E C, Brandt L A, Hart S C, Fasth B. Global-scale similarities in nitrogen release patterns during long-term decomposition. Science, 2007, 315(5810): 361-364. |
| [39] | Enríquez S, Duarte C M, Sand-Jensen K. Patterns in decomposition rates among photosynthetic organisms: the importance of detritus C: N: P content. Oecologia, 1993, 94(4): 457-471. |
| [40] | 吴琴, 尧波, 幸瑞新, 朱丽丽, 胡启武. 鄱阳湖典型湿地土壤有机碳分布及影响因子. 生态学杂志, 2012, 31(2): 313-318. |
 2016, Vol. 36
2016, Vol. 36




