文章信息
- 曾昭霞, 王克林, 刘孝利, 曾馥平, 宋同清, 彭晚霞, 张浩, 杜虎
- ZENG Zhaoxia, WANG Kelin, LIU Xiaoli, ZENG Fuping, SONG Tongqing, PENG Wanxia, ZHANG Hao, DU Hu
- 桂西北喀斯特区原生林与次生林鲜叶和凋落叶化学计量特征
- Stoichiometric characteristics of live fresh leaves and leaf litter from typical plant communities in a karst region of northwestern Guangxi, China
- 生态学报, 2016, 36(7): 1907-1914
- Acta Ecologica Sinica, 2016, 36(7): 1907-1914
- http://dx.doi.org/10.5846/stxb201409211866
-
文章历史
- 收稿日期: 2014-09-21
- 网络出版日期: 2015-08-05
2. 中国科学院环江喀斯特生态系统观测研究站, 环江 547100;
3. 湖南农业大学资环学院, 长沙 410128
2. Huanjiang Observation and Research Station of Karst Ecosystem, Chinese Academy of Sciences, Huanjiang 547100, China;
3. College of Resources & Environment, Hunan Agricultural University, Changsha 410128, China
氮(N)和磷(P)是各种蛋白质和遗传物质的重要组成元素,由于自然界中N和P元素供应往往受限,成为生态系统生产力的主要限制因素[1, 2]。自然界结构性元素C和限制性元素N、P相互作用,调节着植物的生长[1, 3]。植物通过叶的光合作用固定碳(C),并以凋落物的形式将C和养分逐步补偿给土壤[4]。叶的光合和蒸腾驱动陆地生态系统中水和C、N、P等元素的生物地化循环[5],而凋落物是维系植物体地上C与养分库与土壤C与养分库形成循环的重要生态过程[6]。“生态化学计量学(Ecological stoichiometry)”利用生态过程中多重化学元素(主要是C、N、P等元素)的平衡关系,为研究C、N、P等元素在生物地球化学循环和生态过程中的计量关系及其规律提供了一种新思路[7, 8, 9, 10]。该理论认为[11],有机体能够控制自身的许多特性,包括营养平衡、pH值稳定等,使得内部环境不随外部环境的变化而剧烈变化,生物个体主要元素组成维持在一个狭窄的范围内[12, 13],那么,植物新凋落的叶片相对于新鲜叶片其主要元素分别具有怎样的计量特征以及两者之间是否存在内在关联呢?
我国桂西北喀斯特区独特的地质环境背景加上不合理的土地开发方式造成该区植被破坏严重、水土流失加剧,生态环境脆弱,环境容量小,抗干扰能力差,区域生态环境质量不断恶化,生态服务功能下降[14, 15]。植被退化是这一系列环境问题的重要诱因,如何合理保护现有植被成为石漠化治理的难点和热点。许多学者已经围绕喀斯特区域植被及凋落物进行了相关研究[15, 16],但多以植物或凋落物作为独立对象进行深入研究,较少对两者计量关系差异及相互关系进行综合分析。本文研究了桂西北喀斯特区域3个原生林群落和3个自然恢复28年的次生林群落中6个建群种植物鲜叶以及凋落叶的C、N、P化学计量学特征、比较其差异并分析其相关性,探讨6种植物养分再吸收规律及其对石生环境的适应策略,以促进生态化学计量学理论在喀斯特生态系统中的应用与发展,同时为该区的生态功能恢复与植被重建提供参考。
1 研究区域概况研究区位处广西壮族自治区环江毛南族自治县(107°54′01″—108°05′51″E,25°07′01″—25°12′22″N),属亚热带气候。该区年均日照1451.1 h,年均气温19.3 ℃,年有效积温6260 ℃(≥10 ℃),无霜期310 d,年均降雨量1529 mm。该区森林覆盖率94.8%,保存有世界上喀斯特地貌连片面积最大、保存最完整、原生性最强的原生林。该区植被属中亚热带石灰岩常绿凋落叶阔叶混交林,是石灰岩森林植被顶级群落,为典型的喀斯特原始森林。本研究选取的3种代表性原生林的建群种分别为圆果化香(Platycarya longipes Wu)、伞花木(Eurycorymbus cavaleriei Hand.)和青檀(Pteroceltis tatarinowii Maxim)(表 1)。
| 项目Item |
原生林 Primary forest |
次生林 Secondary forest | ||||
|
圆果化香 Round-fruited Dye-tree (RD) | 伞花木 Eurycorymbus (EU) | 青檀 Wing-hackberry (WH) | 圆叶乌桕 Round-leaved Tallow-tree (RT) | 八角枫 Chinese Alangium (CA) | 黄荆 Negundo Chaste-tree (NC) | |
| 高度*Height/m | 5.42±0.45 | 8.12±0.57 | 8.92±0.67 | 5.68±0.55 | 4.02±0.53 | 2.17±0.41 |
| 郁闭度Canopy density | 0.57 | 0.60 | 0.51 | 0.58 | 0.71 | 0.66 |
| 物种数Species number | 13 | 17 | 9 | 27 | 30 | 34 |
| 均匀度Evenness | 0.81 | 0.79 | 0.82 | 0.62 | 0.64 | 0.59 |
| 辛普森指数Simpson′s index | 0.84 | 0.82 | 0.89 | 0.58 | 0.67 | 0.63 |
| *建群种平均高 | ||||||
3种典型次生林位于环江县中国科学院环江喀斯特生态系统研究观测站(E108°18′57″—108°19′58″,N24°43′59″—24°44′49″),属典型的峰丛洼地喀斯特地貌。该区从1985年开始自然恢复,本文选取3种代表性群落的建群种分别为圆叶乌桕(Sapium rotundifolium Hemsl)、八角枫(Alangium chinense (Lour.)Harms)和黄荆(Vitex negundo Linn)(表 1)。
2 研究方法 2.1 样品收集在20 m×30 m样方内,按“梅花”五点法布置凋落物收集框,收集框为孔径1 mm尼龙网制成的长宽高为1 m×1 m×0.25 m的方形钢架容器,放置时底部距地面15 cm,每块样地放置5个收集框,凋落物样每月收集。本研究于2013年4月进行采样,于凋落物中分拣出各群落建群种凋落叶的部分装入信封。同时于每个群落随机选取建群树种5株,摘取新长出完全展开且未被啃食的成熟叶片15—20片放入信封。所采集样品一并放置烘箱中75 ℃烘至恒重、磨碎、过60目筛,以备养分分析。
2.2 样品分析有机碳(OC)用重铬酸钾-外加热法(GB 9834-88)测定,全氮(TN)用半微量凯氏定氮法(GB 7886-87)测定,全磷(TP)含量测定方法为硝酸-高氯酸消煮-钼锑抗比色法(GB 7887-87)。
2.3 数据处理本文数据分析采用Office 2003 Excel进行数据的整理与初步分析,计算平均值以及标准误差等。应用SPSS 13.0统计分析软件进行统计分析:采用单因素方差分析(One-Way ANOVA)对鲜叶和凋落叶C、N、P含量以及C:N、C:P、N:P进行差异性检验。植物鲜叶与凋落叶C:N、N:P比值相关性采用Pearson相关分析。为改善数据的正态性,在对叶片的N与P以及N、P与叶片N:P进行相关性分析时对数据进行了以10为底的对数转换[5]。
3 结果与分析 3.1 植物鲜叶与凋落叶C、N、P含量特征如表 2所示,6个群落建群种新鲜叶片C、N、P含量均大于凋落叶(鲜叶的C、N、P平均含量分别为404.3、22.5、1.75 mg/g,而凋落叶C、N、P平均含量分别为376.5、19.0、1.35 mg/g),原生林新鲜叶中C含量明显高于次生林,次生林黄荆鲜叶C含量最低,仅为(372.4±4.8) mg/g,但6种群落凋落叶C含量差异不明显。3种原生林鲜叶N、P含量均显著大于凋落叶(P<),而3种次生林仅黄荆鲜叶N、P含量显著高于凋落叶(P<0.05)。
|
类型 Type | 群落Species | C/(mg/g) | N/(mg/g) | P/(mg/g) | |||
|
鲜叶 Live leaf | 凋落叶 Litter leaf | 鲜叶 Live leaf | 凋落叶 Litter leaf | 鲜叶 Live leaf | 凋落叶 Litter leaf | ||
| 原生林 | 圆果化香(RD) | 416.3±2.5abA | 378.4±9.1bB | 23.4±4.2aA | 19.6±1.2B | 1.7±0.3A | 1.2±0.1bB |
| Primary | 伞花木(EU) | 429.6±6.4a | 401.1±9.2a | 23.7±3.3aA | 19.4±1.9B | 1.6±0.5A | 1.1±0.0bB |
| forest | 青檀(WH) | 408.3±7.8bA | 369.4±6.6bB | 24.9±2.7aA | 20.2±2.2B | 1.7±0.8A | 1.2±0.1bB] |
| 次生林 | 圆叶乌桕(RT) | 404.4±3.7b | 388.9±4.5ab | 19.9±2.8b | 17.9±4.3 | 1.7±0.6 | 1.5±0.8a |
| Secondary | 八角枫(CA) | 397.2±5.1bA | 364.2±4.6bcB | 21.2±2.3b | 18.2±7.1 | 1.9±0.4A | 1.5±0.4aB |
| forest | 黄荆(NC) | 372.4±4.8c | 356.7±7.5c | 21.7±3.7bA | 18.8±3.4B | 1.9±0.7A | 1.6±0.4aB |
| 表中所示为平均值± 标准误差;同行相同参数项不同大写字母表示差异显著,同列相同参数不同小写字母表示种间差异显著(P< 0.05) | |||||||
而对于6个树种而言,3种原生林鲜叶C含量高于次生林,但凋落叶C含量与次生林差异不明显。3种原生林鲜叶N含量显著高于次生林(P< 0.05),但6个树种的凋落叶N含量无显著差异。3个原生林群落建群种的平均C、N含量均显著大于次生林(P<),而P含量则略小于次生林,尤其原生林凋落叶P含量显著低于次生林(P<0.05)(表 2)。
3.2 植物鲜叶与凋落叶C-N-P生态化学计量特征 3.2.1 植物鲜叶与凋落叶C:N、C:P和N:P特征对于所研究植物,鲜叶C:N、C:P、N:P均值分别为17.8、244.9、13.8,分别小于凋落叶C:N、C:P、N:P比值(19.3、315.3、16.3)(图 1)。次生林鲜叶与凋落叶的C:N比值(分别为18.7、20.0)均大于原生林(16.4、18.3),而C:P、N:P(209.1、242.8)则小于原生林(240.2、307.8)。原生林鲜叶N:P比为13—15之间,凋落叶N:P则在16—18之间;次生林鲜叶N:P比为11—12之间,而凋落叶N:P比在11—13之间。

|
| 图 1 不同林地凋落叶与鲜叶C:N, C:P, N:P Fig.1 The C:N, C:P, N:P of live leaf and litter leaf in the study forests. RD, EU, WH, RT, CA与NC分别代表3种原生林群落圆果化香(Round-fruited Dye-tree)、 伞花木(Eurycorymbus)与青檀(Wing-hackberry)及 3中次生林群落圆叶乌桕(Round-leaved Tallow-tree)、 八角枫(Chinese Alangium)和黄荆(Negundo Chaste-tree) |
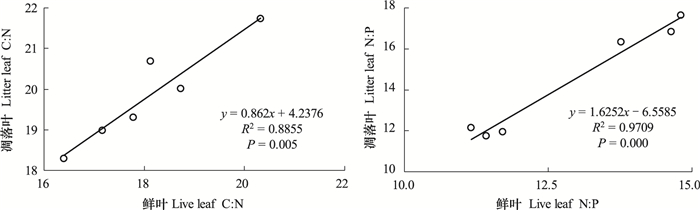
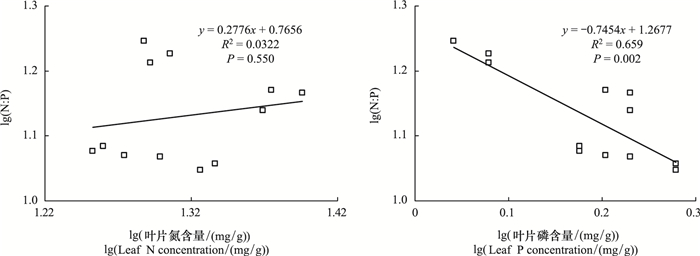
植物鲜叶和凋落叶的C:N与N:P比均为极显著正相关(两者R2分别为0.8855,P<0.01以及0.9709,P<0.001)(图 2)。6个群落凋落叶片N、P含量总体上呈现正相关(图 3,R2=0.1839,P=0.164)。叶片的N:P比率与N含量呈正相关(图 4,R2=0.0322;P=0.550),与P含量呈现显著负相关关系(图 4,R2=0.659;P<0.05)。
|
| 图 2 植物鲜叶与凋落叶C:N、N:P相关性 Fig.2 The relationships of C:N and N:P between live leaf and litter leaf |

|
| 图 3 叶片氮与磷含量(对数)相关关系 Fig.3 The relationships between leaf N and leaf P concentration |
|
| 图 4 叶片氮、磷含量与N:P比值(对数)相关关系 Fig.4 The relationships between leaf N:P ratios and leaf N, P concentration |
氮(N)和磷(P)是植物的基本营养元素,对植物生命各种功能具有直接影响[2, 17, 18],在植物的各种生理代谢中发挥着重要的作用,彼此独立而又相互影响[5],并最终影响植物叶片的碳(C)固定[19, 20]。Han等人[21]对中国753个陆地植被物种的叶片N、P含量及其化学计量学的研究结果显示,中国陆地植被叶片的平均N、P含量分别为20.2、1.46 mg/g。本研究中6种植物新鲜叶片N、P平均含量分别为22.5、1.75 mg/g,而凋落叶N、P平均含量分别为19.0、1.35 mg/g。本研究采集样品时间正是在生长初期,叶片输导组织、支持组织发育都不完善,细胞大多具有分裂能力,需要大量的蛋白质和核酸,因此对N、P的选择性吸收较多,浓度相对Han等人[21]的研究结果偏高,平川等[22]认为植物叶片营养元素含量与自身结构特点和生长节律有很大关系,这也与孙书存和陈灵芝[23]的研究结果一致。
N、P元素循环特征限制着生态系统大多重要生态过程[24, 25],而凋落物的N、P养分含量及N:P比值与植物再吸收能力相关[15],本研究6个群落建群种植物凋落叶的N:P比变化与植物鲜叶N:P比呈现一致的规律,这体现出凋落物秉承了植物活体的特性,而6种植物鲜叶N、P含量均大于凋落叶,N:P比值均小于凋落叶,表明植物体对N的再吸收率大于P[23, 24]。当环境中N、P含量较低时植物会通过从土壤中吸收养分和植物养分再吸收等途径加快养分循环速度、提高养分利用效率[16],当植物高速生长时会通过富集P素(高P素含量、低N:P比值)合成rRNA来满足其需要,因此N:P比也可以很好地反映植物的生长速率[26],低N:P比表征植物具有较快的生长速率[27],本研究中3个次生林建群种植物鲜叶与凋落叶的N:P比均小于原生林(图 1),这表明次生林相对于原生林有更快的生长速率。N:P比值还与凋落物分解速率有关,一般认为,N:P比值越高,凋落物的分解受P素限制越强,分解速率相对越慢[4, 16],本研究中3个原生林建群种凋落叶N:P比值均大于次生林3个建群种,说明原生林凋落物分解相对较慢,有利于养分的储存。喀斯特区域特殊的地质背景,导致土壤和养分流失迅速[14, 15],而其高温高湿环境有利于凋落物的分解,在雨水的淋溶和冲刷作用下,凋落物分解析出的营养元素更易流失,进而影响到土壤中储存的养分量[15],原生林能相对多的保留养分以供植物吸收,更能适应喀斯特石生环境。
研究表明,陆地生态系统的生产力经常受N、P或二者的共同限制[28]。叶片作为植物的主要光合器官,其N:P比值大小常被用来表明生态系统生产力受到哪种元素的限制作用[7, 24, 29, 30, 31, 32]。本研究中原生林鲜叶N:P比为13—15之间,该范围接近于Han等人[21]基于中国753种陆地植物叶片的N、P调查所得出的几何平均值14.4以及全球平均水平(13.8)[18],这反映出成熟林主要元素计量比趋同的特征。次生林鲜叶N:P比为11—12之间,也处于Güsewell等[7]与Tessier等[30]所报导的木本植物N、P养分限制临界值之间,表明喀斯特脆弱区3种典型次生林自然恢复28年后,施肥可能对生物量增加没有明显效果,3种植物均已通过长期对喀斯特石生环境的适应,调整自身养分利用策略,达到相对稳定的状态。
植物叶片的C:N和C:P比表征着植物吸收营养所能同化C的能力,在一定程度上反映了植物的N、P养分的利用效率,具有重要的生态学意义[33, 34]。本研究6种植物鲜叶C:N、C:P比均值分别为17.8、244.9,其C:N比小于全球平均水平的22.5[18],这可能与采样时间有关;而C:P则大于全球水平的232[18],表明喀斯特森林植被对P素的利用效率较高,这也反映了喀斯特森林或许存在P素亏缺。喀斯特区域光照充足,植物光合作用强,有利于有机物的积累,但是由于该区土层浅薄且土壤养分随水土流失严重,造成土壤营养元素存留量少而导致植物吸收量不足[15]。
对于研究中的3个典型原生林与3个次生林群落来说,其植物鲜叶和凋落叶的C:N与N:P比均呈极显著正相关(图 2),这也验证了叶片养分元素间具有共变的特性[16]。6个群落凋落叶片N、P含量呈正相关关系(图 3),叶片N、P元素含量间良好的线性相关决定了其N:P比值的变异性要小于N、P含量本身的变异性,即N:P比具有相对的稳定性,这反映了不同森林类型植物叶片N、P含量的相对一致性,这是高等陆生植物C-N-P元素计量的普遍规律[18]也是植物最基本的特性之一[35],体现了绿色植物中固C过程中N、P等养分利用效率的权衡策略。生长速率假说认为,自养生物加大生物量的积累速率需要提高其P含量、降低其N:P比值来加速蛋白质的合成,加强同化作用[27, 36]。研究结果在一定程度上验证了生长速率假说,体现了植物群落对环境的适应。
本文对喀斯特区域3个原生林群落建群种与3个次生林群落建群种植物生长季初的新鲜叶片和凋落叶的C、N、P元素含量及其生态化学计量特征进行了分析,发现6种植物对N的再吸收强于P。原生林能相对多的保留养分以供植物吸收,更能适应喀斯特石生环境。而经过28a的自然恢复,3种次生林群落植物均已通过自身对环境的适应达到相对稳定的状态。研究对该区植被建设具有一定的指导意义,但没有考虑不同物候期植物的养分限制性状况,今后需进一步开展相关研究,以期得出更加全面、系统的结论,为喀斯特脆弱区的植被保护与恢复重建提供理论基础与数据支撑。
| [1] | Elser J J, Bracken M E S, Cleland E E, Gruner D S, Harpole W S, Hillebrand H, Ngai J T, Seabloom E W, Shurin J B, Smith J E. Global analysis of nitrogen and phosphorus limitation of primary producers in freshwater, marine and terrestrial ecosystems. Ecology Letters, 2007, 10(12): 1135-1142. |
| [2] | Vitousek P M, Howarth R W. Nitrogen limitation on land and in the sea: How can it occur?. Biogeochemistry, 1991, 13(2): 87-115. |
| [3] | Elser J J, Urabe J. The stoichiometry of consumer-driven nutrient recycling: theory, observations, and consequences. Ecology, 1999, 80(3): 540-550. |
| [4] | 王维奇, 徐玲琳, 曾从盛, 仝川, 张林海. 河口湿地植物活体-枯落物-土壤的碳氮磷生态化学计量特征. 生态学报, 2011, 31(23): 7119-7124. |
| [5] | 韩文轩, 吴漪, 汤璐瑛, 陈雅涵, 李利平, 贺金生, 方精云. 北京及周边地区植物叶的碳氮磷元素计量特征. 北京大学学报: 自然科学版, 2009, 45(5): 855-860. |
| [6] | Vitousek P M, Turner D R, Parton W J, Sanford R L. Litter decomposition on the Mauna Loa environmental matrix,Hawai'i: patterns, mechanisms, and models. Ecology, 1994, 75(2): 418-429. |
| [7] | Güsewell S. N: P ratios in terrestrial plants: variation and functional significance.New Phytologist, 2004, 164(2): 243-266. |
| [8] | Sterner R W, Elser J J. EcologicalStoichiometry: the Biology of Elements from Molecules to the Biosphere. Princeton: Princeton University Press, 2002. |
| [9] | Sterner R W, George N B. Carbon, nitrogen, and phosphorus stoichiometry of cyprinid fishes. Ecology, 2000, 81(1): 127-140. |
| [10] | 贺金生, 韩兴国. 生态化学计量学: 探索从个体到生态系统的统一化理论. 植物生态学报, 2010, 34(1): 2-6. |
| [11] | 曾德慧, 陈广生. 生态化学计量学: 复杂生命系统奥秘的探索. 植物生态学报, 2005, 29(6): 1007-1019. |
| [12] | 吴统贵, 吴明, 刘丽, 萧江华. 杭州湾滨海湿地3种草本植物叶片N、P化学计量学的季节变化. 植物生态学报, 2010, 34(1): 23-28. |
| [13] | Zhang L X, Bai Y F, Han X G. Application of N: P stoichiometry to ecology studies. Acta Botanica Sinica, 2003, 45(9): 1009-1018. |
| [14] | 王克林. 生态脆弱区域农业与环境协调发展策略. 中国生态农业学报, 2001, 9(3): 86-88. |
| [15] | 曾馥平, 彭晚霞, 宋同清, 王克林, 吴海勇, 宋希娟, 曾昭霞. 桂西北喀斯特人为干扰区植被自然恢复22年后群落特征. 生态学报, 2007, 27(12): 5110-5119. |
| [16] | 潘复静, 张伟, 王克林, 何寻阳, 梁士楚, 韦国富. 典型喀斯特峰丛洼地植被群落凋落物C:N:P生态化学计量特征. 生态学报, 2011, 31(2): 335-343. |
| [17] | Elser J J, Fagan W F, Denno R F, Dobberfuhl D R, Folarin A, Huberty A, Interlandi S, Kilham S S, McCauley E, Schulz K L,Siemann E H, Sterner R W. Nutritional constraints in terrestrial and freshwater food webs. Nature, 2000, 408(6812): 578-580. |
| [18] | Reich P B, Oleksyn J. Global patterns of plant leaf N and P in relation to temperature and latitude.Proceedings of the National Academy of Sciences of the United States of America, 2004, 101(30): 11001-11006. |
| [19] | 安卓, 牛得草, 文海燕, 杨益, 张洪荣, 傅华. 氮素添加对黄土高原典型草原长芒草氮磷重吸收率及C: N: P化学计量特征的影响. 植物生态学报, 2011, 35(8): 801-807. |
| [20] | Güsewell S, Koerselman W, Verhoeven J T A. Biomass N: P ratios as indicators of nutrient limitation for plant populations in wetlands.Ecological Applications, 2003, 13(2): 372-384. |
| [21] | Han W X, Fang J Y, Guo D L, Zhang Y. Leaf nitrogen and phosphorus stoichiometry across 753 terrestrial plant species in China. New Phytologist, 2005, 168(2): 377-385. |
| [22] | 平川, 王传宽, 全先奎. 环境变化对兴安凋落叶松氮磷化学计量特征的影响. 生态学报, 2014, 34(8): 1965-1974. |
| [23] | 孙书存, 陈灵芝. 东灵山地区辽东栎叶养分的季节动态与回收效率. 植物生态学报, 2001, 25(1): 76-82. |
| [24] | Aerts R, Chapin F S III. The mineral nutrition of wild plants revisited: a re-evaluation of processes and patterns. Advances in Ecological Research, 1999, 30: 1-67. |
| [25] | Chapin F S III. The mineral nutrition of wild plants.Annual Review of Ecology and Systematics, 1980, 11: 233-260. |
| [26] | 王维奇, 仝川, 曾从盛. 不同质地湿地土壤碳、氮、磷计量学及厌氧碳分解特征. 中国环境科学, 2010, 30(10): 1369-1374. |
| [27] | Elser J J, Acharya K, Kyle M, Cotner J, Makino W, Watts T, Hobbie S, Fagan W, Schade J, Hood J, Sterner R W. Growth rate-stoichiometry couplings in diverse biota. Ecology Letters, 2003, 6(10): 936-943. |
| [28] | 王晶苑, 王绍强, 李纫兰, 闫俊华, 沙丽清, 韩士杰. 中国四种森林类型主要优势植物的C: N: P化学计量学特征. 植物生态学报, 2011, 35(6): 587-595. |
| [29] | 王绍强, 于贵瑞. 生态系统碳氮磷元素的生态化学计量学特征. 生态学报, 2008, 28(8): 3937-3947. |
| [30] | Tessier J T, Raynal D J. Use of nitrogen to phosphorus ratios in plant tissue as an indicator of nutrient limitation and nitrogen saturation. Journal of Applied Ecology, 2003, 40(3): 523-534. |
| [31] | Xia C X, Yu D, Wang Z, Xie D. Stoichiometry patterns of leaf carbon, nitrogen and phosphorous in aquatic macrophytes in eastern China. Ecological Engineering, 2014, 70: 406-413. |
| [32] | Zhang L X, Bai Y F, Han X G. Differential responses of N: P stoichiometry of Leymus chinensis and Carex korshinskyi to N additions in a steppe ecosystem in Nei Mongol. Acta Botanica Sinica, 2004, 46(3): 259-270. |
| [33] | 黄建军, 王希华. 浙江天童32种常绿阔叶树叶片的营养及结构特征. 华东师范大学学报: 自然科学版, 2003, (1): 92-97. |
| [34] | 杨阔, 黄建辉, 董丹, 马文红, 贺金生. 青藏高原草地植物群落冠层叶片氮磷化学计量学分析. 植物生态学报, 2010, 34(1): 17-22. |
| [35] | 吴统贵, 陈步峰, 肖以华, 潘勇军, 陈勇, 萧江华. 珠江三角洲3种典型森林类型乔木叶片生态化学计量学. 植物生态学报, 2010, 34(1): 58-63. |
| [36] | Niklas K J, Owens T, Reich P B, Cobb E D. Nitrogen/phosphorus leaf stoichiometry and the scaling of plant growth.Ecology Letters, 2005, 8(6): 636-642. |
 2016, Vol. 36
2016, Vol. 36




