文章信息
- 魏利军, 汤龙升, 李胜男, 周建, 孔繁翔, 史小丽
- WEI Lijun, TANG Longsheng, LI Shengnan, ZHOU Jian, KONG Fanxiang, SHI Xiaoli
- CO2升高对枝角类群落结构影响的原位模拟
- Effects of a simulated increase in atmospheric CO2 concentration on cladoceran zooplankton collected from Lake Taihu
- 生态学报, 2016, 36(7): 1846-1853
- Acta Ecologica Sinica, 2016, 36(7): 1846-1853
- http://dx.doi.org/10.5846/stxb201409201861
-
文章历史
- 收稿日期: 2014-09-20
- 网络出版日期: 2015-08-05
2. 南京师范大学生命科学学院, 南京 210046
2. School of Biological Sciences, Nanjing Normal University, Nanjing 210046, China
由于人类活动的影响,全球大气二氧化碳(CO2)浓度已经从工业前的270 μL/L上升至现在的380 μL/L,已有研究报告预计未来100年之内,大气CO2浓度将达到750 μL/L[1]。湖泊作为内陆水体的重要组成单元,大气CO2浓度升高会显著影响其碳化学环境[2],导致表层水体的CO2水气扩散通量以及水体中HCO-3和CO2-3的含量升高[3]。CO2作为浮游植物的直接碳源,其浓度升高会影响浮游植物的生理和生态过程,不仅增加了浮游植物光合作用的碳源,可能会削弱浮游植物对碳浓缩机制(Carbon Concentrating Mechanism,CCM)的依赖性[4, 5],进而影响水体中浮游动物的数量和群落结构。
太湖是中国五大淡水湖之一,对长江三角洲的发展至关重要。长期的富营养化导致太湖浮游植物优势种由绿藻和硅藻逐渐转变为蓝藻[6]。研究表明,大气CO2浓度升高会降低太湖蓝藻在春、夏、秋3个季节的竞争优势,而绿藻的竞争优势会得到加强[7];相对蓝藻而言,绿藻对浮游动物具有更强的可食性,其对CO2水平的生理响应,会直接影响浮游动物的数量和群落结构,因此本研究选取绿藻门的斜生栅藻作为浮游动物的食物,利用透析袋培养斜生栅藻与枝角类浮游动物,揭示CO2浓度升高对斜生栅藻的生长及枝角类浮游动物群落结构的影响。
1 材料与方法 1.1 实验材料 1.1.1 斜生栅藻的来源实验采用斜生栅藻(Scenedesmus obliquus)由中国科学院水生生物研究所藻种库提供,采用BG-11培养基[8]无菌条件下在光照培养箱内培养。
1.1.2 枝角类浮游动物的选择与培养实验中选择的枝角类均分离自太湖,其中春季枝角类选用溞属(Daphnia)、网纹溞属(Ceriodaphnia)以及象鼻溞属(Bosmina)三类,夏季为溞属(Daphnia)、网纹溞属(Ceriodaphnia)和秀体溞属(Diaphanosoma),同时为避免室内培养(7 d)的枝角类浮游动物无法适应野外环境,实验开始前在太湖实验站对其进行了原位驯化(3 d)。
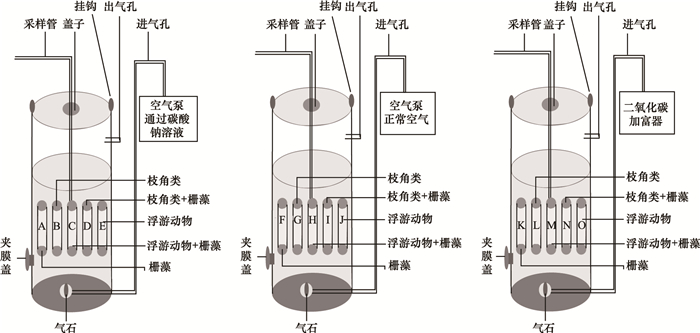
1.2 实验设计 1.2.1 原位实验野外实验分两季(春季:2012-04-29—2012-05-26;夏季:2012-08-16—2012-09-05)在中国科学院太湖生态系统研究站(无锡本部:31°25′15′′N,120°12′55′′E)进行,取太湖梅梁湾水样置于150 L塑料桶(高70 cm、内径58 cm,共9个),置于太湖岸边的水池内。本研究设置的低浓度水平(270 μL/L)由当地空气通过Na2CO3 溶液吸收制备,作为对照组的现有水平(380 μL/L)采用当地空气,高CO2浓度水平(750 μL/L)由CO2加富器制备(CO2 enrichlor CE-300,中国),采用CO2红外检测仪(Testo 535,德国)跟踪并及时修正的CO2浓度水平;每个浓度梯度设置3个平行组,采用气石鼓气(微小气泡)的形式模拟大气CO2浓度升高的过程,控制鼓气速度为1.0 L/min(图 1)。
|
| 图 1 实验装置原理图 Fig.1 Schematic diagram of the experimental setup |
模拟实验中,控制实验大桶内各营养盐参数基本维持初始状态,通过高频率测定水体各项营养盐指标(总氮,总磷,铵态氮,硝态氮,磷酸根浓度)并及时添加KH2PO4、NH4Cl、NaNO3等形式的营养盐,使不同CO2处理组之间的营养盐浓度无显著性差异,并基本维持初始状态。
此外,控制实验在距离太湖水体2—4 m的水池内进行,保证了实验水体温度、光照和太湖一致,温度相差小于±0.5 ℃。所以,本研究基本做到了单因素(CO2)的控制实验,可以模拟大气CO2升高对太湖浮游动物群落的影响。
1.2.3 斜生栅藻和枝角类控制实验将室内纯培养的斜生栅藻置于装有湖水的多个透析袋中,控制初始藻密度约为5×105个/mL。一部分透析袋用于斜生栅藻的培养,用于研究CO2对斜生栅藻生长的影响,另一部分透析袋中添加枝角类,添加的数量参考太湖水体中的数量。其中透析袋的体积约为350 mL,截留分子量为14000Da,能够保证透析袋内与桶内水进行正常交换,水体理化性质保持一致,同时防止透析袋内浮游植物和浮游动物向外扩散,将其置于不同CO2浓度的大桶内,每隔一定天数采样,采样时每个浓度组取出两个透析袋作为平行,研究CO2浓度升高对栅藻生物量的影响,并观察枝角类种群数量及群落结构的变化情况。
1.3 实验方法 1.3.1 水体理化参数总氮(原液)、溶解性总氮(过GF/C膜滤液)采用碱性过硫酸钾消解紫外分光光度法(GB11894-89)测定;总磷(原液)、溶解性总磷(过GF/C膜滤液)先经过碱性过硫酸钾消解,然后用钼酸铵分光光度法(GB11893-89)测定;铵态氮采用纳氏试剂分光光度法(HJ535-2009)法测定;硝态氮采用酚二磺酸分光光度法(GB7480-87)法测定。
1.3.2 斜生栅藻和枝角类计数斜生栅藻计数是通过鲁哥试剂固定的样品浓缩后用血球计数板在显微镜10×40倍镜下观察计数,通过浓缩倍数得出斜生栅藻密度,枝角类浮游动物通过显微镜观察计数[9]。
1.3.3 数据分析本研究利用sigmaplot 12.5及R 3.0.2进行双因素方差分析(Two-Way ANOVA)和画图,其中P <0.01表示存在极显著性差异,P <0.05表示显著性差异。
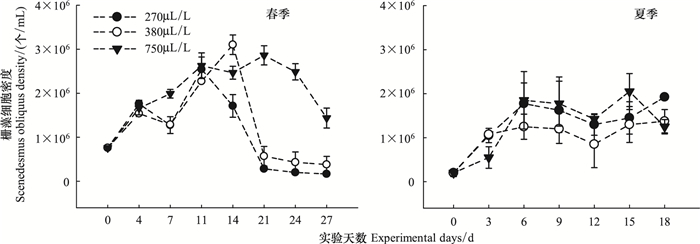
2 结果与分析 2.1 CO2升高对斜生栅藻密度的影响春季在270 μL/L和380 μL/L的CO2浓度下,斜生栅藻密度先缓慢上升,到11—14 d时达到峰值,然后出现缓慢下降,实验期间斜生栅藻平均密度分别为1.39×106、1.59×106个/mL,当CO2浓度为750 μL/L时,斜生栅藻在实验后期藻密度在高水平保持波动,实验期间平均藻密度为2.06×106个/mL;夏季斜生栅藻在实验初期快速生长,第6天后,保持在一个平稳的水平,后期稍有下降,在270、380 μL/L和750 μL/L下,实验期间的平均密度分别为1.33×106、1.04×106 、1.30×106个/mL(图 2)。
|
| 图 2 不同CO2浓度对春夏两季斜生栅藻密度的影响 Fig.2 The effect of CO2 concentration on Scenedesmus obliquus density during different seasons |
随着时间的变化,斜生栅藻密度在两季均存在显著性差异。在单独CO2浓度影响下,春季斜生栅藻密度在3个CO2浓度组间存在极显著性差异(P<0.01),高CO2浓度下斜生栅藻密度总体水平要高于低浓度组。春季温度光照等条件适宜斜生栅藻的生长,但实验后期可能受营养盐的限制,斜生栅藻密度出现了下降,此时高CO2浓度提高了斜生栅藻光合活性[10, 11, 12, 13, 14],可能会增强斜生栅藻对低营养环境的耐受力,延缓了其生物量的降低。
单独CO2浓度影响下,夏季斜生栅藻密度不存在显著性差异。夏季高CO2浓度组斜生栅藻密度略微高于低浓度组,但差异性不显著。夏季,虽然实验期间斜生栅藻有一个生长的过程,但初期过后无明显变化,由于绿藻生长的适宜N/P为5/1—10/1,适宜温度为25—30 ℃[15],而夏季太湖梅梁湾区域N/P在16.8/1左右,同时夏天湖水温度在30 ℃以上[16],可见夏季湖区的营养盐和温度限制了斜生栅藻的生长,此时栅藻对CO2不敏感,斜生栅藻的密度并没有达到春季的最高水平,因此斜生栅藻的生长受CO2浓度影响不明显。总体而言,当斜生栅藻快速生长,密度较高时,水体中的CO2已经不能满足其生长,增加CO2浓度能够促进斜生栅藻生长,并有利于其生存。
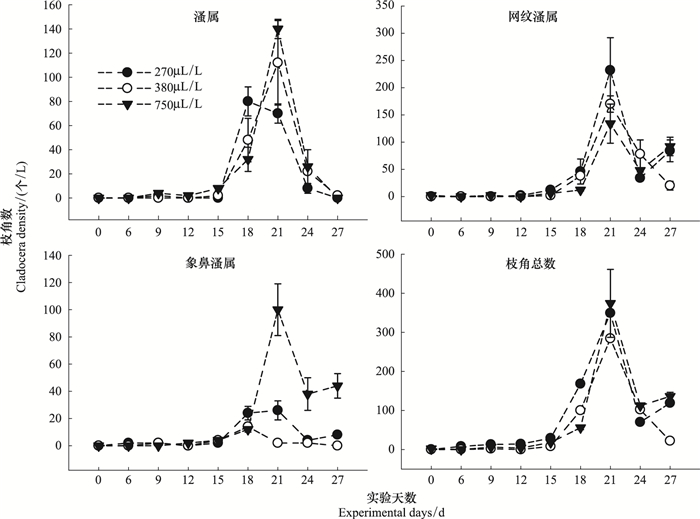
2.2 CO2升高对枝角类种群数量的影响春季不同种群枝角类的数量在实验期间均出现先增加后减少的趋势,大约在实验进行的第21天达到峰值。随着CO2浓度的升高,溞属的最大密度逐渐增大,在270、380 μL/L和750 μL/L CO2浓度下,最大密度分别达到了80、110个/L和140个/L。象鼻溞属的数量也在750 μL/L CO2浓度下达到最大值。网纹溞属随着CO2浓度升高数量变化幅度逐渐减小,在3个CO2浓度梯度下,最大密度分别为235、170、130个/L。在3个CO2浓度梯度下,整个枝角类平均数量分别为86、58个/L和79个/L。枝角类数量在春季实验中,随时间的变化,在时间和CO2浓度的交互作用下,存在极显著差异性(P <0.01)(图 3)。
|
| 图 3 不同CO2浓度对春季枝角类种群数量的影响 Fig.3 The effect of CO2 concentration on Cladocera density in spring |
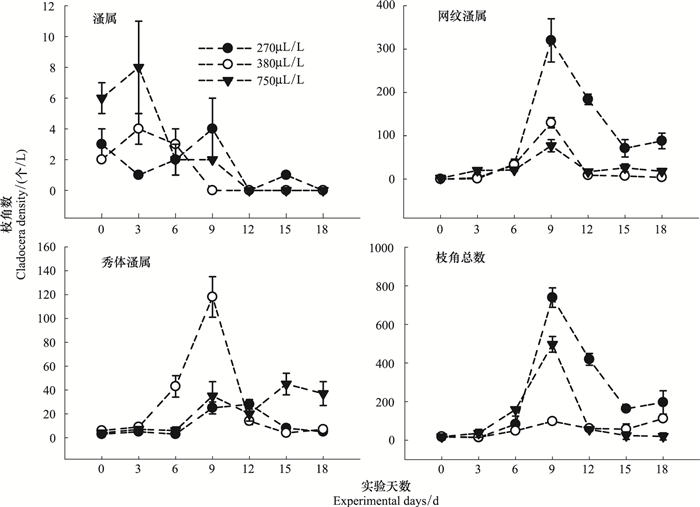
夏季枝溞属数量在实验期间呈现逐渐减少的趋势,网纹溞属和秀体溞属则呈现先增加后减少的趋势,大约在实验进行的第9天达到峰值。网纹溞属随着CO2浓度的升高,最大数量逐渐减小,在270、380 μL/L、750 μL/L CO2浓度下,最大数量分别为320、125个/L和60个/L。秀体溞属在当前CO2浓度下生长的最快,但在实验后期会在750 μL/L CO2浓度下保持稳定,约每升40个。在3个CO2浓度梯度下,夏季平均枝角数量分别为233、59个/L和116个/L。枝角类数量在夏季实验中,随时间的变化,在时间和CO2浓度的交互作用下,存在极显著差异性(P <0.01)(图 4)。
|
| 图 4 不同CO2浓度对夏季枝角类种群数量的影响 Fig.4 The effect of CO2 concentration on Cladocera density in summer |
春季和夏季由于水温等条件适宜枝角类大量繁殖,因此实验初期有一个明显的生长过程,但后期由于食物缺乏,环境容纳量有限等因素限制,故最后种群数量又出现下降[17, 18, 19]。由于不同种群的枝角类对CO2升高的响应不一样,因此CO2浓度升高对整个枝角类浮游动物数量影响的趋势并不明显。
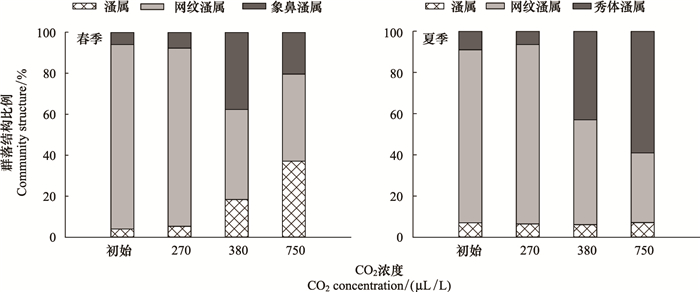
2.3 CO2升高对不同季节枝角类群落结构的影响通过比较实验期间不同枝角类种群在3个CO2浓度梯度下的平均数量,可以看出CO2水平升高对枝角类群落结构的影响。春季在270、380、750 μL/L 3个CO2浓度下,溞属在枝角类群落中所占比例随浓度升高而升高,从初始的4%一直上升至37.1%;网纹溞属所占比例则随CO2浓度升高而降低,其中在270 μL/L和380 μL/L两个浓度下下降尤为明显,从86.9%降至44%;象鼻溞属所占比例数在3个浓度下相对初始状态均有所上升,但在380 μL/L浓度下数值最高,由初始的6%上升到37.7%,变化最为明显(图 5)。3个梯度下网纹溞属占绝对优势,网纹溞属体积明显小于溞属,这可能是因为富营养化水体有利于小个体枝角类动物形成优势[20, 21]。随CO2浓度升高,网纹溞属在枝角类群落中所占比例有所下降,相应的溞属和象鼻溞属所占比例逐渐增大。可见,CO2浓度升高对食物组成及质量带来影响会间接影响到枝角类群落,对于网纹溞属CO2浓度越高胁迫效应越明显,对于溞属和象鼻溞属,CO2浓度升高有利于其生存;CO2浓度升高对枝角类群落的直接影响还有待进一步研究。
|
| 图 5 不同CO2浓度对春季和夏季枝角类群落结构的影响 Fig.5 The effect of CO2 concentration on Cladocera community structure in spring and summer |
夏季在270、380、750 μL/L 3个CO2浓度下,溞属在枝角类群落中所占比例基本保持不变,数值保持在初始的7%左右;网纹溞属所占比例同样随着CO2浓度升高而降低,和春季有相同的趋势,在270 μL/L和380 μL/L两个浓度下从87%降至50.8%,但仍为优势种;秀体溞属在CO2浓度为270 μL/L时所占比例有所下降,但在380 μL/L和750 μL/L下迅速升高,从初始的9%增加到43%和59%,促使其成为优势种(图 5)。可见,夏季高温可能抑制了溞属的生长和繁殖,不利于其生存;随CO2浓度升高网纹溞数量所占比例同样有所降低,有利于秀体溞属生长繁殖。
本研究结果表明CO2浓度升高,会显著增加斜生栅藻生物量,但食物数量的增加并不能在相同程度上促进所有枝角类动物的生长。事实上CO2浓度的升高还会改变食物的质量,大量的研究表明浮游藻类的化学计量值C:P比值会随着CO2浓度的升高而显著增加[22, 23]。在枝角类中,一般象鼻溞属(Bosmina)和秀体溞属(Diaphanosoma)的C:P比例较大,即含磷量较低,而另一些枝角类如网纹溞属(Ceriodaphnia)的C:P比较小,即含磷量较高。因此,CO2浓度升高会产生相对高C:P比的食物,更有利于象鼻溞属和秀体溞属的生长,而不利于网纹溞属的生长。对溞属(Daphnia)而言,不同种类差异也较大,如溞属种类Daphnia pulicaria的C:P比是Daphnia magna的2倍[24],因此溞属对CO2升高的响应在种间还存在差异。
3 结论(1)CO2浓度升高有利于斜生栅藻生长,其生物量随CO2浓度的升高而增加。
(2)CO2浓度的变化能显著改变枝角类的群落结构。CO2浓度的升高更加有利于象鼻溞属、秀体溞属和春季溞属的生长,而不利于网纹溞属的生长。这可能是由于CO2浓度的升高使得浮游藻类的C:P有所增加,食物质量的改变进而影响了枝角类的群落结构。
| [1] | IPCC. Summary for Policymakers of Climate Change 2007: The Physical Science Basis//Contribution of Working Group I to the Fourth Assessment Report of the Intergovernmental Panel on Climate Change. Cambridge: Cambridge University Press, 2007. |
| [2] | Xia J R, Gao K S. Effects of doubled atmospheric CO2 concentration on the photosynthesis and growth of Chlorella pryenoidosa cultured at varied levels of light. Fisheries science, 2003, 69(4): 767-771. |
| [3] | Stumm W, Morgan J J. Aquatic Chemistry: Chemical Equilibria and Rates in Natural Waters. 3rd ed. New York: John Wiley and Sons, 1996: 206-315. |
| [4] | Meehl G A, Stocker T F, Collins W D, Friedlingstein P, Gaye A T, Gregory J M, Kitoh A, Knutti R, Murphy J M, Noda A, Raper S C B, Watterson I G, Weaver A J, Zhao Z C. Global climate projections//Solomon S, Qin D, Manning M, Chen Z, Marquis M, Averyt K B, Tignor M, Miller H L, eds. Climate Change 2007: The Physical Science Basis. Contribution of Working Group I to the Fourth Assessment Report of the Intergovernmental Panel on Climate Change. Cambridge: Cambridge University Press, 2007: 747-845. |
| [5] | Houghton J T, Ding Y, Griggs D J, Noguer M, van der Linden P J, Dai X, Maskell K, Johnson C A. Climate change 2001: The scientific basis. Cambridge: Cambridge University Press, 2001: 1-32. |
| [6] | 钱奎梅, 陈宇炜, 宋晓兰. 太湖浮游植物优势种长期演化与富营养化进程的关系. 生态科学, 2008, 27(2): 65-70. |
| [7] | 赵旭辉. 模拟大气CO2浓度升高对太湖浮游植物生理特性和群落结构的影响[D]. 北京: 中国科学院研究生院, 2013. |
| [8] | 岳龙, 付秋果, 张素芬, 王伟, 汪海燕, 叶庆富. 栅藻的优化培养及脂质提取方法研究. 核农学报, 2012, 26(6): 894-899. |
| [9] | 黄祥飞, 陈伟民, 蔡启铭. 湖泊生态调查观测与分析. 北京: 中国标准出版社, 2000: 1-247. |
| [10] | Hein M, Sand-Jensen K. CO2 increases oceanic primary production. Nature, 1997, 388(6642): 526-527. |
| [11] | Schippers P, Lürling M, Scheffer M. Increase of atmospheric CO2 promotes phytoplankton productivity. Ecology letters, 2004, 7(6): 446-451. |
| [12] | Schippers P, Vermatt J E,de Klein J, Mooij W M. The effect of atmospheric carbon dioxide elevation on plant growth in freshwater ecosystems. Ecosystems, 2004, 7(1): 63-74. |
| [13] | 夏建荣, 高坤山. CO2浓度升高对斜生栅藻生长和光合作用的影响. 植物生理学通讯, 2002, 38(5): 431-433. |
| [14] | Gao K S, Aruga Y, Asada K, Ishihara T, Akano T, Kiyohara M.Enhanced growth of the red alga Porphyra yezoensis Ueda in high CO2 concentrations. Journal of Applied Phycology, 1991, 3(4): 355-362. |
| [15] | 贾含帅, 刘汉湖, 胡舒, 周江. 4种环境因子对景观水体绿藻生长繁殖的影响. 中国城市林业,2011, 9(6): 52-54. |
| [16] | 徐海, 秦伯强, 朱广伟. 太湖不同湖区夏季蓝藻生长的营养盐限制研究. 中国环境科学, 2012, 32(12): 2230-2236. |
| [17] | 牛翠娟, 娄安如, 孙儒泳, 李庆芬. 基础生态学(第二版). 北京: 高等教育出版社, 2007: 1-412. |
| [18] | DeMott W R. Foraging strategies and growth inhibition in five daphnids feeding on mixtures of a toxic cyanobacterium and a green algae. Freshwater Biology, 1999, 42(2): 263-274. |
| [19] | Hietala J, Reinikainen M, Walls M. Variation in life history responses ofDaphnia to toxic Microcystis aeruginosa. Journal of Plankton Research, 1995, 17(12): 2307-2318. |
| [20] | 杨州, 孔繁翔. 浮游动物诱发藻类群体的形成. 生态学报, 2005, 25(8): 2083-2089. |
| [21] | Geng H, Xie P, Deng D G, Zhou Q. The rotifer assemblage in a shallow, eutrophic Chinese lake and its relationships with cyanobacterial blooms and crustacean zooplankton. Journal of Freshwater Ecology, 2005, 20(1): 93-100. |
| [22] | Burkhardt S, Zondervan I, Riebesell U. Effect of CO2 concentration on C:N:P ratio in marine phytoplankton: A species comparison. Limnology and Oceanography, 1999, 44(3): 683-690. |
| [23] | Verschoor A M,van Dijk M A, Huisman J, van Donk E. Elevated CO2 concentrations affect the elemental stoichiometry and species composition of an experimental phytoplankton community. Freshwater Biology, 2013, 58(3): 597-611. |
| [24] | Sterner R W, Andersen T, Elser J J, Hessen D O, Hood J M, Urabe J, McCauley E. Scale-dependent carbon: nitrogen:phosphorus seston stoichiometry in marine and freshwaters. Limnology and Oceanography, 2008, 53(3): 1169-1180. |
 2016, Vol. 36
2016, Vol. 36




