文章信息
- 郭凯, 赵文, 董双林, 姜志强
- GUO Kai, ZHAO Wen, DONG Shuanglin, JIANG Zhiqiang
- “海蜇-缢蛏-牙鲆-对虾”混养池塘悬浮颗粒物结构及其有机碳库储量
- Structure of suspended particles andorganic carbon storage in jellyfish-shellfish-fish-prawn polyculture ponds
- 生态学报, 2016, 36(7): 1872-1880
- Acta Ecologica Sinica, 2016, 36(7): 1872-1880
- http://dx.doi.org/10.5846/stxb201409101785
-
文章历史
- 收稿日期: 2014-09-10
- 网络出版日期: 2015-08-05
2. 大连海洋大学辽宁省水生生物学重点实验室, 大连 116023
2. Key Laboratory of Hydrobiology in Liaoning Province, Dalian Ocean University, Dalian 116023, China
悬浮颗粒物是养殖水域生态系统中重要的生态因子之一,其含量及结构会对养殖水环境及生物群落产生一定的影响[1]。水体中悬浮颗粒物包括无机悬浮颗粒物和有机悬浮颗粒物两部分,其中有机颗粒物包括浮游植物、浮游动物、浮游细菌及腐质等,它们都是水生动物重要的饵料资源,对养殖生态系统的物质循环和能量流动具有重要作用,而无机悬浮颗粒物主要为泥、沙等物质,其含量多少会对贝类、海蜇等滤食性动物的摄食生理产生直接影响,直接关系到养殖产量[2]。有机碳是水体有机物质的重要表征,对水体悬浮颗粒物结构及其有机碳的分布进行研究,对深入了解和掌握水域生态系统的结构和功能具有重要意义[1],因此,对水体中悬浮颗粒物结构及其有机碳储量的研究已引起了国内、外学者的广泛关注[3, 4, 5, 6, 7, 8, 9, 10, 11]。
目前,有关养殖池塘悬浮颗粒物的研究已有相关报道。赵文等分别对轮虫培育池塘、盐碱池塘及刺参养殖池塘的悬浮颗粒物结构进行了研究[12, 13, 14];郭赣林等和杨建雷等分别对淡水养鱼池塘的悬浮颗粒物结构进行了研究[15, 16];刘国才等对对虾养殖池塘的悬浮颗粒物进行了研究[17],但对“海蜇-缢蛏-牙鲆-对虾”多元混养池塘悬浮颗粒物的研究未见报道。“海蜇-缢蛏-牙鲆-对虾”混养是辽宁丹东东港市近年来普遍施行的一种养殖方式,在该种混养模式养殖对象中海蜇是浮游生活的滤食性动物,牙鲆属于底层肉食性鱼类,缢蛏是底栖滤食性贝类,对虾是杂食性甲壳动物,因此,该种混养模式属于典型的多营养层级立体养殖模式。本文选取了两个该种混养模式的池塘作为研究对象,与其他养殖模式进行了比较,旨在阐明该种混养模式下水体中悬浮颗粒物的结构及其有机碳分布特征,并为池塘科学养殖及水质管理提供基础数据,为深入研究不同养殖模式的碳循环特点和探讨低碳渔业提供参考。
1 材料与方法 1.1 实验池塘概况于2013年5—10月对辽宁丹东东港市(N 39°51′; E 124°09′)两个“海蜇-缢蛏-牙鲆-中国对虾”混养池塘的悬浮颗粒物及其有机碳储量进行了研究。两个实验池塘(1#和2#)的面积分别为6hm2和8.53 hm2,水深为1.6—2.0m,每月换水两次,月换水量约30cm。实验期间,水温16.0—28.5℃,pH7.0—8.5,透明度0.40—0.90m,盐度14.5—27.0;溶解氧DO 3.79—11.06mg/L。日常投喂经过切碎的饵料鱼(玉筋鱼)、磨碎的虾汁、人工配合饲料及肥水产品(主要成分为氨基酸、微量元素等),池塘的放养及投饵情况见表 1。
| 生物Organisms | 饵料Feed | ||||
| 种类 Species |
放养密度/(个/hm
2)
Stocked density |
种类
Kinds |
投饵量/(kg hm
-2 a
-1)
Feed given |
||
| 1 # | 2 # | 1 # | 2 # | ||
| 表示未投喂 | |||||
| 海蜇 Rhopilema esculentum | 2.80×10 3 | 1.51×10 3 | 饵料鱼Bait fish | 6533 | 11489 |
| 缢蛏 Sinonova culaconstricta | 9.68×10 5 | 1.15×10 6 | 人工饵料Formula feed | 867 | - |
| 牙鲆 Paralichthys olivaceus | 1.08×10 3 | 1.52×10 3 | 肥水饵料Fertilizer products | 167 | - |
| 中国对虾 Penaeus chinensis | 8.00×10 4 | 5.63×10 4 | 鱼粉、豆粉Fishmeal, legume flour | 933 | 47 |
| 虾汁Shrimp sauce | 658 | 2345 | |||
实验期间,共采样8次,采样的具体时间及天气情况示于表 2。每个实验池塘设置3个采样点采集混合样品,用5L的水生-80型采水器采集池塘的有机碳及悬浮颗粒物样品、浮游植物及小型动物样品各1L,浮游植物样品用10‰—15‰的鲁哥氏液进行固定,经过沉淀、浓缩后在显微镜下进行种类鉴定及计数定量;浮游动物样品采集50L水,并经过25#浮游生物网过滤(孔径64μm),获得的浮游动物样品加入5%甲醛固定,在显微镜下进行种类鉴定及计数定量,具体操作按照《水生生物学》进行[18]。浮游细菌的样品采集水样100mL,置于预先经过75%的乙醇消毒处理后的塑料瓶子中,加入2%—3%的无颗粒甲醛进行固定,实验室内利用荧光显微计数法(AODC)进行定量[19],并在镜下测量细菌的粒径大小,计算出细菌的平均体积。
| 日期Date | 温度/℃ Temperature | 天气 Weather | 风向 Wind direction | 风速 Wind speed levels |
| 05-21 | 13—19 | 晴间多云 | 南 | 3—4 |
| 06-19 | 19—29 | 晴 | 北 | 微风 |
| 07-06 | 21—29 | 晴 | 南 | 微风 |
| 07-22 | 21—28 | 多云 | 北 | 微风 |
| 08-09 | 23—29 | 晴间多云 | 南 | 微风 |
| 08-21 | 19—28 | 阵雨转多云 | 南 | 微风 |
| 09-04 | 14—25 | 晴 | 北 | 微风 |
| 10-22 | 10—19 | 晴间多云 | 北 | 微风 |
将一定体积的水样过滤在两张经过处理的直径为25mm,孔径为0.2μm的Whatman GF/F玻璃纤维滤膜上(450℃,灼烧2h),同时将1张新膜(经过预处理)在滤液里浸泡作为对照(目的是校正滤过过程中滤膜吸收的溶解有机碳),即3张滤膜,用浓盐酸熏蒸15—30min,然后置于烘箱中烘干(60℃,24h)[20],用日本岛津公司生产的总有机碳分析仪(SSM-5000A)测定POC含量;DOC采用经过0.2μm的Whatman GF/F玻璃纤维滤膜过滤后的水样利用有机碳分析仪直接进行测定。
1.2.3 总悬浮颗粒物及其有机质含量将一定体积的水样过滤在经过预先处理过的直径为25mm,孔径为0.2μm的Whatman GF/F玻璃纤维滤膜上(450℃灼烧2h,并称重),在60℃下烘干24h后称重,再将烘干样品在550℃下灼烧2h后再称重。根据空白滤膜重(W0)、样品滤膜烘干重(W60)、灼烧减重(W550)及过滤水样体积(V)计算水样中悬浮颗粒物(TPM)及有机物的含量(POM)[17]:
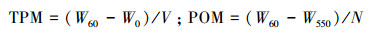
采用Excel软件对实验数据进行处理,并以mean±S.D. 形式表示。按照浮游生物生物量(湿重)的1/7换算浮游生物干重[21];浮游生物碳可由浮游生物的干重乘以系数0.40换算[10, 11, 22, 23, 24]。用有机悬浮颗粒物含量减去浮游生物干重即可得到腐质和浮游细菌量;浮游细菌的体积经过镜下观察测得,细菌的生物量以5.6×10-13g/μm3进行换算(以碳表示)[22];浮游细菌的干重按照系数0.10换算[19, 25]。
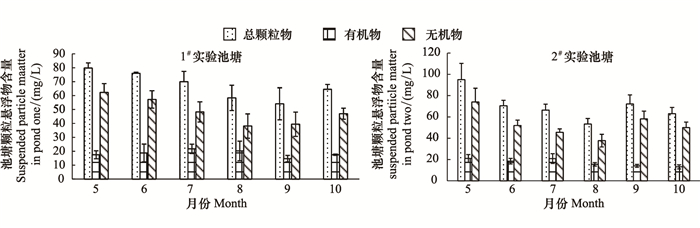
2 结果 2.1 总颗粒悬浮物含量、构成及其季节变化实验池塘颗粒悬浮物含量、构成及其季节变化示于图 1。由图 1可见,1#池塘总悬浮颗粒物含量变动于(54.11—79.75)mg/L之间,平均为(67.12±6.03)mg/L;无机悬浮颗粒物含量变动于(38.13—62.26)mg/L之间,平均为(48.72±7.38)mg/L;有机悬浮颗粒物含量变动于(14.70—21.75)mg/L之间,平均为(18.41±3.75)mg/L。2#池塘总悬浮颗粒物含量变动于(53.25—95.00)mg/L,平均为(70.05±7.63)mg/L;无机悬浮颗粒物含量变动于(37.75—74.00)mg/L,平均为(52.88±6.64)mg/L;有机悬浮颗粒物含量变动于(13.12—21.00)mg/L;平均为(17.17±2.64)mg/L。整体上,两个池塘的总悬浮颗粒物含量都在5、6月份相对较高。1#和2#池塘有机悬浮颗粒物占总悬浮颗粒物的比例分别为27.42%和24.51%,无机物与有机物的比例分别为2.65:1和3.08:1。
|
| 图 1 实验池塘颗粒悬浮物含量、构成及其季节变化 Fig.1 Concentration, structure and seasonal dynamic of suspended particle matter in experimental ponds |
实验池塘浮游生物干重、组成及其季节变化总结于图 2。从图 2可见,1#池塘浮游植物干重变化于(0.038—0.205)mg/L之间,平均为(0.103±0.027)mg/L;浮游动物干重变化于(0.002—0.438)mg/L之间,平均为(0.082±0.036)mg/L;浮游生物总干重变化于为(0.052—0.642)mg/L之间,平均为(0.184±0.231)mg/L;浮游植物干重占浮游生物总量的55.83%;浮游动物干重占浮游生物总量的44.17%。2#池塘浮游植物干重变化于(0.042—0.213)mg/L之间,平均为(0.153±0.040)mg/L;浮游动物干重变化于(0.000—0.289)mg/L之间,平均为(0.064±0.025)mg/L;浮游生物总干重变化于为(0.048—0.428)mg/L之间,平均为(0.217±0.136)mg/L;浮游植物干重占浮游生物总量的70.54%;浮游动物干重占浮游生物总量的29.46%。整体上,浮游生物干重的月变化较大,两个池塘中的浮游生物干重分别占有机悬浮颗粒物的1.02%及1.26%。

|
| 图 2 实验池塘浮游生物干重、组成及其季节变化 Fig.2 Dry weight,structureand seasonal dynamic of plankton in experimental ponds |
实验池塘腐质及浮游细菌含量及其季节变化示于图 3。由图 3可见,1#池塘腐质和浮游细菌含量变动于(14.62—21.54)mg/L之间,平均为(18.22±2.47)mg/L,占有机悬浮颗粒物的98.99%。2#池塘腐质和浮游细菌含量变动于(12.89—20.70)mg/L之间,平均为(16.95±3.39)mg/L,占有机悬浮颗粒悬浮物的98.72%。

|
| 图 3 实验池塘腐质及浮游细菌含量及其季节变化 Fig.3 The concentration and seasonal dynamic of particle detritus and bacteria 1#,实验池塘1 experimental pond one; 2#, 实验池塘2 experimental pond two |
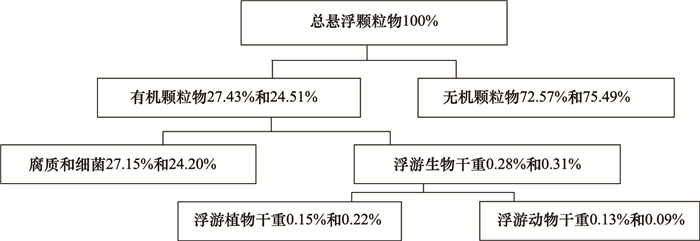
通过以上的研究结果,可以得出两个实验池塘的总悬浮颗粒物组成上以无机悬浮颗粒物为主,而腐质和浮游细菌则是有机悬浮颗粒物的主要组成部分(图 4)。
|
| 图 4 实验池塘悬浮颗粒物结构 Fig.4 Structure of suspended particles matter in experimental ponds |
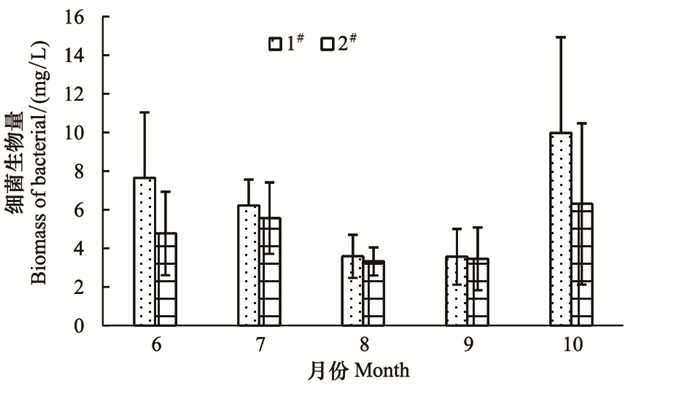
1#池塘浮游细菌密度变动于(1.24—4.54)×107个/mL之间,平均为(2.65±1.21)×107个/mL;2#浮游细菌密度变动于(1.43—3.04)×107 个/mL之间,平均为(2.10±0.64)×107 个/mL。浮游细菌的体积经过镜下观察测得平均体积为0.3925μm3/个,细菌的生物量换算系数为5.6×10-13g/μm(以碳表示)[21],通过计算得到浮游细菌的生物量(图 5)。由图 5可见,1#池塘的浮游细菌生物量变化于(2.72—9.97)mg/L之间,平均为(5.82±2.10)mg/L;2#池塘的浮游细菌生物量变化于(3.15—6.69)mg/L之间,平均为(4.61±1.87)mg/L。
|
| 图 5 实验池塘浮游细菌的生物量 Fig.5 The biomass of bacterial in experimental ponds |
实验池塘有机碳含量及其季节变化示于表 3。从表 3可见,1#池塘溶解有机碳(DOC)的变化范围为(4.56—7.59)mg/L,平均为(5.58±1.15)mg/L;颗粒有机碳(POC)的变化范围为(1.23—2.62)mg/L,平均为(1.73±0.51)mg/L;总有机碳(TOC)的变化范围为(6.09—10.21)mg/L,平均为(7.31±1.51)mg/L。2#池塘的溶解有机碳(DOC)的变化范围为(3.61—5.67)mg/L,平均为(4.53±0.81)mg/L;颗粒有机碳(POC)的变化范围为(1.41—3.01)mg/L,平均为(1.89±0.60)mg/L;总有机碳(TOC)的变化范围为(5.11—8.28)mg/L,平均为(6.42±1.31)mg/L。
|
月份 Month | 实验池塘1 experimental pond one | 实验池塘2 experimental two | ||||
|
颗粒有机碳 Particles organic carbon(POC)/ (mg/L) |
溶解有机碳 Dissolved organic carbon(DOC)/ (mg/L) |
总有机碳 Total organic carbon(TOC)/ (mg/L) |
颗粒有机碳 Particles organic carbon(POC)/ (mg/L) |
溶解有机碳 Dissolved organic carbon(DOC)/ (mg/L) |
总有机碳 Total organic carbon(TOC)/ (mg/L) | |
| 5 | 2.62±0.38 | 7.59±2.86 | 10.21±3.20 | 3.01±0.50 | 5.27±0.27 | 8.28±0.24 |
| 6 | 1.23±0.52 | 6.22±1.77 | 7.45±1.64 | 1.99±0.26 | 5.67±0.60 | 7.66±0.70 |
| 7 | 1.25±0.20 | 4.84±0.82 | 6.09±0.78 | 1.93±0.56 | 4.53±0.63 | 6.46±0.86 |
| 8 | 1.67±0.24 | 4.80±0.51 | 6.47±0.64 | 1.50±0.30 | 4.29±0.67 | 5.79±0.90 |
| 9 | 1.77±0.36 | 5.48±1.65 | 7.24±1.76 | 1.50±0.13 | 3.61±0.17 | 5.11±0.27 |
| 10 | 1.86±0.11 | 4.56±0.03 | 6.42±0.14 | 1.41±0.17 | 3.82±0.23 | 5.23±0.52 |
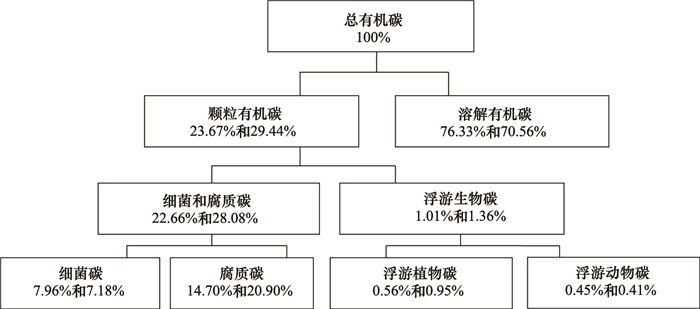
POC包括浮游动、植物碳、腐质及浮游细菌碳等。经计算得知,两个实验池塘中,溶解有机碳(DOC)是总有机碳(TOC)的主要组成部分,而细菌和腐质碳是颗粒有机碳的主要组成部分,其中腐质碳>细菌碳>浮游植物碳>浮游动物碳(图 6)。
|
| 图 6 实验池塘中有机碳的组成 Fig.6 Composition of organic carbon in experimental ponds |
研究表明,养殖水体中悬浮颗粒物含量及其组成因养殖模式及区域而异。本文测得的两个“海蜇-缢蛏-牙鲆-对虾”混养池塘的悬浮颗粒物平均含量基本接近,但明显高于轮虫培育池塘[12]、盐碱养鱼池塘[13]和淡水养鱼池塘[15],总体上与刺参、对虾养殖池塘相近[14, 17]。比较而言,该种养殖模式下,池塘的有机悬浮颗粒物含量却相对较低(表 4)。产生这种现象的原因主要是因为实验池塘位于辽宁丹东东港沿海地区,该地区近邻鸭绿江及大洋河,属于河口区域,同时拥有天然的滩涂资源,池塘及近海底质以泥沙为主,加之风力、养殖动物的搅动等因素的影响下,颗粒沉积物发生再悬浮现象,往往导致池塘颗粒悬浮物中泥沙等无机颗粒物含量相对较高。两个池塘的悬浮颗粒物含量均5月份最高,而其他月份相对较低,产生这种现象的原因与样品采集时当地的气候条件有关,由于养殖池塘水较浅,在5月份时该地区的风浪较大,因此,颗粒沉积物在风力的作用下很容易产生再悬浮现象,导致水中悬浮颗粒物含量增加。已有研究表明,较高浓度的悬浮颗粒物会对滤食性贝类的摄食生理产生影响[2],因此,在养殖过程中应加强对水中悬浮颗粒物的监测和管理,尤其是泥沙等无机颗粒物,建议对养殖池塘周边环境进行改造,如土坝上加设塑料隔膜,并在坝上种植固土的植物等,换水时尽量减少大量泥沙的进入。
|
养殖模式 Culture model |
总悬浮颗粒物 Total suspended particle matter/ (mg/L) |
有机颗粒物 Organic suspended particle matter/% |
无机颗粒物 Inorganic suspended particle matter/% |
浮游生物干重 Total dry weight of plankton/% |
浮游植物干重/ 浮游动物干重 Dry weight of phytoplankton/ Dry weight of zooplankton |
腐质和细菌 Detritus and bacteria/% |
参考文献 References |
|
轮虫培育池塘 Rotifer-cultured pond | 11.50 | 66.80 | 33.20 | 35.80 | 5.75 | 31.00 | [12] |
|
盐碱养鱼池塘 Fish- cultured saline-alkaline pond | 15.53 | 57.62 | 42.38 | 12.00 | 0.25 | [13] | |
|
刺参养殖池塘 Sea cucumber-cultured pond | 73.10 | 30.87 | 69.13 | 0.92 | 4.11 | 29.95 | [14] |
|
淡水养鱼池塘 Fish- cultured fresh water pond | 37.53 | 67.00 | 33.00 | 25.05 | 16.30 | 41.94 | [15] |
|
对虾养殖池塘 Shrimp- cultured pond | 72.26 | 62.00 | 38.00 | 1.24 | 4.50 | 60.76 | [17] |
|
多元混养池塘 Polyculture pond | 68.59 | 26.00 | 74.00 | 0.30 | 2.00 | 25.70 | [本文] |
| 表示未统计 | |||||||
对于同一地域、相同的养殖模式下,不同池塘的水体悬浮颗粒物结构也存在一定的区别。本文中两个实验池塘的悬浮颗粒物含量虽然较为接近,但相比之下2#池塘要略高于1#池塘,而有机颗粒物含量则是1#池塘要高于2#池塘,这主要是由于不同池塘之间养殖生物的放养量、投饵种类及数量等生产管理方法不同。如1#池塘放养的海蜇数量要高于2#池塘,但牙鲆放养量要低于2#池塘,因此,2#池塘受到底层鱼类搅动的影响较大。养殖动物放养量的不同就会造成生产过程中投放饵料的种类及数量会有一定的区别,从饵料投放种类及数量可以看出,1#池塘的小颗粒的饵料投放量要明显高于2#池塘,而相对颗粒较大、不能在水中长时间悬浮的饵料鱼的投喂量相对较低,因此,1#池塘悬浮颗粒物中有机物所占比例要高于2#池塘。
很多研究表明,水体有机悬浮颗粒物中腐质及细菌所占比例相对较高,一般为62.60%—98.00%;而浮游生物干重所占比例相对较小,仅占2.00%—37.40%(其中浮游植物干重要高于浮游动物),腐质链在池塘养殖生态系统的物质循环和能量流动方面起主要作用[14, 15, 17]。本文的研究结果基本符合这一特点,但浮游生物的干重相对较低,这主要是因为水体悬浮颗粒物中大量泥沙的存在使得浮游生物干重所占比例降低,另外,养殖动物对浮游生物的摄食也是主要的影响因素,如海蜇及缢蛏等对浮游生物的滤食强度较大,池塘的浮游生物量偏低,饵料及生物的排泄物等构成了有机颗粒悬浮物的主要组成部分,因此,腐质和浮游细菌占有机颗粒物的比例远高于浮游生物,其中腐质所占比例最大。相比之下,1#池塘中浮游生物干重要略低于2#池塘,这主要也是因为生产管理方法上的差异所造成的,是水环境和生物摄食综合作用的结果。另外,从时间变化看,两个实验池塘的浮游生物干重均在5月时相对较高,而在其他时间相对较低;其中浮游动物干重的时间变化规律较明显,即在养殖初期的5月份浮游动物的干重相对较高,在养殖中期的7、8月份浮游动物的干重相对较低,在养殖后期的9、10月份又开始有升高的现象,产生这种现象的主要原因是养殖刚刚开始的阶段,养殖动物对浮游动物的摄食强度相对较小,随时间的延长养殖生物对浮游动物的摄食强度也会增大,到了养殖后期,随着养殖动物的收获,对浮游动物的摄食强度开始减弱。
3.2 悬浮物中有机碳组成特征水体中的总有机碳(TOC)包括颗粒有机碳(POC)和溶解有机碳(DOC)两部分。多数研究表明,一般水体中的DOC含量往往要高于POC含量,但随着水体富营养水平的升高,DOC/POC值会发生明显变化,如在自然水体中DOC/POC值可达6:1—23:1,而在淡水养殖池塘DOC/POC值可达1:1,说明DOC/POC值与水体营养水平呈正相关[20]。产生这种现象的原因主要是因为水体中营养物质的增加会导致浮游生物量上升,从而使POC含量增大,而DOC由于其周转率高,含量相对较稳定,所以DOC/POC值不断降低[13]。本文的研究结果表明,DOC/POC为2.80,TOC:DOC:POC为1:0.74:0.26,这与盐碱池塘[13]、刺参[26]及对虾养殖池塘[20]的研究结果基本一致,但高于高产鱼池[27];腐质及浮游细菌碳是颗粒有机碳的主要组成部分,这也与淡水养鱼池塘及刺参养殖池塘研究结果相近[15, 26];但浮游生物碳所占比例相对较低,这主要是由于池塘中浮游生物量低而造成的。另外,按照生态学中能量流动的原理,浮游植物碳一般要高于浮游动物碳,本文的研究结果基本符合这一规律(表 5)。另外,两个实验池塘的总有机碳(TOC)、溶解有机碳(DOC)及颗粒有机碳(POC)含量与悬浮颗粒物具有相同的时间变化规律,均为5、6月份时含量相对较高,这是天气、养殖动物的摄食及人工投饵综合作用的结果。
|
养殖模式 Culture model |
总有机碳 Total organic carbon (TOC)/ (mg/L) |
溶解有机碳 Dissolved organic carbon (DOC)/ % |
颗粒有机碳 Particles organic carbon (POC)/ % |
溶解有机碳/ 颗粒有机碳 Dissolved organic carbon/Particlesorganic carbon(DOC/POC) |
总有机碳/溶解 有机碳/颗粒有机碳 Total organic carbon/Dissolved organic carbon/Particles organic carbon (TOC/DOC/POC) |
腐质和细菌碳 Dissolved organic carbon/Particles organic carbon/ % |
浮游 生物碳 Plankton carbon/ % |
浮游 植物碳 Phytoplankton carbon/ % |
浮游 动物碳 Zooplankton carbon/ % |
浮游植物碳/ 浮游动物碳 Phytoplankton carbon/Zooplankton carbon |
参考文献 References |
|
养鱼池塘 Fish pond | 7.36 | 73.00 | 27.00 | 2.76 | 1:0.73:0.27 | 18.00 | 9.00 | 2.00 | 7.00 | 0.29 | [13] |
|
养鱼池塘 Fish pond | 20.07 | 56.00 | 44.00 | 1.29 | 1:0.56:0.44 | 27.00 | 17.00 | 16.00 | 1.00 | 16.00 | [15] |
|
刺参养殖池塘 Sea cucumber pond | 6.99 | 68.00 | 32.00 | 2.13 | 1:0.68:0.32 | 25.50 | 6.50 | 5.20 | 1.30 | 4.27 | [26] |
|
对虾养殖池塘 Shrimp pond | 13.05 | 76.00 | 24.00 | 3.17 | 1:0.76:0.24 | [20] | |||||
|
多元养殖池塘 Polyculture pond | 6.87 | 73.65 | 26.35 | 2.80 | 1:0.74:0.26 | 25.19 | 1.16 | 0.74 | 0.42 | 1.80 | [本文] |
| 表示未统计 | |||||||||||
“海蜇-缢蛏-牙鲆-对虾”混养模式下两个实验池塘的总悬浮颗粒物含量相对较高,其中泥沙等无机悬浮颗粒物是主要的组成部分;有机悬浮颗粒物中,浮游生物所占比例相对较小,腐质和细菌是有机悬浮颗粒物主要的组成部分;颗粒有机碳中,浮游生物碳所占比例较小,腐质和细菌碳是颗粒有机碳主要的组成部分,说明腐质链在该种养殖生态系统的物质循环和能量流动中起主要作用。
| [1] | 赵文. 养殖水域生态学. 北京: 中国农业出版社, 2011. |
| [2] | 宋强, 方建光, 刘慧, 张继红, 王玲玲, 王巍. 沉积再悬浮颗粒物对3种滤食性贝类摄食生理的影响. 海洋水产研究, 2006, 27(4): 21-28. |
| [3] | Burns N M, Rosa F. In situ measurement of the settling velocity of organic carbon particles and 10 species of phytoplankton. Limnology and Oceanography, 1980, 25(5): 855-864. |
| [4] | Gasith A. Tripton sedimentation in eutrophic lakes: Simple correction for the resuspended matter.Verhandlungen des InternationalenVereinLimnologie, 1975, 19: 116-122. |
| [5] | Hessen D O,Andersen T,Lyehe A. Carbon metabolism in a humic lake: Pool sires and cycling through zooplankton. Limnology and Oceanography, 1990, 35(1): 84-89. |
| [6] | Jones J R, Knowlton M F. Suspended solids in Missouri reservoirs in relation to catchment features and internal processes. Water Research, 2005, 39(15): 3629-3635. |
| [7] | 孙作庆, 杨鹤鸣. 胶州湾海水中颗粒有机碳含量的分布与变化. 海洋科学, 1992, (2): 52-55. |
| [8] | 陈金斯, 李飞永, 洪华生. 珠江口悬浮颗粒物质研究Ⅱ. 有机碳和氮的来源、分布和转移. 热带海洋, 1988, 7(3): 90-97. |
| [9] | 常秀岭, 刘家寿, 胡传林, 彭建华, 俞伏虎. 湖北浮桥水库悬浮物季节变化. 湖泊科学, 2010, 22(2): 300-306. |
| [10] | 谢平. 武汉东湖颗粒悬浮物的结构与元素组成. 水生生物学报, 1996, 20(3): 197-204. |
| [11] | 林婉莲, 刘鑫洲. 武汉东湖生态系中浮游物的营养结构. 海洋与湖沼, 1990, 21(5): 411-417. |
| [12] | 赵文, 李晓东, 赵振兴, 刘青. 轮虫培育池生态系统颗粒悬浮物的研究. 应用生态学报, 2004, 15(2): 313-315. |
| [13] | 赵文, 董双林, 李德尚, 张兆琪. 盐碱池塘围隔生态系统的悬浮物结构及有机碳库储量. 生态学报, 2002, 22(12): 2133-2140. |
| [14] | 赵文, 张义伟, 魏杰, 于晓辉. 刺参养殖池塘颗粒悬浮物结构及其沉积作用. 生态学报, 2009, 29(11): 5749-5757. |
| [15] | 郭赣林, 赵文. 淡水鱼池生态系统的悬浮物结构及有机碳库储量. 大连水产学院学报, 2006, 21(2): 127-130. |
| [16] | 杨建雷, 高勤峰, 董双林, 王芳, 田相利. 草鱼、鲢鱼和鲤鱼混养池塘中浮游生物和悬浮颗粒物组成变化的研究. 中国海洋大学学报, 2011, 41(10): 23-29. |
| [17] | 刘国才, 李德尚, 卢静, 陈兆波, 董双林. 对虾养殖围隔生态系颗粒悬浮物的研究. 应用生态学报, 1999, 10(3): 350-352. |
| [18] | 赵文. 水生生物学. 北京: 中国农业出版社, 2005. |
| [19] | Hobble J E, Daley R J, Jasper S. Use of nuclepore filters for counting bacteria by fluorescence microscopy. Applied and Environment Microbiology, 1997, 33(5): 1225-1228. |
| [20] | 刘国才, 李德尚, 董双林, 陈兆波. 对虾养殖生态系有机质含量及其不同测定方法的数值比较. 海洋通报, 1999, 18(4): 50-54. |
| [21] | 何志辉. 吉林镇贲养鱼场鱼池生态系的分析. 水产学报, 1993, 17(1): 24-35. |
| [22] | Bratbak G. Bacterial biovolume and biomass estimations. Applied and Environment Microbiology, 1965, 49(6): 1488-1493. |
| [23] | Omori M. Weight and Chemical composition of some important oceanic zooplankton in the North Pacific Ocean. Marine Biology, 1969, 3(1): 4-10. |
| [24] | Hirota R. Dry weight and chemical composition of the important zooplankton in the setonaikai (Inland sea of Japan). Bulletin of the Plankton Society of Japan, 1981, 28: 19-24. |
| [25] | Hecky R E, Kling H J. The phytoplankton and protozooplankton of the euphotic zone of Lake Tanganyika: species composition, biomass, chlorophyll content, and spation-temporal distribution. Limnology and Oceanography, 1981, 26(3): 548-564. |
| [26] | 赵文. 刺参池塘养殖生态学及健康养殖理论. 北京: 科学出版社, 2009. |
| [27] | 雷衍之, 于淑敏, 徐捷. 无锡市河埒口高产鱼池水质研究Ⅰ: 水化学和初级生产力. 水产学报, 1983, 7(3): 185-198. |
 2016, Vol. 36
2016, Vol. 36




