文章信息
- 曾令清, 付世建, 曹振东
- ZENG Lingqing, FU Shijian, CAO Zhendong
- 鲫幼鱼(Carassius auratus)标准代谢个体差异与力竭后代谢特征及行为的关联
- Correlations between standard metabolic rate and metabolic characteristics after exhaustive exercise, and behavior in the juvenile crucian carp (Carassius auratus)
- 生态学报, 2016, 36(6): 1746-1755
- Acta Ecologica Sinica, 2016, 36(6): 1746-1755
- http://dx.doi.org/10.5846/stxb201408251683
-
文章历史
- 收稿日期: 2014-08-25
- 网络出版日期: 2015-07-29
稳定个体差异(CIDs)是自然界普遍存在的现象,它是指动物表型特征(如形态、生理和行为)存在个体差异并且这种差异在一段时间内保持稳定,即表型特征可重复测量[1, 2]。能量代谢是动物生理功能维持和行为特征展现的内在基础,多以动物个体的耗氧率(MO2)表征,常见参数包括标准代谢率(SMR)、最大代谢率(MMR)和代谢空间(AS=MMR-SMR)和相对代谢空间(FAS=MMR/SMR)等。由于SMR是评价动物生活史的重要参数之一,多数研究以标准代谢率的个体差异作为研究起点[3, 4, 5],因为SMR的高低在一定程度上影响动物其它机体生理功能(如生长、运动、繁殖)的水平[2, 3]。早期研究主要聚焦于小型哺乳类、两栖爬行类和鸟类等脊椎动物[3],而近期鱼类的相关研究也逐渐引起研究者的广泛关注[3, 4, 5]。考察动物SMR的个体差异对其它生理功能影响的研究包括诸多方面,其中与MMR、AS等指标的关联受到广泛关注[6, 7, 8],上述相关参数可通过动物力竭运动后的代谢恢复(如EPOC)获得。动物的个性行为(Animal personality)包括勇敢性(Boldness)、好斗性(Aggression)、探索性(Exploration)、活跃性(Activity)和群集性(Sociability)等指标[1, 2, 9]。个性行为的产生和改变是动物体内生理过程的整体反映,也是对栖息环境变化的适应性表现,常与能量消耗密切相关[1]。因此,动物个性行为的个体差异可能存在能量学机制[1, 2]。动物体内能量的有效补充需要通过外界食物获取而得到满足,而食物获取常与动物的运动能力和捕食能力密切相关,并且运动能力(如捕食或反捕食能力)可能影响动物个体的存活率[5]。快速启动(Fast-start)是鱼类的另外一种主要以无氧代谢供能的运动行为,其持续时间通常少于1 s,在其捕食与逃避敌害等方面均具有重要的生态学意义[10, 11, 12]。鱼类快速启动能力的评价参数包括反应时间(RT)、最大游泳速度(Umax)、最大加速度(Amax)、单位时间质心移动距离等[10]。与其它表型特征一样,鱼类的快速启动能力也存在明显的个体差异[5]。那么,鲫幼鱼SMR的个体差异是否与其它能量代谢指标存在普遍关联,而与哪些指标之间的关联更为紧密是一个研究人员普遍关注的科学问题;另外,实验鱼SMR的个体差异是否还与其运动行为、个性行为具有某种联系也值得关注。
鲫(Carassius auratus)是一种广泛分布在温带水域的杂食性鱼类,适应能力强。该鱼不仅是一种常见经济养殖鱼类,而且也是常用于基础研究的实验对象[13, 14]。至今,该种鱼能量代谢与个性行为和运动行为之间的关联研究尚未见报道。为回答上述有关科学问题,本研究以鲫幼鱼为实验对象,考察该种鱼的能量代谢特征(SMR、MMR、AS和FAS)、个性行为(勇敢性和活跃性)和运动行为(快速启动)的个体差异,分析能量代谢与个性行为、运动行为的内在关联,为鱼类生理功能、个性行为与能量代谢之间关联的研究提供基础资料。
1 材料和方法 1.1 实验鱼来源及其驯化实验鱼来源于重庆市当地人工养殖基地,购回后将鱼置于实验室循环控温水槽(1.2 m × 0.55 m × 0.55 m)驯养2周。驯化期间,每天以人工颗粒浮性饵料(通威公司)饱足投喂两次(9:00、21:00),投饵30 min后用虹吸管清除残饵和粪便。水槽用水为曝气4 d后的自来水,日换水量约10%。用充气泵不停向水体充入空气使溶氧水平大于7 mg/L,水温控制在(25.0±0.5)℃,光周期为12 L: 10 D。
1.2 实验设计驯养结束,挑选大小相近、体格健壮的80尾鲫[体重为(13.39±0.16)g,体长为(8.08±0.05)cm,n=80]并禁食24 h。随后将鱼转移至流水式代谢仪中的呼吸室驯化24 h。隔天用溶氧仪测定单尾鱼的耗氧率以表征其标准代谢率(SMR),筛选高SMR个体和低SMR个体各20尾。SMR筛选标准:先获得单尾鱼在7个时间点(09:00,11:00,13:00,15:00,17:00,19:00,21:00)SMR的平均值,并计算每尾鱼SMR的变异系数(Coefficient of variation,CV=标准差/平均值),再对实验鱼SMR排序;在高(或低)SMR个体中挑选CV较小的实验鱼作为高SMR个体,反之亦然。将筛选出来实验鱼(n=40)放入鱼类运动力竭装置的环形水道中追赶至力竭,随后将鱼迅速转移至呼吸室内并进行为期30 min的恢复代谢测定。测定结束后将鱼转移至多单元格循环水槽中的单元格单独驯养2 d。在此期间,饵料类型和投喂制度均与驯养期间一致。最后分别测定单尾鱼的运动行为(快速启动)和个性行为(勇敢性、活跃性)。在能量代谢测定之后,由于个别实验鱼较为胆小而跳出驯化单元格,这些鱼将不再参与后续的实验测定。在本研究中该种鱼的快速启动和个性行为分析的实际样本量分别为39和38。
1.3 实验方法与参数计算 1.3.1 能量代谢(1)SMR
在呼吸室驯化结束后,用溶氧仪(HQ30d,Hach Company,Loveland,USA)于当天7个时间点分别测定单尾鱼的SMR。呼吸室水流速度介于80—100 mL/min,该流速可使呼吸室进水口与出水口的溶氧差值大于0.5 mg/L,但未造成轻度低氧环境。呼吸代谢仪的环境条件(水温、溶氧、光照)均与实验鱼驯养期间相同。SMR的计算公式如下:

(2)MMR、AS与EPOC
在本研究中,通过人工追赶高流速水体中实验鱼的方式可诱导其MMR(mg O2 h-1 kg-1),并计算实验鱼的AS(MMR-SMR)和FAS(MMR/SMR)。将实验鱼从呼吸室取出至鱼类运动力竭装置(Φ外=56 cm,Φ内=33 cm,水深15 cm)的环形水道(流速为60 cm/s)中;在环形水道中实验鱼逆流游泳,鱼体因较高的水体流速而不能保持稳定游泳运动而向后退,此时人工连续驱赶实验鱼直至其运动力竭;处于运动力竭状态的鱼通常失去平衡且用手继续追逐时不再有明显应激反应,整个过程一般在5 min之内完成[13, 14, 15, 16];随后将实验鱼迅速(10 s内完成)转移至呼吸室内进行30 min的恢复代谢测定。数据采集时间分别设定为1、2、3、4、5、6、7、8、9、10、15、20、25、30 min,水流速度约500 mL/min。经计算,在该流水速度下呼吸室的水体置换率99%的历时小于1 min。因此,将第1 min的耗氧率作为单尾鱼的最大代谢率。如果单尾鱼的即刻代谢率低于该鱼120% SMR,那么则可认为单尾鱼的代谢已恢复,该时间称为EPOC恢复历时。EPOC总量(Magnitude of EPOC)是指实验鱼在运动力竭后恢复过程中高于运动前消耗的差值在时间上的总和。
1.3.2 游泳行为鲫的快速启动用高速摄像测定仪完成,该仪器主要包括高速摄像机(德国BASLER公司A504K)、LED矩阵光源、运动水槽(底部刻有1 cm × 1 cm网格线)等组件,水槽四周贴纸以避免环境干扰。该仪器的结构介绍详见相关文献[17],水深为10 cm,水温控制在(25.0±0.5) ℃,溶氧水平大于7 mg/L,光照条件与驯养期间相同。
将鱼在驯化区适应1 h,再将鱼轻轻赶至实验区,当鱼处于静止状态、头朝向区域中心且距离水槽边缘大于1倍体长时,开启高速摄影机(分辨率1024×1024;频率500 fps)同时并进行电刺激(电压20 v,持续时间20 ms),拍摄时间持续1 s,该刺激条件足以引发实验鱼进行快速启动行为。拍摄结束后,将鱼放入相应单元格饲养,第2天重复测定1次以增加数据可靠性。用图像处理软件(ACDsee v8.0)对拍摄的图像进行处理并采用软件(tpsdig2)进行数据分析,再通过计算分别获得单尾鱼的反应时间(RT)、最大线速度(Umax)、最大线加速度(Amax)和120 ms移动距离(S120)。单尾鱼的快速启动参数测量值为两次测定结果的平均值。
1.3.3 个性行为本研究用以评价实验鱼的个性行为指标包括勇敢性和活跃性。将实验鱼转移至个性行为观察装置(60 cm × 30 cm × 30 cm,水深15 cm)的适应区中驯化10 min[9],进行垂直摄像(25 fps),再对所获视频资料定量分析。行为观察装置分3个区域,包括适应区(长20 cm,上方加有不透明的隔板)、实验区(长36 cm,定量分析实验鱼进入该区域的行为指标)和动力区(长4 cm,循环水和充氧)。在适应区与实验区有一隔板并且隔板上安置一个门(10 cm × 10 cm),当门打开之后,实验鱼可随意在适应区和实验区之间来回游动。每一行为学指标重复测定两次并取平均值,以减少实验的偶然性和环境误差。
勇敢性用于评价鱼类在新异环境中的勇敢程度,其参数包括潜伏期(L)、曝露时间(ET)和探头频率(AF)等[9]。其中,潜伏期是指在俯视角度上从视频拍摄开始到实验鱼的吻部首次刚好超过门线的最短时间(s);曝露时间是指实验鱼在实验区的时间总和(s);探头频率是指鱼头部越过门线随后退回适应区的频率(次/ min),即实验鱼未进入实验区。实验鱼的潜伏期越短,曝露时间越长以及探头频率越高,说明该尾鱼的勇敢性越强,反之亦然。驯化结束后,打开隔板的门并连续拍摄10 min,最后对视频进行勇敢性参数定量分析。
活跃性评价鱼类在生存环境中的活跃程度,其参数包括运动时间比(PTM)和撞墙频率(FHW)等[9, 13]。运动时间比是指单位时间鱼体质心移动时间占总时间(10 min)的比例(%),而撞墙频率是指实验鱼吻部触碰实验区内壁的频率(次/min)。实验鱼的运动时间比和撞墙频率越高,说明该尾鱼的活跃性越强,反之亦然。在勇敢性测定完毕后将实验鱼置于实验区驯化1 h,同时关闭隔板的门;驯化结束后,连续拍摄10 min,最后对视频进行活跃性参数定量分析。
1.4 数理统计实验数据采用Excel(2003)进行常规计算,再采用STATISTICA(7.0)和SPSS(19.0)软件进行统计分析。不同SMR组形态参数的差异用T-检验。不同SMR组运动后恢复代谢特征的差异则采用协方差分析(Analysis of covariance)。采用皮尔逊(Pearson)相关分析方法对能量代谢、游泳能力和个性行为的各组分之间相关性,以及SMR与游泳行为和个性行为的相关性进行统计分析。3个指标体系的变异系数比较采用单因素方差分析(One way analysis of variance,ANOVA),若组间存在显著性差异,则进行最小显著差异法(LSD)多重比较。所有统计值均以平均值±标准误表示,显著水平为P<0.05。
2 结果 2.1 鲫幼鱼形态参数和运动后代谢恢复特征高SMR鲫的体重、体长及肥满度均与低SMR组的无显著差异(表 1,P>0.05)。整体上分析,鲫的体重、体长及肥满度分别为(13.54±0.20)g、(8.05±0.07)cm和(2.61±0.06)g/cm3,3个形态指标的变异系数CV分别为6.73%、3.87%和10.49%,其中体长的CV最小,而肥满度的CV最大。
| 组别 Groups | 样本量 Sample numbers n | 标准代谢率/ (mg O2 h-1 kg-1) Stand metabolic rate,SMR | 体重 Body mass | 体长 Body length | 肥满度 Condition factor | |||
| 平均值±标准误 Mean±SE/g | 变异系数 Coefficient of variation, CV/% | 平均值±标准误 Mean±SE/cm | 变异系数 Coefficient of variation, CV/% | 平均值±标准误 Mean±SE/ (g/cm3) | 变异系数 Coefficient of variation, CV/% | |||
| 高标准代谢率组 Higher standard metabolic rate | 20 | 208.9± 6.0 | 13.57± 0.21 | 6.94 | 7.99± 0.07 | 4.02 | 2.67± 0.06 | 10.18 |
| 低标准代谢率组 Lower standard metabolic rate | 20 | 138.2± 4.0 | 13.51± 0.20 | 6.68 | 8.11± 0.07 | 3.66 | 2.55± 0.06 | 10.49 |
| 整体Total | 40 | 173.5± 9.5 | 13.54± 0.20 | 6.73 | 8.05± 0.07 | 3.87 | 2.61± 0.06 | 10.49 |
| T检验 | 7.900 | 0.195 | — | -1.211 | — | 1.300 | — | |
| P | <0.001 | 0.847 | — | 0.241 | — | 0.209 | — | |
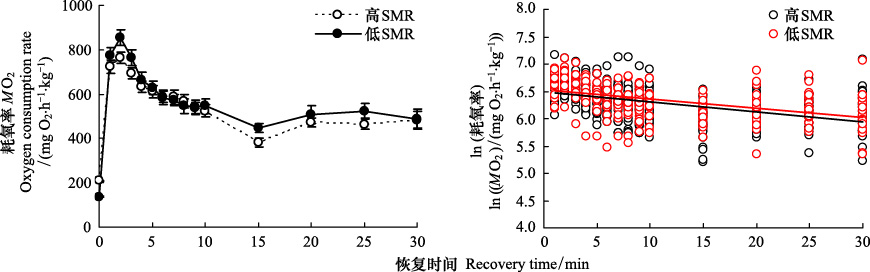
在运动力竭后,高SMR组和低SMR组的代谢水平迅速从SMR上升至MMR,然后在2—10 min快速下降至稳定水平,但该稳定水平(10—30 min)仍然显著高于SMR(图 1,P<0.05)。对恢复代谢数据求对数,高SMR与低SMR的拟合方程分别为Y=-0.0181x+6.479(n=20,r=0.437)和Y=-0.0173x+6.533(n=20,r=0.462)。协方差分析显示高SMR组代谢的恢复速率(斜率)与低SMR的无显著差异(F=0.068,P = 0.795),并且两拟合方程的截距也无明显差异(F=1.792,P=0.267)。
|
| 图1 鲫幼鱼在运动力竭后代谢率的恢复特征 Fig.1 The characteristics of recovery metabolism in the crucian carp |
对于能量代谢而言,鲫的SMR、MMR、AS和EPOC总量的平均值分别为173.5、834.1、660.5 mg O2 h-1 kg-1和178.5 mg O2/kg,变化倍率分别为3.1、2.2、2.9和9.2,变异系数分别为9.5、35.5、39.4和34.3(表 2)。对于快速启动能力而言,鲫的RT、Umax、Amax和S120分别为7.1 s、1.62 m/s、0.24 m/s2和76.1 mm,相应的变化倍率分别为7、3.1、5.7和3.1,相应的变异系数分别为46.2、24.0、40.8和24.8(表 2)。对于个性行为而言,36.8%(n=14)的鲫未穿越门线进入实验区,即潜伏期达到最长600 s;整体上分析,鲫的L、ET、AF、PTM和FHW分别为317.4 s、95.2 s、0.28次/min、71.2%和4.0次/min(表 2),其变异系数分别为81.7、149.9、124.5、39.3和100.3,个性行为的变异系数明显大于能量代谢和快速启动能力,而后两者无显著差异(F=8.694,P=0.006)。
| 指标类型 Type of index | 动物个性 Animal personality | 实验参数 Experimental parameters | 样本量 Sample numbers n | 平均值±标准误 Mean±SE | 最大值 Maximum | 最小值 Minimum | 变化倍率 Variation rate | 变异程度 Degree of variation | |
| 标准差 Standard Deviation | 变异系数 Coefficient of variation, CV/% | ||||||||
| 能量代谢 Energy | 标准代谢率/ (mg O2 h-1 kg-1) | 40 | 173.5±9.5 | 298.2 | 96.2 | 3.1 | 42.3 | 9.5 | |
| metabolism | 最大代谢率/ (mg O2 h-1 kg-1) | 40 | 834.1±35.5 | 1280.5 | 571.9 | 2.2 | 158.6 | 35.5 | |
| 代谢空间/ (mg O2 h-1 kg-1) | 40 | 660.5±39.4 | 1084.9 | 371.0 | 2.9 | 176.4 | 39.4 | ||
| EPOC总量/ (mg O2/kg) | 40 | 178.5±13.7 | 327.5 | 35.7 | 9.2 | 61.2 | 34.3 | ||
| 快速启动 Fast-start | 反应时间/ms | 39 | 7.1±0.7 | 14 | 2 | 7.0 | 3.3 | 46.2 | |
| 最大线速度 /(m/s) | 39 | 1.62±0.09 | 2.57 | 0.83 | 3.1 | 0.39 | 24.0 | ||
| 最大线加速度 /(m/s2) | 39 | 0.24±0.02 | 0.51 | 0.09 | 5.7 | 0.10 | 40.8 | ||
| 120ms移动距离 /mm | 39 | 76.1±4.2 | 114.2 | 36.4 | 3.1 | 18.8 | 24.8 | ||
| 个性行为 Personality | 勇敢性 Boldness | 潜伏期/s | 38 | 317.4±58.0 | 600 | 0 | N/A | 259.4 | 81.7 |
| behaviour | 曝露时间/s | 38 | 95.2±31.9 | 565 | 0 | N/A | 142.8 | 149.9 | |
| 探头频率/ (次/min) | 38 | 0.28±0.08 | 1.5 | 0 | N/A | 0.35 | 124.5 | ||
| 活跃性 Activity | 运动时间比/ % | 38 | 71.2±6.3 | 99 | 8 | 12.4 | 30.0 | 39.3 | |
| 撞墙频率/ (次/min) | 38 | 4.0±0.9 | 18.4 | 0.2 | 92 | 4.0 | 100.3 | ||
| N/A为Not applicable的缩写,表示该栏目不适合 | |||||||||
结果发现,鲫的SMR与AS、FAS、EPOC总量均呈负相关(所有P < 0.05),但与MMR不相关(表 3,P=0.05),MMR与AS、FAS、EPOC总量均呈正相关(所有P < 0.001),AS与FAS和EPOC总量呈正相关(所有P < 0.001),FAS与EPOC总量也呈正相关(P < 0.001)。RT与Umax、Amax、S120均呈负相关(表 3,所有P < 0.01);Umax与Amax和S120呈现正相关(P < 0.01);Amax与S120呈正相关(P=0.026)。PTM与ET和FHW呈正相关(表 3, P < 0.01),但与L、AF不相关(P > 0.05);L与ET、AF呈负相关(P < 0.001),与FHW不相关(P=0.183);ET与AF、FHW呈正相关(P < 0.05),而AF与FHW不相关(P=0.156)。
| 指标类型 Type of index | 相关性结果 Result of correlations | ||||
| 能量代谢 Energy metabolism | 最大代谢率MMR | 代谢空间AS | 相对代谢空间FAS | EPOC总量 | |
| 标准代谢率SMR r P | -0.213 0.050 | -0.520 <0.001 | -0.822 <0.001 | -0.401 0.010 | |
| 最大代谢率MMR r P | 0.974 <0.001 | 0.723 <0.001 | 0.696 <0.001 | ||
| 代谢空间AS r P | 0.847 <0.001 | 0.722 <0.001 | |||
| 相对代谢空间FAS r P | 0.595 <0.001 | ||||
| 快速启动 Fast-start | 最大线速度Umax | 最大线加速度Amax | 120ms移动距离S120 | ||
| 反应时间RT r P | -0.537 <0.001 | -0.493 0.001 | -0.457 0.003 | ||
| 最大线速度Umax r P | 0.779 <0.001 | 0.581 <0.001 | |||
| 最大线加速度Amax r P | 0.356 0.026 | ||||
| 个性行为 AnimalPersonality | 潜伏期 L | 暴露时间 ET | 探头频率 AF | 撞壁频率 FHW | |
| 运动时间比PTM r P | -0.266 0.106 | 0.472 0.003 | 0.246 0.136 | 0.526 <0.001 | |
| 潜伏期L r P | -0.610 <0.001 | -0.664 <0.001 | -0.221 0.183 | ||
| 暴露时间ET r P | 0.370 0.022 | 0.410 0.010 | |||
| 探头频率AF r P | 0.235 0.156 | ||||
| SMR: 标准代谢率Standard metabolic rate; MMR: 最大代谢率Maximum metabolic rate; AS: 代谢空间Metabolic scope; FAS: 相对代谢空间Factorial aerobic scope; EPOC: 过量耗氧Excess post-exercise oxygen consumption; RT: 反应时间Response time; Umax: 最大线速度Maximum linear speed,; Amax: 最大线加速度Maximum linear acceleration speed; S120: 120 ms移动距离Distance during a period of 120 ms; L : 潜伏期Latency; PTM: 运动时间比Percent time spent moving; ET: 曝露时间Exposed time; AF: 探头频率Appearance frequency; FHW: 撞墙频率Frequency of hit wall | |||||
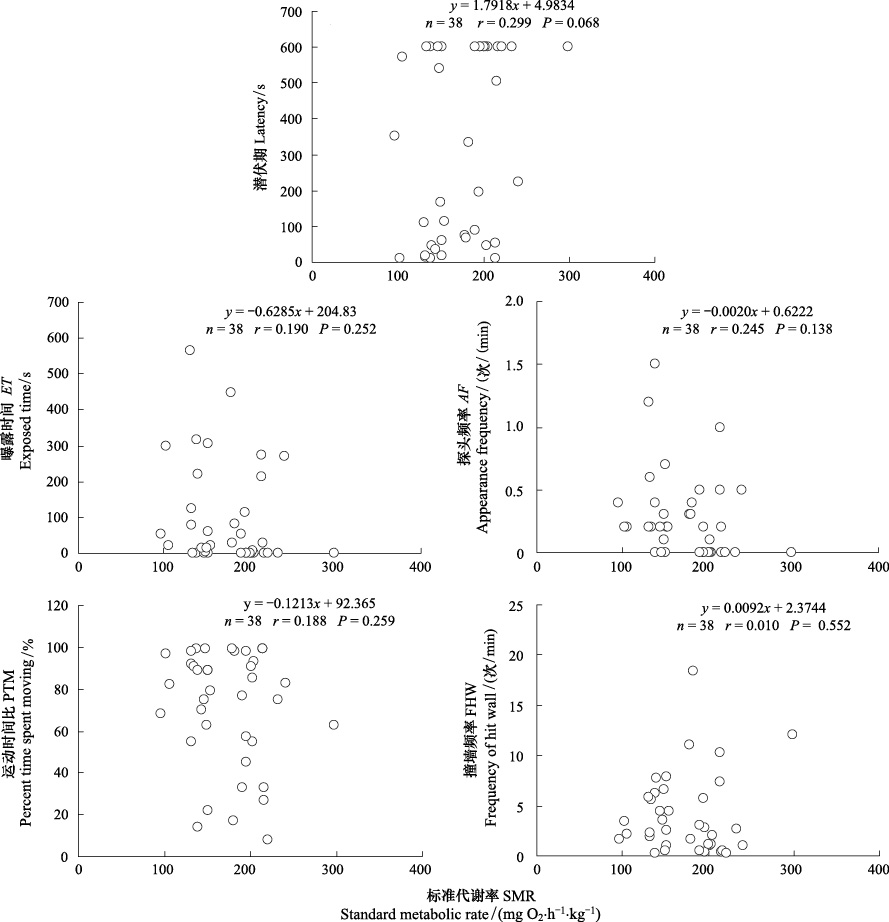
鲫的SMR与RT呈正相关(图 2,P=0.021),与Amax呈负相关(图 2,P=0.037),但与Umax、S120均不相关(图 2,二者P > 0.05)。该种鱼的SMR与勇敢性指标如L、ET和AF以及活跃性指标如PTM、FHW均不相关(图 3)(所有P > 0.05)。

|
| 图2 鲫幼鱼标准代谢率与快速启动参数的相关性 Fig.2 Correlations between SMR and components of fast-start in the crucian carp |
|
| 图3 鲫幼鱼标准代谢率与个性行为的相关性 Fig.3 Correlations between SMR and components of animal personality in the crucian carp |
在鱼类能量代谢的相关研究中,SMR和MMR代表机体能量代谢的上限与下限,不仅影响动物的能量分配,而且与个体的游泳行为(如运动力竭)和生长性能等方面密切相关[1, 3, 18]。鱼类SMR与MMR以及EPOC的关系备受关注[14]。研究发现,随种类活跃性的增强鱼类的SMR和MMR均升高,即二者呈正相关[13];有关鳟(Salmo trutta)的研究发现肝脏中两种有氧代谢关键酶活性分别与SMR和MMR呈正相关,揭示这种个体能量代谢特征正相关联的生化机制[8]。实验室先前研究发现南方鲇(Silurus meridionalis)的SMR与其摄食代谢峰值(最大摄氧能力)呈正相关[16];在不同溶氧水平条件下该种鱼的SMR与摄食代谢峰值(最大摄氧能力)也均呈正相关[7];鲤(Cyprinus carpio)[19]、大西洋鲑(Salmo salar)[20]以及鳟[8]也具有相似的研究结果。本实验室过往研究显示鲫的SMR与其MMR呈正相关[14];然而,本研究却发现鲫的SMR与MMR不相关。有关南方鲇的研究发现,该种鱼的SMR与其运动后MMR也并不相关[16],上述研究表明不同鱼类SMR与MMR的关联不尽相同,该方面的研究观点仍需要更多的种类加以验证。
本研究发现,高SMR鲫个体具有较小AS,该现象与大西洋鲑的实验结果一致[6]。有研究认为,高SMR个体鱼类的维持能量支出较多,需要通过个体竞争优势进行更频繁的社群斗争(如好斗性),进而获得较高的社群等级和更多的资源(如食物和领域)[6, 21]。这种现象表明,在MMR相当的情况下由于SMR的上升会导致AS的水平下降。本研究发现高SMR鲫个体的MMR与低SMR的无显著差异,SMR与AS呈负相关的现象可能是由于上述原因所致。此外,EPOC总量是鱼类在运动力竭后超过SMR的额外耗氧量,它部分程度反映了鱼体的无氧代谢能力[13, 14, 15, 16]。鱼类的SMR普遍存在个体差异,并且不同鱼类SMR与EPOC总量的关系较为类似。文献报道,鲫幼鱼的SMR与EPOC总量呈负相关[14]。另外,转基因银大马哈鱼(Oncorhynchus kisutch)的SMR高于同种的非转基因个体,前者的EPOC总量明显大于后者,导致该种鱼SMR与EPOC总量呈负相关[22],但这种现象是基因操控的结果。实验发现鲫幼鱼的SMR与EPOC总量也呈负相关。上述研究结果表明,这些鱼类的无氧代谢能力与标准代谢水平之间存在功能权衡,即高SMR个体的无氧代谢能力较低,而低SMR个体的无氧代谢能力却较高。
3.2 鲫幼鱼的SMR与快速启动及个性行为的关系人们不仅关注鱼类的SMR与MMR,AS以及EPOC总量之间的关系,而且最近研究发现,鲤幼鱼的SMR与在自发游泳中的尾鳍平均摆动次数呈现正相关,而与临界游泳速度不相关[19]。在快速启动的研究中,发现鲫幼鱼的SMR与Umax及S120无关,与Amax呈负相关,而与RT呈正相关(图 2),表明低SMR鲫个体在栖息环境中能较快对捕食者等环境胁迫作出逃逸反应,同时以较高的加速度完成这一逃逸行为过程,提示鲫的SMR越低,其捕食或逃避能力可能越强。造成这种负相关现象的可能原因是,在经历相同禁食时间后低SMR个体能更好地维持较高的生理功能状态,而高SMR个体由于能量消耗较多使其该方面功能受到一定程度的负面影响。
鱼类SMR的个体差异可能是导致个性行为差异的能量学基础,通常认为SMR较高的鱼类个体在个性行为上表现得较为勇敢、敢于探索、较为好斗,即鱼类SMR与上述个性行为指标呈正相关[2]。研究报道,SMR越高的大西洋鲑其好斗性越强,但SMR与其特殊生长率不相关[23]。同样以大西洋鲑为实验对象的文献报道,该种鱼的SMR与好斗性和社群等级地位均呈正相关[24]。欧鲈(Dicentrarchus labrax)的SMR在食物资源丰富且可预测条件下与其勇敢性行为指标不相关[25]。本研究显示鲫的SMR与活跃性及勇敢性指标也均不相关。在本研究实验期间,食物资源丰富且可预测(每天固定时间和地点饱足投喂)、水槽的物理空间均质、水体理化因子(如水温和溶氧)较为稳定,即环境条件的异质性低。产生SMR与个性行为不相关现象原因可能与本研究的实验环境条件有关。在自然界中,鱼类的栖息环境复杂多变,面临的多方面(如人类捕捞、肉食性鱼类和水面捕食者等)的捕食压力,其异质性明显高于实验室完全人工的养殖环境或半野外环境[26, 27]。因此在实验条件下获得的研究结果,未必都能够真切反映自然条件下鱼类能量代谢与行为之间的内在关联。
致谢: 感谢重庆师范大学李秀明副教授对本研究的帮助,感谢2009级本科生温倩、潘本兰和朱鹏程对实验的帮助。| [1] | Careau V, Thomas D, Humphries M M,Réale D. Energy metabolism and animal personality. Oikos, 2008, 117(5): 641-653. |
| [2] | Biro P A, Stamps J A. Do consistent individual differences in metabolic rate promote consistent individual differences in behavior?. Trends in Ecology and Evolution, 2010, 25(11): 653-659. |
| [3] | Burton T, Killen S S, Armstrong J D, Metcalfe N B. What causes intraspecific variation in resting metabolic rate and what are its ecological consequences?. Proceeding of the Royal Society B: Biological Sciences, 2011, 278(1724): 3465-3473. |
| [4] | Dingemanse N J, Kazem A J N, Réale D, Wriqht J. Behavioural reaction norms: animal personality meets individual plasticity. Trends in Ecology and Evolution, 2010, 25(2): 81-89. |
| [5] | Marras S, Killen SS, Claireaux G,Domenici P, McKenzie D J. Behavioural and kinematic components of the fast-start escape response in fish: individual variation and temporal repeatability. The Journal of Experimental Biology, 2011, 214(18): 3102-3110. |
| [6] | Cutts C J, Metcalfe N B, Taylor A C. Juvenile Atlantic Salmon (Salmo salar) with relatively high standard metabolic rates have small metabolic scopes. Functional Ecology, 2002, 16(1): 73-78. |
| [7] | Chen B J, Cao Z D, Fu S J. Hypoxia impairs the digestive advantage of individual southern catfish (Silurus meridionalis) with high resting metabolic rates and postprandial metabolic responses. Marine and Freshwater Behaviour and Physiology, 2014, 47(3): 197-204. |
| [8] | Norin T, Malte H. Intraspecific variation in aerobic metabolic rate of fish: relations with organ size and enzyme activityin brown trout. Physiological and Biochemical Zoology, 2012, 85(6): 645-656. |
| [9] | Lacasse J, Aubin-Horth N. A test of the coupling of predator defense morphology and behavior variation in two threespine stickleback populations. Current Zoology,2012, 58(1): 53-65. |
| [10] | Domenici P, Blake R.The kinematics and performance of fish fast-start swimming. The Journal of Experimental Biology, 1997, 200(8): 1165-1178. |
| [11] | Lyon J P, Ryan T J, Scroggie M P. Effects of temperature on the fast-start swimming performance of an Australian freshwater fish. Ecology of Freshwater Fish, 2008, 17(1): 184-188. |
| [12] | Law T, Blake R.Comparison of the fast-start performances of closely related, morphologically distinct threespine sticklebacks (Gasterosteus spp.). The Journal of Experimental Biology, 1996, 199(12): 2595-2604. |
| [13] | Fu S J, Zeng L Q, Li X M,Pang X, Cao Z D, Peng J L, Wang Y X. Effect of meal size on excess post-exercise oxygen consumption in fishes with different locomotive and digestive performance. Journal of Comparative Physiology B, 2009, 179(4): 509-517. |
| [14] | 唐国伟, 曹振东, 付世建. 温度、种内标准代谢差异与鲫幼鱼力竭运动后过量耗氧的关系. 生态学杂志, 2013, 32(12): 3255-3260. |
| [15] | Zeng L Q, Zhang Y G, Cao Z D, Fu S J. Effect of temperature on excess post-exercise oxygen consumption in juvenile southern catfish (Silurus meridionalis Chen) following exhaustive exercise. Fish Physiology and Biochemistry, 2010, 36(4): 1243-1252. |
| [16] | Fu S J, Cao Z D, Peng J L, Wang YX. Is peak postprandial oxygen consumption positively related to growth rate and resting oxygen consumption in a sedentary catfish Silurus meridionalis? Journal of Fish Biology, 2008, 73(3): 692-701. |
| [17] | Wang F, Chen B J, Cao Z D,Wang Y X, Fu S J. The influence of starvation on fast-start performance of Spinibarbus sinensis. Acta Ecologia Sinica, 2012, 32(6): 291-296. |
| [18] | Norin T, Malte H.Repeatability of standard metabolic rate, active metabolic rate and aerobic scope in young brown trout during a period of moderate food availability. The Journal of Experimental Biology, 2011, 214(10): 1668-1678. |
| [19] | 张曦. 鲤鱼(Cyprinus carpio)幼鱼标准代谢的种内差异与运动能力和摄食代谢的关系[D]. 重庆: 重庆师范大学, 2012. |
| [20] | Millidine K J, Armstrong J D, Metcalfe N B. Juvenile salmon with high standard metabolic rates have higher energy costs but can process meals faster. Proceedings of the Royal Society B, 2009, 276(1664): 2103-2108. |
| [21] | 陈永鹏, 曹振东, 付世建. 锦鲫幼鱼的社群等级地位及其与标准代谢率、血糖和临界游泳能力的关系. 生态学报, 2010, 30(7): 1940-1945. |
| [22] | Lee C G, Devlin R H, Farrell A P. Swimming performance, oxygen consumption and excess post-exercise oxygen consumption in adult transgenic and ocean-ranched cohosalmon. Journal of Fish Biology, 2003, 62(4):753-766. |
| [23] | Cutts C J, Metcalfe N B, Taylor A C. Aggression and growth depression in juvenile Atlantic salmon: the consequences of individual variation in standard metabolic rate. Journal of Fish Biology, 1998, 52(5): 1026-1037. |
| [24] | Reid D, Armstrong J D, Metcalfe N B. The performance advantage of a high resting metabolic rate in juvenile salmon is habitat dependent. Journal of Animal Ecology, 2012, 81(4): 868-875. |
| [25] | Killen S S, Marras S, McKenzie D J. Fuel, fasting, fear: routine metabolic rate and food deprivation exert synergistic effects on risk-taking in individual juvenile European sea bass. Journal of Animal Ecology,2011, 80(5): 1024-1033. |
| [26] | Martin-Smith K M, Armstrong J D. Growth rates of wild stream-dwelling Atlantic salmon correlate with activity and sex but not dominance. Journal of Animal Ecology, 2002, 71(3): 413-423. |
| [27] | Maclean A, Huntingford F A, Ruxton G D, Morgan I J, Hamilton J, Armstrong J D. Testing the assumptions of the ideal despotic distribution with an unpredictable food supply: experiments in juvenile salmon. Journal of Animal Ecology, 2005, 74(2): 214-225. |
 2016, Vol. 36
2016, Vol. 36




