文章信息
- 熊德成, 黄锦学, 刘小飞, 林伟盛, 林成芳, 陈光水, 谢锦升, 杨玉盛
- XIONG Decheng, HUANG Jinxue, LIU Xiaofei, LIN Weisheng, LIN Chengfang, CHEN Guangshui, XIE Jinsheng, YANG Yusheng
- 中亚热带杉木人工林细根生物量空间变异与取样数量估算
- Spatial heterogeneity of fine roots and appropriate sampling methods in a subtropical Chinese fir plantation
- 生态学报, 2016, 36(6): 1599-1607
- Acta Ecologica Sinica, 2016, 36(6): 1599-1607
- http://dx.doi.org/10.5846/stxb201408171627
-
文章历史
- 收稿日期: 2014-08-17
- 网络出版日期: 2015-07-29
2. 福建师范大学地理研究所, 福州 350007
2. School of Geographical Sciences, Fujian Normal University, Fuzhou 350007, China
细根(多指直径≤2 mm的根),是树木根系的组成部分,具有重要的生理和生态学功能[1]。研究表明,虽然细根占林木根系总生物量的比例不足30%,但由于细根周转迅速,每年通过枯死细根向土壤归还碳、养分和能量甚至超过地上部分枯落物[2]。因此精确估算细根生物量和细根动态在估计森林碳预算中具有十分重要的作用[3]。研究表明不论在大尺度还是在小尺度上,不论在水平方向还是在垂直方向上,地下根系均表现为高度的空间异质性现象[4, 5]。然而在准确采集根系生物量过程中,设计合理采样方案的重要性往往被忽略[6],由于目前多采用随机或“S”型取样的限制,从而没有详加考虑细根空间分布的异质性,可能导致所得结果不能真实反映林地细根生物量的状况,细根生物量估计仍存在很大的不确定性[7, 8]。在国外,细根取样问题受到较多的关注,许多研究者试图从影响取样的各个方面(取样数量、取样体积、取样方法等)探讨细根最优取样方法[9]。目前一些研究已经根据根系生物量空间变异系数的大小和特定的样本容量公式来估算根系所需的取样数量[5, 10]。综上所述如何在有限的样本前提下,提高细根生物量的估算精度显得十分重要。森林细根生物量主要包括乔木部分和林下植被的根系,在生态系统中林下植被在总的细根生物量中占有很重要的部分[11, 12, 13],然而大多数细根生物量的研究通常只对乔木部分进行了估计,对不同森林类型林下植被细根生物量的估计还比较缺乏,尤其是对乔木和林下植被生物量空间异质性的分析,从而影响了森林生态系统中碳库和周转速率的估计。目前有关温带森林和热带森林中细根的空间变异性已有部分研究[5, 14, 15],而有关亚热带的相关报道还十分缺乏,从而影响了对细根生物量的估计。
杉木林(Cunninghamia lanceolata)是我国南方集体林区最重要的商品林之一,在我国人工林中占据重要地位。因此准确的估计其细根生物量在空间上的分布,尤其是乔木层和林下植被的差异对其生产力维持机制,物质循环特点以及碳吸存潜力等有重要作用。基于以上原因本文以50年生杉木人工林为研究对象,采用土钻取样方法,研究其在1 m垂直深度内细根生物量的空间变异,并对获取细根生物量所需的取样数量进行估计,以期为准确测定杉木人工林细根生物量等提供参考,同时亦为森林生态系统的细根碳储量评估提供基础数据。
1 试验地概况研究地位于福建省三明市格氏栲自然保护区(26°11′N,117 °28′E)内,本区属中亚热带海洋季风气候,具有冬冷夏热、水热同季、湿润多雨的特点,年均气温19.1 ℃,年均降水量1749 mm,年均蒸发量1585 mm,相对湿度81%。本文研究对象为选取该区约50年生的杉木人工林为研究对象,该林地造林时间为1964年,坡向SW25°,坡度30°,林分密度为1200株/hm2,平均胸径24.9 cm,平均树高21.4 m。林地中植物种类较为丰富,其中乔木层主要有杉木(Cunninghamia lanceolata)外,还分布有木荷(Schima superb)、马尾松(Pinus massoniana)、虎皮楠(Daphnipnyllum oldhami)、南酸枣(Choerospondias axillaris)、格式栲(Castanopsis kawakamii)等。灌木主要有杜茎山(Maesa japonica)、粗叶榕(Ficus hirta)、毛冬青(Ilex pubescens)、黄楠(Machilus grijsii)、大叶紫珠(Callicarpa kochiana)、狗骨柴(Tricalysia dubia)等。草本植物主要有华山姜(Alpinia zerumbet)、乌毛蕨(Blechnum orientale)、刺齿凤尾蕨(Pteris dispar)、团叶鳞始蕨(Lindsaea orbiculata)、芒萁(Dicranopteris dichotoma)、狗脊(Woodwardia japonica)、草珊瑚(Sarcabdra glabra)。藤本植物主要有细圆藤(Pericampylus glaucus)、香花崖豆藤(Millettia dielsiana)、网脉酸藤子(Embelia rudis)、菝葜(Smilax china)、五味子(Schisandra chinensls)、玉叶金花(Mussaenda pubescens)等。
2 研究方法 2.1 根系取样与处理取样时间主要集中在2013年10月,在50年生杉木人工林增温样地内选取坡面一致的地段设置长期试验样地,沿坡位设置4个区组,每个区组5个样地,共计20块大小为10 m×10 m的样地,各样地间隔在5 m左右,本研究为增温样地本底调查研究的一部分。取样时为了避免对样地的破坏主要是在每块样地外进行,取样点位于每个样地周边的中点位置附近,每个样地共计采集5个样点,20块样地共100个采样点。取样时主要是用内径为5 cm的土钻在每个样点钻取土芯,钻取土芯前,先去除掉地表枯落物,再分层进行取样,取样共分10层(0—10,10—20,20—30,30—40,40—50,50—60,60—70,70—80,80—90,90—100 cm),然后分别装入塑料袋内进行标签,并立即带回实验室处理。
在实验室将取回的土芯样品放置在孔径0.5 mm的土壤筛用清水进行冲洗,将洗净后的活根按根直径0—1 mm、1—2 mm进行分级,并根据根系外形、颜色等特征将根系区分出杉木根和林下植被活根和死根根系,实验之前专门挖取一定的杉木细根进行辨别。一般杉木细根表皮多呈棕色,侧枝较多,出生不久的根系一般呈白色;死根为黑色、皮层脱落或表皮褶皱易断的根系。最后将各层分级好的细根分别放入65 ℃烘箱内48 h,烘干至恒重。文中根系生物量的计算公式如下:
单位面积生物量(g/m2)=每根土芯根系干重(g)×104/[π×(5 cm/2)2]
2.2 数据分析数据经整理后分别对不同类型细根不同径级、不同土层细根的单位面积生物量进行描述性统计分析。描述性统计主要包括最大/最小值、平均值、标准差、中值、变异系数等,同时采用SPSS17.0中Shapiro-Wilk检验对数据是否符合正态分布进行检验。采用蒙特-卡罗统计模拟方法对不同细根类型不同径级、不同土层细根在精度为80%,置信水平为95%条件下的最佳取样数量进行估计。
相关图表均在Excel和origin8.0软件中完成。
3 研究结果 3.1 杉木人工林细根的空间变化特征 3.1.1 不同细根类型不同径级细根生物量的描述统计通过对不同径级(0—1、1—2、0—2 mm)细根生物量描述性统计分析发现:不同径级细根的单位面积生物量具有一定的差异性。杉木细根、林下植被细根、总细根(杉木+林下植被细根)单位面积生物量均表现为随径级增大而降低(表 1)。杉木细根各个径级平均值分别为(123.05±76.51) g/m2、(105.12±84.21) g/m2、(228.17±131.58) g/m2,林下植被细根各个径级平均值分别为(82.83±69.95) g/m2、(41.32±49.60) g/m2、(124.14±98.6) g/m2,总细根各个径级平均值分别为(205.88±100.49) g/m2、(146.44±93.23) g/m2、(352.32±161.82) g/m2(表 1)。同时各个细根类型随径级增大生物量中位值均呈减小的趋势,从最大值与最小值之间的相差幅度看,0—1mm径级总细根相差幅度最大(443.77 g/m2),其次是林下植被和杉木细根(分别为374.47 g/m2、346.85g/m2),1—2 mm径级和0—2 mm径级细根均表现为总细根相差幅度最大(433.92、898.55 g/m2),其次是杉木细根(408.0、672.1 g/m2)、林下植被细根(254.06、490.44 g/m2)(表 1)。
| 细根类型 Fine root type | 径级/mm Diameter class | 生物量Biomass/(g/m2) | 变异系数 Coefficient of variation | 峰度 Kurtosis | 偏度 Sknewness | P | ||||
| 最大值 Maximum | 最小值 Minimum | 平均值 Mean | 标准差 Standard deviation | 中值 Median | ||||||
| 杉木 | 0—1 | 352.71 | 5.86 | 123.05 | 76.51 | 109.63 | 62.18 | 0.25 | 0.84 | <0.001 |
| Chinese fir | 1—2 | 408 | 0 | 105.12 | 84.21 | 74.32 | 80.11 | 2.54 | 1.5 | <0.001 |
| 0—2 | 692.99 | 20.89 | 228.17 | 131.58 | 203.14 | 57.67 | 1.43 | 0.99 | 0.063 | |
| 林下植被 | 0—1 | 379.72 | 5.25 | 82.83 | 69.95 | 70.52 | 84.45 | 4.35 | 1.91 | <0.001 |
| Undergrowth | 1—2 | 254.06 | 0 | 41.32 | 49.6 | 27.62 | 120 | 5.64 | 2.12 | <0.001 |
| vegetation | 0—2 | 492.69 | 2.25 | 124.14 | 98.6 | 95.43 | 79.43 | 1.93 | 1.44 | <0.001 |
| 总细根 | 0—1 | 489.68 | 45.91 | 205.88 | 100.49 | 189.89 | 48.81 | 0.63 | -0.06 | <0.001 |
| Total | 1—2 | 448.34 | 14.42 | 146.44 | 93.23 | 132.84 | 63.67 | 1.1 | 1.22 | <0.001 |
| fine root | 0—2 | 948.03 | 49.48 | 352.32 | 161.82 | 330.9 | 45.93 | 0.67 | 0.68 | 0.086 |
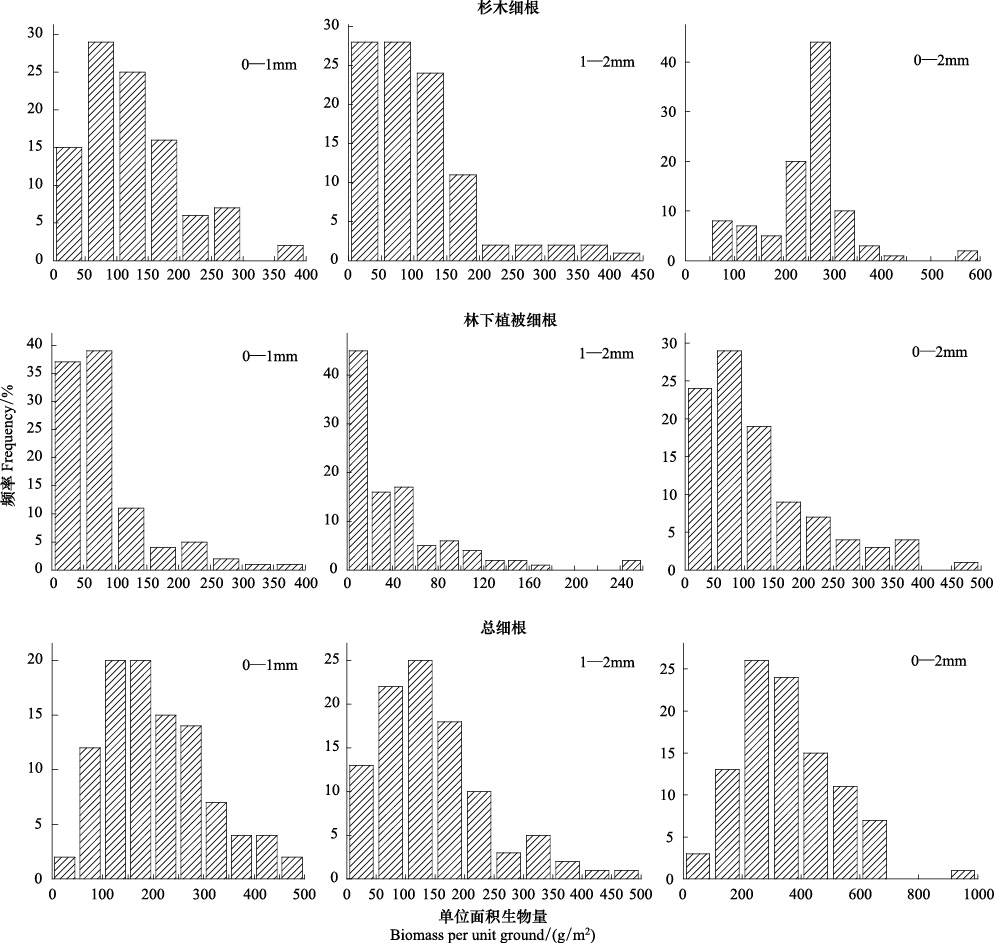
相关研究认为,当变异系数(CV)≤10%属弱变异性,10%﹤CV﹤100%属中等变异性,CV≥100%属强变异性[16]。本研究中各个细根类型生物量变异系数均随着径级(主要是0—1 mm、1—2 mm)的增加呈增大的趋势,变异系数除林下植被1—2mm细根CV﹥100%,为强度变异外,其余细根类型各径级变异系数在40%—90%之间,属中等变异;同时各个细根类型0—2 mm细根也均表现出中等变异(表 1)。Shapiro-Wilk分布检验表明,仅0—2 mm杉木细根和总细根单位面积生物量符合正态分布,其余各个细根类型不同径级单位面积生物量均不符合正态分布,且均呈明显的右偏分布(图 1)。
|
| 图1 不同细根类型不同径级细根生物量频率分布图 Fig.1 Frequency distribution of fine root biomass per unit ground areaof different root diameter class for different type |
为充分了解整个林分细根生物量的分布状况,研究中着重分析了总细根各个径级细根在不同土层的生物量分布情况。分析发现:同一径级细根生物量平均值和中值随土层深度增加而降低,各个土层不同径级(0—1、1—2 mm)细根单位面积生物量平均值和中值也主要表现出降低的趋势(表 2)。各个土层不同径级细根生物量变异系数随径级升高而增大,而同一径级不同土层中1—2 mm细根生物量随土层增加变异系数基本表现为增大,而0—1 mm只在0—30 cm土层表现出这一规律(表 2)。除0—20 cm土层及50—60 cm土层0—1 mm细根生物量变异系数表现出中度变异外(变异系数分别为65.22%、82.79%、98.86%),其余土层各个径级均表现为强度变异(100.67%—452.22%);各个土层0—2 mm细根生物量仅在0—10 cm和10—20 cm表现为中度变异(60.05%、87.53%),其余土层均为强度变异(106.97%—263.14%)(表 2)。Shapiro-Wilk检验表明,总细根各个土层不同径级单位面积生物量均不符合正态分布(表 2)。
| 土层/cm Soil depth | 径级/mm Diameter class | 生物量Biomass/(g/m2) | 变异系 数/% Coefficient of variation | 峰度 Kurtosis | 偏度 Sknewness | P | ||||
| 最大值 Maximum | 最小值 Minimum | 平均值 Mean | 标准差 Standard deviation | 中值 Median | ||||||
| 0—10 | 0—1 | 284.99 | 0 | 77.63 | 50.63 | 69.86 | 65.22 | 3.15 | 1.37 | <0.001 |
| 1—2 | 229.55 | 0 | 37.49 | 39 | 28.59 | 104.03 | 8.7 | 2.5 | <0.001 | |
| 0—2 | 364.23 | 0 | 115.13 | 69.13 | 97.25 | 60.05 | 2.58 | 1.36 | <0.001 | |
| 10—20 | 0—1 | 126.83 | 0 | 32.6 | 26.99 | 25.6 | 82.79 | 2.08 | 1.42 | <0.001 |
| 1—2 | 264.36 | 0 | 26.18 | 35.65 | 16.61 | 136.17 | 19.57 | 3.5 | <0.001 | |
| 0—2 | 391.18 | 0 | 58.77 | 51.44 | 54.98 | 87.53 | 16.87 | 3.07 | <0.001 | |
| 20—30 | 0—1 | 238.22 | 0 | 27.87 | 31.37 | 19.9 | 112.56 | 23.32 | 4.1 | <0.001 |
| 1—2 | 171.21 | 0 | 22.33 | 33.63 | 9.99 | 150.6 | 7.88 | 2.64 | <0.001 | |
| 0—2 | 338.9 | 0 | 50.2 | 53.7 | 37.12 | 106.97 | 11.19 | 2.91 | <0.001 | |
| 30—40 | 0—1 | 88.66 | 0 | 16.43 | 16.54 | 12.08 | 100.67 | 4.47 | 1.83 | <0.001 |
| 1—2 | 255.69 | 0 | 18.86 | 34.57 | 7.82 | 183.3 | 23.96 | 4.26 | <0.001 | |
| 0—2 | 275.82 | 0 | 35.3 | 40.02 | 25.76 | 113.37 | 12.91 | 2.86 | <0.001 | |
| 40—50 | 0—1 | 114.5 | 0 | 16.58 | 18.56 | 11.64 | 119.94 | 9.43 | 2.5 | <0.001 |
| 1—2 | 87.8 | 0 | 11 | 17.78 | 2.01 | 161.64 | 6.46 | 2.38 | <0.001 | |
| 0—2 | 138.45 | 0 | 27.58 | 30.78 | 18.34 | 111.6 | 3.12 | 1.75 | <0.001 | |
| 50—60 | 0—1 | 62.17 | 0 | 13 | 12.85 | 9.38 | 98.86 | 2.9 | 1.54 | <0.001 |
| 1—2 | 192.61 | 0 | 14.6 | 28.38 | 4.99 | 194.36 | 14.95 | 3.59 | <0.001 | |
| 0—2 | 205.61 | 0 | 27.6 | 32.29 | 18.65 | 117 | 9.39 | 2.61 | <0.001 | |
| 60—70 | 0—1 | 174.57 | 0 | 7.71 | 20.11 | 0 | 260.99 | 48.54 | 6.22 | <0.001 |
| 1—2 | 69.2 | 0 | 3.75 | 11.05 | 0 | 294.47 | 15.63 | 3.72 | <0.001 | |
| 0—2 | 174.57 | 0 | 11.38 | 23.37 | 0 | 205.36 | 23.84 | 4.09 | <0.001 | |
| 70—80 | 0—1 | 71.74 | 0 | 6.65 | 12.25 | 0 | 184.28 | 8 | 2.51 | <0.001 |
| 1—2 | 59.11 | 0 | 4.07 | 10.44 | 0 | 256.35 | 10.43 | 3.12 | <0.001 | |
| 0—2 | 78.83 | 0 | 10.64 | 18 | 0 | 169.17 | 2.86 | 1.85 | <0.001 | |
| 80—90 | 0—1 | 47.18 | 0 | 3.71 | 8.35 | 0 | 225.31 | 9.69 | 3 | <0.001 |
| 1—2 | 127.8 | 0 | 7.05 | 19.85 | 0 | 281.56 | 17.85 | 3.94 | <0.001 | |
| 0—2 | 134.22 | 0 | 10.62 | 23.11 | 0 | 217.61 | 9.95 | 2.96 | <0.001 | |
| 90—100 | 0—1 | 52.94 | 0 | 3.7 | 8.78 | 0 | 236.97 | 13.16 | 3.4 | <0.001 |
| 1—2 | 25.45 | 0 | 0.81 | 3.68 | 0 | 452.22 | 61.39 | 7.47 | <0.001 | |
| 0—2 | 99.26 | 0 | 5.1 | 13.42 | 0 | 263.14 | 25.76 | 4.51 | <0.001 | |
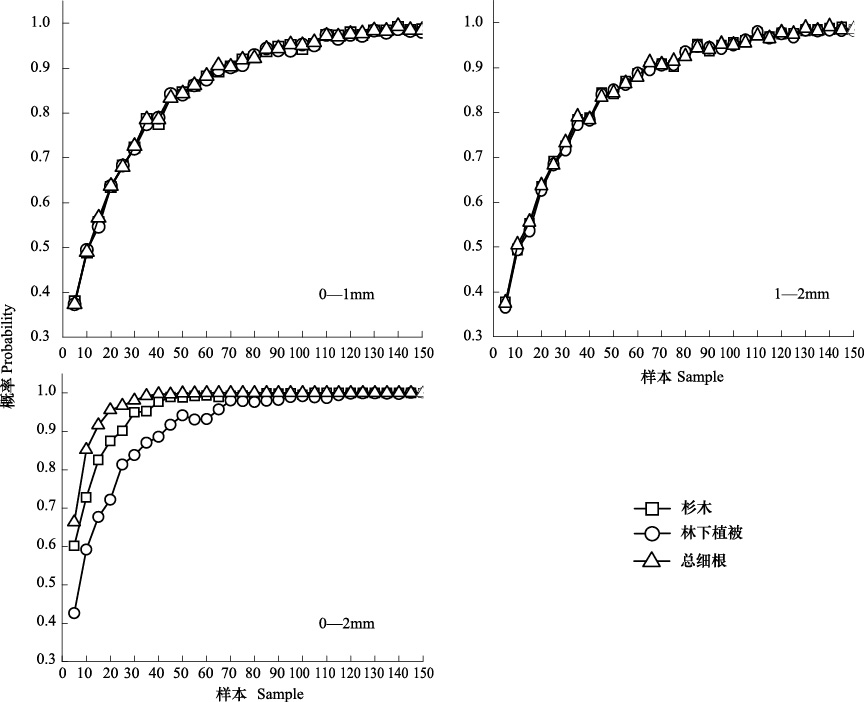
通常情况下考虑到取样及样品处理工作量之间的权衡,一般认为细根取样采用置信水平为95%、精度为80%的样本容量比较合适,本研究也采用这一原则。通过蒙特-卡罗统计模拟分析发现:在该置信水平和估计精度下,细根取样样本容量因不同细根类型和不同径级而有所差异,随着径级的增加,不同类型细根相应的取样数量增加,基本表现为各个径级林下植被细根满足测定所需要的样本容量均最大,总细根最小(图 2)。0—1 mm根系生物量杉木、林下植被以及总细根取样数量分别为95、98、93可以满足测定要求;1—2 mm根系生物量杉木、林下植被以及总细根取样数量分别为96、98、93个可以满足测定要求;而0—2 mm根系生物量杉木、林下植被以及总细根取样数量分别为32、63、18个可以满足测定要求(图 2)。
|
| 图2 95%置信水平与80%估计精度下取值概率与样本量的关系 Fig.2 Statistical characteristics of fine root biomass at different soil depth |
蒙特-卡罗统计模拟方法发现:同一土层总细根随径级增加相应的取样数量增加,同一径级总细根随土层加深取样数量也增加(表 3)。在置信水平为95%,精度为80%情况下,0—1 mm径级细根从表层到底层分别需要取样39、63、117、97、119、94、613、318、478、532个方可满足测定单位面积生物量的需求;1—2 mm径级细根从表层到底层分别需要取样97、168、207、302、219、333、769、598、722、3168个可满足测定单位面积生物量的需求;同时0—2 mm径级细根从表层到底层取样数量分别为38、59、103、125、120、123、382、262、432、628个可满足测定需求(表 3)。
| 径级/mm Diameter class | 取样数量/个 | |||||||||
| 0—10* | 10—20 | 20—30 | 30—40 | 40—50 | 50—60 | 60—70 | 70—80 | 80—90 | 90—100 | |
| 0—1 | 39 | 63 | 117 | 97 | 119 | 94 | 613 | 318 | 478 | 532 |
| 1—2 | 97 | 168 | 207 | 302 | 219 | 333 | 769 | 598 | 722 | 3168 |
| 0—2 | 38 | 59 | 103 | 125 | 120 | 123 | 382 | 262 | 432 | 628 |
| *土层Soil depth (cm) | ||||||||||
目前有关细根生物量空间变异的研究还比较缺乏,有限的研究也主要是单纯的对林地总细根生物量进行估计,本研究通过对杉木人工林林内杉木、林下植被、总细根(杉木+林下植被)不同径级、不同土层单位面积生物量的研究直接证实了其在空间上存在高度的异质性现象,这与众多有关人工林及天然林的研究具有类似的结果[5, 14, 17, 18]。根系生物量这一空间变异可能主要与林地的立地条件有关,因为土壤环境具有高度的异质性,不同土层深度根系的生长、分布不仅受自身遗传特性的影响,更容易受到土壤环境的影响[19],如在林地中不同地点不同土层在养分含量、土壤物理性质(土壤容重、孔隙度等)均存在着一定的异质性[20, 21]。此外细根生物量的水平格局还受林下土壤湿度、光照、温度的综合影响,例如树冠对降水的再分配及对降水化学性质的影响,能显著改变林冠下及树干周围的土壤湿度、化学性质等,并进而显著改变靠近树干一定范围内的细根水平分布[22, 23]。本研究发现林下植被不同径级细根生物量在空间上表现出较强变异性,尤其是1—2 mm根系更是为强度变异,因此在林木细根研究中对林下植被根系的这种异质性应引起高度的重视,这对准确的估计林下植被在地下生态系统中的作用(如对土壤有机碳的贡献)十分关键;同时杉木细根、总细根不同径级细根生物量均表现为中度变异,这可能主要是因为林下植被部分由于种类比较丰富,根系结构复杂,因此增大了这种空间异质性而引起的。而总细根不同土层除表层部分径级为中度变异外,其余土层各个径级均为强度变异,且随土层增加,变异加大,这可能主要是由于表层细根分布更均匀,底层土壤本身细根生物量相对较低,同时受树木个体大小、主根分布深度、离树干位置、土层厚度等变异的综合影响,导致底层土壤细根生物量的变异程度加大。
本研究发现仅杉木和总细根0—2 mm细根单位面积生物量符合正态分布,其余细根类型不同径级、不同土层细根均不符合正态分布,且表现出明显右偏分布,根据右偏分布的特点可以看出研究结果的平均值被严重低估,这与细根取样的方法及数量有密切的关系。土壤中根系分布的高度空间异质性使得根系参数估计与取样数量密切相关,根系属性变异越大,为达到一定精确度所要求的取样数量越多[24]。地下根系空间分布的异质性,降低了地下根系分布状态的可预知性,从而也增加了地下生物量研究时取样点设置的难度,在进行细根生物量研究时,经常采用的方式是增加取样点的数目,但此时面临的两个突出问题是如何量化取样点的数目以及如何进行空间取样点的布设[15]。目前有关细根取样数量的研究还十分缺乏,一般而言,土钻直径越大,取到的细根越多,所需的取样数量越少,相反土钻直径越小所需的取样数量越多,即取样数量受取样体积的影响[25, 26]。相比于大多数研究所采用的土钻(直径一般为7 cm),本研究所采用的土钻(直径5 cm)直径偏小,因此在保证取样数量的同时合理增大取样工具的直径将有利于实验的精度。同时传统的野外调查取样时经常采取的30个左右的样点以及采用随机或"S"形曲线的空间布点方法很难满足要求[27, 28],在估计林地细根生物量上存在着很大的不确定性,Metcalfe等[5]对热带雨林细根的研究证实了这一点。同时孙志虎等[15]对落叶松纯林表层的细根研究亦表明,当取样数量为82时细根生物量才基本呈正态分布;黄超超等[17]对本区常绿阔叶林细根研究发现当取样数量为96时仅在0—1 mm细根单位面积生物量表现出正态分布,这也表明本研究中所取的100个点所估计的细根单位面积生物量与实际值之间仍存在一定的误差;同时其研究发现在置信水平为95%、估计精度为80%的条件下,0—1 mm细根生物量需要的取样数量为16,1—2 mm细根生物量需要的取样数量为42,相较之下本研究中在相同的置信水平和估计精度下0—1 mm和1—2 mm细根所需要的取样数量范围均为93个,这可能与林分类型以及所研究的土层深度有关,黄超超等[17]研究的是常绿阔叶林,不同的林分类型其树种组成、林分结构和土壤理化性质等不同,因而影响林分细根生长与分布,进而影响细根取样数量;同时其研究的土层深度为80 cm,本研究深度为1 m。本研究中0—2 mm各个细根类型不同径级以及不同土层取样数量大部分均要求较少,这可能主要是因为针对的是整个细根水平(≤2 mm),在一定程度上削弱了由于具体细化细根分级造成的变异,但同时也不难发现即使针对0—2 mm细根要满足深层土壤细根生物量测定的需求同样还需要较大的样本量。本研究中细根生物量随径级增加变异系数增大,所需取样数量也相应增加,这可能主要与不同径级细根的生理功能有关,因为植物根系吸收水分和养分主要依靠径级较小的根系进行,由于径级较小根系表面积较小因此这就需要更多的根系参与,这也使得0—1 mm根系在空间分布上更多更均匀,因此其变异相对较小;而径级较大的1—2 mm根系则主要参与养分和水分的传输以及支撑作用,空间分布范围较小,因此其变异较大;同时总细根生物量随着土层深度增加变异系数和取样数量也具有类似的规律,这可能主要与林地内不同植株大小、土壤养分的垂直变化及离树干位置等因素有关[29]。
本研究还发现在相同的置信水平及估计精度下杉木细根、林下植被细根相比于总细根均需要更多的取样数量才能满足测定生物量的需求,这也表明在研究林地目的树种及林下植被根系生物量的差异时应充分考虑取样的数量以提高估计的精度,以往的研究在取样数量上可能会相对偏少。此外本研究采用蒙特-卡罗统计模拟方法对取样数量进行了估计,这对数据在不服从正态分布条件下的估计具有较好的精确性,也为与其它相关方法进行比较提供了较好的参考。本研究在计算过程中与大多数研究一样也主要是对数据进行求平均值的方式,并未考虑根系取样点位置的具体信息,这也在一定程度上无法精确反映细根生物量的分布情况。王树棠等[18],孙志虎等[15]通过地统计学的研究发现通过这一方法能较好的对林地根系生物量进行较好的估计。理论上讲,估计的准确性随取样数量的增加而提高[6],但根系采样需要耗费大量的时间,随采样数量的增加而引起的时间和花费的大量增加常常使大量采样变得不切实际[30]。因此在保证取样数量的同时,合理的改变野外取样方法或者采用更为精确的计算方法来推算生物量,以提高对细根生物量的估计精度将成为今后研究的重点。
| [1] | Ruess R W, Hendrick R L, Burton A J, Hendrick R L, Burton A J, Pregitzer K S, Sveinbjornssön B, Allen M F, Maurer G E. Coupling fine root dynamics with ecosystem carbon cycling in black spruce forests of interior Alaska. Ecological Monographs, 2003, 73(4): 643-662. |
| [2] | Vogt K A, Grier C C, Vogt D J. Production turnover and nutrient dynamics of above and belowground detritus of world forests. Advances in Ecological Research, 1986, 15: 303-377. |
| [3] | Brunner I, Godbold D L. Tree roots in a changing world. Journal of Forest Research, 2007, 12(2): 78-82. |
| [4] | 廖利平, 邓仕坚, 于小军, 韩士杰. 不同连栽代数杉木人工林细根生长、分布与营养物质分泌特征. 生态学报, 2001, 21(4): 569-573. |
| [5] | Metcalfe D, Meir P, Aragao L E O C, Da Costa A, Almeida S, Braga A, Goncalves P, Athaydes J, Malhi Y, Williams M. Sample sizes for estimating key ecosystem characteristics in a tropical terra firme rainforest. Forest Ecology and Management, 2008, 255(3/4): 558-566. |
| [6] | Bengough A G, Castrignano A, Pagès L, van Noordwijk M. Sampling strategies, scaling and statistics//Smit A L, Bengough A G, Engels C, van Noordwijk M, Pellerin S, van de Geijn S C, eds. Root Methods. Berlin Springer, 2000, 147-173. |
| [7] | 郭忠玲, 郑金萍, 马元丹, 韩士杰, 李庆康, 于贵瑞, 范春楠, 刘万德, 邵殿坤. 长白山几种主要森林群落木本植物细根生物量及其动态. 生态学报, 2006, 26 (9): 2855-2862. |
| [8] | Rytter R M. Biomass production and allocation, including fine-root turnover, and annual N up take in lysimeter-grown basket willows. Forest Ecology and Management, 2001, 140(2/3): 177-192. |
| [9] | Garten C T Jr, Kang S, Brice D J, Schadt C W, Zhou J Z. Variability in soil properties at different spatial scales (1 m-1 km) in a deciduous forest ecosystem. Soil Biology and Biochemistry, 2007, 39(10): 2621-2627. |
| [10] | Liski J. Variation in soil organic carbon and thickness of soil horizons within a boreal forest stand-effect of trees and implications for sampling. Silva Fennica, 1995, 29(4): 255-266. |
| [11] | Laiho R, Finér L. Changes in root biomass after water-level drawdown on pine mires in Southern Finland. Scandinavian Journal of Forest Research, 1996, 11(1/4): 251-260. |
| [12] | Chen W J, Zhang Q F, Cihlar J, Bauhus J, Price D T. Estimating fine-root biomass and production of boreal and cool temperate forests using aboveground measurements: a new approach. Plant Soil, 2004, 265:31-46. |
| [13] | Helmisaari H S, Derome J, NÖjd P, KuKKola M. Fine root biomass in relation to site and stand characteristics in Norway spruce and Scots pine stands. Tree Physiology, 2007, 27(10):1493-1504. |
| [14] | Berhongaray G, King J S, Janssens I A, Ceulemans R. An optimized fine root sampling methodology balancing accuracy and time investment. Plant and Soil, 2013, 366(1/2): 351-361. |
| [15] | 孙志虎, 王庆成. 采用地统计学方法对水曲柳人工纯林表层根量的估计. 生态学报, 2005, 25(4): 923-930. |
| [16] | 张春华, 王宗明, 任春颖, 宋开山, 张柏, 刘殿伟. 松嫩平原玉米带土壤碳氮储量的空间特征. 应用生态学报, 2010, 21(3): 631-639. |
| [17] | 黄超超, 黄锦学, 熊德成, 卢正立, 王韦韦, 杨智杰, 陈光水. 基于土芯法的亚热带常绿阔叶林细根空间变异与取样数量估计. 生态学报, 2013,33(18):5636-5643. |
| [18] | 王树堂, 韩士杰, 张军辉, 王存国, 徐媛, 李雪峰, 王树起. 长白山阔叶红松林表层土壤木本植物细根生物量及其空间分布. 应用生态学报, 2010, 21(3): 583-589. |
| [19] | 韦兰英, 上官周平. 黄土高原子午岭天然柴松林细根垂直分布特征. 西北农林科技大学学报:自然科学版, 2007, 35(7): 70-74. |
| [20] | Majdi H, Kangas P. Demography of fine roots in response to nutrient applications in a Norway spruce standin southwestern Sweden. Ecoscience, 1997, 4(2): 199-205. |
| [21] | 史建伟, 王孟本, 陈建文, 曹建庭. 柠条细根的空间分布特征及其季节动态. 生态学报, 2011, 31(3): 726-733. |
| [22] | 耿玉清, 单宏臣, 谭笑, 孙向阳, 王登芝. 人工针叶林林冠空隙土壤的研究. 北京林业大学学报, 2002, 24: 16-19. |
| [23] | Olsthoorn A F M. Klap J M, Oude Voshaar J H. The relation between fine root density and proximity of stems in closed Douglas-fir plantations on homogenous sandy soils: implications for sampling design. Plant and Soil, 1999, 211(2): 215-221. |
| [24] | Casper B B, Jackson R B. Plant competition underground. Annual Review of Ecology and Systematics, 1997, 28: 545-570. |
| [25] | 宇万太, 于永强. 植物地下生物量研究进展. 应用生态学报, 2001,12(6): 927-932. |
| [26] | Taylor B N, Beidler K V, Cooper E R, Strand A E, Pritchard S G. Sampling volume in root studies: the pitfalls of under-sampling exposed using accumulation curves. Ecology Letters, 2013, 16(7):862-869. |
| [27] | 李凌浩, 林鹏, 邢雪荣. 武夷山甜槠林细根生物量和生长量研究. 应用生态学报, 1998, 9(4): 337-340. |
| [28] | 杨玉盛, 陈光水, 何宗明, 陈银秀, 黄荣珍. 杉木观光木混交林细根的分布. 热带亚热带植物学报, 2002,10(2): 111-117. |
| [29] | Macinnis-Ng C M O, Fuentes S, O'Grady A P, Palmer A R, Taylor D, Whitley R J, Yunusa-I, Zeppel M J B, Eamus D. Root biomass distribution and soil properties of an open woodland on a duplex soil. Plant and Soil, 2010, 327(1/2): 377-388. |
| [30] | Metcalfe D B, Williams M, AragãoL E O C, da Costa A C, de Almeida S S, Braga A P, Goncalves P H L, de Athaydes J, Junior S, Malhi Y, Meir P. A method for extracting plant roots from soil which facilitates rapid sample processing without compromising measurement accuracy. New Phytologist, 2007, 174(3): 697-703. |
 2016, Vol. 36
2016, Vol. 36




