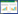文章信息
- 卢圣鄂, 王蓥燕, 陈勇, 涂仕华, 张小平, 辜运富
- LU Sheng'e, WANG Yingyan, CHEN Yong, TU Shihua, ZHANG Xiaoping, GU Yunfu.
- 不同施肥制度对石灰性紫色水稻土中氨氧化古菌群落结构的影响
- Impact of different long-term fertilization systems on ammonia oxidation Archaea community structures in Calcareous Purple Paddy soil
- 生态学报[J]. 2016, 36(21): 6919-6927
- Acta Ecologica Sinica[J]. 2016, 36(21): 6919-6927
- http://dx.doi.org/10.5846/stxb201504140752
-
文章历史
- 收稿日期: 2015-04-14
- 网络出版日期: 2016-03-03
2. 四川省农业科学院土壤肥料研究所, 成都 610066
2. Soil and Fertilizer Institute, Sichuan Academy of Agricultural Sciences, Chengdu 610066, China
自然界的氮循环主要包括硝化作用、固氮作用、反硝化作用和氨氧化作用4个过程,均由微生物驱动,而硝化作用是地球氮素循环中心环节,其中氨氧化(NH3→NO2-)是硝化作用的限速步骤,决定着硝化过程的速率[1]。传统观点认为变形菌纲的氨氧化细菌(AOB)是地球氮素循环过程硝化作用的主要承担者[2],但新近研究发现氨氧化古菌(AOA)广泛分布于海洋、土壤、温泉和湿地[3]等生态系统中,在全球氮素循环过程中起着重要的作用。AOA通过氨单加氧酶(AMO)控制氨氧化成亚硝酸盐的速率,amoA是编码氨单加氧酶活性位点多肽的基因,由于amoA基因自身较强保守性,被作为分子标记广泛应用于氨氧化微生物分子生态学研究[4]。
AOA是农田生态系统硝化过程的主要驱动者且受到农业管理措施的明显胁迫,施肥制度、土壤pH和土壤类型是影响AOA群落结构的重要因子[5-7]。长期定位施肥会对土壤中的硝化作用和氨氧化微生物的种群结构及丰度等形成明显影响[8-9]。土壤pH因直接影响土壤中氨态氮的有效性而影响氨氧化微生物的种群结构、数量和丰度等特征[6]。研究表明,在中性和碱性土壤上施用高量氮肥会显著改变AOB的群落组成和丰度,而对AOA的影响有限[10-12]。但在酸性土壤上的研究结论却与之相反,长期施肥会显著影响AOA群落结构特征[13-15]。综上,土壤类型不一样,不同施肥制度对土壤氨氧化微生物的影响也不尽一致,受施肥制度影响下的土壤AOA的垂直分布变化特征也尚不清楚。
石灰性紫色水稻土是四川乃至全国广泛分布的一种重要农业土壤,面积约4.00×106 hm2 [16]。该类土壤土质较疏松,有机质含量较低,氮、磷低,土体浅薄,保水抗旱能力差。为保护石灰性紫色水稻土质量,规范施肥管理措施,四川省于20世纪80年代在该类土壤上建立了“NPK长期肥效试验”。本文探索了石灰性紫色水稻土AOA群落结构对不同施肥制度的响应特征和垂直分布变化,以期为认识不同施肥制度下石灰性紫色水稻土的氮素循环特征及微生物驱动机制,保护石灰性紫色水稻土质量提供基础理论依据。
1 材料与方法 1.1 实验设计长期定位实验点位于四川遂宁市船山区联盟乡二村五组(30°10′50′′N,105°03′26′′E),气候为亚热带季风气候,全年气候温和,雨量充沛。土壤为原生钙质紫色土属,遂宁组母质,二泥田土种。试验始于1982年,完全随机区组设计,共8个处理:(1) 不施肥(CK);(2) 氮肥(N);(3) 氮磷肥(NP);(4) 氮磷钾肥(NPK);(5) 农家肥(M:主成分为猪厩肥,有机质含量1.5 mg/kg);(6) 氮肥+农家肥(NM);(7) 氮磷肥+农家肥(NPM);(8) 氮磷钾肥+农家肥(NPKM)。肥料施用量:氮肥(N)55.2 kg/hm2;钾肥(KCl)31.5 kg/hm2;磷肥(P2O5)13.2 kg/hm2;农家肥3×104 kg/hm2,等氮量设计。实验开始时土壤的养分情况为:pH 8.6,有机质15.9 g/kg,全氮0.109%,碱解氮66.3 mg/kg,全钾2.689%,有效钾130.6 mg/kg,缓效钾699.4 mg/kg,全磷0.135%,有效磷3.9 mg/kg。
1.2 土样采集与预处理于2013年7月1日水稻淹水种植期间,在小区内按“梅花型”布点取样,用土钻分别钻取0—20 cm(L1) ,20—40 cm(L2) ,40—60 cm(L3) 和60—90 cm(L4) 深的土样,分层混匀,用无菌PET树脂袋封装放于冰盒中带回实验室。取混合均匀的新鲜土样立即提取土壤总DNA,另取部分土样于室温下风干后进行土壤理化性质测定,剩余土样于-20 ℃保存备用。
1.3 土壤基本理化性质测定测定方法参照鲁如坤土壤农业化学分析方法[17]。
1.4 土壤AOA群落结构的PCR-DGGE分析 1.4.1 土壤微生物总DNA提取采用Fast DNA Spin Kit for Soil(Qbiogene,Carlsbad,CA,USA)的试剂盒方法,称取0.5 g新鲜土壤样品,重复3次,按试剂盒上的步骤进行土壤微生物总DNA的提取。
1.4.2 amoA基因的PCR扩增PCR引物CrenamoA-23f的序列:5′-ATGGTCTGGCTWAGACG-3′,引物CrenamoA-616r的序列:5′-GCCATCCATCTGTATGTCCA-3′[18]。反应体系:PCR Master Mix(TIANGEN BIOTECH. BEIJING)25 μL,每种引物0.5 μL(25 pmol/μL,10 ng土壤总DNA,加ddH2O至终体积50 μL。反应程序:预变性95 ℃ 5 min,变性95 ℃ 30 s,退火温度52 ℃ 30 s,延伸温度72 ℃ 45 s,共进行32个循环,72 ℃ 10 min,最后于4 ℃恒温保存。取PCR产物各2 μL,1.0%琼脂糖凝胶电泳检测,凝胶成像系统(Gel Doc Documentation System,Bio-Rad,USA)下观察。
1.4.3 DGGE分析取PCR产物15 μL进行DGGE分析,变性剂梯度为30%—60%,聚丙烯酰胺凝胶浓度8%(100%的变性剂为尿素7 mol和40%的去离子甲酰胺)。在1×TAE缓冲液中,50 V 30 min进胶,再在150 V 60 ℃下电泳5 h,电泳后用硝酸银[19]对凝胶进行染色,然后用数码相机拍照。利用凝胶成像系统(Gel Doc Documentation System,Bio-Rad,USA)中自带的Quantity One 4.4软件对DGGE图谱进行分析。
1.5 DGGE条带的克隆及测序PCR产物用Clean-UpTM试剂盒(MO BIO Labs,Solana Beach,CA,USA)进行纯化,纯化后的PCR产物与pGEM-T Vector进行连接,利用E. coli DH5α感受态细胞进行转化,用氨苄青霉素(100 mg/L)抗性和PCR进行检测,采用蓝白斑筛选阳性克隆子,送上海生物工程技术有限公司进行测序。
1.6 数据处理基础数据的处理利用Excel 2007进行,Duncan单因素方差分析用SPSS 17.0完成。DGGE图谱利用Bio-Rad公司的Quantity One 4.4分析。用MEGA 6.0构建AOA amoA基因系统发育树。用Shannon多样性指数(H),丰富度(S)和均匀度(EH)等评价AOA群落结构多样性。采用CANOCO 4.5.1 软件(Microcomputer Power,Ithaca,USA)分析AOA群落结构和土壤理化因子间的关系。多样性指数计算公式为:H=-∑(ni/N)ln(ni/N),EH=H/lnS,式中ni为单一条带的强度,N为所有条带的总强度,S为每一泳道总的条带数。
2 结果与分析 2.1 土壤理化性质不同施肥制度对石灰性紫色水稻土理化性质产生明显影响(表 1)。相对于无肥处理(pH=7.53) ,农家肥配施无机肥处理下的土壤pH介于7.24—7.41之间,显示施肥会降低土壤pH。就不同土壤深度而言,0—20 cm土壤的pH低于其它深度。无机肥处理下的土壤有机质含量介于1.44%—3.85%之间,农家肥与无机肥配施下的土壤有机质介于1.91%—3.28%之间,而CK处理下的有机质含量为1.7%。而农家肥与化肥配施会增加土壤总氮含量。就不同深度而言,0—20 cm土壤的总氮含量高于其它深度。农家肥配施化肥会降低土壤硝氮含量,总体上,0—20 cm土壤的硝态氮含量高于其它层次。相对于无肥和化肥处理,配施农家肥的4种施肥处理(M,NM,NPM,NPKM)下的氨态氮变化比较平稳。施肥会增加表层土(0—20 cm)中的氨态氮含量,不同深度土壤的氨态氮含量变化趋势不明显。
| 施肥处理 Fertilizer treatments | 酸碱度pH | 土壤有机质SOM | 全氮TN | 硝态氮Nitrate | 氨态氮Ammonium | |||||||||||||||
| L1 | L2 | L3 | L4 | L1 | L2 | L3 | L4 | L1 | L2 | L3 | L4 | L1 | L2 | L3 | L4 | L1 | L2 | L3 | L4 | |
| CK | 7.03a | 7.53ab | 7.71a | 7.64cd | 1.7e | 1.31c | 0.40f | 1.36bc | 0.11d | 0.10c | 0.04c | 0.08b | 6.70a | 2.52cd | 2.77a | 1.12cd | 3.93c | 8.71bc | 7.12bc | 7.61a |
| N | 7.24bc | 7.55bc | 7.71a | 7.66cd | 1.44f | 0.53e | 1.46bc | 0.96d | 0.14cd | 0.03d | 0.11b | 0.07b | 3.80c | 4.56a | 2.08ab | 1.03cd | 6.16bc | 12.2a | 7.59bc | 7.96a |
| NP | 7.27b | 7.59cd | 7.68ab | 7.62d | 1.71e | 0.59e | 1.02de | 1.95a | 0.14cd | 0.06cd | 0.09b | 0.12a | 5.49b | 3.64b | 2.76a | 5.03a | 9.87a | 6.07cd | 8.85a | 4.62b |
| NPK | 7.41bc | 7.51a | 7.63b | 7.66cd | 3.85a | 0.25e | 1.85a | 1.42bc | 0.256a | 0.02d | 0.14a | 0.08b | 2.43d | 2.12de | 1.01cd | 1.89bc | 5.14bc | 5.75cd | 5.85cd | 4.32b |
| M | 7.44c | 7.62de | 7.71a | 7.76a | 1.91d | 0.85d | 0.87e | 1.46b | 0.16ab | 0.08c | 0.10b | 0.09ab | 1.14e | 2.68c | 2.01bc | 2.11b | 7.98ab | 6.41c | 6.51bc | 4.51b |
| NM | 7.43c | 7.72f | 7.72a | 7.72ab | 2.64c | 2.42a | 1.65ab | 1.52b | 0.12bc | 0.21a | 0.07bc | 0.08b | 3.45c | 2.25de | 1.39cd | 2.02b | 7.79ab | 2.74d | 5.50cd | 7.79a |
| NPM | 7.48c | 7.72f | 7.71a | 7.72a | 2.75c | 1.95b | 1.00e | 1.21c | 0.18bc | 0.15b | 0.07bc | 0.08b | 5.78b | 1.41e | 0.52d | 2.31b | 7.37ab | 10.0ab | 8.26ab | 5.76ab |
| NPKM | 7.46c | 7.65e | 7.73a | 7.72bc | 3.28b | 1.25c | 1.26cd | 1.44bc | 0.18bc | 0.08c | 0.09b | 0.10ab | 2.1e | 2.39de | 2.71bc | 0.53d | 8.29bc | 7.98cd | 5.39d | 6.75b |
| SOM:土壤有机质 Soil organic matter;TN:全氮 Total nitrogen;CK:对照;N:氮肥 Nitrogen;NP:氮磷肥 Nitrogen and phosphorus;NPK:氮磷钾肥 Nitrogen;phosphorus and potassium;M:农家肥 Manure;NM:氮肥+农家肥 Nitrogen+manure;NPM:氮磷肥+农家肥 Nitrogen and phosphorus+ manure;NPKM:氮磷钾肥+农家肥 Nitrogen;phosphorus and potassium+ manure | ||||||||||||||||||||
不同施肥处理土壤AOA群落结构的DGGE图谱见图 1。不同施肥处理土壤AOA的DGGE图谱在电泳条带数量、强弱和位置均存在一定程度的差异,显示不同施肥制度影响了石灰性紫色水稻土的AOA群落结构。图中共同的条带(a、b、c和d箭头所示),说明供试土壤在不同采样深度存在共有的AOA类群,但其亮度不同,表明长期不同施肥处理AOA在DNA水平上有改变。不同深度土壤AOA种群结构表现出明显差异。在0—20 cm处,不同施肥制度下土壤AOA种群结构变化不明显。土壤深度增加,AOA丰富度减小,AOA群落结构表现出差异。在20—40 cm处,N处理下AOA群落结构最简单,NPK和NPKM肥料处理下的AOA群落结构最复杂;在40—60 cm深度,N处理的AOA群落结构最简单,CK其次,而氮肥配施农家肥处理下的AOA最复杂;在60—90 cm深度,CK处理下的AOA群落结构最简单,NP处理下的AOA群落结构最复杂。
|
| 图 1 石灰性紫色水稻土AOA 的DGGE图谱分析 Fig. 1 DGGE profile of AOA communities of the Calcareous Purple Paddy soil L1:0—20cm深度,L2:20—40 cm深度,L3:40—60 cm深度,L4:60—90 cm深度; 施肥处理从左到右依次为无肥(CK);氮肥(N);氮磷肥(NP);氮磷钾肥(NPK);农家肥(M);氮肥加农家肥(NM);氮磷肥加农家肥(NPM);氮磷钾肥加农家肥(NPKM); 字母a、b、c、d表示各处理间的共同条带;其中L1-1-2等编号表示切胶回收条带 |
不同施肥制度下不同深度土壤AOA多样性指数(H)、丰富度(S)、均匀度(EH)存在显著差异(P<0.05) (表 2)。在0—20 cm处,不同施肥制度下土壤AOA群落结构多样性和丰富度变化不明显。伴随着土壤深度的增加,AOA多样性和丰富度减小。在20—40 cm处,N肥处理下AOA多样性指数和丰富度最低,NPKM肥料处理下的AOA多样性指数和丰富度最高;40—60 cm处也是N肥处理下土壤AOA多样性指数和丰富度最低,CK其次,NM肥处理下的AOA最高;在60—90 cm深度,CK处理下的AOA多样性指数和丰富度最低,NP处理下的AOA最高。
| 施肥处理 Fertilizer treatments | Shannon 多样性指数 Shannon′s diversity index (H) | 均匀度 Evenness (EH) | 丰富度 Richness (S) | |||||||||
| L1 | L2 | L3 | L4 | L1 | L2 | L3 | L4 | L1 | L2 | L3 | L4 | |
| CK | 2.38c | 2.40c | 1.88e | 1.78e | 0.992a | 0.937d | 0.967cd | 0.916f | 12c | 11c | 7c | 6d |
| N | 2.54ab | 2.23b | 1.68f | 2.25ab | 0.991ab | 0.870e | 0.949c | 0.939d | 13bc | 10d | 7c | 7c |
| NP | 2.61a | 2.46c | 2.25c | 2.47a | 0.991ab | 0.988b | 0.984a | 0.978a | 15a | 13a | 10bc | 11a |
| NPK | 2.46b | 2.58a | 2.16d | 2.17cd | 0.988b | 0.979bc | 0.956d | 0.942cd | 14b | 13a | 10bc | 9b |
| M | 2.46b | 2.40c | 2.40b | 2.21a | 0.991ab | 1.004b | 0.955e | 0.921e | 14b | 12b | 11b | 10ab |
| NM | 2.46b | 2.40c | 2.43a | 2.06d | 0.986b | 0.866f | 0.975bc | 0.939d | 15a | 12b | 11b | 9b |
| NPM | 2.36d | 2.49bc | 2.35c | 2.18c | 0.988b | 0.946c | 0.976b | 0.945c | 14b | 12b | 12a | 10ab |
| NPKM | 2.36d | 2.54b | 2.37bc | 2.24b | 0.985c | 1.024a | 0.973c | 0.966b | 13bc | 13a | 11b | 10ab |
| 数字后具相同字母表示差异不显著,数字后具不同字母表示差异显著(Duncan 新复极差法测验P=0.05) | ||||||||||||
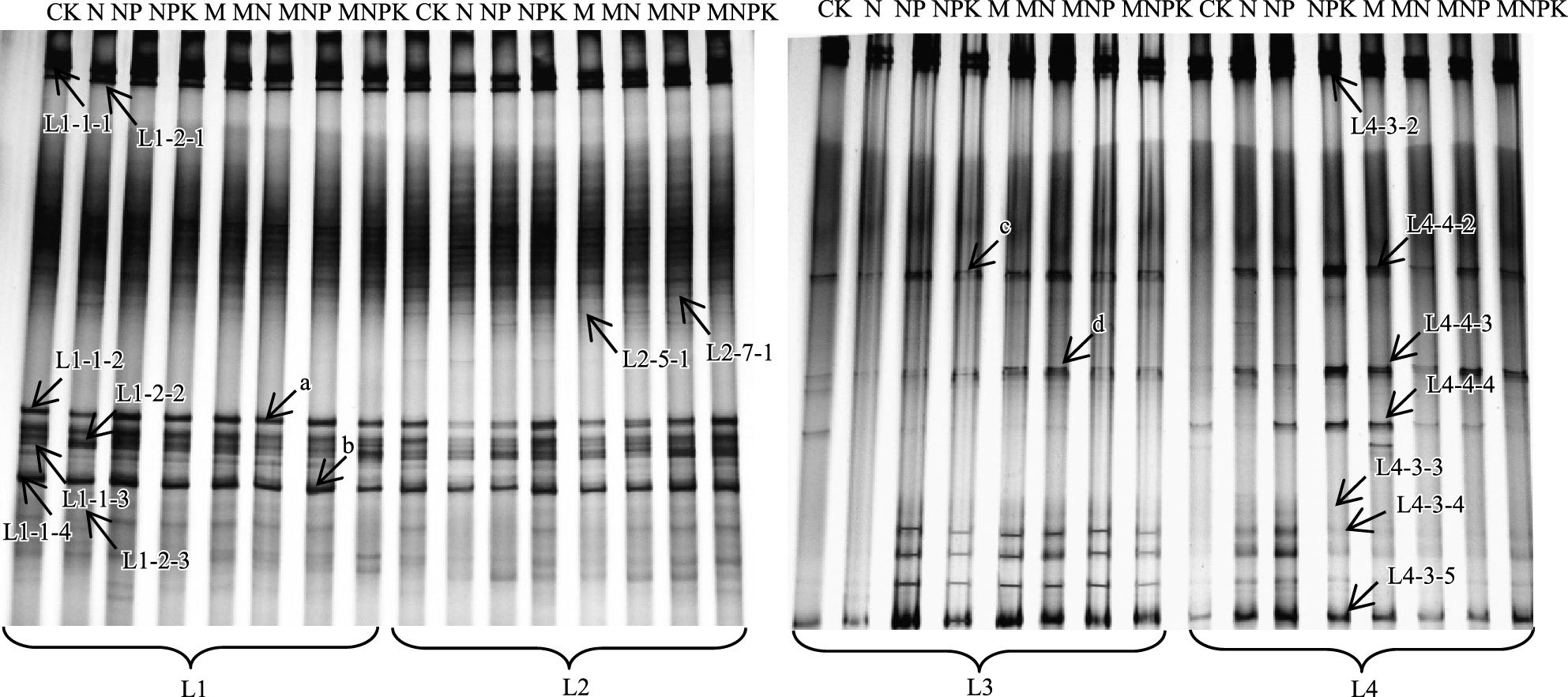
对石灰性紫色水稻土中优势AOA序列和GenBank数据库中的相关序列比对后利用MEGA 6.0进行系统发育分析(图 2),结果将16条序列主要分成2个群。第1个群与来源于底泥和土壤中的氨氧化古细菌amoA基因相似,分为3个簇;第2个群与底泥和水体样品相关,分为1个簇,并与已知氨氧化古菌Candidatus Nitrososphaera gargensis(GI:EU281321) 聚在一起。与该类土中AOA亲缘关系较近的已知基因序列既有来自土壤的,又有来自沉积物和水体的。在16条DGGE图谱切胶回收条带中,KP400767,KP400765与长江河口沉积物古菌序列KC735504聚在一起;KP400756,KP400753和崇明东部潮滩沉积物古菌序列JQ345856聚在一起;KP400760,KP400766与淹水稻田土古菌序列KJ908047聚在一起;KP400768,KP400757与高原湖泊沉积物古菌序列KJ005035聚在一起;KP400764,KP400761与淹水稻田土古菌序列KJ907957聚在一起;KP400758,KP400763分别与高海拔湿地沉积物古菌序列KJ645381,水稻土古菌序列KJ542817聚在一起;KP400762,KP400755分别与大运河古菌序列KF537053、长江河口古菌序列KC735430聚在一起;系统发育结果显示石灰性紫色水稻土AOA群落结构较复杂。石灰性紫色水稻土中的氨氧化古细菌均属于奇古菌门,与已知氨氧化古菌Candidatus Nitrososphaera gargensis(GI:EU281321) 相似。
|
| 图 2 石灰性紫色水稻土中AOA amoA基因的系统发育树(加粗的编号为本实验所得序列) Fig. 2 Phylogentic tree of the archaea amoA gene sequences retrieved from the Calcareous Purple Paddy soil amended with different fertilization systems,the bold codes refers the sequences obtained in this study |
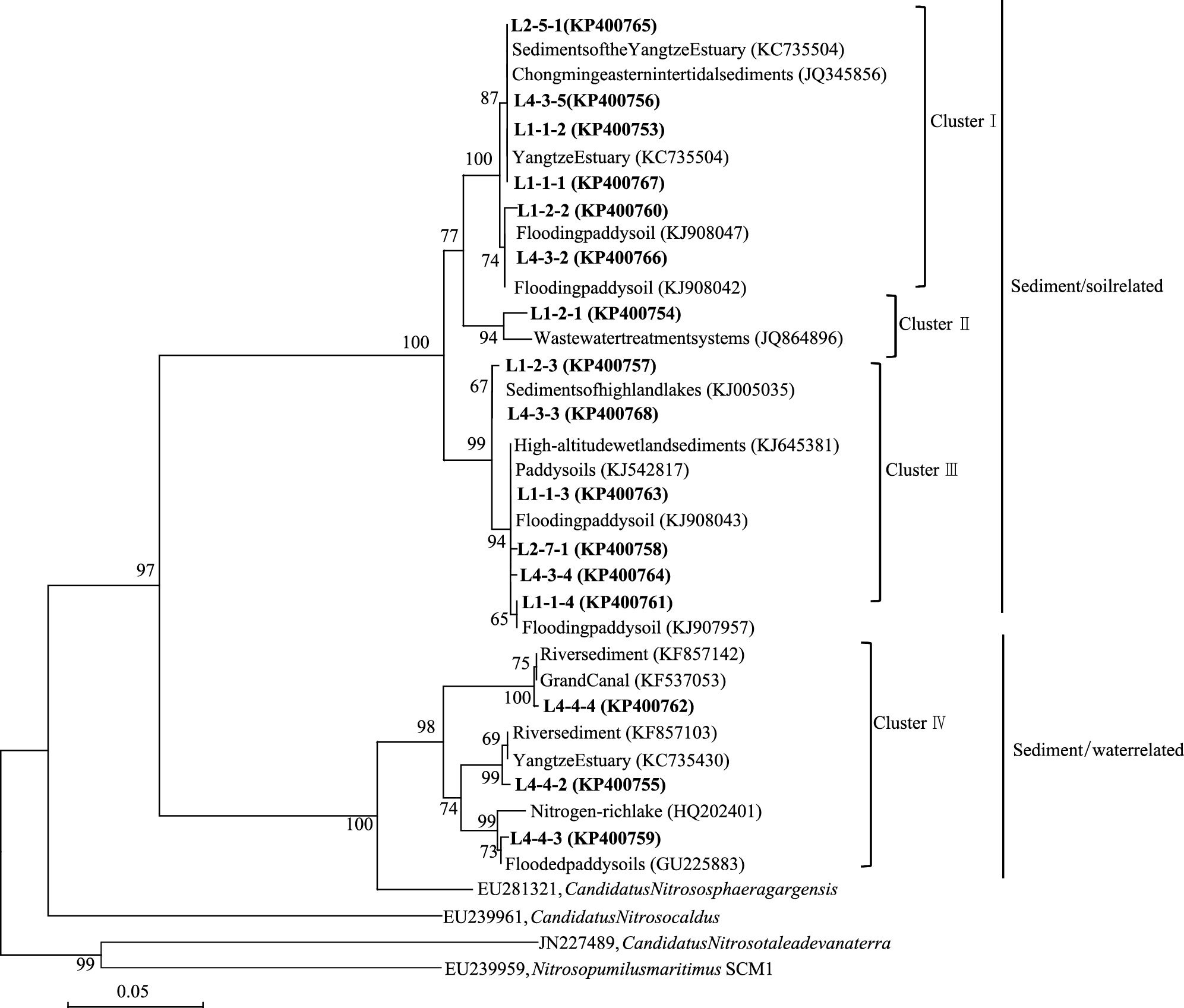
将DGGE图谱条带的位置和亮度分别类比于物种的种类和数量[20],运用冗余分析(RDA)进行AOA群落结构与环境参数间相关性分析(图 3)。冗余分析图中箭头表示环境因子,箭头所处的象限表示环境因子与排序轴间的正负相关性,箭头连线长度表示该环境因子与样本分布相关程度的大小,箭头连线间的夹角代表环境因子间的相关程度[21]。排序轴特征值分别为0.112、0.035、0.018和0.016,分别解释了11.2%、3.5%、1.8%和1.6%的AOA群落变化,pH的影响高于其它环境因子。从图中可以看出土壤pH(P=0.012) 是造成影响群落差异的主要因素,对AOA群落结构具有显著影响。AP(P=0.76) ,TN(P=0.364) ,NH3+-N(P=0.402) ,SOM (P=0.49) ,P>0.05,对AOA群落没有显著影响。
|
| 图 3 氨氧化古菌群落与环境因子变化的RDA排序图 Fig. 3 RDA ordination diagram of ammonia oxidation archaea communities associated with environmental variable 图中数字为土样编号; 1—8采自L1深度,对应施肥处理分别为:CK,N,NP,NPK,M,NM,NPM,NPKM;编号9—16采自L2深度,数字由小到大分别对应L1中1—8对应的施肥处理;17—24为L3深度,数字由小到大分别对应L1中1—8对应的施肥处理;25—32为L4深度样品,数字由小到大分别对应L1中1—8对应的施肥处理 |
农业管理措施是影响土壤中各种微生物活动、群落结构等的重要因素,如翻耕、灌溉、施肥等因素都会影响到土壤中各种微生物的多样性[22]。实验结果表明,在0—20 cm处,不同施肥制度下土壤AOA群落结构变化不明显。土壤深度增加,AOA丰富度减小,群落结构出现差异。在20—40 cm处,N肥处理下AOA多样性指数和丰富度最低,NPKM肥料处理下的AOA多样性指数和丰富度最高;40—60 cm深度,寡氮处理下AOA多样性指数和丰富度最低,CK其次,而NM处理下的AOA最高;在60—90 cm深度,CK处理AOA多样性指数和丰富度最低,NP处理下的最高。Shen等[11]研究表明,在中性和碱性土壤上施用高量氮肥会显著改变AOB的群落组成和丰富度,而对AOA的影响有限。但在酸性土上的研究结论却与之相反,Wu等[12]研究证实长期施肥会显著影响AOA群落结构特征,且AOA比AOB在硝化作用中起更重要的作用[23]。本文通过研究长期定位施肥对石灰性紫色水稻土AOA群落结构的影响,显示不同施肥制度下的土壤AOA种群结构在0—20 cm变化不明显,这与前人的研究结果一致[11, 24]。总体而言,石灰性紫色水稻土表层土壤AOA群落结构对不同施肥制度响应不明显;土壤深度增加,不同施肥制度下AOA群落结构和丰富度表现出差异。
3.2 不同土壤深度对AOA群落结构的影响土壤是一个复杂的异质体系,土壤奇古菌分布不仅与土壤养分状况紧密相关,也与不同土壤深度理化性质的相互作用有很大的关系[25-26]。本试验显示石灰性紫色水稻土L1、L2深度中的AOA群落丰富度S高于L3、L4深度,其中L1深度AOA丰富度S最高。可能是因为水稻淹水时土壤处于厌氧状态,而水稻根系能够分泌O2,为水稻根层提供充足的氧,来支持非专一性的好氧反应。另有研究表明,奇古菌门(Thaumarchaeota)硝化球菌属的AOA更偏好根际的生长环境[27]。且土壤表层养分更充足,AOA可用来为自己提供能量的底物更多。向燕等[28]研究表明太湖沉积物中AOA群落结构垂直分布变化不明显。但梁龙等[29]等的研究却发现AOA的数量在百花湖沉积物中存在比较明显的分层现象,其中深层沉积物(22—30 cm)中的AOA数量是浅层沉积物(1—21 cm)的2倍左右。上述研究反映出,AOA群落结构在环境样品垂直方向上的变化会受到样品特性的显著影响。而石灰性紫色水稻土中的AOA群落结构表现出明显的垂直减少特征,分析原因可能是不同土壤深度的养分状况、通气性等理化性质有较明显差异,会选择性胁迫氨氧化古菌群落的演化,从而导致氨氧化古菌对不同土壤深度产生特异的生态适应[30-32]。
3.3 土壤环境参数对AOA群落的影响土壤微生物生境的改变往往造成其群落特征发生变化,RDA则直接将环境变量作为约束条件考虑到排序分析中,从而解释环境因子对微生物群落结构的影响[33]。本文RDA分析显示,排序轴特征值分别为0.112、0.035、0.018和0.016,分别解释了11.2%、3.5%、1.8%和1.6%的AOA群落变化,pH的影响高于其他环境因子,显示土壤pH是造成影响石灰性紫色水稻土AOA群落结构变化的主要因素。而AP,TN,NH3+-N,SOM对AOA群落没有显著影响。与本文结果相似,Zhou等研究发现紫色土中AOA群落结构多样性与pH成正相关[8]。而对南中国地区水稻土氨氧化古菌和氨氧化细菌群落结构的研究中亦发现pH是影响AOA群落结构变化的关键因子[6]。
4 结论本文显示不同深度石灰性紫色水稻土中AOA受不同施肥制度影响各不相同,土壤深度增加,施肥对土壤AOA群落结构的影响愈加明显。石灰性紫色水稻土中的AOA均属于奇古菌门(Thaumarchaeota),与已知氨氧化古菌Candidatus Nitrososphaera gargensis(GI:EU281321) 相似。pH是影响石灰性紫色水稻土AOA群落结构的重要因子。
| [1] | Prosser J I. Autotrophic nitrification in bacteria. Advances in Microbial Physiology , 1990, 30 : 125–181. DOI:10.1016/S0065-2911(08)60112-5 |
| [2] | Purkhold U, Pommerening-Röser A, Juretschko S, Schmid M C, Koop H P, Wagner M. Phylogeny of all recognized species of ammonia oxidizers based on comparative 16S rRNA and amoA sequence analysis:Implications for molecular diversity surveys. Applied and Environmental Microbiology , 2000, 66 (3) : 5368–5382. |
| [3] | Leininger S, Urich T, Schloter M, Schwark L, Qi J, Nicol G W, Prosser J I, Schuster S C, Schleper C. Archaea predominate among ammonia-oxidizing prokaryotes in soils. Nature , 2006, 442 (7104) : 806–809. DOI:10.1038/nature04983 |
| [4] | 郑有坤, 王宪斌, 辜运富, 张小平. 若尔盖高原湿地土壤氨氧化古菌的多样性. 微生物学报 , 2014, 54 (9) : 1090–1096. |
| [5] | Chen X, Zhang L M, Shen J P, Xu Z H, He J Z. Soil type determines the abundance and community structure of ammonia-oxidizing bacteria and archaea in flooded paddy soils. Journal of Soils and Sediments , 2010, 10 (8) : 1510–1516. DOI:10.1007/s11368-010-0256-9 |
| [6] | Li H, Weng B S, Huang F Y, Su J Q, Yang X R. pH regulates ammonia-oxidizing bacteria and archaea in paddy soils in Southern China. Applied Microbiology and Biotechnology , 2015, 99 (14) : 6113–6123. DOI:10.1007/s00253-015-6488-2 |
| [7] | 贾仲君, 翁佳华, 林先贵, ConradR. 氨氧化古菌的生态学研究进展. 微生物学报 , 2010, 50 (4) : 431–437. |
| [8] | Zhou Z F, Shi X J, Zheng Y, Qin Z X, Xie D T, Li Z L, Guo T. Abundance and community structure of ammonia-oxidizing bacteria and archaea in purple soil under long-term fertilization. European Journal of Soil Biology , 2014, 60 : 24–33. DOI:10.1016/j.ejsobi.2013.10.003 |
| [9] | 武传东, 闫倩, 辛亮, 王保莉, 曲东. 长期施用氮肥和磷肥对渭北旱塬土壤中氨氧化古菌多样性的影响. 农业环境科学学报 , 2012, 31 (4) : 743–749. |
| [10] | Chu H Y, Fujii T, Morimoto S, Lin X G, Yagi K, Hu J L, Zhang J B. Community structure of ammonia-oxidizing bacteria under long-term application of mineral fertilizer and organic manure in a sandy loam soil. Applied and Environmental Microbiology , 2007, 73 (2) : 485–491. DOI:10.1128/AEM.01536-06 |
| [11] | Shen J P, Zhang L M, Zhu Y G, Zhang J B, He J Z. Abundance and composition of ammonia-oxidizing bacteria and ammonia-oxidizing archaea communities of an alkaline sandy loam. Environmental Microbiology , 2008, 6 (10) : 1601–1611. |
| [12] | Wu Y C, Lu L, Wang B Z, Lin X G, Zhu J G, Cai Z C, Yan X Y, Jia Z J. Long-term field fertilization significantly alters community structure of ammonia-oxidizing bacteria rather than archaea in a paddy soil. Soil Science Society of America Journal , 2011, 75 (4) : 1431–1439. DOI:10.2136/sssaj2010.0434 |
| [13] | He J Z, Shen J P, Zhang L M, Zhu Y G, Zheng Y M, Xu M G, Di H J. Quantitative analyses of the abundance and composition of ammonia-oxidizing bacteria and ammonia-oxidizing archaea of a Chinese upland red soil under long-term fertilization practices. Environmental Microbiology , 2007, 9 (9) : 2364–2374. DOI:10.1111/emi.2007.9.issue-9 |
| [14] | Chen X, Zhang L M, Shen J P, Wei W X, He J Z. Abundance and community structure of ammonia-oxidizing archaea and bacteria in an acid paddy soil. Biology and Fertility of Soils , 2011, 47 (3) : 323–331. DOI:10.1007/s00374-011-0542-8 |
| [15] | Alam M S, Ren G D, Lu L, Zheng Y, Peng X H, Jia Z J. Conversion of upland to paddy field specifically alters the community structure of archaeal ammonia oxidizers in an acid soil. Biogeosciences , 2013, 10 (8) : 5739–5753. DOI:10.5194/bg-10-5739-2013 |
| [16] | Zhu B, Wang T, You X, Gao M R. Nutrient release from weathering of purplish rocks in the Sichuan Basin, China. Pedosphere , 2008, 18 (2) : 257–264. DOI:10.1016/S1002-0160(08)60015-6 |
| [17] | 鲁如坤. 土壤农业化学分析方法. 北京: 中国农业科技出版社, 2000. |
| [18] | Tourna M, Freitag T E, Nicol G W, Prosser J I. Growth, activity and temperature responses of ammonia-oxidizing archaea and bacteria in soil microcosms. Environmental Microbiology , 2008, 10 (5) : 1357–1364. DOI:10.1111/j.1462-2920.2007.01563.x |
| [19] | Riesner D D, Steger G, Zimmat R, Owens R A, Wagenhöfer M, Hillen W, Vollbach S, Henco K. Temperature-gradient gel electrophoresis of nucleic acids:analysis of conformational transitions, sequence variations, and protein-nucleic acid interactions. Electrophoresis , 1989, 10 (5/6) : 377–389. |
| [20] | 杜萍, 刘晶晶, 沈李东, 胡宝兰, 曾江宁, 陈全震, 寿鹿, 廖一波. Biolog和PCR-DGGE技术解析椒江口沉积物微生物多样性. 环境科学学报 , 2012, 32 (6) : 1436–1444. |
| [21] | 秦华, 李国栋, 叶正钱, 徐秋芳, 曹志洪. 集约种植雷竹林土壤细菌群落结构的演变及其影响因素. 应用生态学报 , 2010, 21 (10) : 2645–2651. |
| [22] | 李娟, 赵秉强, 李秀英, HwatB S. 长期有机无机肥料配施对土壤微生物学特性及土壤肥力的影响. 中国农业科学 , 2008, 41 (1) : 144–152. |
| [23] | Zhang L M, Hu H W, Shen J P, He J Z. Ammonia-oxidizing archaea have more important role than ammonia-oxidizing bacteria in ammonia oxidation of strongly acidic soils. International Society for Microbial Ecology , 2012, 6 (5) : 1032–1045. |
| [24] | 秦子娴. 长期施肥中性紫色水稻土氮素矿化及氨氧化菌的分子生态学研究[D]. 重庆:西南大学, 2014. |
| [25] | Fan H X, Fairley D J, Rensing C, Pepper I L, Wang G J. Identification of similar non-thermophilic Crenarchaeota in four Chinese and America pristine soils. Biodiversity Science , 2006, 14 (3) : 18l–187. |
| [26] | Ke X B, Angel R, Lu Y H, Conrad R. Niche differentiation of ammonia oxidizers and nitrite oxidizers in rice paddy soil. Environmental Microbiology , 2013, 15 (8) : 2275–2292. DOI:10.1111/emi.2013.15.issue-8 |
| [27] | Nicol G W, Glover L A, Prosser J I. The impact of grassland management on archaeal community structure in upland pasture rhizosphere soil. Environmental Microbiology , 2003, 5 (3) : 152–162. DOI:10.1046/j.1462-2920.2003.00399.x |
| [28] | 向燕, 吴宇澄, 刘国锋, 刘正文, 吴庆龙. 太湖竺山湾沉积物中氨氧化原核生物的垂直分布与多样性. 生态学报 , 2010, 30 (6) : 1423–1430. |
| [29] | 梁龙, 梁小兵. 氨氧化细菌和氨氧化古菌在百花湖沉积物中的垂直分布. 矿物岩石地球化学通报 , 2014, 33 (2) : 221–225. |
| [30] | Briones A M, Okabe S, Umemiya Y, Ramsing N B, Reichardt W, Okuyama H. Influence of different cultivars on populations of ammonia-oxidizing bacteria in the root environment of rice. Applied and Environmental Microbiology , 2002, 68 (6) : 3067–3075. DOI:10.1128/AEM.68.6.3067-3075.2002 |
| [31] | Nicolaisen M H, Risgaard-Petersen R, Revsbech N P, Reichardt W, Ramsing N B. Nitrification-denitrification dynamics and community structure of ammonia-oxidizing bacteria in high yield irrigated Philippine rice field. FEMS Microbiology Ecology , 2004, 49 (3) : 359–369. DOI:10.1016/j.femsec.2004.04.015 |
| [32] | Wang Y N, Ke X B, Wu L Q, Lu Y H. Community composition of ammonia-oxidizing bacteria and archaea in rice field soil as affected by nitrogen fertilization. Systematic and Applied Microbiology , 2009, 32 (1) : 27–36. DOI:10.1016/j.syapm.2008.09.007 |
| [33] | 尹锴, 崔胜辉, 赵千钧, 花利忠, 石龙宇, 吝涛. 基于冗余分析的城市森林林下层植物多样性预测. 生态学报 , 2009, 29 (11) : 6085–6094. |
 2016, Vol. 36
2016, Vol. 36