文章信息
- 戴雅婷, 侯向阳, 闫志坚, 吴洪新, 解继红, 张晓庆, 高丽
- DAI Yating, HOU Xiangyang, YAN Zhijian, WU Hongxin, XIE Jihong, ZHANG Xiaoqing, GAO Li.
- 库布齐沙地两种植被恢复类型根际土壤微生物和土壤化学性质比较研究
- Soil microbes and the chemical properties of the rhizosphere and non-rhizosphere soil under two types of vegetation restoration in the hobq sandy land of inner mongolia, China
- 生态学报[J]. 2016, 36(20): 6353-6364
- Acta Ecologica Sinica[J]. 2016, 36(20): 6353-6364
- http://dx.doi.org/10.5846/stxb201504190802
-
文章历史
- 收稿日期: 2015-04-19
- 网络出版日期: 2016-01-22
2. 农业部牧草资源与利用重点实验室, 呼和浩特 010010
2. Key Laboratory of Grassland Resources and Utilization, Ministry of Agriculture, Huhhot 010010, China
植被恢复是荒漠化生态系统恢复与重建的第一步, 是改善生态环境的关键, 已成为恢复生态学的研究重点之一[1]。植被恢复过程中, 植物根系通过分泌物、根产物和植物残体等形式, 不仅影响根际土壤微生物生长代谢和种群结构, 而且改变了根际土壤的化学物理环境[2], 而较好的土壤养分条件又可以促进植被生长发育, 进而促进植被演替进程[3]。因此, 通过了解不同植被类型根际与非根际土壤理化及生物学等性质, 可以直接或间接反映植被对土壤的改良作用及植被恢复的生态效果。
根际是连接植物、土壤和微生物的纽带, 许多重要的土壤生态过程都发生在这一微小区域, 随着恢复生态学研究的深入以及多学科交叉, 根际土壤环境的研究不断受到重视, 已成为生态学、土壤学、微生物学、环境学等学科交叉研究的热点, 国内外研究主要集中在根际与非根际土壤理化性质、土壤微生物多样性、土壤酶活性等方面[4-7]。在现有研究报道中, 仅有少量学者在黄土丘陵区、西宁南山区开展了根际微域角度的植被恢复评价研究[8-9], 对于鄂尔多斯高原干旱、半干旱区不同植被恢复类型根际和非根际土壤养分、生物学性质比较分析及土壤质量评价的相关研究较少。
库布齐沙地是我国西北沙漠与东部农业的生态屏障, 也是具有特殊地理景观的生态过渡地带。多年来, 由于自然和人为的影响, 该地区植被破坏严重, 土壤沙化和荒漠化问题严重, 使其成为退化生态系统恢复与重建的重点区域。加快植被恢复和提高土壤质量是库布齐沙地水土保持、防风固沙和生态系统恢复的主要目标。在库布齐沙地植被恢复的过程中形成了自然恢复状态下的植被群落和人工种植的植被群落类型, 其中油蒿是当地
天然分布的优良固沙植被, 其枝条分枝角度大, 空间扩展能力强, 且根系通过对土壤的固定、与土壤的物质交换能促进土壤发育[10]。中间锦鸡儿因其耐旱、耐沙埋、抗风蚀、成活率高、固沙能力强等特性, 成为库布齐沙地广泛种植的防风固沙、水土保持树种[11]。有学者研究发现不同灌木树种通过根际效应对土壤的改良效果不同[12-13], 因此, 对当地不同植被恢复类型根际和非根际土壤性质进行比较研究, 对于一个地区科学筛选植被恢复方式及种类具有重要参考价值和现实意义。为此, 本研究选取库布齐沙地自然恢复的油蒿群落、人工种植的中间锦鸡儿群落作为研究对象, 通过测定根际和非根际土壤理化性质、微生物学特征, 并建立土壤质量指标体系进行综合评价, 以期通过比较自然恢复与人工种植的两种植被改良根际和非根际土壤的效果, 对库布齐沙地生态系统植被恢复与重建提供科学参考和理论支持。
1 研究区概况与研究方法 1.1 研究区概况试验样地位于内蒙古鄂尔多斯市达拉特旗黄河南岸的库布齐沙带东段, 农业部鄂尔多斯沙地草原生态环境重点野外科学观测试验站内, 地处库布齐沙漠和沿河平原的交界处, 气候干旱, 风沙较大, 形成典型的荒漠草原干旱、半干旱的风沙地貌, 土壤为风成沙性母质上形成的风沙土, 地层多数由侏罗系白垩系的砂岩、砂砾岩组成, 交接程度松散, 极易形成风化沙粒。试验站所处位置属于温带大陆性气候, 年平均气温6.1℃, 最低温度为-32.3℃, 最高温度为38.3℃, 年降水量在310 mm左右, 而且都集中在6、7、8三个月中, 夏季降水变率在33%—43%之间, 地表蒸发强烈, 全年蒸发量为2 130.2 mm, 湿润度为0.4, 无霜期156d。试验区天然植被在长期的人类活动影响下, 形成天然灌丛、人工灌丛、人工草地等多种植被群落类型, 主要为耐风蚀与干旱的灌木中间锦鸡儿(Caragana intermedia)、油蒿(Artemisia ordosica)、羊柴(Hedysarum mongolicum)、沙柳(Salix psammophila)、白沙蒿(Artemisia sphaerocephala)等。
1.2 研究方法 1.2.1 样地选择本试验在研究区选择2种不同的植被恢复类型:油蒿群落(Artemisia ordosica)、中间锦鸡儿群落(Caragana intermedia), 并以流动沙地作对照(LS)。其中, 用YH表示研究区固定沙地自然恢复16a的油蒿群落;ZJ表示研究区人工种植16年后形成的中间锦鸡儿群落。
| 样地 Plot | 群落类型 Community type | 海拔 Altitude/m | 地理位置 Geographical position | 优势物种 Dominant species | 覆盖度 Coverage/% |
| YH | 天然灌丛 | 1045 | 40°19′096″N, 109°59′557″E | 油蒿Artemisia ordosica | 65 |
| ZJ | 人工灌丛 | 1043 | 40°19′243″N, 109°59′684″E | 中间锦鸡儿Caragana intermedia | 50 |
| LS | 流动沙地 | 1041 | 40°19′232″N, 109°59′499″E | 白沙蒿Artemisia sphaerocephala | 10 |
| YH:油蒿群落,ZJ:中间锦鸡儿群落, LS:并以流动沙地 | |||||
土壤样品于2011年4月采集, 在各样地中按“S”型选取9株植物, 采集0—10、10—20、20—30、30—40cm不同深度根际、非根际土壤。采集方法参考Riley等[14]的抖落法, 附着植物根系周围1cm的土壤作为根际土壤, 采集离植物根系20cm以外的土壤作为非根际土壤。分层混合, 3次重复。土样分装于无菌塑料袋中包扎密封, 带回实验室于4℃冷藏。
1.2.3 测定方法(1)土壤微生物测定
土壤微生物数量测定采用稀释涂布平板法。细菌采用牛肉膏蛋白胨琼脂培养基培养;放线菌采用高氏1号琼脂培养基培养;真菌采用马丁氏培养基培养。将培养基在12l℃下灭菌20min, 选用2个稀释度, 3次重复, 培养温度为25—28℃, 在2—7d内对细菌、真菌、放线菌进行分别计数。
土壤微生物量碳采用熏蒸法进行测定, 土壤微生物量氮采用凯氏定氮法进行测定。
(2)土壤理化性质测定
土壤含水量测定采用烘干法, pH值测定采用1:2.5土水比浸提酸度计法, 有机质测定采用重铬酸钾外加热容量法, 全氮测定采用凯氏定氮法, 速效氮测定采用碱解蒸馏法, 全磷测定采用NaOH熔融-钼锑抗比色法, 速效磷测定采用Olsen法, 速效钾测定采用乙酸铵浸提-火焰光度计法。
1.2.4 土壤质量评价方法在研究土壤微生物与土壤理化性质之间的相关关系基础上, 应用主成分分析法, 以各指标特征值贡献率为权重, 加权计算两种植物根际、非根际土壤理化和微生物指标值, 运用土壤综合指标数法, 综合评价其土壤健康状况。
(1)由于评价指标之间的量纲不同, 各指标间绝对值大小和变幅差异较大, 甚至差几个数量级, 因此, 为保证计算结果准确, 在应用主成分分析法之前, 对原始数据进行标准化处理。
各评价指标标准化公式:
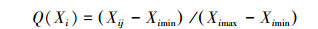
|
(1) |
式中, Q(Xi)表示各因子的隶属度值, Xij为各因子值, Ximax和Ximin分别为第i项因子中的最大值和最小值。
(2)由于土壤质量的各个指标重要性不同, 所以一般用权重系数来表示各指标的重要性程度, 本研究运用SPSS软件计算因子主成分负荷量, 确定各因子在土壤质量中的作用大小, 公式为:
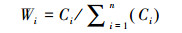
|
(2) |
式中, Wi为土壤各指标的权重, Ci为第i个土壤指标的因子负荷量。
3)计算土壤质量综合指数(SQI)的计算公式为:
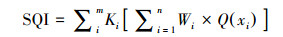
|
(3) |
式中, n为评价指标的个数, 取14;m为所选主成分个数, 取3;ki为第i个主成分的方差贡献率。
1.3 数据分析采用SPSS 18.0对所得试验数据进行方差分析、多重比较、逐步回归分析及主成分分析, 采用Sigmaplot进行作图。
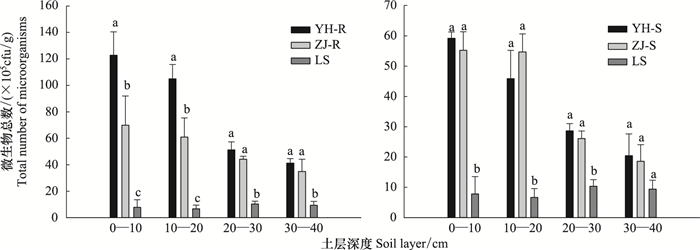
2 结果与分析 2.1 两种植被恢复类型土壤微生物性质差异比较 2.1.1 土壤微生物数量差异比较土壤中微生物的分布一方面可以反映土壤物质能量的转化循环程度, 另一方面也可以反映出土壤肥力状况。与流沙对照相比, 两种植被恢复类型根际、非根际土壤微生物总数显著提高(P<0.05), 其中, 油蒿根际、非根际土壤微生物总数提高了9.23倍和5.73倍, 中间锦鸡儿提高了6.49倍和4.20倍。比较两种植被恢复类型, 油蒿根际、非根际土壤微生物总数在0—40cm土层总体高于中间锦鸡儿(图 1), 两者在根际0—20cm土层差异显著(P<0.05)。
|
| 图 1 两种植物根际与非根际土壤微生物总数 Fig. 1 The distribution of total number of microorganisms in rhizosphere and non-rhizosphere soil of two plants YH:油蒿群落,ZJ:中间锦鸡儿群落, LS:并以流动沙地; R=rhizospheric, S=non-rhizospheric; 不同小写字母代表同一土层不同植物间差异显著(P<0.05) |
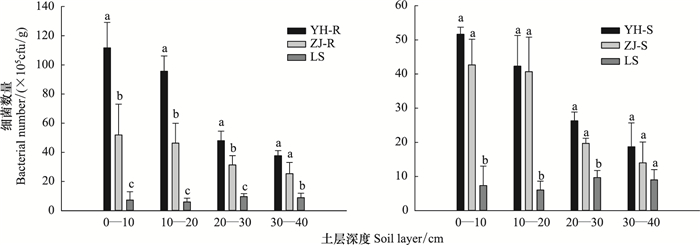
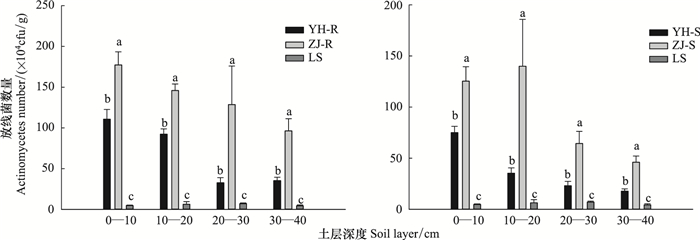
从各样地土壤微生物三大类群分布来看, 与流沙对照相比, 两种植被恢复类型根际、非根际土壤细菌、真菌、放线菌数量均有显著提高(P<0.05), 尤其是根际环境对细菌、真菌等生长繁殖的促进作用更为显著。其中, 油蒿根际土壤细菌、真菌、放线菌数量提高了8.16倍、3.91倍、11.14倍, 中间锦鸡儿根际土壤细菌、真菌、放线菌数量提高了3.84倍、11.47倍、23.57倍。比较两种植被恢复类型, 油蒿根际土壤细菌数量高于中间锦鸡儿(图 2), 两者在0—30cm土层差异显著(P<0.05)。中间锦鸡儿根际土壤真菌和放线菌数量高于油蒿(图 3, 图 4), 在0—40cm土层差异显著(P<0.05)。在两种植被恢复类型非根际土壤中, 放线菌数量具有显著性差异(中间锦鸡儿>油蒿), 细菌、真菌数量均无显著差异。
|
| 图 2 两种植物根际与非根际土壤的细菌数量 Fig. 2 The distribution of bacterial number in rhizosphere and non-rhizosphere soil of two plants |

|
| 图 3 两种植物根际与非根际土壤真菌的数量 Fig. 3 The distribution of fungi number in rhizosphere and non-rhizosphere soil of two plants |
|
| 图 4 两种植物根际与非根际土壤放线菌的数量 Fig. 4 The distribution of actinomycetes number in rhizosphere and non-rhizosphere soil of two plants |
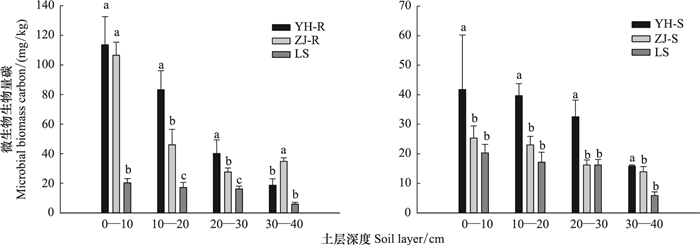
从各样地土壤微生物量碳含量分布来看(图 5), 与流沙对照相比, 油蒿根际和非根际、中间锦鸡儿根际土壤微生物量碳含量显著提高(P < 0.05), 其中, 油蒿根际和非根际土壤微生物量碳含量分别提高了300.05%、118.31%, 中间锦鸡儿根际土壤微生物量碳含量提高了236.34%, 非根际土壤微生物量碳含量与流沙对照无显著差异。比较两种植被恢复类型, 油蒿根际、非根际土壤微生物量碳含量总体高于中间锦鸡儿, 分别提高了96.95%和174.22%。从图 6可以看出, 各样地土壤微生物量氮含量分布为:与流沙对照相比, 两种植被恢复类型根际、非根际土壤微生物量氮含量均显著增加(P<0.05), 其中, 油蒿根际、非根际土壤微生物量氮含量提高了2858.13%、1674.52%, 中间锦鸡儿提高了1895.06%、936.25%。比较两种植被恢复类型, 油蒿根际、非根际土壤微生物生物量氮含量总体高于中间锦鸡儿, 分别提高66.72%和92.65%。土壤微生物生物量是土壤有机质的活性部分及速效养分的来源, 参与调节土壤矿化和物质能量流动过程[15], 可以用来反映土壤微生物功能活性[16]。土壤微生物量碳对土壤养分循环起着重要作用, 比有机碳更能反应土壤质量的变化[17], 土壤微生物生物量氮是土壤微生物同化、矿化活性的重要指标, 是植物氮素的“活性库”[18]。以上结果表明, 两种植被恢复类型对土壤微生物活性有不同程度的促进作用, 其中, 自然恢复的油蒿群落对土壤有效碳和氮的利用和转化能力要高于中间锦鸡儿群落。
|
| 图 5 两种植物根际和非根际土壤微生物量碳含量 Fig. 5 The distribution of soil microbial biomass C in rhizosphere and non-rhizosphere soil of two plants |

|
| 图 6 两种植物根际和非根际土壤微生物生物量氮含量 Fig. 6 The distribution of soil microbial biomass N in rhizosphere and non-rhizosphere soil of two plants |
由表 2可以看出, 试验区沙地土壤pH值总体呈弱碱性。与流沙对照相比, 两种植被恢复类型土壤pH值升高明显(P<0.05), 其中, 中间锦鸡儿根际pH值显著高于油蒿根际, 两者在非根际土壤中无显著差异;有机质和全量养分方面, 与流沙对照相比, 两种植被恢复类型土壤有机质、全氮、全磷含量均有所提高, 其中, 油蒿根际和非根际土壤有机质含量分别提高了303.58%和142.86%, 全氮含量分别提高了273.88%和158.62%, 全磷含量分别提高了87.27%和97.41%, 中间锦鸡儿根际和非根际土壤有机质含量分别提高了121.43%和85.72%, 全氮含量分别提高了67.35%和30.27%, 全磷含量分别提高了143.60%和140.42%。比较两种植被恢复类型, 油蒿根际土壤有机质、全氮含量显著高于中间锦鸡儿(P<0.05), 中间锦鸡儿土壤全磷含量总体高于油蒿。
| 化学性质 Chemical property | 土层 Soil layer /cm | YH-R | YH-S | ZJ-R | ZJ-S | LS |
| pH | 0—10 | 7.35±0.08b | 7.72±0.04a | 7.67±0.05a | 7.77±0.07a | 7.06±0.06c |
| 10—20 | 7.58±0.05b | 7.74±0.04a | 7.78±0.06a | 7.78±0.04a | 7.15±0.05c | |
| 20—30 | 7.65±0.13a | 7.77±0.05a | 7.82±0.03a | 7.79±0.07a | 7.11±0.02b | |
| 30—40 | 7.66±0.18a | 7.79±0.05a | 7.85±0.04a | 7.8±0.04a | 7.10±0.03b | |
| 有机质 | 0—10 | 0.53±0.07a | 0.28±0.04b | 0.36±0.08b | 0.30±0.07b | 0.16±0.04c |
| Organic matter/% | 10—20 | 0.29±0.06a | 0.18±0.03b | 0.12±0.05b | 0.10±0.02b | 0.05±0.02c |
| 20—30 | 0.17±0.03a | 0.11±0.03a | 0.08±0.04b | 0.06±0.03b | 0.03±0.02b | |
| 30—40 | 0.14±0.03a | 0.11±0.04a | 0.06±0.03b | 0.06±0.03b | 0.04±0.01b | |
| 全氮 | 0—10 | 369.91±4.81a | 226.27±1.73b | 211.03±4.44b | 167.80±1.19c | 110.25±1.30d |
| Total N /(mg/kg) | 10—20 | 198.54±3.03a | 177.72±1.31a | 77.90±2.43b | 52.51±0.52b | 50.64±0.49b |
| 20—30 | 183.70±4.33a | 129.26±1.22a | 50.53±1.71b | 55.41±0.77b | 49.77±0.61b | |
| 30—40 | 142.24±2.32a | 85.50±0.68b | 60.93±1.11b | 35.98±0.60c | 28.82±0.19c | |
| 全磷 | 0—10 | 273.43±1.22a | 237.31±2.32b | 291.30±2.31a | 295.85±2.59a | 122.97±3.02c |
| Total P /(mg/kg) | 10—20 | 198.44±3.30b | 214.61±2.17b | 285.17±4.02a | 253.40±1.20a | 125.00±1.45c |
| 20—30 | 191.02±1.04c | 221.43±1.39b | 262.21±1.57a | 274.97±2.39a | 107.95±1.88d | |
| 30—40 | 182.90±1.17c | 218.25±1.77b | 261.51±2.64a | 261.66±1.36a | 95.72±1.62d | |
| 速效氮 | 0—10 | 48.31±0.24a | 31.10±0.28b | 11.34±0.30c | 11.18±0.09c | 10.84±0.20c |
| Available N /(mg/kg) | 10—20 | 34.34±0.43a | 31.02±0.28a | 2.27±0.09c | 11.25±0.22b | 2.26±0.10c |
| 20—30 | 41.57±0.20a | 31.14±0.33b | 8.01±0.21c | 11.55±0.15c | 6.01±0.13c | |
| 30—40 | 27.65±0.17a | 27.61±0.22a | 6.54±0.19c | 15.70±0.10b | 6.32±0.13c | |
| 速效磷 | 0—10 | 1.02±0.26a | 1.03±0.26a | 未检出 | 未检出 | 1.02±0.29a |
| Available P /(mg/kg) | 10—20 | 未检出 | 8.25±1.45a | 0.47±0.14b | 6.49±1.58a | 0.05±0.06c |
| 20—30 | 未检出 | 2.91±0.18b | 1.63±0.36c | 6.08±1.33a | 0.07±0.12d | |
| 30—40 | 未检出 | 6.48±0.73a | 5.68±0.24b | 5.51±0.46b | 0.08±0.08c | |
| 速效钾 | 0—10 | 192.54±1.89a | 140.02±2.49c | 163.87±1.84b | 200.05±3.16a | 69.00±0.47d |
| Available K /(mg/kg) | 10—20 | 85.51±0.54a | 98.50±1.86a | 90.06±1.07a | 76.37±0.76b | 64.55±0.47b |
| 20—30 | 67.52±0.21b | 94.08±0.83a | 67.51±0.61b | 57.59±0.65c | 88.04±0.71a | |
| 30—40 | 62.53±0.08b | 76.07±0.75a | 75.05±0.42a | 61.96±0.29b | 76.52±0.34a | |
| YH-R:油蒿群落根际土壤, YH-S:油蒿群落非根际土壤, ZJ-R:中间锦鸡儿群落根际土壤, ZJ-S:中间锦鸡儿群落非根际土壤, LS:流动沙地;同行不同小写字母表示同一土层不同土壤类型间有显著性差异(P<0.05) | ||||||
速效养分方面, 与流沙对照相比, 两种植被恢复类型根际、非根际土壤速效氮、速效钾含量有不同程度提高。其中, 油蒿根际、非根际土壤速效氮含量分别提高了501.99%和379.37%, 速效钾含量分别提高了36.90%和37.09%, 中间锦鸡儿根际和非根际土壤速效氮含量提高了11.12%和96.43%, 速效钾提高了33.0%和32.83%。比较两种植被恢复类型, 油蒿根际、非根际速效氮含量显著高于中间锦鸡儿(P<0.05), 速效钾含量在两者间无显著差异。速效磷含量除油蒿根际外, 均显著高于流沙对照(P<0.05), 总体表现为中间锦鸡儿>油蒿。
上述结果表明, 植被的生长恢复对于土壤有效养分的积累具有促进作用, 由于植物根系分泌物以及植物自身的生理代谢的不同, 导致了两种植物对土壤有效养分的促进作用不同。除磷元素外, 自然恢复的油蒿群落根际、非根际环境对土壤养分的正向积累作用较中间锦鸡儿明显。
2.3 两种植被恢复类型土壤微生物与土壤化学性质相关性分析土壤微生物与土壤化学性质之间关系密切, 土壤微生物可以促进土壤有机质的积累, 土壤养分的积累又可增强微生物活性, 为微生物提供碳源。从表 3可以看出, 有机质和速效钾含量是影响微生物数量与生物量碳、氮含量的主要因素, 与微生物各指标呈显著正相关。全氮与微生物总数、细菌、放线菌、生物量碳呈显著正相关, pH值和速效磷含量与微生物总数、细菌、放线菌、生物量碳呈显著负相关, 速效氮含量与细菌数量呈显著正相关。全磷、含水量与微生物各指标相关性程度均不显著。
| 因子 Factor | 微生物总数 Total number of microorganisms | 细菌 Bacterial number | 真菌 Fungi number | 放线菌 Actinomycetes number | 微生物量碳 Microbial biomass C | 微生物量氮 Microbial biomass N |
| 有机质Organic matter | 0.8803** | 0.8533** | 0.5628* | 0.7342** | 0.8387** | 0.6202* |
| pH值pH Value | -0.7385** | -0.7296** | -0.3774 | -0.5475* | -0.5444* | -0.2233 |
| 全氮Total N | 0.8827** | 0.8818** | 0.4481 | 0.6048* | 0.7026** | 0.4065 |
| 全磷Total P | 0.4101 | 0.4737 | -0.055 | -0.0403 | 0.029 | -0.2784 |
| 速效氮Available N | 0.4631 | 0.5156* | -0.1043 | 0.052 | 0.0829 | -0.2248 |
| 速效磷Available P | -0.6483** | -0.619* | -0.4885 | -0.5878* | -0.5286* | -0.4814 |
| 速效钾Available K | 0.7189** | 0.67** | 0.5092* | 0.735** | 0.8266** | 0.7549** |
| 含水量Water content | -0.2246 | -0.3121 | 0.3204 | 0.2865 | 0.2331 | 0.3513 |
| r0.05=0.4973, r0.01=0.6226, *一般相关, **密切相关 | ||||||
土壤质量综合指数是土壤因子的集成和综合, 土壤质量评价可以敏感反映出土壤生态系统的变化以及土壤恢复退化的能力[19]。本研究应用主成分分析法, 以各指标特征值贡献率为权重, 加权计算两种植被恢复类型根际、非根际土壤化学和微生物学指标值, 运用土壤综合指标数法, 综合评价其土壤健康状况。
对原始试验数据进行标准化处理, 得到两种植被恢复类型土壤质量指标的隶属度值(表 4), 由表 4可知, 流沙对照样地除速效磷外, 其他指标隶属度值均为0。油蒿根际土壤细菌数量、微生物总数、微生物量碳和氮含量、有机质、全氮、速效氮隶属度值均为1, 中间锦鸡儿根际土壤真菌、放线菌数量、全磷隶属度值为1。
| 指标Index | 数据Data | YH-R | YH-S | ZJ-R | ZJ-S | LS |
| 细菌Bacterial number | A | 73.25 | 34.75 | 38.75 | 29.25 | 8 |
| B | 1.000 | 0.410 | 0.471 | 0.326 | 0.000 | |
| 真菌Fungi number | A | 27.00 | 13.58 | 68.58 | 15.42 | 5.50 |
| B | 0.341 | 0.128 | 1.000 | 0.157 | 0.000 | |
| 放线菌Actinomycetes number | A | 67.75 | 37.75 | 137.08 | 93.92 | 5.58 |
| B | 0.473 | 0.245 | 1.000 | 0.672 | 0.000 | |
| 微生物总数 | A | 80.05 | 38.54 | 52.53 | 38.66 | 8.56 |
| Total number of microorganisms | B | 1.000 | 0.419 | 0.615 | 0.421 | 0.000 |
| 微生物量碳Microbial biomass C | A | 63.94 | 32.47 | 53.76 | 19.61 | 14.87 |
| B | 1.000 | 0.359 | 0.793 | 0.097 | 0.000 | |
| 微生物量氮Microbial biomass N | A | 7.77 | 4.66 | 5.24 | 2.72 | 0.26 |
| B | 1.000 | 0.586 | 0.663 | 0.328 | 0.000 | |
| 有机质Organic matter | A | 0.28 | 0.17 | 0.16 | 0.13 | 0.07 |
| B | 1.000 | 0.476 | 0.429 | 0.286 | 0.000 | |
| pH值pH Value | A | 7.56 | 7.76 | 7.78 | 7.79 | 7.11 |
| B | 0.662 | 0.956 | 0.985 | 1.000 | 0.000 | |
| 全氮Total N | A | 22.36 | 15.47 | 10.01 | 7.79 | 5.98 |
| B | 1.000 | 0.579 | 0.246 | 0.111 | 0.000 | |
| 全磷Total P | A | 21.14 | 22.29 | 27.50 | 27.14 | 11.29 |
| B | 0.608 | 0.679 | 1.000 | 0.978 | 0.000 | |
| 速效氮Available N | A | 3.79 | 3.02 | 0.7 | 1.24 | 0.63 |
| B | 1.000 | 0.756 | 0.022 | 0.193 | 0.000 | |
| 速效磷Available P | A | 0.26 | 4.67 | 1.95 | 4.52 | 0.31 |
| B | 0.000 | 1.000 | 0.383 | 0.966 | 0.011 | |
| 速效钾Available K | A | 10.2 | 10.21 | 9.91 | 9.89 | 7.45 |
| B | 0.996 | 1.000 | 0.891 | 0.884 | 0.000 | |
| 含水量Water content | A | 4.06 | 4.39 | 3.06 | 3.35 | 0.86 |
| B | 0.907 | 1.000 | 0.623 | 0.705 | 0.000 | |
| A:土壤指标的测定值, B:土壤指标的隶属度值 | ||||||
两种植被恢复类型土壤质量评价指标主成分分析结果见表 5, 由表 5可以看出, 第1主成分的方差贡献率达61.58%, 第1和第2主成分的方差贡献率达84.20%, 第1、第2和第3主成分的累计方差贡献率达98.54%。一般认为当累计方差贡献率高于85%时即可用来反映系统的变异信息, 因此, 用第1、第2和第3各主成分可以代表两种固沙植物土壤质量的变异信息。第1主成分主要反映的是细菌、微生物总数、微生物量碳、微生物量氮、有机质、速效钾以及含水量指标的综合变量, 说明这些指标在土壤质量评价中起着重要作用;第2、第3主成分主要反映的是放线菌、真菌、pH值、全磷以及速效磷等指标的综合变量, 这些指标在土壤质量评价中具有一定的作用, 但其影响较小。
| 指标 Index | 第1主成分 The first principal component | 第2主成分 The second principal component | 第3主成分 The third principal component | |||
| 负荷量 Values of component capacity | 权重 Weights | 负荷量 Values of component capacity | 权重 Weights | 负荷量 Values of component capacity | 权重 Weights | |
| 细菌Bacterial number | 0.3165 | 0.0884 | -0.1838 | 0.0544 | -0.0580 | 0.0195 |
| 真菌Fungi number | 0.1682 | 0.0470 | 0.2321 | 0.0687 | -0.5103 | 0.1716 |
| 放线菌Actinomycetes number | 0.1943 | 0.0543 | 0.3709 | 0.1098 | -0.3285 | 0.1104 |
| 微生物总数Total number of microorganisms | 0.3261 | 0.0911 | -0.0945 | 0.0280 | -0.1174 | 0.0395 |
| 微生物量碳Microbial biomass C | 0.2927 | 0.0818 | -0.1336 | 0.0396 | -0.3045 | 0.1024 |
| 微生物量氮Microbial biomass N | 0.3318 | 0.0927 | -0.1061 | 0.0314 | -0.0677 | 0.0228 |
| 有机质Organic matter | 0.3146 | 0.0879 | -0.2110 | 0.0625 | 0.0004 | 0.0001 |
| pH值pH Value | 0.2401 | 0.0671 | 0.3773 | 0.1117 | 0.1590 | 0.0535 |
| 全氮Total N | 0.2783 | 0.0777 | -0.3066 | 0.0908 | 0.1192 | 0.0401 |
| 全磷Total P | 0.2282 | 0.0637 | 0.4114 | 0.1218 | 0.0007 | 0.0002 |
| 速效氮Available N | 0.2364 | 0.0660 | -0.3066 | 0.0908 | 0.3297 | 0.1108 |
| 速效磷Available P | 0.0393 | 0.0110 | 0.3967 | 0.1175 | 0.4901 | 0.1648 |
| 速效钾Available K | 0.3128 | 0.0874 | 0.1723 | 0.0510 | 0.1761 | 0.0592 |
| 含水量Water content | 0.3005 | 0.0839 | 0.0747 | 0.0221 | 0.3128 | 0.1052 |
| 特征根Eigenvalue | 8.6218 | 3.1664 | 2.0080 | |||
| 方差贡献率Rate of variance/% | 61.5846 | 22.6173 | 14.3430 | |||
| 累计方差贡献率Cumulative rate/% | 61.5846 | 84.2019 | 98.5449 | |||
由规格化特征向量得出土壤质量评价系统的第一、第二和第三主成分方程:

|
由各土壤质量隶属度值(表 4)及其权重值(表 5), 根据式(3)计算即可得到两种植被恢复类型土壤质量的综合评价指数(表 6)。由表 6得出土壤综合指数排序为:油蒿根际>中间锦鸡儿根际>油蒿非根际>中间锦鸡儿非根际>流沙对照, 通过SQI值对比可以看出与流沙对照相比, 两种植被恢复类型均对土壤质量有大幅提高, 其中, 油蒿根际与非根际土壤SQI值明显高于中间锦鸡儿, 土壤质量达到一个相对较高的水平。
| 样地Plot | 得分Score | 名次Ranking | 样地Plot | 得分Score | 名次Ranking |
| YH-R | 0.7853 | 1 | ZJ-S | 0.4942 | 4 |
| YH-S | 0.6025 | 3 | LS | 0.0006 | 5 |
| ZJ-R | 0.6415 | 2 |
植被恢复过程中, 根系向土壤分泌质子、离子及有机物质, 改善了根际土壤环境, 促进了土壤微生物数量及活性。陈家模[20]、罗明等[21]研究均得出, 在流动沙地建立植物群落后, 土壤微生物数量和活性显著提高。在本研究中, 油蒿群落和中间锦鸡儿群落根际、非根际土壤微生物数量、微生物生物量碳和氮含量均比流动沙地有大幅提高, 说明两种植被恢复类型可不同程度提高土壤微生物数量及活性。其中, 在根际土壤中, 油蒿土壤微生物总数、细菌数量、微生物生物量碳和氮含量均显著高于中间锦鸡儿, 而放线菌和真菌数量均为中间锦鸡儿高于油蒿。在较高营养土壤中, 细菌大量存在, 有机质分解彻底, 纤维素和木质素较少, 从而不利于真菌群落的生长。在土壤养分下降的条件下, 细菌生长繁殖受到抑制, 真菌有明显上升趋势, 放线菌菌丝体产生的孢子使其种群能够在严酷环境中更有生存优势[22], Beatriz等[23]认为土壤真菌和放线菌比例升高是土壤质量退化的标志。本研究的结果反映出自然恢复的油蒿群落根际土壤环境比人工种植的中间锦鸡儿群落更有利于微生物活动, 土壤营养状况较好, 人工种植的中间锦鸡儿群落根际土壤肥力呈下降趋势。韩艳洁[24]对几种乔木树种天然及人工林根际微生物比较研究发现, 天然林根际土壤养分富集, 根际土壤微生物数量及活性均大于人工林。曹成有等[25]研究发现, 小叶锦鸡儿天然群落土壤微生物量大于人工群落, 与本研究的结论一致。
3.2 两种植被恢复类型土壤化学性质差异比较植被的存在, 促进了土壤养分循环, 增加了主要土层有机质含量。有研究指出, 流动沙地种植植被后, 沙面枯落物堆积, 容重变小, 养分条件得到改善[26-27]。在本研究中, 两种植被恢复类型根际、非根际土壤有机质、全氮、全磷、速效氮、速效钾含量均比流动沙地有不同程度地提高, 试验结果表明沙地植被恢复可有效提高土壤肥力。植被恢复类型的不同, 对土壤营养物质的积累和循环作用不同。在本研究中, 油蒿根际、非根际土壤有机质、全氮、速效氮含量显著高于中间锦鸡儿。油蒿群落是当地分布广泛的优势种, 生长旺盛, 根系分泌物对土壤环境的改造能力较强, 对土壤养分的富集作用较为明显, 而中间锦鸡儿根际土壤环境营养物质相对缺乏。
一般认为, 根系分泌物及根产物等引起根际土壤养分富集效应。值得注意的是, 在本研究中, 两种植被恢复类型根际土壤全磷、速效磷含量以及中间锦鸡儿根际土壤速效氮含量均低于非根际土壤, 出现不同程度的亏缺现象。Zoysa等[28]研究发现, 由于植物根系和微生物对磷元素的吸收利用强烈, 而当土壤磷缓冲能力较强的时候, 非根际土壤中的磷无法迅速运输至根际, 土壤固定磷解吸附作用较弱, 造成植物根际磷元素出现了不同程度的亏缺。厉婉华[29]研究也指出杉木等植物根际土壤速效氮含量出现与非根际接近甚至亏缺现象, 可能与根际土壤脲酶活性有关[9]。总而言之, 有关速效养分变化的研究很多, 但研究结果各不相同, 产生差异的原因可能与植物根系分泌物、土壤pH值、钙离子、微生物活性以及植物吸收、转化和利用能力等因素有关。
3.3 两种植被恢复类型土壤微生物与土壤化学性质之间的相关性土壤是对微生物产生显著影响的生态微环境, 如土壤养分、水分、物理性状等因子直接或间接影响着微生物结构与活性[30], 而微生物从另一方面又对土壤肥力改善与稳定性产生作用。在对土壤微生物与土壤化学性质的相关研究中, 许多研究表明有机质是影响土壤微生物数量和生物量的重要因子[31-32], 与细菌数量、微生物量呈正相关[33]。土壤全量和速效养分对微生物数量和生物量的相关关系在不同的研究中结论不同[34-35], 研究区域、研究方法与植被类型等不同均是土壤微生物与土壤环境的相互关系产生差异的原因。在本研究中, 影响油蒿和中间锦鸡儿群落土壤微生物数量和生物量碳和氮的土壤因子是有机质、pH值、全氮、速效氮、速效磷、速效钾, 其中, 对两种植被恢复类型土壤微生物数量和生物量有正向作用的主要因子是土壤有机质、速效钾和全氮含量。
3.4 两种植被恢复类型土壤质量评价土壤质量评价是检测土壤退化与恢复效果的重要手段, 也是评价土壤可持续利用与有效管理的基础。科学的选取评价指标, 对于准确评价土壤质量具有重要意义。郑昭佩等[36]提出应该加入土壤微生物学指标进行土壤质量综合评价。本研究选取了14个基于土壤微生物学和化学性质的指标, 可在一定程度上反映土壤肥力和生物活性。有研究表明, 植被恢复可有效提高土壤综合质量[3], 通过土壤综合指数可以衡量土壤质量的改善效果。在本研究中, 土壤综合指数排序为:油蒿根际>中间锦鸡儿根际>油蒿非根际>中间锦鸡儿非根际>流沙对照, 与流沙对照相比, 油蒿、中间锦鸡儿群落土壤SQI值分别提高了1307.83倍和822.67倍。从研究结果来看, 两种植被恢复类型均不同程度的改善了土壤状况, 其中, 自然恢复的油蒿群落恢复效果较好, 能较大幅度提高土壤质量, 在库布齐沙地生态恢复过程中可以重点考虑作为适合途径之一。
| [1] | 彭少麟. 恢复生态学与植被重建. 生态科学 , 1996, 15 (2) : 26–31. |
| [2] | 陆雅海, 张福锁. 根际微生物研究进展. 土壤 , 2006, 38 (2) : 113–121. |
| [3] | 吕春花, 郑粉莉. 黄土高原子午岭地区植被恢复过程中的土壤质量评价. 中国水土保持科学 , 2009, 7 (3) : 12–18. |
| [4] | 安韶山, 李国辉, 陈利顶. 宁南山区典型植物根际与非根际土壤微生物功能多样性. 生态学报 , 2011, 31 (18) : 5225–5234. |
| [5] | 孟令军, 耿增超, 殷金岩, 王海涛, 吉鹏飞. 秦岭太白山区6种中草药根际与非根际土壤化学性质及酶活性. 应用生态学报 , 2012, 23 (10) : 2685–2692. |
| [6] | 孟令军, 耿增超, 王海涛, 殷金岩, 姜林, 林伟达. 秦岭太白山区鹿蹄草根际与非根际土壤养分及酶活性研究. 西北农林科技大学学报:自然科学版 , 2012, 40 (5) : 157–165. |
| [7] | Adriaensen K, van der Lelie D, van Laere A, Vangronsveld J, Colpaert J V. A zinc-adapted fungus protects pines from zinc stress. New Phytologist , 2004, 161 (2) : 549–555. DOI:10.1046/j.1469-8137.2003.00941.x |
| [8] | 张超.黄土丘陵区根际微生物对退耕地植被恢复的响应[D].北京:中国科学院, 2013. http://cdmd.cnki.com.cn/article/cdmd-80129-1013025852.htm |
| [9] | 邱权, 李吉跃, 王军辉, 王宁, 孙奎, 何茜, 苏艳, 潘昕. 西宁南山4种灌木根际和非根际土壤微生物、酶活性和养分特征. 生态学报 , 2014, 34 (24) : 7411–7420. |
| [10] | 靳虎甲, 王继和, 李毅, 马全林, 张德魁, 刘有军. 油蒿生态学研究综述. 西北林学院学报 , 2009, 24 (4) : 62–66. |
| [11] | 牛西午, 丁玉川, 张强, 徐强. 柠条根系发育特征及有关生理特性研究. 西北植物学报 , 2003, 23 (5) : 860–865. |
| [12] | 邢尚军, 张建锋, 郗金标, 宋玉民. 白刺造林对重盐碱地的改良效果. 东北林业大学学报 , 2003, 31 (6) : 96–98. |
| [13] | 苏永中, 赵哈林, 张铜会. 几种灌木、半灌木对沙地土壤肥力影响机制的研究. 应用生态学报 , 2002, 13 (7) : 802–806. |
| [14] | Riley D, Barber S A. Salt accumulation at the soybean (Glycine max (L.) Merr.) root-soil interface. Soil Science Society of America Journal , 1970, 34 (1) : 154–155. DOI:10.2136/sssaj1970.03615995003400010042x |
| [15] | 刘志恒. 现代微生物学(第二版). 北京: 科学出版社, 2008. |
| [16] | Rogers B F, Tate Ⅲ R L. Temporal analysis of the soil microbial community along a toposequence in Pineland soils. Soil Biology and Biochemistry , 2001, 33 (10) : 1389–1401. DOI:10.1016/S0038-0717(01)00044-X |
| [17] | 王珊, 李廷杆, 张锡洲, 周建新. 设施土壤中微生物数量及其生物量碳的变化研究. 中国农学通报 , 2005, 21 (4) : 198–201. |
| [18] | 周桦, 宇万太, 姜子绍, 张璐. 不同土地利用方式对土壤微生物生物量氮的影响. 土壤通报 , 2008, 39 (4) : 734–737. |
| [19] | 刘占锋, 傅伯杰, 刘国华, 朱永官. Soil quality:Concept, indicators and its assessment. 生态学报 , 2006, 26 (3) : 901–913. |
| [20] | 陈家模.四种人工固沙植物群落对土壤养分及生物活性的改良作用[D].沈阳:东北大学, 2009. http://www.cnki.com.cn/article/cjfdtotal-fxky200604036.htm |
| [21] | 罗明, 单娜娜, 文启凯, 潘伯荣. 几种固沙植物根际土壤微生物特性研究. 应用与环境生物学报 , 2002, 8 (6) : 618–622. |
| [22] | 李阜棣, 喻子牛, 何绍江. 农业微生物学实验技术. 北京: 中国农业出版社, 199682–83. |
| [23] | Ramos B, Lucas Garcia J A, Probanza A, Doménech J, Gutierrez Mañero F J. Influence of an indigenous European alder (Alnus glutinosa L·Gaertn) rhizobacterium (Bacillus pumilus) on the growth of alder and its rhizosphere microbial community structure in two soils. New Forests , 2003, 25 (2) : 149–159. DOI:10.1023/A:1022688020897 |
| [24] | 韩艳洁. 内蒙古大青山几种乔木树种根际微生物数量和动态分布. 干旱区资源与环境 , 2010, 24 (9) : 185–188. |
| [25] | 曹成有, 蒋德明, 滕晓慧, 崔振波. 小叶锦鸡儿固沙群落土壤微生物生物活性的季节动态. 水土保持学报 , 2011, 25 (3) : 185–188. |
| [26] | 朱丽霞, 章家恩, 刘文高. 根系分泌物与根际微生物相互作用研究综述. 生态环境 , 2003, 12 (1) : 102–105. |
| [27] | 王永魁. 几种固沙植物对沙土影响的研究. 林业科学 , 1985 (5) : 15–23. |
| [28] | Zoysa A K N, Loganathan P, Hedley M J. A technique for studying rhizosphere processes in tree crops:soil phosphorus depletion around camellia (Camellia japonica L.) roots. Plant and Soil , 1997, 190 (2) : 253–265. DOI:10.1023/A:1004264830936 |
| [29] | 厉婉华. 栓皮栎、杉木和火炬松根际与非根际土壤氮素及pH差异的研究. 南京林业大学学报 , 1996, 20 (2) : 49–52. |
| [30] | Young I M, Crawford J W. Interactions and self organization in the soil microbe complex. Science , 2004, 304 (5677) : 1634–1637. DOI:10.1126/science.1097394 |
| [31] | 马晓梅.塔里木荒漠河岸林主要建群植物根际微生物分布特点[D].乌鲁木齐:新疆农业大学, 2007. http://cdmd.cnki.com.cn/article/cdmd-10758-2007136650.htm |
| [32] | Ekblad A, Nordgren A. Is growth of soil microorganisms in boreal of forests limited by carbon or nitrogen availability. Plant and Soil , 2002, 242 (1) : 115–122. DOI:10.1023/A:1019698108838 |
| [33] | Sharma P, Rai S C, Sharma R, Sharma E. Effects of land use change on soil microbial C, N and P in a Himalayan watershed. Pedobiologia , 2004, 48 (1) : 83–92. DOI:10.1016/j.pedobi.2003.09.002 |
| [34] | 何友军, 王清奎, 汪思龙, 于小军. 杉木人工林土壤微生物生物量碳氮特征及其与土壤养分的关系. 应用生态学报 , 2006, 17 (12) : 2292–2296. |
| [35] | 齐雅静.油松、虎榛子不同林型根际微生物组成及功能多样性研究[D].呼和浩特:内蒙古农业大学, 2010. http://cdmd.cnki.com.cn/article/cdmd-10129-2010150122.htm |
| [36] | 郑昭佩, 刘作新. 土壤质量及其评价. 应用生态学报 , 2003, 14 (1) : 131–134. |
 2016, Vol. 36
2016, Vol. 36