文章信息
- 戚德辉, 温仲明, 王红霞, 郭茹, 杨士梭
- QI Dehui, WEN Zhongming, WANG Hongxia, GUO Ru, YANG Shisuo.
- 黄土丘陵区不同功能群植物碳氮磷生态化学计量特征及其对微地形的响应
- Stoichiometry traits of carbon, nitrogen, and phosphorus in plants of different functional groups and their responses to micro-topographical variations in the hilly and gully region of the Loess Plateau, China
- 生态学报[J]. 2016, 36(20): 6420-6430
- Acta Ecologica Sinica[J]. 2016, 36(20): 6420-6430
- http://dx.doi.org/10.5846/stxb201504090720
-
文章历史
- 收稿日期: 2015-04-09
- 网络出版日期: 2016-01-22
2. 中国科学院教育部水土保持与生态环境研究中心, 杨凌 712100;
3. 西北农林科技大学水土保持研究所, 杨凌 712100
2. Research Center of Soil and Water Conservation and Ecological Environment, Chinese Academy of Sciences and Ministry of Education, Yangling 712100, China;
3. Institute of Soil and Water Conservation, Northwest Agriculture and Forest University, Yangling 712100, China
生态化学计量学是利用生物学、化学和物理学的基本原理, 来研究生态过程中能量和多种化学元素的平衡关系, 为研究C、N、P等重要元素在生态系统过程中的耦合关系提供了技术方法[1-2]。碳(C)作为植物体各种生理生化过程的能量来源, 是植物体内干物质最主要的构成元素, 氮(N)和磷(P)是植物的基本营养元素, 也是各种蛋白质和遗传物质的重要组成元素[3-4]。在一定程度上, 元素化学计量比可以反映植物的生态策略, 如C:N和C:P比值可以反映出植物生长速度, 并且可以表明植物生长速度与植物N和P的利用效率的相关性[5], 植物叶片的N:P值可以作为判断限制植物生长的营养元素指标[6]。
地形变化会形成不同的土壤和气候小环境, 如地形变化会影响太阳辐射、温度、湿度及土壤营养获得性, 从而影响到植物群落的组成和分布[7]。其中, 坡向通过改变地面与风向的夹角以及地面接受的太阳辐射, 影响不同坡向上太阳光照度、温度、土壤性质和植被分布。研究表明, 高寒草甸区叶P含量和叶N含量均表现出阴坡>阳坡[7]。坡位则直接影响到光照条件, 对土壤的深度、质地和矿物质含量都有一定的影响[8-9]。因此, 地形条件会影响到植物的生态化学计量特征, 并影响到植物的的适应策略。黄土丘陵地区地形复杂, 生境多样, 植被分布多成镶嵌状。在该地区已开展了部分植物化学计量方面的研究工作, 如王凯博[10]等研究了黄土丘陵区燕沟流域典型植物叶片C、N、P化学计量特征季节变化, 朱秋莲[11]等对黄土丘陵沟壑区不同植被区土壤生态化学计量特征进行了研究, 郑淑霞[12]研究了黄土高原叶片营养性状的空间格局, 但对复杂地形条件下的植物生态化学计量特征鲜有报道, 限制了人们对不同地形条件下植物的生长适应策略以及不同功能群植物的限制性营养元素等的认识和了解。
本研究在黄土丘陵地区森林草原带, 选择不同立地条件(坡向、坡位)的不同功能群植物为研究对象, 通过对植物叶片、细根C、N、P含量及其化学计量特征的研究, 试图回答以下问题:(1)在不同微地形条件(坡向、坡位)下, 各功能群植物叶片、细根C、N、P含量及其化学计量特征的差异性;(2)不同功能群植物C、N、P含量及其化学计量特征的相关性以及黄土丘陵区植物叶片和细根C、N、P含量及其化学计量特征之间的相关关系。研究为深入认识和理解不同草地功能群植物生长的限制元素以及对微地形环境的适应策略提供依据。
1 材料与方法 1.1 研究区概况研究区位于陕西省延安市安塞县(108°5′44″—109°26′18″E, 36°30′45″—37°19′03″ N)附近, 属暖温带森林草原区, 气候为大陆性半干旱季风气候, 年平均气温8.9 ℃ (极端最高温36.8 ℃, 极端最低温-23.6 ℃), 年平均降水量约505 mm, 蒸发量约1000 mm, 平均年日照时数约为2395 h, 日照百分率达54%, 全年无霜期约170 d, 该区土壤类型为黄绵土, 土质疏松, 侵蚀严重, 水土流失形势严峻[13]。境内沟壑纵横、川道狭长、梁峁遍布, 山高、坡陡、沟深, 地形对土壤养分、水分具有强烈的再分配作用, 并影响到群落物种组成的空间格局[14]。近10多年来, 随着植被恢复的开展, 该区逐渐在不同地形环境下形成了以达乌里胡枝子(Lespedezadavurica)、长芒草(Stopa bungeana)、白羊草(Bothriochloa ischaemun)、铁杆蒿(Artemisia gmelinii)、茭蒿(Artemisia giraldii)等为建群种的草本群落。
1.2 研究方法 1.2.1 实验设计野外调查于2013年8月—9月进行。在安塞周围地区, 选择人类活动干扰较少、自然植被发育较好的3个完整断面, 区分阴、阳坡, 在不同的坡位布设样点, 每个断面7个点(峁顶1个、上坡、中坡、下坡阴阳坡各1个), 共计21个采样点。在每个采样点, 首先利用手持GPS记录样地的经纬度、海拔, 使用罗盘测量样地坡向、坡位信息, 并记录样点周围的环境信息(表 1);然后, 设置2—3个1 m×1 m的样方, 记录每个样方内植物名称, 测定多度、盖度、生物量等, 并采集植物化学分析样品。本次共调查了6个科15种草本植物, 物种数或观测值≥3次的植物以豆科(Leguminosae)、禾本科(Gramineae)和菊科(Asteraceae)植物为主, 3个科的植物在各样点出现的频度分别为33.3%、57.1%、66.6%。
| 样点Site | 纬度Latitude | 经度longitude | 海拔Elevation/m | 坡位Position | 坡向Aspect | 优势物种Coenotype |
| 1 | 36°50′59.9″ | 109°18′52.2″ | 1150 | 2 | 1 | 白羊草Bothriochloa ischaemum |
| 2 | 36°51′01.5″ | 109°16′50.5″ | 1221 | 2 | 2 | 达乌里胡枝子Lespedeza davurica、茭蒿Artemisia giraldii |
| 3 | 36°51′10.9″ | 109°18′17.5″ | 1306 | 1 | 4 | 达乌里胡枝子L. davurica、香青兰Dracocephalum moldavica |
| 4 | 36°51′12.1″ | 109°18′51.9″ | 1269 | 2 | 3 | 白羊草B. ischaemum、丛生隐子草Cleistogenes caespitosa、铁杆蒿Artemisia sacrorum |
| 5 | 36°51′10.6″ | 109°18′45.3″ | 1284 | 3 | 3 | 铁杆蒿A. sacrorum |
| 6 | 36°51′12.8″ | 109°18′45.9″ | 1290 | 3 | 2 | 中华隐子草Cleistogenes Chinensis、铁杆蒿A. sacrorum |
| 7 | 36°51′26.8″ | 109°19′02.9″ | 1171 | 3 | 1 | 铁杆蒿A. sacrorum |
| 8 | 36°51′55.7″ | 109°20′18.5″ | 1230 | 3 | 2 | 白羊草B. ischaemum、铁杆蒿A. sacrorum、茭蒿A.giraldii、达乌里胡枝子L. davurica |
| 9 | 36°51′58.6″ | 109°20′18.7″ | 1251 | 3 | 3 | 白羊草B. ischaemum、铁杆蒿A. sacrorum、草木樨状黄芪Astragalus melilotoides Pall、达乌里胡枝子L. davurica |
| 10 | 36°51′58.0″ | 109°20′13.4″ | 1235 | 2 | 1 | 白羊草B. ischaemum、铁杆蒿A. sacrorum、茭蒿A. giraldii、长芒草Stipa bungeana. |
| 11 | 36°52′27.3″ | 109°19′53.6″ | 1234 | 1 | 4 | 白羊草B. ischaemum、达乌里胡枝子L. davurica、阿尔泰狗娃花Heteropappus altaicus |
| 12 | 36°52′13.5″ | 109°19′53.2″ | 1246 | 2 | 3 | 白羊草B. ischaemum |
| 13 | 36°52′12.3″ | 109°20′00.5″ | 1228 | 3 | 2 | 白羊草B. ischaemum、达乌里胡枝子L. davurica |
| 14 | 36°52′09.3″ | 109°20′01.1″ | 1187 | 3 | 1 | 达乌里胡枝子L.davurica |
| 15 | 36°45′07.8″ | 109°15′00.7″ | 1238 | 3 | 3 | 铁杆蒿A. sacrorum、异叶败酱Patrinia heterophylla |
| 16 | 36°45′08.2″ | 109°15′00.2″ | 1219 | 3 | 2 | 铁杆蒿A. sacrorum、异叶败酱P. heterophylla |
| 17 | 36°45′10.3″ | 109°15′00.2″ | 1203 | 3 | 1 | 异叶败酱P. heterophylla |
| 18 | 36°45′22.9″ | 109°15′08.2″ | 1213 | 2 | 1 | 白羊草B. ischaemum |
| 19 | 36°45′26.0″ | 109°15′05.0″ | 1254 | 2 | 2 | 白羊草B. ischaemum、茭蒿A. giraldii |
| 20 | 36°45′27.0″ | 109°15′05.7″ | 1254 | 1 | 4 | 长芒草S.bungeana、阿尔泰狗娃花H. altaicus |
| 21 | 36°45′28.8″ | 109°15′02.1″ | 1266 | 2 | 3 | 铁杆蒿A. sacrorum、茭蒿A. giraldii |
| 坡向Aspect:1无坡向No aspect; 2阳坡South; 3阴坡North; 坡位Slope Position:1下坡Lower slope 2中坡Middle slope 3上坡Upper slope 4峁顶Mao slope | ||||||
样地的设置采用典型采样法, 在每个样方内, 以自然恢复且长势良好的植物为研究对象, 每种植物沿东西南北4个方向采集光照条件良好、完全伸展且没有病虫害的叶片(去掉叶柄)约300 g。然后用铁铲挖取该植物根系(约30 cm深的土块), 清理掉土壤和杂质, 采集直径小于2 mm的细根300 g左右。将采集的样品用自封袋编号封装后放入车载冰箱保存, 用于室内分析。带回的细根用清水洗掉附着的泥土, 然后和叶片样品一起于105 ℃下杀青10 min, 之后放入80℃的烘箱内烘干48—72 h至恒重。将烘干的叶片和细根样品粉碎, 植物叶片与细根的全碳含量(g/kg)用重铬酸钾外加热法测定, 全氮含量(g/kg)采用凯氏定氮仪法分别测定, 磷含量(g/kg)采用钼锑抗比色法测定[15]。
1.3 数据处理在数据分析前, 对数据进行对数转换, 以符合正态分布。采用单因素方差和Post Hoc多重比较对不同功能群植物以及同一功能群植物在不同坡向、坡位条件下C、N、P及其化学计量的差异性进行比较分析, 运用Pearson相关系数检验各功能群植物叶片和细根C、N、P及其化学计量的相关性。利用Excel 2003进行数据预处理、用sigmaplot10.0作图、用SPSS 19.0软件对数据进行统计分析, 显著性水平为0.05。
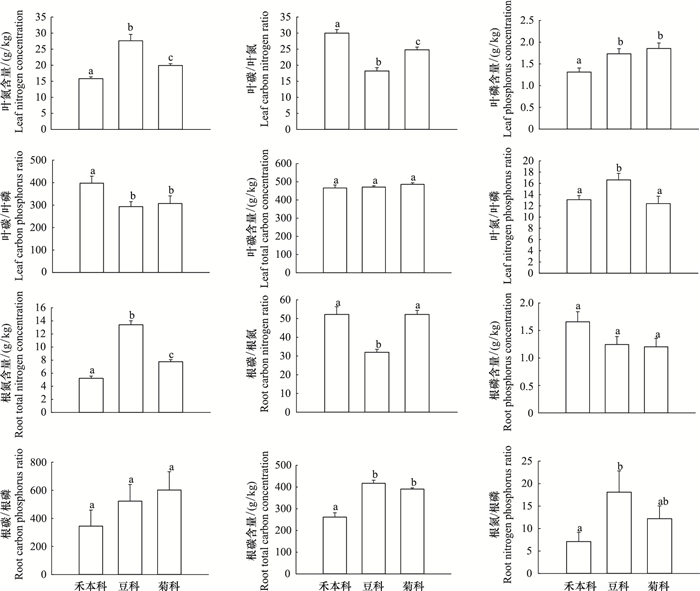
2 结果与分析 2.1 不同科属植物的C、N、P含量及其化学计量特征的差异性不同科属植物的C、N、P含量及其化学计量特征具有较大的差异(图 1)。叶N含量, 叶P含量, 根N含量, 根C含量, 叶C/N, 叶C/P, 叶N/P, 根C/N, 根N/P在科属水平上差异性显著(P < 0.05)。其中豆科叶N含量最高(27.62±1.98) g/kg, 禾本科最低(15.82±0.57) g/kg;叶P含量禾本科最低(1.31±0.09) g/kg, 菊科最高(1.85±0.13) g/kg;豆科根N含量最高(13.41±0.62) g/kg, 禾本科最低(5.22±0.34) g/kg;禾本科根C含量最低(261.96±19.92) g/kg, 豆科最高(417.27±14.38) g/kg;叶C/N禾本科最高(30.00±1.13) g/kg, 豆科最低(18.21±1.04) g/kg;叶C/P禾本科最高(397.44±31.48) g/kg;叶N/P豆科最高(16.61±1.17) g/kg, 菊科最低(12.40±1.31) g/kg;根C/N豆科最低(31.98±1.63) g/kg;根N/P豆科最高(18.09±4.73) g/kg。可以看出叶N含量, 根N含量, 叶N/P, 根N/P豆科最高, 菊科次之, 禾本科最低。叶C/N, 叶C/P在禾本科最高, 菊科次之, 豆科最低(图 1)。
|
| 图 1 不同科属植物C、N、P含量及化学计量比 Fig. 1 C, N, P content and stoichiometric ratio of different genera plants 不同字母表示差异显著(P < 0.05) |
不同科属植物C、N、P含量及其化学计量特征随微地形变化呈现出较大的差异性(图 2, 仅显示差异性显著的科属)。禾本科根C/N在阴坡、阳坡差异显著(P < 0.05), C/N在阴坡小于阳坡;豆科植物根N含量在不同坡位间差异显著(P < 0.05), 根N含量在峁顶最高, 下坡最低。菊科植物叶N含量, 叶C含量, 根N含量, 叶C/N, 根C/N在不同坡向和坡位间差异显著(P < 0.05), 其中叶N含量在峁顶最高;叶C含量在峁顶最低;根N含量在峁顶最高;叶C/N在峁顶最低;根C/N在峁顶最低。禾本科植物叶N/P在中坡位最高(15.52±1.71), 其他坡位叶N/P值小于14, 在下坡位最低, 其值为(11.90±1.14);豆科植物叶N/P在中坡位值最高(18.72±2.01), 其次为上坡位, 其值为(17.78±2.42), 在下坡值为(15.23±3.10), 在峁顶最低, 值为(15.13±2.25);菊科植物叶N/P值在上坡位最高(14.24±4.10), 在其他坡位叶N/P值均小于14, 在下坡位最低, 其值为(9.40±0.71)。

|
| 图 2 不同科属植物C、N、P含量及其化学计量比随微地形的变化 Fig. 2 Changes of C, N, P content and its stoichiometric ratio of different genera plants along with the change of micro topography |
表 2为豆科植物C、N、P含量及其化学计量特征的相关性。豆科植物叶N含量和叶P含量呈正相关(P < 0.05), 与根C/N呈极显著负相关(P < 0.01);叶C含量与根C含量和根C/N呈负相关(P < 0.05);根N含量与叶C/N呈负相关(P < 0.05);根C含量与叶C/P比呈正相关(P < 0.05);叶C/N与根C/N呈极显著正相关(P < 0.01);叶C/P与叶N/P呈极显著正相关(P < 0.01);根C/P与根N/P呈极显著正相关(P < 0.01)(表 2)。
| 指标Index | 叶N含量LN | 叶P含量LP | 叶C含量LC | 根N含量RN | 根P含量RP | 根C含量RC | 叶C/NLC/LN | 叶C/PLC/LP | 叶N/PLN/LP | 根C/NRC/RN | 根C/PRC/RP | 根N/PRN/RP |
| 叶N含量 | 1 | |||||||||||
| 叶P含量 | 0.493* | 1 | ||||||||||
| 叶C含量 | -0.124 | -0.229 | 1 | |||||||||
| 根N含量 | 0.418 | 0.117 | -0.057 | 1 | ||||||||
| 根P含量 | -0.117 | -0.414 | 0.156 | -0.249 | 1 | |||||||
| 根C含量 | -0.317 | -0.542* | 0.256 | 0.334 | 0.275 | 1 | ||||||
| 叶C/N | -0.460 | -0.494* | 0.147 | 0.206 | 1 | |||||||
| 叶C/P | -0.375 | -0.120 | 0.405 | 0.507* | 0.372 | 1 | ||||||
| 叶N/P | 0.191 | 0.256 | 0.258 | 0.264 | -0.449 | 0.644** | 1 | |||||
| 根C/N | -0.603** | -0.481* | 0.137 | 0.437 | 0.618** | 0.436 | -0.067 | 1 | ||||
| 根C/P | -0.022 | 0.379 | -0.034 | 0.350 | 0.011 | -0.379 | -0.364 | -0.362 | 1 | |||
| 根N/P | 0.065 | 0.397 | -0.072 | -0.116 | -0.066 | -0.401 | -0.312 | -0.447 | 0.989** | 1 | ||
| ** P < 0.01, * P < 0.05;LN:叶N含量Leaf nitrogen concentration; LP:叶P含量Leaf phosphorus concentration; LC:叶C含量Leaf carbon concentration; RN:根N含量Root nitrogen concentration; RP:根P含量Root phosphorus concentration; RC:根C含量Root carbon concentration; LC/LN:叶C/N Leaf C:N ratios; LC/LP:叶C/P Leaf C:P ratios; LN/LP:叶N/P Leaf N:P ratios; RC/RN:根C/N Root C:N ratios; RC/RP:根C/P Root C:P ratios; RN/RP:根N/P Root N:P ratios | ||||||||||||
表 3为禾本科植物C、N、P含量及其化学计量特征的相关性。由表 3可以看出, 禾本科植物叶N含量与叶P含量和根N含量呈极显著正相关(P < 0.01);叶P含量与根P含量和叶C/N呈显著负相关(P < 0.05);根N含量与根C含量呈极显著正相关(P < 0.01);根P含量与叶C/N呈显著正相关(P < 0.05), 与叶C/P和叶N/P呈极显著正相关(P < 0.01);叶C/N与叶C/P呈极显著正相关(P < 0.01);叶C/P比和叶N/P呈极显著正相关(P < 0.01);根C/P与根N/P呈极显著正相关(P < 0.01)。
| 指标Index | 叶N含量LN | 叶P含量LP | 叶C含量LC | 根N含量RN | 根P含量RP | 根C含量RC | 叶C/NLC/LN | 叶C/PLC/LP | 叶N/PLN/LP | 根C/NRC/RN | 根C/PRC/RP | 根N/PRN/RP |
| 叶N含量 | 1 | |||||||||||
| 叶P含量 | 0.552** | 1 | ||||||||||
| 叶C含量 | 0.254 | 0.108 | 1 | |||||||||
| 根N含量 | 0.534** | 0.042 | 0.150 | 1 | ||||||||
| 根P含量 | -0.149 | -0.470* | 0.282 | -0.169 | 1 | |||||||
| 根C含量 | 0.225 | -0.170 | 0.061 | 0.507** | -0.029 | 1 | ||||||
| 叶C/N | -0.437* | -0.184 | 0.485* | -0.091 | 1 | |||||||
| 叶C/P | -0.295 | -0.056 | 0.631** | -0.034 | 0.749** | 1 | ||||||
| 叶N/P | 0.006 | 0.117 | 0.543** | 0.110 | 0.391 | 0.880** | 1 | |||||
| 根C/N | -0.203 | -0.228 | -0.089 | 0.057 | 0.057 | 0.009 | 0.021 | 1 | ||||
| 根C/P | 0.130 | 0.235 | -0.124 | 0.213 | -0.294 | -0.317 | -0.230 | 0.086 | 1 | |||
| 根N/P | 0.165 | 0.274 | -0.131 | 0.137 | -0.323 | -0.351 | -0.266 | -0.134 | 0.934** | 1 | ||
| ** P < 0.01, * P < 0.05 | ||||||||||||
表 4为菊科植物C、N、P含量及其化学计量特征的相关性。由表 4可以看出, 菊科植物叶P含量和根C含量呈显著负相关(P < 0.05);根C含量与叶C/P和叶N/P呈显著正相关(P < 0.05);叶C/P与根C/N呈显著正相关(P < 0.05), 与叶N/P呈极显著正相关(P < 0.01);根C/P与根N/P呈极显著正相关(P < 0.01)。
| 指标Index | 叶N含量LN | 叶P含量LP | 叶C含量LC | 根N含量RN | 根P含量RP | 根C含量RC | 叶C/NLC/LN | 叶C/PLC/LP | 叶N/PLN/LP | 根C/NRC/RN | 根C/PRC/RP | 根N/PRN/RP |
| 叶N含量 | 1 | |||||||||||
| 叶P含量 | 0.178 | 1 | ||||||||||
| 叶C含量 | -0.314 | -0.398 | 1 | |||||||||
| 根N含量 | 0.289 | 0.250 | -0.193 | 1 | ||||||||
| 根P含量 | 0.208 | -0.184 | 0.126 | -0.045 | 1 | |||||||
| 根C含量 | -0.068 | -0.489* | 0.211 | 0.193 | 0.018 | 1 | ||||||
| 叶C/N | -0.353 | -0.275 | -0.086 | 0.193 | 1 | |||||||
| 叶C/P | -0.165 | -0.266 | 0.074 | 0.473* | 0.334 | 1 | ||||||
| 叶N/P | 0.161 | -0.223 | 0.127 | 0.429* | -0.009 | 0.923** | 1 | |||||
| 根C/N | -0.229 | -0.397 | 0.182 | 0.041 | 0.245 | 0.427* | 0.396 | 1 | ||||
| 根C/P | -0.127 | 0.081 | -0.216 | 0.049 | -0.055 | -0.110 | -0.118 | -0.099 | 1 | |||
| 根N/P | -0.061 | 0.126 | -0.189 | -0.132 | -0.088 | -0.170 | -0.166 | -0.257 | 0.981** | 1 | ||
| ** P < 0.01, * P < 0.05 | ||||||||||||
表 5为植物C、N、P含量及其化学计量特征的相关性。叶N含量与叶P含量, 根N含量, 根C含量极显著正相关(P < 0.01), 与根N/P呈显著正相关(P < 0.05), 与叶C/P、根C/N呈极显著负相关(P < 0.01);叶P含量与根N含量、根C/P、根N/P呈显著正相关(P < 0.05), 与根P含量极显著正相关(P < 0.01), 与叶C/N极显著负相关, 与根C/N显著负相关(P < 0.05);根N含量与根C含量极显著正相关(P < 0.01), 与叶N/P显著正相关(P < 0.05), 与叶C/N极显著负相关(P < 0.01), 与叶C/P显著负相关(P < 0.05);根P含量与叶C/P极显著正相关, 与叶C/N极显著正相关(P < 0.05);根C含量与叶C/N极显著负相关(P < 0.01);叶C/N与叶C/P、根C/N极显著正相关(P < 0.01), 与根N/P显著负相关(P < 0.05);叶C/P与叶N/P极显著正相关(P < 0.01), 与根C/P、根N/P显著负相关(P < 0.05);根C/N与根N/P呈显著负相关(P < 0.05);根C/P与根N/P呈极显著正相关(P < 0.01)(表 5)。
| 指标Index | 叶N含量LN | 叶P含量LP | 叶C含量LC | 根N含量RN | 根P含量RP | 根C含量RC | 叶C/NLC/LN | 叶C/PLC/LP | 叶N/PLN/LP | 根C/NRC/RN | 根C/PRC/RP | 根N/PRN/RP |
| 叶N含量 | 1 | |||||||||||
| 叶P含量 | 0.423** | 1 | ||||||||||
| 叶C含量 | 0.017 | -0.037 | 1 | |||||||||
| 根N含量 | 0.752** | 0.281* | 0.021 | 1 | ||||||||
| 根P含量 | -0.177 | 0.394** | 0.177 | -0.234 | 1 | |||||||
| 根C含量 | 0.399** | 0.112 | 0.137 | 0.638** | -0.173 | 1 | ||||||
| 叶C/N | -0.468** | -0.730** | 0.298* | -0.479** | 1 | |||||||
| 叶C/P | -0.356** | -0.290* | 0.410** | -0.147 | 0.530** | 1 | ||||||
| 叶N/P | 0.055 | 0.265* | 0.218 | 0.223 | -0.203 | 0.697** | 1 | |||||
| 根C/N | -0.485** | -0.279* | 0.001 | 0.126 | 0.428** | 0.222 | -0.075 | 1 | ||||
| 根C/P | 0.079 | 0.248* | -0.101 | 0.184 | -0.181 | -0.257* | -0.171 | -0.037 | 1 | |||
| 根N/P | 0.248* | 0.298* | -0.091 | 0.195 | -0.301* | -0.305* | -0.123 | -0.289* | 0.899** | 1 | ||
| ** P < 0.01, * P < 0.05 | ||||||||||||
植物C、N、P含量以及化学计量特征反映了植物对水分胁迫等不利环境的防御和适应策略[10]。叶N含量, 叶P含量, 根N含量, 根C含量, 叶C/N, 叶C/P, 叶N/P, 根C/N, 根N/P在科属水平上差异性显著(P < 0.05), 表明了不同科属植物对外界环境防御和适应策略的差异性。植物叶片N、P含量越高, 表明其光合速率越高, 生长速率越快, 资源竞争能力越强, 而叶片C含量高则表明其比叶重大, 光合速率低, 生长速率慢, 具有较强的防御能力[16-17]。本研究中豆科植物有较高的叶N含量和叶P含量, 表明豆科植物具有较强的资源获取能力和较高的利用效率, 而菊科具有最高的叶C含量, 表明菊科植物主要通过增强防御能力来适应不利环境。植物叶片的C/N和C/P值与植物对C的同化能力有关, 一定程度上可反映植物的营养利用效率[18]。本研究表明, 禾本科植物拥有最高的LC/LN值和较高的LC/LP值, 具有有较强的C同化能力。植物叶片的N:P值可以作为判断限制植物生长的营养元素指标, N/P小于14的植物生长主要受到N元素的限制, N/P大于16的植物生长主要受P元素的限制[6]。由图 1看出叶N/P豆科植物最高(16.61±1.17) g/kg, 菊科植物最低(12.40±1.31) g/kg, 表明黄土丘陵区不同科属植物生长受限制的营养元素不同, 豆科植物生长主要受P元素的限制, 禾本科和菊科植物生长主要N元素的限制。与全球尺度上植被叶片N/P的均值11.8相比[19], 黄土丘陵区各科属植被中叶片的N/P均较高, 说明黄土丘陵区的植被生产力主要受P的限制。
本次研究表明, 黄土丘陵区15种典型草本植物叶片的C含量高于全球492种陆生植物的叶片C含量[25] (表 6);与一些单个生态系统相比, 黄土丘陵区植物C含量也呈现较高水平, 例如, 显著高于新疆草地植物的434 mg/ g [22-23]、西藏草地的435 mg/g[22-23]和内蒙古草地的450 mg/g[22-23], 说明黄土丘陵区草本植物总体对干旱等不利环境具有较强的防御能力。N、P元素作为植物体内两种容易短缺的营养元素, 是限制陆地生态系统生产力的重要因子[26]。Han等[24]通过对我国陆生植物叶片N、P的研究发现, 我国陆生植物的叶片N含量为20.24mg/g与Elser等[25]对全球植物叶片的N含量20.60mg/g比较接近, 但叶片中P含量1.46mg/g显著低于全球陆地生物的测定值1.99 mg/g[25], N/P比大于16, 说明我国植物的生长主要受P限制。本次研究中植物叶片N含量20.44mg/g显著低于内蒙古草地N含量26.8mg/g[22-23]、新疆草地25.9mg/g[22-23]、西藏草地28.6mg/g[22-23], 但与Han等[24]测定的陆生植物的叶片N含量20.24mg/g(表 6)相接近;叶片P含量1.52mg/g低于内蒙古草地叶片P含量1.8mg/g[22-23]、新疆草地叶片P含量2.0mg/g[22-23]和西藏草地叶片P含量1.9mg/g[22-23], 相比之下, 与Han[24]等对中国陆地植物叶片P测定的的结果较为相近, 叶片N/P与郑淑霞[20]等在黄土高原的测定值相近, 大于宋彦涛[21]等松嫩草地的测定值, 说明在黄土丘陵地区, 植物的生长受到P限制较大。
| 研究区域Study area | 全碳/(mg/g)Total C | 全氮/(mg/g)Total N | 全磷/(mg/g)Total P | 碳/氮C/N | 碳/磷C/P | 氮/磷N/P | 参考文献References |
| 黄土丘陵区Hilly and gully region of the Loess Plateau | 474.09±56.86 | 20.44±8.67 | 1.52±0.57 | 25.00±6.61 | 337.46±149.08 | 15.08±5.26 | 本研究 |
| 黄土高原Loess Plateau | 438.00±43 | 24.10±8.5 | 1.60±0.6 | 21.2±10.2 | 312±135 | 15.4±3.9 | [20] |
| 松嫩草地Songnen grassland | 24.2 | 2.0 | 13.0 | [21] | |||
| 内蒙古草地Inner Mongolia grassland | 450.00±19.9 | 26.8±7.7 | 1.8±0.71 | 18.7±5.2 | 250 | 16.4±5.68 | [22-23] |
| 新疆草地Xinjiang grassland | 434.00±27.3 | 25.9±8.9 | 2.0±1.00 | 18.8±6.2 | 217 | 13.4±4.02 | [22-23] |
| 西藏草地Xizang grassland | 435.00±39.9 | 28.6±8.8 | 1.9±0.81 | 17.0±5.4 | 228.95 | 15.7±5.26 | [22-23] |
| 中国China | 20.24±8.4 | 1.46±0.99 | 16.30±9.32 | [24] | |||
| 全球World | 464.20±32.1 | 20.60±12.2 | 1.99±1.49 | 22.5±10.6 | 232±145 | 12.70±6.82 | [25] |
豆科和菊科植物叶N和叶P含量呈显著正相关(P < 0.05), 验证了高等陆生植物养分计量的普遍规律, 叶N和叶P这种正相关关系, 是种群能够稳定生长发育的有力保障, 也是植物最基本的特性之一[27], 豆科、禾本科、菊科植物叶片和细根C、N、P含量及其化学计量比之间存在不同的相关关系(表 2—表 4), 这表明不同科属植物通过叶片和细根不同功能间的调整以及相互作用关系来适应外界环境的变化, 并且不同科属植物对外界环境的适应策略有很大的差异, 这与施宇[28]等研究结论一致。豆科植物与禾本科植物C、N、P含量及其化学计量比之间具有紧密的相关关系, 说明豆科与禾本科植物对环境具有较强的整体适应性(可通过各个性状的协调来适应), 相比较而言, 菊科植物C、N、P含量及其化学计量比之间的相关性较差, 说明菊科植物更多是通过各性状的适应性变化来响应环境变化。叶片N含量和叶片P含量、根N含量、根C含量呈极显著正相关;叶P含量和根P含量、根N含量呈显著正相关(表 5), 这与周鹏[29]、徐冰[30]等的研究结果一致, 这可能是由于植物生长时, 通过根系吸收土壤中的N、P等营养元素, 同时将吸收来的营养元素输送给植物体其他各个器官, 叶片利用这些营养物质进行光合作用, 并把光合作用固定的能量输送给根系和其他器官。植物叶片与细根N、P含量的相关性表明, 植物体生长代谢的过程具有协调性、整体性, N、P等营养元素在地上、地下主要器官之间的分配遵循一定的规律[30]。植物叶片和细根C、N、P含量及其化学计量特征的相关性密切, 也表明植物体叶片和细根的协调能力强, 可以更好地适应丘陵山地的恶劣环境。
本研究结果表明:除禾本科根C/N在阴坡、阳坡差异显著之外, 禾本科、豆科和菊科植物C、N、P含量及其化学计量特征在阴坡、阳坡存在差异, 但差异不显著。这可能是因为采样过程中, 阴坡、阳坡相隔比较近, 所选样地没有在正阳坡, 正阴坡的位置, 导致采样中阴阳坡光照, 温度, 土壤水分, 养分等因子变化较小, 使得由于坡向引起的微环境的变化没有引起不同科属植物植物C、N、P含量及其化学计量特征的变化。禾本科植物化学计量特征在不同坡位间差异不显著;豆科植物根N含量在坡位间差异显著(P < 0.05), 根N含量在峁顶最高, 这可能是黄土高原地区土壤表层土壤有效N含量峁顶最高[31], 因此豆科植物可以通过对土壤中N素的吸收和自身的固氮能力来增加根N含量。菊科植物叶N含量, 叶C含量, 根N含量, 叶C/N, 根C/N在不同坡位间差异显著(P < 0.05), 其中叶C/N, 根C/N在不同坡位间差异显著(P < 0.05)可能是因为叶N和根N含量在不同坡位间差异较大导致的。豆科和菊科植物叶N含量和根N含量在峁顶最高, 峁顶位置光照充足, 较高的叶N含量有利于植物充分利用光照进行光合作用制造有机物, 较高的根N含量有利于根对水分的吸收[32], 进而抵御干旱的环境, 有利于植物更好的适应外界环境。综上可以看出, 豆科叶N含量、根N含量、根C含量、叶N/P、根N/P最高, 叶C/N、根C/N最低;在阴阳坡差异不显著;豆科植物根N含量在不同坡位间差异显著(P < 0.05), 根N含量在峁顶最高。禾本科叶C/N、叶C/P最高, 叶N含量、叶P含量、根C含量最低;禾本科在阴阳坡差异显著;菊科叶P含量最高, 叶N/P最低;在阴阳坡差异不显著;菊科植物叶N含量, 叶C含量, 根N含量, 叶C/N, 根C/N在不同坡向和坡位间差异显著(P < 0.05), 并且叶N含量在峁顶最高;叶C含量在峁顶最低;根N含量在峁顶最高;叶C/N在峁顶最低;根C/N在峁顶最低。禾本科和豆科C、N、P含量及化学计量比间的相关性密切, 菊科相对较弱(表 2—表 4), 这可能与菊科植物C、N、P含量及化学计量比对微地形变化比较敏感有关(图 2)。比较而言, 豆科植物与禾本科植物对环境具有较强的整体适应性(可通过各个性状的协调来适应), 菊科植物C、N、P含量及其化学计量比之间的相关性较差, 说明菊科植物更多是通过各性状的适应性变化来响应环境变化。
| [1] | Elser J J, Dobberfuhl D R, MacKay N A, Schampel J H. Organism size, life history, and N:P stoichiometry. BioScience , 1996, 46 (9) : 674–684. DOI:10.2307/1312897 |
| [2] | 贺金生, 韩兴国. 生态化学计量学:探索从个体到生态系统的统一化理论. 植物生态学报 , 2010, 34 (1) : 2–6. |
| [3] | Dawson T P, Curran P J. Technical note A new technique for interpolating the reflectance red edge position. International Journal of Remote Sensing , 1998, 19 (11) : 2133–2139. DOI:10.1080/014311698214910 |
| [4] | Güsewell S. N:P ratios in terrestrial plants:variation and functional significance. New Phytologist , 2004, 164 (2) : 243–266. DOI:10.1111/j.1469-8137.2004.01192.x |
| [5] | Niklas K J, Cobb E D. N, P, and C stoichiometry of Eranthis hyemalis (Ranunculaceae) and the allometry of plant growth. American Journal of Botany , 2005, 92 (8) : 1256–1263. DOI:10.3732/ajb.92.8.1256 |
| [6] | Aerts R, Chapin Ⅲ F S. The mineral nutrition of wild plants revisited:a re-evaluation of processes and patterns. Advances in Ecological Research , 1999, 30 : 1–67. DOI:10.1016/S0065-2504(08)60016-1 |
| [7] | 刘旻霞.高寒草甸坡向梯度上植物群落组成及其氮磷化学计量学特征的研究[D].兰州:兰州大学, 2013. http://cdmd.cnki.com.cn/article/cdmd-10730-1013239276.htm |
| [8] | 祁建, 马克明, 张育新. 辽东栎(Quercus liaotungensis)叶特性沿海拔梯度的变化及其环境解释. 生态学报 , 2007, 27 (3) : 930–937. |
| [9] | 祁建, 马克明, 张育新. 北京东灵山不同坡位辽东栎(Quercus liaotungensis)叶属性的比较. 生态学报 , 2008, 28 (1) : 122–128. |
| [10] | 王凯博, 上官周平. 黄土丘陵区燕沟流域典型植物叶片C、N、P化学计量特征季节变化. 生态学报 , 2011, 31 (17) : 4985–4991. |
| [11] | 朱秋莲, 邢肖毅, 张宏, 安韶山. 黄土丘陵沟壑区不同植被区土壤生态化学计量特征. 生态学报 , 2013, 33 (15) : 4674–4682. |
| [12] | Zheng S X, Shangguan Z P. Spatial patterns of leaf nutrient traits of the plants in the Loess Plateau of China. Trees , 2007, 21 (3) : 357–370. DOI:10.1007/s00468-007-0129-z |
| [13] | 张健, 刘国彬, 许明祥, 王兵, 王翼龙, 齐智军. 黄土丘陵区沟谷地植被恢复群落特征研究. 草地学报 , 2008, 16 (5) : 485–490. |
| [14] | 杨士梭, 温仲明, 苗连朋, 戚德辉, 花东文. 黄土丘陵区植物功能性状对微地形变化的响应. 应用生态学报 , 2014, 25 (12) : 3413–3419. |
| [15] | Bao S D. Analysis Methods for Soil Agro-Chemistry. Beijing: China Agriculture Press, 2000. |
| [16] | Wright I J, Reich P B, Westoby M, Ackerly D D, Baruch Z, Bongers F, Cavender-Bares J, Chapin T, Cornelissen J H C, Diemer M, Flexas J, Garnier E, Groom P K, Gulias J, Hikosaka K, Lamont B B, Lee T, Lee W, Lusk C, Midgley J J, Navas M L, Niinemets V, Oleksyn J, Osada N, Poorter H, Poot P, Prior L, Pyankov V I, Roumet C, Thomas S C, Tjoelker M G, Veneklaas E J, Villar R. The worldwide leaf economics spectrum. Nature , 2004, 428 (6985) : 821–827. DOI:10.1038/nature02403 |
| [17] | Poorter L, Bongers F. Leaf traits are good predictors of plant performance across 53 rain forest species. Ecology , 2006, 87 (7) : 1733–1743. DOI:10.1890/0012-9658(2006)87[1733:LTAGPO]2.0.CO;2 |
| [18] | 黄建军, 王希华. 浙江天童32种常绿阔叶树叶片的营养及结构特征. 华东师范大学学报:自然科学版 , 2003 (1) : 92–97. |
| [19] | Reich P B, Oleksyn J. Global patterns of plant leaf N and P in relation to temperature and latitude. Proceedings of the National Academy of Sciences of the United States of America , 2004, 101 (30) : 11001–11006. DOI:10.1073/pnas.0403588101 |
| [20] | 郑淑霞, 上官周平. 黄土高原地区植物叶片养分组成的空间分布格局. 自然科学进展 , 2006, 16 (8) : 965–973. |
| [21] | 宋彦涛, 周道玮, 李强, 王平, 黄迎新. 松嫩草地80种草本植物叶片氮磷化学计量特征. 植物生态学报 , 2012, 36 (3) : 222–230. |
| [22] | He J S, Fang J Y, Wang Z H, Guo D L, Flynn D F B, Geng Z. Stoichiometry and large-scale patterns of leaf carbon and nitrogen in the grassland biomes of China. Oecologia , 2006, 149 (1) : 115–122. DOI:10.1007/s00442-006-0425-0 |
| [23] | He J S, Wang L, Flynn D F B, Wang X P, Ma W H, Fang J Y. Leaf nitrogen:phosphorus stoichiometry across Chinese grassland biomes. Oecologia , 2008, 155 (2) : 301–310. DOI:10.1007/s00442-007-0912-y |
| [24] | Han W X, Fang J Y, Guo D L, Zhang Y. Leaf nitrogen and phosphorus stoichiometry across 753 terrestrial plant species in China. New Phytologist , 2005, 168 (2) : 377–385. DOI:10.1111/j.1469-8137.2005.01530.x |
| [25] | Elser J J, Fagan W F, Denno R F, Dobberfuhl D R, Folarin A, Huberty A, Interlandi S, Kilham S S, McCauley E, Schulz K L, Siemann E H, Sterner R W. Nutritional constraints in terrestrial and freshwater food webs. Nature , 2000, 408 (6812) : 578–580. DOI:10.1038/35046058 |
| [26] | 张珂, 何明珠, 李新荣, 谭会娟, 高艳红, 李刚, 韩国君, 吴杨杨. 阿拉善荒漠典型植物叶片碳、氮、磷化学计量特征. 生态学报 , 2014, 34 (22) : 6538–6547. |
| [27] | 吴统贵, 吴明, 刘丽, 萧江华. 杭州湾滨海湿地3种草本植物叶片N、P化学计量学的季节变化. 植物生态学报 , 2010, 34 (1) : 23–28. |
| [28] | 施宇, 温仲明, 龚时慧. 黄土丘陵区植物叶片与细根功能性状关系及其变化. 生态学报 , 2011, 31 (22) : 6805–6814. |
| [29] | 周鹏, 耿燕, 马文红, 贺金生. 温带草地主要优势植物不同器官间功能性状的关联. 植物生态学报 , 2010, 34 (1) : 7–16. |
| [30] | 徐冰, 程雨曦, 甘慧洁, 周文嘉, 贺金生. 内蒙古锡林河流域典型草原植物叶片与细根性状在种间及种内水平上的关联. 植物生态学报 , 2010, 34 (1) : 29–38. |
| [31] | 卢金伟, 李占斌, 郑良勇, 郭彦彪. 陕北黄土区土壤水分养分空间分异规律. 山地学报 , 2002, 20 (1) : 108–111. |
| [32] | Sardans J, Peñuuelas J, Estiarte M, Prieto P. Warming and drought alter C and N concentration, allocation and accumulation in a Mediterranean shrubland. Global Change Biology , 2008, 14 (10) : 2304–2316. DOI:10.1111/gcb.2008.14.issue-10 |
 2016, Vol. 36
2016, Vol. 36