文章信息
- 陈荣荣, 刘全全, 王俊, 刘文兆, UpendraM.Sainju
- CHEN Rongrong, LIU Quanquan, WANG Jun, LIU Wenzhao, Upendra M. Sainju
- 人工模拟降水条件下旱作农田土壤“Birch效应”及其响应机制
- Response of soil "Birch Effect" to simulated rainfalls in dry croplands
- 生态学报, 2016, 36(2): 306-317
- Acta Ecologica Sinica, 2016, 36(2): 306-317
- http://dx.doi.org/10.5846/201403120428
-
文章历史
- 收稿日期: 2014-03-12
- 网络出版日期: 2015-06-08
2. 中国科学院水利部水土保持研究所, 杨凌 712100;
3. USDA-ARS Northern Plains Agricultural Research Laboratory, Sidney, MT 59270 USA
2. Institute of Soil and Water Conservation, Chinese Academy of Sciences and Ministry of Water Resources, Yangling 712100, China;
3. USDA-ARS Northern Plains Agricultural Research Laboratory, Sidney, MT 59270, USA
土壤呼吸是调控全球碳平衡的关键过程之一,其微小的变化就对大气中CO2浓度产生较大影响[1]。降水事件导致土壤水分状况快速变化,刺激土壤有机质矿化过程,导致土壤呼吸速率较正常状态提高数倍到数十倍然后快速回落[2, 3]。这种由于降水或土壤干湿变化导致的土壤CO2脉冲释放现象近年来被称为“Birch效应”[4]。偶然的降水事件,即使降水量很小也会大量增加土壤CO2的释放,而这些CO2的脉冲释放在生态系统碳平衡中充当重要的角色,并直接影响土壤碳循环过程。此现象已成为当前全球变化生态学领域重要的研究课题之一,Xu等、Jarvis等和Inglima等已在不同类型的生态系统中验证了“Birch效应”[5, 6, 7],目前国内外研究多集中于不同类型生态系统多次干湿交替过程中“Birch效应”的变化特征分析[8, 9, 10],但针对于降水格局本身的改变对土壤“Birch效应”的影响及其土壤学响应机制的研究尚少涉及。
近年来,解释降水导致 “Birch效应的主要两种响应机制:干土复湿破坏土壤团粒结构释放团粒体内包裹的有机碳/质底物的“底物供给”机制[11, 12]和土壤水势快速变化刺激微生物代谢释放出胞内物质的“微生物胁迫”机制[13]。例如,Xiang[14]在美国加利福尼亚草原的试验表明“底物供给机制”是解释“Birch效应”的主导机制;Wu和Brookes[3]的草地实验结果与Fierer和Schimel[15]在美国加利福尼亚林地的研究则证明了“微生物胁迫”在Birch效应中的主导作用。此外,还有学者则认为“Birch效应”是两种机制共同作用的结果[16]。不同的主导机制对土壤碳库和土壤碳氮平衡产生的影响不同,“底物供给”机制会释放团粒中稳态碳,破坏土壤中碳氮平衡,而“微生物胁迫”机制则会导致微生物量碳 (MBC) 的增加。通过测定降水前后的土壤可提取性碳(EOC)、微生物量碳 (MBC)、氯仿熏蒸-K2SO4提取态有机碳(CFE)的碳分组变化可以定量两种机制的相对重要性[16]。为了准确评估降水激发效应对土壤碳/氮收支的影响,需要针对典型的生态系统阐明两种机制的相对重要性。
在我国黄土高原地区,降水是限制当地农田生态系统生产力形成的主控因子,同时由于对土壤CO2释放的激发效应降水事件本身也会影响生态系统碳循环过程。从气象观测资料来看,黄土高原地区气候在过去几十年呈显著的暖干趋势,而对未来气候的预测中,该地区降水量和极端降水事件发生概率均会增加[17],在此背景下,有必要深入开展降水格局变化对土壤“Birch效应”的影响及其土壤学响应机制的研究。本文基于田间模拟降水试验,结合土壤呼吸速率和土壤碳分组分析,研究降水量变化对土壤CO2释放过程及其响应机制的影响,旨在加深对旱作农田土壤碳循环过程的理解,为准确预测全球气候变化条件下降水变化对农田生态系统碳平衡的影响提供科学依据。
1 材料与方法 1.1 研究区概况试验地位于中国科学院长武农业生态试验站(107°44.703′E,35°12.78′N),该区塬面地势平坦海拔1200 m,年均降雨584 mm,多分布在7—9月份,年平均气温9.1 ℃。农业生产全部依靠自然降水,属典型的旱作农业区。土壤属黑垆土,pH值为8.4,土壤有机质含量约 3%,土质均匀疏松。降雨分布不均,年际间变异大,干旱频繁[18]。
1.2 试验设计根据试验站多年降水资料,在小麦拔节期(2013年5月2日)和夏闲期(2013年8月22日)通过人工降水设备模拟单次不同降水量降水事件,夏闲期降水前7—10 d试验区内无降水,保证土壤处于干旱或缺水的状况。降水量处理设计1、3、8、16、32 mm共5个水平,其中1 mm和8 mm为多年夏季降水资料最小值和中值,3 mm为常规小量降水,16 mm为中量降水,32 mm用于模拟极端降水事件[19-0]。试验采用杨凌241 T旋转微喷设备模拟降水,保证单位时间的降水强度保持一致,水滴均匀的落在小区内且不形成径流。每处理3次重复,随机区组排列,各小区长4 m宽3 m,区与组间距分别为2 m与1 m。
1.3 样品采集与测定采用静态箱-气相色谱法[21, 22]测定5个降水梯度农田土壤CO2的排放速率。静态箱由两部分组成:一个置于地下8 cm地上4 cm的固定基座和一个带有通风口和采样口的气室。静态箱由聚乙烯化合物(PVC)制成(直径25 cm、高12 cm),外层用反光锡纸包裹作为隔热层,底部设有一层软橡胶在采样时可以与基座密封。基座在人工模拟降水前48 h安置,以消除由于安置基座引起土壤扰动导致的土壤呼吸波动。气体采样时将箱体罩在事先安置的基座上密闭0、20 min和40 min后用注射器(30 mL)收集气体样品,然后用气相色谱仪(安捷伦6820)分析,用TCD检测器测定样品的CO2浓度,高纯氮做载气。采用Hutchinson和Mosier提出的HM模型[23]计算气体通量。气体样品采集时间分别为降水前0.5 h、降水后0.5、1.5、4、8、12、24、48 h和72 h。
气样采集同时分别取基座附近[16]0—5 cm和5—15 cm两个层次的土样,原状冷藏保存土样至实验分析(3 d内)。土样采回后,剔除石块和动植物残体等杂质过(2 mm)筛及均质化,由于部分土壤湿度过大,置于室温晾晒,经常翻动土样防止部分微生物风干死亡。采用氯仿熏蒸-K2SO4提取法[24]获得土壤氯仿熏蒸提取碳(CFE)和可提取态有机碳(EOC),简言之,对于CFE的提取,在真空容量器中用氯仿熏蒸24 h,通过0.5 mol K2SO4浸提1 h,过0.45 μm滤膜,利用TOC仪测定浸提液中有机碳浓度,EOC提取采取上述相同的步骤,但不经过氯仿熏蒸。然后用以下公式[25]计算获得微生物量碳(MBC)
式中,Ec为熏蒸和未熏蒸样品浸提测定的有机碳差值(Ec=CFE-EOC)。采集气样的同时分别用TDR100便携式土壤水分速测仪(精度±3.0%)和数字温度传感器(-50 ℃±300 ℃)测量基座边缘0—5 cm土壤体积含水量(%)和0—5 cm土壤温度(℃)。
1.4 数据处理采用EXCEL2010对数据进行预处理并制图。土壤温度(T)和土壤水分(W)对土壤呼吸(SR)的影响分别用SR=αexp(βT)模型和SR=aW2+bW+c模型进行模拟,用SR=a+bT+cW多因子模型拟合SR与T和W的双变量关系[26],方程参数拟合、数据的相关分析、方差分析和回归分析在SPSS 20.0中进行。用土壤呼吸脉冲释放的强度表示土壤呼吸变化程度,即土壤呼吸速率峰值与降水前土壤呼吸速率的比值。用温度敏感性系数Q10值来表示土壤呼吸随温度变化程度,即温度每增加10 ℃土壤呼吸增加的倍数[27, 28],计算公式[29]为:
式中,SR为土壤呼吸速率(μmol m-2 s-1),T为土壤温度(℃),a和b为模拟计算参数值。 2 结果分析 2.1 降水前土壤性质表1所示,5月和8月模拟降水前的土壤体积含水量普遍较低且差异性不显著,大致为6.9%—9.1%,但是两个时期的土壤温度差异性达到显著水平(P < 0.05),5月土壤温度为14.3—17.5 ℃,8月土壤温度远高于5月大致为26.2—28.1 ℃。土壤呼吸速率在拔节期略高于夏闲期,土壤碳组分中的CFE和MBC拔节期均大于夏闲期,差异性达到显著水平,其中MBC达到极显著水平,EOC拔节期较夏闲期不显著。
| 项目Item | 5 月 May | 8 月 August | ||||||||
| 1 mm | 3 mm | 8 mm | 16 mm | 32 mm | 1 mm | 3 mm | 8 mm | 16 mm | 32 mm | |
| SWC/% | 6.9 a | 7.4 a | 8.1 a | 8.2 a | 8.7 a | 9.1 b | 8.0 a | 7.7 a | 6.9 a | 8.1 a |
| ST/℃ | 14.4 a | 15.7 a | 14.3 a | 17.5 a | 16.5 a | 28.1 b | 27.9 b | 25.1 b | 26.2 b | 27.9 b |
| SR/(μmol m -2 s -1) | 0.39 a | 0.41 a | 0.38 a | 0.42 a | 0.42 a | 0.34 b | 0.31 b | 0.30 b | 0.39 a | 0.37 b |
| CFE/(mg/kg) | 354 a | 334 a | 331 a | 323 a | 319 a | 302 b | 329 a | 313 b | 301 b | 311 b |
| EOC/(mg/kg) | 227 a | 216 a | 222 a | 218 a | 227 a | 226 a | 234 a | 228 a | 218 a | 239 a |
| MBC/(mg/kg) | 281 a | 261 a | 243 a | 233 a | 203 b | 170 c | 212 b | 188 c | 186 c | 161 c |
| SWC: 土壤体积含水量soil water content; ST: 土壤温度Soil temperature; SR: 土壤呼吸速率Soil respiration;CFE: 氯仿熏蒸-K 2SO 4提取态有机碳Chloroform-fumigated extracted carbon;EOC: 土壤可提取性碳Extractable organic carbon;MBC: 土壤微生物量碳Microbial organic carbon | ||||||||||
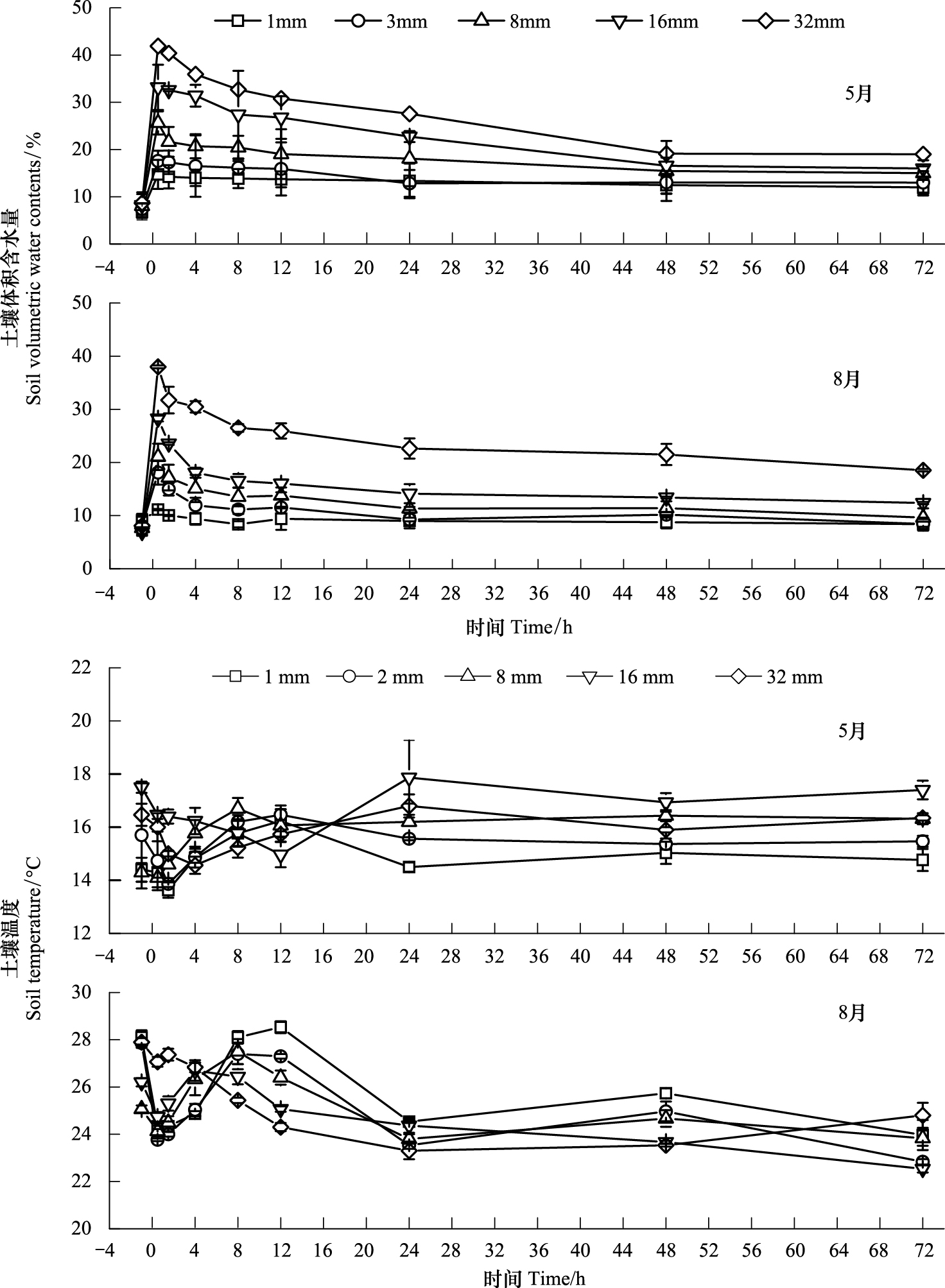
降水事件短期内显著提高了土壤含水量(图1),在模拟降水后0.5—1.5 h土壤含水量达到峰值,5月和8月模拟降水土壤含水量峰值分别为14.72%—41.9%和11.13%—38.0%。1、3 mm和8 mm模拟降水在4 d后恢复到原始水平,而16 mm和32 mm处理在降水后5 d依然略高于降水前水平(数据未列出)。
|
| 图 1 两次模拟降水后土壤体积含水量和土壤温度变化 Fig.1 Dynamics of soil volumetric water content and soil temperature after rainfall simulations |
受土壤水分和气温日差的影响,土壤温度在降水后1.5 h内随土壤水分的升高而降低,在4 h恢复到降水前水平。总体来看,土壤温度随降水量的增加而降低且变化趋势与土壤含水量相反,5月份的土壤温度要低于8月份。
2.3 土壤呼吸降水对土壤呼吸具有显著激发作用(图2),5月和8月模拟降水后1—32 mm处理土壤呼吸速率最大值分别为0.86—1.30 μmol m-2 s-1和1.08—1.48 μmol m-2 s-1,分别较降水前增加了2.23—3.19和2.90—4.05倍。1—16 mm处理土壤呼吸速率在降水后4 h达到峰值,32 mm在8 h达到峰值,降水量的增加推后了土壤呼吸速率峰值出现时间。达到峰值后,土壤呼吸速率迅速下降,1—8 mm降水在72 h恢复到降水前水平,16 mm和32 mm降水后96 h才恢复到降水前水平。

|
| 图 2 两次模拟降水后,不同降水梯度下土壤呼吸的动态变化 Fig.2 The variations of soil respiration following the two rainfall simulation |
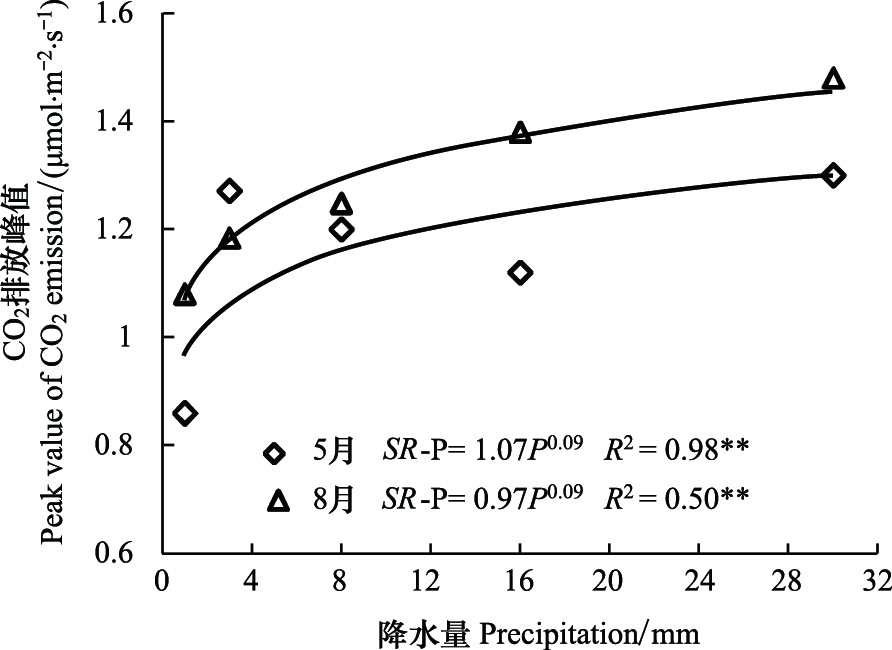
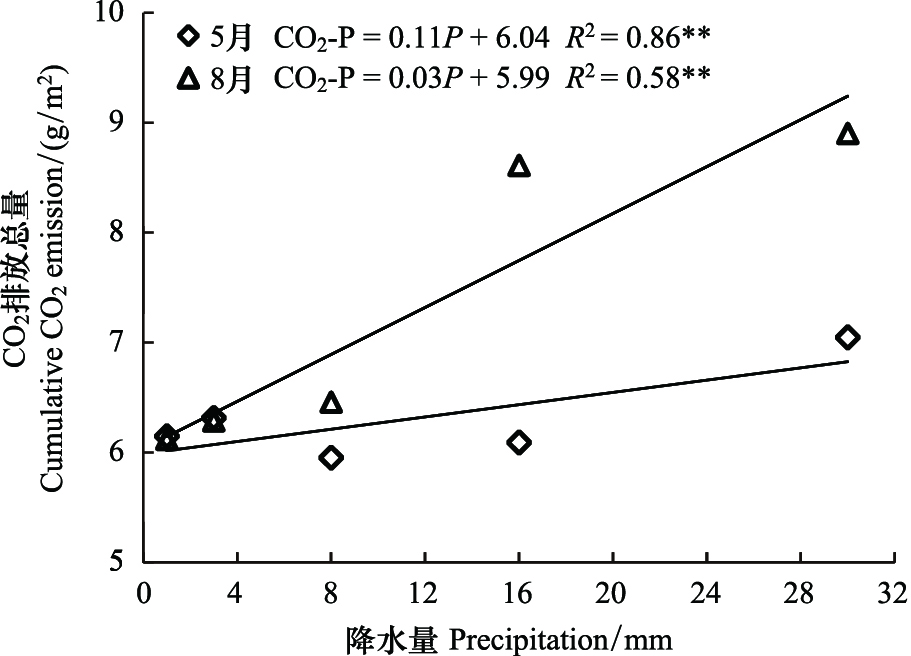
回归分析表明,土壤呼吸速率峰值与降水量的关系(图3),土壤呼吸峰值随降水量的增加而增大(P﹤0.01)。降水后72 h内土壤CO2累积释放量随降水量的增加呈显著线性增长(图4),降水量的增加会增加土壤CO2累积释放量(P﹤0.01),说明降水量的增加可以增强土壤“Birch效应”。
|
| 图 3 土壤呼吸峰值(SR-P)与降水量(P)之间关系 Fig.3 The relationship between peak value of soil respiration (SR-P) and precipitation (P) |
|
| 图 4 土壤呼吸总量(CO2-P) 与降水量(P)之间关系 Fig.4 The relationship between cumulative of soil respiration (CO2-P) and precipitation (P) |
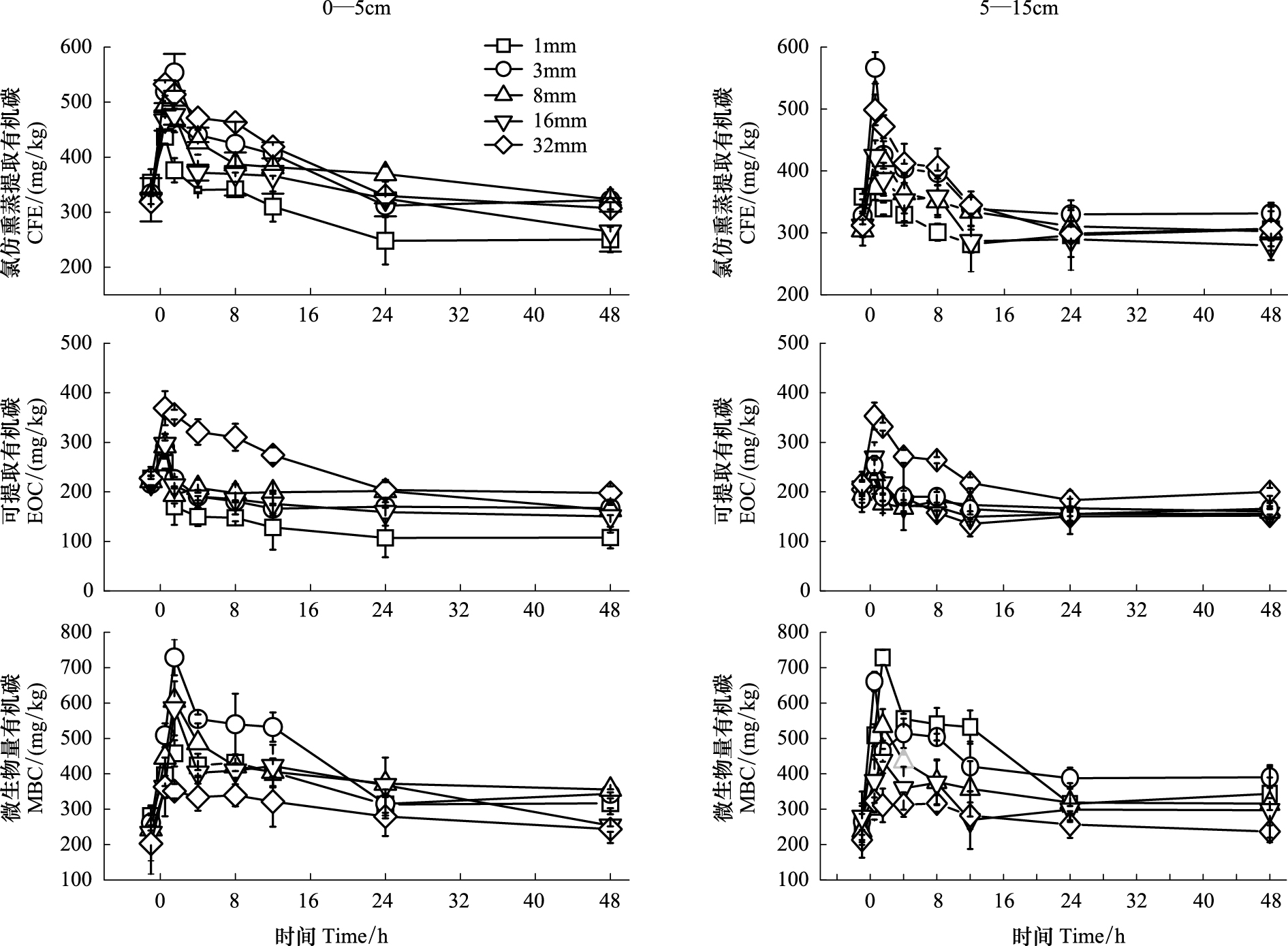
5月小麦拔节期模拟降水处理0—5 cm和5—15 cm土层碳组分浓度在降水后均有增长,并在降水后(0.5—1.5 h)达到峰值,然后逐步降低(图5)。在0—5 cm土层不同降水量对碳分组浓度变化有显著影响,其中EOC和CFE峰值浓度均随降水量增加而增大,1、3、8、16、32 mm降水量处理土壤EOC的峰值浓度分别较降水前增长了13.9%、34.1%、32.6%、36.1%和62.3%,分别较降水前增加了13.9%、34.1%、31.8%、36.1%、62.3%。土壤MBC峰值浓度并未随降水量的增加而增加,土壤MBC峰值浓度在降水达3 mm后出现转折,降水量梯度上土壤MBC峰值浓度(降水后1.5 h)较降水前分别增长了63.1%、179.0%、149.0%、151.0%、79.1%。
|
| 图 5 5月份小麦拔节期人工降水后土壤CFE、 EOC、MBC变化趋势 Fig.5 Dynamics of soil CFE、 EOC and MBC after precipitation simulation at wheat jointing stage in May CFE: 氯仿熏蒸-K2SO4提取态有机碳Chloroform-fumigated extracted carbon; EOC: 土壤可提取性碳Extractable organic carbon; MBC: 土壤微生物量碳Microbial organic carbon |
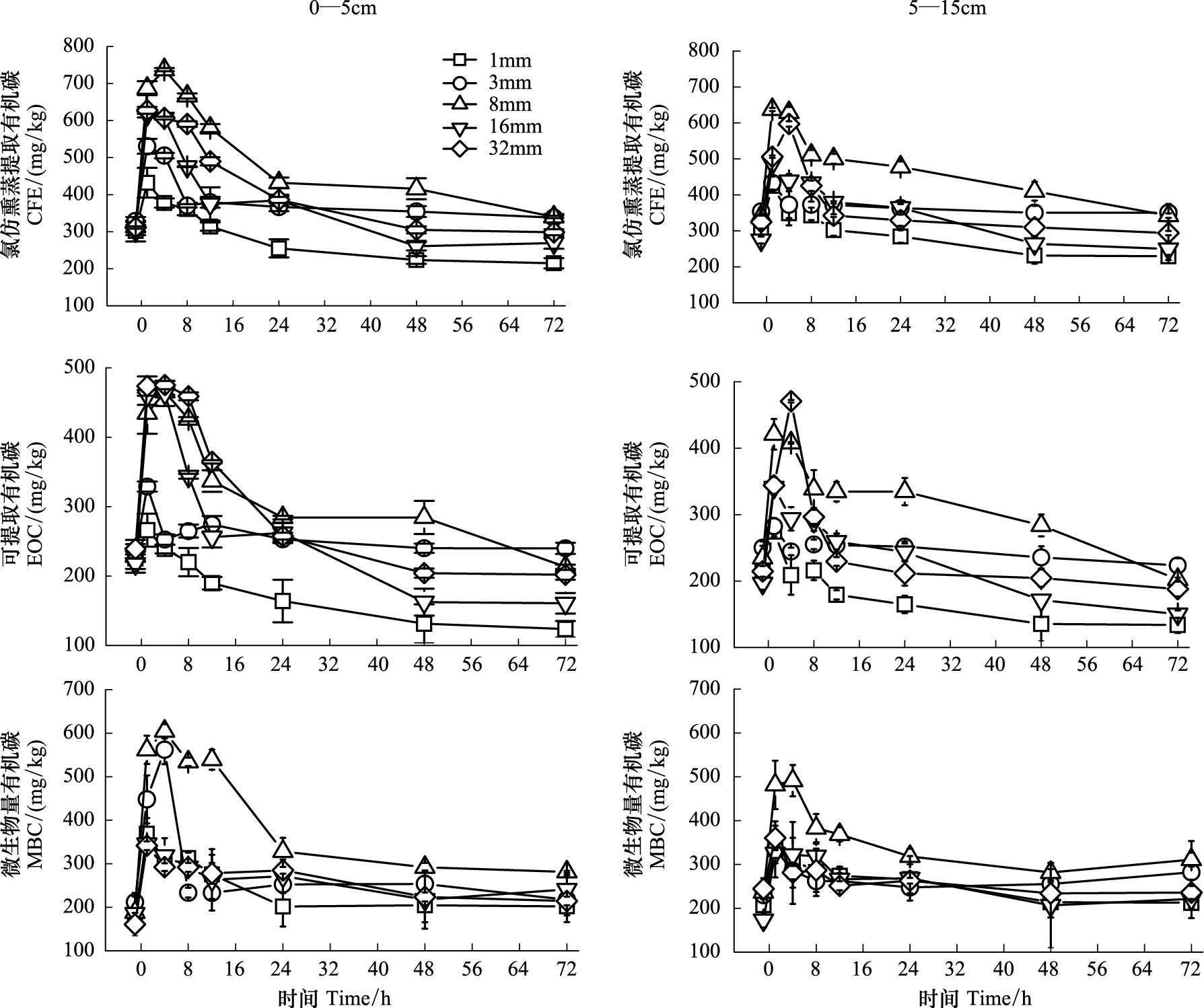
8月份夏闲期模拟降水处理0—5 cm土壤碳组分变化趋势与拔节期相似,不同的是峰值时间推迟到降水后1—4 h(图6)。模拟降水后土壤EOC浓度峰值随降水量的增加而增大,最大值出现在32 mm降水后4 h为475 mg/kg。而土壤MBC和CFE浓度峰值随降水量的变化存在拐点,MBC和CFE浓度峰值在8 mm降水后最大,分别为604 mg/kg和500 mg/kg。当降水量小于8 mm 时土壤MBC和CFE浓度峰值随降水量增大而增大,当降水量大于8 mm 时降水量的增加会减小MBC和CFE的峰值浓度。
|
| 图 6 8月份夏闲期人工降水后土壤CFE、 EOC、MBC变化趋势 Fig.6 Dynamics of soil CFE、 EOC and MBC after precipitation simulation during summer fallow in August |
拔节期和夏闲期模拟降水后5—15 cm土层中土壤碳组分变化趋势与0—5cm相似,只是变化幅度和峰值均小于表层。
3 讨论 3.1 不同降水量对土壤“Birch效应”的影响降水导致土壤呼吸速率脉冲变化在不同生态系统均有报道,其中多数研究结果表明降水事件会激发土壤呼吸快速释放[30],但也有研究表明,降水后水分填充土壤空隙,阻碍气体扩散,抑制土壤呼吸[31]。此外,张红星等[18]在黄土高原对强降水的研究表明降雨对土壤呼吸促进还是抑制取决于雨前、雨中、以及雨后的土壤水分状态。本研究中人工模拟降水后土壤呼吸速率呈现明显的单峰型变化(图2),土壤呼吸的峰值较降水前提高了2—4倍,这与金冠一等[9]在太岳山油松人工林模拟降水后的观测和Shigeru Mariko等[32]在蒙古草原的降水模拟研究结果一致,但低于Casals等[16]在地中海地区的观测结果,作者在其研究中发现降水后土壤呼吸提高了约10倍。不同区域生态系统、土壤性质、植被类型、降水格局和观测技术的差异可能是不同地区研究结果存在差异的原因。
降水量的影响则主要表现在以下几个方面:
(1)土壤呼吸速率峰值随降水量增加而呈幂函数式提高,32 mm降水较其它降水量显著推迟了呼吸峰值的出现时间。推后的原因可能是与小降水量相比,32 mm降水后土壤含水量过高(38%—41.9%),阻碍气体扩散,短期内抑制了土壤微生物活性[31],不利于CO2在土壤中的产生和扩散。禹朴家等[33]在古尔班通古特沙漠南缘的研究中也发现增雨后沙丘土壤呼吸曲线最大值推后了2—8 h。
(2)降水导致的累计CO2释放量与降水量呈显著线性增长关系,5、8月试验期间32 mm处理CO2累积释放量较1 mm处理分别提高了14.6%和45.5%。累计CO2释放量随降水量增加可能是因为在干旱条件下,土壤水分是土壤呼吸的主要限制因子,降水量越大对土壤水分的改善越大且土壤处于相对湿润的时间越久(图1),土壤呼吸对降水激发效应的响应时间越长(图2)[34]。吴林等[35]在古尔班通古特沙漠发现降水后累积碳通量与降水强度呈非线性增长关系,而Andong和Petra[30]的室内实验则表明在干土复湿后累积土壤呼吸量减少了。不同区域降水前土壤水分含量、降雨模式差异和土壤基质的差异,可能是导致不同的地区对于累计CO2释放量的研究得出不同结论的原因。
上述不同降水量的降水对土壤呼吸的激发效应在小麦拔节期均要弱于夏闲期,表现为拔节期的土壤呼吸脉冲释放强度和CO2累计释放量均小于夏闲期(图2),这可能有两方面原因:其一,5月为冬小麦生长关键期,土壤根际微生物代谢活动和根呼吸增强,可能改变了土壤呼吸速率和模式,抑制Birch效应[36];其二,作物的存在减弱了降水对土壤表面的物理冲击作用,降低对土壤团粒的破坏作用,减少底物供应[30]。而夏季休闲期则刚好相反,裸露干燥的地表一旦发生降水,土壤团粒破坏后,其内部包裹的有机碳外露,刺激土壤呼吸加速[16]。
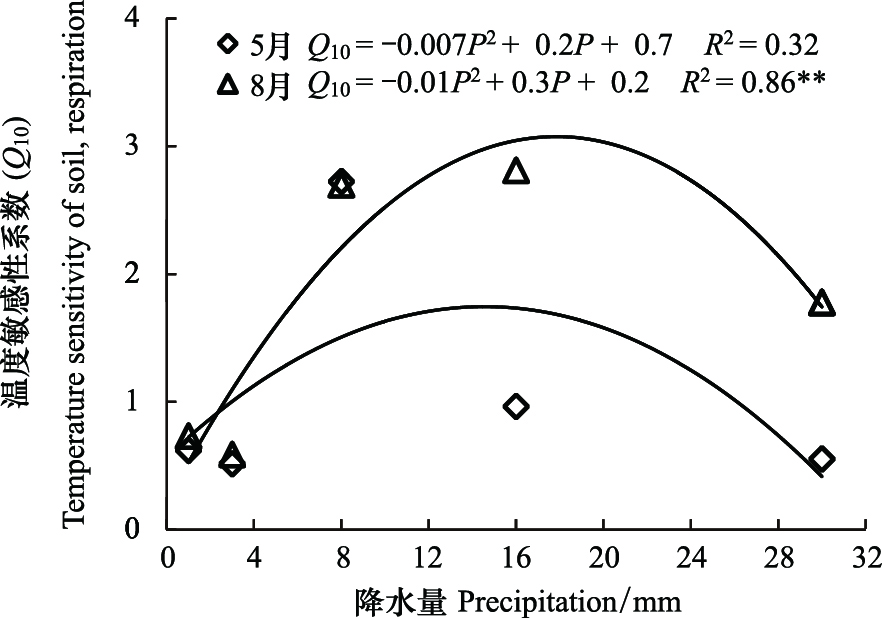
3.2 模拟降水条件下的土壤呼吸水温调控机理国内外学者一般用温度敏感性系数Q10值来表示土壤呼吸对温度的响应关系,降水一般通过改变土壤水分和温度来调节土壤呼吸敏感性。降水后土壤水分增加,促进微生物对底物的利用,提高土壤呼吸温度敏感性[37],土壤温度对土壤呼吸的影响在不同地区和不同生态系统均有报道,多数报道表明土壤温度对土壤呼吸有积极的影响[8, 9]。本研究由公式(2)和(3)计算得拔节期和夏闲期土壤呼吸的Q10(图7),采用二次曲线拟合降水量和土壤呼吸温度敏感性系数Q10之间的关系(图7),经计算5、8月份二次曲线的拐点分别为14.2 mm和15 mm。说明随降水量增加土壤呼吸敏感性会提高,然而一旦超过拐点,降水量继续增加使土壤含水量过高,降低土壤温度抑制了土壤呼吸,减小土壤呼吸Q10值(图7)。高翔等[38]在旱作农田实验也表明在土壤含水量过高的情况下,土壤呼吸对温度的敏感性会降低。
|
| 图 7 降水量(P)和土壤呼吸温度敏感性系数(Q10)的关系 Fig.7 The relationship between precipitation (P) and Q10 of soil respiration |
此外,小降水量(1 mm、3 mm)处理土壤呼吸Q10值小于1。Xu等[39]和Wei等[40]在干旱区的研究也发现了类似的结果。可能源于两个原因:1)试验是在干旱地区进行,土壤处于干旱或是水分亏缺的条件下,水分是生态系统碳平衡瞬时响应的首要因子[40]。在降水量较小时,土壤温度对土壤呼吸的影响没有土壤水分显著。2)土壤温度和土壤水分的变化趋势相反(图1),高温总是伴随着较低的土壤体积含水量。
用双变量非线性模型拟合了土壤呼吸和水热因子之间的关系(表2),5月1—32 mm降水处理和8月3—32 mm降水处理0—5 cm土层土壤水热因子对土壤呼吸的影响程度均达到显著水平(P<0.05)。5月和8月1—32 mm降水处理土壤水分和温度对土壤呼吸变化的解释分别达60%—69%和65%—77%。该双因子模型对实验结果的拟合结果优于单因子模型的拟合结果(结果未列出)。表明在模拟降水后干土复湿的过程中,土壤呼吸速率变化受土壤水分和温度共同影响。
| 时间Time | 降水量/mmRainfall | R p=a+bT+cW | 样本数Sample numbers | |||||||
| a | b | c | P T | P W | P | R 2 | F | |||
| 5月 May | 1 | -0.42 | 0.04 | 0.04 | 0.247 | 0.000 | 0.000 | 0.61 | 18.82 | 27 |
| 3 | -0.88 | 0.05 | 0.07 | 0.254 | 0.000 | 0.000 | 0.65 | 21.86 | 27 | |
| 8 | -1.46 | 0.12 | 0.02 | 0.004 | 0.022 | 0.005 | 0.69 | 26.80 | 27 | |
| 16 | 0.72 | -0.04 | 0.03 | 0.069 | 0.000 | 0.000 | 0.68 | 25.65 | 27 | |
| 32 | 1.35 | -0.07 | 0.02 | 0.198 | 0.000 | 0.000 | 0.67 | 24.08 | 27 | |
| 8月 August | 1 | 0.83 | -0.02 | 0.05 | 0.397 | 0.003 | 0.032 | 0.69 | 1.18 | 27 |
| 3 | -1.79 | 0.06 | 0.06 | 0.015 | 0.000 | 0.002 | 0.71 | 8.43 | 27 | |
| 8 | -3.43 | 0.15 | 0.03 | 0.000 | 0.000 | 0.000 | 0.74 | 38.19 | 27 | |
| 16 | -4.38 | 0.22 | -0.02 | 0.000 | 0.024 | 0.000 | 0.77 | 45.39 | 27 | |
| 32 | -0.35 | 0.02 | 0.03 | 0.615 | 0.000 | 0.000 | 0.65 | 25.80 | 27 | |
本试验是在土壤干旱或是水分亏缺的条件下进行,1—16 mm降水后土壤体积含水量均低于30%,主要表现为促进土壤呼吸,而32 mm降水后8 h内土壤体积含水量高于30%以上,推迟了土壤呼吸峰值。这与高翔[38]和张红星等[18]的研究结果类似(表2),即存在一个阈值决定土壤水分是促进或抑制土壤呼吸。土壤含水量低于阈值时,土壤水分改善促进微生物活动[38],增强土壤呼吸,而土壤含水量超过阈值继续升高则表现为堵塞土壤空隙和阻碍气体扩散,抑制微生物和根系活动,抑制土壤呼吸。
3.3 “Birch”效应的土壤学响应机制为了解释在不同时期不同降水量条件下土壤“Birch效应”的主导机制,对数据做了Pearson简单相关分析和逐步线性回归分析(表3),相关分析结果表明,小麦拔节期模拟降水后土壤呼吸与CFE的相关性仅在3 mm处理下达到显著水平,SR与MBC的相关性在1—32 mm处理下均达到极显著水平(P < 0.01),而土壤呼吸与EOC之间不相关。在夏闲期模拟降水后,1—32 mm处理土壤呼吸与CFE显著相关性,土壤呼吸与EOC相关性随降水量的增加而增强,而与MBC相关性随降水量的增加而减弱。从CFE、EOC和MBC中挑选出和土壤呼吸相关性最大的变量,发现五月份拔节期1—32 mm模拟降水后土壤MBC对土壤呼吸影响最显著(P < 0.01),表明该时期“Birch”效应产生的机制主要以微生物胁迫占主导。原因可能是在降水前土壤处于干旱或缺水的状态,微生物多处于休眠的状态,降水后土壤水分得以改善,微生物迅速利用底物进行新陈代谢,通过释放渗透调节物质来适应迅速增加的土壤水势,释放的大量含碳化合物随后被幸存微生物快速分解,从而释放大量的CO2[15, 41]。对土壤碳组分的观测也表明在模拟降水后的约1—1.5 h土壤MBC达到最大值(图5,图6)。这与Fierer[41]等、Mikha[42]等研究结果相同。Xu等[7]的野外试验研究也认为微生物对降水的响应大约需要1个小时,微生物量碳的变化规律表明干旱区降水后存在微生物胁迫机制。然而,Books[3]和Xiang等[14]均提出土壤“Birch效应”主要以“底物供给机制”占主导,他们的试验降水处理模式采为多次干湿交替过程,而连续干湿交替可能会抑制土壤微生物活性或使土壤微生物产生适应性[14],这可能与本文研究结果显著不同的原因。
| 试验时间/月份Expt. time/month | 降水量mmPrecipitation amount | 逐步回归分析方程Stepwise regression equations | R | P | 样本数Sample numbers |
| 5 | 1 | SR=0.004(0.185)+0.001MBC ** | 0.589 | 0.005 | 27 |
| 3 | SR=0.196(0.196)+0.001MBC ** | 0.606 | 0.004 | 27 | |
| 8 | SR=0.146(0.203)+0.001MBC ** | 0.467 | 0.002 | 27 | |
| 16 | SR=0.217(0.159)+0.001MBC ** | 0.529 | 0.008 | 27 | |
| 32 | SR=0.227(0.195)+0.001MBC ** | 0.435 | 0.003 | 27 | |
| 8 | 1 | SR=0.084(0.162)+0.002MBC ** | 0.576 | 0.003 | 27 |
| 3 | SR=0.264(0.122)+0.001MBC ** | 0.562 | 0.004 | 27 | |
| 8 | SR=0.170(0.134)+0.002CFE *** | 0.805 | 0.000 | 27 | |
| 16 | SR=0.328(0.146)+0.002EOC ** | 0.596 | 0.002 | 27 | |
| 32 | SR=0.142(0.124)+0.002EOC *** | 0.790 | 0.000 | 27 | |
| 公式括弧内表示标准误差, r表示相关系数,P表示参数方程拟合的显著性(** P<0.05,*** P<0.05) | |||||
在夏闲期模拟试验中,1 mm和3 mm处理下MBC对土壤呼吸影响最显著(P < 0.01),而降水量增加到8 mm时,CFE对土壤呼吸影响最显著(P < 0.001),当降水量增加到16 mm以上时,土壤呼吸主要与EOC相关,说明在夏闲期,当单次模拟降水量小于8 mm时,“Birch”效应产生的机制以微生物胁迫占主导,降水量增加到8 mm时,底物供给和微生物胁迫两种机制共同作用于“Birch”效应,当降水量大于等于16 mm时,“Birch”效应产生的机制转变为以“底物供给机制”占主导。这种机制转变的原因可能是夏闲期无作物遮挡,降水冲击对土壤团聚体的破坏随着降水量的增加而增大。对土壤碳组分的观测也表明土壤中的EOC是随着降水量的增加而增加,这与Xiang等[14]和Brookes[3]等在草地土壤模拟降水试验的研究结果相同。在作物拔节期响应机制没有出现转变可能是由于降水量没有达到转换要求或由于作物对水势的阻挡作用从而减弱了激发效应。
4 结论黄土高原旱作农田进行人工模拟单次降水量试验表明,降水事件后土壤CO2在降水后短期内出现脉冲释放,表现出显著的“Birch效应”。降水量与土壤呼吸速率峰值之间存在的幂函数关系,而降水后累计CO2释放量随降水量的增加而呈线性增加。增加降水量可以增强土壤呼吸速率但会推迟土壤呼吸峰N值出现时间,同时提高土壤呼吸的温度敏感性,但当超过降水量临界点后降水量的增加反而会降低Q10值。对土壤碳组分的测定表明,在冬小麦拔节期模拟降水引发的“Birch效应”主要以“微生物胁迫”占主导;在夏闲期,解释“Birch效应”的机制随着降水量的增大,会出现从“微生物胁迫机制”向“底物供给机制”转变。与夏闲期相比,作物生长使冬小麦生育期间土壤“Birch效应”弱化,并改变其响应机制。
| [1] | Liu S H, Fang J Y. Effect factors of soil respiration and the temperature's effects on soil respiration in the global scale. Acta Ecologica Sinica, 1997, 17(5):469-476. |
| [2] | Borken W,Matzner E. Reappraisal of drying and wetting effects on C and N mineralization and fluxes in soils. Global Change Biology, 2009, 15(4):808-824. |
| [3] | Wu J, Brookes P C. The proportional mineralisation of microbial biomass and organic matter caused by air-drying and rewetting of a grassland soil. Soil Biology and Biochemistry, 2005, 37(3):507-515. |
| [4] | Birch H F. Mineralisation of plant nitrogen following alternate wet and dry conditions. Plant and Soil, 1964, 20(1):43-49. |
| [5] | Alberti G Inglima I, Bertolini T, Vaccari F P, Gioli B, Miglietta B, Cotrufo M F, Peressotti A. Precipitation pulses enhance respiration of Mediterranean ecosystems:the balance between organic and inorganic components of increased soil CO2 efflux. Global Change Biology, 2009, 15(5):1289-1301. |
| [6] | Jarvis P G, Rey A, Petsikos C,Wingate L,Rayment M,Pereira J,Banza J,David J,Miglietta F,Borghetti M,Manca G,Valentini R. Drying and wetting of Mediterranean soils stimulates decomposition and carbon dioxide emission:the "Birch Effect". Tree Physiology, 2007, 27(7):929-940. |
| [7] | Xu L K, Baldocchi D D, Tang J W. How soil moisture, rain pulses, and growth alter the response of ecosystem respiration to temperature. Global Biogeochemical Cycles, 2004, 18(4):GB4002,doi:10.1029/2004GB002281. |
| [8] | 张丁辰, 蔡典雄, 代快. 旱作农田不同耕作土壤呼吸及其对水热因子的响应. 生态学报, 2013, 33(6):1916-1925. |
| [9] | 金冠一, 赵秀海, 康峰峰, 汪金松. 太岳山油松人工林土壤呼吸对强降雨的响应. 生态学报, 2013, 33(6):1832-1841. |
| [10] | 张丽华, 陈亚宁, 李卫红, 赵锐锋, 华永辉. 准噶尔盆地两种荒漠群落土壤呼吸速率对人工降水的响应. 生态学报, 2009, 29(6):2819-2826. |
| [11] | Birch H F. The effect of soil drying on humus decomposition and nitrogen availability. Plant and Soil, 1958, 10(1):9-31. |
| [12] | Inglima I, Alberti G, Bertolini T, Vaccari F P, Gioli B, Miglietta F, Cotrufo M F, Peressotti A. Precipitation pulses enhance respiration of Mediterranean ecosystems:the balance between organic and inorganic components of in-creased soil CO2 efflux. Global Change Biology,2009,15, 1289-1301. |
| [13] | Kieft T L, Edith S, Mary K F. Microbial biomass response to a rapid increase in water potential when dry soil is wetted. Soil Biology and Biochemistry, 1987, 19(2):119-126. |
| [14] | Xiang S R, Doyle A, HoldenP A, Schimel J P. Drying and rewetting effects on C and N mineralization and microbial activity in surface and subsurface California grassland soils. Soil Biology and Biochemistry, 2008, 40(9):2281-2289. |
| [15] | Fierer N, Schimel J P. A proposed mechanism for the pulse in carbon dioxide production commonly observed following the rapid rewetting of a dry soil. Soil Science Society of Americal Journal, 2003, 67(3):798-805. |
| [16] | Casals P, Gimeno C, Carrara A, Lopez-Sangil L, Sanz M. Soil CO2 efflux and extractable organic carbon fractions under simulated precipitation events in a Mediterranean Dehesa. Soil Biology and Biochemistry, 2009, 41(9):1915-1922. |
| [17] | 任国玉, 丁一汇, 石广玉, 宫鹏, 郑循华, 翟盘茂, 张德二, 赵宗慈, 王绍武, 王会军, 罗勇, 陈德亮, 高学杰, 戴晓苏. 气候变化国家评估报告(I):中国气候变化的历史和未来趋势. 气候变化研究进展, 2006, 2(1):3-8. |
| [18] | 张红星, 王效科, 冯宗炜,宋文质,刘文兆,李双江,庞军柱,欧阳志云. 黄土高原小麦田土壤呼吸对强降雨的响应. 生态学报, 2008, 28(12):6189-6196. |
| [19] | 李志, 郑粉莉, 刘文兆. 1961-2007年黄土高原极端降水事件的时空变化分析. 自然资源学报, 2010, 25(2):291-299. |
| [20] | 刘宪锋, 任志远, 张翀, 林志慧. 1959-2008年黄土高原地区年内降水集中度和集中期时空变化特征. 地理科学进展, 2012, 31(9):1157-1163. |
| [21] | Liebig M A, Tanaka D L, Gross J R. Fallow effects on soil carbon and greenhouse gas flux in Central North Dakota. Soil Science Society of America Journal, 2010, 74(2):358-365. |
| [22] | Davidson E A, Savage K, Verchot L V, Navarro R. Minimizing artifacts and biases in chamber-based measurements of soil respiration. Agricultural and Forest Meteorology, 2002, 113(1/4):21-37. |
| [23] | Mosier A R, Hutchinson G L. Improved soil cover method for field measurement of nitrous oxide fluxes. Soil Science Society of America Journal, 1981, 45(2):311-316. |
| [24] | Vance E D, Brookes P C, Jenkinson D S. An extraction method for measuring soil microbial biomass C. Soil Biology and Biochemistry, 1987, 19(6):703-707. |
| [25] | Jenkinson D S. Determination of microbial biomass carbon and nitrogen in soil//Wilson J R, ed, Advances in Nitrogen Cycling in Agricultural Ecosystems. Wallingford:CAB International, 1988:368-386. |
| [26] | Deng Q, Hui D F, Zhang D Q, Zhou G Y, Liu J X, Liu S Z, Chu G W, Li J. Effects of precipitation increase on soil respiration:a three-year field experiment in subtropical forests in China. PloS One, 2012, 7(7):e41493. |
| [27] | Davidson E A, Janssens I A, Luo Y Q. On the variability of respiration in terrestrial ecosystems:moving beyond Q10. Global Change Biology, 2006, 12(2):154-164. |
| [28] | 陈全胜, 李凌浩, 韩兴国, 阎志丹, 王艳芬, 张淼, 熊小刚, 陈世苹, 张丽霞, 高英志, 唐芳, 杨晶, 董云社. 典型温带草原群落土壤呼吸温度敏感性与土壤水分的关系. 生态学报, 2004, 24(4):831-836. |
| [29] | Luo Y Q, Wan S Q, Hui D F, Wallace L L. Acclimatization of soil respiration to warming in a tall grass prairie. Nature, 2001, 413(6856):622-625. |
| [30] | Shi A D, Marschner P. Drying and rewetting frequency influences cumulative respiration and its distribution over time in two soils with contrasting management. Soil Biology & Biochemistry, 2014, 72:172-179. |
| [31] | Bouma T J, Bryla D R. On the assessment of root and soil respiration for soils of different textures:interactions with soil moisture contents and soil CO2 concentrations. Plant and Soil, 2000, 227(1/2):215-221. |
| [32] | Mariko S, Urano T, Asanuma J. Effects of irrigation on CO2 and CH4 fluxes from Mongolian steppe soil. Journal of Hydrology, 2007, 333(1):118-123. |
| [33] | 禹朴家, 徐海量, 王炜,张鹏,赵新风,龚君君. 沙丘不同部位土壤呼吸对人工降水的响应. 中国沙漠, 2012, 33(2):437-441. |
| [34] | Asensio D, Peñuelas J, Llusià J, Ogaya R, Filella I. Interannual and interseasonal soil CO2 efflux and VOC exchange rates in a Mediterranean holm oak forest in response to experimental drought. Soil Biology and Biochemistry, 2007, 39(10):2471-2484. |
| [35] | 吴林, 苏延桂, 张元明. 模拟降水对古尔班通古特沙漠生物结皮表观土壤碳通量的影响. 生态学报, 2012, 32(13):4103-4113. |
| [36] | Dilustro J J, Collins B, Duncan L, Crawford C. Moisture and soil texture effects on soil CO2 efflux components in southeastern mixed pine forests. Forest Ecology and Management, 2005, 204(1):87-97. |
| [37] | Davidson E A, Janssens I A. Temperature sensitivity of soil carbon decomposition and feedbacks to climate change. Nature, 2006, 440(7081):165-173. |
| [38] | 高翔, 郝卫平, 顾峰雪, 郭瑞, 夏旭, 梅旭荣, 李洁. 降雨对旱作春玉米农田土壤呼吸动态的影响. 生态学报, 2012, 32(24):7883-7893. |
| [39] | Xu W H, Wan S Q. Water-and plant-mediated responses of soil respiration to topography, fire, and nitrogen fertilization in a semiarid grassland in northern China. Soil Biology and Biochemistry, 2008, 40(3):679-687. |
| [40] | Shi W Y, Tateno R, Zhang J G, Wang Y D, Yamanaka N, Du S. Response of soil respiration to precipitation during the dry season in two typical forest stands in the forest-grassland transition zone of the Loess Plateau. Agricultural and Forest Meteorology, 2011, 151(7):854-863. |
| [41] | Schimel J, Balser T C, Wallenstein M. Microbial stress-response physiology and its implications for ecosystem function. Ecology, 2007, 88(6):1386-1394. |
| [42] | Mikha M M, Rice C W, Milliken G A. Carbon and nitrogen mineralization as affected by drying and wetting cycles. Soil Biology and Biochemistry, 2005, 37(2):339-347. |
 2016, Vol. 36
2016, Vol. 36






