文章信息
- 姜沛沛, 曹扬, 陈云明, 王芳
- JIANG Peipei, CAO Yang, CHEN Yunming, WANG Fang.
- 不同林龄油松(Pinus tabulaeformis)人工林植物、凋落物与土壤C、N、P化学计量特征
- Variation of C, N, and P stoichiometry in plant tissue, litter, and soil during stand development in Pinus tabulaeformis plantation
- 生态学报[J]. 2016, 36(19): 6188-6197
- Acta Ecologica Sinica[J]. 2016, 36(19): 6188-6197
- http://dx.doi.org/10.5846/stxb201507211532
-
文章历史
- 收稿日期: 2015-07-21
- 修订日期: 2016-04-21
2. 西北农林科技大学黄土高原土壤侵蚀与旱地农业国家重点实验室, 杨凌 712100;
3. 中国科学院水利部水土保持研究所, 杨凌 712100;
4. 西北农林科技大学水土保持研究所, 杨凌 712100
2. State Key Laboratory of Soil Erosion and Dryland Farming on Loess Plateau, Institute of Soil and Water Conservation, Northwest A & F University, Yangling 712100, China;
3. Institute of Soil and Water Conservation, Chinese Academy of Sciences and Ministry of Water Resources, Yangling 712100, China;
4. Institute of Soil and Water Conservation, Northwest A & F University, Yangling 712100, China
生物体最基本的组成是元素,特别是碳(C)、氮(N)、磷(P),生物的生长过程实质上是对这些元素的积聚与相对比例的调节过程[1-2]。生态化学计量学是研究多重元素化学平衡的一门科学,它强调的是活的有机体组成元素(特别是C、N、P)之间的联系[3]。
目前,国外对植物生态化学计量学特征已有大量研究,国内相关研究虽然起步较晚但发展迅速,对不同森林类型、不同区域和不同演替阶段的植物叶片的化学计量特征进行了大量研究[4-10],对植物枝、干、根等器官化学计量特征的报道则较少;进行土壤及凋落物养分化学计量特征的研究也较多[11-12],但将叶片、凋落物与土壤三者联系起来探讨的研究却相对较少[13],研究某一树种随林龄植物不同器官(叶、枝、干、根)、凋落物与土壤C、N、P化学计量特征变化的研究则更少。植物通过光合作用固定C,并以凋落物的形式将C和养分逐渐补给给土壤[14],凋落物分解过程中养分的返还量、土壤养分供应量、植物养分需求量以及植物对其自身养分需求的自我调节,使得植物—凋落物—土壤系统养分含量具有明显的时空变化[15]。随着林龄的增加,森林生态系统的组成结构、内部环境以及土壤性质也会随之发生改变,进而影响养分分配格局,而将叶片、凋落物与土壤三者联系起来探讨随着林龄的增加主要元素分配及化学计量特征的变化对于进一步从生态化学计量角度上掌握碳循环的调控机制具有重要意义,同时也可以为促进生态化学计量学理论发展提供新的科学依据,为减缓温室效应提供新的研究思路。
油松(Pinus tabuliformis)具有耐干旱、耐贫瘠,根系发达,适应性强等特点,是黄土高原主要的乡土树种之一,也是山地沟壑营造防护林和用材林的优良树种[16]。本研究以陕西省北部延安市境内子午岭林区不同林龄油松人工林为研究对象,对油松不同器官(叶、枝、干、根)、凋落物及土壤的 C、N、P 含量进行测定和分析,探讨它们随林龄的变化,比较它们之间C、N、P含量及其比值的异同以及相互之间可能存在的关系,以期为油松人工林的生产、改善和林木生长环境的调节作出指导,为提高生态系统养分利用效率和林地生产力提供依据,并为油松人工林的土壤肥力管理提供参考。
1 材料与方法 1.1 研究区概况研究区位于延安市境内子午岭林区(108°53′—109°38′E,35°27′—36°50′N),属温带半湿润区,地处抬升山地,海拔 1010—1275 m,年均降水量为 587.6 mm,年平均气温为7.4 ℃,土壤为原生(山坡)或次生(沟谷)黄土[17-18]。研究区内主要树种有辽东栎(Quercus liaotungensis)、油松和刺槐(Robinia pseudoacacia),其中辽东栎多属天然次生林,刺槐和油松则以人工林为主,且油松人工林林分树种单一,为绝对优势树种[18]。林下灌木主要有黄刺玫(Rosa xanthina)、陕西荚蒾(Viburnum schensianum)、忍冬(Lonicera Japonica)、绣线菊(Spiraea pubescens)、兴安胡枝子(Lespedeza davurica)、毛樱桃(Prunusto merttosa)、等;草本植物主要有披针苔草(Carex lanceolata)、铁杆蒿(Artemisia sacrorum)、北京隐子草(Cleistogenes hancei)、艾蒿(Artemisia argyi)等。
1.2 研究方法 1.2.1 样地设置依据国家林业局 2004 年对黄土丘陵区油松人工林林龄划分标准:幼龄林 (≤20a)、中龄林(21—30a)、近熟林 (31—40a)、成熟林 (41—60a),2012年7月以空间代替时间的方法在陕西省延安市子午岭林区范围内选取立地条件相近的不同生长阶段(9、23、33、47a)的油松人工林作为研究样点。每个研究样点随机设置 3 个50 m×20 m的样方(以样方情况代表样地基本信息),样地基本信息见表 1。
| 林龄 Age/a | 样地 Plot No. | 海拔 Altitude/m | 坡向 Aspect | 坡度 Slope/(°) | 坡位 Slope position | 平均胸径 DBH/cm | 平均树高 Height/m | 林分密度 Density/ (株/hm2) | 郁闭度 Crown density | 林下优势种 Dominant species |
| 9 | 1 | 1204 | N | 7 | 中坡 | 2.2 | 2.3 | 3990 | 0.2 | 黄刺玫-铁杆蒿 |
| 2 | 1198 | N | 6 | 中坡 | 2.2 | 2.2 | 4260 | 0.2 | Rosa xanthina-Artemisia | |
| 3 | 1183 | NE50 | 9 | 中坡 | 2.2 | 2.3 | 3870 | 0.2 | sacrorum | |
| 23 | 1 | 1275 | NW30 | 16 | 上坡 | 9.7 | 8.1 | 3450 | 0.8 | 黄刺玫-披针苔草 |
| 2 | 1215 | N | 32 | 上坡 | 8.5 | 6.6 | 2520 | 0.9 | Rosa xanthina- | |
| 3 | 1247 | NE40 | 8 | 上坡 | 7.9 | 6.4 | 3660 | 0.8 | Carex lanceolata | |
| 33 | 1 | 1101 | NW73 | 26 | 下坡 | 11.4 | 8.7 | 2580 | 0.6 | 黄刺玫-披针苔草 |
| 2 | 1035 | NW80 | 34 | 中坡 | 10.7 | 9 | 2070 | 0.7 | Rosa xanthina- | |
| 3 | 1271 | SW75 | 32 | 上坡 | 12.4 | 14.6 | 2150 | 0.7 | Carex lanceolata | |
| 47 | 1 | 1069 | NW55 | 17 | 上坡 | 13.9 | 13.9 | 1370 | 0.7 | 黄刺玫-披针苔草 |
| 2 | 972 | NE75 | 25 | 中坡 | 13.9 | 13.9 | 1770 | 0.8 | Rosa xanthina- | |
| 3 | 1051 | NW40 | 34 | 中坡 | 14.2 | 14.2 | 1380 | 0.8 | Carex lanceolata |
对每个样地内的乔木进行每木检尺,记录胸径和树高(9年生油松林起测径阶为2cm,23、33、47年生油松林起测径阶为5cm),并统计株数。按大、中、小径级选择标准木3株,分东、西、南、北四个方位采摘其冠下部(距地面2—3m)的成熟叶片,用高枝剪在每株标准木的树冠南向的上、中、下3个冠层分别随机选取树枝3条,用砍刀砍取适量树干,并挖取适量树根,从3株标准木获取的叶、枝、干、根,同器官混合成1份样品(每份约重300g)。按对角线在相应的油松林林下选择 3个1 m×1 m的小样方收集地表凋落物,将样品混匀后放入纸质档案袋中带回实验室。植物样品置于85℃烘干至恒重,粉碎机磨碎后测定C、N、P 含量。同时在每个样地内,采用S 型路线选择5个点,用土钻采集表层0—20 cm土壤,将5个点混匀后带回实验室。土壤样品风干后,剔除草根、石头等杂物,研磨后过0.25 mm的筛后测定 C、N、P含量。
植物、凋落物和土壤全C采用重铬酸钾-外加热法测定;全N、全P采用浓H2SO4 -H2O2消煮法,消煮后的待测液供全N、全P的测定,其中全N采用凯氏定氮仪测定(KDY-9830,KETUO),全P采用高氯酸-硫酸消化-钼锑抗比色法测定(UV-2450 紫外分光光度计)[19]。
1.2.3 数据处理方法采用方差分析(ANOVA) 检验油松同一林龄不同器官以及不同林龄间植物、凋落物和土壤C、N、P含量及其比值差异是否显著。采用Pearson相关分析对油松叶片、凋落物和土壤C、N、P含量及其比值进行相关性分析。以上所有统计分析均在SPSS statistics 19.0中完成。文中C∶N、C∶P、N∶P比值均采用质量比,通过原子比除以1.17、2.58、2.21可分别换算得到C∶N、C∶P、N∶P比值的质量比。图表中均采用平均值±标准差。
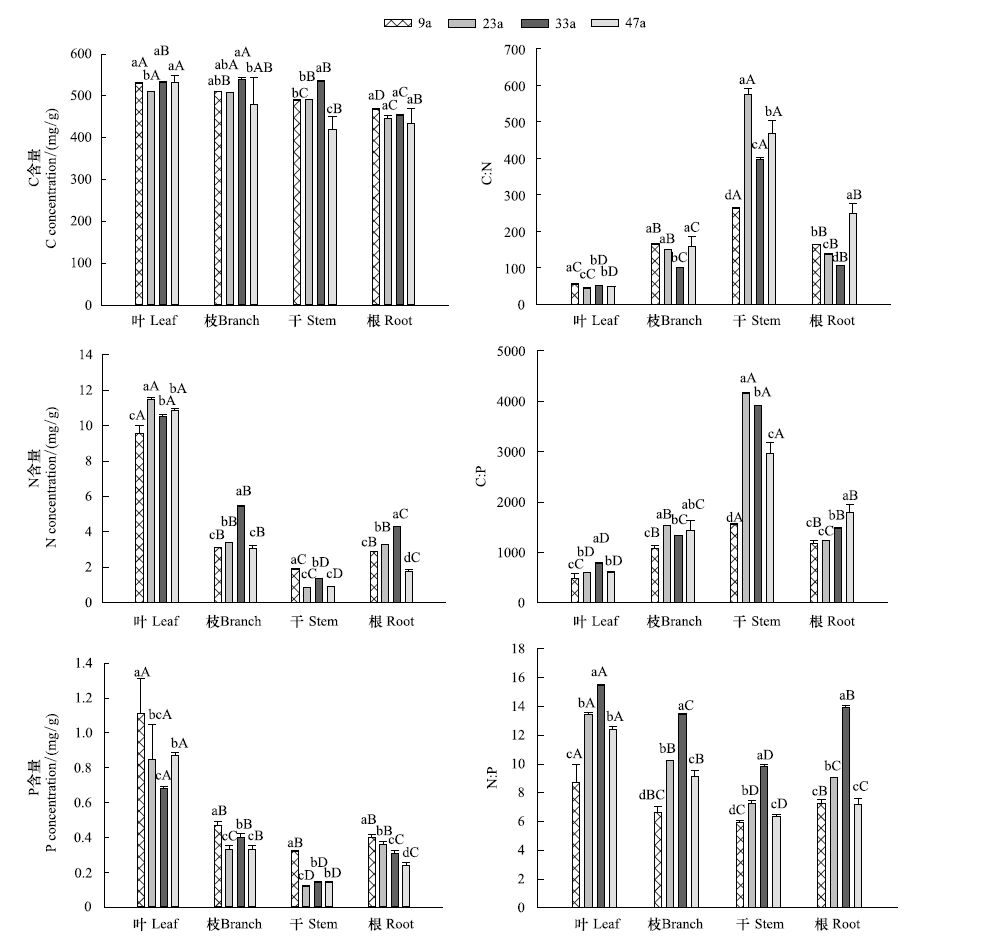
2 结果 2.1 不同林龄油松人工林植物C、N、P含量及其化学计量比除根中C含量在林龄间差异不显著外,其它器官中C、N、P含量及其比值在各林龄间均差异显著(P<0.05)。叶中C含量随林龄而降低在23a达到最低后增加,且变化显著;枝中C含量随林龄略有增加,但差异不显著,在33a达到最大后显著降低;干中C含量随林龄先显著增加,在33a达到最大后显著降低(图 1)。叶、枝和根中N含量随林龄先增加后降低,且变化显著,其中叶在23a、枝和根在33a达到最大值;干中N含量无明显变化规律(图 1)。叶和干中P含量随林龄先降低后增加,且变化显著,其中叶在33a、干在23a达到最小值;枝中P含量无明显变化规律;根中P含量随林龄显著降低(图 1)。叶、枝和根中C∶N随林龄先降低后增加,且变化显著,其中叶在23a、枝和根在33a达到最小值;干中C∶N随林龄无明显变化规律(图 1)。叶和干中C∶P随林龄先增加后降低,且变化显著,其中叶在33a、干在23a达到最大值;枝中C∶P随林龄无明显变化规律;根中C∶P随林龄显著增加(图 1)。叶、枝、干、根中的N∶P随林龄的变化趋势一致,均随林龄先增加,在33a达到最大值后降低,且变化显著(图 1)。9、23、33、47年生油松林C、N、P含量及N∶P比值均在叶中最高;C∶N比值均在干中最高,根中次之; C∶P比值均在干中最高,其它器官大小次序不一(图 1)。
|
| 图 1 不同小写字母表示不同林龄间差异显著,不同大写字母表示同一林龄不同组分间差异显著(P<0.05) Fig. 1 Variation of different organs C,N,P stoichiometric during stand development in Pinus tabulaeformis plantation |
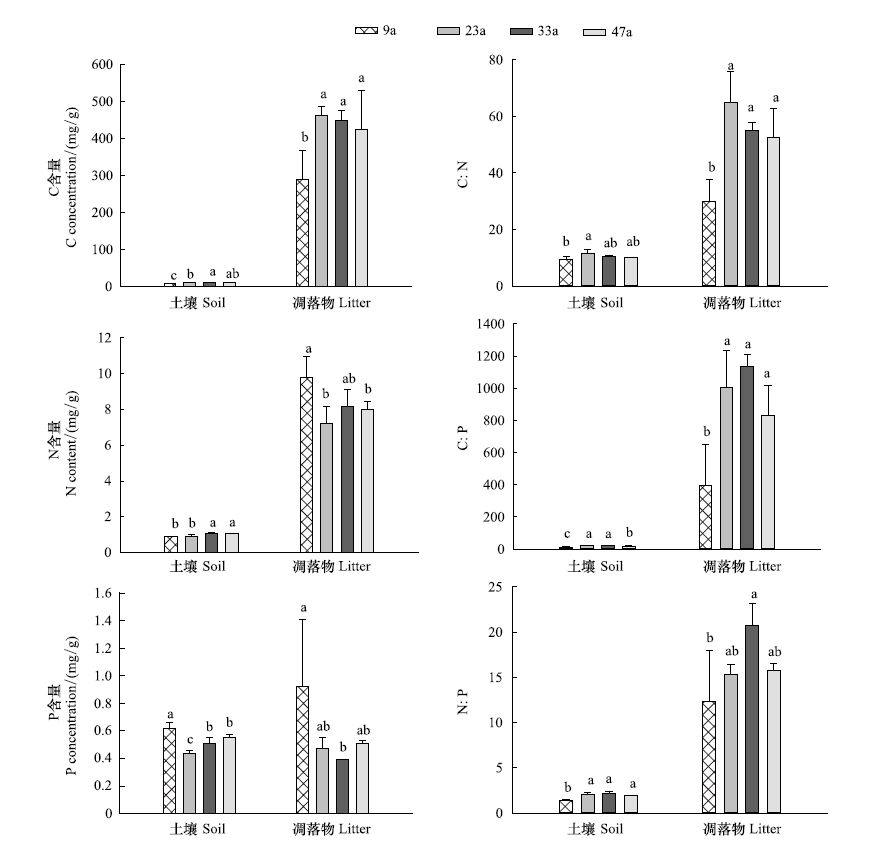
不同林龄土壤和凋落物C、N、P含量及其比值差异显著(P<0.05),且后者均大于前者(图 2)。土壤和凋落物中C和P含量随林龄变化趋势基本一致,其中C含量随林龄均先增加后降低,且变化显著,其中土壤在33a、凋落物在23a达到最大值;P含量随林龄均先降低后增加,且变化显著,其中土壤在23a、凋落物在33a达到最小值。土壤N含量随林龄先显著增加,在33a达到最大值后略有降低但差异不显著;凋落物N含量随林龄先显著降低,在23a达到最小值后基本保持稳定(图 2)。土壤与凋落物中C∶N、C∶P、N∶P随林龄变化趋势大致相同,其中 C∶N随林龄均先显著增加,在23a达到最大后降低但其后差异不显著(图 2);C∶P随林龄先增加后降低,且变化显著,其中土壤在23a,凋落物在33a达到最大值(图 2);N∶P随林龄先显著增加,在33a达到最大值后降低但其后差异不显著(图 2)。
|
| 图 2 不同林龄油松人工林土壤和凋落物C、N、P含量及化学计量比 Fig. 2 Variation of soil and litter C,N,P stoichiometry during stand development in Pinus tabulaeformis plantation |
C、N、P两两之间,在叶片中不存在显著相关性;凋落物中,只有C和P显著负相关,N和P显著正相关;土壤中,只有C和N显著正相关,C和P显著负相关(P<0.05,表 2)。叶片C与凋落物C、N、P均不存在显著相关性;叶片N与凋落物C、N显著正相关和负相关;叶片P与凋落物C显著负相关,与凋落物N、P显著正相关(P<0.05,表 2)。叶片C和N只与土壤P显著正相关和负相关,叶片P只与土壤C显著正相关(P<0.05,表 2)。土壤C与凋落物C显著正相关,与凋落物N、P显著负相关;土壤N与凋落物C、N、P均不存在明确相关性;土壤P与凋落物C显著负相关,与凋落物N、P显著正相关(P<0.05,表 2)。
| 组分 Components | 叶片C Leaf C | 叶片N Leaf N | 叶片P Leaf P | 凋落物C Litter C | 凋落物N Litter N | 凋落物P Litter P | 土壤C Soil C | 土壤N Soil N |
| 叶片N Leaf N | -0.54 | 1 | ||||||
| 叶片P Leaf P | 0.010 | -0.389 | 1 | |||||
| 凋落物C Litter C | -0.181 | 0.635* | -0.670* | 1 | ||||
| 凋落物N Litter N | 0.378 | -0.654* | 0.636* | -0.434 | 1 | |||
| 凋落物P Litter P | 0.100 | -0.415 | 0.853** | -0.740** | 0.630* | 1 | ||
| 土壤C Soil C | -0.067 | 0.572 | 0.921** | 0.730** | -0.679* | -0.823** | 1 | |
| 土壤N Soil N | 0.352 | 0.150 | -0.601 | 0.358 | -0.155 | -0.356 | 0.681* | 1 |
| 土壤P Soil P | 0.581* | -0.813** | 0.574 | -0.655* | 0.708* | 0.658* | -0.612* | -0.055 |
| *P<0.05;* *P<0.01 | ||||||||
C∶N、C∶P、N∶P两两之间,在叶片中只有C∶P与N∶P极显著正相关;凋落物和土壤中,只有C∶N和C∶P之间和C∶P和N∶P之间均极显著正相关(P<0.01,表 3)。叶片C∶N只与凋落物C∶N极显著负相关,叶片C∶P与凋落物C∶P和N∶P均极显著正相关,叶片N∶P与凋落物C∶N、C∶P、N∶P均极显著正相关(P<;0.01,表 3)。叶片C∶N与土壤C∶N、C∶P、N∶P均显著负相关,叶片C∶P和N∶P与土壤C∶P和N∶P显著正相关(P<0.05,表 3)。土壤C∶P和N∶P与凋落物C∶N、C∶P、N∶P之间均显著正相关;土壤C∶N与凋落物C∶N和C∶P均显著正相关(P<0.05,表 3)。
| 组分 Components | 叶片C∶N Leaf C∶N | 叶片C∶P Leaf C∶P | 叶片N∶P Leaf N∶P | 凋落物C∶N Litter C∶N | 凋落物C∶P Litter C∶P | 凋落物N∶P Litter N∶P | 土壤C∶N Soil C∶N | 土壤C∶P Soil C∶P |
| 叶片C∶P Leaf C∶P | -0.183 | 1 | ||||||
| 叶片N∶P Leaf N∶P | -0.541 | 0.925** | 1 | |||||
| 凋落物C∶N Litter C∶N | -0.745** | 0.541 | 0.754** | 1 | ||||
| 凋落物C∶P Litter C∶P | -0.551 | 0.769** | 0.872** | 0.894** | 1 | |||
| 凋落物N∶P Litter N∶P | -0.154 | 0.787** | 0.733** | 0.512 | 0.823** | 1 | ||
| 土壤C∶N Soil C∶N | -0.617* | 0.364 | 0.564 | 0.778* | 0.670* | 0.400 | 1 | |
| 土壤C∶P Soil C∶P | -0.774** | 0.680* | 0.885** | 0.891** | 0.876** | 0.601* | 0.751** | 1 |
| 土壤N∶P Soil N∶P | -0.667* | 0.726** | 0.876** | 0.737** | 0.792** | 0.605* | 0.401 | 0.905** |
| * P<0.05;** P<0.01 | ||||||||
本研究中叶片C含量、C∶N及C∶P比值与黄土高原126个植物样品[8]、中国753种陆生植物叶片[20]、Elser等[21]研究的全球492种陆生植物叶片以及McGroddy等[7]研究的全球森林叶片等结果相比均偏高,而N、P含量及N∶P比值偏低,但与本研究区域相近的黄土高原的常绿植物叶片的C、N、P含量及比值相近,N∶P比值还明显高于McGroddy 等[7]温带针叶的比值(表 4)。这可能是由于与阔叶树种相比,常绿针叶树种含有大量的富碳次生产物(例如,树脂、单宁和蜡),这增加了其C∶N、C∶P比值,且常绿树种往往会分配较多养分用于构建保卫构造,如分配较多氮于非溶性蛋白以增强其细胞壁韧性或增加叶肉细胞密度以抵御环境胁迫和病虫的侵害,故其叶寿命和比叶重较高,但光合和养分利用效率较低[8]。
| 地区Region | 类型Types | C/(mg/g) | N/(mg/g) | P/(mg/g) | C∶N | C∶P | N∶P | 参考文献 References |
| 本研究区 This study area | 油松 Pinus tabuliformis | 526.18±11.99 (12) | 10.61±0.74 (12) | 0.88±0.18 (12) | 49.85±4.31 (12) | 619.16±116.55 (12) | 12.53±2.60 (12) | 本文This study |
| 黄土高原 Loess Plateau | 植物Plant | 438±43 (126) | 24.1±8.5 (126) | 1.6±0.55 (126) | 21.2±10.2 (126) | 312±135 (126) | 15.4±3.0 (126) | [8] |
| 常绿Evergreen | 516±16 (9) | 10.6±1.7 (9) | 0.83±0.24 (9) | 49.6±7.3 (9) | 660±154 (9) | 13.4±2.9 (9) | ||
| 中国China | 植物Plant | - | 20.2±8.4 (554) | 1.46±0.99 (745) | - | - | 16.3±9.32 (547) | [20] |
| 全球Global | 植物Plant | 464±32.1 (492) | 20.6±12.2 (398) | 1.99±1.49 (406) | 22.5±10.6 (398) | 232±145 (406) | 12.7±6.82 (325) | [21] |
| 全球Global | 植物Plant | - | - | - | 43.6±3.5* (55,37.3) | 1334.1±137.6* (59,517.1) | 27.8±1.4* (55,12.6) | [7] |
| 温带针叶 Temperate Coniferous | - | - | - | 59.5±7.0* (19,50.9) | 1231.8±140.3* (19,477.4) | 21.7±1.7* (20,9.8) | ||
| a) 括号中前一个数字为样本数 b) 带*数字为摩尔比,括号中后一个数字为转换后的质量比 | ||||||||
9年生幼龄林生长速度较快,需要大量核糖体合成蛋白质,由于核糖体是植物体中重要的P库,所以本研究中9年生幼龄林叶中P含量最高,而核糖体合成的蛋白质则在23年生依旧保持快速生长的中龄林中达到最大,因此23年生中龄林叶中N含量最高。Zhang等[22]在内蒙古草地生态系统的研究认为,C∶N和C∶P比值随叶年龄的增大而增加,这与本研究中叶、枝、干、根中C∶P比值和干、根中的C∶N比值随着林龄的增大而增加的结果相同,这可能是由于随着树木体型的增大,导致了N、P含量的稀释效应[23]。树木在幼龄和中龄期快速生长、代谢活动旺盛,需要酶来合成大量蛋白质,而到了近熟和成熟林时期富含碳的结构性物质积累,导致C∶N比值上升[24]。植物叶片C∶N、C∶P比值可以表征植物吸收营养元素同化C的能力,在一定程度上可以反映出单位养分供应量所能达到的生产力、植物对营养的利用效率以及植物的生长速度[9, 25]。生长速率假说认为,生物体在快速生长过程中,会分配大量P到rRNA中,以使核糖体能够快速合成大量蛋白质,所以生物个体的生长速率与体内C∶P、N∶P比值负相关[26]。本研究中C∶P、N∶P比值随林龄先增加后降低,这与生长速率假说并不相符,这可能是由于植物具有贮存物质的功能以及 RNA 中的 P 占植物全磷的比例较低,使得高等植物是否符合生长率假说更具不确定性[2]。N、P作为植物生长的主要限制性元素,在植物体内存在功能上的联系,N∶P比值则经常作为判断生态系统受N或受P限制的判断指标。研究表明,植物生长受N和P限制的N∶P阈值为14和16,即当N∶P小于14 时,植物生长主要受 N 限制;当N∶P大于16 时,植物生长主要受P限制;当N∶P位于14和16之间时,受N和P的共同限制[27]。本研究中,除了33年生油松林叶中N∶P比值大于14,其它各个器官各林龄段的N∶P比值均小于14,故可判断该区域受N限制较为严重。叶、枝、干、根中N∶P比值随林龄先增加在33a达到最大值后降低,表明随着林龄的增加油松林生长受N限制的情况有所缓解,这与崔宁洁等[13]在马尾松林的研究结果一致,所以在油松人工林,特别是幼龄林的管理中,可适当增施氮肥以促进幼苗生长。
3.2 不同林龄油松人工林土壤和凋落物C、N、P含量及其化学计量比本研究中土壤P含量(0.42—0.67 mg/g)明显低于全球水平的2.8 mg/g[10],这与杨佳佳等[28]在黄土高原刺槐林的研究结果一致,这可能与地表土壤对磷的吸附作用、黄土高原地区强烈的风化和水土流失作用有关,亦与中国土壤磷含量普遍低于全球平均水平的规律一致。与全球不同生态系统土壤C∶N∶P摩尔比的平均水平59.5∶16∶1(换算成质量比为23.06∶3.12∶1)相比[29],本研究土壤的C∶N∶P比值(19.68∶1.88∶1)偏低(表 5)。研究表明,中国土壤 C∶N比平均值在10∶1—12∶1之间[30],本研究土壤的 C∶N比平均值为10.38在此范围之内。与叶片相比,凋落物C、N、P含量明显下降,而C∶N、C∶P和N∶P比值则有所上升(表 4,表 5),这反映出了植物对营养元素的再吸收特征,即营养元素从衰老叶片中转移并被运输到植物其它组织的过程[25],这种将营养元素从衰老叶片或其它植物组织中再吸收或再分配的能力,使得营养元素在植物体内的留存时间增加,以提供植物新的生物量生产所需的大部分养分[31]。凋落物C、N、P含量及其比值与McGroddy等[7]的研究结果相比,表现为C含量、C∶N比值偏高,而N、P含量以及N∶P比值偏低,这与叶片与其它区域比较的结果基本一致,但C∶P比值明显低于McGroddy 等[7]在全球森林叶片研究中得到的结果,这与叶片与其它区域的比较的结果相左,这可能是由于本研究的P素再吸收率要低于McGroddy等[7]研究中的P素再吸收率,也可能是由于研究区域环境不同,营养元素的分解速率不同造成的(表 5)。
| 地区Region | 类型Types | C/(mg/g) | N/(mg/g) | P/(mg/g) | C∶N | C∶P | N∶P | 参考文献 References |
| 陕西省 Shaanxi Province | 油松 Pinus tabuliformis | 405.70±92.34 (12) | 8.29±1.25 (12) | 0.57±0.3 (12) | 50.57±15.26 (12) | 842.51±336.65 (12) | 16.08±4.11 (12) | 本文 |
| 全球 Global | 植物 Plant | - | - | - | 66.2±6.3* (106,56.58) | 3144.1±341.9* (104,1218.6) | 45.5±3.2* (99,20.59) | [7] |
| 温带针叶 Temperate Coniferous | - | - | - | 87.8±6.9* (25,75.0) | 2352.9±350.3* (19,911.9) | 26.0±4.6* (20,11.8) | ||
| a)括号中前一个数字为样本数; b) 带*数字为摩尔比,括号中后一个数字为转换成的质量比 | ||||||||
土壤与凋落物C、P含量及C∶N、C∶P、N∶P比值随林龄的变化趋势完全一致,表明土壤与凋落物之间有着密切的关系。土壤中C含量先显著增加,在33a达到最大值后略有降低但差异不显著,这与Zhou 等[32]、Luyssaert 等[33]和崔宁洁等[13]认为的土壤有机碳积累与植被群落年龄正相关的结论基本一致。一般来讲,土壤有机质 C∶N 比值与其分解速率呈反比,而土壤 C∶P 比值是表示P有效性高低的重要指标。研究表明,凋落物在P素较低的情况下N 及木质素含量较高(即较高的N∶P比值),因此可以认为N∶P比值是影响凋落物分解和养分归还速率的重要因素之一,较高的 N∶P 比值表明分解速度较慢[11]。本研究中,凋落物N∶P比值随着林龄先显著增加,在33a达到最大后下降,表明凋落物分解速率随林龄呈大致降低趋势,有利于养分存储,故可认为,研究区内成年油松林凋落物更有助于减缓水土流失。
3.3 油松林叶片、凋落物与土壤C、N、P及其比值的相关性分析本研究中叶片与凋落物N、P含量及C∶N、C∶P、N∶P比值之间存在显著相关性,表明凋落物中养分承自植物叶片,二者之间关系紧密。植物和土壤的C、N、P 含量之间均不存在显著相关性,表明土壤C、N、P 供应量对乔木叶片 C、N 、P 含量影响不大[12]。植物通过光合作用固定C,同时将部分C转移到土壤,并以凋落物的形式将 C 和养分逐步补偿给土壤[14],因此植物、凋落物与土壤的C、N、P含量之间有着密切的联系。本文相关分析的结果也显示了在油松叶片、凋落物和土壤C、N、P含量及其比值之间存在密切相关关系,这说明生态系统内部C、N、P 元素循环是在植物、凋落物和土壤3个库之间运输和转换的[7]。所以说探讨植物-凋落物-土壤的相互作用及其生态化学计量关系特征,并从生态化学计量特征的角度上掌握养分循环的调控机制,可以为促进生态化学计量学理论的发展提供新的科学依据,也可以为减缓温室效应提供新的研究思路。
| [1] | Elser J J, Fagan W F, kerkhoff A J, Swenson N G, Enquist B J. Biological stoichiometry of plant production:metabolism, scaling and ecological response to global change. New Phytologist , 2010, 186 (3) : 593–608. DOI:10.1111/j.1469-8137.2010.03214.x |
| [2] | 曾冬萍, 蒋利玲, 曾从盛, 王维奇, 王纯. 生态化学计量学特征及其应用研究进展. 生态学报 , 2013, 33 (18) : 5484–5492. |
| [3] | Elser J J, Dobberfuhl D R, Mackay N A, Fagan W F, Markow T A, Cotner J B, Harrison J F, Hobbie S E, Odell G M, Weider L W. Organism size, life history, and N:P stoichiometry. BioScience , 1996, 46 (9) : 674–684. DOI:10.2307/1312897 |
| [4] | Yu Q, Chen Q S, Elser J J, He N P, Wu H H, Zhang G M, Wu J G, Bai Y F, Han X G. Linking stoichiometric homoeostasis with ecosystem structure, functioning and stability. Ecology Letters , 2010, 13 (11) : 1390–1399. DOI:10.1111/j.1461-0248.2010.01532.x |
| [5] | ÅgrenG I, WeihM. Plant stoichiometry at different scales:element concentration patterns reflect environment more than genotype. New Phytologist , 2012, 194 (4) : 944–952. |
| [6] | 阎恩荣, 王希华, 周武. 天童常绿阔叶林演替系列植物群落的N:P化学计量特征. 植物生态学报 , 2008, 32 (1) : 13–22. |
| [7] | McGroddy M E, Daufresne T, Hedin L O. Scaling of C:N:P stoichiometry in forests worldwide:implications of terrestrial Redfield-type ratios. Ecology , 2004, 85 (9) : 2390–2401. DOI:10.1890/03-0351 |
| [8] | Zheng S X, Shangguan Z P. Spatial patterns of leaf nutrient traits of the plants in the Loess Plateau of China. Trees , 2007, 21 (3) : 357–370. DOI:10.1007/s00468-007-0129-z |
| [9] | 刘万德, 苏建荣, 李帅锋, 张志钧, 李忠文. 云南普洱季风常绿阔叶林演替系列植物和土壤C、N、P化学计量特征. 生态学报 , 2010, 30 (23) : 6581–6590. |
| [10] | 任书杰, 于贵瑞, 陶波, 王绍强. 中国东部南北样带654种植物叶片氮和磷的化学计量学特征研究. 环境科学 , 2007, 28 (12) : 2665–2673. |
| [11] | 潘复静, 张伟, 王克林, 何寻阳, 梁士楚, 韦国富. 典型喀斯特峰丛洼地植被群落凋落物C:N:P生态化学计量特征. 生态学报 , 2011, 31 (2) : 335–343. |
| [12] | 俞月凤, 彭晚霞, 宋同清, 曾馥平, 王克林, 文丽, 范夫静. 喀斯特峰丛洼地不同森林类型植物和土壤C、N、P化学计量特征. 应用生态学报 , 2014, 25 (4) : 947–954. |
| [13] | 崔宁洁, 刘小兵, 张丹桔, 张健, 刘洋, 邓长春, 纪托未, 陈亚梅. 不同林龄马尾松(Pinus massoniana)人工林碳氮磷分配格局及化学计量特征. 生态环境学报 , 2014, 23 (2) : 188–195. |
| [14] | 王维奇, 徐玲琳, 曾从盛, 仝川, 张林海. 河口湿地植物活体-枯落物-土壤的碳氮磷生态化学计量特征. 生态学报 , 2011, 31 (23) : 7119–7124. |
| [15] | ÅgrenG I, BosattaE. Theoretical Ecosystem Ecology-Understanding Element Cycles. Cambridge University Press , 1998 : 234–234. |
| [16] | 罗伟祥. 西北主要树种培育技术. 北京: 中国林业出版社, 2007238–245. |
| [17] | 韩娟娟, 程积民, 万惠娥, 杨晓梅, 孟蕾, 范文娟, 胡秀娟. 子午岭辽东栎群落碳储量研究. 西北林学院学报 , 2010, 25 (5) : 18–23. |
| [18] | 杨玉姣, 陈云明, 曹扬. 黄土丘陵区油松人工林生态系统碳密度及其分配. 生态学报 , 2014, 34 (8) : 2128–2136. |
| [19] | 鲍士旦. 土壤农化分析. 北京: 中国农业出版社, 200545–52. |
| [20] | Han W X, Fang J Y, Reich P B, Woodward F I, Zhang Z Y. Biogeography and variability of eleven mineral elements in plant leaves across gradients of climate, soil and plant functional type in China. Ecology Letters , 2011, 14 (8) : 788–796. DOI:10.1111/ele.2011.14.issue-8 |
| [21] | Elser J J, Fagan W F, Denno R F, Dobberfuhl D R, Folarin A, Huberty A, Interlandi S, Kilham S S, McCauley E, Schulz K L, Siemann E H, Sterner R W. Nutritional constraints in terrestrial and freshwater food webs. Nature , 2000, 408 (6812) : 578–580. DOI:10.1038/35046058 |
| [22] | Zhang H Y, Wu H H, Yu Q, Wang Z W, Wei C Z, Long M, Kattge J, Smith M, Han X G. Sampling date, leaf age and root size:Implications for the study of plant C:N:P stoichiometry. PLoS one , 2013, 8 (4) : e60360. DOI:10.1371/journal.pone.0060360 |
| [23] | McJannet C L, Keddy P A, Pick F R. Nitrogen and phosphorus tissue concentrations in 41 wetland plants:a comparison across habitats and functional groups. Functional Ecology , 1995, 9 (2) : 231–238. DOI:10.2307/2390569 |
| [24] | ÅgrenG I. Stoichiometry and nutrition of plant growth in natural communities. Annual Review Ecology, Evolution, and Systematics , 2008, 39 (1) : 153–170. |
| [25] | Wardle D A, Walker L R, Bardgett R D. Ecosystem properties and forest decline in contrasting long-term chronosequences. Science , 2004, 305 (5683) : 509–513. DOI:10.1126/science.1098778 |
| [26] | Aerts R. Nutrient resorption from senescing leaves of perennials:are there general pat terns. Journal of Ecology , 1996, 84 (4) : 597–608. DOI:10.2307/2261481 |
| [27] | Koerselman W, Meuleman A F M. The vegetation N:P ratio:a new tool to detect the nature of nutrient limitation. Journal of Applied Ecology , 1996, 33 (6) : 1441–1450. DOI:10.2307/2404783 |
| [28] | 杨佳佳, 张向茹, 马露莎, 陈亚南, 党廷辉, 安韶山. 黄土高原刺槐林不同组分生态化学计量关系研究. 土壤学报 , 2014, 51 (1) : 133–142. |
| [29] | Cleveland C C, Liptzin D. C:N:P stoichiometry in soil:is there a "Redfield ratio" for the microbial biomass? Biogeochemistry, 2007, 85(3):235-252. Biogeochemistry , 2007, 85 (3) : 235–252. DOI:10.1007/s10533-007-9132-0 |
| [30] | 黄昌勇. 土壤学. 北京: 中国农业出版社, 2000. |
| [31] | Meier C E, Grier C C, Cole D W. Below-and aboveground N and P use by Abies amabilis stands. Ecology , 1985, 66 (6) : 1928–1942. DOI:10.2307/2937389 |
| [32] | Zhou G Y, Liu S G, Li Z A, Zhang D Q, Tang X L, Zhou C Y, Yan J H, Mo J M. Old-growth forests can accumulate carbon in soils. Science , 2006, 314 (5804) : 1417–1417. DOI:10.1126/science.1130168 |
| [33] | Luyssaert S, Schulze E D, B rner A, Knohl A, Hessenm ller D, Law B E, Ciais P, Grace J. Old-growth forests as global carbon sinks. Nature , 2008, 455 (7210) : 213–215. DOI:10.1038/nature07276 |
 2016, Vol. 36
2016, Vol. 36