文章信息
- 付世建, 聂利娟, 吴慧, 况璐, 黄清
- FU Shijian, NIE Lijuan, WU Hui, KUANG Lu, HUANG Qing.
- 群体大小对青幼鱼群体特征的影响
- The effect of group size on school structure in juvenile black carp
- 生态学报[J]. 2016, 36(19): 6062-6070
- Acta Ecologica Sinica[J]. 2016, 36(19): 6062-6070
- http://dx.doi.org/10.5846/stxb201507181514
-
文章历史
- 收稿日期: 2015-07-18
- 网络出版日期: 2016-01-15
- 修订日期: 2015-11-05
鱼类集群行为指的是由于社会原因产生的个体聚集现象,为鱼类的重要行为之一,自然界超过50%鱼类种类在整个生活史或生活史特定时期表现出集群行为[1]。相关研究中,研究者通常关注个体行为及其交互作用如何影响群体特征[2],其中最重要的特征为凝聚力和协调性,前者主要通过群体的最近邻距离(NND)来衡量,而后者通常通过不同个体之间游泳速度的同步性和鱼群排列的极性等来衡量[3-4]。研究发现集群生活的个体在逃避敌害、觅食和寻找配偶等多方面体现出生态学收益,但同时可能造成食物资源的竞争加剧、能量消耗增加(用于维持群体中的特定位置)[5-7],且群体中社群等级的存在也可能对群体的形成、大小和生态学收益产生限制[8]。因此,集群的代价和收益可能因物种特征及特定的环境条件(如捕食压力和食物资源)而异,与群体的凝聚力和协调性密切相关。据此,本研究的第一个目标是探讨鱼群大小对青鱼(Mylopharyngodon piceus)凝聚力和协调性的影响。
研究发现鱼类群体特征的维系一定程度上通过个体对其近邻的位置和活动的反应来实现[4, 9],体现出自组织结构的特征[10-11]。自组织结构理论认为群体在没有固定领导者或外部刺激的条件下形成一个极化结构,个体在群体的位置是随机的,对群体决策起着均等的作用[11]。尽管鱼群常常表现出典型的自组织结构的行为特征,鱼群中不同个体是否存在分工以及不同个体在群体决策和集体活动中所起的作用是否均等一直是相关研究的热点问题,且存在着较大争议[2, 12-13]。鉴于技术手段的限制,群体中不同个体的行为模式及其对群体特征的影响一直无法系统开展,最近方便易行的动物轨迹追踪软件的开发为鱼类集群行为的系统深入研究提供了可能[14]。因此,本研究的第2个目标是通过该软件测定个体在群体中处于领头鱼位置的比例及其变化,以期检验青鱼群体中是否存在群体运动的个体分工差异以及群体大小的影响。
通过鱼群中个体间的信息交流和共识决策的形成,群体能够提高认知水平和解决特定问题的能力,产生集体智慧[15-17]。具体表现之一是鱼群对于捕食者的刺激信息可以通过对邻近个体行为的反应迅速扩散,以产生一致的逃避行为。这种信息传递的效率和群体的凝聚力和协调性密切相关,存在最适的群体大小和密度[18]。另外,群体大小对鱼群的勇敢性和警觉性等具有重要影响[7, 19]。因此理论上群体对捕食者刺激反应可能受群体大小的重要影响,而本研究的第3个目标是检验群体大小对青幼鱼刺激反应的影响及其与群体特征(凝聚力和协调性)之间可能的关联。
迄今为止,有关鱼类集群的研究主要集中在几种行为学模式动物上,对于我国淡水中最大类群的鲤科鱼类却鲜有报道。因此,本研究选取常见的鲤科鱼类青幼鱼为研究对象,运用最新的视频轨迹跟踪系统软件[14],拍摄和分析其不同大小群体中青幼鱼的运动轨迹,进而分析不同群体的速度和空间分布等行为学特征。研究同时分析了不同个体在群体中的位置分布以及不同群体大小对恐吓刺激反应的影响。
1 材料与方法 1.1 实验鱼的驯化与处理实验青幼鱼购于重庆当地养殖场,购回后在室内循环控温水槽中驯养两周,水温为(25±0.5) ℃。驯养期间每天在8: 00以商品饲料作饵料饱足投喂1次,投喂1h后用虹吸管清除残饵和粪便;驯养用水为经曝气控温后的自来水,并用充气泵向水体中持续充入空气以保证水体溶氧在90%饱和溶氧以上。日换水量约为水体总量的10%,昼夜光周期为L∶D=12h∶12h。驯化结束选取身体健康、大小相似的180尾鱼(体重(2.43±0.04) g,体长(5.34±0.03cm))作为实验对象。
1.2 实验方案实验分别设计1、2、4、8四个群体大小实验组,每组12个重复。实验水体温度为(25±0.5) ℃。为消除昼夜节律的影响,所有实验测定均在白天进行(9:00—17:00) 。为消除消化活动对行为的影响,所有实验鱼禁食2d后进行相关测定。
1.3 实验竞技场、实验鱼运动轨迹的获取及参数计算实验竞技场为实验室自制圆形行为观察设备(直径100 cm,高度20 cm)。实验水深为7 cm[5]。实验光源由12组日光灯(5组为8 W,另8组为4瓦)提供,以保证竞技场没有阴影也光照均匀。实验鱼转入竞技场后,用摄像设备(BNT 187Y3,aoni)持续拍摄15 min(30帧/s),随后敲击竞技场壁进行3次恐吓刺激,每次刺激间隔约20s。拍摄完成后用格式化工厂(http://format-factory.softonic.cn)软件将图像由.wmv转换为.avi格式,随后导入图像跟踪软件idTracker对图像进行分析[14],获得每尾实验鱼拍摄期间每帧的运动轨迹,得到每尾鱼每帧图像的27000个坐标点。根据像素和实物的相对大小转化为实验鱼实际位置(cm)的坐标点。随后进行自发游泳速度和空间位置特征的相关计算。为消除转运的影响,相关统计数据仅采用6—15 min的轨迹数据。
除单尾鱼实验组外,其余各实验组随机选取1尾鱼作为焦点鱼(Focal fish),仅对焦点鱼的游泳速度和空间分布参数进行统计。有关焦点鱼相关参数计算公式如下:
 (1)
(1)
式中,x(t)和y(t)分别为焦点鱼在t时刻的横、纵坐标点,dt为每帧图像的时间间隔
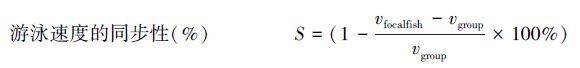 (2)
(2)
vfocalfish为焦点鱼游泳速度,vgroup为群体所有鱼的平均游泳速度。
 (3)
(3)
式中,x(t)和y(t)分别为焦点鱼和计算距离的另一尾鱼在t时刻的横、纵坐标点。4和8个体组计算出焦点鱼和其余实验鱼的距离后,其最小的数值即为焦点鱼的NND。
为了进一步考察青鱼的集群性和群体中不同个体位置是否随机,在每分钟选取36帧图像(2%),逐帧观察群体中不同个体运动方向和焦点鱼处于群体最前方的次数,得到群体排列的极性(P,%)和焦点鱼位于领头者比例(Lp,%),其计算公式如下:
 (4)
(4)
 (5)
(5)
实验鱼对刺激的反应参数通过人工观测视频得到,反应率(R,%)和反应的一致性(C,%)的计算公式如下:
 (6)
(6)
 (7)
(7)
对刺激展现相同行为指该群体所有鱼都对刺激均有反应或者均没有反应。
1.4 参数统计与分析数据采用Excel(2003) 进行常规计算后,再用SPSS17.0软件进行相关统计分析。群体大小对游泳速度、空间分布以及对刺激反应的相关数据采用单因素方差分析,如差异显著采用Duncan多重比较分析各组间的统计差异;2、4和8实验组焦点鱼处于领头鱼的比例与预期比例的差异采用非参数统计的二项式检验。所有数据结果均以平均值±标准误(Mean±SE)表示,显著水平定为P<0.05。
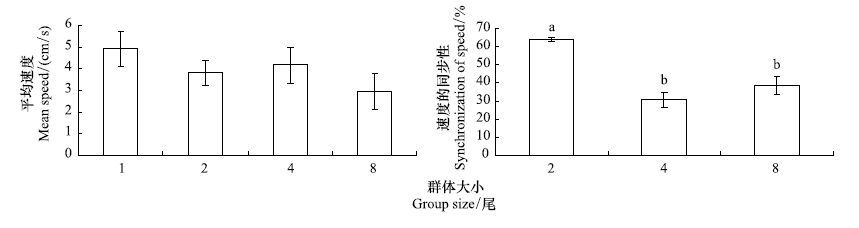
2 实验结果 2.1 群体大小对自发游泳的影响无论群体大小,实验鱼的自发游泳速度多介于0—10 cm/s之间(图 1);对第6—15 min游泳速度的分布分析发现,各实验组的自发游泳速度最高频率均出现在0—5 cm/s(图 1)。统计分析发现不同群体大小自发运动的平均速度(图 2)没有显著差异,但同组不同个体游泳速度间的同步性随群体数量的增加而显著下降(P <0.05) (图 2)。

|
| 图 1 不同群体大小青鱼的自发运动的游泳速度及其频率分布(1800桢/min)(平均值±标准误,N=12) Fig. 1 The spontaneous swimming speed and its frequency distribution of black carp juveniles with different group sizes (mean±S.E.,N=12) |
|
| 图 2 不同群体大小青鱼自发运动的速度及其同步性(平均值±标准误,N=12) Fig. 2 The effect of group size on mean swimming speed and its synchronization of swimming speed in juveniles of black carp (mean±S.E.,N=12) |
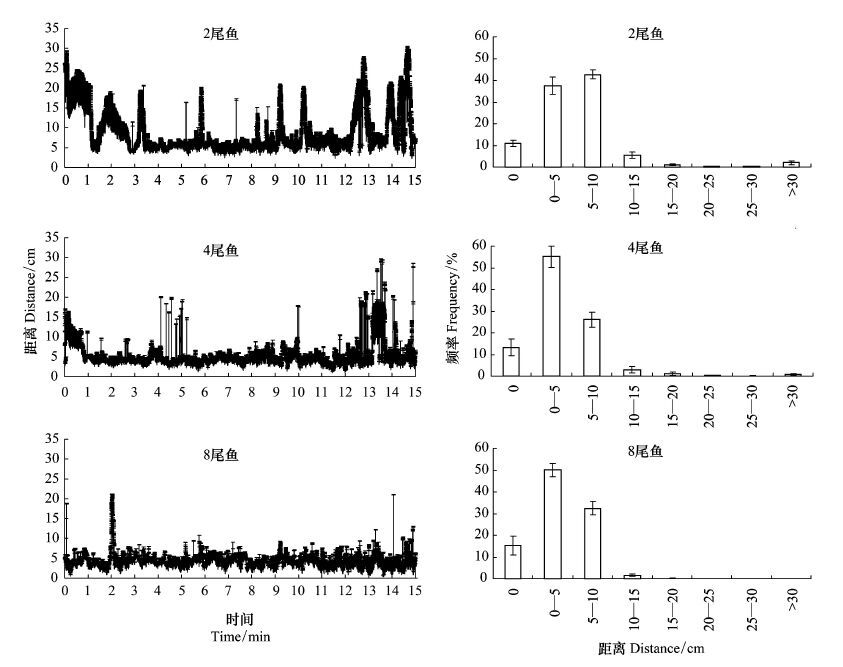
无论群体大小,焦点鱼和群体内其它个体的NND多出现在0—10 cm(图 3);对焦点鱼的NND的分析发现,2个体组NND出现频率最高的距离为5—10 cm,其次是0—5 cm。而4和8个体组频率最高出现在0—5 cm,其次为5—10 cm(图 3)。因此,个体NND随群体个体数量上升而显著下降(P <0.05) (图 4)。
|
| 图 3 不同群体大小青鱼的最近邻距离及其频率分布(1800桢/min)(平均值±标准误,N=12) Fig. 3 The nearest neighbor distance and its frequency distribution of black carp juveniles with different group sizes (mean±S.E.,N=12) |
|
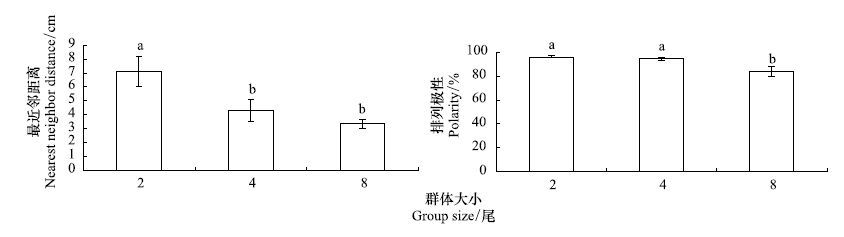
| 图 4 不同群体大小青鱼的最近邻距离及群体方向的极性(平均值±标准误,N=12) Fig. 4 The effect of group size on nearest neighbor distance and the polarity of orientation in juveniles of black carp (mean±S.E.,N=12) |
8个体组的极性显著小于2和4个体组。但总体上不同实验组青鱼均保持较高的极性,2和4个体组有92%—95%个体保持方向一致,而8个体组依然有84%个体保持方向一致(图 4)。
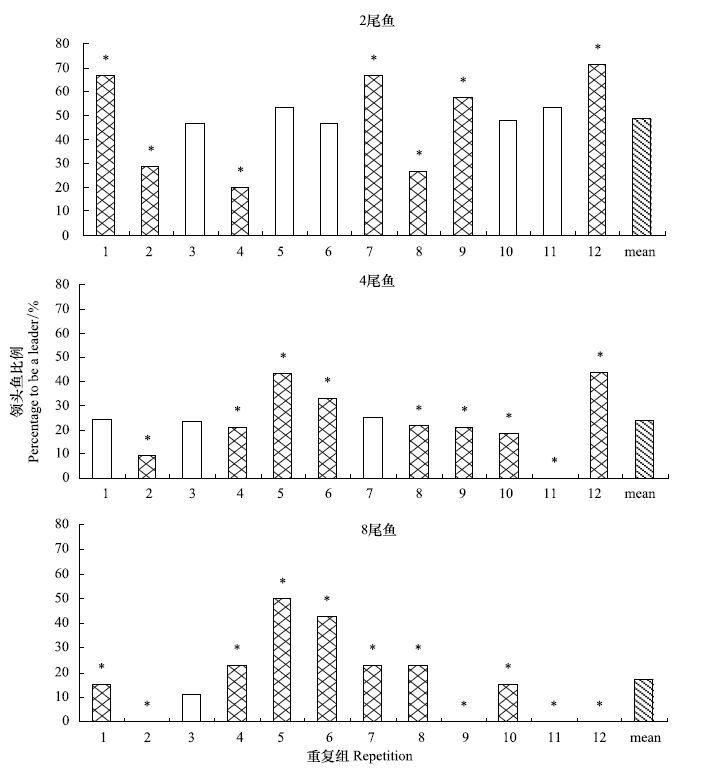
2.3 群体中个体领头鱼比例的变化对于2、4和8个体组的实验鱼,每尾鱼处于领头鱼位置的预期概率分别为50%、25%和12.5%。分析发现12尾焦点鱼位于领头鱼位置的总体平均值与预期概率十分接近,但各实验组内12尾焦点鱼处于领头鱼位置比例差异较大(图 5),与预期值有显著差异的数量分别为7、9和11尾。其位于领头鱼位置概率的变异系数(CV,标准差占平均值的比例)随群体个数的增加而加大,分别为33.86%、52.31%和98.19%。
|
| 图 5 不同群体大小青鱼12尾焦点鱼处于群体领头位置的比例 Fig. 5 The percentage of 12 repetition focal fish to swim in the front of a group in fish group with different group sizes |
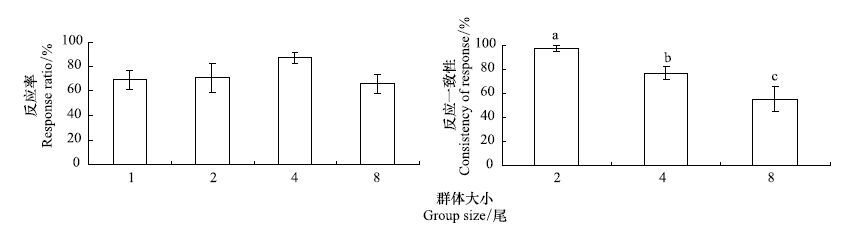
不同群体的反应率保持在66%—87%,不同实验组间没有显著差异(图 6),但反应的一致性随群体中个体数量的上升而显著下降(P <0.05) (图 6)。
|
| 图 6 不同群体个体青鱼对刺激的反应率及群体内不同个体对刺激反应的一致性(平均值±标准误,N=12) Fig. 6 The response ratio and it consistency to artificial frighten stimulus in juvenile black carp with different group sizes (mean±S.E.,N=12) |
一般认为集群生活的鱼类在防御敌害和觅食效率等方面均具有潜在的生态学收益。防御敌害的机制可能涉及针对捕食者的混乱效应(Confusion effect)、针对猎物的稀释效应(Dilution effect)及集体警觉的优势(Many-eye′s effect);捕食效率提高的机制可能涉及通过对同伴行为的效仿更快地发现食物以及协作防御节约更多时间用于觅食等。因此集群行为是鱼类普遍存在的行为。然而,群体的数量并非越大越为有利,而且群体可获得的空间大小、栖息地的物理和生物环境(如食物丰度)、种类的社群结构和社会利益冲突等均可能对群体大小产生限制。因此研究群体大小和群体特征的关系对理解鱼类集群行为的形成和维持机制至关重要。本研究发现青鱼具有集群行为,且随群体中个体数量增加,凝聚力上升,但协调性下降。群体中不同个体在群体中的位置存在差异且随群体大小上升而加剧。群体大小对刺激反应率没有显著影响,但协调性的下降导致群体成员对恐吓反应的一致性下降。
3.1 群体大小对群体凝聚力和协调性的影响青幼鱼超过90%的DNN位于0—10 cm之间(即0—2 BL),与食蚊鱼(Gambusia affinis)(6 cm/s,2 BL/s)[4]和金体美洲鳊(Notemigonus crysoleucas)(1.5—2 BL/s)等相似[9]。迄今为止,有关鲤科鱼类(斑马鱼除外)的集群研究十分匮乏,本研究发现青鱼NND较小,且随着群体增大而显著下降,这和霓虹灯鱼 (Paracheirodon innesi)、唐鱼(Tanichthys albonubes)、神仙鱼(Pterophyllum scalare)和虎皮鱼(Barbus tetrazona)等研究结果一致[19-20]。说明与大多数鱼类一样,青幼鱼群体有较高的群体凝聚力,存在典型的集群行为。
本研究通过分析群体的极性以及个体间游泳速度的同步性来考察群体大小对青幼鱼群体协调性的影响,发现8尾鱼实验组表现为更低的速度同步性和极性。类似结果在其它鱼类的研究中也有报道,如狭鳕(Theragra chalcogramma)的研究发现群体的协调性如排列的整齐度、个体间的同步性和群体的极性并不受群体大小的影响[21],而食蚊鱼的研究发现8个体组比4个体组有更低的速度同步性[2]。可能原因包括随着群体数量上升个体间个性差异增大、信息交流传递干扰等因素。但8个体组青幼鱼依然保持约85%的极性,其下降幅度远远小于随机的理论计算值。这也进一步说明青鱼具有典型的集群行为。
3.2 青鱼群体分布的个体变异探索和确定个体行为和社会交互作用如何影响和产生特定群体行为,特别是领导行为(Leadership)是理解集群行为的基础之一。自组织结构的典型特征是群体中的个体主要通过局部信息(Local information)交流,通过对近邻行为的简单模仿或特定的规则形成复杂多变的群体行为。因此自组织结构内部的个体作用和位置可能是随机且均等的[11]。然而从生态学的视角来分析,处于群体不同位置的个体在获取食物和遭遇捕食者的概率上有着较大的差异,因此鱼群不同个体的社群等级、生理状况(如游泳能力、能量储备等)可能对其在群体的位置具有显著影响[22]。本研究发现对于2、4和8群体的青幼鱼,随机挑选的焦点实验鱼处于群体前端,即领导者的概率多数偏离预期概率,且个体之间的变异随着群体个体数量的上升而加大。说明青幼鱼在空间分布上存在个体差异且受群体大小影响。这提示随着群体个体增加,群体中个体作用分工和(或)社群等级作用更为凸显。但这种差异是否具有稳定性,位置分布与个体在生理和行为特征(如个体侵略性、勇敢性)的关联以及不同位置个体的生态效益和代价有待研究。
3.3 群体大小对恐吓刺激反应的影响由于混乱效应、稀释效应及集体警觉的存在,一般认为随着群体大小上升,捕食者对单个个体的捕食压力下降。这可能导致群体成员的勇敢性和警觉性的下降进而影响群体成员对恐吓刺激的反应[7]。另外,群体间不同个体的信息交流和模仿理论会增大对刺激的反应率[17]。然而本研究未发现不同群体大小对外界刺激反应率的差异。可能原因是随着群体数量的上升,成员勇敢性提高和警觉性下降的作用抵消了群体成员间的信息交流和行为模仿的正向作用。另外鱼群对刺激的反应和物种的特性也可能对其产生影响,如对4种鱼类的研究发现个体侵略性、勇敢性均与群体大小有关,但不同种类因领域意识差异而表现为不同的形式[20]。 青鱼对刺激反应的一致性随着群体数量的上升而下降可能协调性的降低有关。
总之,本研究发现青鱼具有典型的集群行为。随着群体数量的上升,凝聚力上升(表现为NND的减小),但协调性有所下降(表现为速度同步性、群体排列极性和刺激反应一致性的下降);这种群体特征的改变对刺激反应率没有影响,但导致反应的一致性降低;群体中不同个体的分布具有个体差异,且随群体数量的上升,个体间的差异加剧,提示群体不同个体在集群行为和(或)决策上存在分工。在不同种类间比较群体大小与群体特征的关联,探讨不同选择压力下集群行为的收益和代价,并从进化和系统发生的角度研究鱼类集群行为。
| [1] | Shaw E. Schooling fishes. American Scientist , 1978, 66 (2) : 166–175. |
| [2] | Herbert-Read J E, Krause S, Morrell L J, Schaerf T M, Krause J, Ward A J W. The role of individuality in collective group movement. Proceedings of the Royal Society B:Biological Sciences , 2012, 280 (1752) : 20122564. DOI:10.1098/rspb.2012.2564 |
| [3] | 石小涛, 王博, 王雪, 陈求稳, 白艳勤, 高柱, 涂志英, 刘德富. 胭脂鱼早期发育过程中集群行为的形成. 水产学报 , 2013, 37 (5) : 705–710. |
| [4] | Herbert-Read J E, Perna A, Mann R P, Schaerf T M, Sumpter D J T, Ward A J W. Inferring the rules of interaction of shoaling fish. Proceedings of the National Academy of Sciences of the United States of America , 2011, 108 (46) : 18726–18731. DOI:10.1073/pnas.1109355108 |
| [5] | Milinski M, Heller R. Influence of a predator on the optimal foraging behaviour of sticklebacks (Gasterosteus aculeatus L.). Nature , 1978, 275 (5681) : 642–644. DOI:10.1038/275642a0 |
| [6] | Pitcher T J, Magurran A E, Winfield I J. Fish in larger shoals find food faster. Behavioral Ecology and Sociobiology , 1982, 10 (2) : 149–151. DOI:10.1007/BF00300175 |
| [7] | Goldenberg S U, Borcherding J, Heynen M. Balancing the response to predation-the effects of shoal size, predation risk and habituation on behaviour of juvenile perch. Behavioral Ecology and Sociobiology , 2014, 68 (6) : 989–998. DOI:10.1007/s00265-014-1711-1 |
| [8] | Wong M Y L. Group size in animal societies:the potential role of social and ecological limitations in the group-living fish, Paragobiodon xanthosomus. Ethology , 2011, 117 (7) : 638–644. DOI:10.1111/j.1439-0310.2011.01913.x |
| [9] | Katz Y, Tunstrøm K, Ioannou C C, Huepe C, Couzin I D. Inferring the structure and dynamics of interactions in schooling fish. Proceedings of the National Academy of Sciences of the United States of America , 2011, 108 (46) : 18720–18725. DOI:10.1073/pnas.1107583108 |
| [10] | Couzin I D, Krause J. Self-organization and collective behavior in vertebrates. Advances in the Study of Behaviour , 2003, 32 : 1–75. DOI:10.1016/S0065-3454(03)01001-5 |
| [11] | Sumpter D J T. The principles of collective animal behaviour. Philosophical Transactions of the Royal Society B:Biological Sciences , 2006, 361 (1465) : 5–22. DOI:10.1098/rstb.2005.1733 |
| [12] | Reebs S G. Can a minority of informed leaders determine the foraging movements of a fish shoal?. Animal Behaviour , 2000, 59 (2) : 403–409. DOI:10.1006/anbe.1999.1314 |
| [13] | Ward A J W, Herbert-Read J E, Jordan L A, James R, Krause J, Ma Q, Rubenstein D I, Sumpter D J T, Morrell L J. Initiators, leaders, and recruitment mechanisms in the collective movements of damselfish. The American Naturalist , 2013, 181 (6) : 748–760. DOI:10.1086/670242 |
| [14] | Pérez-Escudero A, Vicente-Page J, Hinz R C, Arganda S, de Polavieja G G. idTracker:tracking individuals in a group by automatic identification of unmarked animals. Nature Methods , 2014, 11 (7) : 743–748. DOI:10.1038/nmeth.2994 |
| [15] | Conradt L, Roper T J. Consensus decision making in animals. Trends in Ecology & Evolution , 2005, 20 (8) : 449–456. |
| [16] | Krause J, Ruxton G D, Krause S. Swarm intelligence in animals and humans. Trends in Ecology & Evolution , 2010, 25 (1) : 28–34. |
| [17] | Gleason P E, Weber P G, Weber S P. Effect of group size on avoidance learning in zebra fish, Brachydanio rerio (Pisces:Cyprinidae). Animal Learning & Behavior , 1977, 5 (2) : 213–216. |
| [18] | Sumpter D J T, Krause J, James R, Couzin I D, Ward A J W. Consensus decision making by fish. Current Biology , 2008, 18 (22) : 1773–1777. DOI:10.1016/j.cub.2008.09.064 |
| [19] | Shelton D S, Price B C, Ocasio K M, Martins E P. Density and group size influence shoal cohesion, but not coordination in zebrafish (Danio rerio). Journal of Comparative Psychology , 2015, 129 (1) : 72–77. DOI:10.1037/a0038382 |
| [20] | Saxby A, Adams L, Snellgrove D, Wilson R W, Sloman K A. The effect of group size on the behaviour and welfare of four fish species commonly kept in home aquaria. Applied Animal Behaviour Science , 2010, 125 (3/4) : 195–205. |
| [21] | Sogard S M, Olla B L. The influence of hunger and predation risk on group cohesion in a pelagic fish, walleye pollock Theragra chalcogramma. Environmental Biology of Fishes , 1997, 50 (4) : 405–413. DOI:10.1023/A:1007393307007 |
| [22] | Killen S S, Marras S, Steffensen J F, McKenzie D J. Aerobic capacity influences the spatial position of individuals within fish schools. Proceedings of the Royal Society B:Biological Sciences , 2012, 279 (1727) : 357–364. DOI:10.1098/rspb.2011.1006 |
 2016, Vol. 36
2016, Vol. 36