文章信息
- 何芳兰, 金红喜, 王锁民, 韩生慧, 曾荣, 马俊梅
- HE Fanglan, JIN Hongxi, WANG Suomin, HAN Shenghui, ZENG Rong, MA Junmei.
- 沙化对玛曲高寒草甸土壤微生物数量及土壤酶活性的影响
- Effect of desertification on soil microbial biomass and enzyme activities in Maqu alpine meadow
- 生态学报[J]. 2016, 36(18): 5876-5883
- Acta Ecologica Sinica[J]. 2016, 36(18): 5876-5883
- http://dx.doi.org/10.5846/stxb201503200536
-
文章历史
- 收稿日期: 2015-03-20
- 网络出版日期: 2016-01-05
2. 甘肃省治沙研究所, 兰州 730070;
3. 甘肃河西走廊森林生态系统国家定位观测研究站, 武威 733000;
4. 甘肃民勤荒漠草地生态系统国家野外科学观测研究站, 民勤 733300;
5. 民勤县林业局, 民勤 733300
2. Gansu Desert Control Research Institute, Lanzhou 730070, China;
3. Gansu Hexi Corridor Forest Ecosystem National Research Station, Wuwei 733000, China;
4. Gansu Minqin National Field Observation and Research Station on Ecosystem of Desertification Rangeland, Minqin 733300, China;
5. Foresty Bureau of Minqin county, Minqin 733300, China
土壤微生物生物量、土壤呼吸和酶活性等生物特性比土壤有机质、养分含量等其它理化性状对土壤质量的变化做出更敏感地响应[1]。土壤酶参与土壤的发生发育以及土壤肥力形成和演化的全过程, 具有高度催化作用, 其活性常作为表征土壤肥力的指标之一[2]。因此, 土壤微生物及酶活性常常被用作自然和农业生态系统中土壤胁迫过程或生态恢复过程的早期敏感性和肥力指标。
玛曲县位于甘肃省西南部(100°45′45″—102°29′00″ E, 33°06′30″—34°30′15″ N), 是青藏高原的重要组成部分和黄河主要的水源涵养区, 高寒草甸是其最主要的自然资源和牧民赖以生存的物质基础[3]。近年来, 在人为因素和自然因素的共同影响下, 高寒草甸生态系统发生了严重的沙化, 由斑点状分布的半固定、半沙漠向集中连片全沙化和流动沙丘退化, 沙化草甸面积已达53.3km2, 并且以平均每年2km2的速度递增[4]。在黄河沿岸形成约有220km的沙丘带, 沙丘高达12—15m。
玛曲高寒草甸的沙化引起了诸多研究学者重视。李昌龙等[5-9]对玛曲草甸沙化特征、植被生物量、土壤理化性质、土壤养分等进行研究, 指出玛曲高寒草甸沙化导致土壤颗粒变粗, 土壤含水量和养分显著下降, 同时大量高寒物种流失、植被盖度下降、植物多样性下降、生产力降低。郑华平等[10]在对沙化草地进行施肥研究, 发现施肥增加了植被物种丰富度和生物量。陈文业等[11]提出了玛曲高寒草甸沙化治理模式, 通过草方格+山生柳密植扦插+种草的治理模式可使植被覆盖度达到78%。但是, 玛曲高寒草甸沙化过程中土壤微生物结构和土壤酶活性的变化研究未见报道。为此, 本文试图通过对玛曲不同沙化程度草甸土壤微生物数量和土壤酶活性进行研究与分析, 探讨土壤微生物数量、土壤酶活性与高寒草甸沙化的动态关系, 为高寒草甸沙化生态系统生态植被重建与恢复提供理论依据。
1 研究区概况及材料方法 1.1 研究区概况试验样地位于甘肃省玛曲县东南部(102°3′24″—102°10′4 ″E;33°55′1″—33°57′48″ N), 海拔3430—3442 m。该区域冬春季漫长, 严寒多风;夏秋季短, 多雨潮湿;年均气温1.2 ℃, 降水量615 mm, 年蒸发量1352.4 mm;年均风速2.5 m/s, 最大风速36 m/s, 全年平均8级以上的大风日数77 d, 最多日数达121 d, 每年12月至翌年5月为大风季节。土壤类型为高寒草甸土, 地表部分被沙土覆盖, 植物稀疏, 植物种类主要以高山嵩草(Kobresia pygmaea)、青藏苔草(Carex moorcroftii)、高寒早熟禾(Poa koelzii)、垂穗披碱草(Elymus nutans)、裂叶独活(Heracleum millefolium)、藏虫实(Corispermum tibeticum)以及毛穗赖草(Leymus paboanus)等草本植物为主。
1.2 材料与方法 1.2.1 样地布设2013年8月, 依据魏兴琥、苏大学[6, 12]关于高寒草甸和天然草原沙化程度分级指标, 在玛曲县选择典型样地9个, 每个样地内分别筛选未沙化(ND)、轻度沙化(SLD)、中度沙化(MD)以及重度沙化(SD)样方3个(表 1)。
| 沙化程度 Desertification degree | 地貌特征 Geomorphological features |
植被优势种 Dominant populations |
植被盖度/% Vegetation coverage | 流沙覆盖度/% Sand coverage |
| ND | 高寒嵩草草甸 | 高山嵩草、青藏苔草 | >90 | 0 |
| SLD | 轻度风蚀或沙埋 | 藏青苔草、早熟禾 | 50—90 | 0—5 |
| MD | 中度风蚀或沙埋 | 藏青苔草、裂叶独活 | 30—50 | 5—25 |
| SD | 半流动沙丘或沙垄 | 毛穗赖草、藏虫实 | 10—30 | 25—50 |
| ND:无沙化草甸None desertification;SLD:轻度沙化草甸Slight desertification;MD:中度沙化草甸Moderate desertification;SD:重度沙化草甸Severe desertification | ||||
每个样方内随机选5个点, 挖0—40cm深的坡面, 每个坡面0—20cm层自下而上取约300g鲜土后, 将5个点土样混合后立即装入无菌袋中, 置于便携式小冰箱内;此外, 用铝盒在每个坡面上0—20cm之间取样, 用便携式电子称立即称重。
1.2.3 土壤颗粒、含水率、pH测定土壤颗粒粒径用马尔文粒度仪测定,土壤含水率用烘干法测定, 土壤pH用无二氧化碳蒸馏水(水土比5:1)浸提后pH计测定[13]。
1.2.4 土壤微生物测定土壤微生物数量测定:土壤微生物数量用平板表面涂抹法计数[14]。真菌采用马丁-孟加拉红培养基, 细菌采用牛肉膏蛋白胨琼脂培养基, 放线菌采用改良高氏一号培养基[15-16]。
1.2.5 土壤酶活性测定土壤蔗糖酶活性采用比色法, 土壤脲酶活性采用靛酚蓝比色法, 土壤磷酸酶活性采用磷酸苯二钠比色法, 土壤过氧化氢酶采用容量法[17-18]。
1.2.6 数据分析试验数据用Excel和SPSS 17.0软件进行处理。
2 结果分析 2.1 沙化过程中土壤颗粒组成、含水量以及pH的变化玛曲高寒草甸沙化过程中, 土壤颗粒组成、土壤含水率以及pH均发生了显著变化(P < 0.05)(表 2)。由表 2可以看出, 高寒草甸从未沙化退化到轻度沙化, 土壤粘粒体积百分比、粉粒体积百分比、土壤含水率相对减少75.19%、80.07%、71.23%, 细砂粒体积百分比、粗砂粒百分比以及pH值相对增加50.60%、169.27%、4.76%;高寒草甸从轻度沙化退化到中度沙化, 土壤粘粒体积百分比、粉粒体积百分比、细砂粒体积百分比、土壤含水量相对减少24.14%、7.89%、38.19%、32.59%, 粗砂粒相对增加170.53%, 而pH基本没有变化;高寒草甸从中度沙化退化到重度沙化, 土壤粘粒体积百分比、细砂粒体积百分相对减少15.51%、19.09%, 粗砂粒体积百分比增加18.20%, 其它土壤特征值没有发生显著变化。
| 沙化程度 Desertification degree | 0.01—2um (粘粒) Clay particles | 2—20μm (粉粒) Silt particles | 20—200μm (细砂粒) Fine sand | 200—2000μm (粗砂粒) Coarse sand | 含水率/% Water content |
pH |
| ND | 9.35±0.01a | 35.67±0.65a | 48.44±0.38b | 6.54±0.33d | 21.76±0.78a | 7.36±0.02b |
| SLD | 2.32±0.04b | 7.11±0.19b | 72.95±1.09a | 17.61±0.94c | 6.26±0.29b | 7.71±0.03a |
| MD | 1.76±0.01c | 6.54±0.09bc | 45.09±02.9c | 47.64±0.97b | 4.22±0.01c | 7.74±0.03a |
| SD | 1.75±0.01c | 5.46±0.06c | 36.48±0.42d | 56.31±0.45a | 3.92±0.20c | 7.79±0.03a |
| 同一列不同字母表示差异显著(P < 0.05) | ||||||
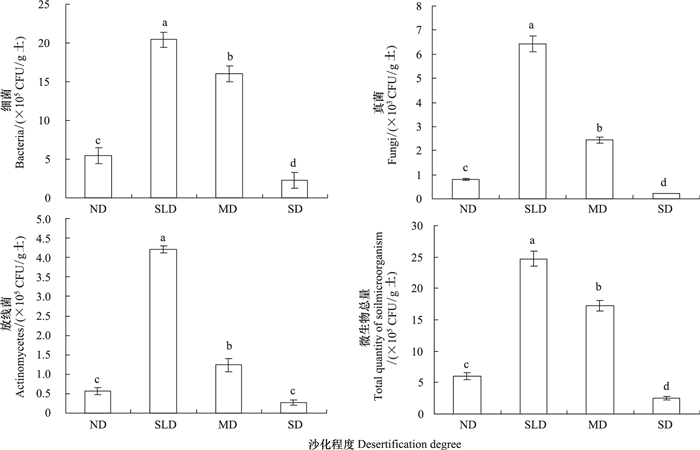
从图 1可以看出, 高寒草甸沙化过程中土壤微生物(细菌、真菌、放线菌)数量发生了显著的变化(P < 0.05)。随沙化程度的加剧, 3类微生物的数量均先急剧增大, 然后又急剧减小。细菌数量、真菌数量、放线菌数量及微生物总量在轻度沙化阶段出现了最大值, 其值分别是未沙化阶段的3.72、8.13、7.52倍以及4.04倍。不同沙化阶段高寒草甸土壤中3类微生物数量及总的微生物数量分别为:轻度沙化>中度沙化>未沙化>重度沙化。
|
| 图 1 玛曲高寒草甸沙化对土壤微生物数量影响 Fig. 1 Effect of desertification on the numbers of soil microorganisms in Maqu alpine meadow |
为了进一步了解高寒草甸沙化过程土壤微生物菌群组成的动态变化, 对土壤系统主要微生物细菌、真菌、放线菌数量百分比进行了分析(表 3)。从表 3可以看出, 随着沙化程度的加剧, 3类微生物数量百分比均发生了显著变化(P < 0.05)。其中, 细菌数量的百分比呈现出减小—增大—减小的趋势, 中度沙化阶段百分比值最大(92.53%);真菌数量的百分比则表现为先增大后减小, 在轻度沙化阶段的样地中, 达到最大值(0.25%);放线菌数量的百分比是增大—减小—增大, 其轻度沙化阶段的值最大(17.05%)。此外, 在整个高寒草甸沙化的过程中, 土壤细菌一直在整个菌群体系中占主要位置, 其数量百分比一直在82%以上, 其次依次是放线菌、真菌。
| 沙化程度 Desertification degree | 细菌 Bacteria |
真菌 Fungi | 放线菌 Actinomycetes |
| UD | 90.61±3.12 b | 0.13±0.01 b | 9.26±0.45 c |
| SLD | 82.64±1.25 d | 0.25±0.02 a | 17.05±2.13 a |
| MD | 92.53±2.34 a | 0.14±0.01 c | 7.17±0.45 d |
| SD | 89.21±2.45 c | 0.08±0.01 d | 10.71±1.34 b |
从图 2可以看出, 沙化对高寒草甸土壤蔗糖酶活性、脲酶活性、中性磷酸酶活性及过氧化氢酶活性均不同程度影响, 除中性磷酸酶外, 各水平间差异显著(P < 0.05)。其中, 从未沙化向轻度沙化草甸的退化过程中, 蔗糖酶活性、脲酶活性以及过氧化氢酶活性分别降低了40.61%、6.57%和4.97%, 中性磷酸酶几乎没有变化;从轻度沙化草甸向中度沙化草甸退化过程中, 蔗糖酶活性、脲酶活性、中性磷酸酶活性以及过氧化氢酶活性分别降低了55.17%、27.13%、79.50%和20.71%;从中度沙化草甸退化到重度沙化草甸过程中, 除中性磷酸酶外, 其它3种酶的活性继续减小。此外, 随高寒草甸沙化程度加剧, 4种酶活性均呈现出不同程度的降低。

|
| 图 2 沙化对玛曲高寒草甸土壤酶活性影响 Fig. 2 Effect of desertification on soil enzyme activity in Maqu alpine meadow |
为了进一步了解玛曲高寒草甸沙化过程中土壤物理性质、土壤微生物数量及土壤酶活性的相互关系, 对14个指标值进行了相关性分析(表 4)。由表 4可以看出, 土壤粘粒、粉粒与粗砂粒、含水量、pH值、4种酶活性间呈现出显著相关性(P < 0.05);土壤细砂粒与粗砂粒、真菌、放线菌、中性磷酸酶、过氧化氢酶之间呈现出显著相关性(P < 0.05);粗砂粒与土壤含水率、pH值、4种土壤酶活性间呈现显著相关性(P < 0.05);细菌与真菌、放线菌之间存在显著正相关关系(P < 0.05);4种土壤酶活性两两之间存在极显著地正相关关系(P < 0.01)。
| 指标 Indexes | 粘粒 Clay particles | 粉粒 Silt particle | 细砂粒 Fine sand | 粗砂粒 Coarse particle | 含水率 Water content | pH值 pH value |
细菌 Bacteria |
真菌 Fungi |
放线菌 Actinomycetes |
蔗糖酶 Invertase |
脲酶 Urease | 中性磷酸酶 Phosphatase | 过氧化氢酶 Catelase |
| 粘粒Clay particles | 1.000 | ||||||||||||
| 粉粒Silt particle | 0.999** | 1.000 | |||||||||||
| 细砂粒Fine sand | -0.016 | -0.057 | 1.000 | ||||||||||
| 粗砂粒Coarse particle | -0.763** | -0.736** | -0.634* | 1.000 | |||||||||
| 含水率Water content | 0.999** | 0.996** | 0.028 | -0.791** | 1.000 | ||||||||
| pH值pH value | -0.993** | -0.993** | -0.013 | 0.777** | -0.996** | 1.000 | |||||||
| 细菌Bacteria | -0.385 | -0.393 | 0.474 | -0.015 | -0.345 | 0.289 | 1.000 | ||||||
| 真菌Fungi | -0.334 | -0.359 | 0.784** | -0.253 | -0.287 | 0.256 | 0.915** | 1.000 | |||||
| 放线菌Actinomycetes | -0.394 | -0.367 | -0.355 | 0.527 | -0.388 | 0.316 | 0.655* | 0.298 | 0.186 | ||||
| 蔗糖酶Invertase | 0.892** | 0.872** | 0.434 | -0.970** | 0.910** | -0.893** | -0.177 | 0.022 | 0.083 | 1.000 | |||
| 脲酶Urease | 0.648* | 0.634* | 0.508 | -0.834** | 0.683* | -0.710** | 0.418 | 0.470 | 0.475 | 0.783** | 1.000 | ||
| 中性磷酸酶Phosphatase | 0.633* | 0.604* | 0.735** | -0.967** | 0.670* | -0.670* | 0.269 | 0.479 | 0.528 | 0.888** | 0.910** | 1.000 | |
| 过氧化氢酶Catelase | 0.717** | 0.695* | 0.605* | -0.948** | 0.751** | -0.762** | 0.261 | 0.406 | 0.440 | 0.889** | 0.959** | 0.978** | 1.000 |
| +正相关, -负相关, *显著相关(P < 0.05), **极显著相关(P < 0.01) | |||||||||||||
本试验表明, 随着玛曲高寒草甸土壤沙化程度的逐渐加剧, 土壤0—20cm层中细菌、真菌以及放线菌数量均发生了显著变化, 其变化趋势是先增大后减小。李昌龙、安富博等人[5, 19]研究表明, 玛曲高寒草甸植被地下生物量、土壤养分等均随其沙化程度增加逐渐减小, 这说明植被和土壤营养物质并不是影响该阶段土壤微生物变化的主导因素。Hassink、Foster以及李君锋等人[20-22]研究表明, 土壤微生物与土壤孔隙大小、土壤含水率有很大关系。因此本研究认为, 可能因为玛曲未沙化区域的植被生长良好、土壤含水量率高、土壤粘粒含量高, 致使土壤含水量大多呈饱和状态, 土壤中过多的水分影响到土壤含氧量, 最终致使未沙化土壤中微生物数量较小;当土壤逐渐演替到轻度沙化时, 因土壤粘粒含量减少、细砂粒含量增大、土壤含水率减小、土壤通气性改善, 土壤生物迅速繁殖, 促使轻度沙化土壤微生物数量急剧增大。当土壤由轻度沙化演替到中度或重度沙化时, 土壤微生物下降可能是受土壤理化性质和植被双重影响。该区域土壤pH在7.3—7.8之间, 土壤微生物群落中, 细菌数量最大, 这与胡亚林等人[23]研究一致。
本研究中发现, 随着玛曲高寒草地沙化程度加重, 土壤蔗糖酶、脲酶、中性磷酸酶以及过氧化氢酶活性均呈现出逐渐减少的趋势。土壤酶主要来源于土壤微生物和植物根系分泌物及动植物残体分解释放的酶, 这说明玛曲高寒草甸在未沙化向轻度沙化退化过程中, 影响土壤酶活性变小的主要因子是植物, 而不是土壤微生物。但是, 在轻度沙化向中度、重度演化过程中, 土壤理化性质、土壤微生物以及植物共同影响着土壤酶活性变化, 这与林娜、万忠梅等人[24-25]研究报道相一致, 至于那个因子对这种变化起主导作用还有待于进一步研究。此外, 在野外实地取样过程中发现, 随沙化程度逐渐加剧, 土壤中微小动物种类和数量均逐渐减少, 这说明土壤中微小动物也是影响土壤酶活性变化因子之一。
土壤微生物与土壤理化性质、土壤酶活性、植物根系等之间存在一定关系, 同时其群落内也存在复杂的互馈关系, 包括共生、互生、捕食等。本研究通过对土壤细菌、真菌、放线菌、蔗糖酶、脲酶、中性磷酸酶、过氧化氢酶、pH值、土壤水分以及土壤颗粒组成进行相关性分析, 发现土壤微生物与土壤酶活性之间的相关性不显著, 这与王笛等人[26-27]的研究结果存在差异。此外, 本研究发现细菌与真菌之间存在显著相关性, 但Mackie等人[28]研究表明, 细菌的挥发性物质影响着真菌的生长。因此, 本研究认为部分因子之间表现出的相关性是因为在高寒草甸整个沙化过程中, 某些因子受环境和植被变化导致统一变化趋势所致, 比如真菌与细菌以及4种酶之间正相关;相反, 有些因子之间的确存在相关性, 但因其它因子影响大于其影响, 从变化趋势上体现不出相关性, 比如土壤微生物数量与土壤酶活性之间。
针对玛曲高寒草甸沙化过程植被组成、土壤物理性质、土壤微生物以及土壤酶活性等动态变化, 本研究认为沙化首先了驱使土壤颗粒组成和植被组成发生了变化, 土壤颗粒组成和植被组成的变化致使土壤生物特征、土壤肥力以及土壤酶等发生了变化。因此, 在玛曲沙化高寒草甸恢复过程中, 首先通过多种措施逆转主动因子——沙化, 土壤生态系统才能实现逆向演变。
4 结论沙化对玛曲高寒草甸土壤微生物数量及土壤酶活性有极大的影响。(1) 随沙化程度的加剧, 细菌数量、真菌数量、放线菌数量以及微生物总数量均出现了先增大后减小的趋势, 在发生沙化的高寒草甸土壤中, 细菌占土壤微生物的主要组分, 然后依次是放线菌和真菌。(2) 土壤蔗糖酶、脲酶、中性磷酸酶以及过氧化氢酶活性随沙化程度加剧急剧减小。(3) 玛曲高寒草甸沙化过初期, 驱使土壤微生物数量变化的主导因子是土壤孔隙度和含水量;其沙化后期, 驱使土壤酶活性变化的主导因子是土壤微生物、土壤孔隙度和土壤含水量。(4) 沙化直接改变玛曲高寒草甸土壤颗粒组成和植物组成, 间接改变了土壤微生物数量和土壤酶活性。
| [1] | Dick R P, Breakwill D, Turco R. Soil Enzyme Activities and Biodiversity Measurements as Integrating Biological Indicators. Wisconsin: Soil Science Society of America Special Publication, 1996247–272. |
| [2] | 杨万勤, 王开运. 土壤酶研究动态与展望. 应用与环境生物学报 , 2002, 8 (5) : 564–570. |
| [3] | 逯军峰, 董治宝, 胡光印, 宋翔, 魏振海. 甘肃省玛曲县土地沙漠化发展及其成因分析. 中国沙漠 , 2012, 32 (3) : 604–609. |
| [4] | 王辉, 任继周, 袁宏波. 黄河源区高寒草地沙化进程中土壤物理性质的变化(简报)-以玛曲为例. 草业学报 , 2007, 16 (1) : 30–33. |
| [5] | 李昌龙, 徐先英, 金红喜, 王多泽, 李菁菁. 玛曲高寒草甸沙化过程中群落结构与植物多样性. 生态学报 , 2014, 34 (14) : 3953–3961. |
| [6] | 陈文业, 张瑾, 戚登臣, 赵明, 张继强, 李广宇, 魏强, 王芳, 朱丽, 刘振恒, 孙飞达, 康建军, 罗文莉. 黄河首曲-玛曲县高寒草甸沙化动态演变趋势及其驱动因子定量分析. 草业学报 , 2013, 22 (3) : 11–21. |
| [7] | 牛叔文, 马利邦, 曾明明. 过牧对玛曲草地沙化的影响. 生态学报 , 2008, 28 (1) : 145–153. |
| [8] | 魏兴琥, 李森, 杨萍, 董玉祥, 张春来. 藏北高山嵩草草甸植被和多样性在沙漠化过程中的变化. 中国沙漠 , 2007, 27 (5) : 750–757. |
| [9] | 王鹤龄, 牛俊义, 郑华平, 陈子萱. 玛曲高寒沙化草地生态位特征及其施肥改良研究. 草业学报 , 2008, 17 (6) : 18–24. |
| [10] | 郑华平, 陈子萱, 王生荣, 牛俊义. 施肥对玛曲高寒沙化草地植物多样性和生产力的影响. 草业学报 , 2007, 16 (5) : 34–39. |
| [11] | 陈文业, 郑华平, 戚登臣, 李广宇, 柴春山, 刘正恒, 宗文杰, 杨鑫光, 陈炜青. 黄河首曲沙化草地恢复重建模式研究. 草业科学 , 2008, 25 (6) : 14–18. |
| [12] | 苏大学, 张自和, 陈佐忠, 胡兴宗. GB 1937-2003. 北京: 中国国家标准出版社, 2003. |
| [13] | 鲍士旦. 土壤农化分析. 北京: 中国农业出版社, 1981. |
| [14] | 许光辉, 郑洪元. 土壤微生物分析方法手册. 北京: 农业出版社, 1986. |
| [15] | 中国科学院南京土壤研究所微生物室. 土壤微生物研究法. 北京: 科学出版社, 1985. |
| [16] | 姚槐应, 黄昌勇主编. 土壤微生物生态学及其实验技术. 北京: 科学出版社, 2006. |
| [17] | 赵兰坡, 姜岩. 土壤磷酸酶测定方法探讨. 土壤通报 , 1986, 17 (3) : 138–141. |
| [18] | 关松荫. 土壤酶及其研究法. 北京: 农业出版社, 1986. |
| [19] | 安富博, 李银科, 纪永福, 唐志红, 金红喜, 赵艳丽, 肖斌. 黄河首曲高寒草甸的土壤特征及其对沙化的响应. 中国水土保持 , 2014 (12) : 48–51. |
| [20] | Hassink J, Bouwman L A, Zwart K B, Brussaard L. Relationships between habitable pore space, soil biota and mineralization rates in grassland soil. Soil Biology and Biochemistry , 1993, 25 (1) : 47–55. DOI:10.1016/0038-0717(93)90240-C |
| [21] | Foster R C. Microenvironments of soil microorganisms. Biology and Fertility of Soils , 1988, 6 (3) : 189–203. |
| [22] | 李君锋, 杨建文, 杨婷婷, 达文燕, 胡磊, 景彩虹, 姚健, 牛世全. 甘肃玛曲高寒草甸土壤微生物季节变化特征的研究. 草业科学 , 2012, 29 (2) : 189–197. |
| [23] | 胡亚林, 汪思龙, 颜绍馗. 影响土壤微生物活性与群落结构因素研究进展. 土壤通报 , 2006, 37 (1) : 170–176. |
| [24] | 林娜, 刘勇, 李国雷, 于海群. 森林土壤酶研究进展. 世界林业研究 , 2010, 23 (4) : 21–25. |
| [25] | 万忠梅, 吴景贵. 土壤酶活性对生态环境的响应研究进展. 西北农林科技大学学报 , 2009, 40 (4) : 591–596. |
| [26] | 王笛, 马风云, 姚秀粉, 辛贺, 宋雪, 张钟心. 黄河三角洲退化湿地土壤养分、微生物与土壤酶特性及其关系分析. 中国水土保持科学 , 2012, 10 (5) : 94–98. |
| [27] | 许景伟, 王卫东, 李成. 不同类型黑松混交林土壤微生物、酶及其与土壤养分关系的研究. 北京林业大学学报 , 2000, 22 (1) : 51–55. |
| [28] | Mackie A E, Wheatley R E. Effects and incidence of volatile organic compound interactions between soil bacterial and fungal isolates. Soil Biology and Biochemistry , 1999, 31 (3) : 375–385. DOI:10.1016/S0038-0717(98)00140-0 |
 2016, Vol. 36
2016, Vol. 36