文章信息
- 张婷凤, 周瑞莲, 张玥, 王艳芳, 贾有余
- ZHANG Tingfeng, ZHOU Ruilian, ZHANG Yue, WANG Yanfang, JIA Youyu.
- 冬春季海岸滨麦碳水化合物变化差异性与其环境异质性的关系
- Relationship between the changes of carbohydrate metabolism in Leymus mollis (Trin.) Hara and the environmental heterogeneties on coast during winter and spring
- 生态学报[J]. 2016, 36(16): 5182-5192
- Acta Ecologica Sinica[J]. 2016, 36(16): 5182-5192
- http://dx.doi.org/10.5846/stxb201501260207
-
文章历史
- 收稿日期: 2015-01-26
- 网络出版日期: 2015-12-01
2. 内蒙古农牧科学院资源环境与检测技术研究所, 呼和浩特 010030
2. Inner Mongolia Academy of Agriculture and Animal Husbandry Sciences and Institute of Resources Environment and Detection Technology, Hohhot 010030, China
植物均生长在环境异质的空间中,这种环境异质性给植物生长、生理、繁殖带来不可避免的影响[1]。而植物表型可塑性是植物适应环境异质性的一个潜在策略[2],也是生物体在其生长环境发生改变的条件下,可以改变其表型的一种内在能力,是物种具有更宽的生态幅和更好的耐受性的基本因素[3]。
研究发现,外来入侵种喜旱莲子草(Alternanthera philaxeroides (Mart) Griseb) 分枝强度、茎节长度随土壤氮含量升高而增加,在氮养分最高时根系生物量最低[4];日本忍冬在有支撑物的条件下,节间长度缩短了15.3%,节间数目增加了一倍,枝条的生物量增加了43%[5]。植物通过个体各器官生物量投资的优化配比来适应多样化环境,以增强其入侵能力[4-5]。有研究发现,生态因子对植物体表型可塑性影响是有针对性的,其中土壤水分主要影响植物体构件数目,土壤盐分主要影响生物量,光照条件影响植物的物候表性特征[6-8]。金戴戴随着盐分浓度的增加植株干重、总叶面积、分株数和总匍匐茎长度显著减小[8]。森林中处于竞争力强的树种遮荫下的树木,一般会积极地伸长茎或枝来决定其最佳的叶片高度,尽可能地截获光能,以达到植物的上层[9]。广幅种桃叶蓼(Polygonum persicaria)在土壤水涝胁迫时能通过快速重新调整根系使之向表土层分布以保持较高的生长速率[10]。耐阴性不同的种,其生长更直接与净同化率相关,耐阴种相对生长率、净同化率在光照条件下明显提高,但在低光照条件下没有变化,但种间可塑性差异在高营养条件下变小[10-13]。异质环境是表型可塑性产生的根源[9]。目前对植物表型可塑性研究,就试验方法而言大都采用人工控制生态因子的方法;就研究内容大多集中在植物结构特征、功能可塑性上;研究材料均采用植物的生活早期。由于可塑性响应包括环境限制对植物生长和生理的影响,目前关于植物对环境适应在生长可塑性上研究较多,而对生理可塑性研究较少。
滨麦(Leymus mollis (Trin.) Hara)是一种可在海岸不同生态断带上生存的多年生草本植物。它即可在近高潮线高盐度土壤上生存,又能在远离高潮线土壤盐度降低区域生长,但不清楚其生理可塑性调控机理。碳水化合物是植物进行各项生命活动的能源物质,参与植物形态构建,影响植株的生长[14]、作为低温保护物质与植物抗冷力相关[15-16]、作为可储存和转移的物质在植物适应逆境胁迫起关键作用[16-18]。有研究发现,假俭草[19]和多年生牧草[20] 秋季匍匐茎和根中大量积累碳水化合物是其能忍耐严寒的重要原因。那么处于不同生态断带土壤盐度、海风强度、微环境不同的滨麦在冬季越冬中,根叶碳水化合物转移和重新分配上是否有差异?这种差异在滨麦适应不同盐和海风环境中的作用,目前国内外尚未见报道。本试验以烟台不同生态断带滨麦为材料,通过对其在冬季降温和春季升温过程中,其根、茎、叶中结构和非结构碳水化合物含量的分析,以探讨气温变化过程中不同生态断带滨麦不同器官间碳水化合物含量变化与气温变化关系、不同生态断带滨麦在碳水化合物转移上表现差异性与土壤盐和海风强度的关系及它们对盐适应的生理可塑性。从碳水化合物能量的储存和转移揭示滨麦对微环境差异的适应机理。
1 材料与方法 1.1 样地自然概况试验材料来源于烟台市西泊子海岸沙地。烟台市地处山东半岛中部,位于东经119°34′—121°57′,北纬36°16′—38 °23′。该地区属于温带季风气候,年平均降水量为651.9 mm,主要集中在7 — 8月,占年降雨量的49%;年平均气温11.8 ℃,最热月为8月(24.6 ℃),历年极端最高气温38.4 ℃,土壤pH值为4.22—6.79。西泊子海岸沙地土壤多为风沙土。年平均风速内陆地区3—4 m/s,沿海地区4—6 m/s。 西泊子研究区天然群落主要有筛草(Carex kobomugi)、砂引草(Messerschmidia sibirica Linn)、肾叶打碗花(Calystegia soldanella (L.) R. Br)和滨麦(Leymus mollis (Trin.) Hara)等。
1.2 试验地和试验材料的选择试验在烟台西泊子海岸沙丘上进行。选随远离高潮线沙地地势逐渐增高、生境呈梯度变化(本文称不同生态断带)的沙丘为试验地。选不同生态断带上生长的滨麦为试验材料,各生态断带位点上滨麦均为在自然条件下生长多年而形成的自然种群,无年龄差异。具体做法是,在2013年秋季,在西泊子海岸沙丘上选植物生长健壮、无动物侵袭、无污染物侵染、无人为干扰的地段为试验地,并做标记。并将该地海岸高潮线定位0 m,将远离高潮线10 m(由于滨麦在距高潮线10m处开始出现)、30 m和50 m处设为植物和土壤样品的采集点并做标记。
1.3 试验地取样(1) 取材时间 分为晚秋、冬季和春季3个阶段。晚秋阶段气温下降迅速,故试验地取样密度加大,从2013年11月1日到11月30日,每10 d取样1次; 冬季冷冻稳定期仅在2013年12月10日和2014年1月10日取样;春季气温升高期,由于气温升高迅速,故试验地取样密度也加大,从 2014年4月1日开始,每10 d取样一次到4月30日为止。
取样方法:在每个取样位点画出一条与海平行的线,每次取样均在平行线附近并挨着顺次取样。取样具体做法是:每次在上一次取样的样地旁,用小铁锨垂直向下挖取一个约30 cm × 30cm× 30cm的土柱,同时用手将多余的沙子掏出,并小心尽量不伤及根茎。将挖出的根茎上沙子小心清理后,将整株滨麦带回实验室。每次挖取3个土柱为3个重复。在实验室小心将植株上的干枯叶片和沙子清除,然后将清理好的整株材料分为根(须根)、根茎、顶芽、叶片。具体做法:用剪刀将叶片和根部剪开,清理除去枯死叶片,剩余为叶片实验材料;接着处理根部,将根茎最前端顶部白色嫩芽(约5—7 cm)剪下,这部分为顶芽;最后用剪刀将根茎上须根剪下为根,剩余的为根茎部。将所有材料先在烘箱105 ℃杀青,然后在65 ℃烘至恒重,最后将其粉碎成粉末,用于碳水化合物含量测定。
1.4 测定方法参考张志良版的《植物生理学实验指导》[21] 测定碳水化合物的方法,对滨麦可溶性糖,淀粉,纤维素进行测定。每次测定重复3次。淀粉含量测定是将提取过可溶性糖的残渣先用高氯酸水解后用蒽酮比色法进行测定,纤维素含量的测定是将提取过淀粉的残渣用硫酸水解后用蒽酮比色法进行测定。
1.5 数据处理用Microsoft Office Excel 2003对数据进行处理并作图。实验数据3个以上重复的平均值±标准差(mean±SD,standard deviation)。
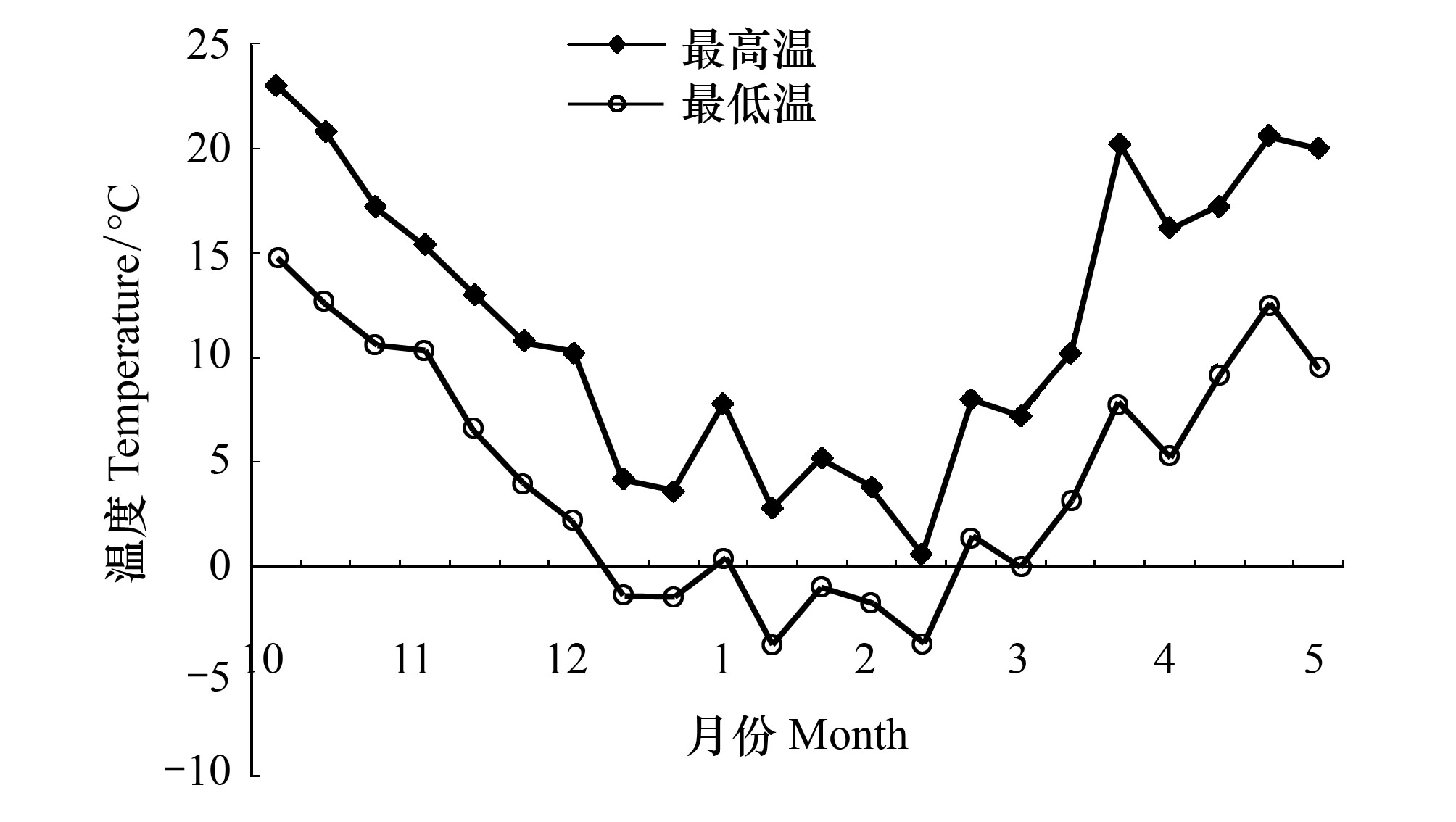
2 结果与分析 2.1 2013秋季到2014春季气温变化可以将晚秋冬季和春季气温变化分为3个阶段(图 1)。第1阶段晚秋入冬,气温下降期,从10月底到12月,这时最高平均气温由10月底的20 ℃降至12月的4 ℃,但最低气温均在零度以上;第2阶段冬季,气温持续冷冻期,从2013年12月到2014年 2月间,3个月最高平均气温均保持约4 ℃,最低温度在零下3 ℃; 第3阶段春季,气温上升阶段,自3月初气温快速上升,3月最高平均气温上升到13 ℃,4月升高至19 ℃,3月最低平均气温也上升至5 ℃,4月升至10 ℃。烟台海岸晚秋冬春季气温变化明显,季节分明。
|
| 图 1 2013秋冬—2014春季最高和最低气温变化 Fig. 1 Changes in maximum and minimum temperature from winter,2013 to spring,2014 |
在距高潮线10、30、50 m处的滨麦形态有较明显差异(表 1)。近高潮线(10 m)沙地较为湿润、风力较大、日平均气温较低,滨麦植株低矮、根茎肥硕且在沙下约20 cm,须根也较粗壮。在距高潮线30 m处,沙地平缓、沙地湿度降低、风力减小、滨麦植株较高、根茎较细且位于沙下10—15 cm,须根也较细。在距高潮线50 m处,沙地较为干旱、风力较小,滨麦种群密度增大、植株最高、根茎干细,节间特别明显,须根细长。研究表明,随远离高潮线土壤湿度降低、土壤盐度下降、海风风力减小,滨麦生长势加大、根系发育变弱,滨麦形态可塑性与环境变化相关。
| 距高潮线距离/m Distance from high tide line | 月份 Month | 温度/℃Temperature | 湿度/%Huminity | 风速/(m/s)Wind rate | 株高/cmPlant height | ||||||
| 早 | 中 | 晚 | 早 | 中 | 晚 | 早 | 中 | 晚 | |||
| 10 | 7 | 35.4 | 42.8 | 36.5 | 45.7 | 57.8 | 48.8 | 1.9 | 1.7 | 1.1 | 43.8±7.5 |
| 9 | 24.5 | 31.9 | 23.2 | 61.4 | 39.1 | 78.5 | 1.3 | 1.9 | 3.1 | ||
| 30 | 7 | 34.7 | 45.3 | 36.6 | 50.2 | 50.1 | 49.4 | 1.6 | 1.1 | 0.6 | 44.6±6.2 |
| 9 | 28.3 | 38.3 | 24.3 | 52.5 | 28.4 | 73.8 | 0.7 | 1.8 | 2.2 | ||
| 50 | 7 | 38.7 | 45.7 | 37.1 | 37.5 | 48.9 | 46.5 | 0.4 | 0.8 | 0.5 | 58.8±10.7 |
| 9 | 27.8 | 41.5 | 51.6 | 51.6 | 25.8 | 76.5 | 0.3 | 1.3 | 1.1 | ||
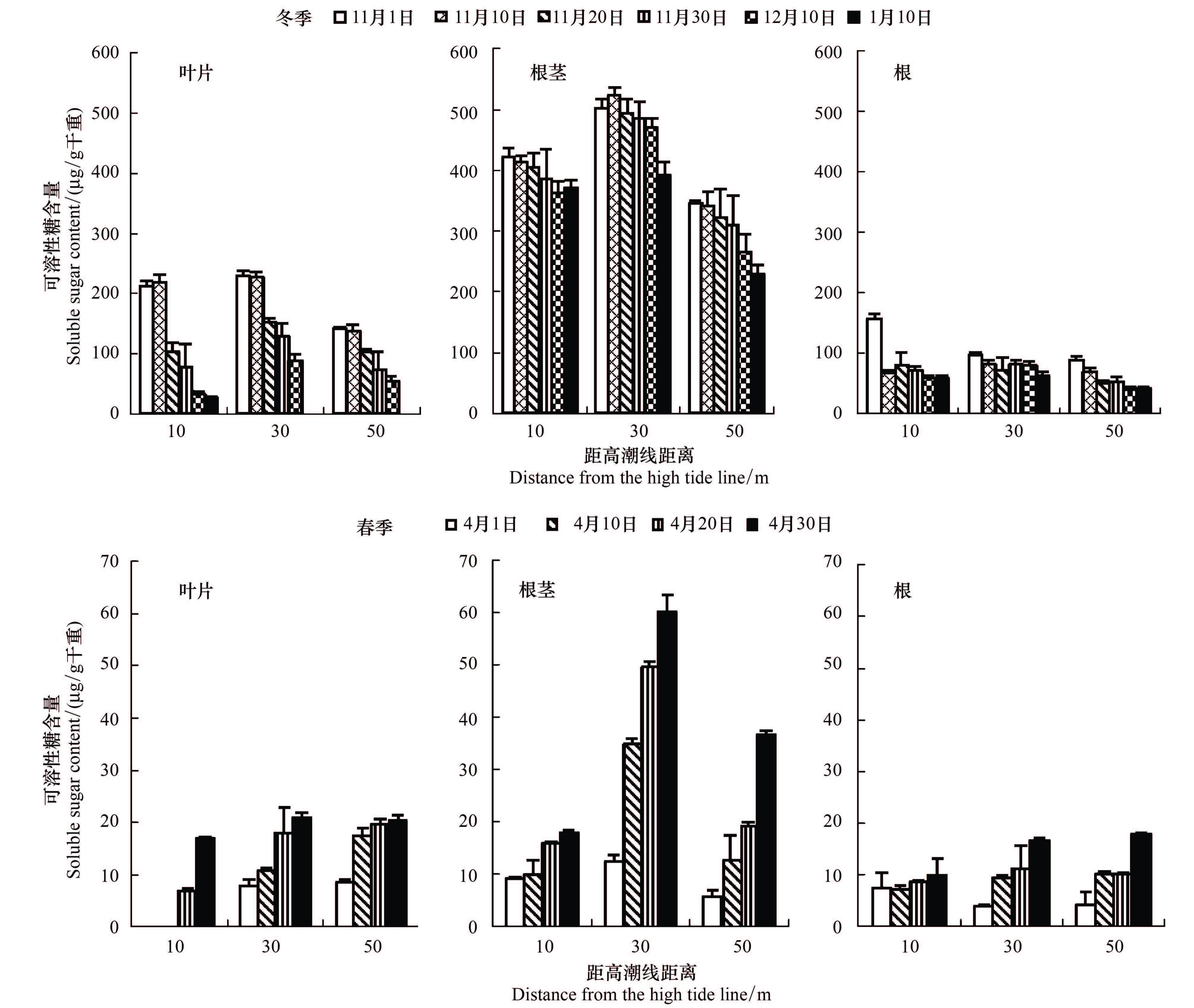
烟台海岸冬初地上叶片开始枯黄,而在入秋地下根茎顶部开始膨胀形成大量白色稚嫩的芽,并在春季气温上升向上生长形成新的植株。研究表明,在入冬、冬季和春季不仅不同生态断带滨麦可溶性糖含量不同,而且随温度的变化滨麦各器官可溶性糖含量也不相同(图 2)。
|
| 图 2 冬春季不同生态断带滨麦叶片和地下各器官可溶性糖含量变化 Fig. 2 Changes in the contents of soluble sugar in the leaves and different parts of roots of Leymus mollis growing on coastal dunes at different zone far from the high tide in winter,and spring |
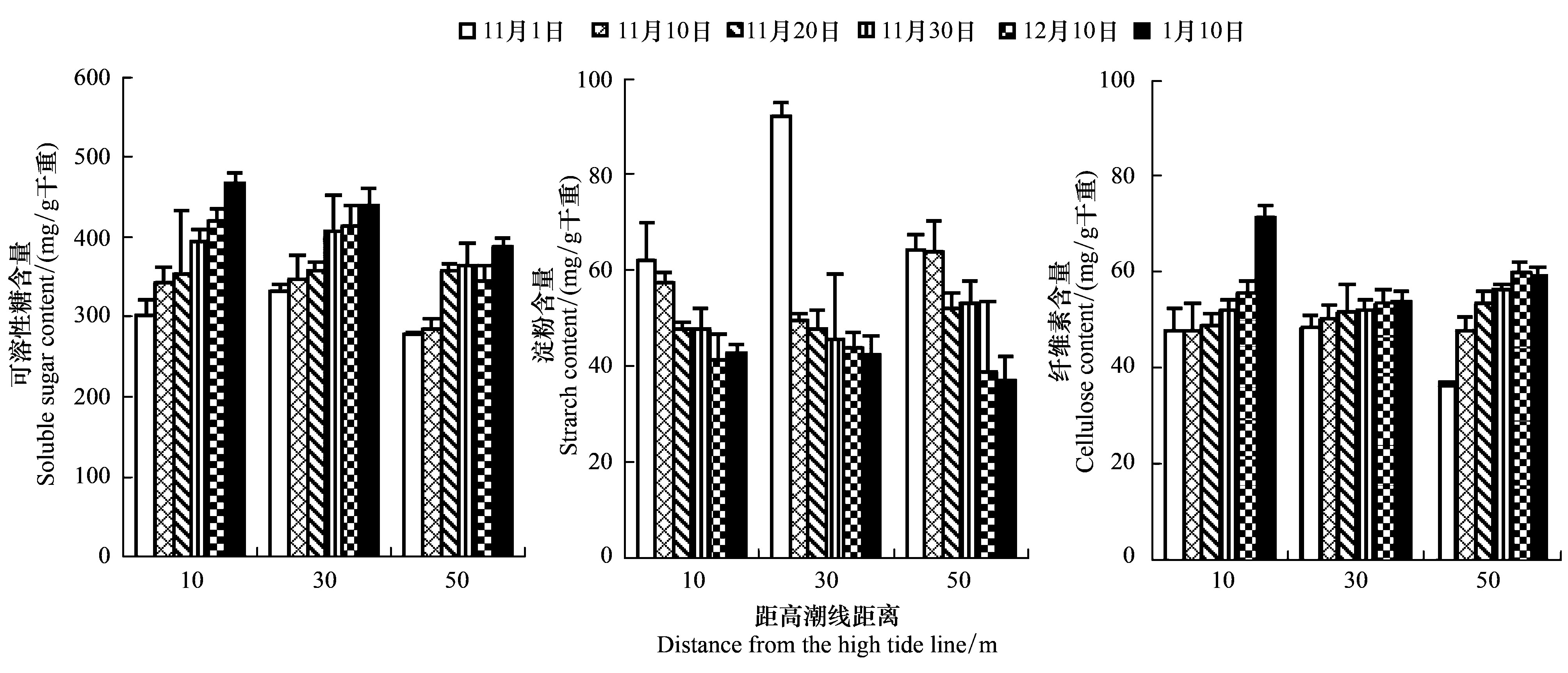
晚秋随气温下降,不同生态断带地上叶片开始变黄,叶中可溶性糖含量大幅度下降。在距高潮线10、30、50 m处的滨麦叶片可溶性糖含量在降温期分别下降64%、44% 和48%; 在冷冻期分别降低65%、31% 和26%。 同时,随气温降低滨麦地下部(根+根茎+芽)总可溶性糖含量趋于增加(图 2,图 3),在11月底达到最高值,但增加幅度不大。然而,地下不同器官可溶性糖含量变化不同。 随气温下降顶芽和根茎可溶性糖含量趋于上升,位于10、30、50 m处滨麦芽中可溶性糖含量在降温期分别增加了30%、22% 和31%,在冷冻期增加19%、 8% 和6%; 根茎中可溶性糖含量趋于缓慢下降,在降温期和冷冻期,10、30、50 m仅分别下降12%、22% 和35%;不同生态断带根中糖含量变化不明显(图 2)。然而冬季位于50 m处的滨麦,其芽、根茎、根和叶片中可溶性糖含量均最低,并与10 m和30 m的差异显著(P<0.05)(图 2,图 3)。 就同一植株,滨麦将大量可溶性糖储存在芽和根茎中,例如在30 m处滨麦芽和根茎中可溶性糖含量分别较根高384%和505%。
|
| 图 3 冬季不同生态断带滨麦芽中可溶性糖、淀粉和纤维素含量的变化 Fig. 3 Changes in the contents of soluble sugar,starch,and cellulose in the buds of Leymus mollis growing on coastal dunes at different zone far from the high tide during winter |
随春季气温增高(图 1),不同生态断带滨麦开始返青,但50m处滨麦返青较早,10 m处滨麦返青较晚。随着植株萌动生长,不同生态断带滨麦地下和地上部可溶性糖含量均增高,但绝对量上仍以30 m和50 m处滨麦较高(图 2)。
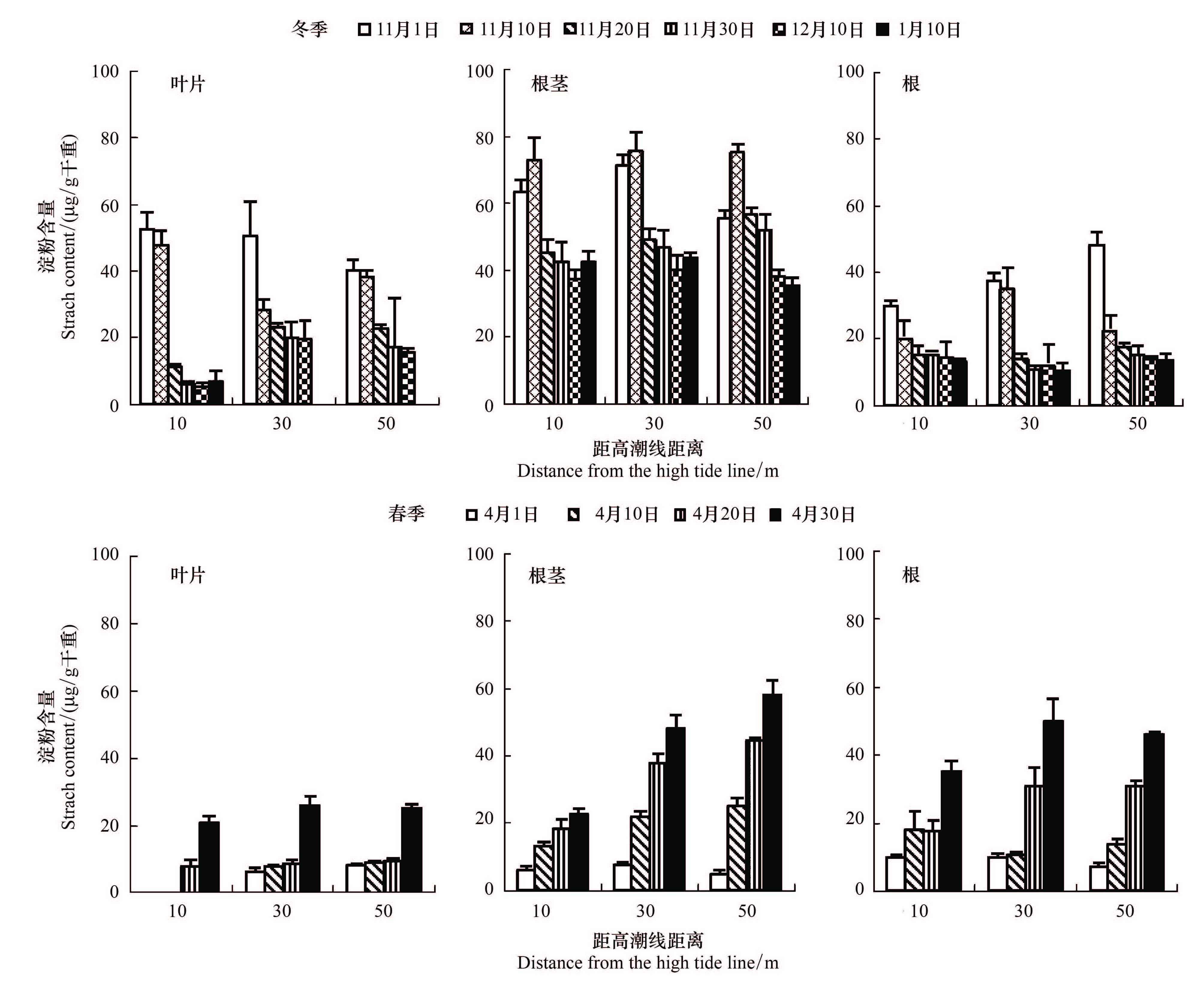
2.4 不同生态断带滨麦各部位淀粉含量变化研究表明,在入冬、冬季和春季不仅不同生态断带滨麦淀粉含量不同,而且随温度的变化各器官淀粉含量也不相同(图 3,图 4)。晚秋随气温下降,地上叶片开始变黄,地上叶片淀粉含量大幅度下降,在降温期下降幅度最大,冷冻期下降幅度减小。不同生态断带上,10 m处滨麦叶片淀粉降幅(87%)明显高于30 m(60%)和50 m(61%)。同时,随晚秋气温下降,不同生态断带滨麦地下部(根+根茎+芽)平均淀粉含量差异不显著,但均趋于下降(图 3,图 4)。值得注意的是,不同生态断带滨麦地下部淀粉含量变化时间上略有差异,位于50 m处的滨麦芽和根茎淀粉含量在降温期下降幅度略低于30 m和10 m,但在冷冻期芽和根茎中淀粉含量下降幅度(30%、32%)明显大于30 m(7%、7.2%)和10 m(10%、1%)。冬季滨麦将大量淀粉储存在芽和根茎中,例如在30 m处滨麦芽和根茎中淀粉含量较根高170%和175%。
|
| 图 4 冬春季不同生态断带滨麦叶片和地下各器官淀粉含量变化 Fig. 4 Changes in the starch content in the leaves and different parts of roots of Leymus mollis growing on coastal dunes at different zone far from the high tide in winter,and spring |
随春季气温增高(图 1),滨麦返青生长,地上叶片和地下部各器官淀粉含量迅速增高,尤其根茎增长显著(图 4)。不同生态断带地上叶片淀粉含量平均增加2—3倍,地下根茎平均增加4—5倍。但不同生态断带滨麦地上和地下积累量有差异,10 m处滨麦地上叶片因生长略晚淀粉积累较晚,但积累迅速;30 m和50 m处滨麦返青早,地下根茎中淀粉积累量较高。不同生态断带滨麦根茎中淀粉含量最高,10、30、50 m处滨麦根茎中淀粉含量分别较根高50%、127%、170%。研究表明,生长中的滨麦会将较多的淀粉储存在根茎中。
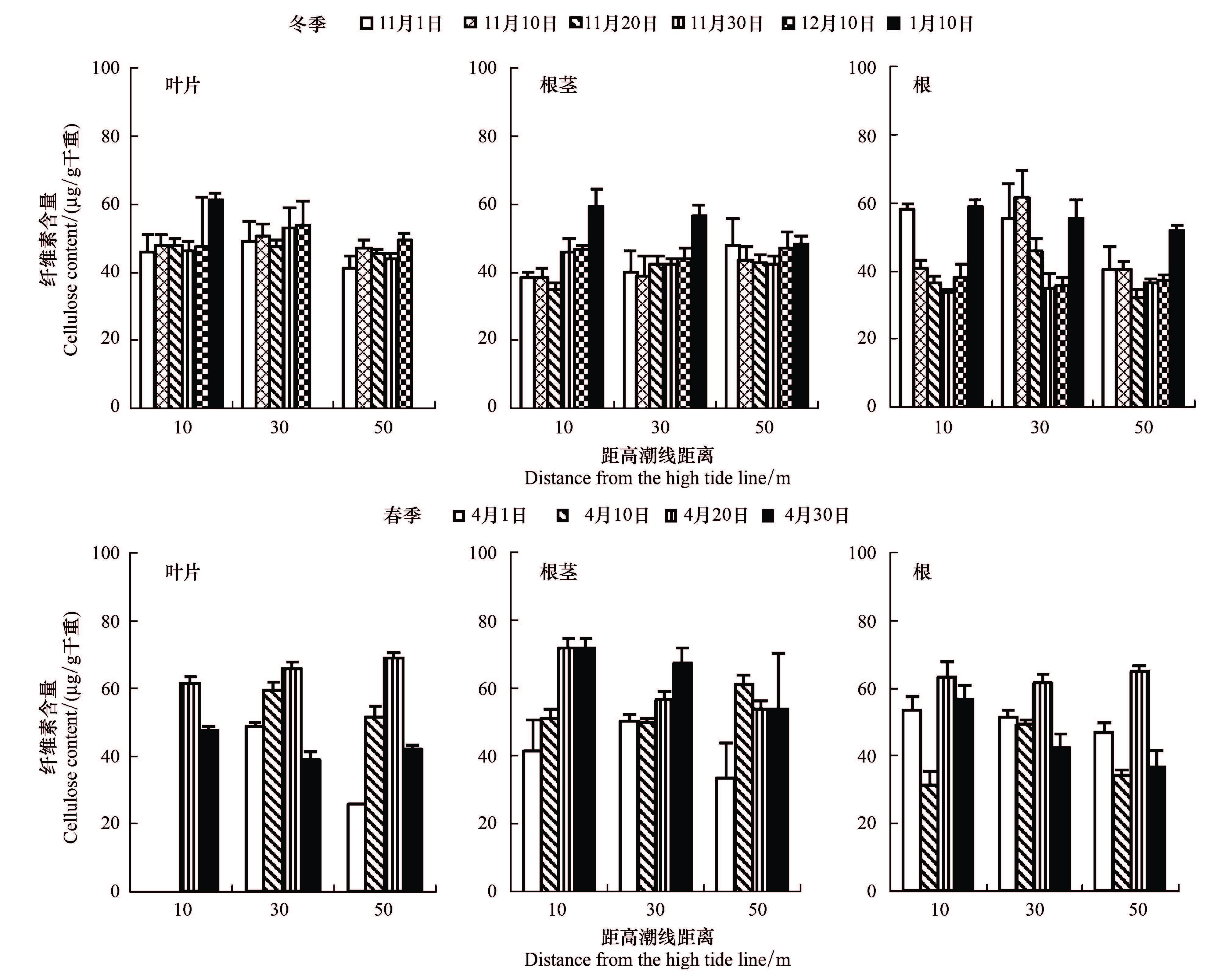
2.5 不同生态断带滨麦各部位纤维素含量变化研究表明,在降温期、冷冻期和春季升温过程中不同生态断带滨麦地上和地下器官中纤维素含量均发生不同变化(图 3,图 5)。在晚秋随叶片开始变黄,叶片中纤维素含量略有增加,在降温期和冷冻期,位于10、30、50 m的滨麦叶片中纤维素含量分别增加33%、10%、20%,其中10 m处滨麦叶片纤维素含量增加幅度较大,且绝对含量高于50 m 处滨麦(图 5)。
|
| 图 5 冬春季不同生态断带滨麦叶片和地下各器官纤维素含量变化 Fig. 5 Changes in the cellulose content in the leaves and different parts of roots of Leymus mollis growing on coastal dunes at different zone far from the high tide in winter,and spring |
随气温下降不同生态断带滨麦地下部纤维素含量在降温期趋于缓慢下降,在冷冻期增加,但不同生态断带滨麦地下部纤维素含量的变化幅度不同(图 3,图 5)。其中,10 m处滨麦地下部纤维素含量在降温期下降(10%),在冷冻期大幅增加(44%)。而50 m处滨麦在降温期变化不明显,在冷冻期增加(18%),但其增幅低于10 m处滨麦。地下部各器官纤维素含量在降温期变化略有不同。在降温期根中纤维素含量下降,芽和根茎中纤维素含量增加。而且,不同生态断带滨麦地下部纤维素对降温和冷冻期响应不同,10 m处滨麦芽和根茎中纤维素含量在降温期增幅较小(9%,19%),冷冻期增幅较大(38%,30%),50 m处的滨麦芽纤维素在降温期增幅较大(55%),冷冻期增幅较小。
随春季气温升高,不同生态断带滨麦地上部和地下部纤维素对温度变化响应一致,均在生长初期上升,在快速生长期降低(图 5)。其中10 m滨麦地上和地下部纤维素含量和增加幅度均高于远离高潮线滨麦,两者差异显著(P<0.05)。
3 讨论与结论结果表明,海岸不同生态断带滨麦生活在异质环境中(表 1),随远离高潮线土壤盐度下降,滨麦地下根茎和芽由粗壮变细小、地上枝叶由低矮变细长。不同生态断带滨麦形态可塑性差异与环境异质性相关。这不仅表明滨麦具有很大的生态幅,还说明其有很强的适应和利用环境维持最大生产量的能力。滨麦是多年生植物,成功越冬是其延续生存的关键。大量研究表明,碳水化合物是植物越冬的主要能源物质[22-23]。尽管不同生态断带滨麦在形态可塑性上存在差异,那么滨麦在冬季越冬体内碳水化合物转移和转化分配上是否存在差异呢?以及形态可塑性和生理可塑性间是否有密切关系,目前尚不清楚。
结果表明,随晚秋气温下降,不同生态断带滨麦地上叶片平均可溶性糖含量大幅度下降,而地下部(根+根茎+芽)总可溶性糖含量增加了12.4%(图 2,图 3)。同时,在降温期不同生态断带地上叶片淀粉平均含量下降幅度(69%)大于地下部(36%),在冷冻期,无论地上还是地下部淀粉含量下降幅度减小(图 3,图 4)。随春季气温增高(图 1),滨麦萌动生长,地上和地下部根茎中淀粉含量迅速增高(图 4)。这是由于大多数多年生草本植物生活型为地面芽植物,其越冬的生长点位于地下,它们通过在冬季来临前,将地上叶片储存的养分转移至地下根部,以叶片枯死减少养分消耗这种逃避方式越过寒冷的冬季。所以秋季降温成了这种物质转移的信号。转移到地下根际的非结构性碳水化合物在维护根际细胞渗透势、持水力、根际细胞呼吸代谢、春季的返青生长有重要作用[24]。
另外,滨麦的地下器官包括:根茎、芽、根。但研究发现入冬滨麦非结构碳水化合物的转移在地下各器官间不均衡,而且地下各器官中结构性碳水化合物变化不同。例如,首先随气温下降,顶芽可溶性糖平均含量趋于上升(降温期平均增加28%,在冷冻期增加了11%)、同时淀粉下降(30%、16%)、纤维素含量增加(24%、15%)(图 3);而根茎可溶性糖(10%、16%)和淀粉(32%、13%)下降和纤维素含量增加(图 2,图 4,图 5)。但是就地下各器官结构和非结构碳水化合物绝对值而言,芽和根茎中可溶性糖含量较高,根中较低(图 2,图 3),芽、根茎和根可溶性糖分别占地下部器官总糖的44%、47%和9%; 淀粉占地下部器官总淀粉的42%、42%和16%;纤维素占地下部器官总纤维素的37%、32%、31%。研究表明,(1)冬季地下芽和根茎是非结构性碳水化合物的“库”,是碳水化合物的主要贮藏部位[25]。有研究发现,根茎型的羊草以无性克隆生长为主,每年将大量的营养物质贮存在根茎等地下器官中,以利于繁殖和种群扩张生长[26]。越冬的紫花苜蓿地下根茎粗度、体内营养物质的积累量与根茎耐寒力和越冬力呈正相关[27]。滨麦属于根茎型多年生牧草,其地下部分包括芽、根茎和不定根。其中,根茎顶部芽是分生组织具有持续的强烈分裂的能力,这里既是植物芽产生的部位,也是未来枝叶和植物继续生存的保证。因此将较多的非结构性碳水化合物转移至此在提高该组织抗冻力、维护其安全越冬和再生是十分重要的,也是其成为入冬后营养“库”端的原因。而地下根茎是不定根和地上枝条产生的部位也是植株持续生活的载体,故可能成为第2个营养输入的“库”。在冬季冷冻期芽中可溶性糖增加,而根茎中可溶性糖和淀粉含量均趋于下降,这进一步表明根茎中可溶性糖和淀粉向芽转移。根茎顶部的芽是滨麦越冬生存的重要部位,是营养输送的重要“库”,其“库”中非结构碳水化合物作为渗透调节物质可增加细胞浓度、降低冰点、维护细胞水分;作为营养物质为地下芽和根茎呼吸提供能量[15, 28-29]。(2)地下器官间结构和非结构碳水化合物间发生转移和转化。不仅根茎和根中可溶性糖向顶芽转移,而且该部位的淀粉下降。淀粉的下降可能一部分转化为可溶性糖用于呼吸、渗透调节,另外合成纤维素用于增加芽和根茎机械能力以利于其在土壤中穿行和种群的扩展。为此,入秋气温下降时,滨麦通过将地上部叶中非结构碳水化合物向生命活跃的芽和根茎中转运为冬季海岸滨麦安全越冬提供了物质保障。
本研究还发现,不同生态断带环境影响海岸滨麦非碳水化合物在地上地下转移和结构和非结构碳水化合物转化。生活在近高潮线10 m处的滨麦,冬季地上非结构性碳水化合物转移地下较早,地下部储存了较多的非结构碳水化合物,春季返青晚,根叶中积累较多的结构性碳水化合物。而生活在远离高潮线50 m处的滨麦,冬季转移到地下部芽、根茎、根中的可溶性糖均较少(图 2,图 3),滨麦芽和根茎淀粉含量在冷冻期下降幅度大,而10 m和30 m处则在低温期下降幅度大。在春季50 m处滨麦生长返青较早,滨麦叶片和地下部非结构性碳水化合物含量较高(图 2,图 4),纤维素含量较低(图 5)。结果表明:不同生态断带滨麦碳水化合物转移存在的差异。有研究发现,植物的养分含量即受自身生理特性作用,又受生长地环境条件的制约。其中生态过程决定着植物体内物质和能量的转化[30-31]。长期生活在低温环境的植物进化出一系列适应机制,其中包括降低结构性碳水化合物含量并提高可溶性碳水化合物含量,而较温暖的地区则相反[32-33]。而且有研究发现,随着草地产草量的增加,粗纤维含量上升[34-35]。在海岸近高潮线处土壤Na+含量很高,此处生长的滨麦根叶中Na+较高,而且可溶性糖含量也较高[36-37]。随着植物生长和干物质的不断积累,机械组织不断增长导致机械组织中纤维素含量较多[38]。本实验中,近高潮线10 m处的滨麦是生活在迎风坡上,这里海风强度高、土壤盐浓度高、相对温度较低(表 1)。因而在冬季较早地将地上叶片中非结构性碳水化合物养分转移至地下器官并储存起来,并将其主要转运到与繁殖生长相关的地下根茎和芽中导致地下根茎和芽粗壮。而大量非结构碳水化合物在其提高细胞持水力、降低冰点、作为渗透调节剂维护地下器官的水分平衡起重要作用;同时维持较高的淀粉含量和稳定的纤维素为地下器官冬季呼吸消耗提供能源,提高其抗冻力和耐盐性。在春季由于受海风和气温较低影响而返青生长较晚。但在返青生长后,其叶片将大量可溶性糖和淀粉用于纤维素合成可能是导致非结构性碳水化合物含量较低的原因,而叶片中较高的纤维素含量在增强叶片机械组织提高其抗风能力是有利的。因此在10 m处生长的滨麦冬季维持地下部较高的可溶性糖,春季返青叶片中维持较高的纤维素含量与其抗冻、抗盐、抗风密切相关。随着远离高潮线,海风风力减小、地势平坦、温度提高,生长在50 m处的滨麦晚秋生活期略有加长,不仅冬季地上非结构碳水化合物向地下转移的晚,并且储存量较低,导致根茎细长,芽短而细,且春季返青生长较早使叶片和地下部非结构碳水化合物含量较高。50 m处生长的滨麦冬季地下部较少的可溶性糖含量与土壤较低的盐度呈正相关,春季返青早也与微环境温度较10 m高有关。由此可见,在越冬和返青生长过程中,不同生态断带滨麦地上和地下部非结构碳水化合物转移和转化上的差异与其适应异质环境、维持较高的生态幅和形成多抗逆性有关。
综上所述,生活在海岸带的滨麦主要是通过营养繁殖扩大种群,其地下根茎的延伸生长在维持植物的延续生长中起重要作用。在冬季不同生态断带滨麦随温度降低将大量非结构性碳水化合物转移至地下繁殖器官根茎和芽中以维持其渗透势和水分平衡,淀粉和纤维素为越冬呼吸消耗提供能量而在越冬生存中起重要作用。但处于高盐土壤和受海风影响大的近高潮线滨麦冬季较早地将可溶性糖转移至地下器官,并维持地下部较高的可溶性糖,春季返青叶片中维持较高的纤维素含量与其抗冻、抗盐、抗风密切相关。而生活在远离高潮线土壤盐度低、海风强度变小环境的滨麦(50 m处),冬季地下部较少的可溶性糖含量与土壤较低的盐度呈正相关,春季返青早也与微环境温度较高有关。因此,而不同生态断带滨麦冬季地下部非结构性碳水化合物储存量的多寡和春季叶片结构性碳水化合量的多少与其生活环境的异质性相关。滨麦较强的生理可塑性可能是其可适应不同盐度土壤、不同海风风力、不同温度环境而具有抗盐耐风沙和较大生态幅的关键。 为此,滨麦较大的生理可塑性为其开发利用提供了可能性,也为提高其生产力制定合理的耕作措施提供了依据。
| [1] | Hutchings M J, De Kroom H. Foraging in plants the role of morphological plasticity in resource acquisition. Advances in Ecological Research , 1994, 25 (1) : 159–238. |
| [2] | Poor A, Hershock C, Rosella K, Goldberg D E. Do physiological integration and soil heterogeneity influence the clonal growth and foraging of Schoenoplectus pungens?. Plant Ecology , 2005, 181 (1) : 45–56. DOI:10.1007/s11258-005-2429-y |
| [3] | Zhai Y, Lv Y F, Li X, Wu W M, Bo W H, Shen D F, Xu F, Pang X M, Zheng B S, Wu R L. A synthetic framework for modeling the genetic basis of phenotypic plasticity and its costs. New Phytologist , 2014, 201 (1) : 357–365. DOI:10.1111/nph.12458 |
| [4] | 许凯扬, 叶万辉, 李静, 李国民. 入侵种喜旱莲子草对土壤养分的表型可塑性反应. 生态环境 , 2005, 14 (5) : 723–726. |
| [5] | 耿宇鹏, 张文驹, 李博, 陈家宽. 表型可塑性与外来植物的入侵能力. 生物多样性 , 2004, 12 (4) : 447455. |
| [6] | 申时才, 徐高峰, 李天林, 张付斗, 张玉华. 5种入侵植物补偿反应及其形态可塑性比较. 西北植物学报 , 2012, 32 (1) : 173–179. |
| [7] | 郭立冬, 何兴东. 不同气温与土壤湿度条件下籽蒿幼苗的表型可塑性. 中国沙漠 , 2011, 31 (4) : 987–991. |
| [8] | 于海飞, 董鸣, 张称意, 张淑敏. 匍匐茎草本金戴戴对基质盐分含量的表型可塑性. 植物生态学报 , 2002, 26 (2) : 140–148. |
| [9] | 胡启鹏, 郭志华, 李春燕, 马履一. 植物表型可塑性对非生物环境因子的响应研究进展. 林业科学 , 2008, 44 (5) : 135–142. |
| [10] | Bell D L, Sultan S E. Dynamic phenotypic plasticity for root growth in Polygonum: a comparative study. American Journal of Botany , 1999, 86 (6) : 807–819. DOI:10.2307/2656702 |
| [11] | Portsmuth A, Niinemets V. Structural and physiological plasticity in response to light and nutrients in five temperate deciduous woody species of contrasting shade tolerance. Functional Ecology , 2007, 21 (1) : 61–77. |
| [12] | Niinemets V. Photosynthesis and resource distribution through plant canopies. Plant, Cell and Environment , 2007, 30 (9) : 1052–1071. DOI:10.1111/pce.2007.30.issue-9 |
| [13] | 张治安, 杨福, 陈展宇, 徐克章. 菰叶片净光合速率日变化及其与环境因子的相互关系. 中国农业科学 , 2006, 39 (3) : 502–509. |
| [14] | Loewe A, Elinig W, Shi L B, Dizengremel P, Hampp R. Mycorrhiza formation and elevated CO2 both increase the capacity for sucrose synthesis in source leaves of spruce and aspen. New Phytologist , 2000, 145 (3) : 565–574. DOI:10.1046/j.1469-8137.2000.00598.x |
| [15] | 周瑞莲, 张普金. 春季高寒草地牧草根中营养物质含量和保护酶活性的变化及其生态适应性研究. 生态学报 , 1999, 16 (4) : 402–407. |
| [16] | 江志坚, 黄小平, 张景平. 环境胁迫对海草非结构性碳水化合物储存和转移的影响. 生态学报 , 2012, 32 (19) : 6242–6250. |
| [17] | Turner L R, Donaghy D J, Lane P A, Rawnsley R P. Patterns of leaf and root regrowth, and allocation of water-soluble carbohydrate reserves following defoliation of plants of prairie grass (Bromus willdenowii Kunth.).. Grass and Forage Science , 2007, 62 (4) : 497–506. DOI:10.1111/gfs.2007.62.issue-4 |
| [18] | Alcoverro T, Zimmerman R C, Kohrs D G, Alberte R S. Resource allocation and sucrose mobilization in light-limited eelgrass Zostera marina. Marine Ecology Progress Series , 1999, 187 : 121–131. DOI:10.3354/meps187121 |
| [19] | Cai Q S, Wang S Z, Cui Z P, Sun J H, Ishii Y. Changes in freezing tolerance and its relationship with the contents of carbohydrates and proline in overwintering centipedegrass (Eremochloa ophiuroides (munro) hack.).. Plant Production Science , 2004, 7 (4) : 421–426. DOI:10.1626/pps.7.421 |
| [20] | Gaudet D A, Laroche A, Yoshida M. Low temperature wheat fungal interactions: A carbohydrate connection. Physiologia Plantarum , 1999, 106 (4) : 437–444. DOI:10.1034/j.1399-3054.1999.106412.x |
| [21] | 张志良, 瞿伟菁. 植物生理学实验指导 (第三版). 北京: 高等教育出版社, 2003127–133. |
| [22] | 潘庆民, 白永飞, 韩兴国, 杨景成. 植物非结构性贮藏碳水化合物的生理生态学研究进展. 植物学通报 , 2002, 19 (1) : 30–38. |
| [23] | 高英志, 王艳华, 王静婷, 刘鞠善, 王德利. 草原植物碳水化合物对环境胁迫响应研究进展. 应用生态学报 , 2009, 20 (11) : 2827–2831. |
| [24] | Shi C G, Silva L C R, Zhang H X, Zheng Q Y, Xiao B X, Wu N, Sun G. Climate warming alters nitrogen dynamics and total non-structural carbohydrate accumulations of perennial herbs of distinctive functional groups during the plant senescence in autumn in an alpine meadow of the Tibetan Plateau, China. Agricultural and Forest Meteorology , 2015, 200 : 21–29. DOI:10.1016/j.agrformet.2014.09.006 |
| [25] | 白永飞, 许志信, 段淳清, 李德新. 典型草原主要牧草植株贮藏碳水化合物分布部位的研究. 中国草地 , 1996 (1) : 7–9. |
| [26] | 张光辉, 李增嘉, 潘庆民, 宁堂原, 杨景成. 内蒙古典型草原羊草和大针茅地下器官中碳水化合物含量的季节性变化. 草业学报 , 2006, 15 (3) : 42–49. |
| [27] | 孙启忠, 王育青, 侯向阳. 紫花苜蓿越冬性研究概述. 草业学报 , 2004, 21 (3) : 21–25. |
| [28] | 周瑞莲, 赵哈林. 高寒山区牧草生长过程中低温保护物质的作用. 中国草地 , 2001, 23 (5) : 19–26. |
| [29] | 周瑞莲, 赵哈林. 春季高寒山区牧草低温保护物质变化与其脱冻适应间系研究. 西北植物学报 , 2004, 24 (2) : 199–204. |
| [30] | Aerts R, Chapin F S Ⅲ. The mineral nutrition of wild plants revisited: a re-evaluation of processes and patterns. Advances in Ecological Research , 1999, 30 : 1–67. DOI:10.1016/S0065-2504(08)60016-1 |
| [31] | Kerkhoff A J, Fagan W F, Elser J J, Enquist B J. Phylogenetic and growth form variation in the scaling of nitrogen and phosphorus in the seed plants. The American Naturalist , 2006, 168 (4) : E103–E122. DOI:10.1086/507879 |
| [32] | Xu S X, Zhao X Q, Sun P, Zhao T B, Zhao W, Xue B. A simulative study on effects of climate warming on nutrient contents and in vitro digestibility of herbage grown in Qinghai-Xizang Plateau. Acta Botanica Sinica , 2002, 44 (11) : 1357–1364. |
| [33] | Körner C. Alpine Plant Life: Functional Plant Ecology of High Mountain Ecosystems. Berlin: Springer-Verlag, 2003. |
| [34] | Surprenant J, Barnes D K, Busch R H, Marten G C. Bidirectional selection for neutral detergent fiber and yield in reed canarygrass. Canadian Journal of Plant Science , 1988, 68 (3) : 705–712. DOI:10.4141/cjps88-083 |
| [35] | Cusicanqui J A, Lauer J G. Plant density and hybrid influence on corn forage yield and quality. Agronomy Journal , 1999, 91 (6) : 911–915. DOI:10.2134/agronj1999.916911x |
| [36] | 周瑞莲, 王相文, 左进城, 杨润亚, 黄清荣, 刘怡. 海岸不同生态断带植物根叶抗逆生理变化与其Na+含量的关系. 生态学报 , 2015 . DOI:10.5846/stxb201310032406 |
| [37] | Zhang J X, Nguyen H T, Blum A. Genetic analysis of osmotic adjustment in crop plants. Journal of Experimental Botany , 1999, 50 (332) : 291–302. DOI:10.1093/jxb/50.332.291 |
| [38] | Niklas K J. Plant allometry, leaf nitrogen and phosphorus stoichiometry, and interspecific trends in annual growth rates. Annals of Botany , 2006, 97 (2) : 155–163. |
 2016, Vol. 36
2016, Vol. 36