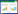文章信息
- 易科浪, 代志刚, 刘碧云, 蔺庆伟, 曾磊, 徐栋, 贺锋, 吴振斌
- YI Kelang, DAI Zhigang, LIU Biyun, LIN Qingwei, ZENG Lei, XU Dong, HE Feng, WU Zhenbin.
- 空间层次及人工基质对着生藻类建群特性的影响
- Effects of vertical location and artificial substrate on colonization of algal periphyton
- 生态学报[J]. 2016, 36(15): 4864-4872
- Acta Ecologica Sinica[J]. 2016, 36(15): 4864-4872
- http://dx.doi.org/10.5846/stxb201501060033
-
文章历史
- 收稿日期: 2015-01-06
- 网络出版日期: 2015-11-16
2. 中国科学院大学, 北京 100049;
3. 河南师范大学, 新乡 453007
2. University of Chinese Academy of Sciences, Beijing 100049, China;
3. College of Life Sciences, Henan Normal University, Xinxiang 453007, China
着生藻类(Periphytic algae)是指生长在水下各种基质表面上的所有藻类[1],当其进入到一个新的空间,着生藻类便开始定居、建群,发展成为成熟的群落[2],其群落在水下基质表面呈絮状、丝状或为一层粘质、褐绿色的藻垫[3]。着生藻类建群是一个复杂过程,可以在短时间内能获得大量的群落结构和演替特征等方面信息,因此着生藻类建群过程得到了水生态学者的广泛关注[4-6]。
着生基质是着生藻类开始群落的第一步,Cattanoe等通过检阅16年来20家期刊,发现有27种基质用于定量比较研究[7]。由于缺少标准方法,天然基质上的着生藻类群落研究受到了一定程度的限制,后期研究者更多利用具有标准采样面积和可知的采样时间的人工基质替代天然基质[7]。载玻片是早期使用最频繁的人工基质,后期如瓷砖、人工水草、花岗岩、塑料等材料也逐渐兴起[8-10]。但是由于研究目的、环境等方面不同,目前有关不同基质着生藻类群落的生长状况也没有一致结论。
前期研究表明,着生藻类在建群早期的群落一般以硅藻为主,因此有关着生藻类的研究多集中在对硅藻的分析上[11-12],而忽略了建群后期对其他类型藻类研究[13]。Cattanoe等[7]研究显示在着生藻建群60d时,绿藻占了67%,蓝藻占40%,显然短时间建群中绿藻和蓝藻所产生的作用和能力可能被低估。在着生藻类的空间着生特点方面,国内外相关研究也较少,一般是将着生基质至于水体底部,在国内,兰波在研究洱海着生藻类时进行了0、0.5、1、1.5 m等4个不同的设置[14];王丽卿等在淀山湖生态示范区的附着藻类的研究中,进行0.1、0.5、1.0、1.5 m等4个水层的研究[15]。
杭州西湖是中国主要的观赏性淡水湖泊,属于半封闭性水体,营养负荷重,自净能力弱,加上周围旅游、经济的迅速发展,致使营养物质大量积累,引起着生藻类疯长,有的区域出现“水华”现象[16]。有些着生丝状藻类的存在会通过物理缠绕、营养竞争、遮光、化感等作用影响高等水生植物的生长[17]。因此研究着生藻类在富营养化水体中不同空间层次及不同人工基质上的分布规律,揭示其着生藻类水华形成具有重要意义。
本研究选择西湖钱塘江引水玉皇山预处理场中丝状藻类爆发的生态塘作为实验水体,将两种粗糙度不同的石质材料花岗岩和瓷砖分别置于水体不同水层中进行附着,以期了解附着材料和空间层次对着生藻类建群过程的影响,为后期着生藻类水华生态控制提供理论参考。
1 材料与方法 1.1 样点设置生态塘(N 30.21°E 120.15°)位于杭州钱塘江引水玉皇山预处理场内,面积约2500 m2。在生态塘中选取两处等深的位点(图 1),1 #位点位于塘中心,靠近进水口一侧,其生境是水体中有大量的狐尾藻(Myriophyllum verticillatum L.)、菹草(Potamogeton crispus)等沉水植物;2 #位点生境附近主要有少量芦苇(Phragmites australis)等挺水植物。
|
| 图 1 样点布设图 Fig. 1 Diagram of the studying site layout |
将市场购买的10 cm×10 cm规格的花岗岩和瓷砖两种石质的人工基质用蒸馏水浸泡24 h,并用硬毛刷刷去上面的杂质,自然风干,制作成实验中所使用的附着材料待用。
1.3 空间层次的设置将上述制作的附着材料通过一定长度的尼龙绳悬挂于生态塘中1 #和2 #位点的的木桩上,使得两种附着材料分别距水体底部1 m处和水体中部0.5 m处。
1.4 样品采集和处理2014年5月3日至2014年7月13日期间,每隔10 d进行着生藻样和水样的采集,共进行7次。将从水体中取出的人工基质,用硬毛牙刷刷取基质表面的着生藻类,蒸馏水定容至100 mL,并将其分为两份:50 mL用于叶绿素a的测定,方法参照APHA[18];剩余50 mL鲁哥氏液固定后用于着生藻类的种类鉴定和定量分析,方法参照施之新[19]。在采集水样前进行水体溶解氧、水温、电导率等在线指标的测定,采集水样进行总氮、总磷、硝酸盐氮、亚硝酸盐氮、铵态氮等理化指标的测定,方法参照水和废水监测方法(第四版)[20]。
1.5 数据处理及统计分析(1)单位面积着生藻类的藻类数量Ni=(C1·L·ni)/(C2·R·h· S)[20],式中Ni表示单位面积i种种类的个体数(个/cm2);C1表示标本定容水量数(mL);C2表示实际计数的标本水量(mL);L表示藻类计数框每边的长度(μm);h表示视野中平行线间的距离(μm);R表示计数的行数;ni表示实际计数所得i种藻类个体数;S表示刮取基质的总面积(cm2)。
(2)Jaccard系数Sj=c/(a+b-c),式中Sj表示群落相似性系数,a表示群落A具有的物种数,b表示群落B的物种数,c表示群落A和B共有的物种数。
(3)Shannon-Weaver多样性指数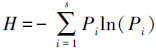
(4)使用SPSS 19.0做相关的单因素方差分析、相关性分析及显著性检验,并用Origin 8.0做相关的图形。
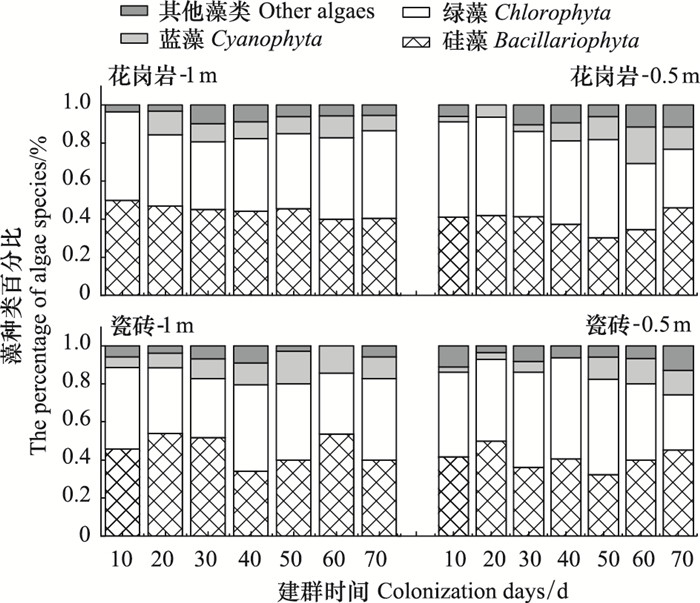
2 结果 2.1 着生藻类的种类组成变化通过镜检,生态塘人工基质上附着的藻类共8门(硅藻门、蓝藻门、绿藻门、隐藻门、裸藻门、甲藻门、金藻门和黄藻门)73属117种;其中硅藻、蓝藻和绿藻为优势类群。花岗岩基质上着生的硅藻种类数占总藻种类数的比例随建群过程而呈减小趋势;而瓷砖基质上着生的硅藻种类数的百分比呈先增后减的趋势,硅藻最多可达65.38%。绿藻在建群中一直处于较稳定状态,无特别明显的变化,其最高百分比可达53.13%。蓝藻在建群过程中,其种类数呈增长趋势并在后期趋于稳定(图 2, 图 3)。
|
| 图 2 1#着生藻类种类数百分比组成的变化 Fig. 2 Variations of the percentage of periphyton species at No.1 station |

|
| 图 3 2#着生藻类种类数百分比组成的变化 Fig. 3 Variations of the percentage of periphyton species at No.2 station |
在建群10d,主要以舟形藻(Navicula sp.)、脆杆藻(Fragilaria sp.)、栅藻(Scenedesmus sp.)等单细胞为主的藻类在基质上逐渐附着,其细胞密度最大百分比可达53.3%。20d至40d期间,曲壳藻(Achnanthes sp.)、丝藻(Ulothrix sp.)、伪鱼腥藻(Pseudanabaenoidaena sp.)、颤藻(Oscillatoria sp.)也逐渐成为优势种。到50d时,鞘丝藻(Lyngbya sp.)和颤藻(Oscillatoria sp.)主导着整个群落,其细胞密度百分比最大可达48.4%。60d和70d时,丝状藻类出现部分退化,单细胞藻类如舟形藻(Navicula sp.)和曲壳藻(Achnanthes sp.)重新大量出现,与丝状藻类交互生长。如表 1所示。
| 1# | 10d | 20d | 30d | 40d | 50d | 60d | 70d |
| 花岗岩-1 m (Granite-1 m) |
四尾栅藻 13.0 |
舟形藻 19.3 |
曲壳藻 21.9 |
颤藻 28.3 |
鞘丝藻 42.8 |
丝状蓝藻 30.1 |
鞘丝藻 41.5 |
| 花岗岩-0.5 m (Granite-0.5 m) |
栅藻 21.2 |
曲壳藻 17.3 |
曲壳藻 34.2 |
栅藻 16.0 |
鞘丝藻 43.4 |
曲壳藻 25.0 |
舟形藻 26.3 |
| 瓷砖-1 m (Tile-1 m) |
颤藻 18.9 |
舟形藻 24.0 |
颤藻 18.7 |
栅藻 28.1 |
鞘丝藻 44.1 |
鞘丝藻 21.4 |
鞘丝藻 50.8 |
| 瓷砖-0.5 m (Tile-0.5 m) |
栅藻 15.9 |
曲壳藻 30.2 |
曲壳藻 26.4 |
曲壳藻 27.3 |
鞘丝藻 48.4 |
曲壳藻 32.1 |
舟形藻 29.3 |
| 2# | 10d | 20 d | 30 d | 40 d | 50 d | 60 dd | 70d |
| 花岗岩-1 m (Granite-1 m) |
舟形藻 10.1 |
舟形藻 18.5 |
丝藻 17.6 |
伪鱼腥藻21.6 | 鞘丝藻17.2 | 丝状蓝藻 21.0 |
鞘丝藻 29.4 |
| 花岗岩-0.5 m (Granite-0.5 m) |
脆杆藻 30.2 |
脆杆藻 15.7 |
曲壳藻 22.7 |
鞘丝藻 11.3 |
鞘丝藻 45.3 |
鞘丝藻 37.9 |
舟形藻 21.1 |
| 瓷砖-1 m (Tile-1 m) |
脆杆藻 22.3 |
伪鱼腥藻 38.3 |
伪鱼腥藻21.8 | 鞘丝藻 15.4 |
鞘丝藻 22.4 |
鞘丝藻 20.7 |
鞘丝藻 32.7 |
| 瓷砖-0.5 m (Tile-0.5 m) |
舟形藻 53.3 |
伪鱼腥藻 21.5 |
曲壳藻 10.2 |
颤藻 25.4 |
颤藻 24.6 |
鞘丝藻 49.4 |
舟形藻 34.0 |
| 显著性分析表明,不同基质上着生的总藻、硅藻、绿藻和蓝藻的种类数均无显著性差异,同时不同水层中着生的总藻和蓝藻种类数无显著差异,但硅藻和绿藻种类数差异极显著(P < 0.01)。硅藻在水体底部具有更多的种类数,为(15±2)种,水体中部为(13±2)种; 绿藻则在水体中部具有更多的种类数,为(14±3)种,水体底部为(12±3)种 | |||||||
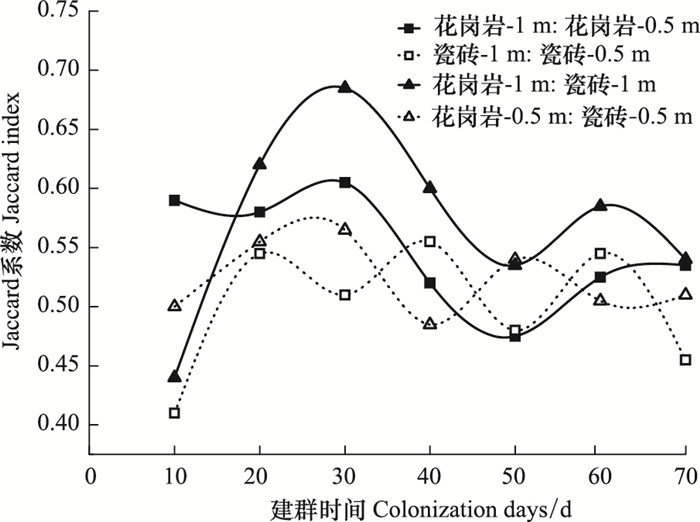
Jaccard指数用于一种描述不同群落间物种的相似性和差异性的指标。通过分析,生态塘中的着生藻类在不同基质和不同水层上所体现出的相似性系数在建群期间先增加后降低最后再小幅度增加至不变,整个过程中其均值为0.54。通过比较,花岗岩材料在不同水层所附着的着生藻类的相似性系数为0.55,瓷砖上的为0.50;在水体底部,Jaccard系数为0.57,水体中部的为0.52。从图 4可看出,不同基质、不同水层中的着生藻类群落相似性系数差异不大,同时通过显著性分析,几者之间也无显著性差异。Sullian认为当相似性指数大于0.5时,表明群落间具有很好的相似性[7]。所以,使用花岗岩和瓷砖两种材料,将其放置于水体底部和水体中部时,他们的群落相似性都很高(图 4)。
|
| 图 4 不同人工基质和空间层次中着生藻类物种的相似性系数 Fig. 4 Jaccard index of the periphyton species at different artificial substrates and vertical location |
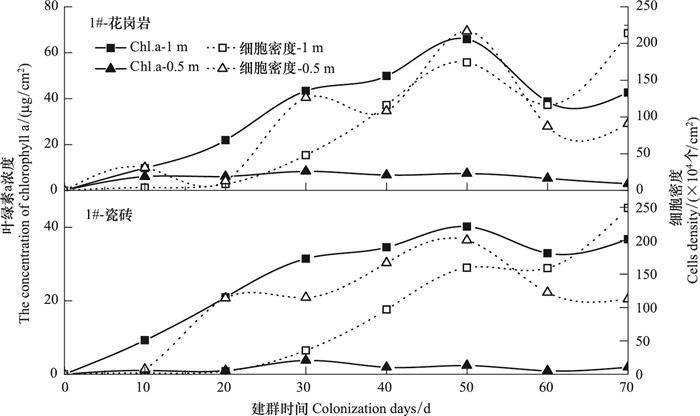
参照裴国凤[1]的研究,建群期间着生藻类的生物量通过叶绿素a和总藻细胞密度两个指标的变化来分析,如图 5所示。
|
| 图 5 1 #花岗岩和瓷砖在不同水层中叶绿素a浓度和细胞密度的变化 Fig. 5 Changes of chlorophyll a and cell density of granite and tile placed at different water column at No.1 station |
通过对建群时期生物量进行分析发现,无论是叶绿素a还是细胞密度着生藻类在不同基质上均无显著差异。但是着生藻类的生物量指标中只有叶绿素a在不同空间层次中具有极显著差异(P < 0.01), 细胞密度则无显著性差异,水体底部叶绿素a均值为25.74μg/cm2,水体中部为13.79μg/cm2。
1 #花岗岩(图 5, 1 #-Granite)将1 #水体底部(1 m)和中部(0.5 m)花岗岩上附着的藻类作比较,底部着生藻类叶绿素a浓度显著高于中部,分别为(38.89±18.38)μg/cm2、(19.05±5.41)μg/cm2;底部叶绿素a达峰值的时间为50d,中部较短为30d。细胞密度在底部和中部则无显著差异,底部达峰值的时间为70d,其值为2.14×106 ind/cm2,中部较短为50d,值为2.17×106 ind/cm2。着生藻类群落生物量达到峰值经过短暂的成熟稳定期后,由于连续2d的降雨使群落出现衰退迹象,表现出生物量的减少;当生物量开始上升时,意味着群落进入了二次生长时期。
1 #瓷砖(图 5, 1 #-Tile) 1 #瓷砖上着生藻类叶绿素a和细胞密度的变化和1 #花岗岩上的变化一致,水体底部与中部差异显著,峰值分别为40.22、20.77μg/cm2;底部细胞密度峰值为2.49×106 ind/cm2、中部为2.01×106 ind/cm2,着生藻类生物量达峰值后叶绿素a先减少后出现小幅度的二次增长,细胞密度则一直减少。
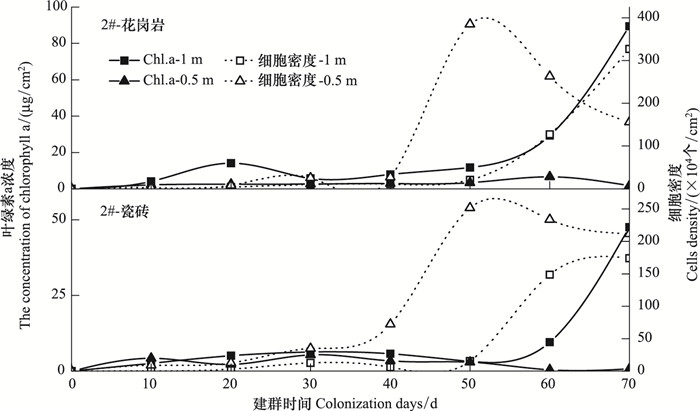
2 #花岗岩(图 6, 2 #-Granite) 2 #花岗岩在水体底部和中部附着的着生藻类叶绿素a和细胞密度均无显著差异。底部着生藻类的叶绿素a在70d达到峰值,值为89.47μg/cm2;中部的则在60d,为27.69μg/cm2。花岗岩在底部时细胞密度达峰值时间为70d,值为3.27×106 ind/cm2;中部50d时达峰值,为3.85×106 ind/cm2。
|
| 图 6 2 #花岗岩和瓷砖在不同水层中叶绿素a浓度和细胞密度的变化 Fig. 6 Changes of chlorophyll a and cell density of granite and tile placed at different water column at No.2 station |
2 #瓷砖(图 6, 2 #-Tile) 2 #瓷砖在水体底部和中部附着的着生藻类生物量无显著差异。底部叶绿素a在70d达峰值,中部则在30d,其峰值分别为47.52、25.18μg/cm2。底部细胞密度在70d时达峰值,中部在50d时,其峰值分别为1.74×106、2.52×106 ind/cm2。
通过上述分析,1 #和2 #不同空间层次的生物量达峰值的时间存在明显的不同,在底部的着生藻类生物量达峰值的时间更长,为70d或50d,而中部较短为60d、50d或30d。1 #的花岗岩和瓷砖上附着的着生藻类叶绿素a具有显著差异,1 #水体底部叶绿素a浓度显著高于中部,2 #叶绿素a无显著区别;而细胞密度在1 #和2 #均无显著差异。
2.4 Shannon-Weaver多样性指数Shannon-Weaver多样性指数一定程度上可指示水体环境,当H≥3时指示水体清洁,2≤H < 3指示轻度污染,1≤H < 2指示中度污染[21],可初步判断生态塘的水环境处于轻度或中度污染。在建群过程中,着生藻类群落多样性呈下降趋势,在花岗岩上着生藻类多样性指数均值为2.53,瓷砖上则为2.47;在水体底部的藻类多样性指数几乎都高于水体中部(图 7)。通过显著性分析,不同人工基质和不同水层上所附着的着生藻类群落多样性指数无显著差异。

|
| 图 7 着生藻类Shannon-Weaver多样性指数的变化 Fig. 7 Changes of Shannon-Weaver diversity index in periphytic algae |
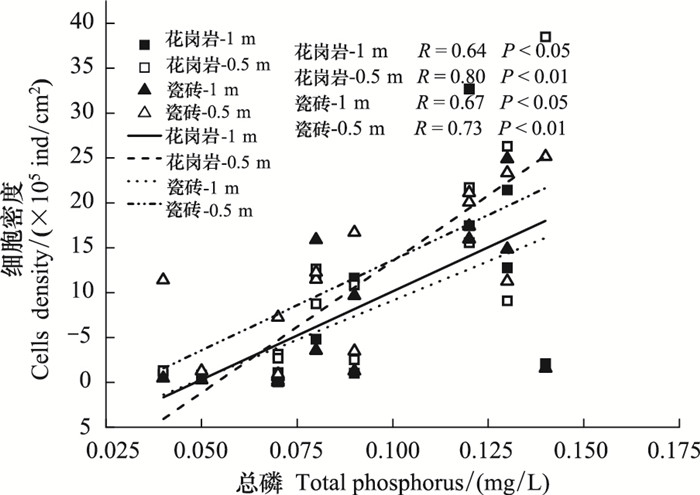
通过对着生藻类细胞密度与水体总磷、总氮、硝酸盐氮、亚硝酸盐氮、铵态氮等理化指标作相关性分析,着生藻类细胞密度与总氮、硝酸盐氮、亚硝酸盐氮、氨氮和COD无相关性,但是与总磷有极显著地相关性,如表 2所示。通过线性分析,水体中部的着生藻类与总磷具有较水体底部更显著的正相关关系(图 8)。
| 水质指标 Water qualities |
总磷 Total phosphorus |
总氮 Total nitrogen |
硝酸盐氮 Nitrate |
亚硝酸盐氮 Nitrite |
铵态氮 Ammonia |
化学需氧量 COD |
| 相关性系数Correlation coefficient | 0.859** | -0.144 | 0.147 | 0.328 | 0.234 | 0.492 |
| 显著性Significance | 0.000 | 0.624 | 0.615 | 0.223 | 0.421 | 0.074 |
| **表示在0.01水平上显著相关 | ||||||
|
| 图 8 着生藻类细胞密度与总磷关系图 Fig. 8 Correlation between periphytic algae cell density and total phosphorus |
由于光学显微镜、扫描电镜等仪器的运用,着生藻类的群落从传统的显微镜分析发展为详细地观察其三维结构,跟踪整个建群过程,目前研究表明,着生藻类的建群最先自生境中颗粒或溶解态的有机物吸附于基质上开始,这些有机物为细菌的生长奠定了基础并为其他有机体的吸附生长创造了条件;随后以面着生的机会型硅藻如Gomphonema parvulum、Amphipleura pellucida等开始吸附于基质上并开始生长;然后以点着生的具有莲座状或者粘质垫子的直立的、短茎或者长茎的硅藻及丝状藻类开始出现[3]。本实验生态塘中着生藻类的建群基本符合以上建群过程和特征,在早期优势藻类是具有固着在空的胶质管上的结构的舟形藻(Navicula sp.);能分泌胶质的针杆藻(Synedra sp.)、脆杆藻(Fragilaria sp.)、异极藻(Gomphonema sp.)等单细胞藻类[9]。在中后期出现具有相似的粘性结构的鞘丝藻(Lyngbya sp.)、伪鱼腥藻(Pseudanabaena sp.)、颤藻(Oscillatoria sp.)等蓝藻门为主的丝状藻类;在60d时由于大雨冲刷使得水体中部的着生藻类群落受到影响,其丝状藻类大量减少,为单细胞藻类的重新复兴创造了条件。
花岗岩和瓷砖两种人工基质对着生藻类种类组成、优势藻类组成、藻类细胞密度和叶绿素a均无显著性影响,同时其微生境的群落相似性系数都在0.5左右,无显著区别。兰波通过对洱海周丛藻类的研究得出基质的类型对周丛藻类生物量无显著影响[14],这进一步证明着生藻类的种类组成与基质表面粗糙程度无关,而与藻类的生活习性和细胞构造有关。但念宇指出基质不同会造成着生藻种间多样性的差异,推测可能与基质表面粗糙程度和水流方向有关[9],兰波也指出基质粗糙度会显著提高周丛藻类的生物多样性[14],本研究的藻类多样性与基质粗糙度无关,可能是由于花岗岩和瓷砖都为石质基质,其粗糙度的区别不如玻片与石头、竹子、塑料等差别显著;同时由于生态塘面积较小,水流方向并不显著。Cattaneo等通过大量调查基质的材料、质地、颜色等对着生藻类建群的影响,但是结论都不一致,因此认为基质的选择并不是特别重要,材料本身对建群的影响不及建群时间、富营养程度、温度的影响大[7]。
着生藻类总藻、硅藻、绿藻种类数在不同空间层次中具有显著性差异:硅藻种类数在水体底部(1 m)多于水体中部(0.5 m);绿藻种类数则是在水体中部更多。原因可能是底泥中具有更多的硅藻藻类,材料平铺于底泥上,当底泥出现局部变化时,硅藻门容易随着底泥的移动转移至实验材料上;同时在实验期间,以刚毛藻(Cladophora sp.)为主的丝状绿藻爆发,漂浮于水体表层,所以在中部的材料比底部的材料能附着更多的绿藻。空间层次对着生藻类的两个生物量指标的影响中只对叶绿素a有显著影响,但是在不同位点它们又呈现出不同的规律:1 #水体底部着生藻类的叶绿素a浓度要高于水体中部,2 #的着生藻类叶绿素a不存在显著区别。其原因可能是1 #比2 #具有更多生物量的沉水植物,它们在水体中生长良好,其植株可达1.5 m,在水体中部对着生藻类的抑制作用可能强于底部。细胞密度和叶绿素a两个指标共同反应着生藻类的生物量各具特点和优势,细胞密度对单细胞藻类的计数结果比丝状藻类的计数结果更精确,而本实验中的着生藻类在建群后期几乎都是丝状藻类,便为计数结果带来了更大的不精确性,其细胞密度便很难成显著性差异。生态塘中水体底部的着生藻类建群达到最高生物量所需时间明显长于水体中部,底部需要为70d或50d,水体中部的则为60、50d或30d,与东湖的着生藻类建群时间相比,杭州玉皇山预处理场生态塘中的着生藻类建群所需时间[1]更长,原因可能是由于东湖营养化程度明显高于西湖。兰波通过研究洱海着生藻类得出夏季生物量0 m>0.5 m>1 m>1.5 m,且达到第一个峰值的时间是30d[14]。两种结果有一定的差异,原因可能是因为生态塘中整个区域都具有非常多的狐尾藻(M.verticillatum L.)、菹草(P.crispus)等沉水植物,其根部对着生藻类的影响可能弱于茎叶,所以导致生态塘着生藻类在底部具有更高的生物量。
对湖泊中着生藻类进行研究发现着生藻类生物量与环境总磷浓度有明显的相关性。例如Toetz通过调查高原浅水湖泊Valley湖时发现磷是主要限制周丛藻类生长的因子[22]。刘玉超通过研究亚热带富营养型湖泊中磷对附着藻类的影响时,也得出磷是附着藻类群落发展的关键因子,磷浓度的增加明显促进着生藻类生物量的积累[23]。兰波通过研究洱海周丛藻类也得出洱海流域周丛藻类分布主要受总磷影响[14]。王霞等通过静态藻类培养试验(AGP)得出松花湖富营养化发生的总磷阈值为0.065 mg/L[24],杨龙等通过添加BG11培养基浓缩液到密云水库原水中作为培养液,培养从密云水库采集的混合藻种,进行动态AGP模拟富营养化水体磷阈值,得出密云水库总磷阈值为0.053—0.064 mg/L[25]。尽管这些研究得出了富营养化发生的阈值,但实验环境与天然湖泊水体环境存在很大的差异。本研究得出生态塘中着生藻类生物量主要受总磷的影响,由于富营养化发生的阈值受到多因素综合影响,所以确定生态塘着生藻类水华发生的阈值还需要开展更加系统深入的研究。
4 结论(1)生态塘中共检出8门73属117种着生藻类,其中以硅藻、蓝藻和绿藻为优势类群,着生藻类优势种在本实验的建群过程中大致呈如下变化规律:绿藻门—硅藻门—蓝藻门—硅藻门和蓝藻门,在建群第10天多以栅藻(Scenedesmus sp.)和脆杆藻(Fragilaria sp.)为主,第20天到40天时发展为舟形藻(Navicula sp.)或曲壳藻(Achnanthes sp.)或伪鱼腥藻(Pseudanabaena sp.),再发展为鞘丝藻(Lyngbya sp.)为优势,至实验末期以鞘丝藻(Lyngbya sp.)与舟形藻(Navicula sp.)为主。
(2)花岗岩和瓷砖两种材料对着生藻类的种类组成、细胞密度和物种多样性均无影响,两种材料上的着生藻类群落具有较高的相似性,一定程度说明着生藻类的附着与基质粗糙度无关,而与藻类的自身生活习性和结构有关。
(3)不同水层对着生藻类种类数、建群生物量、达生物量峰值所需的时间都有显著地影响。水体底部的着生藻类具有更多的硅藻,水体中部则具有更多的绿藻,同时随着建群的发展,蓝藻种类数也在逐渐增加至稳定。通过对着生藻类建群生物量达峰值的时间进行分析,水体中部的着生藻类生物量达到峰值的时间较短为60、50d或30d,底部则需要70d或50d。
(4)生态塘中着生藻类在建群过程中其生长过程主要受总磷的影响。
致谢: 王亚芬、张义、姚远帮助修改文字,国家水专项课题杭州西湖工作站孙健、张垚磊、闵奋力、谭谈帮助野外采样和实验,特此致谢。| [1] | 裴国凤.淡水湖泊底栖藻类的生态学研究.武汉:中国科学院水生生物研究所, 2006. |
| [2] | Stevenson R J, Peterson C G, Kirschtel D B, King C C, Tuchman N C. Density-dependent growth, ecological strategies, and effects of nutrients and shading on benthic diatom succession in streams[J]. Journal of Phycology , 1991, 27 (1) : 59–69. DOI:10.1111/j.0022-3646.1991.00059.x |
| [3] | Hoagland K D, Roemer S C, Rosowski J R. Colonization and community structure of two periphyton assemblages, with emphasis on the diatoms (Bacillariophyceae)[J]. American Journal of Botany , 1982, 69 (2) : 188–213. DOI:10.2307/2443006 |
| [4] | Hillebrand H, Sommer U. Diversity of benthic microalgae in response to colonization time and eutrophication[J]. Aquatic Botany , 2000, 67 (3) : 221–236. DOI:10.1016/S0304-3770(00)00088-7 |
| [5] | Albay M, Akccalan R. Comparative study of periphyton colonisation on common reed (Phragmites australis) and artificial substrate in a shallow lake, Manyas, Turkey[J]. Hydrobiologia , 2003, 506 (1/3) : 531–540. |
| [6] | Ahn C H, Song H M, Lee S, Oh J H, Ahn H, Park J R, Lee J M, Joo J C. Effects of water velocity and specific surface area on filamentous periphyton biomass in an artificial Stream Mesocosm[J]. Water , 2013, 5 (4) : 1723–1740. DOI:10.3390/w5041723 |
| [7] | Cattaneo A, Amireault M C. How artifical are artificial substrata for periphyton?[J]. Joural of the North American Benthological Society , 1992, 11 (2) : 244–256. DOI:10.2307/1467389 |
| [8] | 裴国凤, 刘梅芳. 武汉东湖底栖藻类在不同基质上生长的比较[J]. 湖泊科学 , 2009, 21 (3) : 357–362. |
| [9] | 念宇, 韩耀宗, 杨再福. 不同基质上着生生物群落生态学特性比较研究[J]. 环境科技 , 2009, 22 (5) : 14–17. |
| [10] | 陈向, 刘静, 何琦, 林秋奇, 韩博平, 韦桂峰. 东江惠州河流段人工基质附着硅藻群落的季节性动态[J]. 湖泊科学 , 2012, 24 (5) : 723–731. |
| [11] | Hameed H A. The colonization of periphytic diatom species on artifical substrates in the Ashar canal, Basrah, Iraq[J]. Limnologica-Ecology and Management of Inland Waters , 2003, 33 (1) : 54–61. DOI:10.1016/S0075-9511(03)80007-5 |
| [12] | 刘麟菲.渭河流域着生藻类群落结构与环境因子的关系.大连:大连海洋大学, 2014. |
| [13] | Franca R C S, Lopes M R M, Ferragut C. Structural and successional variability of periphytic algal community in an Amazonian Lake during the dry and rainy season (Rio Branco, Acre)[J]. Acta Amazonica , 2011, 41 (2) : 257–266. DOI:10.1590/S0044-59672011000200010 |
| [14] | 兰波.洱海周丛藻类生态学研究.武汉:华中科技大学, 2011. |
| [15] | 王丽卿, 张玮, 范志锋, 孟智奇, 张瑞雷, 李为星. 淀山湖生态示范区附着藻类季节动态变化研究[J]. 农业环境科学学报 , 2012, 31 (8) : 1596–1602. |
| [16] | 项斯瑞, 吴文卫, 黄三红, 陈丽娟, 姚敏. 近2000年来杭州西湖藻类种群的演替与富营养化的发展过程[J]. 湖泊科学 , 2000, 12 (3) : 219–225. |
| [17] | 马顷.水绵和刚毛藻的生态适应性及其干扰作用对四种沉水植物的影响.新乡:河南师范大学, 2011. |
| [18] | American Public Health Association (APHA). "Standard Methods for the Examination of Water and Waste Water" 18th ed. Washington, DC: American Public Health Association, 1992. |
| [19] | 施之新. 中国淡水藻志 , 2013 . |
| [20] | 国家环境保护总局水和废水监测分析方法编委会. 水和废水监测方法 , 2002 . |
| [21] | 蔡立哲, 马丽, 高阳, 郑天凌, 林鹏. 海洋底栖动物多样性指数污染程度评价标准的分析[J]. 厦门大学学报:自然科学 , 2002, 41 (05) : 641–646. |
| [22] | Toetz D. Water chemistry and periphyton in an alpine wetland[J]. Hydrobiologia , 1995, 312 (2) : 93–105. DOI:10.1007/BF00020765 |
| [23] | 刘玉强, 刘正文. 亚热带富营养型湖泊中磷对附着藻类的影响[J]. 华南农业大学学报 , 2011, 32 (3) : 119–121. |
| [24] | 王霞, 吕宪国, 白淑英, 张竹青, 闫伯茹, 于力, 张学林, 张丽娴. 松花湖富营养化发生的阈值判定和概率分析[J]. 生态学报 , 2006, 26 (12) : 3989–3997. |
| [25] | 杨龙, 王晓燕, 王子健, 贾东民, 吴在兴, 吴敬. 富营养化水体磷阈值的动态AGP模拟研究[J]. 生态环境学报 , 2009, 18 (5) : 1625–1630. |
 2016, Vol. 36
2016, Vol. 36