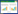文章信息
- 陈建文, 史建伟, 王孟本
- CHEN Jianwen, SHI Jianwei, WANG Mengben.
- 不同林龄柠条细根现存量比较
- A comparative study of fine-root standing crop in different-aged Caragana korshinskii plantations
- 生态学报[J]. 2016, 36(13): 4021-4033
- Acta Ecologica Sinica[J]. 2016, 36(13): 4021-4033
- http://dx.doi.org/10.5846/stxb201411182281
-
文章历史
- 收稿日期: 2014-11-18
- 网络出版日期: 2015-10-30
细根在陆地生态系统生物地球化学循环中扮演着非常重要的角色。据估计,全球细根的碳储量超过大气中碳储量的5%[1],细根生物量占总的森林生物量的2%—5%[2-3]。而在陆地生态系统净初级生产力的分配中,细根占到了33%[1, 3-6],甚至在一些森林生态系统中,其对净初级生产力的分配达到了70%[7-8]。这种细根对净初级生产力的分配比例与其在森林生态系统中所占的生物量比例看似矛盾,实则是因为细根具有较短的寿命和较高的周转率[9-11]。其在年度周转中消耗了大量的净初级生产力。
植物根系在森林生态系统中的地位不言而喻,其分布特征及与地下土壤资源有效性之间的关系对整个森林生态系统的发展与演替有着重要影响。柠条锦鸡儿(Caragana korshinskii)属于豆科(Leguminosae)锦鸡儿属(Caragana)植物[12],为多年生落叶灌木。由于其具有发达的根系,在防风固沙和水土保持方面功能显著。目前人们对柠条的研究主要集中在柠条林地土壤水分分布、地上生物量与生物学特性、种群的蒸散作用、以及生理生态学特性等方面[13-15],而关于细根方面的研究较少。Zhang et al.曾对腾格尔沙漠地区柠条细根分布进行过报道[16];在黄土高原地区,本研究前期曾对柠条幼林细根生长动态进行过一些探讨[17-18]。这些研究均缺乏长期的观测印证。根据气象资料记载,晋西北黄土丘陵区年际间降水差异较大,不同的年降水造成年际间土壤水热条件的差异。本研究旨在探讨不同林龄柠条细根现存量年际动态及其对年际间水热变化的响应,为进一步揭示柠条细根对水分与矿质营养的响应机制提供依据。这对加强柠条林地的田间管理,提高农林生产效力以及黄土高原地区植被重建、生态恢复具有重要意义。
1 材料与方法 1.1 研究地概况本研究设置于山西省五寨县张家坪林场 (38°58.825′N,111°46.296′E),该地海拔1448 m,位于黄土高原东部,属于温带大陆性季风气候。年均温5.19℃,最高温36.7℃,最低温-36.6℃;年均降水437.92 mm;年均日照时数2884.15 h;年均无霜期125 d,以上数据为距离实验站6 km的气象观测站1960—2012年间监测数据。
研究地主要土壤类型为黄土状淡栗褐土,肥力较低。本研究柠条林地选取梁峁缓坡部位相同立地,坡度0—5°,造林前为裸地。其中,柠条幼林源于2002年秋季造林,成林源于1977年秋季造林,播种方式为条播,播种时行距均为2 m。两林地成活率均为90%以上。
1.2 研究方法 1.2.1 微根管的安装2006年10月,在两林地分别设置30 m × 30 m样地,每样地均划分为10 m × 10 m 9个小样地。其中,幼林地随机选取5个小样地,小样地内距离播种行0 cm和50 cm位置分别安装一根微根管;成林地随机选取4个小样地,小样地内距离播种行0、50、100 cm位置分别安装一根微根管。微根管的埋设参照Johnson等的安装方法[19],微根管(长150 cm,外径5.5 cm,内径5.0 cm)管底用胶圈密封,管子与地面呈45°夹角斜插入随机样点,直至垂直深度达到100 cm,漏出地面部分用黑色胶带缠好,而后加封黄色胶带以防透光,管口用塑料瓶(长20 cm,外涂白色涂料)封盖。
1.2.2 细根数据的获得细根图片的采集使用美国Bartz公司生产的BTC—100 (Bartz Technology,Santa Barbara,USA)图像采集系统。微根管的观测每年3月到10月逐月进行。因微根管安装需要一定稳定周期,本研究仅分析2008—2011年观测结果。用RooTracker (Duke University,Durham,NC)根系分析软件对所采集的图片进行数据提取,提取方法采用Kern等的方法[20],对于每一次观测只考虑3种细根状态:(1)新生根,(2) 又观察到的非新生根,(3) 消失的细根。只有当细根消失时才补认为该细根死亡。由于每一次测量中得到的数据是以长度为基础的细根根长数据,所以本研究以单位面积根长为基本单位来确定细根现存量(SC)。
1.2.3 环境因子的测量降雨、土壤温度以及土壤水分与微根管的观测同步进行。降雨量采用距样地6 km的气象观测站数据。在0—100 cm土壤剖面,每20 cm土层深度安装一个温度计(HOBO TidbiT v2 Temp logger,Onset Computer Corporation,USA)记录土壤温度。土壤水分的测量采用烘干法。每次细根观测时,在两样地内各选取3个土壤水分取样点,每个取样点以20 cm为间隔在0—100 cm土层深度取样测定土壤水分(每土层深度每样点取样3份)。
1.3 数据计算 1.3.1 细根参数计算月细根现存量通过以下公式计算:

|
式中,SC (mm/cm2)为细根现存量,RL (mm)为观测到的细根根长,A (cm2)为观测到该根长所对应的观测窗面积。
年度细根现存量用观测年内逐月细根现存量的算术平均来表示。
1.3.2 环境因子土壤温度以相邻两次细根观测日为基准,计算该时间段平均值;降雨量取每两次观测之间的累积值;土壤水分则以测量日为准作为每次观测所对应的土壤水分。
对于每年3月份的细根观测来说,参照Olesinski等的处理方式[21],在3月份测定前给定一个日期作为年度细根生长的起点,并以此时间点到3月份的测定日为一个观测周期;相关的环境因子也以年初给定日期到首次观测日为止进行计算。
1.4 统计分析用单因素方差分析以及Duncan一致性子集检验来比较林分内不同年度不同季节不同土层的细根SC之间的差异。用独立样本t检验来比较两林分细根SC之间的差异。用Pearson相关检验细根SC与环境因子之间的相关性。所有数据分析前进行方差齐次性检验,当方差不齐时,对数据进行对数转换以满足统计假设。统计软件使用SPSS 17.0。
2 结果与分析 2.1 细根现存量垂直分布 2.1.1 逐月细根现存量垂直分布由图 1、图 2可知,2009年7月到2010年9月,幼林细根SC最大值出现在90—100 cm土层,而2010年10月一直到2011年观测结束,最大细根SC却出现于80—90 cm土层深度。而从2009年7月到整个观测期结束,0—20 cm土层细根SC最低。

|
| 图 1 008—2011年3月到7月柠条幼林与成林细根现存量(SC)垂直分布 Fig. 1 The vertical distribution of fine root Standing Crop (SC) in young and mature Caragana korshinskii plantations during March to July from 2008 to 2011 |

|
| 图 2 2008—2011年8月到10月柠条幼林与成林细根现存量 (SC) 垂直分布 Fig. 2 The vertical distribution of fine root Standing Crop (SC) in young and mature Caragana korshinskii plantations during August to October from 2008 to 2011 |
成林细根SC的分布与幼林明显不同(图 1,图 2),2008年3月到6月,成林细根最小SC在0—10 cm或90—100 cm土层深度,从2008年6月开始,90—100 cm土层深度的细根SC开始升高,而0—20 cm土层一直保持细根SC最小分布。与幼林相比,成林最大细根SC分布较浅,位于在50—70 cm土层之间,其中以50—60 cm土层为最高。
2008年3月到2009年6月,幼林细根SC各土层间无显著差异(P>0.05),2009年7月到观测期末,幼林地各土层细根SC差异显著(P<0.05)。在整个观测期内,成林地各土层细根SC差异显著(P<0.05)。2008年3月到2009年8月,幼林地0—10 cm土层细根SC显著高于成林(P<0.05),而2011年8月以后,成林地该土层的细根SC显著高于幼林地(P<0.05)。两林地的另一个显著差异出现在60—70 cm土层,这种差异从2010年4月开始一直持续到整个观测期结束。
2.1.2 逐年细根现存量垂直分布图 3表明,在年度水平,幼林细根SC垂直分布表现为,从表层(0—20 cm)开始,细根SC逐渐升高,到50—60 cm土层出现极大值,而后在60—70 cm土层出现极小值,而后逐渐升高,并在80—100 cm土层深度出现最大分布。成林细根SC的垂直分布则在2008—2010年表现为“单峰”曲线,即从土壤表层开始逐渐升高,在50—60 cm土层达到最高,而后逐渐降低。2011年成林细根SC则在60—70 cm土层出现极小值。
|
| 图 3 2008—2011年柠条幼林与成林细根现存量 (SC) 垂直分布与季节分布 Fig. 3 Vertical and seasonal changes of fine root standing crop (SC) in young and mature Caragana korshinskii plantations from 2008 to 2011 |
整体来看,两林地最大细根SC均出现于50 cm土层以下,而幼林最大细根SC较成林更深。2008年,成林细根SC仅在50—70 cm土层高于幼林,而2009年,成林细根SC在40—80 cm土层高于幼林,到2011年观测结束,成林细根SC在0—100 cm的各个土层均高于幼林。
在年度水平,2008年幼林细根SC各土层间差异不显著(P>0.05),2009—2011年差异极显著(P<0.01);成林细根SC各土层间则在所有观测年差异均极显著(P<0.01)。
2.2 细根现存量季节动态 2.2.1 各土层细根现存量季节动态两林地细根SC的季节变化表现出不一样的特征(图 4)。幼林地0—30 cm土层细根SC在2009年持续下降,而40—100 cm土层细根SC在各观测年内表现出单峰或双峰的生长曲线,2009年最大值出现在5—7月份,其他年份出现在7—8月份。成林地0—10 cm土层细根SC在2009年变化剧烈,在生长季表现出4个细根SC的极大值;10—100 cm土层中,2009年成林地观测到最大细根SC的时间较其他年份为晚,约为9—10月份,其余年份则为8—9月份。

|
| 图 4 2008年3月到2011年10月柠条幼林与成林地不同土层细根现存量 (SC) 季节动态 Fig. 4 Seasonal changes of fine root standing crop (SC) in young and mature Caragana korshinskii plantations from March to October during 2008—2011 |
幼林与成林细根SC季节变化的另一个区别是在每年的生长季末(10月),幼林细根SC减少相对较快,2009年整个土层细根SC减少到了年细根SC的最低,2010—2011年0—50 cm土层细根SC减少到了各年度最低;成林细根SC减少则相对较慢。两林地细根SC的相似之处是,大多数的土层中,细根SC在生长季初(3—4月)表现出一定的增长,这个现象在2011年最为明显(图 4)。
2008年,幼林细根SC仅80—90 cm土层各观测月间差异显著 (P<0.05),成林细根SC仅40—50 cm和80—100 cm土层各观测月间差异显著 (P<0.05)。2009—2011年,两林分所有土层各观测月间无差异 (P>0.05)。
2.2.2 土壤剖面细根现存量季节动态在样地水平,2008年幼林细根SC高于成林,而随着林地的发展,2009年6月份时,幼林细根SC与成林持平(图 3),并在接下来的时间里明显低于成林细根SC。从整个观测期(2008—2011)来看,幼林细根SC表现出先增长,后降低的趋势,并在观测结束时低于观测初期,成林细根SC则表现出明显的增加(图 3)。2008年,幼林最大细根SC出现在8月份,而成林则出现在9月份;2009年,幼林最大细根SC出现在3月份,成林最大细根SC依然出现在9月;其余两个观测年,两林分最大细根SC均出现在8月(图 3)。
在样地水平,仅2008年各月间成林细根SC差异极显著(P<0.01)。2008年6—7月份,幼林地细根SC显著高于成林;2010年6—8月份、2011年5—10月份,成林细根SC显著高于幼林(P<0.05)。
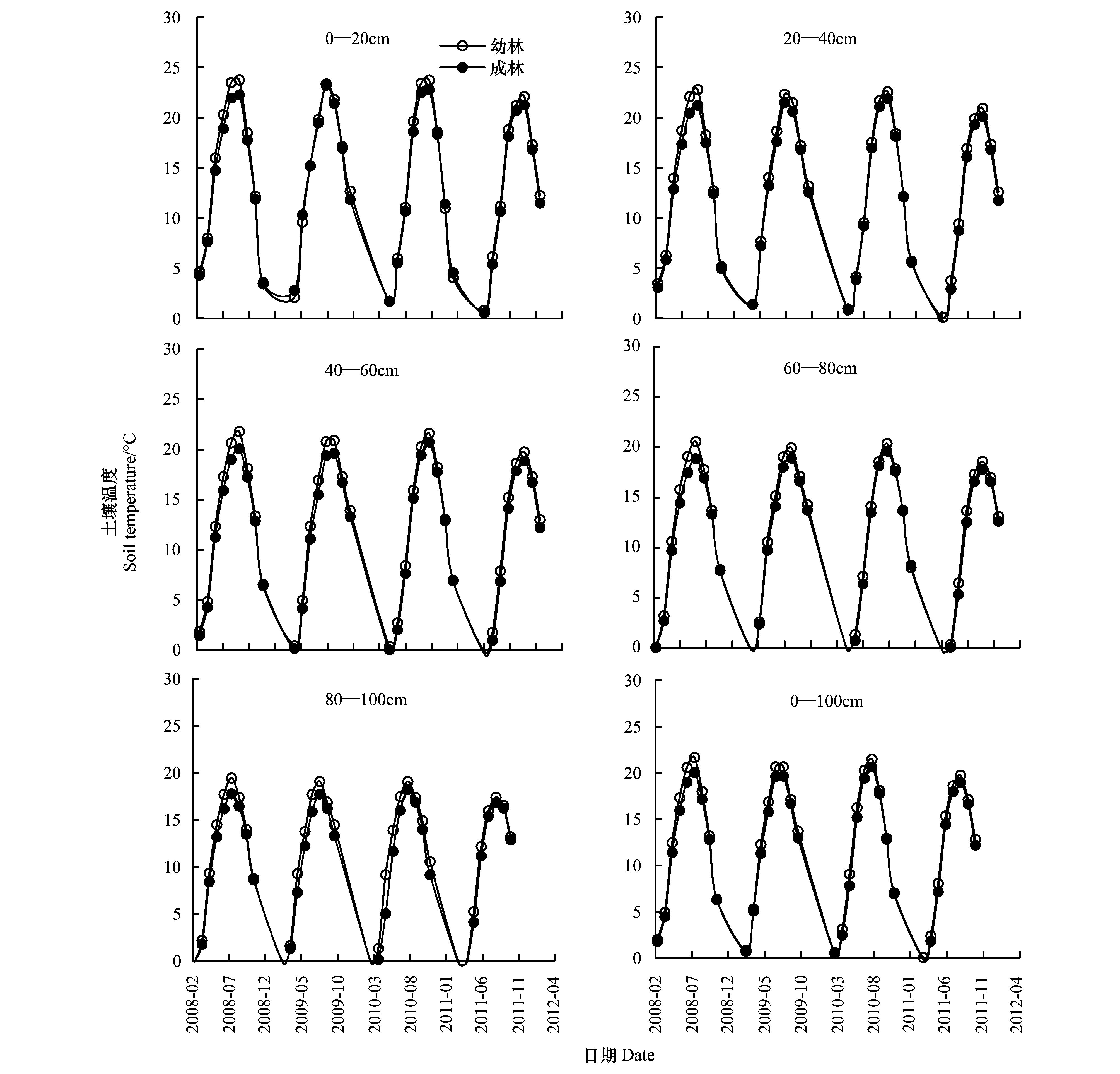
2.3 细根现存量与环境因子的关系 2.3.1 环境因子动态在0—20 cm土层,2009年两林地最高土壤温度出现在7月份,而其余年份则出现在8月份;20—100 cm土层最高土壤温度均出现在每年8月份。垂直分布上,从每年3月到8月底,两林地土壤温度随着土层深度的增加而降低,而9月份以后,土壤温度随着土层深度的增加而升高,幼林地土壤温度在各土层均高于成林地(图 5)。
|
| 图 5 2008—2011年不同土层土壤温度季节变化 Fig. 5 The seasonal changes of soil temperature in different soil layer during 2008—2011 |
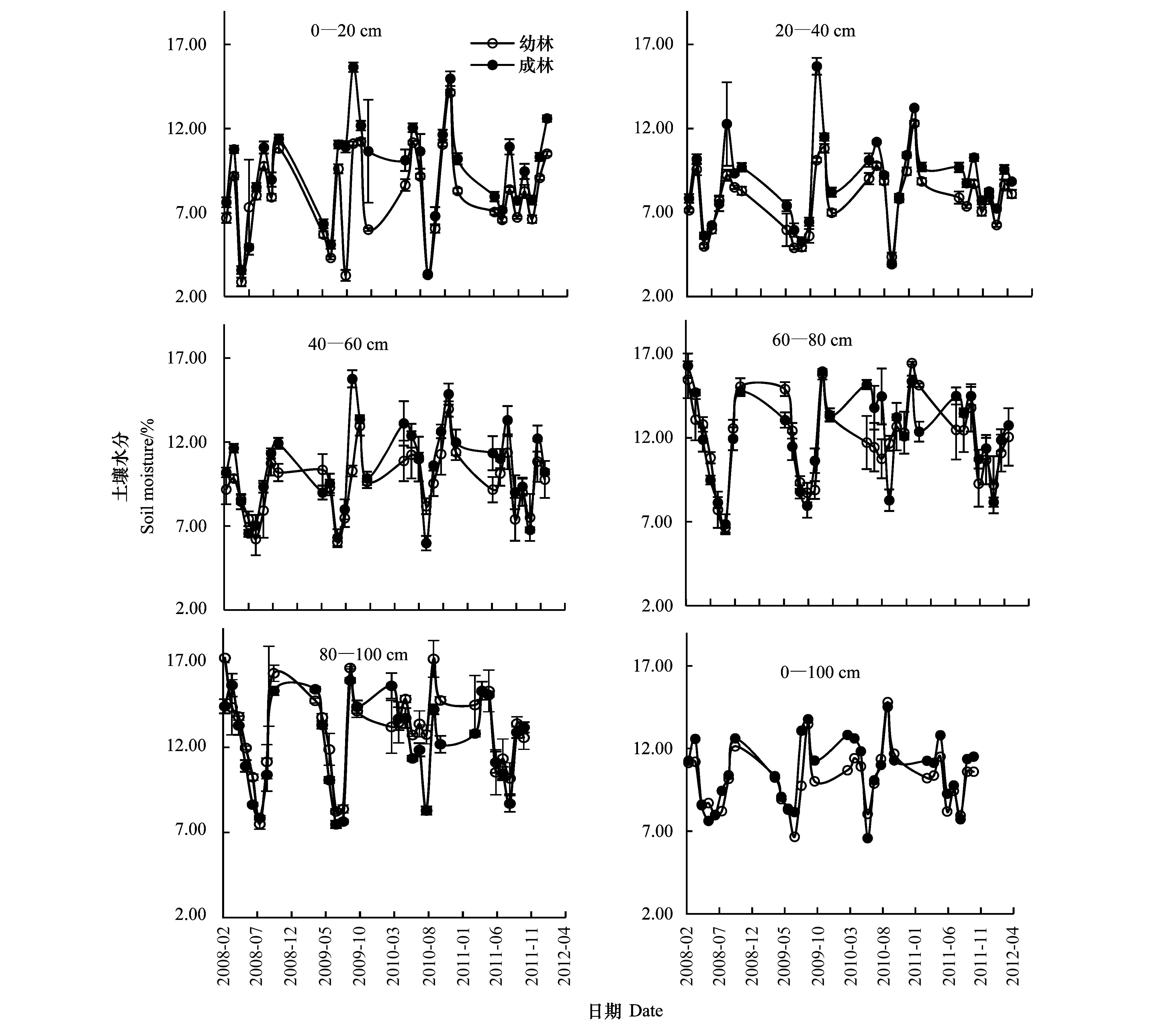
实验区的降水集中在7—9月,但是年际间差异较大,2008年9月份降水相对较少,10月份却出现大量降水。而2009年观测期内降水较其他年份为低(357.4 mm) (表 1)。两林地土壤水分随着降水量的变化而变化(图 6,表 1)。成林60—80 cm土层土壤水分显著高于表层0—20 cm(P<0.05),即使在雨季,该层土壤水分仍表现为高于上层土壤(图 6)。在0—60 cm土层,成林各层土壤水分均高于幼林,而更深层则不然,80—100 cm土层中,幼林土壤水分较成林为高,且2009年达到显著水平(P<0.05)。
| 年份 Year | 3月 March | 4月 April | 5月 May | 6月 June | 7月 July | 8月 August | 9月 September | 10月 October | 合计 Total | 类型 Types |
| 2008 | 3.4 | 58.9 | 28.5 | 63.6 | 75.5 | 95.5 | 72.2 | 100.7 | 498.3 | 偏涝年 |
| 2009 | 0.0 | 10.5 | 15.9 | 22.0 | 82.0 | 125.3 | 95.0 | 6.7 | 357.4 | 偏旱年 |
| 2010 | 0.0 | 21.3 | 46.1 | 19.4 | 116.4 | 119.0 | 116.2 | 22.9 | 461.3 | 正常年 |
| 2011 | 1.2 | 6.3 | 61.6 | 52.9 | 104.4 | 68.8 | 96.9 | 29.9 | 422.0 | 正常年 |
| 50年平均 Mean of 50 years | 3.5 | 21.1 | 35.7 | 64.1 | 107.0 | 107.6 | 59.7 | 27.0 | 425.8 |
|
| 图 6 2008—2011年不同土层土壤水分季节变化 Fig. 6 The seasonal changes of soil moisture in different soil layer during 2008—2011 |
2008年柠条幼林细根SC的季节变化与降雨量显著相关(P<0.05),与土壤温度极显著相关(P<0.01);但其他年份里,幼林细根SC仅于2009年与降雨量显著相关(P<0.05)。成林细根SC在所有的年份里均与土壤温度显著相关(P<0.05),2008—2009年与降雨量显著相关(P<0.05)。两林地细根SC均与土壤水分未发现显著相关(表 2)。
| 年份 Year | 林分 Plantation | 降雨量 Pricipitation | 土壤温度 Soil temperature | 土壤水分 Soil water content |
| 2008 | 幼林 | 0.755* | 0.958** | -0.491 |
| 成林 | 0.831* | 0.825* | -0.105 | |
| 2009 | 幼林 | 0.122 | -0.077 | -0.412 |
| 成林 | 0.709* | 0.788* | 0.486 | |
| 2010 | 幼林 | 0.707* | 0.55 | -0.145 |
| 成林 | 0.809* | 0.911** | -0.128 | |
| 2011 | 幼林 | 0.431 | 0.518 | -0.674 |
| 成林 | 0.538 | 0.768* | -0.483 | |
| *P<0.05,** P<0.01 | ||||
细根的主要功能是对水分和养分的“觅食”,其分布受土壤剖面中水分和养分影响[22-24]。在许多森林生态系统中,细根主要分布于土壤表层[25-26],并随土壤深度的增加而减少。关于柠条根系的研究发现,柠条根系最大分布主要位于10—100 cm土层[27]。荀俊杰等对幼林细根SC的研究中指出,幼龄柠条细根的主要分布区位于50 cm土层以下[17]。研究发现,无论柠条幼林还是成林,细根SC最大分布均位于50 cm土层以下。柠条细根的这种垂直分布格局在黄土高原地区其他森林生态系统的根系中也有发现[28-29],这可能与黄土高原地区不同土层中林木根系可利用的水分含量有很大的关系。梁一民等根据土壤水分将黄土高原地区土壤划分为分为4层[30],其中,0—20 cm土层被划分为微弱利用层,20—100 cm土层被划分为利用层;也即0—20 cm土层中可利用的水分要低于20—100 cm土层。研究发现,两林地表层(0—20 cm)土壤水分受降水影响较大,50 cm 土层以下土壤水分含量相对稳定,且在降水较少的时期高于表层土壤 (图 6,表 1)。
虽然两林地细根的活跃区主要存在于50 cm土层以下,但在50—100 cm土层中,其最大细根SC出现的位置并不一致,在所有观测年内,成林最大细根SC位于50—60 cm土层,而幼林最大细根SC则从观测期初的90—100 cm土层向观测期末的80—90 cm土层分布。王孟本等对晋西北黄土丘陵沟壑区人工林生态系统水分平衡的研究中发现,降水对黄土丘陵区土壤水分的补给较少,因而柠条林土壤水分收支的亏缺经常发生[31],结合本研究中两林地年际间土壤水分的垂直分布变化(图 6),可以推测,由于与其他土层相比,幼林地80—100 cm土层土壤水分年际间变化较小,该层土壤持水力较强,水分含量较高,出于在水分亏缺情况下对土壤水分的“觅食”,幼林细根SC分布于最深层土壤;随着林龄的增长,深层土壤中细根周转增加,柠条细根与土壤之间的物质交换加快,进而使深层土壤的营养状况有所改善,土壤持水力进一步加强,出于对土壤物理化学结构的适应,柠条细根向更上层土壤分布。
Claus等在对欧洲森林生态系统细根研究中发现,不同林龄的3个树种0—10 cm土层中细根生物量差异显著,而10—30 cm土层并未发现任何差异[32]。在黄土高原地区,Chang等发现刺槐(Robinia pseudoacacia)人工林细根生物量在0—100 cm土层中随林龄增长而增加[28]。本研究发现,从2009年6月到观测期结束,成林0—100 cm土层细根SC均高于幼林,在表层(0—20 cm)土壤,出现这种现象的原因一方面是由于成林冠层淋溶物、表层枯落物等较幼林多,进而使得成林土壤表层比幼林具有更高的养分,另一方面,柠条是固氮植物,其土壤表层会随着林龄的增加而具有更高的土壤有机质以及氮含量;而深层(20—80 cm)土壤中,则可能是由于对水分的竞争,成林细根对水分的竞争力要优于幼林。
与Makkonen等的研究结果相似[33],2008—2011年间,在大多数的土层,两林地每年年初(3—4月)会出现相对较高的细根SC的增长,一方面,冬季微小的细根生长会引起年初细根SC的增加,另一方面,早春地上部分对养分和水分的需求尚低,根系生产在对养分和水分的竞争中占优势,进而导致细根SC的积累[33]。
在温带地区,土壤水分和土壤温度的变化会使土壤的营养结构发生变化,进而使得细根对土壤中营养物质的获取能力具有季节性[34-35]。在细根生活史中,一个细根能否正常行使其功能常随土壤环境的变化而变化。研究发现,同一生态系统中的不同物种会对环境做出不同的响应[36],比如土壤温度对欧洲山毛榉(Fagus sylvatica)细根生长的影响要比土壤水分大[36],而这两种环境因子对欧洲云杉(Picea abies)的影响则反之。本研究发现,每观测年内,幼林地30—100 cm土层出现细根SC最大值的时间均较成林地为早,同时,每观测年的生长季末,幼林细根SC下降较成林快。这种现象可能与土壤温度变化有关,如图 5显示,幼林地各土层土壤温度均高于成林,在季节变化中,幼林各层土壤升温较成林快,使得细根生长更早获得适合的温度,进而更早出现年度内细根SC的最大积累。而每年季末,由于幼林细根对温度变化的响应比成林更敏感,幼林细根SC迅速下降。本研究仅发现各观测年内成林细根SC与土壤温度的显著相关性,这可能是由于幼林细根SC在生长季初与季末的较大变化导致了年度水平上与土壤温度较差的相关性。本研究并未发现细根现存量的季节变化与土壤水分的显著相关性,二者表现出不显著的负相关。张帆等的研究中也发现了类似的现象[18]。出现这种负相关的原因可能是:在黄土高原地区,土壤水分是植物生长的限制因子;当有更多的降水补给,土壤水分条件较好时,柠条不需要维持更多的细根现存量来获取土壤中的水分以供给植株生长需要,其细根生产与死亡增加,周转加快,更多的细根现存量用于和土壤中物质与能量的交换;当水分条件较差时,柠条需要维持更多的细根现存量以获取土壤中的水分,这时,细根生产与死亡减少,周转变慢,与土壤中物质和能量的交换减少。
2008年幼林细根SC在生长季的各个阶段均高于成林,2009年幼林与成林细根SC季节变化与其他观测年度有较大差异,这可能与这两年的降雨量有关。王孟本等参照山西省气象科学研究所对生长季降雨量进行了5级分类[37],按照该分类标准,观测期内2008年属于偏涝年,2009年属于偏旱年,其余两年为正常年(表 1)。如上所述,由于成林细根对水分的竞争力要优于幼林,幼林细根对水分的“觅食”需求更高。在偏涝年,幼林细根会迅速对水分条件发生响应,进而形成细根SC的大量积累,而在偏旱年,为了降低因蒸腾拉力等对有限水分的消耗,幼林细根大量死亡,造成细根SC的快速降低。2009年季末(9—10月),成林各土层细根SC均出现不同程度的增长,这应该是由于8月份出现的较高降水(表 1,图 4);而受季末低温的影响,幼林并未表现出明显的细根SC的积累。
综上所述,在垂直分布上,两林地最大细根SC均位于50 cm土层以下,且幼林分布更深,土壤水分在这种垂直分布格局中起关键作用,柠条成林细根对水分的竞争比幼林更具优势。季节上,由于土壤温度升温更快,幼林较成林更早达到最大细根SC。在年度水平,两林地细根SC均受年降雨量的影响,但幼林受年降雨量的影响更大。
| [1] | Jackson R B, Mooney H A, Schulze E D.A global budget for fine root biomass, surface area, and nutrient contents.Proceedings of the National Academy of Sciences of the United States of America,1997,94(14): 7362–7366. |
| [2] | Heljä-Sisko Helmisaari, Kirsi Makkonen, Seppo Kellomäki, Esko Valtonen, Eino Mälkönen.Below- and above-ground biomass, production and nitrogen use in Scots pine stands in eastern Finland.Forest Ecology and Management,2002,165(s1/3): 317–326. |
| [3] | Kristiina A Vogt, Daniel John Vogt, Peter A Palmiotto, Paul Boon, Jennifer O'Hara, Heidi Asbjornsen.Review of root dynamics in forest ecosystems grouped by climate, climatic forest type and species.Plant and Soil,1995,187(2): 159–219. |
| [4] | Richard A Gill, Robert B Jackson.Global patterns of root turnover for terrestrial ecosystems.New Phytologist,2000,147(1): 13–31. |
| [5] | Joseph J Hendricks, Ronald L Hendrick, Carlos A Wilson, Robert A Mitchell, Stephen D Pecot, Dali Guo.Assessing the patterns and controls of fine root dynamics:an empirical test and methodological review.Journal of Ecology,2006,94(1): 40–57. |
| [6] | Kuni Kitajima, Kurt E Anderson, Michael F Allen.Effect of soil temperature and soil water content on fine root turnover rate in a California mixed conifer ecosystem.Journal of Geophysical Research:Biogeosciences,2010,115(G4): 137–139. |
| [7] | Charles C Grier, Ballard T M.Biomass, nutrient distribution, and net production in alpine communities of the Kluane Mountains, Yukon Territory, Canada.Canadian Journal of Botany,1981,59(12): 2635–2649. |
| [8] | Jakub Olesinski, Marek J Krasowski, Michael B Lavigne, John A Kershaw, Pierre Y Bernier.Fine root production varies with climate in balsam fir (Abies balsamea).Canadian Journal of Forest Research,2012,42(2): 364–374. |
| [9] | Hans Persson.Fine-root production, mortality and decomposition in forest ecosystems.Vegetatio,1980,41(2): 101–109. |
| [10] | Hans Å Persson, Ingela Stadenberg.Fine root dynamics in a Norway spruce forest (Picea abies (L.) Karst) in eastern Sweden.Plant and Soil,2010,330(1/2): 329–344. |
| [11] | Jennifer M Withington, Peter B Reich, Jacek Oleksyn, David M Eissenstat.Comparisons of structure and life span in roots and leaves among temperate trees.Ecological Monographs,2006,76(3): 381–397. |
| [12] | 程杰, 王吉斌, 程积民, 罗宗宽.黄土高原柠条锦鸡儿灌木林生长的时空变异特征.林业科学,2013,49(1): 14–20. |
| [13] | Li X R.Influence of variation of soil spatial heterogeneity on vegetation restoratio.Science in China Series D:Earth Sciences,2005,48(11): 2020–2031. |
| [14] | Li X R, Ma F Y, Xiao H L, Wang X P, Kim K C.Long-term effects of revegetation on soil water content of sand dunes in arid region of Northern China.Journal of Arid Environments,2004,57(1): 1–16. |
| [15] | Wang X P, Constance M Brown-Mitic, Er-Si Kang, Zhang J G, Li X R.Evapotranspiration of Caragana korshinskii communities in a revegetated desert area:Tengger Desert, China.Hydrological processes,2004,18(17): 3293–3303. |
| [16] | Zhang Z S, Li X R, Liu L C, Jia R L, Zhang J G, Wang T.Distribution, biomass, and dynamics of roots in a revegetated stand of Caragana korshinskii in the Tengger Desert, northwestern China.Journal of Plant Research,2009,122(1): 109–119. |
| [17] | 荀俊杰, 李俊英, 陈建文, 史建伟, 王孟本.幼龄柠条细根现存量与环境因子的关系.植物生态学报,2009,33(4): 764–771. |
| [18] | 张帆, 陈建文, 王孟本.幼龄柠条细根的空间分布和季节动态.生态学报,2012,32(17): 5484–5493. |
| [19] | Johnson M G, Tingey D T, Phillips D L, Storm M J.Advancing fine root research with minirhizotrons.Environmental and Experimental Botany,2001,45(3): 263–289. |
| [20] | Christel C Kern, Alexander L Friend, Jane M-F Johnson, Mark D Coleman.Fine root dynamics in a developing Populus deltoides plantation.Tree physiology,2004,24(6): 651–660. |
| [21] | Jakub Olesinski, Michael B Lavigne, John A Kershaw Jr, Marek J Krasowski.Fine-root dynamics change during stand development and in response to thinning in balsam fir (Abies balsamea L. Mill.) forests.Forest Ecology and Management,2012,286 48–58. |
| [22] | Espeleta J F, Donovan L A.Fine root demography and morphology in response to soil resources availability among xeric and mesic sandhill tree species.Functional Ecology,2002,16(1): 113–121. |
| [23] | López B, Sabaté S, Gracia C A.Annual and seasonal changes in fine root biomass of a Quercus ilex L. forest.forest. Plant and Soil,2001,230(1): 125–134. |
| [24] | Reiji Fujimaki, Ryunosuke Tateno, Muneto Hirobe, Naoko Tokuchi, Hiroshi Takeda.Fine root mass in relation to soil N supply in a cool temperate forest.Ecological Research,2004,19(5): 559–562. |
| [25] | Marianne K Burke, Dudley J Raynal.Fine root growth phenology, production, and turnover in a northern hardwood forest ecosystem.Plant and Soil,1994,162(1): 135–146. |
| [26] | Bahu John, Harendra N Pandey, Radhey S Tripathi.Vertical distribution and seasonal changes of fine and coarse root mass in Pinus kesiya Royle Ex. Gordon forest of three different ages.Acta Oecologica,2001(5/6): 293–300. |
| [27] | 牛西午.柠条生物学特性研究.华北农学报,1998,13(4): 122–129. |
| [28] | Chang R Y, Fu B J, Liu G H, Yao X L, Wang S.Effects of soil physicochemical properties and stand age on fine root biomass and vertical distribution of plantation forests in the Loess Plateau of China.Ecological Research,2012,27(4): 827–836. |
| [29] | Gan Z T, Zhou Z C, Liu W Z.Vertical distribution and seasonal dynamics of fine root parameters for apple trees of different ages on the loess plateau of China.Agricultural Sciences in China,2010,9(1): 46–55. |
| [30] | 梁一民, 杨文治. 黄土高原人工林草地水分生态条件及生产力//杨文治, 余存祖. 黄土高原区域治理与评价. 北京: 科学出版社, 1992241–297. |
| [31] | 王孟本, 李洪建.晋西北黄土区人工林土壤水分动态的定量研究.生态学报,1995,15(2): 178–184. |
| [32] | Claus A, George E.Effect of stand age on fine-root biomass and biomass distribution in three European forest chronosequences.Canadian Journal of Forest Research,2005,35(7): 1617–1625. |
| [33] | Kirsi Makkonen, Heljä-Sisko Helmisaari.Seasonal and yearly variations of fine-root biomass and necromass in a Scots pine (Pinus sylvestris L.) stand.Forest Ecology and Management,1998,102(2/3): 283–290. |
| [34] | Shih-Chieh Chang, Egbert Matzner.Soil nitrogen turnover in proximal and distal stem areas of European beech trees.Plant and Soil,2000,218(1): 117–125. |
| [35] | Heinz Coners, Christoph Leuschner.In situ measurement of fine root water absorption in three temperate tree species-temporal variability and control by soil and atmospheric factors.Basic and Applied Ecology,2005,6(4): 395–405. |
| [36] | Raphael Mainiero, Marian Kazda, Iris Schmid.Fine root dynamics in 60-year-old stands of Fagus sylvatica and Picea abies growing on haplic luvisol soil.European Journal of Forest Research,2010,129(6): 1001–1009. |
| [37] | 王孟本, 李洪建. 黄土高原人工林水分生态研究. 北京: 中国林业出版社, 200130–31. |
 2016, Vol. 36
2016, Vol. 36