文章信息
- 宁秋蕊, 李守中, 姜良超, 赵颖, 刘溶, 张欣影
- NING Qiurui, LI Shouzhong, JIANG Liangchao, ZHAO Ying, LIU Rong, ZHANG Xinying.
- 亚热带红壤侵蚀区马尾松针叶养分含量及再吸收特征
- Foliar nutrient content and resorption efficiency of Pinus massoniana in the subtropical red soil erosion region
- 生态学报[J]. 2016, 36(12): 3510-3517
- Acta Ecologica Sinica[J]. 2016, 36(12): 3510-3517
- http://dx.doi.org/10.5846/stxb201506301380
-
文章历史
- 收稿日期: 2015-06-30
- 修订日期: 2016-02-16
2. 福建师范大学地理科学学院, 福州 350007;
3. 中央民族大学生命与环境科学学院, 北京 100081
2. School of Geographical Science, Fujian Normal University, Fuzhou 350007, China;
3. College of life and Environmental Sciences, Minzu University of China, Beijing 100081, China
植物对生长环境的适应对策是多种多样的,在自然界中形成了特定的适应性策略以抵抗胁迫环境。生长在养分受限制的地区,植被通常表现出两种适应策略:最优化养分需求或减少养分损失[1]。为最小化养分损失产生一系列适应特征如:降低淋溶造成的养分损失、叶片衰老过程中有效的养分转移、延长叶片或其他组织寿命[2-3]等。养分再吸收是指养分从凋落叶中转移到植物其他组织器官中的过程[4-5],是养分循环的重要组成部分[6],通常用养分再吸收效率(NRE)表示[4, 7]。养分再吸收可以降低植物对土壤养分的依赖性[8-9],被普遍认为是植物适应贫瘠环境的重要策略之一,因而一直是生态学者关注的热点领域[4-5, 8-13]。
关于养分再吸收的研究始于20世纪30年代[4],已有众多学者开展了养分再吸收过程发生机制和影响因素的相关研究,发现影响叶片养分含量及再吸收效率的主要因素有:叶寿命长短[14]、源-汇关系[10, 15]、土壤养分含量[11, 16]、植物生活型[5, 8-9],叶片养分含量[17-18]等。养分再吸收在植物养分保存方面具有重要作用,因此有学者猜测,生长在低土壤养分环境中的植物具有更高的再吸收效率[19-20],也有研究通过人为施肥发现养分再吸收效率随土壤养分含量的增加表现出下降的趋势[21-22],但养分再吸收对土壤养分可利用性的响应目前一直没有定论[23]。另一方面养分再吸收可以反映植物养分限制情况[24],有研究表明在低养分条件下更倾向于生长缓慢、叶片养分含量较低的植物[25],当其生长受到某种元素限制时会表现出对该元素具有较高的再吸收效率[19, 26-27],随养分可利用性的提高,逐渐被具有较高叶片养分含量的物种所替代。
马尾松(Pinus massoniana)具有耐干旱、耐贫瘠等适应性特征[28],是我国南方红壤侵蚀退化区生态恢复的先锋树种,且居全国针叶林面积首位[29]。目前关于马尾松养分循环的研究主要集中在外循环方面,探讨凋落物产量、组分与养分归还量的问题[30-32],对其内循环机制缺乏深入了解,仅有部分研究揭示了林龄[33-34]、密度[35]等对马尾松叶片养分含量及再吸收的影响,尚缺乏从生态恢复角度的相关研究。本文通过分析马尾松不同叶龄阶段针叶养分含量及再吸收特征,探讨叶片养分含量与生境恢复水平、叶龄的关系及养分再吸收机制,以期为红壤侵蚀退化区生态恢复及其养分管理提供理论指导。
1 研究地区与研究方法 1.1 研究区概况研究区位于福建省长汀县河田镇(25°33′—25°48′ N,116°18′—116°31′ E),地处武夷山脉南段河田盆地内,平均海拔高度238 m,是典型的低山丘陵地貌[36]。气候属湿润的中亚热带季风气候,多年平均气温17.5—18.8℃,年降水量1700—2000 mm。土壤主要是花岗岩母质上发育的山地红壤,石英含量高、抗蚀性差、保水保肥能力低[37]。地带性植被为中亚热带常绿阔叶林,主要以壳斗科、樟科、山茶科、蔷薇科等为主[38]。由于长期的人类活动干扰和水土流失,植被多已退化成疏地林、亚热带灌丛或无地林[39-40],在侵蚀退化较为严重地区生长着大面积发育滞缓的马尾松,在极强度侵蚀退化区则形成“小老头松”林。
1.2 研究方法 1.2.1 样地设置综合考虑植被群落结构特征、优势种平均长势、植被覆盖度等指标,选取伯湖、马坑、水东坊、罗地4个不同恢复水平的样地,分别用Ⅰ、Ⅱ、Ⅲ、Ⅳ表示。样地概况如下表 1。
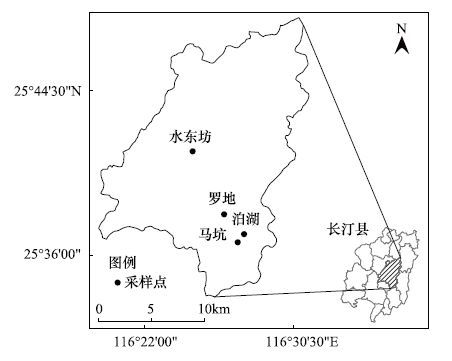
|
| 图 1 研究区地理位置及样地分布图 Fig. 1 Location of studied area and plots |
| 样地 Plots | 位置 Site | 植被群落结构特征 Characteristics of vegetation community structure | 树高/m Height | 胸径/cm DBH | 植被盖度/% Coverage | 全氮、全磷、 全钾/(g/kg) Total N、P、K |
| 伯湖Ⅰ | 25°37.06′N 116°27.61′E | 乔木以少量低矮的马尾松小老头树和大量马尾松幼苗为主;灌木层有稀少的黄瑞木(Adinandra millettii)和小叶赤楠(Sysgium grijsii) | 1.1±0.2 | 3.2±0.1 | 30 | 0.33±0.01 0.06±0.01 1.92±0.23 |
| 马坑Ⅱ | 25°36.64′N 116°26.63′E | 乔木层以高度中等的马尾松和低矮的杨梅为主;灌木层有少量的黄瑞木。草本层以芒萁(Dicranopteris dichotoma)为主,存在少量的其他草本植物。 | 2.7±0.5 | 4.5±0.2 | 45 | 0.26±0.01 0.10±0.01 1.22±0.20 |
| 水东坊Ⅲ | 25°41.32′N 116°24.65′E | 乔木层以马尾松为主,少量阔叶树为辅;灌木层主要有黄瑞木和胡枝子(Lespedezabicolor);草本层以芒萁为主,有部分黑麦草(Lolium perenne)。 | 8.9±0.3 | 15.6±0.4 | 65 | 0.37±0.01 0.07±0.02 1.32±0.06 |
| 罗地Ⅳ | 25°38.09′N 116°26.48′E | 乔木层主要以高大的马尾松为主,以木荷、枫香、油茶为辅。灌木层有黄瑞木、胡枝子;草本层芒萁占绝对优势,还有少量的藤本植物羊角藤(Morinda umbellata)和狼尾草(Pennisetum alopecuroides) | 9.2±0.3 | 9.5±0.1 | 75 | 0.66±0.01 0.07±0.01 1.37±0.06 |
根据颜色梯度和距离枝条远近将叶片分为4个叶龄阶段:新生叶(嫩绿)、壮年叶(浅绿)、成熟叶(深绿)和凋落叶(黄色)。于2014年7月马尾松生长旺季,在4个样地分别采集马尾松各叶龄阶段针叶样品。每个样品约100 g,为采自树冠中部东、西、南、北4个方位的混合样,每个叶龄阶段的针叶样品设3个重复。
在每个样地随机确定6个样点,分别采集表层土壤(0—10 cm)样品带回实验室测定养分含量。
1.2.3 样品处理与养分元素测定植物样品经杀青、烘干、粉碎、过筛、消煮(H2SO4-HClO4)后留待养分含量测定。叶片氮含量采用CHNOS元素分析仪(Elemental Analyzer Vario EL III,德国)测定,磷含量测定采用连续流动分析仪(SKALAR SAN++,荷兰),钾含量用火焰光度法测定(FP-640型火焰光度计,上海精密科学仪器公司)。土壤养分含量测定参照植物样品的测定方法。
1.3 数据处理及计算方法根据Fife和Schlesinger等[41-42]研究表明,叶片衰老过程中质量变化不大,针叶变化量约为1%,阔叶变化量在10%左右,对于针叶树种马尾松因质量减少导致基于单位质量的养分再吸收效率偏低而产生的误差可以忽略不计[33]。综合考虑,本文选取基于单位质量养分含量(mg/g)计算养分再吸收效率,公式如下[11]:
养分再吸收效率(%)=(绿叶的最高养分含量-落叶的养分含量)/绿叶的最高养分含量×100%
利用Excel 2013和SPSS 16.0进行数据的统计计算和相关分析,采用单因素方差分析(One-way ANOVA)和最小显著差异法LSD检验各组数据间的显著差异性。
2 结果与分析 2.1 马尾松针叶养分含量动态变化从表 2可以看出,4个不同恢复水平样地间N、P含量的大小顺序依次为:Ⅳ>Ⅱ>Ⅲ>Ⅰ,K在各样地间的高低顺序为:Ⅲ>Ⅳ>Ⅱ>Ⅰ,各叶龄阶段叶片的养分含量均随生境恢复水平的提高而增大,在样地间存在不同程度的差异。其中,新生叶N、P、K含量在不同样地间差异最大,凋落叶间差异较小。这表明叶片养分含量不仅随生境条件的改变而变化,同时还受到叶龄的影响。
| 元素 Element | 叶龄 Leaf ages | Ⅰ (伯湖) | Ⅱ (马坑) | Ⅲ (水东坊) | Ⅳ (罗地) |
| N/(mg/g) | 新生叶 | 8.47±0.32Aa | 9.94±0.51Ba | 9.15±0.85ABa | 11.09±0.50Ca |
| 壮年叶 | 9.59±0.64Ab | 9.97±0.89Aa | 9.97±0.39Aa | 12.02±0.85Ba | |
| 成熟叶 | 8.54±0.65Aa | 9.16±0.52Aa | 9.25±0.42Aa | 11.82±1.69Ba | |
| 凋落叶 | 6.66±0.17ABc | 6.10±0.52Ab | 6.44±0.53ABb | 7.29±0.83Bb | |
| 均值 | 8.32±1.19 | 8.79±1.74 | 8.70±1.49 | 10.47±2.09 | |
| P/(mg/g) | 新生叶 | 0.46±0.06Aa | 0.62±0.11Ba | 0.55±0.03ABa | 1.02±0.01Ca |
| 壮年叶 | 0.48±0.06Aa | 0.62±0.11Ba | 0.53±0.04ABa | 1.00±0.07Ca | |
| 成熟叶 | 0.34±0.04Ab | 0.46±0.03Bb | 0.36±0.02Ab | 0.64±0.04Cb | |
| 凋落叶 | 0.17±0.03Ac | 0.19±0.02Ac | 0.23±0.12Ac | 0.28±0.06Ac | |
| 均值 | 0.36±0.14 | 0.47±0.20 | 0.42±0.15 | 0.74±0.32 | |
| K/(mg/g) | 新生叶 | 6.97±0.32Aa | 7.67±1.51ABa | 9.46±0.90Ba | 8.52±1.04ABa |
| 壮年叶 | 7.43±1.23Aa | 7.91±1.18ABa | 9.43±0.71Ba | 7.74±0.84ABa | |
| 成熟叶 | 3.75±0.19Ab | 3.56±0.99Ab | 4.49±0.28Ab | 3.99±0.51Ab | |
| 凋落叶 | 2.25±0.12ABc | 1.58±0.49Ab | 2.89±1.11Bc | 1.97±0.60ABc | |
| 均值 | 5.10±2.33 | 5.18±2.98 | 6.57±3.14 | 5.55±2.98 | |
| 同列不同小写字母表示差异显著,同行不同大写字母表示差异显著(P<0.05) | |||||
在叶片生活史的4个阶段中,叶片养分含量在所有样地整体呈“先增加后降低”的变化趋势(表 2),即从新生叶到壮年叶,叶片养分含量快速累积到最大值,从壮年叶到成熟叶、凋落叶的过程中养分含量逐渐降低。该动态规律以N表现最为明显,P和K的变化趋势与N相似,但变化幅度相对较小。在叶片生活史的不同阶段,各样地间叶片养分含量的差异性随叶龄增大逐渐减小。叶片凋落前N含量在各叶龄阶段的差异很小,除I样地外,其余3个样地上各叶龄阶段叶片N含量均无显著差异(P>0.05) 。K含量在壮年叶到成熟叶的过程中大量减少,凋落前变化相对平缓。这表明,在新生叶到凋落叶的整个叶片生活史中,叶片养分含量具有一个快速积累期和一个相对漫长衰减期的动态特征。
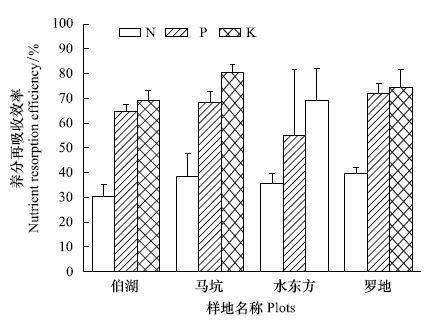
2.2 马尾松针叶凋落前再吸收效率特征如图 2所示,样地间N、P和K再吸收效率分别为(30.34±4.77) %—(39.50±2.63) %、(54.90±26.58) %—(71.83±4.08) %和(69.05±12.98) %—(80.34±3.15) %,各元素再吸收效率大小排序为:K>P>N。N、P再吸收效率最高值出现在样地Ⅳ,K再吸收效率最高值出现在样地Ⅱ,四个不同恢复水平样地间N、P、K再吸收效率均无显著差异(P>0.05) 。
|
| 图 2 不同恢复水平下马尾松针叶凋落前后养分再吸收效率 Fig. 2 Foliar nutrient resorption efficiencies of P. massoniana trees at different restoration levels (mean±SD) |
不同叶龄马尾松叶片中N、P、K含量与其再吸收效率之间的相关系数和回归方程如表 3所示。新生叶、壮年叶、成熟叶的N、P含量均表现出显著相关(P<0.05) ,凋落叶中P、K含量存在显著相关性(P<0.05) ,其它叶龄阶段叶片各元素含量的相关性不显著。N、P再吸收效率与各叶龄阶段叶片的养分含量并未表现出显著相关,K再吸收效率与凋落叶的养分含量达到极显著相关水平(P<0.01) 。
| Y-X | 回归方程Equation | n | r | Y-X | 回归方程Equation | n | r |
| Nn-Pn | Y=4.060x+6.971 | 12 | 0.830* | REN-Nn | Y=2.855x+8.298 | 12 | 0.509 |
| Nq-Pq | Y=4.425x+7.477 | 12 | 0.838* | REN-Nq | Y=3.025x+4.474 | 12 | 0.554 |
| Nm-Pm | Y=8.939x+5.566 | 12 | 0.840* | REN-Nm | Y=1.719x+19.377 | 12 | 0.364 |
| Ns-Ps | Y=3.699x+5.808 | 12 | 0.413 | REN-Ns | Y=-3.419x+58.532 | 12 | -0.355 |
| Kn-Nn | Y=0.119x+7.004 | 12 | 0.103 | REP-Pn | Y=20.452x+51.407 | 12 | 0.353 |
| Kq-Nq | Y=-0.186x+10.054 | 12 | -0.183 | REP-Pq | Y=23.371x+49.606 | 12 | 0.383 |
| Km-Nm | Y=-0.049x+4.412 | 12 | -0.106 | REP-Pm | Y=37.011x+48.225 | 12 | 0.349 |
| Ks-Ns | Y=-0.117x+1.397 | 12 | 0.101 | REP-Ps | Y=-105.172x+88.111 | 12 | -0.577 |
| Pn-Kn | Y=0.056x+0.206 | 12 | 0.318 | REK-Kn | Y=0.380x+70.206 | 12 | 0.061 |
| Pq-Kq | Y=-0.002x+0.677 | 12 | -0.013 | REK-Kq | Y=-0.073x+73.893 | 12 | 0.010 |
| Pm-Km | Y=-0.012x+0.500 | 12 | -0.059 | REK-Km | Y=-0.922x+76.944 | 12 | 0.069 |
| Ps-Ks | Y=0.057x+0.095 | 12 | 0.596* | REK-Ks | Y=-9.766x+94.499 | 12 | -0.906** |
| Nn,Pn,Kn表示新生叶中N、P、K含量;Nq,Pq,Kq表示壮年叶中N、P、K含量;Nm,Pm,Km表示成熟叶中N、P、K含量;Ns,Ps,Ks表示凋落叶中N、P、K含量;REN,REP,REK表示N、P、K再吸收效率;*P<0.05,**P<0.01 | |||||||
叶片养分含量受叶龄的影响,又因各元素生理作用不同,使其含量存在一定差异。在新生叶到凋落叶的整个叶片生活史中,N、P、K含量呈“先增加后降低”的变化趋势,表现为一个养分快速积累期和一个相对漫长的衰减期。在叶片生长初期(即叶龄较小的阶段),叶肉细胞具有较强的分裂能力,需要大量蛋白质和核酸以满足自身的快速生长,对N、P选择吸收较多。另一方面,K具有促进碳水化合物的代谢、利于氨基酸的形成等重要作用,因此在生长初期含量不断升高。从壮年叶到凋落叶的过程中养分含量逐渐降低是发生了养分再吸收,这一过程的存在已得到大量研究证实[4, 8, 11]。较大程度的再吸收使养分能够存留在植物体内参与内循环重新被利用,是马尾松适应养分贫瘠环境的主要对策之一。在叶片衰老呼吸过程中会消耗大量碳水化合物、核酸等并将其降解为小分子随植物体内的溶液外运到其他组织部分,或因光合作用在碳水化合物增加的同时产生了稀释效应,导致养分含量不断降低[16, 43]。
叶片养分含量因生境恢复水平不同而发生改变。与现有研究中马尾松针叶养分含量比较,本研究中 N、P含量普遍偏低,K含量却高于其他地区[33-35],这主要是受到元素本身性质及研究区特殊生境条件的影响。严重的水土流失造成养分贫瘠的土壤环境,同时P作为一种累积型元素在山区表现出较为严重的缺失状态,成为限制植物生长的元素[44]。K含量较高可能是受研究区土壤类型、母质等因素的影响[45]。随生境条件的改善,叶片中P元素含量增加最明显,同时在凋落叶中的含量也低于另外两种元素,反映出马尾松为适应P贫瘠的生境条件提高了对P元素的再吸收能力。
叶片养分含量动态变化中各元素具有协同作用。本研究中除凋落叶外,其他叶龄阶段N、P之间均达到显著相关水平,这表明在叶片生长发育过程中N、P的动态变化存在较强的协同性,与现有研究结果一致[46-49]。N和P是限制植物生长和初级生产力的基础营养元素,是细胞核、细胞膜、ATP等的主要组成物质,在许多生态系统中均是协同变化,共同影响生态系统平衡[49]。叶片养分含量也对养分再吸收产生一定影响,Fife等[41]和Saur等[47]认为两者存在正相关关系,也有研究表明两者表现为负相关[50]或不相关[51],研究结果不一致可能是受植物养分利用特性或是生境不同的影响。研究中凋落叶N含量低,但其再吸收效率相比于P和K两种元素并不高,可能是因为植物可以通过土壤养分源以外的途径获取生长所需的基本氮素,同时受红壤侵蚀退化区养分可利用性较低的限制使叶片衰老前N含量就偏低。
3.2 叶片养分再吸收与贫瘠生境的关系养分再吸收被普遍视为植物适应贫瘠环境的一种生长和竞争策略,一般认为生活在贫瘠生境中的植物比生活在土壤条件较好中的植物具有更高的养分再吸收效率,但也有研究表明这种观点是存在争议的[22, 52],这可能是物种固有特征[15],在养分贫瘠环境下,植物选择的策略更倾向于延长叶片寿命或是降低凋落叶养分含量[14, 52]。本研究得到的结果显示两者没有必然联系,恢复水平较低的Ⅰ样地养分再吸收效率并非最高,这可能受到研究区现阶段仍处于恢复早期的影响,生态恢复水平有限,植物并不能完全依赖土壤养分供给以满足生长的营养需求,叶片养分再吸收仍具有重要作用。可能存在这样一种情况,当水土流失区生态恢复到后期,土壤养分不再作为一种稀缺资源时,养分再吸收效率会随生境恢复水平的提高而降低,可以通过人为施肥模拟恢复后期的土壤养分状况,进一步探讨马尾松叶片养分再吸收效率与生境恢复水平的关系。
不同恢复水平下马尾松针叶N、P、K三种元素再吸收效率高低顺序为K>P>N。普遍认为P是热带山区植物生长的主要限制元素[44],不同恢复水平下马尾松针叶P较高的再吸收效率是对这一营养元素限制做出的反馈调节。K在细胞中起调节渗透压的作用,Ruuhola等[53]指出为保证叶片在凋落前完成其他养分元素的再吸收,K可能需要一直调节细胞渗透压直到其他元素完成再吸收,本研究中马尾松针叶较高的K含量利于在P贫瘠环境中对P的再吸收。植物获取N的途径不唯一,可通过根部吸收土壤中的养分,另外大气氮沉降也是植物氮素的重要来源,这可能是本研究中N再吸收效率相对较低的主要原因。叶片中重要元素的协同变化是植物体内养分元素平衡的表现,但因不同生境条件下土壤环境中的各养分元素含量不同,同时叶片在不同生长阶段对营养元素的吸收具有选择性,造成叶片N/P随生境和叶龄的改变而变化(表 4)。有研究指出当植物生长受到P限制时,会加强对P的再吸收,同时衰老叶N/P会比新生叶更大[26],随叶龄的增长马尾松针叶N/P逐渐增大,凋落前变化幅度最大,这可能受到养分大量转移的影响。总之,植物为维持体内重要营养元素的平衡倾向于对生境中较为贫瘠或使其生长受到限制的元素具有较高的再吸收效率。
| 样地 Plots | 新生叶 New foliage | 壮年叶 Prime foliage | 成熟叶 Mature foliage | 凋落叶 Senescent foliage |
| 伯湖 Ⅰ | 18.65±2.73 | 20.25±2.95 | 25.26±3.51 | 40.08±8.53 |
| 马坑 Ⅱ | 16.34±2.85 | 16.26±1.38 | 19.90±2.00 | 32.15±6.78 |
| 水东坊 Ⅲ | 16.78±1.89 | 18.97±1.99 | 25.61±2.04 | 31.45±10.72 |
| 罗地 Ⅳ | 10.85±0.37 | 12.10±1.50 | 17.88±0.86 | 26.54±6.22 |
| 均值Mean | 15.65±3.57 | 16.89±3.70 | 22.16±6.22 | 32.56±8.67 |
(1) 马尾松叶片N、P、K含量因生境条件不同而发生变化,表现出随生境恢复水平的提高而提高。叶龄也是影响叶片养分含量的一个重要因素,在新生叶到凋落叶的整个叶片生活史中,叶片养分含量具有一个快速积累期和一个相对漫长衰减期的动态特征。
(2) 叶片养分元素动态变化中具有协同作用,除凋落叶外,其他叶龄阶段N、P之间均达到显著相关水平(P<0.05) 。这表明,在叶片生长发育过程中N、P存在较强的协同性,重要元素的协同变化是植物体内营养元素平衡的表现。
(3) 马尾松N、P、K再吸收效率由高到低依次为:K、P、N,较高的再吸收效率是对贫瘠生境中养分限制做出的反馈调节,选择性再吸收限制元素是植物维持体内重要营养元素平衡的一个对策。研究区N再吸收效率相对较低,这表明叶片养分再吸收效率不仅与生境条件有关,同时还与营养元素的获取途径有关。
致谢: 李守丽、罗金明、奉小明、徐凯健帮助写作,康佩佩帮助做图,特此致谢。| [1] | Freschet G T, Cornelissen J H C, van Logtestijn R S P, Aerts R.Substantial nutrient resorption from leaves, stems and roots in a subarctic flora:what is the link with other resource economics traits?.New Phytologist,2010,186(4): 879–889. |
| [2] | Escudero A, del Arco J M, Sanz I C, Ayala J.Effects of leaf longevity and retranslocation efficiency on the retention time of nutrients in the leaf biomass of different woody species.Oecologia,1992,90(1): 80–87. |
| [3] | Reich P B, Walters M B, Ellsworth D S.Leaf life-span in relation to leaf, plant, and stand characteristics among diverse ecosystems.Ecological Monographs,1992,62(3): 365–392. |
| [4] | Killingbeck K T.The terminological jungle revisited:making a case for use of the term resorption.Oikos,1986,46(2): 263–264. |
| [5] | Aerts R.Nutrient resorption from senescing leaves of perennials:are there general patterns?.Journal of Ecology,1996,84(4): 597–608. |
| [6] | Côté B, Fyles J W, Djalilvand H.Increasing N and P resorption efficiency and proficiency in northern deciduous hardwoods with decreasing foliar N and P concentrations.Annals of Forest Science,2002,59(3): 275–281. |
| [7] | van Heerwaarden L M, Toet S, Aerts R.Current measures of nutrient resorption efficiency lead to a substantial underestimation of real resorption efficiency:facts and solutions.Oikos,2003,101(3): 664–669. |
| [8] | 李志安, 邹碧, 曹裕松, 沈承德, 孙彦敏, 杜卫兵, 李勤奋.华南两种豆科人工林体内养分转移特性.生态学报,2003,23(7): 1395–1402. |
| [9] | Killingbeck K T.Nutrients in senesced leaves:keys to the search for potential resorption and resorption proficiency.Ecology,1996,77(6): 1716–1727. |
| [10] | Tully K L, Wood T E, Schwantes A M, Lawrence D.Soil nutrient availability and reproductive effort drive patterns in nutrient resorption in Pentaclethra macroloba.Ecology,2013,94(4): 930–940. |
| [11] | 刘佳庆, 王晓雨, 郭焱, 王守乐, 周莉, 代力民, 于大炮.长白山林线主要木本植物叶片养分的季节动态及回收效率.生态学报,2015,35(1): 165–171. |
| [12] | 李志安, 王伯荪, 林永标, 曾友特.植物营养转移研究进展.武汉植物学研究,2000,18(3): 229–236. |
| [13] | 苏波, 韩兴国, 黄建辉, 渠春梅.植物的养分利用效率(NUE)及植物对养分胁迫环境的适应策略.生态学报,2000,20(2): 335–343. |
| [14] | Wright I J, Westoby M.Nutrient concentration, resorption and lifespan:leaf traits of Australian sclerophyll species.Functional Ecology,2003,17(1): 10–19. |
| [15] | Nambiar E K S, Fife D N.Growth and nutrient retranslocation in needles of Radiata pine in relation to nitrogen supply.Annals of Botany,1987,60(2): 147–156. |
| [16] | 赵琼, 刘兴宇, 胡亚林, 曾德慧.氮添加对兴安落叶松养分分配和再吸收效率的影响.林业科学,2010,46(5): 14–19. |
| [17] | Kobe R K, Lepczyk C A, Iyer M.Resorption efficiency decreases with increasing green leaf nutrients in a global data set.Ecology,2005,86(10): 2780–2792. |
| [18] | Huang J J, Wang X H, Yan E R.Leaf nutrient concentration, nutrient resorption and litter decomposition in an evergreen broad-leaved forest in eastern China.Forest Ecology and Management,2007,239(1/3): 150–158. |
| [19] | Jiang C M, Yu G R, Li Y N, Cao G M, Yang Z P, Sheng W P, Yu W T.Nutrient resorption of coexistence species in alpine meadow of the Qinghai-Tibetan Plateau explains plant adaptation to nutrient-poor environment.Ecological Engineering,2012,44 1–9. |
| [20] | Ralhan P K, Singh S P.Dynamics of nutrients and leaf mass in central Himalayan forest trees and shrubs.Ecology,1987,68(6): 1974–1983. |
| [21] | Norris M D, Reich P B.Modest enhancement of nitrogen conservation via retranslocation in response to gradients in N supply and leaf N status.Plant and Soil,2009,316(1/2): 193–204. |
| [22] | Yuan Z Y, Chen H Y H.Negative effects of fertilization on plant nutrient resorption.Ecology,2015,96(2): 373–380. |
| [23] | Lü X T, Han X G.Nutrient resorption responses to water and nitrogen amendment in semi-arid grassland of Inner Mongolia, China.Plant and Soil,2010,327(1/2): 481–491. |
| [24] | Reed S C, Townsend A R, Davidson E A, Cleveland C C.Stoichiometric patterns in foliar nutrient resorption across multiple scales.New Phytologist,2012,196(1): 173–180. |
| [25] | Aerts R, Chapin III F S.The mineral nutrition of wild plants revisited:a re-evaluation of processes and patterns.Advances in Ecological Research,1999,30 1–67. |
| [26] | Yuan Z Y, Chen H Y H.Global-scale patterns of nutrient resorption associated with latitude, temperature and precipitation.Global Ecology and Biogeography,2009,18(1): 11–18. |
| [27] | Rejmánková E.Nutrient resorption in wetland macrophytes:comparison across several regions of different nutrient status.New Phytologist,2005,167(2): 471–482. |
| [28] | 周政贤. 中国马尾松. 北京: 中国林业出版社, 2001. |
| [29] | 肖祥希.马尾松人工林生态系统养分特性的研究.福建林业科技,2000,27(4): 14–18. |
| [30] | 杨会侠, 汪思龙, 范冰, 张伟东.不同林龄马尾松人工林年凋落量与养分归还动态.生态学杂志,2010,29(12): 2334–2340. |
| [31] | 莫江明, 彭少麟, BrownS, 方运霆, 孔国辉.鼎湖山马尾松林植物养分积累动态及其对人为干扰的响应.植物生态学报,2004,28(6): 810–822. |
| [32] | 项文化, 田大伦.不同年龄阶段马尾松人工林养分循环的研究.植物生态学报,2002,26(1): 89–95. |
| [33] | 李荣华, 汪思龙, 王清奎.不同林龄马尾松针叶凋落前后养分含量及回收特征.应用生态学报,2008,19(7): 1443–1447. |
| [34] | 庄亚珍.不同林龄马尾松针叶养分含量及其再吸收效率.安徽农学通报,2010,16(18): 27–28. |
| [35] | 郭峰, 周运超.不同密度马尾松林针叶养分含量及其转移特征.南京林业大学学报:自然科学版,2010,34(4): 93–96. |
| [36] | 冯加昌. 南方典型红壤区水土保持-社会经济系统协调性研究[D]. 福州:福建师范大学, 2012. |
| [37] | 陈志彪. 花岗岩侵蚀山地生态重建及其生态环境效应[D]. 福州:福建师范大学, 2005. |
| [38] | 李守中, 余丽凡, 邹怡静, 陈金梅, 袁宏伟, 方舟易.长汀侵蚀退化地区生态恢复过程中植被多样性与土壤肥力的变化研究.安徽农学通报,2008,14(19): 49–51. |
| [39] | 曾月娥, 伍世代, 王强.南方丘陵生态脆弱区生态文明区划探讨——以长汀县为例.地理科学,2013,33(10): 1224–1230. |
| [40] | 江洪. 长汀县水土流失遥感监测及其生态安全评价[D]. 福州:福州大学, 2005. |
| [41] | Fife D N, Nambiar E K, Saur E.Retranslocation of foliar nutrients in evergreen tree species planted in a Mediterranean environment.Tree Physiology,2008,28(2): 187–196. |
| [42] | Schlesinger W H, DeLucia E H, Billings W D.Nutrient-use efficiency of woody plants on contrasting soils in the western Great Basin, Nevada.Ecology,1989,70(1): 105–113. |
| [43] | 理永霞, 茶正早, 罗微, 林钊沐, 贝美容.3种桉树幼苗叶片养分变化及其转移特性.林业科学,2009,45(1): 152–157. |
| [44] | 任书杰, 于贵瑞, 陶波, 王绍强.中国东部南北样带654种植物叶片氮和磷的化学计量学特征研究.环境科学,2007,28(12): 2665–2673. |
| [45] | 和继军, 蔡强国, 田磊, 方海燕.植被措施对土壤保育的作用及其影响因素分析.土壤通报,2010,41(3): 706–710. |
| [46] | ŁawniczakA E.Nitrogen, phosphorus, and potassium resorption efficiency and proficiency of four emergent macrophytes from nutrient-rich wetlands.Polish Journal of Environmental Studies,2011,20(5): 1227–1234. |
| [47] | Saur E, Nambiar E K S, Fife D N.Foliar nutrient retranslocation in Eucalyptus globulus.Tree Physiology,2000,20(16): 1105–1112. |
| [48] | 孙书存, 陈灵芝.东灵山地区辽东栎叶养分的季节动态与回收效率.植物生态学报,2001,25(1): 76–82. |
| [49] | 杨惠敏, 王冬梅.草-环境系统植物碳氮磷生态化学计量学及其对环境因子的响应研究进展.草业学报,2011,20(2): 244–252. |
| [50] | Vilela A.Resorption efficiency decreases with increasing green leaf nutrients in a global data set.Ecology,2005,86 2780–2792. |
| [51] | 叶功富, 张立华, 林益明, 王亨, 周海超, 曾琦.福建东山短枝木麻黄小枝氮磷含量及其再吸收率季节动态.生态学报,2009,29(12): 6519–6526. |
| [52] | 张林, 罗天祥.植物叶寿命及其相关叶性状的生态学研究进展.植物生态学报,2004,28(6): 844–852. |
| [53] | Ruuhola T, Leppänen T, Lehto T.Retranslocation of nutrients in relation to boron availability during leaf senescence of Betula pendula Roth.Plant and Soil,2011,344(1/2): 227–240. |
 2016, Vol. 36
2016, Vol. 36