文章信息
- 张中峰, 张金池, 黄玉清, 徐广平, 张德楠, 俞元春
- ZHANG Zhongfeng, ZHANG Jinchi, HUANG Yuqing, XU Guangping, ZHANG Denan, YU Yuanchun.
- 接种菌根真菌对青冈栎幼苗耐旱性的影响
- Effects of mycorrhizal fungi on the drought tolerance of Cyclobalanopsis glauca seedlings
- 生态学报[J]. 2016, 36(11): 3402-3410
- Acta Ecologica Sinica[J]. 2016, 36(11): 3402-3410
- http://dx.doi.org/10.5846/stxb201506261301
-
文章历史
- 收稿日期: 2015-06-26
- 修订日期: 2015-11-30
2. 南京林业大学林学院, 南京 210037
2. College of Forestry, Nanjing Forestry University, Nanjing 210037, China
中国西南岩溶地区由于存在双层地质结构,土层薄且分布不连续,土壤贫瘠干旱造成植被恢复困难,以石漠化为典型代表的生态退化成为制约该地区发展的重大生态环境问题[1-2]。研究发现,菌根真菌的生态学作用与石漠化退化生态系统的限制因子之间有着良好的耦合关系[3-4]。石漠化地区土壤普遍缺磷、富钙,同时存在地质性干旱,而菌根能够通过菌丝体网络扩大根系吸收范围,促进植物对土壤水分和营养元素,尤其是磷的吸收,促进植物生长,提高宿主植物的耐旱性[5-7],因此菌根真菌在石漠化治理上具有很强的潜在应用价值。有学者分别对喀斯特地区植物构树[8]、香樟[9]、光皮树[10]、滇柏和楸树[11]等进行了接种菌根真菌研究,发现接种菌根能促进喀斯特地区植物的养分吸收和光合能力,使植物耐旱性增强,提高造林树种在干旱逆境下的成活率。青冈栎(Cyclobalanopsis glauca)是壳斗科栎属常绿乔木,是中亚热带常绿阔叶林的代表性群落类型之一,是西南喀斯特地区常用的造林树种。壳斗科植物是典型的外生菌根植物,通常被认为易形成外生菌根而不宜形成丛枝菌根[12-13],但近年来研究表明[14-18],壳斗科植物的幼苗能被丛枝菌根真菌侵染形成菌根共生体,并产生显著的菌根效应。本文通过对青冈栎幼苗接种外生菌根、内生菌根和混合接种方式,研究在不同水分条件下,接种菌根真菌对青冈栎幼苗生长和耐旱性的影响作用,为岩溶地区石漠化治理和生态恢复提供理论支撑。
1 材料和方法 1.1 材料试验菌种为摩西球囊霉(Glomus mosseae,Gm)、根内球囊霉(Glomus intraradices,Gi)和彩色豆马勃(Pisolithus tinctorius,Pt),由长江大学园林园艺学院、北京市农林科学院植物营养与资源研究所提供。两种内生菌根真菌用高粱苗在温室大棚内进行扩繁培养,培养4个月后用于接种的菌剂含有孢子、菌丝片段和侵染根段;外生菌根菌剂用珍珠岩与草炭土的混合基质进行扩繁培养,用于接种的菌剂主要含有孢子和菌丝。供试土壤采自贵州喀斯特高原生态综合治理试验示范区,土壤理化性质见表 1。土壤过2mm筛,在0.14MPa,120℃条件下灭菌2h后作为试验基质。青冈栎种子采自喀斯特地区青冈栎次生林,试验前用5% NaClO 消毒15 min,并用灭菌水冲洗多次,备用。
| pH | 全氮/(g/kg)Total N | 全磷/(g/kg)Total P | 有效钾/(g/kg)Avalilable K | 有机质/(g/kg)Organic matter | 田间持水量%(v/v)Field moisture capacity |
| 7.39 | 2.38 | 0.32 | 0.13 | 46.2 | 28.20 |
试验采用完全随机区组设计,包括3个土壤水分处理和5个接种处理(3×5)。土壤水分处理设置为相对土壤田间持水量的75%—85%(正常供水)、55%—65%(中度干旱)和35%—45%(重度干旱);其中,每个处理设置6个重复,接种处理设置为:接种摩西球囊霉处理(Gm)、接种根内球囊霉处理(Gi)、接种彩色豆马勃处理(Pt)、混合接种处理(Mixture inoculation,Mi)和不接种处理(Contrast check,CK)。接种方法:在塑料花盆中装入灭菌土1.5kg,称取菌剂平铺在灭菌土上,同时播入消毒并催芽的青冈栎种子,用灭菌土覆盖。单个菌种接种处理按25g/盆施加菌剂(孢子密度7—12个/g);混合菌种接种处理:3种菌剂按相同重量混合后,再称取25g菌剂施入花盆中;对照处理不加菌剂,加入经微孔滤膜过滤的菌液和25g高温灭菌后的混合菌剂,以保持除目的菌外和其他处理土壤微生物组成一致。在接种后的30d内,各处理用无菌水进行补充水分,按常规育苗方式管理。在幼苗正常生长30d后,每盆定苗5株,并对各处理土壤开始进行不同水分控制,每天用称重法测定土壤水分变化并加入相应失水量,保持各处理土壤水分含量在相应梯度内。在进行水分处理90d后结束试验,每个处理随机选取其中6株(分别在6个重复花盆中各选择1株)进行相关指标测定。
1.3 指标测定与数据处理 1.3.1 侵染率的测定每种处理选取6株(分别在6个重复的花盆中各选择1株),挖出根系混匀随机取10根6—10cm长细根,用水冲洗干净,并剪成1cm长左右片段,然后用10% KOH在90℃透明1h,用5%的乳酸酸化5min,再用0.05%的曲利苯蓝于90℃染色30min,内生菌根用网格交叉法[19]测定根系菌根侵染率,菌根侵染率(%)=交叉点菌根数/根段与线交叉点数×100%。外生菌根侵染率用计数统计方法确定,以形成外生菌根的根段数占观察的总根段数的百分比作为菌根侵染率,菌根侵染率=(菌根侵染根尖数/检查根尖数)×100%。
1.3.2 叶面积、生物量和养分含量测定分别从每种处理选取其中6株(分别在6个重复花盆中各选择1株),将幼苗完整取出清洗,在80℃下烘干至恒重,计算生物量和菌根依赖性,菌根依赖性=(接种处理干重-不接种处理干重)/接种处理干重×100%;将植物地上部样品烘干磨碎过0.25mm筛,称取0.1g,置于100mL消化管中,用水湿润样品,加浓硫酸5mL,然后放置过夜,在消化炉上加热,当溶液全部呈棕黑色时,从消化炉上取下消化管,逐滴加入300g/L H2O2 10滴,并不断摇动消化管。再加热至微沸10min,稍冷后再加入H2O2 5滴,如此反复3次,至消煮液呈清亮色再加热5min,以除尽过剩的双氧水。将消煮液定容至100mL,用上清液测定N、P、K元素含量。植物全氮用奈氏比色法测定,植物全磷含量用钒钼黄比色法,植物全钾含量用火焰光度计法测定[20]。
1.3.3 渗透调节物质含量、抗氧化酶活性和叶绿素含量测定每种处理分别从6个重复花盆中随机选择1株,取植株新鲜叶片,剪碎后混匀。称取0.3g新鲜植物叶片,用蒽酮法测定可溶性糖、称取0.5g新鲜植物叶片,用茚三酮法测定脯氨酸,称取0.5g新鲜植物叶片,采用氮蓝四唑(NBT)光化学还原法测定超氧化物歧化酶(SOD)酶活性,以每单位时间内抑制NBT光化还原的50%为一个酶活性单位(U);称取5g新鲜植物叶片,采用愈创木酚法测定过氧化物酶(POD)酶活性,以每分钟光密度值变化0.01为1个过氧化物酶活性单位;称取2.5g新鲜植物叶片,采用高锰酸钾滴定法测定过氧化氢酶(CAT)酶活性,酶活性采用每g鲜质量样品1min内分解H2O2的mg数表示[20]。称取0.2g新鲜植物叶片,用80%丙酮提取植物叶片叶绿素,并在663nm和645nm条件下测定叶绿素溶液吸光度,利用CT=20.29A645+8.05A663 计算叶绿素总量[21]。
1.3.4 数据处理试验数据采用SPSS 13.0软件统计,利用Two-way ANOVA双因素方差分析检验接种处理和水分处理对青冈栎生长指标的影响,当接种处理与水分处理交互作用显著时,采用Duncan新复极差法检验各处理平均值间差异的显著性;当接种处理与水分处理交互作用不显著时,分别采用Duncan新复极差法检验在同一水分处理下,不同接种处理数据差异显著性,以及在同一接种处理下,不同水分处理数据之间的差异显著性。
2 结果 2.1 不同水分处理条件对青冈栎幼苗侵染率和菌根依赖性的影响试验结果表明,接种处理根系均能与菌根真菌形成菌根共生体,未接种对照处理也受到菌根真菌侵染,但侵染率均小于5%。在3种水分条件下,Gm、Gi和Mi接种处理根系侵染率均显著高于Pt处理,在正常水分和中度干旱条件下,Gm、Gi和Mi接种处理之间根系侵染率无显著差异。随着土壤水分干旱胁迫加重,根系侵染率均显著降低。
如表 3所示,在3种土壤水分条件下,接种处理的青冈栎幼苗总生物量均显著高于未接种处理。与正常水分相比,中度干旱条件下,各接种植株总生物量差异不显著;重度干旱下,除Gi处理外,其余处理生物量均显著下降(P <0.05),Gm、Gi和Mi处理生物量显著高于Pt处理,而Gm、Gi和Mi处理之间无显著性差异。经双因素方差分析,青冈栎生物量在接种处理和水分处理间存在显著的交互作用(P<0.01)(表 2)。
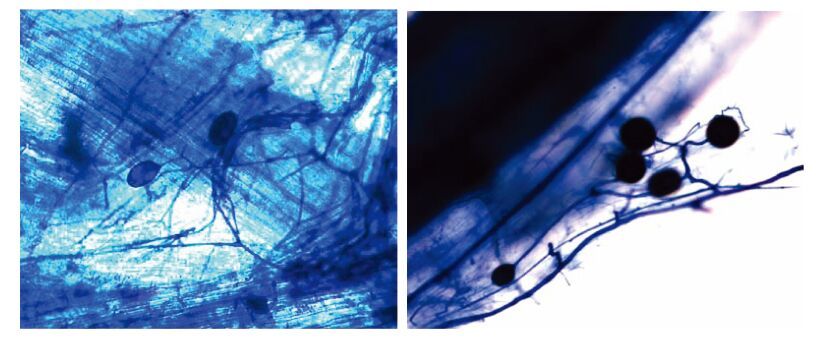
|
| 图 1 青冈栎内生菌根孢子和菌丝形态 Fig. 1 Hyphae and spores of AMF in Cyclobalanopsis glauca roots |
| 处理Treatment | 侵染率Colonization rate | 生物量Biomass | 氮含量Nitrogen | 磷含量Phosphorus | 钾含量Potassium | 叶绿素含量Total chlorophyll |
| 水分Water regime(WC) | ** | ** | * | * | NS | ** |
| 接种Mycorrhiza fungi(MF) | *** | ** | ** | * | * | *** |
| 水分×接种 WC×MF | *** | ** | NS | NS | NS | NS |
| *、**、***和NS分别表示在P <0.05、P<0.01、P<0.001水平显著和不显著 | ||||||
植物对菌根真菌的依赖性是反映植物与菌根真菌之间相互关系的指标。由表 3可知,在正常水分条件下,各处理菌根依赖性均低于37%;在中度干旱条件下,各处理之间菌根依赖性均增加,增加幅度大小顺序为:Pt(47.68%)>Gm(46.27%)>Mi(45.47%)>Gi(40.87%)。相比于中度干旱条件,在重度干旱条件下,仅Gm和Gi处理菌根依赖性增加,Pt和Mi处理菌根依赖性下降,其中Pt处理菌根依赖性下降50.3%。

|
| 图 2 青冈栎外生菌根根尖形态 Fig. 2 Morphological characteristics of ectomycorrhizal of Cyclobalanopsis glauca roots |
| 土壤相对含水量Soil relative water content | 接种Inoculation | 生物量Dry biomass/g | 菌根依赖性Mycorrhizal dependency/% | 侵染率Colonization rate/% |
| 75%85% | CK | 3.01c | 4.41f | |
| 正常水分Normal moisture | Gm | 4.57a | 34.14 | 76.53a |
| Gi | 4.04bc | 25.50 | 68.17a | |
| Pt | 4.72a | 36.23 | 44.5c | |
| Mi | 4.38ab | 31.28 | 70.8a | |
| 55%—65% | Ck | 2.59d | 4.01f | |
| 中度干旱Moderate drought | Gm | 4.62a | 46.27 | 66.2ab |
| Gi | 4.38ab | 40.87 | 62.8b | |
| Pt | 4.75a | 47.68 | 29.6d | |
| Mi | 4.55a | 45.47 | 59.2b | |
| 35%—45% | Ck | 2.13e | 3.59f | |
| 重度干旱Severe drought | Gm | 4.01bc | 46.88 | 57.47b |
| Gi | 3.70bc | 42.43 | 54.23bc | |
| Pt | 2.79d | 23.66 | 18.5e | |
| Mi | 3.55c | 40.00 | 40.2c | |
| CK:未接种处理Non inoculation treatment,Gm:接种摩西球囊霉Glomus mosseae treatment,Gi:接种根内球囊霉,Glomus intraradicestreatmentPt:接种彩色豆马勃Pisolithus tinctorius treatment,Mi:混合接种Mixed inoculation treatment ; 表中同一列标注不同字母表示处理间差异显著(P <0.05) | ||||
由表 2可知,经双因素方差分析,青冈栎幼苗叶片叶绿素含量在接种处理和水分处理间无显著的交互作用。接种和水分胁迫对叶绿素含量均有显著影响(图 3)。随土壤水分胁迫程度增加,植株叶绿素总含量逐渐降低;与正常水分相比,中度干旱条件下各处理叶绿素含量未出现显著变化,但在重度干旱条件下,Pt、Mi和未接种处理叶绿素含量显著下降。在中度干旱条件下,Mi处理叶绿素含量显著高于对照,而其余处理之间叶绿素含量无显著性差异;在重度条件下,接种Gm、Gi和Mi处理叶绿素含量均显著高于未接种处理,而Pt处理与对照之间无显著性差异。

|
| 图 3 菌根真菌对不同水分条件下青冈栎叶绿素含量的影响 Fig. 3 The effect of mycorrhizal fungi on the leaf chlorophyll content of Cyclobalanopsis glauca seedlings under different water conditions |
由表 2可知,经双因素方差分析,青冈栎地上部氮含量、磷含量和钾含量在接种处理和水分处理之间无显著的交互作用。随着土壤含水量降低,植株地上部分氮含量下降(图 4)。在正常水分条件下,各处理植株地上部全氮含量无显著性差异;在中度干旱条件下,除Pt处理全氮含量显著高于对照外,其余接种处理全氮含量与对照处理无显著差异,与正常水分条件相比,各处理条件下氮含量无显著差异;当土壤水分含量达到重度干旱条件时,Pt处理和未接种处理全氮含量显著下降。

|
| 图 4 菌根真菌对不同水分条件下青冈栎氮含量的影响 Fig. 4 The effect of mycorrhizal fungi on the total nitrogen content of Cyclobalanopsis glauca seedlings under different water conditions |
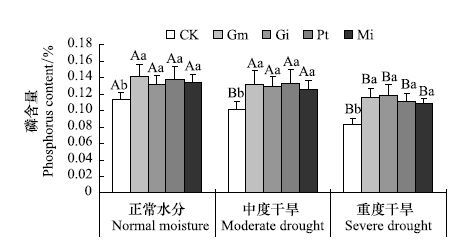
在3种水分条件下,接种处理植株地上部分磷含量均显著高于对照处理(图 5)。在相同水分条件下,接种处理之间植株全磷含量无显著性差异。与正常水分条件相比,在重度干旱条件下,除Gi处理外,其余接种处理磷含量均显著下降,其中Gm、Pt和Mi处理分别下降17.8%、19.0%、18.7%。
|
| 图 5 菌根真菌对不同水分条件下青冈栎磷含量的影响 Fig. 5 The effect of mycorrhizal fungi on the total phosphorus content of Cyclobalanopsis glauca seedlings under different water conditions |
由图 6可知,在相同水分条件下,接种处理植株地上部全钾含量均显著高于对照,接种处理之间无显著性差异;土壤干旱胁迫条件下,各处理间钾含量没有显著差异。

|
| 图 6 菌根真菌对不同水分条件下青冈栎钾含量的影响 Fig. 6 The effect of mycorrhizal fungi on the total potassium content of Cyclobalanopsis glauca seedlings under different water conditions |
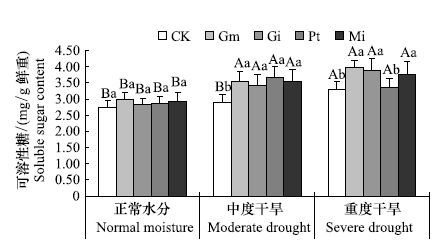
水分胁迫与接种处理显著影响植株可溶性糖与脯氨酸含量,经双因素方差分析,青冈栎可溶性糖与脯氨酸含量在接种处理和水分处理之间无显著的交互作用(表 4)。在正常水分条件下,接种植株与未接种植株可溶性糖含量无显著差异;当土壤水分含量降低达到中度干旱时,Gm和Pt处理可溶性糖含量显著升高,而对照处理无显著变化;与正常水分条件相比,在重度水分胁迫条件下,各处理间可溶性糖含量均显著升高,并且Gm、Gi和Mi处理可溶性糖含量显著高于CK和Pt处理。
| 处理Treatment | 可溶性糖Soluble sugar | 脯氨酸Proline | 超氧化物歧化酶SOD | 过氧化氢酶CAT | 过氧化物酶POD |
| 水分Water regime(WC) | * | * | ** | * | ** |
| 接种Mycorrhiza fungi(MF) | ** | ** | * | * | * |
| 水分×接种WC×MF | NS | NS | ** | NS | ** |
| *、**、***和NS分别表示在P <0.05、P<0.01、P<0.001水平显著和不显著 | |||||
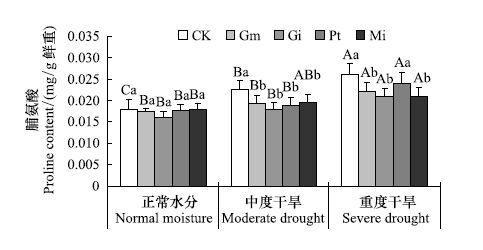
图 8 表明,土壤水分降低使植株脯氨酸含量升高,接种菌根真菌使植株脯氨酸含量降低。在正常水分条件下,各处理之间脯氨酸含量无显著差异,当土壤水分降低至中度干旱状态时,对照处理脯氨酸含量显著升高,而接种处理脯氨酸含量无显著变化;与正常水分相比,在重度胁迫下,除Mi处理无显著变化外,其余处理脯氨酸均显著升高,Gm、Gi和Mi处理含量显著低于对照。
|
| 图 7 菌根真菌对不同水分条件下青冈栎叶片可溶性糖含量的影响 Fig. 7 The effect of mycorrhizal fungi on the soluble sugar content of Cyclobalanopsis glauca seedlings leaf under different water conditions |
|
| 图 8 菌根真菌对不同水分条件下青冈栎叶片脯氨酸含量的影响 Fig. 8 The effect of mycorrhizal fungi on the proline content of Cyclobalanopsis glauca seedlings leaf under different water conditions |
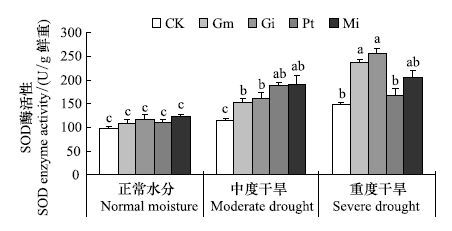
经双因素方差分析(表 4),青冈栎SOD与POD酶活性在接种处理和水分处理间具有显著的交互作用(P <0.01),CAT酶活性在接种处理和水分处理间无显著的交互作用。如图 9所示,在正常水分条件下,未接种处理与接种处理SOD活性无显著性差异。在中度干旱时,接种处理SOD酶活性显著升高,均显著高于对照处理;与正常水分相比,Gm、Gi、Pt和Mi处理分别升高40.9%、36.8%、70.7%和55.8%。在重度干旱条件下Gm、Gi处理SOD酶活性显著高于对照处理,并显著高于Pt和Mi处理。
|
| 图 9 菌根真菌对不同水分条件下青冈栎叶片SOD酶活性的影响 Fig. 9 The effect of mycorrhizal fungi on the activity of SOD enzyme of Cyclobalanopsis glauca seedlings leaf under different water conditions |
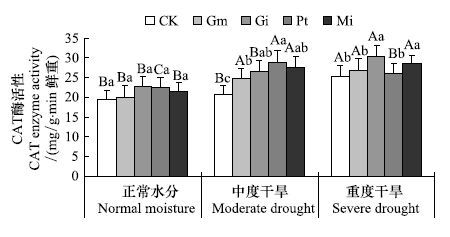
在正常水分条件下,各处理CAT酶活性无显著性差异(图 10);在中度干旱时,Pt和Mi处理CAT酶活性显著升高,其余处理无显著变化,未接种处理CAT酶活性显著低于Gi、Pt和Mi处理。与正常水分条件相比,在重度干旱下,除Pt处理外,其余处理CAT酶活性均显著增加,对照处理酶活性显著低于Gi和Mi处理。
|
| 图 10 菌根真菌对不同水分条件下青冈栎叶片CAT酶活性的影响 Fig. 10 The effect of mycorrhizal fungi on the activity of CAT enzyme of Cyclobalanopsis glauca seedlings leaf under different water conditions |
在正常水分条件下,各处理POD酶活性无显著性差异,但在中度干旱条件下,接种处理POD酶活性显著升高,而未接种处理POD酶活性未出现显著性变化。在重度干旱下,各处理POD酶活性进一步升高,未接种处理POD酶活性显著低于接种处理,Pt处理酶活性显著低于Gm和Gi处理。

|
| 图 11 菌根真菌对不同水分条件下青冈栎叶片POD酶活性的影响 Fig. 11 The effect of mycorrhizal fungi on the activity of POD enzyme of Cyclobalanopsis glauca seedlings leaf under different water conditions |
本试验结果表明,内生菌根真菌和外生菌根真菌均可侵染青冈栎根系。在土壤干旱胁迫条件下,菌根侵染率降低,外生菌根侵染率低于内生菌根侵染率。本研究中,未接种植株根系也受到侵染,这是由于在土壤灭菌过程中未完全杀死土壤中真菌孢子,但与接种处理相比,未接种处理侵染率显著较低,均未超过5%。在严重干旱条件下,外生菌根侵染率显著下降,这可能是由于菌根菌丝扩展和孢子活力在干旱条件下受到抑制造成[22-23]。有研究表明[17],在干旱胁迫时,外生菌根菌丝的生长和孢子萌发会受到抑制。
岩溶石漠化地区土壤普遍缺乏磷元素[24]。由于石漠化土壤中土壤磷酸酶活性较低,使土壤磷元素有效性下降,土壤中磷元素多为难溶性磷。在本研究中,接种菌根处理显著增加了青冈栎植株的磷含量,尤其是在土壤干旱条件下,无论接种内生菌根还是外生菌根,植株磷含量均显著高于未接种处理。有学者对石漠化造林树种刺楸和滇柏[11],香椿[25]接种菌根真菌试验,也观察到植株磷元素显著增加,并且干旱胁迫程度越重,效果越明显。以上结果表明,接种菌根真菌能够改善宿主磷营养状况,增加植株体内磷含量,促进植物生长发育。这主要是由于菌根的活动使土壤酸性磷酸酶活性增加,使土壤中难溶性磷酸盐转变为可溶的多聚磷酸盐,促进有机磷矿化为植物可以吸收的磷元素[26]。此外,菌根真菌能分泌乙酸、柠檬酸等多种低分子有机酸,这些有机酸降低土壤pH值,能活化土壤中难溶性盐,进而促进植物对养分的吸收[27-28]。如在本研究中,接种处理均显著提高了植株钾含量,而钾元素对提高植物耐旱性具有重要作用[29]。
通常在干旱胁迫下,接种菌根真菌能够促进植物合成大量脯氨酸和可溶性糖增强植物的渗透调节作用。本研究中,接种菌根处理可溶性糖含量显著高于未接种处理,这与以前的研究结果一致[29-30],表明在水分胁迫下,菌根真菌通过增加宿主体内糖类含量来降低渗透势,保持植株体内水分。在干旱胁迫时,接种处理青冈栎叶片脯氨酸含量显著低于未接种处理,在其他植物研究中,如枳实生苗[31]、民勤绢蒿[32]、西红柿[33]、金脉刺桐[34]等在干旱胁迫下,接种菌根处理脯氨酸含量也显著低于未接种处理。表明接种菌根真菌后植株水分代谢得到改善,有效减轻植株受胁迫程度[35],从而使菌根化植株体内脯氨酸含量低于非菌根化植株[33]。
在土壤中度干旱条件下,接种处理POD、SOD和CAT酶活性均显著高于未接种处理,在重度干旱条件下,接种处理POD酶活性显著高于未接种处理,只有接种内生菌根真菌处理SOD酶活性显著高于未接种处理,表明在重度干旱条件下,菌根真菌对POD酶活性具有显著促进作用,外生菌根真菌在重度干旱下对SOD酶活性促进作用降低,而接种内生菌根真菌仍具有显著促进作用。表明接种菌根真菌能够促进提高植物抗氧化酶活性[7, 22, 36],减少细胞内由于水分胁迫引起的活性氧积累,从而减轻因干旱对植物造成的膜伤害。总体而言,青冈栎幼苗在正常水分和中度干旱胁迫下,接种外生菌根真菌处理的抗氧化酶活性和养分含量好于接种两种内生菌根真菌处理;但是在重度干旱胁迫下,由于外生菌根侵染率显著下降,其菌根效应降低,而接种外生菌根真菌对青冈栎生长和耐旱性仍具有促进作用。
本研究结果表明,在土壤干旱胁迫下,菌根共生体通过改善植株抗氧化酶活性、调节渗透调节物质、提高养分和维持叶绿素含量,使青冈栎幼苗耐旱性得到增强,有利于青冈栎在缺水的岩溶区生长。在西南喀斯特地区,森林土壤中AMF种类丰富,孢子、菌丝密度高,但在一些石漠化地区,植被覆盖少,土壤退化严重,土壤中AMF孢子种类与密度大大降低,可能对植物根系不能有效侵染。因此,在退化的石漠化地区造林,可利用菌根苗造林,提高造林成活率。
| [1] | 王世杰, 李阳兵.喀斯特石漠化研究存在的问题与发展趋势.地球科学进展,2007,22(6): 573–582. |
| [2] | 陈洪松, 聂云鹏, 王克林.岩溶山区水分时空异质性及植物适应机理研究进展.生态学报,2013,33(2): 317–326. |
| [3] | 王建锋, 谢世友, 许建平.丛枝菌根在石漠化生态恢复中的应用及前景分析.信阳师范学院学报: 自然科学版,2009,22(1): 157–160. |
| [4] | 魏源, 王世杰, 刘秀明, 黄天志.丛枝菌根真菌及在石漠化治理中的应用探讨.地球与环境,2012,40(1): 84–92. |
| [5] | 徐丽娟, 刁志凯, 李岩, 刘润进.菌根真菌的生理生态功能.应用生态学报,2012,23(1): 285–292. |
| [6] | 李涛, 杜娟, 郝志鹏, 张莘, 陈保冬.丛枝菌根提高宿主植物抗旱性分子机制研究进展.生态学报,2012,32(22): 7169–7176. |
| [7] | Wu Q S, He X H, Zou Y N, Liu C Y, Xiao J, Li Y.Arbuscular mycorrhizas alter root system architecture of Citrus tangerine through regulating metabolism of endogenous polyamines.Plant Growth Regulation,2012,68(1): 27–35. |
| [8] | 宋会兴, 钟章成, 王开发.土壤水分和接种VA菌根对构树根系形态和分形特征的影响.林业科学,2007,43(7): 142–147. |
| [9] | 何跃军, 钟章成.喀斯特土壤上香樟幼苗接种不同AM真菌后的耐旱性效应.植物研究,2011,31(5): 597–602. |
| [10] | 杜照奎, 何跃军.光皮树幼苗接种丛枝菌根真菌的光合生理响应.贵州农业科学,2011,39(8): 31–35. |
| [11] | 王如岩, 于水强, 张金池, 周垂帆, 陈莉莎.干旱胁迫下接种菌根真菌对滇柏和楸树幼苗根系的影响.南京林业大学学报: 自然科学版,2012,36(6): 23–27. |
| [12] | Henry L K.Mycorhizas of trees and shrubs.Botanical Gazette,1933,94(4): 791–800. |
| [13] | Watson G W, von der Heide-Spravka K G, Howe V K.Ecological significance of endo-/ectomycorrhizae in the oak sub-genus erythrobalanus.Arboricultural Journal: The International Journal of Urban Forestry,1990,14(2): 107–116. |
| [14] | 庄雪影, 陈咏娟.香港次生林下植物菌根的调查.生物多样性,1997,5(4): 287–292. |
| [15] | Moyersoen B, Fitter A H.Presence of arbuscular mycorrhizas in typically ectomycorrhizal host species from Cameroon and New Zealand.Mycorrhiza,1999,8(5): 247–253. |
| [16] | Dickie I A, Koide R T, Fayish A C.Vesicular-arbuscular mycorrhizal infection of Quercus rubra seedlings.New Phytologist,2001,151(1): 257–264. |
| [17] | Querejeta J I, Egerton-Warburton L M, Allen M F.Topographic position modulates the mycorrhizal response of oak trees to interannual rainfall variability.Ecology,2009,90(3): 649–662. |
| [18] | Toju H, Yamamoto S, Sato H, Tanabe A S, Gilbert G S, Kadowaki K.Community composition of root-associated fungi in a Quercus-dominated temperate forest: "codominance" of mycorrhizal and root-endophytic fungi.Ecology and Evolution,2013,3(5): 1281–1293. |
| [19] | Giovannetti M, Mosse B.An evaluation of techniques for measuring vesicular arbuscular mycorrhizal infection in roots.New Phytologist,1980,84(3): 489–500. |
| [20] | 李合生. 植物生理生化实验原理和技术. 北京: 高等教育出版社, 2000. |
| [21] | 王学奎. 植物生理生化实验原理和技术.(第二版). 北京: 高等教育出版社, 2006. |
| [22] | Huang Z, Zou Z R, He C X, He Z Q, Zhang Z B, Li J M.Physiological and photosynthetic responses of melon (Cucumis melo L.Plant and Soil,2011,339(1/2): 391–399. |
| [23] | Gong M G, Tang M, Chen H, Zhang Q M, Feng X X.Effects of two Glomus species on the growth and physiological performance of Sophora davidii seedlings under water stress.New Forests,2013,44(3): 399–408. |
| [24] | 龙健, 李娟, 汪境仁, 李阳兵.典型喀斯特地区石漠化演变过程对土壤质量性状的影响.水土保持学报,2006,20(2): 77–81. |
| [25] | 甘春雁, 姚瑞玲, 项东云, 陈健波.丛枝菌根化香椿幼苗对干旱胁迫的生长响应.广西林业科学,2013,42(1): 20–24. |
| [26] | 宋勇春, 冯固, 李晓林.泡囊丛枝菌根对红三叶草根际土壤磷酸酶活性的影响.应用与环境生物学报,2000,6(2): 171–175. |
| [27] | 袁玲, 方德华, 汪智慧, 魏兴元, 黄建国.钾对外生菌根真菌的分泌作用及氮、磷、钾含量的影响.生态学报,2001,21(2): 254–258. |
| [28] | 张亮, 王明霞, 张薇, 黄建国, 袁玲.外生菌根真菌对土壤钾的活化作用.微生物学报,2014,54(7): 786–792. |
| [29] | Abbaspour H, Saeidi-Sar S, Afshari H, Abdel-Wahhab M A.Tolerance of Mycorrhiza infected Pistachio (Pistacia vera L.Journal of Plant Physiology,2012,169(7): 704–709. |
| [30] | Wu Q S, Xia R X, Hu Z J.Effect of arbuscular mycorrhiza on the drought tolerance of Poncirus trifoliata seedlings.Frontiers of Forestry in China,2006,1(1): 100–104. |
| [31] | 吴强盛, 夏仁学.水分胁迫下丛枝菌根真菌对枳实生苗生长和渗透调节物质含量的影响.植物生理与分子生物学学报,2004,30(5): 583–588. |
| [32] | 贺学礼, 高露, 赵丽莉.水分胁迫下丛枝菌根AM真菌对民勤绢蒿生长与抗旱性的影响.生态学报,2011,31(4): 1029–1037. |
| [33] | Aroca R, del Mar Alguacil M, Vernieri P, Ruiz-Lozano J M.Plant responses to drought stress and exogenous ABA application are modulated differently by mycorrhization in tomato and an ABA-deficient mutant (Sitiens).Microbial Ecology,2008,56(4): 704–719. |
| [34] | Manoharan P T, Shanmugaiah V, Balasubramanian N, Gomathinayagam S, Sharma M P, Muthuchelian K.Influence of AM fungi on the growth and physiological status of Erythrina variegata Linn.European Journal of Soil Biology,2010,46(2): 151–156. |
| [35] | 贺学礼, 马丽, 孟静静, 王平.不同水肥条件下AM真菌对丹参幼苗生长和营养成分的影响.生态学报,2012,32(18): 5721–5728. |
| [36] | Zhang H S, Wu X H, Li G, Qin P.Interactions between arbuscular mycorrhizal fungi and phosphate-solubilizing fungus (Mortierella sp.Biology and Fertility of Soils,2011,47(5): 543–554. |
 2016, Vol. 36
2016, Vol. 36




