文章信息
- 马文超, 刘媛, 孙晓灿, 陈锦平, 魏虹
- MA Wenchao, LIU Yuan, SUN Xiaocan, CHEN Jinping, WEI Hong.
- 镉在土壤-香根草系统中的迁移及转化特征
- Transfer and transformation characteristics of cadmium from soil to Vetiveria zizanioides
- 生态学报[J]. 2016, 36(11): 3411-3418
- Acta Ecologica Sinica[J]. 2016, 36(11): 3411-3418
- http://dx.doi.org/10.5846/stxb201506261297
-
文章历史
- 收稿日期: 2015-06-26
- 修订日期: 2015-11-24
工业排污,农业耕作等生产活动造成的土壤重金属污染问题日益严重。目前,我国重金属污染土壤总面积已达2×107 hm2,占我国耕地总面积的1/5[1]。2014年全国土壤污染状况调查公报显示我国土壤环境状况不容乐观,土壤总超标率为16%,无机污染物超标点位数占全部超标点位的82.8%,其中Cd的点位超标率高达7%[2]。Cd是毒性最强的重金属元素之一,其易溶于水、有效态含量高,易进入食物链,对人体健康构成巨大威胁[3]。传统的物理、化学修复方法存在成本高、破坏土壤理化性质、易造成二次污染等弊端[4]。植物修(Phytoremediation) 是利用植物来转移、容纳或转化重金属污染物使其对环境无害的技术,具有成本低,不破坏生态环境等优点[5-7]。
目前研究者已筛选出遏蓝菜(Thlaspi caerulescens)[8]、龙葵(Solanum Nigrum L.)[9],宝山堇菜 (Viola baoshanensis)[10]等具有重金属高富集能力的植物,但这些植物生物量小,根系不够发达,限制其对于土壤中重金属的大量富集以及对深层土壤的修复能力,目前国内外研究的热点开始向具有大生物量的植物转移[11]。香根草 (Vetiveria zizanioides) 是禾本科多年生草本植物,生物量大、根系发达、生长迅速、抗逆性强。香根草具有较强的Cd 耐性,可长时间适应低浓度 Cd 胁迫,甚至是短时间的高浓度Cd胁迫[12]。香根草能吸收Cd并储存在体内,具有较强的稳定能力,在Cd污染土壤的修复方面有一定应用潜力[13]。目前对于香根草的研究大多针对其富集能力以及Cd胁迫下的生理响应,未综合考虑香根草的富集能力以及对土壤中重金属形态产生的影响,对于Cd在土壤-香根草系统中的迁移及转化特征尚不明确。
本文以香根草为研究对象,采用盆栽试验方式,设置梯度浓度Cd胁迫,测定香根草各部分组织中Cd的含量以及土壤中各种形态的Cd含量,通过探究Cd在土壤-香根草体系中的迁移及转化特征,明确香根草对土壤中的Cd的清除效果,评价香根草是否适用于Cd污染土壤的植物修复。
1 材料与方法 1.1 试验材料及方法本试验以重庆市綦江苗圃基地当年生香根草分蘖苗作为研究对象,2014年5月选取生长基本一致的香根草分蘖苗移栽入培养盆中,每盆1株。盆高20 cm,内径15 cm,装入风干后过5 mm筛的紫色土4 kg,土壤基本理化性质见表 1。适应性培养50 d后选取长势基本一致的香根草80盆,随机分为4组,采取一次性浇灌的方式向土壤中加入CdCl2·2.5H2O,分别设置Cd浓度梯度为0 mg/kg (无Cd处理)、2 mg/kg (低浓度处理)、20 mg/kg (中浓度处理)和80 mg/kg土壤干重(高浓度处理),各处理分别定义为无Cd处理 (CKP)、低浓度处理 (LP)、中浓度处理 (MP)和高浓度处理 (HP)。同时,设置无植物组相对应处理4组,各处理5个重复,分别定义为无Cd处理 (CK)、低浓度处理 (L)、中浓度处理 (M)和高浓度处理 (H)。所有培养盆置于西南大学三峡库区生态环境教育部重点实验室试验基地大棚下进行培养,试验期间进行常规田间管理。自试验处理之日起,0、40、90 d分别从香根草组各抽取5个重复对植物进行相关指标测定,同期对两组各处理土壤进行取样并测定。
| pH | 有机质Organicmatter/% | 全氮Total N/ (g/kg) | 全磷Total P/ (g/kg) | 全钾Total K/ (g/kg) | 碱解氮AlkaliHydrolysable N/ (mg/kg) | 有效磷Available P/ (mg/kg) | 速效钾Available K/ (mg/kg) | 总CdTotal Cd/(mg/kg) | 有效CdAvailable Cd/ (mg/kg) |
| 7.11 | 2.62 | 1.31 | 1.11 | 16.82 | 122.72 | 29.72 | 119.54 | 0.15 | 0.03 |
收获植物全株,将香根草分为地上部分和根,用20 mmol EDTA-Na2漂洗5 min,去除表面吸附的Cd离子,然后迅速用超纯水冲洗干净。放于80℃烘箱中烘至恒重,将烘干后的样品用球磨仪进行粉碎,密封保存待3次取样完成后统一测量。土壤经自然风干,去除杂质,研磨后过100目尼龙筛,用简单连续提取法提取土壤中不同形态的Cd,分别用CaCl2提取中性交换态Cd,螯合剂DTPA提取螯合态Cd,最终用强酸溶解残渣提取残渣态Cd[14]。用ICAP 6000 电感耦合等离子体发射光谱仪进行Cd含量测定。
1.2.2 评价指数计算利用Cd含量数据计算生物富集系数 (BCF)、转移系数 (TF) 和生物有效性 (BF),用以评价香根草对Cd的积累及转化能力。计算公式如下:
生物富集系数 (BCF) = 根或地上部分Cd浓度 (mg/kg干重) /土壤中Cd浓度(mg/kg干重)[15]
转移系数 (TF) = 地上部分平均Cd含量(mg/kg干重) /根部平均Cd(mg/kg干重)[16]
Cd的生物有效性指数 (BF) =(中性交换态Cd含量+螯合态Cd含量)/Cd总量[16]
1.2.3 数据分析利用统计分析软件SPSS 20.0进行数据处理,运用单因素方差分析(One-way ANOVA)分析不同浓度Cd处理对香根草各部分Cd积累量及土壤中各种形态Cd含量的影响,双因素方差分析(Two-way ANOVA)分析香根草和不同处理浓度对土壤中Cd形态的影响。Duncan多重比较(Duncan′s multiple range test)检验各处理之间的差异,采用Origin 8.5作图分析。
2 试验结果 2.1 不同浓度Cd胁迫下香根草各部分的积累量图 1为香根草地上部分和根部在试验期间Cd的积累量。随处理浓度的升高和处理时间的延长,香根草地上部分和根部的Cd积累量均显著上升,香根草根部的Cd含量显著高于地上部分。处理90 d时,高浓度处理组地上部分和根部的Cd积累量分别达到180.42 mg/kg和241.54 mg/kg。在实验期间各浓度处理组香根草的存活率为100%,随着Cd积累量的增大,香根草的生物量有所减少,但未阻碍其正常生长。

|
| 图 1 不同Cd浓度胁迫下香根草各部位的Cd累积量 Fig. 1 Effects of the different Cd concentration on Cd content of Vetiveria zizanioides |
不同Cd浓度处理和种植香根草对处理90 d土壤中的总Cd含量及Cd形态影响见表 2。双因素方差分析结果显示,种植香根草对土壤中中性交换态、残渣态、生物有效态Cd(中性交换态+螯合态)含量有显著影响,对土壤中总Cd含量有极显著影响,对螯合态Cd含量无显著影响。浓度处理则对5个指标均有极显著影响。
| 处理Treatment | 中性交换态Neutral exchange form | 螯合态Chelate form | 残渣态Residue | 生物有效态Bio-available | 总Cd量Total Cd |
| CK | 0.00±0.00Aa | 0.05±0.02Aa | 0.09±0.01Aa | 0.05±0.02Aa | 0.14±0.03Aa |
| L | 0.25±0.01Aa | 0.51±0.02Aa | 1.07±0.02Aa | 0.76±0.02Aa | 1.82±0.02Bb |
| M | 3.27±0.07Bb | 6.29±0.30Cc | 9.50±0.34Bb | 9.56±0.34Cc | 19.06±0.22Cd |
| H | 21.60±0.29Dd | 20.00±0.12Dd | 37.30±0.68Ee | 41.60±0.82De | 78.89±0.26Ee |
| CKP | 0.00±0.00 Aa | 0.03±0.02Aa | 0.06±0.02Aa | 0.04±0.02Aa | 0.10±0.06Aa |
| LP | 0.24±0.02Aa | 0.42±0.02Aa | 1.05±0.03Aa | 0.66±0.03Aa | 1.72±0.02Bc |
| MP | 3.14±0.19Bb | 3.87±0.27Bb | 11.55±0.50Cc | 7.02±0.11Bb | 18.57±0.19Cd |
| HP | 19.05±1.33Cc | 20.94±0.92Dd | 31.86±0.93Dd | 40.04±1.15Dd | 71.89±0.78Df |
| 植物处理Plant treatment | * | ns | * | * | ** |
| 浓度处理Concentration | ** | ** | ** | ** | ** |
| 植物×浓度Plant× Concentration | ns | ** | ** | * | * |
| 表中数值为平均值±标准误(n=5);不同小写字母分别表示同列数据之间有显著差异(P <0.05),不同大写字母表示同列数据之间有极显著差异(P<0.01);**: P<0.01;*:P<0.05;ns: P>0.05;CK: 无植物组无Cd处理control check without plant;L: 无植物组低浓度Cd处理low treatment group without plant;M: 无植物组中浓度Cd处理medium treatment group without plant;H: 无植物组高浓度Cd处理high treatment group without plant;CKP: 香根草组无Cd处理control check with plant;LP: 香根草组低浓度Cd处理low treatment group with plant; MP: 香根草组中浓度Cd处理medium treatment group with plant;HP: 香根草组高浓度Cd处理high treatment group with plant | |||||
两者的交互效应对中性交换态Cd含量无显著影响,对螯合态和残渣态Cd含量有极显著影响,对生物有效态和总Cd含量有显著影响。经90 d处理后,香根草组与无植物组相比不同浓度处理组土壤中总Cd含量均降低,LP、HP组与相应的无植物组之间差异显著。与无植物组相比,香根草组土壤中生物有效态Cd含量降低,其中MP、HP组生物有效态Cd含量显著低于无植物组。香根草各处理组土壤中性交换态和螯合态Cd含量均降低,高浓度处理组显著低于相应的无植物处理组。香根草组残渣态Cd低于无植物组,其中LP和HP显著低于相应的无植物处理组。
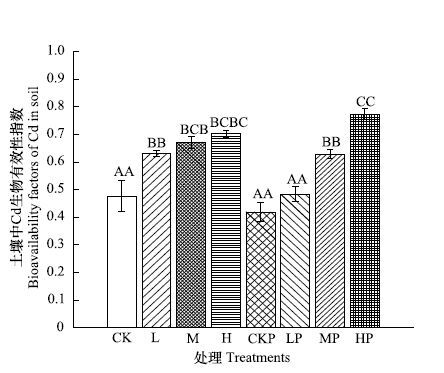
图 2为不同Cd浓度处理香根草组和无植物组土壤中Cd的生物有效性。由图可知,土壤中Cd的生物有效性指数随处理浓度的升高而增加。香根草组土壤生物有效性除HP组外均低于无植物处理组,其中LP组与L组间差异显著。
|
| 图 2 不同Cd浓度处理香根草和无植物土壤中Cd的生物有效性指数 Fig. 2 Bioavailability factors (BFs) of Cd in soils with Vetiveria zizanioides and no plant under different Cd treatments |
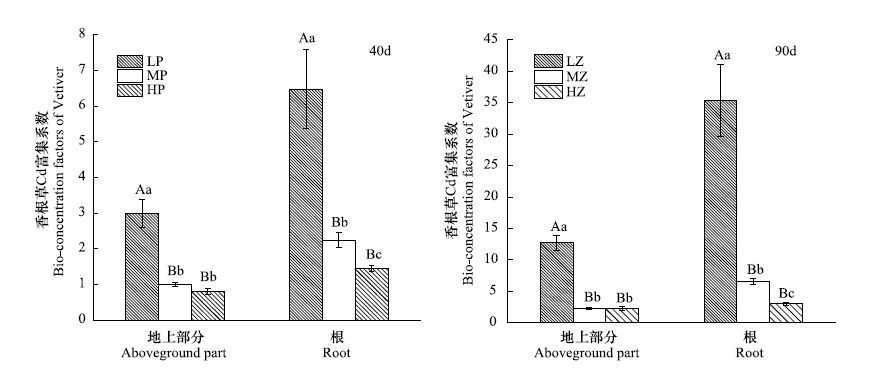
香根草根部的生物富集系数在40 d、90 d两次取样时均随土壤Cd处理浓度升高而显著下降(图 2),其地上部分LP组的生物富集系数显著高于MP和HP组,MP和HP组无显著差异。香根草根部LP组的富集系数显著高于MP和HP组,如40 d和90 d时香根草MP、HP组根部生物富集系数较LP组分别降低65.4%、77.8%和81.4%、91.5%。随着处理时间的延长,90 d时香根草的生物富集系数均大于40 d时的结果,其中90 d时香根草HP组地上部分和根部的生物富集系数分别是40 d时的2.95倍和2.22倍。
|
| 图 3 不同浓度的Cd胁迫下香根草的富集系数 Fig. 3 Effects of the different Cd concentration on Bio-concentration factor of Vetiveria zizanioides |
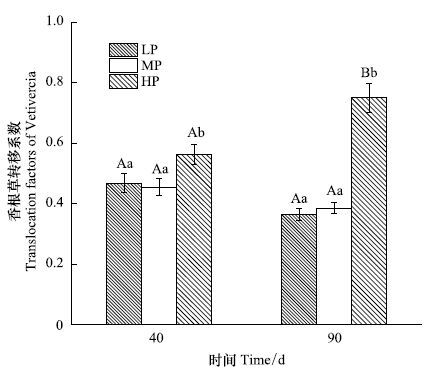
在40 d、90 d两次取样时香根草LP和MP组的转移系数均显著低于HP组(图 4),HP组的转移系数在40 d和90 d时分别达到0.56和0.74,分别是LP组的1.20倍和2.05倍,是MP组的1.24倍和1.94倍。随着处理时间的延长,90 d时LP组和MP组的转移系数较40 d天时均降低,与40 d相比,90 d时HP组的转移系数有所增加,是40 d的1.34倍。
|
| 图 4 不同浓度的Cd胁迫对香根草转移系数 Fig. 4 Effects of the different Cd concentration on translocation factor of Vetiveria zizanioides |
用于重金属污染治理的富集植物,其体内重金属积累量直接决定其修复效率。以往研究的焦点集中于超富集植物,即具有能够超量吸收积累重金属能力的植物[17]。就重金属Cd而言,超富集植物即自然条件下叶片或地上部分干重的Cd含量大于 100 mg/kg的植物[18]。魏树和[19]等研究发现龙葵(Solanum nigrum L)茎和叶中的Cd积累量分别达到104 mg/kg和125 mg/kg;杜瑞英[20]等研究发现象草(Pennisetum purpureum)地上部分Cd含量可达200 mg/kg,根部可达91 mg/kg。但以上植物的生物量较小,在实际应用中对土壤中Cd的修复效果有限。
研究表明香根草对Cd有一定的耐性和富集能力,刘国云[21]等通过水培研究发现香根草对于Cd的积累量随处理浓度的升高而增加,本试验结果与其一致,试验中不同处理香根草体内Cd含量存在显著差异。香根草对Cd的积累量随时间的延长而增加,试验期间香根草生物量在试验中的Cd处理浓度和时间范围内未受明显影响,说明香根草可在一定范围Cd胁迫下生长。本试验中,处理90 d时,高浓度处理组香根草地上部分和根系的Cd积累量分别高达180.42 mg/kg和241.54 mg/kg,显示出较强的Cd富集能力。
富集系数可以反映植物对于重金属吸收、积累能力,用以修复重金属污染的植物富集系数在1以上为好[22]。研究表明,孔雀草(Tagetes patula)和胡杨(Populus euphratica)的富集系数随重金属处理浓度的升高而下降[23-24],本试验的结果与其一致。香根草对于低浓度的Cd富集效果最为明显,40 d时低浓度处理组香根草地上部分和根部富集系数分别达到2.99和6.48,显著高于中高浓度处理组。但随着处理时间的延长,香根草各部分的富集系数显著上升,90 d时高浓度组地上部分和根部的Cd积累量较40 d时分别增加66.3%和52.6%。
植物通过根系吸收重金属并将部分重金属转移至地上部分,大多数植物根部的重金属富集量高于地上部分[11]。植物根细胞可贮存较多的Cd,减少Cd向地上部分的运输[25]。研究表明Cd可取代叶绿体中的Fe2+、Zn2 +、Mg2+等与其体内富含巯基 (— SH) 的蛋白质结合,破坏叶绿体微结构,抑制叶绿素前体的合成,并导致叶绿素分解,造成叶绿素含量降低[26]。本试验两次取样结果均显示香根草根部的Cd含量高于地上部分,香根草40 d和90 d时高浓度组的转移系数分别为0.56和0.75,均小于1。香根草这种Cd储藏策略可降低Cd对地上部分产生的毒害作用。
通常认为土壤中的总Cd含量越高其潜在的危害越大,但Cd在土壤中的生物活性直接决定Cd污染的危害程度。沈阳张士灌区长期直接使用工业废水灌溉农田,梁彦秋等人研究发现该污染区域土壤中有效态Cd含量占50%,导致该地区农作物Cd含量严重超标[27]。邓朝阳等人研究发现,土壤有效态Cd含量与土壤总Cd含量有显著的线性关系[28]。研究表明植物能够影响其根际土壤中重金属的形态[29-31],但尚无定论。有研究认为植物通过根际分泌物来对土壤中难溶态的Cd进行活化,提高土壤中Cd的生物有效性[31]。李花粉等研究发现根际分泌物中的有机酸可促进难溶态的Cd溶解,如小麦和水稻在缺铁的情况下会从根部大量释放植物铁载体,能够活化根际难溶态的Cd,从而影响土壤中Cd的形态[32]。植物也可通过根系吸附、沉积,或者通过络合作用降低金属离子价态来固定重金属,从而降低土壤中有效态重金属含量[18]。本试验中,各处理组土壤中总Cd的生物有效性指数随处理浓度的增加而增加,说明Cd浓度越高,生物活性态Cd的含量也就越大,其生物毒性越强。本试验中,香根草组与无植物组相比土壤中生物有效态Cd和总Cd含量均降低,说明种植香根草可降低土壤中Cd含量。与无植物组相比,香根草各处理组残渣态Cd含量减少表明种植香根草使残渣态Cd转化为生物有效态Cd,将来研究中需继续关注其具体作用机制。低浓度处理组香根草根际土中Cd生物有效性指数显著低于无植物组,随着处理时间的延长,土壤生物有效性有所降低。处理90 d时香根草组土壤中的生物有效态Cd含量和总Cd含量大多显著低于相应的无植物处理组,说明香根草在试验处理范围内对土壤中的Cd具有较好的清除效果,且随着处理时间的延长清除效果越显著。
4 结论(1) 香根草通过根系吸收土壤中的Cd,将部分Cd转移至地上部分,转移系数随处理浓度增加和处理时间延长而增大,但其转移系数始终小于1。
(2) 香根草能有效降低土壤中的总Cd含量,其Cd积累量随处理浓度的增高和处理时间的延长而增加,但随着处理浓度的增加,其富集系数显著降低。
(3) 种植香根草使其根际土中Cd形态发生转化,可提高香根草对Cd清除效率。
本试验中香根草对于不同处理土壤中Cd均有清除效果,其中对于HP组清除效果最为显著,综合香根草生物量大,生长快速的特点,可考虑将其用于Cd污染地区的植物修复。
| [1] | Willey N.Phytoremediation: Methods and Reviews.Totowa, New Jersey: Humana Press,2007 351–379. |
| [2] | 环境保护部, 国土资源部. 全国土壤污染状况调查公报. 中国国土资源报, (2014-04-18) [2015-06-25].http://www.gtzyb.com/yaowen/20140418_62262.shtml. |
| [3] | DalCorso G, Farinati S, Maistri S, Furini A.How plants cope with cadmium: staking all on metabolism and gene expression.Journal of Integrative Plant Biology,2008,50(10): 1268–1280. |
| [4] | 王庆仁, 崔岩山, 董艺婷.植物修复-重金属污染土壤整治有效途径.生态学报,2001,21(2): 326–331. |
| [5] | Salt D E, Blaylock M, Kumar N P B A, Dushenkov V, Ensley B D, Chet I, Raskin I.Phytoremediation: a novel strategy for the removal of toxic metals from the environment using plants.Nature Biotechnology,1995,13(5): 468–474. |
| [6] | 廖晓勇, 陈同斌, 阎秀兰, 聂灿军.提高植物修复效率的技术途径与强化措施.环境科学学报,2007,27(6): 881–893. |
| [7] | 韦朝阳, 陈同斌.重金属超富集植物及植物修复技术研究进展.生态学报,2001,21(7): 1196–1203. |
| [8] | Baker A J M, Proctor J.The influence of cadmium, copper, lead, and zinc on the distribution and evolution of metallophytes in the British Isles.Plant Systematics and Evolution,1990,173(1/2): 91–108. |
| [9] | Wei S H, Clark G, Doronila A I, Jin J, Monsant A C.Cd hyperaccumulative characteristics of Australia ecotype Solanum nigrum L.International Journal of Phyoremediation,2013,15(3): 199–205. |
| [10] | 刘威, 束文圣, 蓝崇钰.宝山堇菜(Viola baoshanensis)-一种新的镉超富集植物.科学通报,2003,48(19): 2046–2049. |
| [11] | Pulford D, Watson C I.Phytoremediation of heavy metal-contaminated land by trees-a review.Environment International,2003,29(4): 529–540. |
| [12] | 高伟, 魏虹, 贾中民, 田晓峰.香根草对镉胁迫的光合响应.西南师范大学学报:自然科学版,2012,37(10): 59–64. |
| [13] | 努扎艾提·艾比布, 刘云国, 曾光明, 徐立, 宋华晓, 陈贝贝.香根草对镉毒害的生理耐性和积累特性.环境科学学报,2009,29(9): 1958–1963. |
| [14] | Maiz I, Arambarri I, Garcia R, Millán E.Evaluation of heavy metal availability in polluted soils by two sequential extraction procedures using factor analysis.Environmental Pollution,2000,110(1): 3–9. |
| [15] | Islam M S, Ueno Y, Sikder M T, Kurasaki M.Phytofiltration of arsenic and cadmium from the water environment using Micranthemum umbrosum(J.International Journal of Phytoremediation,2013,15(10): 1010–1021. |
| [16] | Park S, Kim K S, Kang D, Yoon H, Sung K.Effects of humic acid on heavy metal uptake by herbaceous plants in soils simultaneously contaminated by petroleum hydrocarbons.Environmental Earth Sciences,2013,68(8): 2375–2384. |
| [17] | 陈同斌, 阎秀兰, 廖晓勇, 黄泽春, 雷梅.关于hyperaccumulator中文译名的探讨.环境科学学报,2005,25(9): 1148–1150. |
| [18] | Ali H, Khan E, Sajad M A.Phytoremediation of heavy metals-concepts and applications.Chemosphere,2013,91(7): 869–881. |
| [19] | 魏树和, 周启星, 王新, 张凯松, 郭观林.一种新发现的镉超积累植物龙葵(Solanum nigrum L).科学通报,2004,49(24): 2568–2573. |
| [20] | 杜瑞英, 聂呈荣, 林初夏, 刘勇.镉污染土壤对潜在能源植物生长的影响.生态环境,2006,15(4): 735–738. |
| [21] | 刘云国, 宋筱琛, 王欣, 闵宗义, 柳思勉.香根草对重金属镉的积累及耐性研究.湖南大学学报:自然科学版,2010,37(1): 75–79. |
| [22] | Sun Y B, Zhou Q X, Wang L, Liu W T.Cadmium tolerance and accumulation characteristics of Bidens pilosaL.Journal of Hazardous Materials,2009,161(2-3): 808–814. |
| [23] | Liu Y T, Chen Z S, Hong C Y.Cadmium-induced physiological response and antioxidant enzyme changes in the novel cadmium accumulator, Tagetes patula.Journal of Hazardous Materials,2011,189(3): 724–731. |
| [24] | Sun J, Wang R G, Zhang X, Yu Y C, Zhao R, Li Z Y, Chen S.Hydrogen sulfide alleviates cadmium toxicity through regulations of cadmium transport across the plasma and vacuolar membranes in Populus euphraticacells.Plant Physiology and Biochemistry,2013,65 67–74. |
| [25] | Chardonnens A N, Ten Bookum W M, Kuijper L D J, Verkleij J A C, Ernst W H O.Distribution of cadmium in leaves of cadmium tolerant and sensitive ecotypes of Silene vulgaris.Physiologia Plantarum,1998,104(1): 75–80. |
| [26] | Liang P, Pardee A.Differential display of eukaryotic messenger RNA by means of the polymerase chain reaction.Science,1992,257(5072): 967–971. |
| [27] | 梁彦秋, 刘婷婷, 铁梅, 邓斌, 孙鹏, 臧树良.镉污染土壤中镉的形态分析及植物修复技术研究.环境科学与技术,2007,30(2): 57–58. |
| [28] | 邓朝阳, 朱霞萍, 郭兵, 王小玉, 吴九九, 张军.不同性质土壤中镉的形态特征及其影响因素.南昌大学学报:工科版,2012,34(4): 341–346. |
| [29] | Mench M J, Fargues S.Metal uptake by iron-efficient and inefficient oats.Plant and Soil,1994,165(2): 227–233. |
| [30] | 张雯, 魏虹, 孙晓灿, 顾艳文.镉在土壤-金丝垂柳系统中的迁移特征.生态学报,2013,33(19): 6147–6153. |
| [31] | 陈有鑑, 陶澍, 邓宝山, 张学青, 黄艺.不同作物根际环境对土壤重金属形态的影响.土壤学报,2001,38(1): 54–59. |
| [32] | 李花粉, 郑志宇, 张福锁, 毛达如.铁对小麦吸收不同形态镉的影响.生态学报,1999,19(2): 170–173. |
 2016, Vol. 36
2016, Vol. 36




