文章信息
- 马琨, 杨桂丽, 马玲, 汪春明, 魏常慧, 代晓华, 何文寿
- MA Kun, YANG Guili, MA Ling, WANG Chunming, WEI Changhui, DAI Xiaohua, HE Wenshou.
- 间作栽培对连作马铃薯根际土壤微生物群落的影响
- Effects of intercropping on soil microbial communities after long-term potato monoculture
- 生态学报[J]. 2015, 36(10): 2987-2995
- Acta Ecologica Sinica[J]. 2015, 36(10): 2987-2995
- http://dx.doi.org/10.5846/stxb201412072425
-
文章历史
- 收稿日期: 2014-12-07
- 网络出版日期: 2015-09-28
马铃薯是宁夏南部山区的主栽作物。近年来,随着栽培面积持续扩大,轮作倒茬困难,由此带来的连作障碍问题日渐突出,缓解或消除马铃薯连作障碍迫在眉睫。已有研究表明,大豆、黄瓜、草莓等作物连作后会对土壤微生物产生抑制作用,使土壤微生物总数、细菌数量减少,真菌数量增加[1-3]。随地黄种植年限的增加,细菌种类及数量不断减少,特别是芽孢杆菌和放线菌等种类的改变,致使土壤微生物群落多样性水平呈下降趋势[4]。Zhou[5]等认为,连作或间作对根际微生物群落组成的影响不同,这种影响可以一直存在于之后的第2个或第3个生长季节。间作是两种或两种以上作物同时生长在同一土地上的农业生产活动;由于间作作物的物候和生长周期性差异、播种或收获时间的不同,能产生生态位补偿效应;导致不同的作物养分需求,通过较早成熟作物残落物的矿化、增加土壤养分的有效性、增强对作物病虫、草害的抗性[6]。不同间作物种能通过竞争互补和互利,在时间、空间和利用形态上合理分配资源而减少竞争;直接或间接通过影响种间生物或非生物的环境,提升可利用资源的有效性[7]。尤其是在低投入的农业生产中,禾谷类与豆类作物间作通常被认为可以补充土壤氮源[8];在萝卜-玉米、蚕豆-玉米、鹰嘴豆-玉米和大豆-玉米间作体系中作物产量和土壤磷的利用效率,明显有超过单作栽培的优势[9];所以间作栽培下作物对资源的高效利用在很大程度上提高了产量[10];可见,间作是有限土地上使作物产量最大化的一种完善策略。因此,能否采用间作调控方式来缓解马铃薯连作栽培障碍,稳定宁南山区马铃薯的生产可能是一种有益的探索。
土壤微生物是土壤生态系统的重要组成部分,在物质循环过程中扮演着重要的角色,对保持土壤健康至关重要[11]。AM真菌(Arbuscular Mycorrhizal Fungi)作为土壤微生物群落的重要组分,它能与地球上90%的植物建立良好的共生关系,可通过与宿主植物形成菌根,影响根系分泌物[12]、影响土壤微生物群落结构组成,引起多样性的变化[13]。间作能通过改变植物生理特征和根系分泌物而间接影响根际微生物群落组成,通过增加微生物总量来改善土壤环境[14]。因此,只有加深对土壤微生物群落结构、功能的了解,才能够阐明不同作物间作栽培对连作土壤的影响机制。假设,间作调控中较高的植物多样性有助于土壤微生物群落结构、功能及AM真菌多样性的提高。所以,以连作10a马铃薯土壤为基质,从作物种间关系的角度,研究不同作物与马铃薯间作是否能显著改变连作作物根际土壤环境,有利于马铃薯的健康生长,以期为缓解或解决宁夏南部山区马铃薯连作障碍提供理论依据。
1 材料与方法 1.1 研究区概况试验地点位于宁夏固原市张易镇马场村(10605′37.8″—106°06′16.3″E,35°54′45.3″—35°55′17.0″N),该区域海拔2132—2277 m,年均降水量410 mm,年均蒸发量1370 mm,年均气温6 ℃。供试土壤为黑垆土,土壤有机质35.79 g/kg,全氮1.32 g/kg,全磷1.12 g/kg,碱解氮118.07 mg/kg,速效磷94.86 mg/kg,速效钾735.37 g/kg,pH 8.61(1∶5)。
1.2 试验设计试验布设于2012年4月,选择马铃薯连作10a田块,采用单因素随机区组设计,3处理,3重复,小区面积9 m×25 m。处理分别为:a 马铃薯单作(CK);b 玉米‖马铃薯;c 蚕豆‖马铃薯。播前每亩基施农家肥37.5t/hm2、磷酸二铵600 kg/hm2。种植2行玉米或2行蚕豆,间种4行马铃薯。玉米行株距为50 cm×35 cm,蚕豆行株距15 cm×30 cm,马铃薯行距为40 cm×50 cm。供试马铃薯、蚕豆、玉米品种分别为庄薯3号、临蚕6号和长城1124。马铃薯盛花期采集靠近玉米或蚕豆行的马铃薯根际土壤样本,用于土壤微生物群落结构及功能分析;去除表层5cm土壤后,收集土壤样品,湿筛倾析法分离孢子,用于AM真菌多样性鉴定。
1.3 试验方法 1.3.1 土壤微生物群落结构与功能测定利用PLFAs(Phospholipid fatty acids)分析来研究土壤微生物群落结构组成[15-16]。称取相当于10 g烘干土的新鲜土样,加入磷酸缓冲液30 mL,甲醇∶氯仿(2∶1)105 mL混合液振荡2 h后,分别加入氯仿36 mL和无菌水36 mL,避光浸提18—24 h。有机相过滤、浓缩,利用固相萃取技术,通过SPE固相萃取小柱(Bond Elute,500 mg/3 mL)进行脂肪酸分离,氮吹仪浓缩后,加氢氧化钾∶甲醇(1∶1)1 mL,37 ℃加热15 min进行甲基化。加内标液(十九碳酸甲酯)0.5 mL,用GC-MS分析。定量标准品为:Supelco 37 Component FAME Mix(FAME 37,47885-U)。采用Agilent 6890N型气相色谱仪,进样口为300 ℃、He流量为1 mL/min、色谱柱为Agilent HP-5MS,30 m×250 μm×0.25 μm,升温程序为45 ℃(2 min)—300 ℃(4 min),6 ℃/min的色谱条件下平行分析磷脂脂肪酸混合物标样和待检样本。
土壤微生物群落功能多样性采用BIOLOG-ECO板来测定[16]。称取相当于10g干土的新鲜土样,加入无菌生理盐水,振荡30 min后于4 ℃下静止10 min,然后吸取1 mL原液于99 mL无菌生理盐水中,摇匀后吸取125 μL样品接种于ECO板。28 ℃培养,590 nm连续读数7d。
1.3.2 AM真菌孢子形态结构的鉴定AM真菌鉴定根据孢子形态特征进行[17]。参照张美庆[18]等的方法,统计AM真菌的相对多度、分离频度。相对多度(RA):指采样点某属或种的孢子数/该采样点AM真菌总孢子数×100%;分离频度(F):菌根真菌某种或属的出现次数/土样数。出现频率>20%的种为优势种,10%<出现频率>20%为常见种,出现频率<10%为稀有种。
1.3.3 数据处理与分析利用EXCEL进行数据处理,DPS v 7.05进行方差分析(LSD法)。
2 结果与分析 2.1 间作栽培对连作土壤微生物群落结构的影响土壤中提取的PLFA可作为主要微生物类群的指示标志,特征脂肪酸的改变就可以表征某一类群的微生物群落变化[19]。根际土壤微生物群落的总磷脂脂肪酸含量在17.79—21.79 μg/g (图1),其中,尤其以16:1ω5c(AMF)、i16:0(细菌)和18:2ω6t(腐生真菌),18:1ω9t(革兰氏阴性菌),18:1ω9c(革兰氏阳性菌)4种脂肪酸含量较高。处理中18:1ω9c(革兰氏阳性菌)生物量占有绝对优势,间作蚕豆后,马铃薯根际土壤微生物的18:1ω9c含量比对照升高了10.93%,而间作玉米则降低了37.53%;16:1ω5c(AMF)和i16:0(细菌)微生物生物量次于18:1ω9c表征的土壤微生物类群;这两种主要的PLFA均表现出与18:1ω9c相似的变化规律,蚕豆间作的增加幅度在6.73%—25.46%,而玉米间作这两种脂肪酸含量下降幅度为8.95%—24.79%。尽管玉米间作马铃薯主要微生物群落组成中脂肪酸的种类没有明显改变,但主要的PLFA类型均较对照有所降低,说明玉米与马铃薯间作调控改变了根际微生物与环境的关系,在一定程度上削弱了马铃薯根际土壤微生物群落构成中主要微生物的生物量。而蚕豆间作马铃薯提高了主要微生物种群的生物量,该间作体系可能对改善连作马铃薯根际微生物群落结构和土壤健康状况有更好的促进作用。推测认为,这可能与蚕豆根瘤菌的固氮及其与马铃薯根系的交互作用有关。

|
| 图 1 间作栽培对马铃薯根际土壤PLFA类型的影响 Fig. 1 Relative kinds of phospholipids fatty acids (PLFAs) in potato rhizosphere under different cropping manner |
尽管PLFA分析提供的群落结构组成只是一种表型结果,但它描述的是类似于生态功能群的概念,可以指示主要群落组成及生理变化[20]。试验结果显示,间作调控后马铃薯根际土壤微生物群落结构相较于对照发生了显著变化(表1)。玉米间作组成中主要微生物种群的PLFA整体低于对照和蚕豆间作处理,其中革兰氏阴性菌、阳性菌、假单孢菌、AM真菌分别比对照下降了35.13%、28.01%、24.79%、8.95%。但,群落真菌组成,却比对照增加了21.11%。蚕豆间作表现出截然相反的趋势,主要微生物类群生物量均显著增加;和对照相比,革兰氏阳性菌、阴性菌、AM真菌、真菌生物量比例分别增加了11.73%、6.13%、25.46%和 6.73%。尽管玉米间作以PLFA表征的微生物群落生物量下降,但土壤微生物主要功能群的组成却表现出与马铃蚕豆间作相似的趋势,即细菌所占比例均下降,真菌所占比例上升;相关研究也认为植物群落结构是与土壤微生物群落高度相关,植物群落结构可以通过影响植物枯落物的质量、数量及分泌物,最终导致微生物群落的改变[21]。间作栽培下,随不同作物种间关系的改变,玉米、蚕豆可能会通过竞争互补和互利作用影响马铃薯根系分泌物的数量、类型和土壤养分的有效性,间接影响了马铃薯根际土壤碳源组成及碳循环,而导致微生物群落结构发生改变。
| 处理 Treatment | 生物量Biomasses/(μg/g) | ||||||||
| 革兰氏阳性菌(G+) | 好氧菌 Aerobic Bacteria (G+) | 菌根真菌 AMF | 假单胞菌 Pseudomonas (G-) | 革兰氏阴性菌 (G-) | 真菌 Fungi | 其它菌群 Other | 真菌/细菌Fungi/Bacteria | 菌群总生物量Total Biomass | |
| 单作monoculture | 7.58 | 0.82 | 3.46 | 3.32 | 0.90 | 0.61 | 1.11 | 0.32 | 17.80 |
| 马‖玉Potato-Maize | 4.96 | 0.48 | 3.15 | 2.50 | 0.54 | 1.77 | 1.24 | 0.58 | 14.65 |
| 马‖蚕Potato-Faba bean | 8.37 | 1.01 | 4.34 | 3.54 | 0.94 | 2.73 | 0.86 | 0.51 | 21.79 |
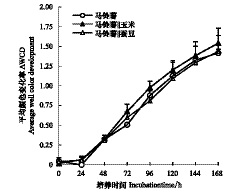
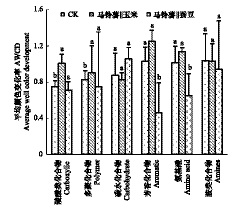
微生物对不同碳源的利用能力可以反映代谢功能类群的差异[13]。由图2可见,在培养0—24 h,平均颜色变化率(AWCD)没有明显差别;72 h后,微生物群落生理代谢剖面出现差异;与其它处理相比,玉米间作马铃薯AWCD总体要高出12.9%—33.1%。144 h时,相比马铃薯单作,AWCD值提高了8.81%,蚕豆间作马铃薯AWCD下降了1.52%,蚕豆间作与对照间基本没有差异。这表明玉米间作一定程度上提高了微生物群落的功能多样性;随群落微生物结构的变化,蚕豆间作引起土壤微生物功能多样性差异表现不明显。但,间作调控后土壤微生物优先利用的碳源类型和利用程度有显著差别(图3)。受玉米根系的影响,羧酸类、多聚化合物、芳香类、氨基酸类化合物成为马铃薯根际微生物主要利用的碳源;和对照相比,土壤碳源的利用强度分别提高了34.43%、8.95%、21.56%、12.29%。而蚕豆间作,除了碳水化合物的利用强度提高了20.89%以外,芳香化合物和氨基酸类化合物的利用强度却明显降低,仅相当于对照的44.94%和63.86%;也仅为玉米间作处理的36.97%、56.87%。可见,玉米、蚕豆与马铃薯根系间的相互作用会形成不同的种间关系;蚕豆间作马铃薯,在根系的交互作用影响下,有利于以碳水化合物为碳源的微生物种群增长;玉米间作马铃薯,有利于以羧酸类、多聚化合物、芳香类化合物、氨基酸类为碳源的微生物类群功能显著增加,相应导致了根际土壤微生物结构的不同变化。
|
| 图 2 不同间作种植模式下AWCD的变化 Fig. 2 Change of average well color development(AWCD)in different intercropping manner |
|
| 图 3 不同间作种植模式下微生物碳源利用能力的变化 Fig. 3 Difference of soil microbial community in carbon utilization ion in different intercropping manner |
土壤中分离鉴定出AM真菌,共4属43种(表2)。其中,球囊霉属(Glomus)34种,占AMF总数的79.07%;无梗球囊霉属(Acaulospra)7种,占总数的16.28%;盾巨孢球囊霉属(Scutellospora)、内养球囊霉属(Endospora)各1种,均占总数的2.33%。各处理均以球囊霉属的AM真菌占优势,是优势属。盾巨孢囊霉属的AM真菌仅出现在马铃薯间作蚕豆处理,内养霉囊属AM真菌仅出现在对照处理。对照处理共鉴定出AM真菌总数为29种,其中球囊霉属24种、无梗囊霉属4种;但玉米间作中球囊霉属仅为17种,无梗囊霉属5种;蚕豆间作为20种,无梗囊霉属2种。两种调控模式下球囊霉属真菌减少了7种和4种。玉米间作下球囊霉属相对多度相较对照提高了6.90%;蚕豆间作降低了24.68%;无梗囊霉属相对多度均表现为显著增加(表3)。此外,AM真菌优势种由单作时的明球囊霉、地球囊霉转变为马铃薯玉米间作体系里的福摩萨球囊霉、球泡球囊霉;福摩萨球囊霉和疣状无梗囊霉是蚕豆间作体系里的优势种。由于不同间作栽培下作物种间的相互影响,AM真菌优势种有一个明显的转变过程,AM真菌多样性显著降低。
| 菌根真菌 Arbuscular mycorrhizal fungi | 马铃薯单作 Potato Monoculture | 马‖玉米 Potato-corn | 马‖蚕豆 Potato-Faba Bean |
| 球囊霉属Glomus | |||
| 树状球囊霉G.arborense | + | ||
| 白色球囊霉G.albidum | + | ||
| 双型球囊霉G.ambisporum | + | ||
| 血管球囊霉G.borele | + | ||
| 苏格兰球囊霉G.caledonium | + | + | + |
| 近明球囊霉G.claroides | + | + | + |
| 明球囊霉G.clarum | + | + | + |
| 缩球囊霉G.constrictum | + | + | |
| 厚皮球囊霉G.callosum | + | + | |
| 卷曲球囊霉G.convolutum | + | ||
| 两型球囊霉G.dimorphicum | + | + | |
| 沙荒球囊霉G.deserticola | + | + | + |
| 道氏球囊霉G.dominikii | + | ||
| 德里球囊霉G.delhiense | + | + | |
| 幼套球囊霉G.etunicatum | + | + | + |
| G.fuegianum | + | ||
| 福摩萨球囊霉G.formosanum | + | + | + |
| 地球囊霉G.geosporum | +) | + | + |
| 球泡球囊霉G.globiferum | + | + | + |
| G.halon | + | + | |
| 异形球囊霉G.heterosporum | + | + | |
| 何氏球囊霉G.hoi | + | + | |
| 根内球囊霉G.intraradix | + | ||
| G.invermayanum | + | ||
| 小果球囊霉G.microcarpum | + | ||
| 黑球囊霉G.melanosporum | + | + | |
| 膨果球囊霉G.pansihalos | + | ||
| G.pulvinatum | + | ||
| 网状球囊霉G.reticulatum | + | ||
| G.rediatum | + | ||
| 扭形球囊霉G.tortuosum | + | + | |
| 三壁球囊霉G.trimurales | + | + | |
| G.tenerum | + | ||
| 地表球囊霉G.versiforme | + | + | |
| 无梗囊霉属Acaulospora | |||
| 细齿无梗囊霉A.denticulata | + | ||
| A.delicata | + | ||
| 光壁无梗囊霉A.laevis | + | ||
| 瑞氏无根囊霉A.rehmii | + | + | |
| A.sporocarpa | + | + | |
| 刺无梗囊霉A.spinosa | + | ||
| 疣状无梗囊霉A.tuberculata | + | + | + |
| 盾巨孢囊霉属Scutellospora | |||
| Scu.taiwanasis | + | ||
| 内养霉囊属Entrophospora | |||
| E.infrequens | + | ||
| 种数合计Total species | 29 | 22 | 23 |
| 处理Treatment | 球囊霉属Glomus | 无梗囊霉属Acaulospora | 盾巨孢囊霉属Scutellospora | 内养囊霉属Endospora | 优势种 Dominant species | ||||
| 相对多度/%Relative abundance | 分离频度 Frequency | 相对多度/% Relative abundance | 分离频度 Frequency | 相对多度/%Relative abundance | 分离频度 Frequency | 相对多度/%Relative abundance | 分离频度Frequency | ||
| 单作Monoculture | 30.75 | 0.89 | 0.29 | 0.04 | - | - | 2.59 | .07 | G.clarum,G.geosporum |
| 马‖玉Potato-Maize | 23.16 | 0.8 | 3.48 | 0.2 | - | - | - | - | G.formosanum,A.tuberculata |
| 马‖蚕Potato-Faba bean | 32.81 | 0.69 | 6.32 | 0.28 | 0.4 | 0.03 | - | - | G.formosanum,G.globiferum |
间作土壤微生物的活性及微生物群落结构与功能显著受土地管理活动、作物种类和作物生理活性的影响,间作优势就是由于作物间的交互作用和作物根际微生物活性变动引起得[22]。Wang[23]等报道,酸性土壤上小麦间作芸薹属植物对土壤微生物群落结构有多种影响,间作改变了小麦根际微生物群落结构。随植物群落多样性的增加,土壤细菌和放线菌的丰富度减少,真菌丰富度增加[24]。试验中细菌群落随栽培措施的改变有较大的变动,优势类群均为细菌群落;其中尤以蚕豆间作处理根际细菌微生物量最高,且表现为革兰氏阳性菌明显高于革兰氏阴性菌。Artursson V和Jansson J K[25]分析认为,根系分泌物的某种成分能促进土壤中革兰氏阳性细菌、AM真菌的积累,相应增加了微生物的总生物量;另一方面,豆科植物的固氮,导致根际土壤养分的提升,可能也是豆科与马铃薯间作时促进土壤PLFA表征的总生物量增加的原因[26]。
Li[27]等,采用PLFA的方法也证实了间作可以影响玉米和豆科根际微生物群落结构。试验中玉米间作马铃薯土壤微生物群落PLFA降低,而马铃薯间作蚕豆下PLFA生物量上升,说明禾本科和茄科作物的交互效应可能会降低微生物群落生物量,豆科与茄科作物的组合有利于提高土壤微生物群落生物量,不同种类植物根系之间会产生不同的根际效应。Zhou[5]等认为,根系分泌物的组成能够强烈受植物发育阶段的影响,根系分泌物释放进入根际后,可能增强土壤生物活性并且改变微生物群落结构;由于物种在生化组成上的不同,植物枯落物和根际沉积(小分子的代谢物、氨基酸、分泌酶、粘液、细胞裂解物)、植物根系间的共生关系也应该是引起微生物群落结构变化的因素。因此,认为,土壤中真菌、细菌群落的组成和多样性很大程度上依赖于可利用的碳源。马铃薯‖蚕豆间作,由于豆科生物固氮菌刺激了生物固氮过程增加了植物养分的供给,改善了根际养分的移动性和有效性,导致植物根际分泌物的增加,使其根际效应比马铃薯‖玉米间作更明显;马铃薯、蚕豆种间效应直接导致了马铃薯较强的作物生理变化而影响其根系分泌物的种类、数量和质量,结果较多的有机物质输入进入土壤,导致土壤有机碳库快速的恢复,这些就提供了更多样化的有机化合物及碳源,刺激形成更多样化的微生物群落,最终,导致马铃薯‖蚕豆根际微生物群落组成及微生物生物量比玉米‖马铃薯系统有更大的变化。此外,试验结果也显示细菌群落随栽培措施的改变有较大的变动,说明在连作和间作系统中土壤微生物群落是不同的。
在微生物碳源利用多样性上,玉米间作马铃薯表现出较高的AWCD值,微生物群落对多种碳源类型均表现较强的利用能力。Thevathasan 和 Gordon[28]认为,较高的植物多样性将增加土壤碳源的多样性,并且能够形成更复杂的土壤空间状态特征。分析认为,马铃薯间作玉米、蚕豆由于物种根系分布深度和生长季节性差异特征,会产生了不同的根际和空间效应,改变了马铃薯与玉米、蚕豆根系间的物质循环;此外,马铃薯与玉米、蚕豆根系间不可避免的接触必然会改变根际微生态环境,相应影响了植物新陈代谢,造成植物根际分泌物数量和质量的变化。因此,马铃薯‖玉米可能更有利于根系产生大量、高质量的根系分泌物,促进了马铃薯‖玉米根际微生物对碳的同化,提升了微生物群落的功能多样性。而蚕豆间作马铃薯,仅表现为显著提升了以碳水化合物为碳源的微生物群落代谢多样性。另外,试验中微生物群落代谢功能多样性主要利用可培养的微生物群落功能多样性来评价,这就有可能限制了在土壤中不能培养但占优势地位的微生物群落的功能表现[29],是否就是造成了不同物种间作下,土壤微生物群落结构变化与功能变化不一致的原因。因此,持续的土壤微生物群落结构与功能观察才能更好的解释土壤微生物结构改变引起的功能响应。
3.1.2 间作栽培对马铃薯根际AM真菌多样性的影响植物根系和AM真菌之间的联系,被证实是陆地超过80%植物的一种成功进化策略,这种共生关系为真菌提供了碳水化合物,而使宿主植物获得了矿质营养[30]。农田管理会影响土著AM真菌对养分的利用效率及作物产量的贡献,在传统生产体系中农业管理活动也会影响土壤系统及AM真菌群落组成和丰富度[30-31]。AM真菌形态学鉴定揭示了单作和间作系统AM真菌组成有明显的差异,尽管相对多度和频率上有差别,但AM真菌在两个间作系统有共同的优势种福摩萨球囊霉(G.formosanum)。已有研究显示,AM真菌分类群的分布变化是由于养分的有效性、土壤类型、土壤扰动和有毒的化合物影响了主要分类群的生境而产生的结果[32]。AM真菌也能够提高土壤中磷溶细菌、菌根促生菌和土壤团聚体促生菌等有益微生物的活性,并能提高豆科植物根瘤菌的固氮能力和活性[33];这也就有助于解释马铃薯豆科间作下,碳源类型由对照处理的芳香化合物、氨基酸类化合物转变为碳水化合物的现象,应该是由于AM真菌优势种群变化,影响了土壤微生物群落结构而产生的结果。此外,土壤pH、宿主植物类型在一定条件下也可通过影响AM真菌,使间作体系里的土著AM真菌优势种改变,影响群落微生物功能,从而改变土壤的健康状态[34]。
3.2 结论间作栽培显著改变了根际土壤微生物主要功能群的结构;玉米、马铃薯间作促进了以羧酸类、多聚化合物、芳香类化合物、氨基酸类化合物为碳源的微生物类群代谢活性,改变了微生物群落的功能多样性。玉米、蚕豆与马铃薯的不同种间关系,导致马铃薯根际土壤微生物群落功能变化和结构变化不完全同步。间作降低了作物根际土壤AM真菌的总种属数,优势种发生改变,福摩萨球囊霉(G.formosanum)是间作系统中的共有优势种。间作栽培下,AM真菌多样性的变化与土壤根际微生物群落结构功能变化密切相关。
| [1] | 王震宇, 王英祥, 陈祖仁.重茬大豆生长发育障碍机制初探.大豆科学,1991,10(1): 31–36. |
| [2] | 马云华, 魏珉, 王秀峰.日光温室连作黄瓜根区微生物区系及酶活性的变化.应用生态学报,2004,15(6): 1005–1008. |
| [3] | 甄文超, 曹克强, 代丽, 张学英.连作草莓根系分泌物自毒作用的模拟研究.植物生态学报,2004,28(6): 828–832. |
| [4] | 张重义, 陈慧, 杨艳会, 陈婷, 林瑞余, 陈新建, 林文雄.连作对地黄根际土壤细菌群落多样性的影响.应用生态学报,2010,21(11): 2843–2848. |
| [5] | Zhou X G, Gao D M, Liu J, Qiao P L, Zhou Xi L, Lu H B, Wu X, Liu D, Jin X, Wu F Z. European Journal of Soil Biology,2014,60 1–8. |
| [6] | Li L, Yang S C, Li X L, Zhang F S, Christie P.Interspecific complementary and competitive interactions between intercropped maize and faba bean.Plant and Soil,1999,212(2): 105–114. |
| [7] | Tang X Y, Bernard L, Brauman A, Daufresne T, Deleporte P, Desclaux D, Souche G, Placella S A, Hinsinger P.Soil Biology and Biochemistry,2014,75 86–93. |
| [8] | Bedoussaca L, Justes E.A comparison of commonly used indices for evaluating species interactions and intercrop efficiency: Application to durum wheat-winter pea intercrops.Field Crops Research,2011,124(1): 25–36. |
| [9] | Xia H Y, Wang Z G, Zhao J H, Sun J H, Bao X G, Christie P, Zhang F S, Li L.Field Crops Research,,154 53–64. |
| [10] | Inal A, Gunes A, Zhang F, Cakmak I.Peanut/maize intercropping induced changes in rhizosphere and nutrient concentrations in shoots.Plant Physiology and Biochemistry,2007,45(5): 350–356. |
| [11] | Fuhrman J A.Microbial community structure and its functional implications.Nature,2009,459(7244): 193–199. |
| [12] | 张玉凤, 冯固, 李晓林.丛枝菌根真菌对三叶草根系分泌的有机酸组分和含量的影响.生态学报,2003,23(1): 30–37. |
| [13] | Kapoor R, Kaur M, Mukerji K G.VAM and phosphorus induced changes in the rhizosphere ecology of Anethu graveolens L.Journal of Environmental Biology,2000,21(3): 185–191. |
| [14] | 宋亚娜, MarschnerP, 张福锁, 包兴国, 李隆.小麦/蚕豆, 玉米/蚕豆和小麦/玉米间作对根际细菌群落结构的影响.生态学报,2006,26(7): 2268–2274. |
| [15] | Niwa S, Kaneko N, Okada H, Sakamoto K.Effects of fine-scale simulation of deer browsing on soil micro- foodweb structure and N mineralization rate in a temperate forest.Soil Biology and Biochemistry,2008,40(3): 699–708. |
| [16] | 马琨, 张丽, 杜茜, 宋乃平.马铃薯连作栽培对土壤微生物群落的影响.水土保持学报,2010,21(4): 229–233. |
| [17] | Shenck N C, Perez Y. Manual for the Identification of VA Mycorrhizal Fungi. 3rd ed. Gainesville, F L: Synergistic Publications, 1990. |
| [18] | 张美庆, 王幼珊, 邢礼军.我国东、南沿海地区AM真菌群落生态分布研究.菌物系统,1998,17(3): 274–277. |
| [19] | He Y, Xu J M, Ma Z H, Wang H Z, Wu Y P.Profiling of PLFA: implications for nonlinear spatial gradient of PCP degradation in the vicinity of Lolium perenne L.Soil Biology and Biochemistry,2007,39(5): 1121–1129. |
| [20] | Wixon D L, Balser T C.Soil Biology and Biochemistry,2013,57 769–774. |
| [21] | Williams A, Birkhofer K, Hedlund K.Above- and below-ground interactions with agricultural management: Effects of soil microbial communities on barley and aphids.Pedobiologia,2014,57(2): 67–74. |
| [22] | Zhang N N, Sun Y M, Wang E T, Yang J S, Yuan H L, Scow K M.Applied Soil Ecology,2015,85 76–85. |
| [23] | Wang D W, Marschner P, Solaiman Z, Rengel Z.Belowground interactions between intercropped wheat and Brassicas in acidic and alkaline soils.Soil Biology and Biochemistry,2007,39(4): 961–971. |
| [24] | Wortman S E, Drijber R A, Francis C A, Lindquist J L.Applied Soil Ecology,2013,72 232–241. |
| [25] | Artursson V, Jansson J K.Use of bromode oxyuridine immunocapture to identify active bacteria associated with arbuscular mycorrhizal hyphae.Applied and Environmental Microbiology,2003,69(10): 6208–6215. |
| [26] | 毕明丽, 宇万太, 姜子绍, 马强, 张璐, 徐永刚.利用PLFA方法研究不同土地利用方式对潮棕壤微生物群落结构的影响.中国农业科学,2010,43(9): 1834–1842. |
| [27] | Li H G, Shen J B, Zhang F S, Marschner P, Cawthray G, Rengel Z.Phosphorus uptake and rhizosphere properties of intercropped and monocropped maize, faba bean, and white lupin in acidic soil.Biology and Fertility of Soils,2010,46(2): 79–91. |
| [28] | Lacombe S, Bradley R L, Hamel C, Beaulieu C.Do tree-based intercropping systems increase the diversity and stability of soil microbial communities? Agriculture, Ecosystems and Environment, 2009, 131(1/2): 25-31.Agriculture, Ecosystems and Environment,2009,131(1/2): 25–31. |
| [29] | Lupwayi N Z, Harker K N, O'Donovan J T, Turkington T K, Blackshaw R E, Hall L M, Willenborg C J, Gan Y T, Lafond G P, May W E, Grant C A.European Journal of Agronomy,2015,62 110–119. |
| [30] | Behie S W, Bidochka M J.Nutrient transfer in plant-fungal symbioses.Trends in Plant Science,2014,19(11): 734–740. |
| [31] | Alguacil M M, Torrecillas E, García-Orenes F, Roldán A.Soil Biology and Biochemistry,2014,76 34–44. |
| [32] | Dai M L, Hamel C, Bainard L D, Arnaud M S, Grant C A, Lupwayi N Z, Malhi S S, Lemke R.Soil Biology and Biochemistry,2014,74 156–166. |
| [33] | 石兆勇, 魏艳丽, 王发园.地球上最广泛的共生体-丛枝菌根.生物学通报,2007,42(8): 22–23. |
| [34] | Sykorová Z, Wiemken A, Redecker D.Co-occurring Gentiana verna and Gentiana acaulis and their neighboring plants in two Swiss upper montane meadows harbor distinct arbuscular mycorrhizal fungal communities.Applied Environmental Microbiology,2007,73(17): 5426–5434. |
 2015, Vol. 36
2015, Vol. 36




