文章信息
- 雷忻, 关鹏周, 贾向荣, 王文强, 延志莲, 田鹏飞
- LEI Xin, GUAN Pengzhou, JIA Xiangrong, WANG Wenqiang, YAN Zhilian, TIAN Pengfei
- 辛基酚胁迫对雄性泥鳅抗氧化酶及卵黄蛋白原的影响
- Incidence of antioxidant enzymes and vitellogenin induced in male loach (Misgurnus anguillicaudatus) exposed to octylphenol
- 生态学报, 2015, 35(8): 2502-2508
- Acta Ecologica Sinica, 2015, 35(8): 2502-2508
- http://dx.doi.org/10.5846/stxb201306091553
-
文章历史
- 收稿日期:2013-06-09
- 网络出版日期:2014-05-16
辛基酚 (octylphenol,OP) 作为一种重要的精细化工原料和中间体,被广泛用于表面活性剂、塑料制品、农药、食物制品等产品的生产中[1, 2]。它是烷基酚乙烯醚 (APEs) 类物质中雌激素活性较强的一种[3, 4],具有易富集、难降解等特点,其引发的毒性可以通过食物链传递和放大,除可对水生生物产生毒害作用外,还可危及陆生动物、鸟类和人类的健康,目前在水体中的污染浓度可达1000 ng/L,已成为当今水环境中重要的污染物[5, 6]。随着陕北能源化工基地建设的快速发展,辛基酚等酚类化合物污染有加剧之势,对当地水生生物及人体的毒害作用不容忽视。
超氧化物歧化酶(SOD)和过氧化氢酶(CAT)是动物体内重要的抗氧化酶(antioxidant enzyme),是机体防御过氧化损伤系统的关键酶,在清除超氧自由基、H2O2以及阻止羟基自由基形成等方面发挥重要作用。它们的活性变化在一定程度上可反映污染物对生物体的影响,是一类敏感的分子生态毒理学指标[7]。卵黄蛋白原 (VTG) 是卵生动物卵黄蛋白的前体,在雌性动物体内受内源性雌激素的调节可在肝细胞中合成,而雄性个体在外源雌激素或类雌激素化合物的诱导下肝细胞也可合成,因此雄性体内VTG的异常变化可作为生物标志物来检测环境污染物的雌激素效应[8]。由于活性氧的含量与雄性个体生精细胞的损伤密切相关[9, 10],因此由环境雌激素引起的氧化损伤可能会导致雄性个体的生殖异常。目前,酚类化合物对鱼类和哺乳动物的抗氧化酶活性影响已有一些研究[11, 12, 13],但OP对鱼类的氧化损伤作用、环境雌激素效应以及两者相互关系的研究鲜有报道。
泥鳅(Misgurnus anguillicaudatus)系一种小型淡水鱼,适应于淤泥、水体 2 种栖息环境,食性广,易驯养,是一种良好的水环境污染监测动物[14]。本研究以泥鳅为试验动物,检测OP胁迫对其急性毒性效应、抗氧化酶活性及卵黄蛋白原的影响,研究OP对鱼类的氧化损伤及环境雌激素效应,旨在为深入探讨酚类化合物对鱼类的毒性效应机制提供资料,同时为当地水环境污染的检测和治理提供科学依据。
1 材料与方法 1.1 材料与药品泥鳅购于陕西延安市农贸市场。在室温下,用经过3 d自然脱氯自来水驯养2周后,挑选健康、强壮的雄性泥鳅进行实验。受试泥鳅平均体质量 (12.3±2.5) g,平均长度为(11.0±2.0) cm。辛基酚,分析纯,成都格雷西亚化学技术有限公司生产。SOD 试剂盒、CAT 试剂盒,购自南京建成生物工程研究所。
1.2 毒性试验 1.2.1 急性毒性试验在正式试验前先进行 2 次预试验,确定OP 最大耐受质量浓度 (1.06 mg/L) 和最小全致死质量浓度 (3.32 mg/L)。按等对数间距,将OP 设置 5 个质量浓度处理组 (1.28、1.55、1.87、2.27、2.75 mg/L),同时设空白对照组(加蒸馏水),每个处理设3 个平行,每组20尾雄性泥鳅。试验开始后,连续 8 h 观察泥鳅的活动、中毒情况及体色变化;每 24 h 统计1 次死亡数,更换1 次受试药液,以保证药液溶氧量、pH值、水温及其他理化指标的稳定[15];计算死亡率。试验共进行96 h。试验期间的管理与驯养期间完全相同,水温18—20 ℃,pH值 6.5—7.0,溶解氧7.5—8.0 mg/L,试验容器为40 L塑料缸,每缸盛 20 L OP处理液。
1.2.2 亚急性毒性试验根据急性毒性试验所得结果,在安全浓度(SC)以下按照等对数法将OP 设置4个质量浓度处理组(0.12、0.19、0.32、0.52 mg/L),同时设置空白对照组(加蒸馏水),每个处理设3 个平行组,每组放入20 尾雄性泥鳅。每48 h 更换1 次受试药液,隔天喂食少许小米和玉米碎粒,取样前1 d 停止喂食[15]。试验期间的管理与急性毒性试验相同。
1.3 抗氧化酶液制备与测定分别于OP暴露7、14、21、28 d时采样,每组随机取5 尾泥鳅,解剖后分别取出肝脏,加4 ℃预冷的生理盐水,冰浴条件下进行匀浆,以10000 r/min、4 ℃离心10 min,取上清液,即为组织酶提取液。
SOD 活性采用SOD 试剂盒测定。以37 ℃条件下,每毫克组织蛋白在1 mL 反应液中SOD 抑制率为50% 时对应的SOD 量为1 个酶活性单位(U/ mg)。
CAT 活性采用CAT 试剂盒测定。以37 ℃条件下,每毫克组织蛋白每秒钟分解1 μmol/L H2O2 定义为1 个酶活性单位(U/ mg)。
1.4 VTG 样品的制备与测定 1.4.1 样品制备分别在OP 中暴露7、14、21、28 d 时处死泥鳅,断尾取血,所得血样在4 ℃下静置4—6 h,10000 r/min离心15 min,取上清,冷冻保存,待测[16, 17]。采血结束后,将泥鳅解剖,根据性腺(雄性:白色精巢,雌性:黄色卵巢)进一步鉴定其性别。
1.4.2 VTG 含量测定采用碱不稳定性蛋白结合磷法测定血清中 VTG 的含量。将样品分加入到含有10% 的三氯乙酸溶液的离心管中,0 ℃过夜,离心去上清;加入5% 三氯乙酸溶液,90 ℃下孵育30 min;离心去上清;分别用无水乙醇、氯仿 ∶ 乙醚 ∶ 无水乙醇 (体积分数1 ∶ 1 ∶ 2) 、丙酮和乙醚按顺序清洗沉淀,弃去上清;加入NaOH,100 ℃水解3 h,待测[17]。将样品转入比色管中,盐酸中和,加显色液(配方:3 mol/L H2SO4∶蒸馏水 ∶ 25 g/L 钼酸铵 ∶ 100 g/L 抗坏血酸=1 ∶ 2 ∶ 1 ∶ 1),37 ℃孵育1.5—2 h;用分光光度计测定780 nm波长处的吸光值,根据吸光值算出磷含量,即可反映VTG 的含量。标准液为无水磷酸二氢钾。
1.5 数据处理运用SPSS 18.0 软件对OP 的质量浓度对数值与泥鳅死亡几率的关系进行回归分析,得到回归方程 y = ax+b。由 Bliss 统计方法计算出 24、48、72 和 96 h 的半致死浓度 (LC50) 和 95% 置信区间 (95% credibility range),由 LC50 可以计算出安全浓度(SC)[18],SC=48 h LC50 ×0.3 / (24 h LC50 /48 h LC50)2。
所有数据均采用SPSS 18.0 统计软件进行单因素方差分析 (One-way ANOVA),用最小显著差数法 (LSD) 进行多重比较,结果表示为平均值±标准差。显著性差异以 P <0.05 表示差异显著; P <0.01 表示差异极显著。
2 结果与分析 2.1 辛基酚对泥鳅的急性毒性效应从症状来看,在试验的最初 6 h 内,OP 较低质量浓度 (1.28、1.55 mg/L) 处理,泥鳅没有明显的中毒症状。而较高质量浓度 (2.27、2.75 mg/L) 处理 2 h 后泥鳅就开始出现中毒症状,游动急速,四处乱窜;6 h 游泳失衡,出现抽搐,不时跃出水面,碰撞桶壁,逐渐侧翻在水中;8 h 开始出现死亡,体表黏液显著增多。
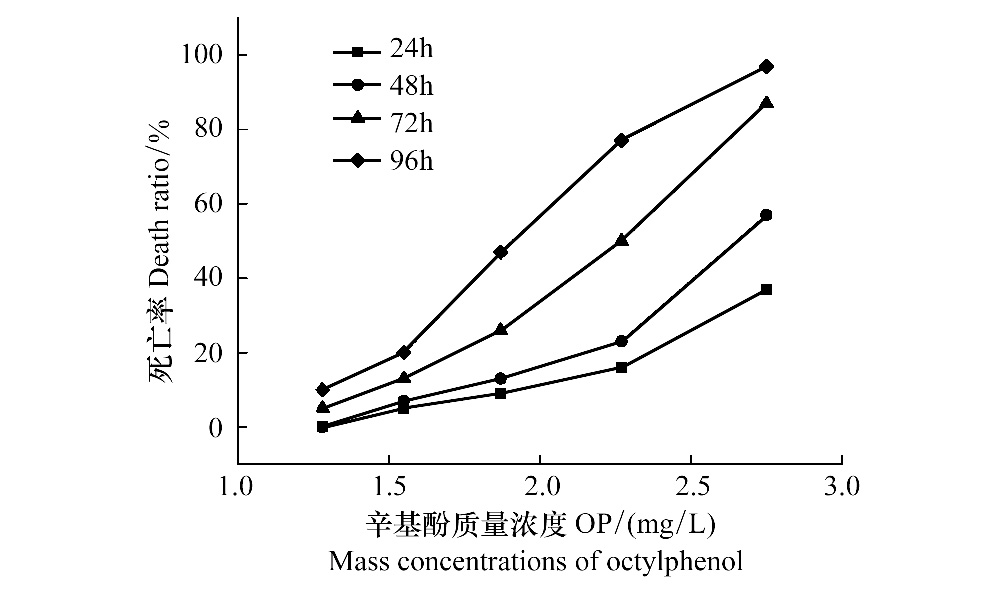
泥鳅暴露在5 个质量浓度OP 中的死亡率变化见图 1。由图 1可见,随着OP 质量浓度的增大,泥鳅死亡率逐渐升高,基本呈正相关趋势。将死亡率转化为死亡几率单位,将OP 质量浓度转化为浓度常用对数,进行回归分析,得到的回归方程见表 1。由表 1可知泥鳅在 24、48、72、96 h 的LC50 和SC 值,并且随着OP 染毒时间的延长,LC50 逐渐减小。
|
| 图 1 泥鳅死亡率与辛基酚质量浓度的关系 Fig. 1 Correlation between the death ratio of Misgurnus anguillicaudatus and octylphenol(OP)concentration |
| 暴露时间/h Time | 回归方程 Regression equation | 相关系数 Correlation coefficient | 半致死浓度/(mg/L) Median lethal concentration (LC50) | 95%置信区间/(mg/L) 95% credibility range | 安全浓度/(mg/L) Safe concentration (SC) |
| 回归方程中,x为OP质量浓度的常用对数值,y为泥鳅死亡几率;**表示差异极显著,P <0.01; 同列数据后不同字母表示不同处理半致死浓度之间差异显著,P <0.05 | |||||
| 24 | y=5.43x+2.20 | 0.95** | 3.26a | 1.90 — 12.07 | |
| 48 | y = 6.98x+1.98 | 0.97** | 2.69b | 1.84 — 5.50 | 0.54 |
| 72 | y=7.75x+2.46 | 0.95** | 2.12c | 1.41 — 5.71 | |
| 96 | y=9.51x+2.48 | 0.98** | 1.82d | 1.37 — 3.15 | |
由表 2 可见,与对照组相比,泥鳅在0.12 mg/L OP 中暴露7、14 d,肝脏 SOD 活性均无显著变化,暴露21 d 时活性才显著降低;而在0.32 mg/L 和 0.52 mg/L OP 中暴露 7 d 时,SOD 活性即有极其显著下降;在0.19 mg/L OP 中暴露14 d 时,SOD 活性有极其显著下降。同一暴露时间,在4 个质量浓度OP 处理组中,最低质量浓度OP (0.12 mg/L) 处理组泥鳅肝脏SOD 活性最高,随着OP 质量浓度的增大,活性逐渐降低,当OP 质量浓度为0.52 mg/L时,SOD 活性最低。
| 暴露时间/ d Time | 对照Control 0.00 mg/L | 超氧化物歧化酶活性/(U/mg) Superoxide dismutase(SOD) activities | |||
| 0.12 mg/L | 0.19 mg/L | 0.32 mg/L | 0.52 mg/L | ||
| *表示OP处理组与对照组之间差异显著 (P <0.05);** 表示处理组与对照组之间差异极显著 (P <0.01); 同列数据后标相同字母者表示差异不显著 (P >0.05);标不同字母表示差异显著 (P <0.05) | |||||
| 7 | 35.95±0.08 | 35.38±0.52 a | 34.55±0.39 a | 31.98±0.88a** | 22.13±0.94a** |
| 14 | 36.34±0.21 | 34.97±0.42 a | 33.36±0.21a** | 29.07±0.74b** | 8.29±0.87b** |
| 21 | 36.78±0.24 | 34.47±0.14a** | 32.15±0.19b** | 25.08±0.82c** | 14.42±0.91c** |
| 28 | 36.90±0.19 | 33.05±0.41b** | 28.54±0.85c** | 21.37±0.73d** | 11.15±0.91d** |
由表 2 还可知,泥鳅在同一质量浓度OP 中暴露不同的时间,SOD 活性差异显著,并随着暴露时间的延长,SOD 活性均显著降低。4 个质量浓度OP 处理组泥鳅肝脏SOD 活性均在28 d 时最低。
2.3 OP 对泥鳅肝脏过氧化氢酶活性的影响由表 3 可见,与对照组相比,泥鳅在0.12 mg/L OP 中暴露7、14 d,肝脏 CAT 活性均无显著变化,暴露21 d 时活性有极显著下降;而在0.19、0.32、0.52 mg/L OP 中暴露 7 d CAT 活性即有极其显著下降。同一暴露时间,在4 个质量浓度OP 处理组中,最低质量浓度OP(0.12 mg/L)处理组泥鳅肝脏CAT 活性最高,随着OP 质量浓度的增大,活性逐渐降低,当OP 质量浓度为0.52 mg/L 时,CAT 活性最低。
| 暴露时间/ d Time | 对照Control 0.00 mg/L | 过氧化氢酶活性Catalase(CAT) activities/(U/mg) | |||
| 0.12 mg/L | 0.19 mg/L | 0.32 mg/L | 0.52 mg/L | ||
| 7 | 26.01±0.17 | 25.35±0.46a | 24.52±0.35a* | 21.86±0.68a** | 12.43±0.42a** |
| 14 | 25.74±0.54 | 24.93±0.48 ab | 23.24±0.18ab** | 18.89±0.43b** | 11.29±0.25ab** |
| 21 | 26.75±0.20 | 23.68±0.50bc** | 22.06±0.34b** | 15.17±0.88c** | 10.51±0.11bc** |
| 28 | 25.87±0.92 | 22.35±0.16c** | 18.48±0.84c** | 12.04±0.63d** | 9.15±0.09c** |
由表 3 还可知,泥鳅在同一质量浓度OP 中暴露不同的时间,CAT 活性差异显著,并随着暴露时间的延长,活性均呈显著降低趋势。4 个质量浓度OP 处理组泥鳅肝脏CAT 活性均在28 d 时最低。
2.4 OP 对泥鳅血清卵黄蛋白原的影响由表 4 可见,与对照组比较,泥鳅在低质量浓度OP (0.12 mg/L) 中暴露7 d 时,血清VTG水平即有极其显著升高,并且随着暴露质量浓度的增加,VTG 水平逐渐升高;在高质量浓度 (0.52 mg/L) 中暴露7 d 时,血清VTG 水平就达到较高值。在4 个质量浓度OP 处理组中,泥鳅血清VTG 水平随着暴露时间的延长 (7、14、21、28 d) 均呈逐渐上升趋势,在0.52 mg/L OP 中暴露28 d 时,VTG 水平最高。
| 暴露时间/d Time | 对照Control 0. 00 mg/L | 卵黄蛋白原水平Vitellogenin(VTG)levels/(mg/L) | |||
| 0.12 mg/L | 0.19 mg/L | 0.32 mg/L | 0.52 mg/L | ||
| 7 | 0.19±0.01 | 11.20±0.08a** | 12.06±0.04a** | 16.34±0.02a** | 18.06±0.05a** |
| 14 | 0.22±0.01 | 13.77±0.07b** | 14.63±0.03b** | 20.62±0.01b** | 22.33±0.03b** |
| 21 | 0.23±0.02 | 21.48±0.03c** | 20.62±0.02c** | 25.76±0.07c** | 27.47±0.06c** |
| 28 | 0.27±0.02 | 23.19±0.01d** | 24.91±0.03d** | 29.18±0.02d** | 28.94±0.09d** |
一般以污染物胁迫鱼类 96 h 的 LC50 值作为环境污染物毒性评价的依据,可将其急性毒性分为5 个等级: <1 mg/L 为剧毒,1 mg/L≤ LC50 <100 mg/L 为高毒,100 mg/L≤ LC50 <1000 mg/L 为中等毒性,1000 mg/L≤ LC50 <10000 mg/L 为低毒,≥10000 mg/L 为微毒[19]。根据本试验结果,OP 96 h LC50 为 1.82 mg/L,属于高毒等级的酚类污染物,其对水生生物的毒害作用非常严重,应引起高度重视。本研究的急性毒性试验结果表明,在相同时间内,泥鳅的死亡率随 OP 质量浓度的增大呈上升趋势,说明在一定剂量范围内,OP 对泥鳅存在明显的急性毒性效应。
抗氧化酶系统是机体维持氧自由基代谢平衡、免受氧化损伤的重要保护系统,其中SOD和CAT 在参与活性氧 (ROS) 的清除和机体保护性防御中起着主要作用[20]。当机体受到环境因子胁迫时,抗氧化酶活性会发生异常,导致机体的氧化损伤。毛阿敏等[21]检测了氯氰菊酯胁迫对克氏原螯虾(Procambarus clarkii) 肝胰腺SOD 和CAT 活性的影响,发现氯氰菊酯对2 种酶活性都具有显著的抑制作用。石洪玥等[11]研究了苯酚对红鳍东方鲀(Takifugu rubripes) 幼鱼肝脏抗氧化酶的影响,认为胁迫16 d 时,SOD 活性被显著抑制。李晖[13]的研究表明由于OP 胁迫对大鼠肝脏SOD 活性有显著抑制作用,导致其肝脏的氧化损伤。本研究结果显示,在OP 亚急性染毒过程中,低剂量 (0.12 mg/L) 胁迫14 d,泥鳅肝脏SOD 和CAT 的活性均无显著变化,但随着OP 胁迫剂量增大和胁迫时间延长,2 种酶的活性均呈现显著降低的趋势,表明在一定时间内,泥鳅受到OP 轻度胁迫时,肝脏2 种抗氧化酶仍能维持正常生理功能,而当受到OP 中、重度胁迫时,2 种抗氧化酶活性被明显的抑制,并随着胁迫剂量增大和时间延长,抑制作用加剧。提示OP 胁迫时会使泥鳅肝脏抗氧化酶系统的防御功能降低,机体内积累过量的ROS,从而导致氧化损伤的发生。
3.2 OP 对泥鳅的雌激素效应VTG 含量与性类固醇激素之间存在着密切关系[22]。由于雄性泥鳅自身内源性雌激素水平极低,血清VTG 水平极其微量,甚至难以检测,因此雄性泥鳅血清VTG 水平的变化能够直接反映外源性雌激素物质的干扰作用。詹翠琼等[23]对暴露在多氯联苯 (Polychlorinated biphenyls,PCBs) 中的雄性孔雀鱼(Poecilia reticulata) VTG 进行检测,发现PCBs 可诱导产生VTG。王宏元等[24]通过对雄性中国林蛙(Rana Chensinensis) 肝细胞雌激素受体和VTG 的检测,认为壬基酚对VTG 有明显的诱导作用。本研究中,暴露在OP 中的雄性泥鳅血清VTG 水平升高极其显著,说明OP 在肝脏合成VTG 过程中具有诱导作用,提示其对雄性泥鳅具有一定的雌激素效应。
赵岩等[25]研究双酚A 对雄性泥鳅血清VTG 的诱导作用时,发现VTG 含量随双酚A 胁迫时间和胁迫剂量的增加而显著升高。本研究对OP 胁迫雄性泥鳅的血清VTG 水平检测结果显示,随着OP 胁迫剂量的增加,VTG 水平呈上升趋势;在同一剂量下,VTG 水平随胁迫时间的延长逐渐升高。说明OP 对雄性泥鳅的血清VTG 的诱导作用与胁迫剂量和时间有密切关系,诱导作用随着剂量增大和时间延长而逐渐增强,提示OP 的雌激素效应也会随剂量和时间的增加而增强,这可能会对雄性泥鳅生殖系统产生影响。
马爱团等[26]研究了己烯雌酚对雄性金色中仓鼠(Mesocricetus auratus) 的生殖毒性与氧化损伤的关系,提出氧化损伤可能是环境雌激素生殖毒性的作用机理之一。本研究中,OP 对抗氧化酶活性的抑制作用会造成泥鳅体内ROS 的积累,而生精细胞对ROS 的敏感性比体细胞更强,少量ROS 就能干扰生精细胞的功能[9],因此氧化损伤会导致雄性泥鳅生殖功能受损,这与上述OP 对雄性泥鳅血清VTG 的诱导规律是相符合的,说明OP 对雄性泥鳅的雌激素效应可能与其氧化损伤有着密切关系。
| [1] | Routledge E J, Sumpter J P. Structural features of alkylphenolic chemicals associated with estrogen activity. The Journal of Biological Chemistry, 1997, 272(6): 3280-3288. |
| [2] | Rey Vázquez G, Meijide F J, Da Cuña R H, Lo Nostro F L, Piazza Y G, Babay P A, Trudeau V L, Maggese M C, Guerrero G A. Exposure to waterborne 4-tert-octylphenol induces vitellogenin synthesis and disrupts testis morphology in the South American freshwater fish Cichlasoma dimerus (Teleostei, Percifomes). Comparative Biochemistry and Physiology Part C: Toxicology and Pharmacology, 2009, 150 (2): 298-306. |
| [3] | White R, Jobling S, Hoare S A, Sumpter J P, Parker M G. Environmentally persistent alkylphenolic compounds are estrogenic. Endocrinology, 1994, 135(1): 175-182. |
| [4] | Jobling S, Sumpter J P, Sheahan D, Osborne J A, Matthiessen P. Inhibition of testicular growth in rainbow trout (Oncorhynchus mykiss) exposed to estrogenic alkylphenolic chemicals. Environmental Toxicology and Chemistry, 1996, 15(2): 194-202. |
| [5] | Rudel R. Predicting health effects of exposures to compounds with estrogenic activity: methodological issues. Environmental Health Perspectives, 1997, 105(S3): 655-663. |
| [6] | 杜克久, 徐晓白. 环境雌激素研究进展. 科学通报, 2000, 45(21): 2241-2251. |
| [7] | 陈琳琳, 张高生, 陈静, 任宗明. 汞、硒暴露对紫贻贝 (Mytilus edulis) 抗氧化酶系统的影响. 生态毒理学报, 2011, 6(4): 383-388. |
| [8] | Chikae M, Ikeda R, Hasan Q, Morita Y, Tamiya E. Effect of alkylphenols on adult male medaka: plasma vitellogenin goes up to the level of estrous female. Environmental Toxicology and Pharmacology, 2003, 15(1): 33-36. |
| [9] | Aitken R J, Baker M A. Reactive oxygen species generation by human spermatozoa: a continuing enigma. International Journal of Andrology, 2002, 25(4): 191-194. |
| [10] | Mishra D P, Shaha C. Estrogen-induced spermatogenic cell apoptosis occurs via the mitochondrial pathway: role of superoxide and nitric oxide. Journal of Biological Chemistry, 2005, 280(7): 6181- 6196. |
| [11] | 石洪玥, 姜志强, 高小强, 宫雪, 吴洪, 李艳秋. 苯酚对红鳍东方鲀幼鱼的急性毒性及对肝脏抗氧化酶的影响. 吉林农业大学学报, 2012, 34(6): 682-687, 704-704. |
| [12] | 李健, 司丽芳, 位志国, 薛帮群, 李翔, 位兰, 李梦云, 陈树林. 辛基酚对成年雄性小鼠血浆和脾脏抗氧化功能的影响. 动物医学进展, 2012, 33(3): 29-32. |
| [13] | 李晖. 辛基酚、壬基酚对雌性大鼠的毒性作用及葛根黄酮干预作用的研究 [D]. 乌鲁木齐: 新疆医科大学, 2008. |
| [14] | 成庆泰, 郑葆珊. 中国鱼类系统检索. 北京: 科学出版社, 1987. |
| [15] | 沈洪艳, 宋存义, 甄芳芳, 任洪强. 对氯硝基苯对锦鲤鱼的急性毒性效应. 河北师范大学学报: 自然科学版, 2007, 31(4): 514-516. |
| [16] | Shi G Q, Shao J, Jiang G B, Wang Q X, Lu Y Q, Liu J F, Liu J M. Membrane chromatography method for the rapid purification of vitellogenin from fish plasma. Journal of Chromatography B, 2003, 785(2): 361-368. |
| [17] | 张艳珍, 陈细华, 危起伟, 邱实, 刘志刚. 中华鲟血清卵黄蛋白原水平的初步观察. 淡水渔业, 2008, 38(5): 10-14. |
| [18] | 张克杰, 张维平. 环境污染生物监测与评价. 北京: 中国环境科学出版社, 1991. |
| [19] | 孔志明. 环境毒理学 (第三版). 南京: 南京大学出版社, 2006. |
| [20] | Palacea V P, Brown S B, Baron C L, Fitzsimons J, Woodin B, Stegeman J J, Klaverkamp J F. An evaluation of the relationships among oxidative stress, antioxidant vitamins and early mortality syndrome (EMS) of lake trout (Salvelinus namaycush) from Lake Ontario. Aquatic Toxicology, 1998, 43(2/3): 195-208. |
| [21] | 毛阿敏, 魏克强, 赵辉, 刘婉莎, 刘娥娥, 吕虹瑞. 高效氯氰菊酯对克氏原螯虾 (Procambarus clarkii) 抗氧化酶活性的影响. 农业环境科学学报, 2013, 32(4): 689-696. |
| [22] | Reis-Henriques M A, Cruz M M, Pereira J O. The modulating effect of vitellogenin on the synthesis of 17β-estradiol by rainbow trout (Oncorhynchus mykiss) ovary. Fish Physiology and Biochemistry, 1997, 16(3): 181-186. |
| [23] | 詹翠琼, 黄絮洁, 方展强, 马广智, 姚静. 多氯联苯对孔雀鱼卵黄蛋白原的诱导及检测. 生态毒理学报, 2007, 2(3): 333-338. |
| [24] | 王宏元, 巨荣菊, 白瑶, 张育辉. 壬基酚对雄性中国林蛙肝细胞中雌激素受体和卵黄蛋白原的影响. 陕西师范大学学报: 自然科学版, 2011, 39(6): 54-59. |
| [25] | 赵岩, 时国庆, 孙春宝, 佟明阳. 双酚A对泥鳅卵黄蛋白原的诱导. 科学技术与工程, 2007, 7(9): 2156-2159. |
| [26] | 马爱团, 陈耀星, 王子旭. 己烯雌酚对成年雄性金色中仓鼠的生殖毒性与氧化损伤的关系. 动物学报, 2007, 53(6): 1076-1082. |
 2015, Vol. 35
2015, Vol. 35




