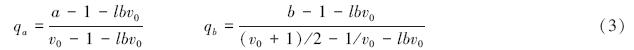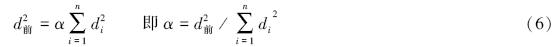文章信息
- 赵艳云, 陆兆华, 夏江宝, 刘京涛
- ZHAO Yanyun, LU Zhaohua, XIA Jiangbao, LIU Jingtao
- 黄河三角洲贝壳堤岛3种优势灌木的根系构型
- Root architecture and adaptive strategy of 3 shrubs in Shell Bay in Yellow River Delta
- 生态学报, 2015, 35(6): 1688-1695
- Acta Ecologica Sinica, 2015, 35(6): 1688-1695
- http://dx.doi.org/10.5846/stxb201307281967
-
文章历史
- 收稿日期:2013-07-28
- 修订日期:2014-07-18
2. 山东省黄河三角洲生态环境重点实验室, 滨州 256603;
3. 滨州学院, 滨州 256603
2. Shandong Provincial Key Laboratory of Eco-Environmental Science for Yellow River Delta, Binzhou 256603, China;
3. Binzhou University, Binzhou 256603, China
陆地生态系统中,5%—95%的净初级生产力是深埋于地下的根系统[1, 2]。根系在植物体固定、水分和营养物质的吸收上发挥了重要作用[3],具有保持水土、固定边坡以及稳定土壤和防止土壤侵蚀的巨大功能[4, 5]。其中,直径>3mm的粗根是根系的重要组成部分,其分支策略、大小(直径)表明了根系贮养、觅养以及各生境下的固定能力[5, 6, 7]。Fitter从20世纪80年代开始,利用几何学中的拓扑结构来分析粗根的分支和连接特征,开拓了植物粗根研究的新纪元[8]。随后,Oppelt等[3]又对该拓扑结构模型进行了指数纠正,模拟结果更接近于现实,这些都对树木根系的觅养行为和生境适应策略的研究提供了良好借鉴。
海岸生态系统具有风暴潮和盐雾时常发生、土壤基质移动、沙埋、地下咸水位较浅等环境条件,加之人类活动的压力扩张、对自然资源的掠夺和原生生境条件改变等,从而决定了在相对较小的区域,植物群落和物种多样性的变异性[9],生态环境极其脆弱[9, 10],保护天然植被,维护生态系统的稳定性是防止海岸侵蚀的重要途径。对适生植物生境适应对策的透彻了解可以为脆弱受损生态系统的植被恢复工作提供强有力的借鉴[11]。而根系是反映植物适应生境能力的重要器官,了解根系的空间分布特征,不仅是探讨植物根-土互作的重要方面,同时,又是探索植物地下-地上部分权衡生境适应对策的主要方向[3, 12]。
黄河三角洲贝壳堤岛是海岸带受全球气候变化影响首当其冲的珍贵生态系统类型之一,特殊的地理位置和土壤基质组成成分使该岛的生境条件极为恶劣,植被稀疏且对环境变化较为敏感[13, 14]。随着人类活动(渔业捕捞、水产养殖、盐化工、土地围垦、石油开采、水利工程建设、贝沙挖掘制瓷以及珍贵药用植物的采集等)的加剧,贝壳堤原有生境遭到了严重的物理化学破坏,海陆间物质能量的流动过程在悄悄的发生改变,势必也影响着植物的生境适应对策[15]。了解该地区植物根系的构型特征,明确不同植物的适应规律和生态学机制,是探讨该地区植物根系-土壤互作的重要途径,也是维护贝壳堤生态系统平衡和防止海岸侵蚀,保护和恢复稳定植被群落的重要环节[4]。基于此,本研究以该地区天然优势灌木柽柳(Tamarix chinensis Lonr.)、酸枣(Ziziphus jujube Mill.)和杠柳(Periploca sepium Bunge.)为研究对象,比较了它们根系拓扑结构的异同点,探讨了根系在贝沙生境下的适应策略,可以为该地区植被保护和恢复提供基础资料。
1 方法和材料 1.1 自然概况研究区域位于山东省无棣贝壳堤与湿地国家自然保护区。该区处于暖温带东亚季风大陆性半湿润气候区,气候温和,四季分明,干湿明显,滩涂、沼泽的大面积分布是该地区海岸湿地生态系统的重要特色。土壤基质为贝沙淤泥质,土壤粒径较粗,兼有淤泥存在,容重在1.2g/cm3左右,孔隙较大,持水持肥能力较弱,白天升温较快,夜间降温迅速,日温差大,主要以多种繁殖方式的多年生草本植物为主,柽柳、酸枣、杠柳等小灌木群落生长良好,由于灌木群落在改善微气候的重要作用,其树下草本群落的生物多样性较大。柽柳主要分布在向海一侧,土壤粒径最粗,地下水位最浅,土壤中含盐量最高,在1.0%左右,酸枣和杠柳群落主要分布在滩脊和向陆一侧,海拔0.7—3m,土壤含盐量低,小于0.5%。
1.2 样品采集于2013年4月下旬—5月上旬,在山东省滨州市无棣县贝壳堤与湿地国家自然保护区植物分布相对较为集中的区域,选择长势良好的柽柳6株、杠柳16株,酸枣各15株,测定其基径、冠幅(为减少实验差误差,植株年龄均为3—5年生)。然后,参照杨小林等[12]的实验方法,利用铁锨、软毛刷等工具小心挖掘出所有直径大d≥ 3mm的根系。带回实验室,用自来水洗净根系上附着的泥沙,尽量保持根系在空间中的自然位置,然后绘制其粗根分支特征,并根据Opplet[3]修正指数进行计算。
1.3 根系参数的测定带回的根系洗净晾干后,立即用0.01mm精度的电子游标卡尺测定各级根系分支前后的直径,用直尺测定不同根端的连接长度,并记录根系内部、外部连接数量。用米尺测各根系的横向根直径与纵向根深。
1.4 理论分析方法 1.4.1 拓扑指数的计算参照杨小林等[12]的计算方法,分别计算相应的参数。例如根系的所有外部连接总数(Mag,简写为M)与最长根系通道内部连接总数(Alt,简写A)相关,符合公式:
因而,通过换算可以利用拓扑指数TI来进行衡量。公式如下:
研究证明,拓扑指数TI越趋于1,根系越接近于鱼尾型分支,当TI越接近于0.5时,根系则为叉状分支[16]。
但是,由于在实际研究中发现,Fitter拓扑模型在很大程度上依赖于M。据此,Oppelt通过实验研究基础上通过新的修正指数来描述根系的过渡模型,其公式表示为:
式中,qa表示最长根系通道内部连接总数进行的线性转换得到的修正值,a表示最长根系通道内部连接总数,qb 表示根系平均拓扑长度的修正拓扑指数,b表示平均拓扑长度,lbv0=lnv0/ln2,v0表示根系所有外部连接的总数,当qa=qb=1时为鱼尾型分支,当qa=qb=0时为叉状分支。
1.4.2 通道模型的计算通道模型指的是植物组织(根系、枝条等)直径在分支前后的相关性。不同学者对管道模型进行了大量验证,其中的一个方程是:
式中,Δ叫做指数参数[17]。Murray[18]观察发现大多数的树木地上枝条分支符合比例d2.5,其中d是最近枝条的直径,通过将各个分支节点的直径进行拟合,Δ恒定为2.5,是个常数。但是他的计算过于简单,仅仅在分支前的枝条部分全部忽略时,才适用该方程。因而后来Mandelbrot[19]表明植物组织的管道模型的值为2,符合Leonardo da Vinci法则,也即认为根系的分支前后的横截面积是相等的,即分支前的横截面积等于分支后的横截面积之和,可以通过下列方程表示:
而随后根据方程(5)van Noordwijk等[20]提出了更加一般性的方程即:
式中,α表示根系分支前与分支后的横截面积比,d前表示根系分支前的直径,di表示分支后的几个分支直径。
本文以Opplet[3]修正指数来研究贝壳堤地区3种优势灌木根系的拓扑结构和连接长度,并验证了根系管道模型的方程6。
2 结果与分析 2.1 根系特征 2.1.1 根系空间分布特征在黄河三角洲贝壳堤岛,酸枣根系粗根的水平分布直径平均为4.38 m,是冠幅直径的8—10倍。垂直剖面上,尽管酸枣一般位于贝壳滩脊上,地下水位较深(1.5—2.5 m),但是酸枣根系的分布深度一般在15.3—25 cm土层,平均根幅/根深比率为28.81。杠柳具有最广阔的地表根系,根幅直径平均为7.1m,冠幅直径大约1.5—2 m,是冠幅直径的15—20倍。柽柳的水平根幅最小,直径为1.18 m,相比其他两种灌木,地下粗根的深度与根水平直径的比例增加(表 1)。
| 小写字母差异代表了显著水平P<0.05的差异 | |||
| 物种 Species | 根深 Coarse root depth/cm | 根系水平直径 Horizontal diameter/cm | 根幅/根深 Root width/length |
| 杠柳Periploca sepium(PS) | 40±7.8a | 710.17±112.46a | 18.24±4.37a |
| 酸枣Ziziphus jujube(ZJ) | 15.3±3.76c | 438.11±113.46b | 28.81±5.19a |
| 柽柳Tamarix chinensis(TC) | 22.87±10.37b | 118.23±15.88c | 5.18±0.64b |
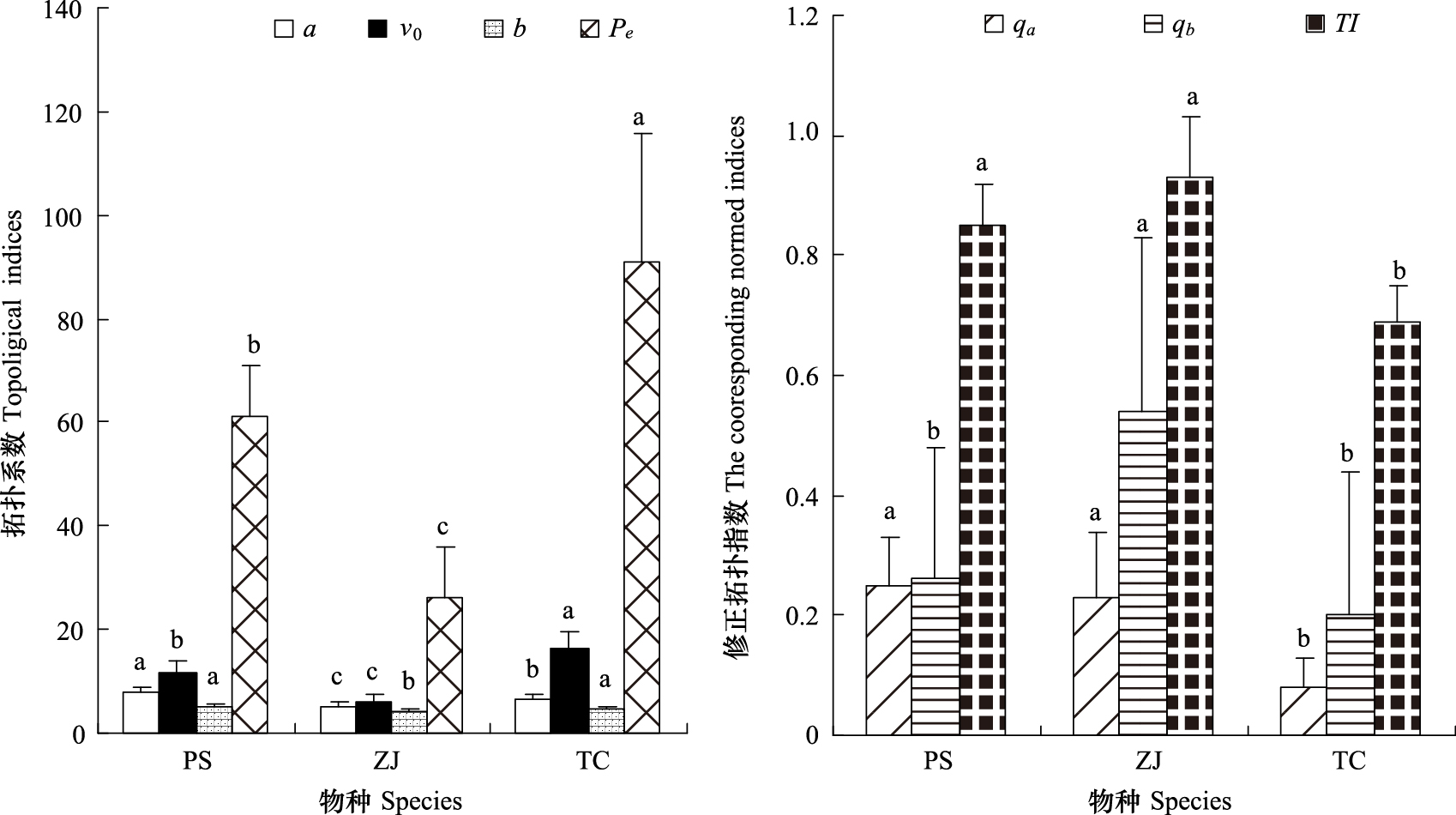
3种灌木中,酸枣的最长通道连接总数、根系所有外部连接总数、平均拓扑长度以及所有连接总数(Pe)最少。通过对a和b进行线性转换以及拓扑指数计算,可以看出,酸枣的qa和qb最大,柽柳的最小,且差异达显著水平(P<0.05)。而对于拓扑指数而言,酸枣的最大(TI=0.93),其次为杠柳和柽柳(TI=0.85和0.69,图 1)。
|
| 图 1 不同植物根系拓扑指数 Fig. 1 The topological indices of different shrubs PS: 杠柳Periploca sepium; ZJ: 酸枣Ziziphus jujube; TC: 柽柳Tamarix chinensis; 图例中的a,V0,b,Pe,qa,qb和TI分别代表最长通道连接总数,根系所有外部连接总数,平均拓扑长度,所有连接总数,最长根系通道内部连接总数的线性转换修正值,根系平均拓扑长度的修正拓扑指数和拓扑指数 |
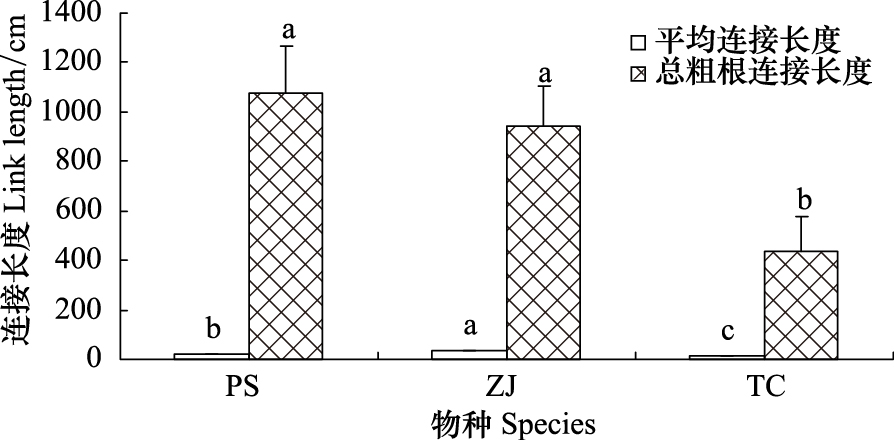
对于总粗根连接长度来说,杠柳的最大,为10.77m,柽柳的最小,为4.39m。但平均连接长度以酸枣的最大(33.51cm),杠柳的次之,为18.24cm,而柽柳的平均连接长度仅有12.93cm,且3种灌木的平均连接长度差异显著(图 2,P<0.05)。
|
| 图 2 根系连接长度 Fig. 2 Root link length |
3 种灌木粗根的延伸策略存在差异,随着连接通道次序的增加,杠柳和酸枣粗根的连接长度增加(斜率分别为18.184和32.656,P<0.001),而柽柳的连接长度,随着连接通道次序的增加呈现先增加后趋于平稳的趋势,符合指数方程(图 3)。
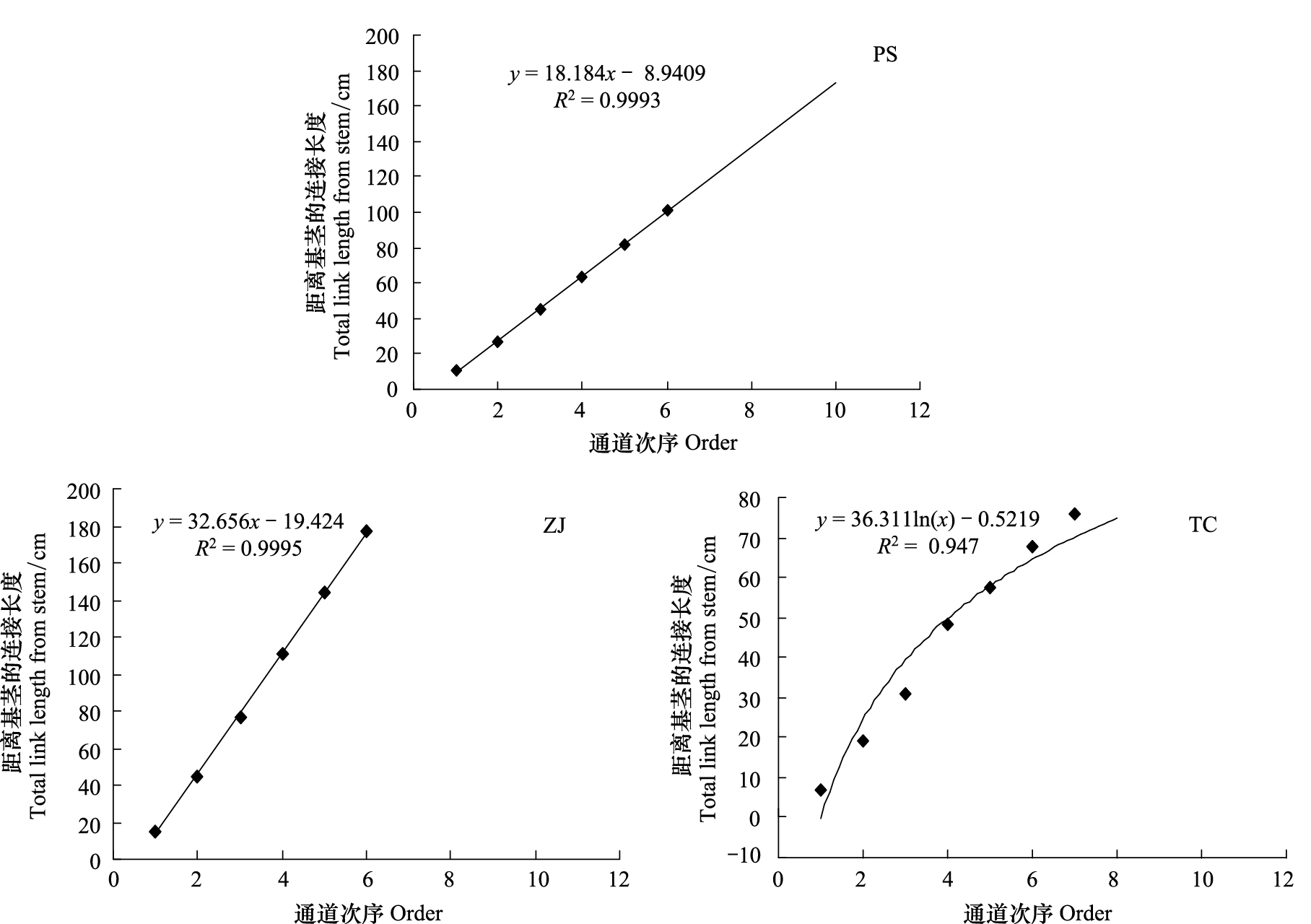
|
| 图 3 不同灌木粗根延伸策略 Fig. 3 Coarse root extension strategies of different shrubs |
根据图 4,3种灌木粗根根系直径缩减速率与距离根茎的连接通道长度的关系表现出一致趋势,越接近根系主根,粗根的直径缩减速率较大,随通道连接长度增加,粗根直径尖细速率迅速降低,随后其值趋向于稳定。3种灌木中,以酸枣(ZJ)的根系直径尖细速率趋向于平缓,柽柳和杠柳的趋势接近。
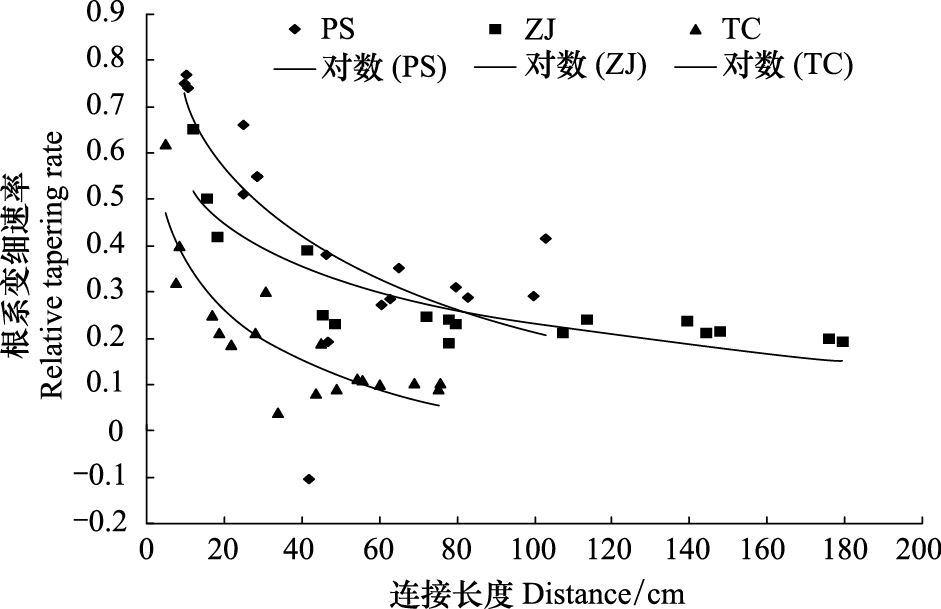
|
| 图 4 根系尖细速率 Fig. 4 Relative tapering of the coarse root |
通过计算杠柳、酸枣、柽柳3种植物的根系横截面积比,并作图(图 5),求得3种植物的通道分支前后的横截面积比分别为:1.04±0.28、1.10±0.36和0.96±0.16,同时,3种植物的根系分支前后的横截面积比和根系直径之间不存在横截面积相等是根系的一般性特征,与根系大小无关,基本符合Leonardo da Vinci法则。
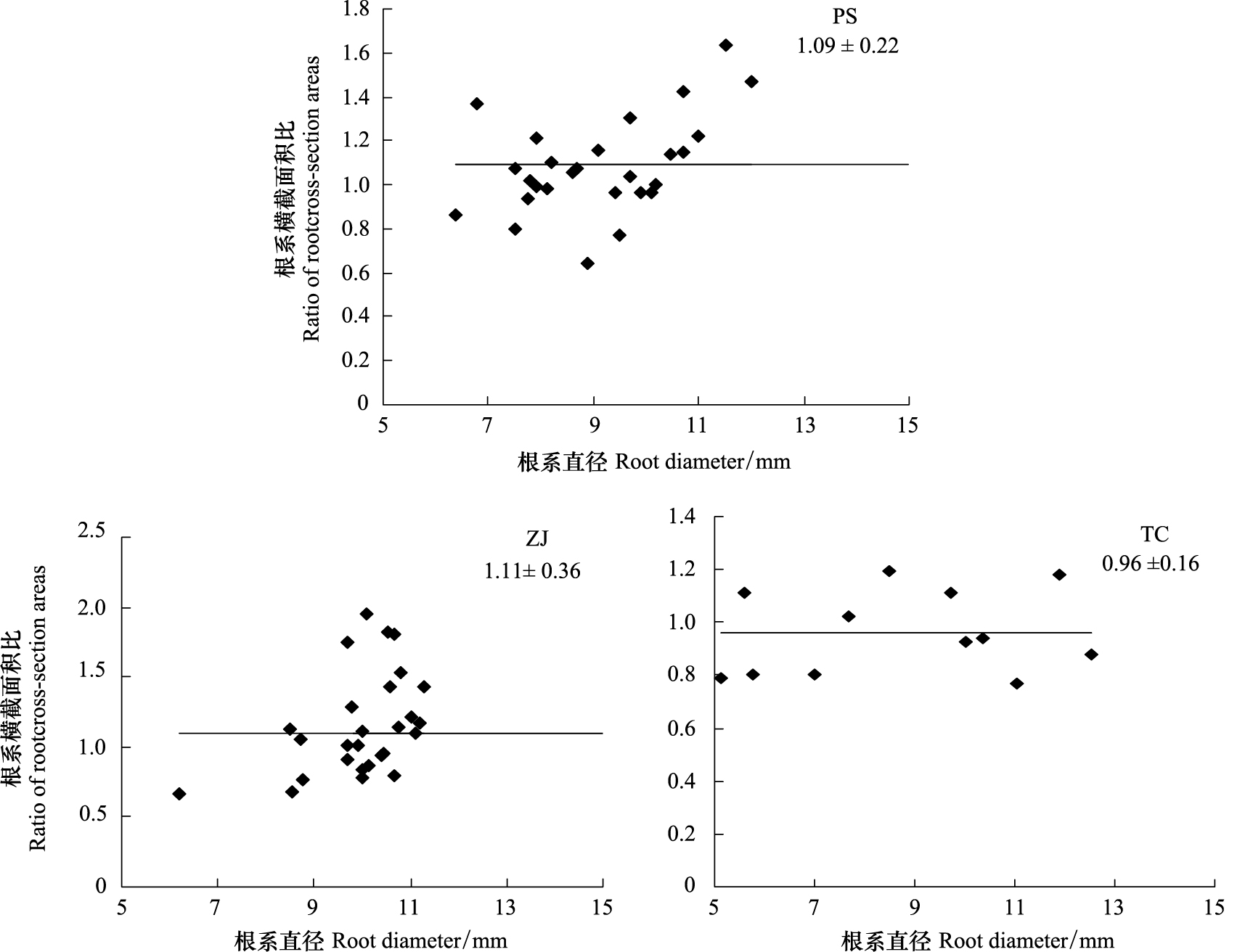
|
| 图 5 不同植物根系分支横截面积比 Fig. 5 The ratio of root cross-section areas in different species |
拓扑结构可以反映根系的觅养策略,特别是侧根对营养物质的竞争能力[21]。物种、土壤养分以及立地环境条件等都可能会对根系的拓扑结构产生影响[7]。但一般而言,鱼尾形(叉状)的分支根系次级分支较少,重叠少,内部竞争少,是瘠薄生境普遍存在的根系分支类型[16, 22]。然而,在贫瘠的生境中也不乏有叉状分支的植物根系存在,Bouma等[22]认为是由于较强的分支强度增强了植物在土壤中的扩展能力,有利于植物对养分的吸收。本文通过对黄河三角洲贝壳堤地区杠柳、酸枣和柽柳研究发现,3种灌木根系的拓扑指数存在差异,酸枣和杠柳趋向于鱼尾形分支,拓扑指数TI分别为0.93和0.85,接近于1,而柽柳的拓扑指数为0.69,接近于0.5,近似于叉状分支。说明,杠柳和酸枣采用类似的根系分支策略,拓扑指数较大,分支较少。柽柳则不然,其主要通过大量的分支,扩大根系的有效觅养空间。
连接长度的增加也是植物提高养分吸收的一个重要策略[12]。黄河三角洲贝壳堤岛3种优势灌木中,总粗根长度以杠柳最大(10.77m),柽柳最小(4.39m),平均连接长度以酸枣的最大,为33.51cm,而柽柳的平均连接长度仅有12.93cm。由此可见,杠柳和酸枣属于连接长度较大的鱼尾形分支,体现了瘠薄的生境条件,而柽柳是平均分支长度仅为12.93cm的鱼尾形分支,究其原因,可能与柽柳灌丛具有典型的沃岛效应有关[23],导致柽柳灌丛下土壤养分积累,因而保证其能够在瘠薄的土壤生境中,将大量的养分资源汇集到灌丛下供给自我利用,并通过不断增加分支,高效的吸收养分,从而能顺利生长。此外,植物根系空间分布特征也可解释这一现象。柽柳是泌盐性植物,其根系能够深扎至地下水位,因而水平根幅较小,垂直根深的比例增加,而酸枣和杠柳则主要分布在表层,依靠强大的分支连接长度来供给其养分来源(图 1),体现了不同的生境适应对策。
根系延伸策略反应了立地的土壤养分条件以及植物的觅养特征。图 3表明,随着连接通道次序的增加,杠柳和酸枣的粗根连接长度增加,体现了植物的生长和生境适应策略。在贝壳堤地区,本文杠柳和酸枣均具有根系近地表横走和萌蘖成苗的现象,这可能与特定生境下,两种灌木通过增加连接长度,大量积累有机物质,伺机萌发成苗,防止内部营养竞争的一种生境适应对策。而对于柽柳而言,其连接长度随通道长度的增加呈现先增加后趋向于平稳的趋势,体现了不同的根系生长对策。
根系直径的变细速率也体现了植物的觅养对策。研究发现,越靠近主轴,植物根系两节点之间的尖细速率较大,而随后,其尖细速率逐渐趋于变缓[7]。本研究表明,3种灌木中,以酸枣的根系直径尖细速率相比其他两种灌木更趋向于平缓,这可能与酸枣的根系萌蘖成苗强度较大有关,其植物根系在延伸时大都膨大,能够储藏大量养分,保证萌蘖的植株成活。此外,对3种灌木分支前后的直径关系比例进行研究发现,杠柳、酸枣和柽柳根系分支前后的横截面积比分别为:1.04±0.28、1.10±0.36和0.96±0.16,且植物根系分支前后的横截面积比和根系直径之间不存在相关关系(R2分别为:0.1963,0.0046和0.0827),由此可以看出,根系分支前后的横截面积相等是根系的一般性特征,与根系大小无关,基本符合Leonardo da Vinci法则。这与杨小林等[12],Eduardo等[24]的研究结果一致。
致谢: 感谢黄河三角洲贝壳堤与湿地国家自然保护区提供试验地点和在实验过程中给予的帮助。| [1] | Ontl T A, Hofmockel K S, Cambardella C A, Schulte L A, Kolka R K. Topographic and soil influences on root productivity of three bioenergy cropping systems. New Phytologist, 2013, 199(3): 727-737. |
| [2] | Lynch J. Root architecture and plant productivity. Plant Physiol, 1995, 109(1): 7-13. |
| [3] | Oppelt A L, Kurth W, Godbold D L. Topology, scaling relations and Leonardo's rule in root systems from African tree species. Tree Physiology, 2001, 21(2/3): 117-128. |
| [4] | Reubens B, Poesen J, Danjon F, Geudens G, Muys B. The role of fine and coarse roots in shallow slope stability and soil erosion control with a focus on root system architecture: a review. Trees, 2007, 21(4): 385-402. |
| [5] | De Baets S, Poesen J, Gyssels G, Knapen A. Effects of grass roots on the erodibility of topsoils during concentrated flow. Geomorphology, 2006, 76(1/2): 54-67. |
| [6] | 王鹏, 牟溥, 李云斌. 植物根系养分捕获塑性与根竞争. 植物生态学报, 2012, 36(11): 1184-1196. |
| [7] | Kalliokoski T, Nygren P, Sievänen R. Coarse root architecture of three boreal tree species growing in mixed stands. Silva Fennica, 2008, 42(2): 189-210. |
| [8] | Fitter A H. The topology and geometry of plant root systems: influence of watering rate on root system topology in Trifolium pratense. Annals of Botany, 1986, 58(1): 91-101. |
| [9] | Provoost S, Jones M L M, Edmondson S E. Changes in landscape and vegetation of coastal dunes in northwest Europe: a review. Journal of Coastal Conservation, 2011, 15(1): 207-226. |
| [10] | Acosta A, Carranza M L, Tzzi C F. Are there habitats that contribute best to plant species diversity in coastal dunes? Biodiversity and Conservation, 2009, 18(4): 1087-1098. |
| [11] | Álvarez-Molina L L, Martínez M L, Pérez-Maqueo O, Gallego-Fernández J B, Flores P. Richness, diversity, and rate of primary succession over 20 year in tropical coastal dunes. Plant Ecology, 2012, 213(10): 1597-1608. |
| [12] | 杨小林, 张希明, 李义玲, 李绍才, 孙海龙. 塔克拉玛干沙漠腹地3种植物根系构型及其生境适应策略. 植物生态学报, 2008, 32(6): 1268-1276. |
| [13] | Xie W J, Zhao Y Y, Zhang Z D, Liu Q, Xia J B, Sun J K, Tian J Y, Sun T Q. Shell sand properties and vegetative distribution on shell ridges of the Southwestern Coast of Bohai Bay. Environmental Earth Sciences, 2012, 67(5): 1357-1362. |
| [14] | 赵艳云, 胡相明, 刘京涛, 孙景宽. 黄河三角洲贝壳堤岛植被特征分析. 水土保持通报, 2011, 31(2): 177-180, 185. |
| [15] | 田家怡, 夏江宝, 孙景宽, 刘庆,张会,赵艳云,谢文军,张承,付荣恕,谢桐音,李甲亮,李田. 黄河三角洲贝壳堤岛生态保护与恢复. 北京: 化学工业出版社, 2011:1-209. |
| [16] | Fitter A H, Stickland T R, Harvey M L, Wilson G W. Architectural analysis of plant root systems. 1. Architectural correlates of exploitation efficiency. New Phytologist, 1991, 118(3): 375-382. |
| [17] | Mandelbrot B B. The fractal geometry of nature. New York: W. H. Freeman, 1983. |
| [18] | Murray C D. A relationship between circumference and weight in trees and its bearing on branching angles. The Journal of General Physiology, 1927, 10(5): 725-729. |
| [19] | Mandelbrot B B. The fractal geometry of trees and other natural phenomena//Geometric Problems and Biological Structures: Buffon's 200th Anniversary. Lecture Notes in Biomathematics. Berlin, Heidelberg: Springer, 1978, 23: 235-249. |
| [20] | van Noordwijk M,Spek LY,de Willigen P.Proxi-real root diameter as predictor of total root size for fractal branching models.I.Theory. Plant and Soil, 1994, 164,107-117. |
| [21] | Biondini M E, Grygiel C E. Landscape distribution of organisms and the scaling of soil resources. The American Naturalist, 1994, 143(6): 1026-1054. |
| [22] | Bouma T J, Nielsen K L, Van Hal J, Koutstaal B. Root system topology and diameter distribution of species from habitats differing in inundation frequency. Functional Ecology, 2001, 15(3): 360-369. |
| [23] | 尹传华, 冯固, 田长彦, 白灯莎, 张福锁. 塔克拉玛干沙漠北缘柽柳灌丛肥岛效应的变化规律及其生态学意义. 北京林业大学学报, 2008, 30(1): 52-57. |
| [24] | Eduardo S,Harry O L,Pekka N.A fractal root model applied for estimating the root biomass and architecture in two tropical legume tree species.Annals of Forest Science, 2004, 61: 337-345. |
 2015, Vol. 35
2015, Vol. 35