文章信息
- 邓长春, 蒋先敏, 刘洋, 张健, 陈亚梅, 和润莲
- DENG Changchun, JIANG Xianmin, LIU Yang, ZHANG Jian, CHEN Yamei, HE Runlian
- 高山林线交错带高山杜鹃的凋落物分解
- Litter decomposition of Rhododendron lapponicum in alpine timberline ecotone
- 生态学报, 2015, 35(6): 1769-1778
- Acta Ecologica Sinica, 2015, 35(6): 1769-1778
- http://dx.doi.org/10.5846/stxb201305231155
-
文章历史
- 收稿日期:2013-05-23
- 修订日期:2014-04-17
2. 四川省阿坝州川西林业局, 理县 623102
2. Forestry Bureau of Western Sichuan in Aba, Lixian 623102, China
凋落物分解是维持生态系统生产力、养分循环、土壤有机质形成的关键生态过程[1, 2, 3]。迄今,国内外科学家开展了大量的凋落物分解研究[4, 5],研究对象涉及到不同气候带、不同植物类型,涉及到的环境因子包括土壤温湿度、土壤类型、植物种类、光照、雪被等[5, 6, 7]。目前,比较一致的结论是“气候控制着区域尺度的凋落物分解速率,而由物种决定的凋落物基质质量控制着小尺度的凋落物分解过程[8]”。一般生态学的理论认为,环境的温度、湿度越高,凋落物分解速率越快,而在冬季低温状况下,凋落物的分解速率很低[9]。然而,近年来不断增加的冬季凋落物分解实验[10, 11, 12, 13, 14, 15]表明,实际情况并非如此。高寒生态系统频繁的冻融循环是影响凋落物分解的重要因子[11],雪被能为凋落物分解者提供了相对稳定的环境[13],因此,冬季的凋落物质量损失也可能高于生长季。那么,究竟是生长季较高的温度还是冬季雪被的绝热保温作用对凋落物分解的影响更为重要?这在全球气候变化十分敏感的高山林线区域还缺乏应有的关注。
高山林线是高山森林、灌丛与草甸之间的生态过渡带,是高山植被垂直带谱中重要的过渡区域,指示着森林分布的极限环境[16],是研究高山生态系统结构、功能和过程对全球气候变化及人类干扰的理想研究区域[17]。川西高山林线交错带季节性雪被覆盖的时间一般为5—6个月[14, 18],在季节性雪被覆盖期间可能存在较大的凋落物质量损失和养分释放,这为研究冬季凋落物分解提供了良好的天然实验室。高山杜鹃(Rhododendron lapponicum (L.) Wahl.)为杜鹃花科高山常绿灌木或小乔木植物,自然生长状态下树高约1—3 m,主要分布在我国西南部2500 m至4500 m的高海拔,常见于山地冷杉林中或林缘草坡上,是我国西部地区高山/亚高山湿润山坡灌木群落的建群种或优势种。
目前,有关林线交错带位置、物种组成、生物多样性、植被格局和生理生态特征已开展了大量的科学研究[19, 20],但有关全球气候变化背景下,林线交错带凋落物分解及区域物质循环的研究工作却鲜见报道。因此,基于林线交错带不同海拔梯度形成的3个植被带在不同季节(雪被期、生长季节)可能对高山杜鹃凋落物分解产生显著影响的假设,以地处青藏高原东缘的灌木优势种高山杜鹃为研究对象,研究林线交错带雪被期与生长季凋落物分解的特征及两者间的联系,为进一步认识高山林线交错带生态系统的生物元素循环提供理论依据。
1 实验方法 1.1 研究区域概况四川省理县米亚罗林区 (31°43′—31°51′N,102°40′—103°02′E),位于青藏高原东缘褶皱带最外缘及岷江支流杂谷脑河的上游,海拔2200—5500 m,年平均气温6—12 ℃,1月平均气温-8 ℃,7月平均气温12.6 ℃,年积温为1200—1 400 ℃,年降水量为600—1100 mm,年蒸发量为1000—1900 mm,具有降水次数多、强度小的特点。地形以石质山地为主,土壤具有粗骨(石砾含量高)和薄层。从低海拔到高海拔,土壤类型依次为山地暗棕壤、棕色针叶林土、高山草甸土。本研究选择米亚罗鹧鸪山(31°51′428″N,102°41′230″E)高山林线交错带。鹧鸪山位于杂谷脑河北侧,海拔3200—4800 m,是大渡河与岷江的分水岭。山地垂直地带性明显,自河谷至山顶依次分布有针阔混交林、暗针叶林、高山灌丛、高山草甸等植被带。在山地林线交错带上,植被类型从低海拔到高海拔由暗针叶林经林线灌丛过渡到高山草甸,地被物厚度逐渐降低,土壤类型由棕色针叶林土过渡到高山草甸土。该区域包括了典型的自然条件下形成的高山林线,能较好地反映川西高山林线交错带植被、土壤及地被物的生态特征。
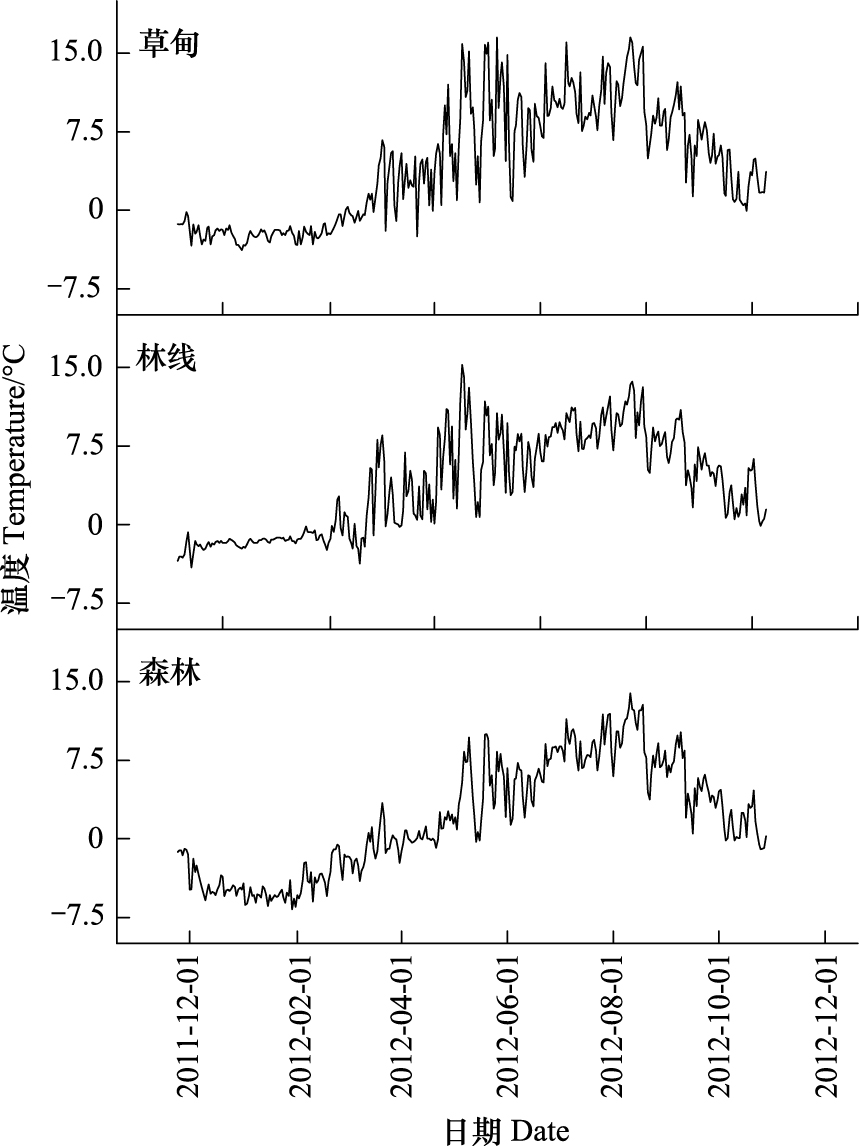
1.2 样地设计采用GPS定位,沿垂直于等高线方向,在高山林线交错带区域(海拔3900—4200 m)设置3条宽度为50 m的定位样带,样带分别经过针叶林 (CF)(3900 m)、林线(TL) (4000 m)和草甸(MD) (4200 m)。在各样带上选择并固定样方,采用iButton(DS1921)监测凋落物分解的温度,每3 h自动记录1次数据(图 1)。3个植被带雪被期(SS,连续7 d出现零下温度的第1天至连续7 d无零下温度的前一天)和生长季(GS,连续7 d无零下温度的第1天至连续7 d出现零下温度的前1天)的平均温度、天数及冻融循环次数(持续时间≥3 h的零上温度交替到零下温度并持续3 h及以上,或持续时间≥3 h的零下温度交替到零上温度并持续3 h及以上,计为冻融1次)见表 1。
|
| 图 1 雪被期和生长季高山林线交错带凋落物分解日平均温度动态 Fig. 1 Dynamics of daily mean temperature of litter during the snowi-ng season and growing season in the alpine timberline ecotone |
| 交错带 Ecotone | 雪被期平均温度 Snowing season mean temperature/℃ | 生长季平均温度 Growing season mean temperature/℃ | 雪被期天数 Days of snowing season/d | 生长季天数 Days of snowing season/d | 冻融循环次数 Frequency of freeze— thaw cycle/time |
| 表中温度为凋落物袋内监测的凋落物分解温度 | |||||
| 草甸 Meadow | -0.40 | 8.32 | 166 | 199 | 63 |
| 林线 Timberline | -1.93 | 7.04 | 170 | 195 | 98 |
| 森林 Coniferous forest | -3.13 | 6.14 | 177 | 188 | 48 |
2011年10月初,在高山林线交错带暗针叶林(海拔3900 m)中,于高山杜鹃凋落高峰期收集新鲜凋落叶,带回自然风干。称取5份凋落叶10 g于65 ℃烘箱烘至恒重,测定其自然风干后的含水量。称取10 g自然风干的凋落叶装入尼龙网材质、大小20 cm×20 cm,网孔大小为底部(贴地面)0.055 mm表面层为1 mm的凋落物袋中,共制备30袋备用。剩余凋落叶65 ℃24 h烘干,磨碎并分析凋落叶初始基质质量。2011年10月底将凋落袋放回林线交错带的3个植被带的固定样方中,每个样方内放置10袋,凋落袋平铺于样地地表,各凋落袋间间隔至少5 cm。于2012年5月9日和10月26日采集凋落物分解袋,每个植被带样地每次采集5袋,采集后立即用封口袋封装,翌日带回实验室,去除杂质、土壤,烘干至恒重,供相关分析测试。有机碳含量采用重铬酸钾-外加热法测定[21];全氮含量采用半微量凯氏定氮法测定[21];全磷含量采用钼锑钪比色法测定[21];木质素和纤维素采用改进的范氏酸性洗涤纤维法测定[22]。
1.4 计算与统计分析用改进的Olson[23]经典指数模型拟合凋落物分解过程:
y=ae-kt
式中,y为凋落物残留率(%);k为分解系数;t为时间(a);a为拟合参数;e为自然对数底。
运用差量法计算凋落物失重率[24]:
Li(%)=100×(Mi-1-Mi)/M0
式中,Li为凋落物失重率(%);M0为凋落物初始重(g); Mi 为不同时间点采样的瞬时残留量(g)。
凋落物全碳、全氮、全磷、木质素和纤维素的释放率(降解率)[24]:
Ri(%)=100×(Mi-1Ci-1-MiCi)/M0C0
式中,Ri为各组分释放率(降解率)(%);Ci为各组分在i时间采样时的含量(实测浓度)(g/kg)或(%);Mi为不同时间点采样的瞬时残留量(g);C0为各组分初始含量(初始浓度)(g/kg)或(%);M0为凋落物初始重(g)。数据统计与分析采用SPSS 20.0和Excel2007,图表绘制采用Excel2007和Origin8.1。采用单因素方差分析(one-way ANOVA)和最小显著差数法(LSD),分析检验凋落物各分解参数植被类型间的差异性;采用T检验,检验各分解参数两个分解阶段(雪被期和生长季)间的差异性;采用双因素方差分析(two-way ANOVA)植被类型和季节及其交互作用对高山杜鹃凋落物各分解参数的影响。
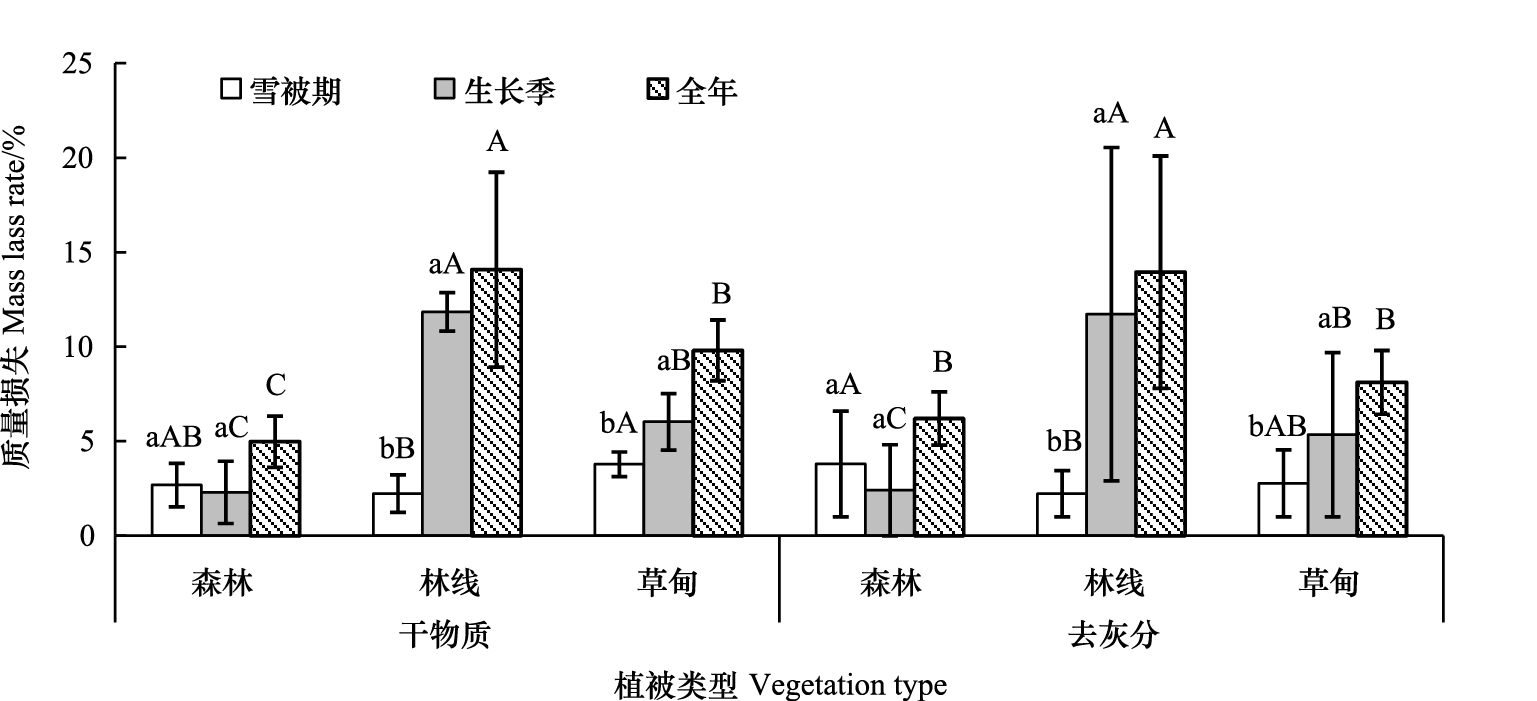
2 结果 2.1 凋落物的质量损失 2.1.1 凋落物的失重率高山杜鹃凋落物分解1a后的干物质失重率和去灰分失重率趋势一致(图 2)。平均干物质损失率为9.62%,去灰分的平均失重率为10.09%,都表现为林线>高山草甸>针叶林。方差分析表明,植被带间凋落物的年失重率差异极显著(P<0.01)。多重比较发现,第1年失重率林线极显著高于草甸与针叶林(P<0.01),且草甸极显著高于针叶林。
|
| 图 2 雪被期和生长季高山杜鹃凋落物的质量损失 Fig. 2 Litter decomposition of R. lapponicum measured as mass loss over snow season and growing season in alpine timberline ecotone 不同小写字母表示同一海拔上季节间差异显著(P<0.05,n=5);不同大写字母表示同一季节不同海拔间差异显著(P<0.05,n=5),比较在“含灰分”与“去灰分”内进行 |
方差分析表明,季节对各植被带凋落物的干物质失重率及去灰分失重率影响极显著 (P<0.01 )。雪被期内干物质失重率表现为高山草甸3.78%显著高于林线2.23%,而草甸与针叶林2.68%及林线与针叶林间均无显著差异;生长季表现为林线11.85%极显著高于草甸6.03%与针叶林2.30%,且草甸显著高于针叶林。对各植被带雪被期和生长季凋落物的干物质失重率进行比较,针叶林表现为雪被期略高于生长季(P>0.05),林线和高山草甸都表现为生长季显著高于雪被期(P<0.01)。全年总体来看,生长季干物质失重率的占第1年干物质失重率的近80%,质量损失主要在发生生长季。
2.1.2 凋落物分解系数用Olson经典分解模型拟合高山林线交错带高山杜鹃凋落物的分解过程,结果如表 2所示,模型拟合的干物质质量损失和去灰分质量损失的分解系数k非常接近,分别为0.145和0.156。计算得出凋落物分解一半的时间约为5a,凋落物分解95%的时间约为20a。
| 类型 Type | 干物质分解模型 Dry matter decomposition model | 去灰分分解模型 Ash-free decomposition model |
| 回归方程 Regression models | y=1.044e-0.145t | y=1.049e-0.156t |
| 分解系数k Decomposition constant k | 0.145 | 0.156 |
| 相关系数 R Correlation coefficient R | 0.744 | 0.735 |
| 半分解时间 T0.5 Time of half decomposition T0.5/a | 5.08 | 4.75 |
| 95%分解时间T0.95 Time of half decomposition T0.95/a | 20.96 | 19.51 |
| 显著性Significance P | <0.0001 | <0.0001 |
如表 3所示,高山杜鹃凋落物分解1a后,全C、全N、全P、木质素和纤维素的含量均发生了不同程度的变化。C含量呈持续下降趋势,年平均降低了12.81%(雪被期2.48%、生长季10.33%),且主要发生在生长季。经雪被期后,暗针叶林与林线C含量均显著下降,而高山草甸C含量无显著变化。凋落物N含量总体上升,海拔梯度之间差异显著,暗针叶林与林线上升幅度显著,而草甸上升幅度较小。凋落物P含量总体下降,下降集中在生长季。经雪被期后,P含量草甸显著高于暗针叶林;经生长季后,暗针叶林与林线均显著高于草甸。木质素含量小幅升高,雪被期3个植被带平均升高1.72%,生长季平均升高了2.00%,季节之间及植被带间均无显著差异。纤维素含量总体大幅下降,雪被期3个植被带平均下降22.95%,生长季平均下降1.38%,下降主要发生在雪被期。
| 组分 Constituent | C /(g/kg) | N /(g/kg) | P /(g/kg) | 木质素 Lignin(L)/% | 纤维素 Cellulose/% | C/N | 木质素(L)/N | C/P | |
| 含量数据:平均值±标准误差;比值数据:平均值(不同小写字母表示同一海拔季节间差异显著(P<0.05,n=5);不同大写字母表示同一季节海拔间差异显著(P<0.05,n=5));SS: snow season;GS: growing season;CF: coniferous forest;TL: timberline;MD: meadow | |||||||||
| 初始值Initial value | 546.1±12.7 | 2.56± 0.52 | 0.53± 0.11 | 33.53±1.96 | 15.33± 1.86 | 220.1 | 13.53 | 1054 | |
| 针叶林CF | 雪被期SS | 520.2±13.4 aB | 2.03± 0.20 bA | 0.42±0.07 bB | 33.94±3.09 aA | 11.41±1.08 aA | 258.8 aA | 16.91 aA | 1287 aA |
| 生长季GS | 467.8±40.59bA | 3.141±0.3843aA | 0.6785±0.1263aA | 33.69±2.427aA | 10.76±0.6012aA | 150.6bB | 10.87bC | 717.6bB | |
| 林线TL | 雪被期SS | 528.873±6.657aB | 2.082±0.1524bA | 0.5200±0.0821aBA | 33.972±2.658aA | 11.79±1.086aA | 255.1aA | 16.36aA | 1040aA |
| 生长季GS | 485.2±23.42bA | 2.645±0.2927aB | 0.5305±0.1147aA | 34.35±2.091aA | 12.32±1.439aA | 185.9bAB | 13.16bB | 942.4aB | |
| 草甸MD | 雪被期SS | 548.6±6.751aA | 2.166±0.2312aA | 0.6421±0.2517aA | 34.41±3.240aA | 12.24±1.228aA | 256.0aA | 16.16aA | 974.1bA |
| 生长季GS | 475.4±40.35bA | 2.265±0.1120aB | 0.2758±0.1398bB | 36.29±3.043aA | 11.73±1.556aA | 210.9 bA | 16.03 aA | 2122 aA | |
从表 3可以看出,C/N和L/N(木质素/N)呈雪被期上升生长季下降的趋势,而C/P呈持续上升趋势。雪被期C/N 3个植被带平均升高了16.60%,而生长季3个植被带都显著下降,草甸C/N下降幅度显著大于暗针叶林。经雪被期后3个植被带L/N均升高,经生长季后暗针叶林和林线L/N显著降低(P<0.05),草甸L/N保持稳定状态。暗针叶林中,C/P雪被期小幅升高,生长季显著下降;高山草甸上,刚好与其相反;而林线上C/P无明显变化,保持基本稳定。
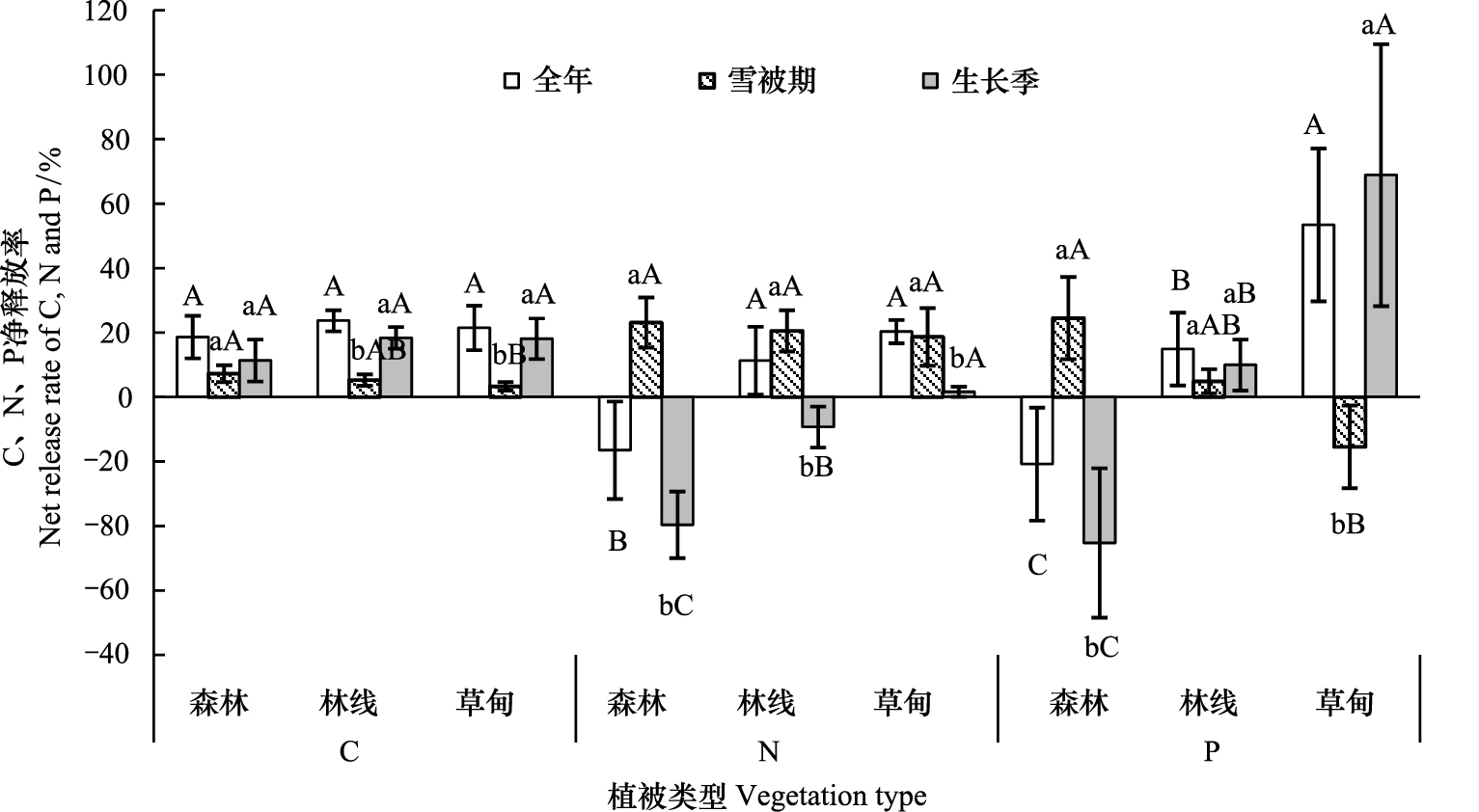
2.3 元素释放及木质素和纤维素的降解 2.3.1 C、N、P的释放从图 3可以看出,高山杜鹃凋落物C总体呈净释放状态,暗针叶林、林线和草甸C年释放率分别为18.65%、23.69%和21.47%,植被带间无显著差异。3个植被带,雪被期平均C释放率为5.31%,生长季为15.95%,C释放率生长季显著高于雪被期(P<0.01)。雪被期暗针叶林的C释放率高于草甸(P<0.05),暗针叶林与林线及林线与草甸间均无显著差异;生长季C释放率海拔之间无显著差异。
|
| 图 3 一年中雪被期和生长季凋落物碳、氮、磷的释放率 Fig. 3 Litter decomposition measured as net release rate of C,N,P over snowing season and growing season during a year in alpine timberline ecotone 不同小写字母表示同一海拔上季节间差异显著(P<0.05,n=5);不同大写字母表示同一季节不同海拔间差异显著(P<0.05,n=5) |
暗针叶林N年释放率为-16.47%,呈富集状态;林线和草甸分别为11.31%和20.35%,均呈释放状态。3个植被带,雪被期平均N释放率为20.81%,生长季为-15.75%,呈先释放后富集状态。雪被期N均呈释放态,3个植被带间无显著差异;生长季3个植被带N的变化差异极其显著,暗针叶林与林线N都不同程度富集,暗针叶林富集程度高于林线(P<0.01),而高山草甸N经过一个生长季后无明显变化,仅少量释放。
暗针叶林P年释放率为-20.75%,呈富集态;林线和草甸分别为14.91%和53.45%,均呈释放态。3个植被带,雪被期P平均释放率为4.47%,生长季为11.20%,呈持续释放态。暗针叶林中,雪被期释放,生长季富集,这与N趋势一致;林线上,两个季节均释放,生长季释放程度略高于雪被期(P>0.05);高山草甸上,雪被期富集,生长季大量释放。林线以上与林线以下两个分解阶段P的变化趋势刚好相反,而林线P的释放表现得相对平和。
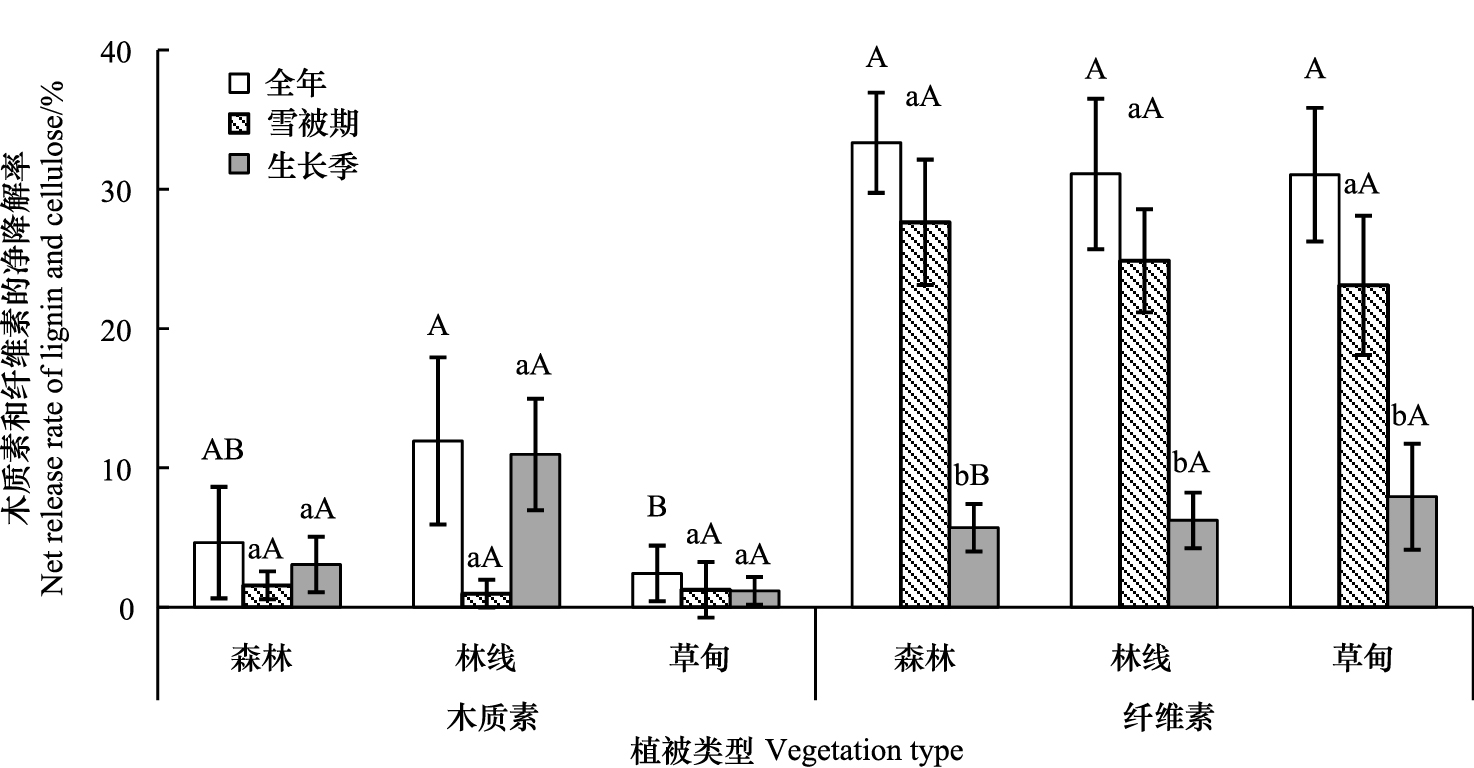
2.3.2 木质素和纤维素的降解如图 4所示,凋落物的木质素第1年降解微弱,林线年降解率最高,这与失重率相吻合。凋落物木质素的年降解率林线11.93%显著高于草甸2.42%,林线与暗针叶林4.64%及草甸与暗针叶林间均无显著差异。雪被期木质素降解率为1.26%,占全年降解率的19.95%;生长季为5.07%,占全年降解率的80.05%,生长季的降解占据重要比例。统计分析表明,雪被期和生长季的木质素降解率无显著差异,植被带间也无显著差异。
|
| 图 4 一年中雪被期和生长季凋落叶的木质素(Lignin)和纤维素(Cellulose)的降解率 Fig. 4 Leaf litter decomposition measured as net release rate of lignin and cellulose over snowing season and growing season during a year in alpine timberline ecotone 不同小写字母表示同一海拔上季节间差异显著(P<0.05,n=5);不同大写字母表示同一季节不同海拔间差异显著(P<0.05,n=5) |
凋落物的纤维素第1年降解明显,且集中于雪被期。纤维素第1年的降解率暗针叶林33.34%、林线31.11%和草甸31.05%,三者间无显著差异。雪被期3个植被带纤维素平均降解率为25.21%,占全年降解率的79.20%;生长季为6.63%,占全年降解率的20.80%,雪被期极显著高于生长季,且占据全年降解率的很大比重。植被带间纤维降解率均无显著差异。
2.4 季节与植被类型对凋落物分解的影响以季节和植被类型作为自变量,对干物质失重率、C释放率、N释放率、P释放率、木质素降解率、纤维素降解率、C/N、L/N和C/P进行双因素方差分析,结果如表 4。可以看出,季节(雪被期与生长季)对干物质失重率、C、N、P释放率、纤维素降解率、C/N和木质素/N均有显著作用,而对木质素降解率和C/P无显著作用;植被类型仅对干物质失重率、N释放率和C/P具有显著作用,而对C释放率、P释放率、木质素降解率、纤维素降解率、C/N和L/N均无显著作用;除木质素和纤维素降解率外,两因素的交互作用对其余指标均具有显著作用。干物质失重率和N释放率对季节和植被类型及两者交互作用响应显著。
| 变量Variable | 季节 Season | 植被类型 Vegetation type | 季节×植被类型 Season×Vegetation type | ||||||
| df | F | P | df | F | P | df | F | P | |
| 干物质失重率Dry mass loss | 1 | 88.12 | <0.001 | 2 | 41.58 | <0.001 | 2 | 53.92 | <0.001 |
| C释放率C release rate | 1 | 57.14 | <0.001 | 2 | 1.07 | 0.356 | 2 | 5.56 | <0.01 |
| N释放率N release rate | 1 | 181.96 | <0.001 | 2 | 16.71 | <0.001 | 2 | 25.23 | <0.001 |
| P释放率P release rate | 1 | 9.43 | <0.01 | 2 | 1.63 | 0.217 | 2 | 6.58 | <0.01 |
| 木质素降解率Lignin release rate | 1 | 1.15 | 0.295 | 2 | 0.65 | 0.529 | 2 | 0.78 | 0.472 |
| 纤维素降解率Cellulose release rate | 1 | 97.52 | <0.001 | 2 | 0.16 | 0.852 | 2 | 1.07 | 0.356 |
| C/N | 1 | 62.66 | <0.001 | 2 | 3.15 | 0.061 | 2 | 3.86 | <0.05 |
| Lignin/N | 1 | 16.49 | <0.001 | 2 | 2.78 | 0.082 | 2 | 4.94 | <0.05 |
| C/P | 1 | 0.85 | 0.366 | 2 | 4.45 | <0.05 | 2 | 8.63 | <0.01 |
从凋落物1a的质量损失来看,高山杜鹃凋落物在林线交错带的平均干物质失重率为9.62%,低于本地区冷杉[24]、红桦[15]和窄叶鲜卑花[14]等凋落物的失重率。高山杜鹃凋落物的分解系数k为0.145,在北极冻原—热带森林的k值0.032—3.734范围[25]中处于较低水平,与川西高山森林的岷江冷杉、红桦、四川红杉和方枝柏4种凋落叶的k值0.201—0.338[15]及北美东部阿巴拉契亚山大叶杜鹃凋落叶k值0.657[26]相比均较小。可见,分解缓慢和分解速率低是高山杜鹃凋落物叶的主要特征之一,这与Wardle[27]等在瑞典北部的研究结果一致,叶片革质且较厚及可利用碳、氮含量较低[26]可能是高山杜鹃凋落叶分解速率低、分解慢的重要原因。
高山林线交错带海拔梯度上形成的不同植被类型对高山杜鹃凋落物质量损失的影响极其显著(P<0.001)。林线全年凋落物的质量损失极显著高于暗针叶林和草甸,首先可能是因为林线上剧烈波动的温度和最为频繁的冻融循环(表 1)严重破坏了凋落叶的物理结构[28, 29],其次可能是因为高山林线处于森林与高山草甸的交接界面,分解者具有较高的生物多样性[30],能量和物质交换更为频繁。雪被期和生长季的交替同样显著地影响着高山杜鹃凋落物的分解(P<0.001)。从整个交错带看来,生长季较高的平均温度可能是高山杜鹃凋落物的质量损失集中在生长季的主要原因[8],但值得注意的是,暗针叶林内凋落物失重率雪被期略高于生长季,而林线和高山草甸上生长季显著高于雪被期,这可能是森林中两个季节的天数相差较小,而草甸和林线的生长季天数高于雪被期天数。暗针叶林密闭的林冠削弱了太阳辐射,雪被较厚且持续时间长,雪被的绝热保温作用可能促进了凋落物的分解[13],而林线与草甸经历了更为频繁的冻融循环,且受雪融水淋洗作用强烈,频繁冻融循环作用和强烈的雪融水淋洗作用是该区域凋落物在生长季初期质量大量损失的重要原因[28, 29, 31]。
3.2 不同季节和植被类型质量变化、元素释放与组分降解的差异及成因高山杜鹃凋落物碳、氮、磷的含量变化和释放效率在两个季节及3个植被带间的差异较大。凋落物碳含量持续降低,碳的释放主要集中在生长季,但暗针叶林中雪被期凋落物的碳的释放量比生长季更高,这与Saccone[13]等的研究一致。凋落物氮含量总体上升,首先可能是因为外源氮在凋落物上被微生物固持[2],导致氮含量上升;其次刘洋[32]等在该区域的研究发现,雪被期土壤微生物生物量氮大量增加,这也可能是导致凋落物中氮含量升高的原因之一。该区域凋落物氮含量与微生物的关系还有待进一步研究。
暗针叶林中雪被期氮、磷均大量释放,生长季中都大量富集,这可能是因为暗针叶林中的较厚雪被给雪下生物群落(微生物和土壤动物)提供了一个相对稳定的环境,土壤生物活性有效促进了凋落物养分的释放[33],生长季到来后,温度上升,暗针叶林阴暗潮湿的环境下微生物大量爆发,微生物对养分固持作用明显,养分在凋落物内富集[34]。在高山草甸上,雪被期磷少量富集,但生长季却大量释放,生长季较高的温度可能是磷大量释放的重要原因[35],同时高山草甸生长季牧草的生长需要大量养分,这种植物养分需求与凋落物养分释放之间可能存在一种相互适应的机制。高山林线上,碳、氮、磷的释放都表现得更为持续而平稳,这可能是高山林线土壤碳、氮、磷含量高于苔原和森林的主要原因[36],而高山林线较高的生物多样性对养分的大量需求可能是其内在动力。
木质素在凋落物基质中属难分解成分,而纤维素属于中等难度分解成分[3]。木质素含量是预测凋落物分解和失重的良好指标[37],凋落物中木质素含量一般为5%—30%[38]。本研究发现,高山杜鹃凋落物木质素初始含量为33.5%,与地中海区域百瑞木(Cistus Incanus)相当[39],高于一般凋落物木质素含量的上限,本研究也证实了高山杜鹃凋落物分解缓慢。经1a分解后,木质素降解量极低,这也与Duboc[40]等在奥地利北部阿尔卑斯山对欧洲花木和南欧黑松的结果相近。林线木质素降解高于暗针叶林与草甸,与失重率高度一致。根据限制因子原理,高山杜鹃凋落物分解缓慢极有可能是因为木质素的限制作用。纤维素第1年大幅降解,年降解率为31.8%,在凋落物1a质量损失中的贡献可能是最大的。值得注意是,在3个植被带上,雪被期纤维素的降解率均显著高于生长季,这是因为冬季雪下土壤呼吸依然维持、土壤微生物活性较高[29, 41]。
C/N、木质素/N和C/P都是凋落物分解速率的良好指标[42]。Parnas[43]等认为氮发生固持的关键值为C/N值>30,而C/N值<30时氮发生矿化,本研究中高山杜鹃凋落物C/N值的初始值为220,即凋落物在分解过程中将发生氮固持作用,而研究结果也证实凋落物氮含量和绝对量均上升(表 2和图 3)。经雪被期后,C/N值、L/N值和C/P值都不同程度升高(表 3),说明季节性雪被对凋落物质量产生了重要影响,雪被下的土壤呼吸及生物活性可能是其主要驱动因子。因林线上养分稳定持续释放,C/N值、L/N值和C/P值的变化幅度与暗针叶林和草甸相比都相对较小。
综上所述,高山杜鹃凋落物的分解集中于生长季,林线交错带内因海拔梯度形成的不同植被类型对其分解具有显著影响。季节性雪被对林线交错带内高山杜鹃分解的影响不仅局限在雪被期内,雪被融化期间频繁冻融作用和雪融水淋洗作用都能显著促进凋落物在生长季初期的分解。因高山杜鹃凋落物分解集中于生长季,季节性雪被的缩减和生长季的延长[44]可能加速高山杜鹃凋落物的分解。另一方面,高山杜鹃凋落物林线与高山草甸的分解速率都显著高于暗针叶林,而高山杜鹃群落可能正向更高海拔扩张[16, 45],这也可能进一步促进林线交错带内高山杜鹃凋落物的分解。因此,我们预测,在全球气候变暖的情景下,雪被缩减、生长季的延长和高山杜鹃群落的扩张将加速高山林线交错带高山杜鹃凋落物的分解。
致谢: 四川农业大学林学院生态林业研究所吴福忠老师在本文写作过程中给予帮助,崔宁洁、欧江、李建平、宋小艳和纪托未等同学及四川省阿坝州川西林业局护林工人周德东在野外采样工作中给予帮助,特此致谢。| [1] | 杨万勤, 邓仁菊, 张健. 森林凋落物分解及其对全球气候变化的响应. 应用生态学报, 2007, 18(12): 2889-2895. |
| [2] | 刘强, 彭少麟. 植物凋落物生态学. 北京: 科学出版社, 2010: 3-5, 54-56. |
| [3] | 郭剑芬, 杨玉盛, 陈光水, 林鹏, 谢锦升. 森林凋落物分解研究进展. 林业科学, 2006, 42(4): 93-100. |
| [4] | Barrett K. Carbon Accumulation and Storage in Amazonian Ecosystems [D]. Massachusetts: Clark University, 2008. |
| [5] | Parton W, Silver W L, Burke I C, Grassens L, Harmon M E, Currie W S, King J Y, Adair E C, Brandt L A, Hart S C. Global-scale similarities in nitrogen release patterns during long-term decomposition. Science, 2007, 315(5810): 361-364. |
| [6] | Berg B, McClaugherty C. Plant litter: Decomposition, humus formation, carbon Sequestration. New York: Springer, 2008. |
| [7] | Baptist F, Yoccoz N G, Choler P. Direct and indirect control by snow cover over decomposition in alpine tundra along a snowmelt gradient. Plant and Soil, 2010, 328(1/2): 397-410. |
| [8] | Aerts R. The freezer defrosting: global warming and litter decomposition rates in cold biomes. Journal of Ecology, 2006, 94(4): 713-724. |
| [9] | Vitousek P M, Turner D R, Parton W J, Sanford R L. Litter decomposition on the Mauna Loa environmental matrix, Hawai'i: patterns, mechanisms, and models. Ecology, 1994, 75(2): 418-429. |
| [10] | Bleak A T. Disappearance of plant material under a winter snow cover. Ecology, 1970, 51(5): 915-917. |
| [11] | Taylor B R, Parkinson D. Does repeated freezing and thawing accelerate decay of leaf litter? Soil Biology and Biochemistry, 1988, 20(5): 657-665. |
| [12] | Wu F Z, Yang W Q, Zhang J, Deng R J. Litter decomposition in two subalpine forests during the freeze-thaw season. Acta Oecologica, 2010, 36(1): 135-140. |
| [13] | Saccone P, Morin S, Baptist F, Bonneville J, Colace M, Domine F, Faure M, Geremia R, Lochet J, Poly F, Lavorel S, Clément J C. The effects of snowpack properties and plant strategies on litter decomposition during winter in subalpine meadows. Plant and Soil, 2012, 363(1/2): 215-229. |
| [14] | 胡霞, 吴宁, 吴彦, 左万庆, 郭海霞, 王金牛. 川西高原季节性雪被覆盖对窄叶鲜卑花凋落物分解和养分动态的影响. 应用生态学报, 2012, 23(5): 1226-1232. |
| [15] | 武启骞, 吴福忠, 杨万勤, 徐振锋, 何伟, 何敏, 赵野逸, 朱剑霄. 季节性雪被对高山森林凋落物分解的影响. 植物生态学报, 2013, 37(4): 296-305. |
| [16] | 刘洋, 张健, 杨万勤. 高山生物多样性对气候变化响应的研究进展. 生物多样性, 2009, 17(1): 88-96. |
| [17] | Li M C, Luo T X, Zhu J J, Kong G Q. Advances in formation mechanism of alpine timberline and associated physio-ecological characteristics of plants. Acta Ecologica Sinica, 2008, 28(11): 5583-5591. |
| [18] | Tan B, Wu F Z, Yang W Q, Liu L, Yu S. Characteristics of soil animal community in the subalpine/alpine forests of western Sichuan during onset of freezing. Acta Ecologica Sinica, 2010, 30(2): 93-99. |
| [19] | Walther G. Plants in a warmer world. Perspectives in Plant Ecology, Evolution and Systematics, 2003, 6(3): 169-185. |
| [20] | Shiyatov S G, Terent Ev M M, Fomin V V, Zimmermann N E. Altitudinal and horizontal shifts of the upper boundaries of open and closed forests in the Polar Urals in the 20th century. Russian Journal of Ecology, 2007, 38(4): 223-227. |
| [21] | Lu R K. Soil and Agro-Chemical Analytical Methods. Beijing: China Agricultural Science and Technology Press, 1999: 146-195. |
| [22] | Rowland A P, Roberts J D. Lignin and cellulose fractionation in decomposition studies using acid-detergent fibre methods. Communications in Soil Science & Plant Analysis, 1994, 25(3/4): 269-277. |
| [23] | Olson J S. Energy storage and the balance of producers and decomposers in ecological systems. Ecology, 1963, 44(2): 322-331. |
| [24] | Zhu J X, He X H, Wu F Z, Yang W Q, Tan B. Decomposition of Abies faxoniana litter varies with freeze-thaw stages and altitudes in subalpine/alpine forests of southwest China. Scandinavian Journal of Forest Research, 2012, 27(6): 586-596. |
| [25] | Gholz H L, Wedin D A, Smitherman S M, Harmon M E, Parton W J. Long-term dynamics of pine and hardwood litter in contrasting environments: toward a global model of decomposition. Global Change Biology, 2000, 6(7): 751-765. |
| [26] | Gulis V, Suberkropp K. Leaf litter decomposition and microbial activity in nutrient-enriched and unaltered reaches of a headwater stream. Freshwater Biology, 2003, 48(1): 123-134. |
| [27] | Wardle D A, Nilsson M, Zackrisson O, Gallet C. Determinants of litter mixing effects in a Swedish boreal forest. Soil Biology and Biochemistry, 2003, 35(6): 827-835. |
| [28] | Sulkava P, Huhta V. Effects of hard frost and freeze-thaw cycles on decomposer communities and N mineralisation in boreal forest soil. Applied Soil and Ecology, 2003, 22(3): 225-239. |
| [29] | Withington C L, Sanford R L Jr. Decomposition rates of buried substrates increase with altitude in the forest-alpine tundra ecotone. Soil Biology and Biochemistry, 2007, 39(1): 68-75. |
| [30] | 黄旭, 文维全, 张健, 杨万勤, 刘洋, 闫帮国, 黄玉梅. 川西高山典型自然植被土壤动物多样性. 应用生态学报, 2010, 21(1): 181-190. |
| [31] | Bokhorst S, Bjerke J W, Melillo J, Callaghan T V, Phoenix G K. Impacts of extreme winter warming events on litter decomposition in a sub-Arctic heathland. Soil Biology and Biochemistry, 2010, 42(4): 611-617. |
| [32] | 刘洋, 张健, 闫帮国, 黄旭, 徐振锋, 吴福忠. 青藏高原东缘高山森林-苔原交错带土壤微生物生物量碳, 氮和可培养微生物数量的季节动态. 植物生态学报, 2012, 36(5): 382-392. |
| [33] | Campbell J L, Mitchell M J, Groffman P M, Christenson L M, Hardy J P. Winter in northeastern North America: a critical period for ecological processes. Frontiers in Ecology and the Environment, 2005, 3(6): 314-322. |
| [34] | Zhang C F, Trofymow J A, Jamieson R C, Meng F, Gordon R, Bourque C P. Litter decomposition and nitrogen mineralization from an annual to a monthly model. Ecological Modelling, 2010, 221(16): 1944-1953. |
| [35] | Rui Y C, Wang Y F, Chen C G, Zhou X Q, Wang S P, Xu Z H, Duan J C, Kang X M, Lu S B, Luo C Y. Warming and grazing increase mineralization of organic P in an alpine meadow ecosystem of Qinghai-Tibet Plateau, China. Plant and Soil, 2012, 357(1/2): 73-87. |
| [36] | Liptzin D, Sanford R L Jr, Seastedt T R. Spatial patterns of total and available N and P at alpine treeline. Plant and Soil, 2013, 365(1/2): 127-140. |
| [37] | Dyer M L, Meentemeyer V, Berg B. Apparent controls of mass loss rate of leaf litter on a regional scale. Scandinavian Journal of Forest Research, 1990, 5(1/4): 311-323. |
| [38] | 阿姆森 K A. 森林土壤: 性质和作用//林伯群, 周重光, 译. 北京: 科学出版社, 1984: 33-46. |
| [39] | Fioretto A, Nardo C D, Papa S, Fuggi A. Lignin and cellulose degradation and nitrogen dynamics during decomposition of three leaf litter species in a Mediterranean ecosystem. Soil Biology and Biochemistry, 2005, 37(6): 1083-1091. |
| [40] | Duboc O, Zehetner F, Djukic I, Tatzber M, Berger T W, Gerzabek M H. Decomposition of European beech and Black pine foliar litter along an Alpine elevation gradient: Mass loss and molecular characteristics. Geoderma, 2012, 189-190: 522-531. |
| [41] | Brække F H, Finér L. Decomposition of cellulose in litter layer and surface peat of low-shrub pine bogs. Scandinavian Journal of Forest Research, 1990, 5(1/4): 297-310. |
| [42] | Taylor B R, Parkinson D, Parsons W F J. Nitrogen and lignin content as predictors of litter decay rates: a microcosm test. Ecology, 1989, 70(1): 97-104. |
| [43] | Parnas H. Model for decomposition of organic material by microorganisms. Soil Biology and Biochemistry, 1975, 7(2): 161-169. |
| [44] | IPCC 2007. Climate Change 2007: The Physical Science Basis, Contribution of Working Group I to the Fourth Assessment Report of the Intergovernmental Panel on Climate Change. Cambridge, United Kingdom and New York: Cambridge University Press. |
| [45] | Gavazov K S. Dynamics of alpine plant litter decomposition in a changing climate. Plant and Soil, 2010, 337(1/2): 19-32. |
 2015, Vol. 35
2015, Vol. 35




