文章信息
- 章典, 李诚, 刘璐, 张胜娟, 张庭廷
- ZHANG Dian, LI Cheng, LIU Lu, ZHANG Shengjuan, ZHANG Tingting
- 岩兰草油对淡水藻类的抑制作用
- Studies on the inhibition of vetiver oil to freshwater algae
- 生态学报, 2015, 35(6): 1845-1851
- Acta Ecologica Sinica, 2015, 35(6): 1845-1851
- http://dx.doi.org/10.5846/stxb201305211135
-
文章历史
- 收稿日期:2013-05-21
- 修订日期:2014-04-25
水体富营养化导致的藻类过度增殖,水华频繁发生,对水生生态系统和水体景观带来了严重的影响。尤其是水华藻类释放的藻毒素,可以溶解在水中,通过食物链等方式最终影响人类的健康和生活。因此,有效控制藻类过度生长及防止水华暴发是目前环境和生态领域中最为关注的问题。
近十年来,水生植物化感作用抑藻研究得到了广泛认可,因水生植物普遍生长于水中,且容易栽种,其释放的化感物质大多为次生代谢产物,在自然环境下可以短期降解,具有生态危险性低、副作用小、抑制效果明显等优点,因此成为实现藻类安全控制的新方法[1]。在水体中直接栽种水生植物抑藻的基础上,从水生植物体内提取化感物质将其直接施入水体,可以快速抑制藻类生长,并且易于操作,特别是为不适宜种植水生植物的水域提供极大便利[2]。
岩兰草 (Vetiveria zizanioides) 属禾本科岩兰草属,是一种多年生两栖类草本植物。其根系特别发达,可延伸到地下3 m,在恶劣的环境中仍然可以存活[3, 4]。其庞大的根系不仅可富集重金属,快速吸收水体中的氮磷,还可分泌化感物质杀灭水体中的有害微生物[5, 6, 7]。
为了寻找到能有效抑藻的化感物质,本文探讨了岩兰草根提取物岩兰草油(vetiver oil)在单独和共培养方式下对水华蓝藻铜绿微囊藻 (Microcystis aeruginosa) 和常见绿藻斜生栅藻 (Scenedesmus obliquus) 生长的影响,并分析了岩兰草油的主要成分,旨在为水华蓝藻治理寻找一条安全、环保、有效的新思路,新方法。
1 材料与方法 1.1 实验材料岩兰草油购自湖北佳诺信生物化工有限公司,纯度>99%。
铜绿微囊藻和斜生栅藻由中国科学院水生生物研究所藻种库提供;铜绿微囊藻采用BG-11培养基培养,斜生栅藻采用HB-4培养基培养。
1.2 培养方法实验前1周,两种藻分别进行扩大培养。培养条件为:光照强度4000 lx,光暗比为12 h ∶ 12 h,温度 (25±1) ℃。每天摇动3—5 次,使藻细胞进入对数生长期。
1.3 实验设计 1.3.1 岩兰草油对单独培养的铜绿微囊藻和斜生栅藻的抑制作用在预实验的基础上进行抑藻实验。取对数生长期的铜绿微囊藻和斜生栅藻分别放入50 mL锥形瓶中,再加入培养基使其藻细胞最终浓度为3.5×105 个/mL,并使最终体积为20 mL。锥形瓶中岩兰草油的最终浓度分别为0、0.1、0.2、0.4、0.8 mL/L,每组设3 个平行,各组置于1.2相同条件下培养。每隔48 h 进行细胞计数。
1.3.2 岩兰草油对铜绿微囊藻和斜生栅藻共培养时的抑制作用将对数生长期的铜绿微囊藻和斜生栅藻用培养基稀释至最终浓度2.5×105个/mL,然后分别取10 mL的藻液共同倒入50 mL锥形瓶。锥形瓶中岩兰草油最终浓度分别为0、0.5、1.0、2.0 mL/L,每组设3个平行,培养条件与1.2相同,共培养10 d。每隔48 h细胞计数。
1.3.3 岩兰草油的成分分析对岩兰草油进行气质联用(GC-MS)分析。气相色谱条件为:进样口温度260 ℃气化,流速1.50 mL/min,分流比100 ∶ 1,柱类型RTX-5,30×0.25×0.25,升温程序初始温度40 ℃,保持2 min后,在10 ℃/min速度下加热至250 ℃,保持5 min;质谱条件为:离子源温度200 ℃,接口温度250 ℃,检测器电压0.81 kV,扫描间隔时间0.5 sec,扫描荷质比40—700 aum,进样体积1 μL。应用NIST质谱数据库,分析质谱图,鉴定岩兰草油中主要化学成分。
1.4 测定方法细胞计数使用血细胞计数板计数;岩兰草油成分分析使用岛津GC-MS QP2010plus气质联用仪。
1.5 数据处理岩兰油对藻类的抑制率公式为:
IR = (1-N/N0)×100%
式中,IR为抑制率;N为加入岩兰草油组的藻密度(个/mL);N0为对照组藻密度 (个/mL)。将岩兰草油浓度与生长抑制率作一元线性回归,求出半效应浓度EC50 (mL/L)。数据采用Excel 2010和SPSS 17.0软件处理,各组间差异采用单因素方差分析(one-way ANOVA),P<0.05表示有显著性差异,P<0.01表示有极显著差异。
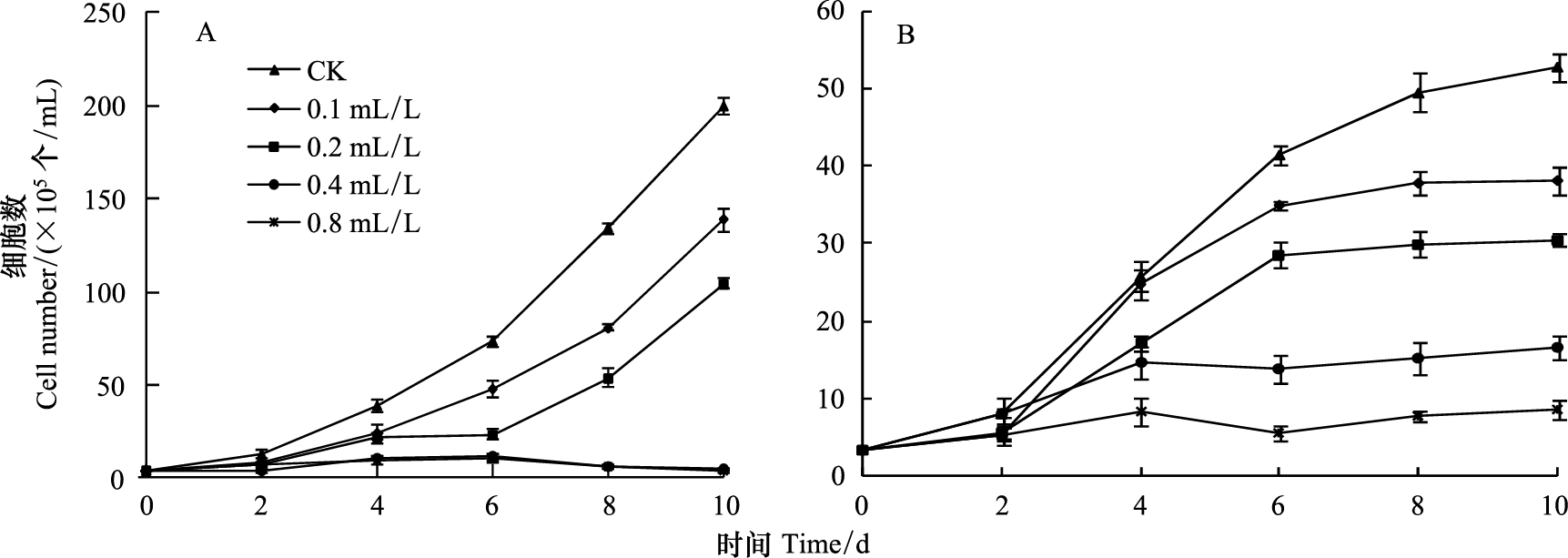
2 结果与分析 2.1 岩兰草油对单独培养的铜绿微囊藻和斜生栅藻生长的影响由图 1可知岩兰草油对铜绿微囊藻和斜生栅藻均有较好的抑制作用,且具有时间和剂量相关性。如各处理组在第2天内变化不大,从第4天 开始表现出不同的变化趋势,在第10天时,最大浓度处理组与对照组差异相当明显 (P<0.01)。两种藻对照组与0.1 和0.2 mL/L处理组均无显著差异 (P>0.05),说明低浓度岩兰草油对两种藻虽表现抑制但抑制效果不明显,0.4 mL/L处理组对斜生栅藻抑制作用明显 (P<0.05),0.8 mL/L处理组对斜生栅藻有极其显著的抑制作用 (P<0.01);而0.4和0.8 mL/L处理组对铜绿微囊藻的抑制作用均非常明显 (P<0.01),通过比较岩兰草油对两种藻的EC50,证明了岩兰草油抑藻具有种属选择性,对铜绿微囊藻的抑制效果要好于斜生栅藻。
|
| 图 1 不同浓度岩兰草油对铜绿微囊藻(A)和斜生栅藻(B)生长的影响 Fig. 1 Effect of vetiver oil on the growth of Microcystis aeruginosa (A) and Scenedesmus obliques (B) at different concentration |
由表 1 和表 2 可见,岩兰草油对两种藻均有抑制作用,随着岩兰草油浓度的升高,抑制率也逐渐增大。比较两种藻抑制率,发现在所有浓度的处理组中,岩兰草油对铜绿微囊藻的抑制率均大于斜生栅藻。在第8天时,当岩兰草油浓度为0.4 mL/L时,对铜绿微囊藻的抑制率已经达到95.67%,而斜生栅藻在岩兰草油浓度为0.8 mL/L时抑制率才达到84.21%。EC50均按第10天计算,得出岩兰草油对铜绿微囊藻的EC50 接近0.20 mL/L,而对斜生栅藻的EC50 为0.30 mL/L,进一步说明了岩兰草油对铜绿微囊藻的抑制效果更好,可能是两种藻的细胞结构不同对岩兰草油的敏感性有差异。
|
岩兰草油浓度/(mL/L) Vetiver oil concentrations | 处理天数Treatment days/d | ||||
| 2 | 4 | 6 | 8 | 10 | |
| 0.1 | 34.49±5.85 | 39.73±10.99 | 35.67±3.97 | 39.69±0.33 | 30.64±1.50 |
| 0.2 | 38.36±6.92 | 42.49±3.19 | 68.40±2.73 | 60.17±3.10 | 47.72±0.47 |
| 0.4 | 34.50±0.77 | 71.96±3.50 | 84.69±2.36 | 95.67±0.83 | 97.76±0.46 |
| 0.8 | 38.07±3.53 | 75.96±0.64 | 85.84±1.94 | 95.67±0.83 | 97.92±0.40 |
| 表中数据为平均值±SE(n=3) | |||||
|
岩兰草油浓度/(mL/L) Vetiver oil concentrations | 处理天数 Treatment days/d | ||||
| 2 | 4 | 6 | 8 | 10 | |
| 0.1 | 36.06±12.50 | 3.88±1.91 | 15.56±1.60 | 23.51±0.65 | 27.83±1.26 |
| 0.2 | 28.80±7.07 | 33.40±1.15 | 31.04±2.22 | 39.39±1.81 | 42.24±0.54 |
| 0.4 | 1.91±17.66 | 43.75±4.99 | 66.85±3.34 | 69.62±2.62 | 68.89±1.92 |
| 0.8 | 33.04±5.63 | 68.38±4.41 | 86.47±2.00 | 84.21±0.54 | 83.72±1.94 |
| 表中数据为平均值±SE(n=3) | |||||
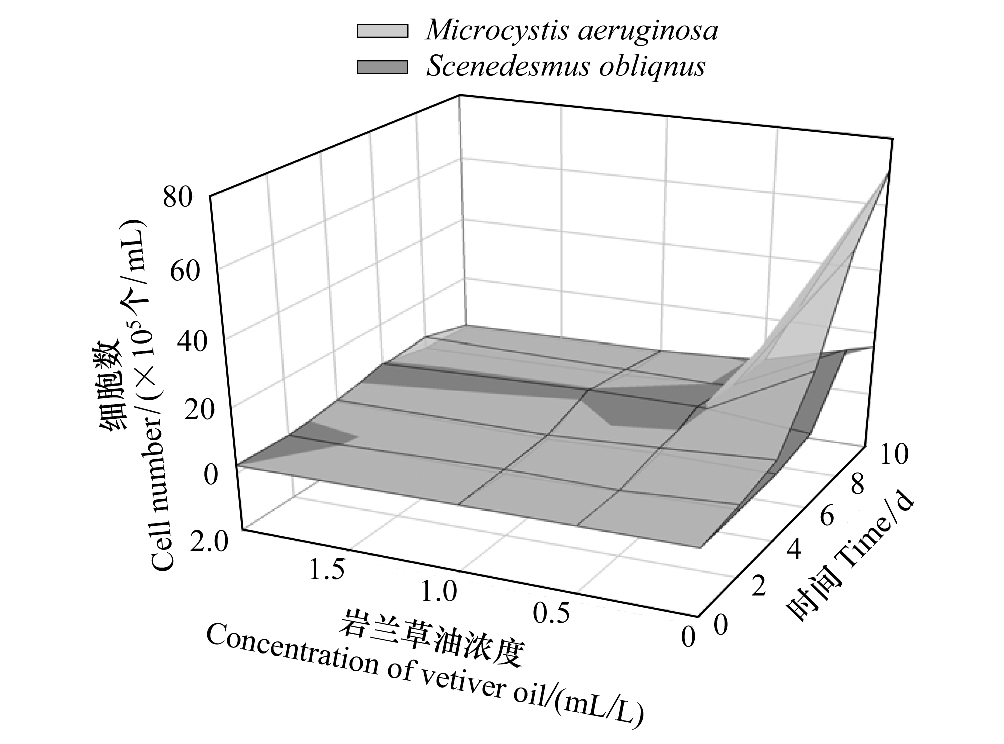
从图 2可以看出,岩兰草油对两种藻均具有抑制效果。但对照组中铜绿微囊藻的数目明显多于斜生栅藻(P<0.05),而在实验组中第6天时的斜生栅藻细胞数目明显高于铜绿微囊藻(P<0.05)。对照组现象出现的原因可能是:(1)斜生栅藻的增长速度小于铜绿微囊藻;(2)铜绿微囊藻释放出化感物质抑制了斜生栅藻的生长,所以对照组中铜绿微囊藻细胞密度大于斜生栅藻;但实验组中,由于岩兰草油的逐渐作用,至第6天时的铜绿微囊藻的细胞密度显著小于斜生栅藻,这更加说明了岩兰草油对铜绿微囊藻的抑制效能高于斜生栅藻。
|
| 图 2 岩兰草油对两种藻共培养时生长的影响 Fig. 2 Effect of vetiver oil on the growth of two species of algae with mixed culture |
为了更好地利用岩兰草油进行藻华的控制,在图 2数据的基础上,参见文献[8, 9]拟合了岩兰草油对铜绿微囊藻与斜生栅藻共存时的抑制模型。岩兰草油对铜绿微囊藻和斜生栅藻共存时的抑制模型与铜绿微囊藻、斜生栅藻单独生长的模型、以及在岩兰草油抑制环境下铜绿微囊藻、斜生栅藻单独生长时的模型既有区别,又有联系。在铜绿微囊藻、斜生栅藻单独生长时藻的总量具有有限增长特点的基础上,考虑到共存条件下两种藻的相互作用,以及在岩兰草油抑制环境下两种藻的相互作用,在传统的Logistic模型的基础上,增加了岩兰草油抑制条件下铜绿微囊藻与斜生栅藻彼此竞争的作用项,以及岩兰草油对铜绿微囊藻以及斜生栅藻的抑制项。
根据1 mL/L岩兰草油对铜绿微囊藻与斜生栅藻共存时的实验数据,拟合出1 mL/L岩兰草油对铜绿微囊藻与斜生栅藻共存时的抑制模型为:
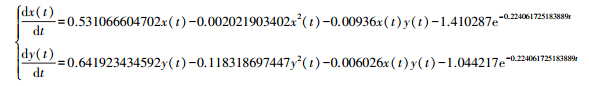
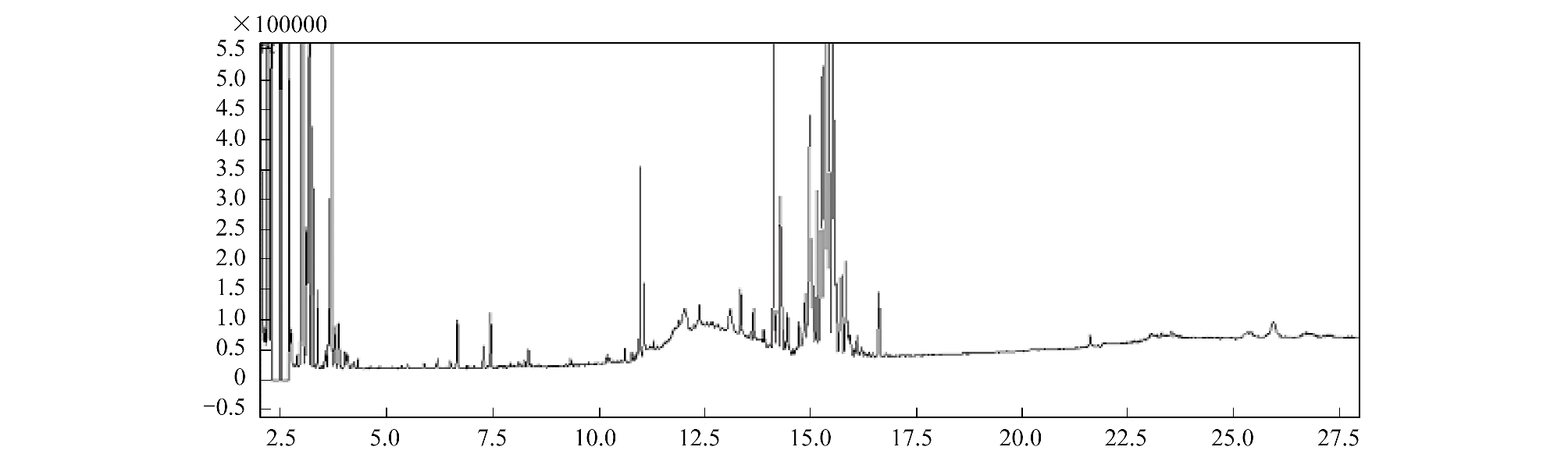
通过GC-MS分析鉴定出岩兰草油中的主要化学成分为8种含量较高的倍半萜烯类物质(图 3,图 4),此外还有醇和酮,分别为1-环己基-丁酮、松油醇、雪松醇、花侧柏烯、α-花柏烯、δ-杜松萜烯、α-芳姜黄烯、β-雪松烯。萜类化感物质是第二大类化感物质,具有很强的化感作用,很多萜类物质具有非常好的抑藻效果[10, 11]。
|
| 图 3 岩兰草油总离子流程图 Fig. 3 Total ionization chromatograph of vetiver oil |
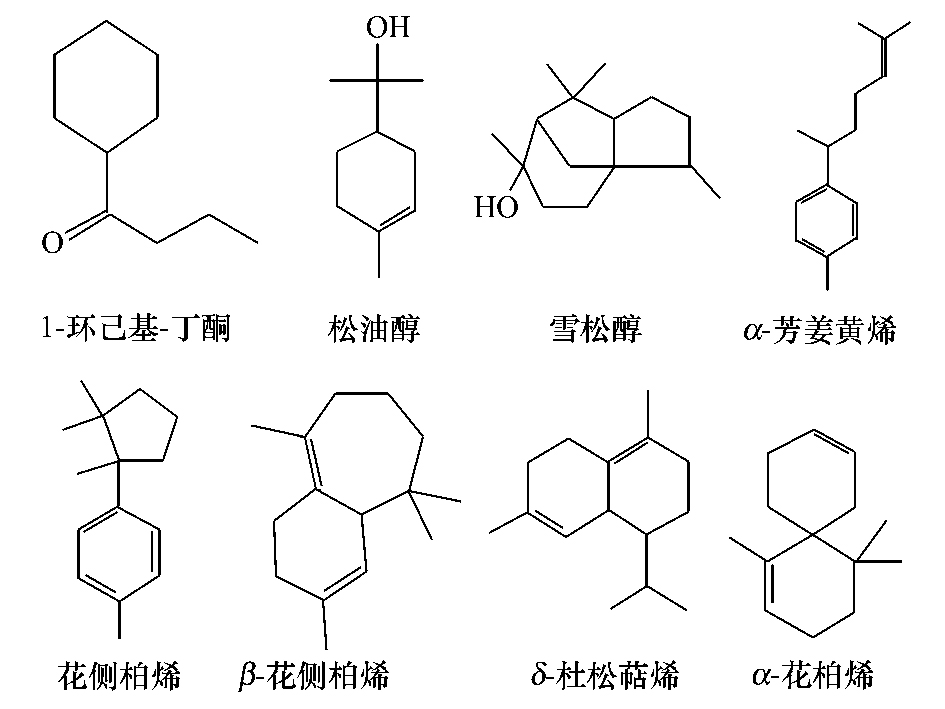
|
| 图 4 岩兰草油中几种主要化感物质 Fig. 4 Several primary chemical substance in vetiver oil |
高等水生植物的化感作用普遍存在于自然界中,但作用效果不尽相同,可解释为不同的植物对另外一种植物有不同的化感作用强度,也可能为同一种植物对不同植物有不同的作用效果。在利用高等水生植物抑藻的研究中,许多结论证明了将水生植物中的有效成分提取出来后,有很好的抑藻效果。如Zhang等[12, 13]分离了普生轮藻以及窄叶香蒲中的化感物质,鉴定了其主要成分分别为脂肪酸类以及酚酸类化感物质,并证明了其对铜绿微囊藻的强烈化感抑制作用;胡光济等使用菖蒲干体提取液对铜绿微囊藻和蛋白核小球藻进行抑藻研究,发现在相同提取液浓度下,铜绿微囊藻受到的抑制作用比蛋白核小球藻明显[14]。这些证据不仅证明了水生植物抑藻的有效性,同时也发现了水生植物的化感作用具有选择性。
本实验结果表明,高等两栖植物岩兰草的提取物岩兰草油对铜绿微囊藻和斜生栅藻均具有良好的抑制效应,而且对铜绿微囊藻的抑制效果要明显好于对斜生栅藻,这个现象再次证明了水生植物化感作用的选择性,而这种选择性在实际中具有很可观的应用价值。同时,在单独抑藻实验的基础上,本实验还开展了对共培养状态下的抑藻研究。结果表明,对照组的共培养体系中,铜绿微囊藻占据种群优势,斜生栅藻的细胞数量较低,这与天然水体铜绿微囊藻占据优势可能具有某些相似的机制;而在岩兰草油的作用下,因化感物质抑藻具有选择性,斜生栅藻至作用第6天时占据优势,进一步说明岩兰草油对铜绿微囊藻的抑制作用强于对斜生栅藻,这在普遍存在的以铜绿微囊藻为绝对优势种群的实际水体的应用具有一定的可行性。
岩兰草油对铜绿微囊藻和斜生栅藻共培养时的抑藻模型是根据实验室特定条件下的试验结果建立起来的藻类生长动力学模型,是对化感物质抑藻的一种定量分析以及对复合化感物质对混合藻类抑藻过程的简化、理想化后建立起来的,具有一定的通用性和精确性。然而所构建的模型所包含的因子还不丰富,还有一些因素被忽略、简化,如真实水体中藻类生长会受到营养盐浓度、温度、水动力条件等因素的影响,这些尚需在以后的研究中逐一论证,因此该模型的通用性和精确性是相对的和近似的,要将该模型应用于真正的生态系统中,还需要进一步的验证、分析以及综合讨论。
另外,在本研究过程中,曾将岩兰草油通过不同有机溶剂进行进一步的纯化,发现纯化后的岩兰草油抑藻效果反而较纯化前差,这提示岩兰草油的抑藻作用可能是其复合化感物质起协同抑制作用的结果。岩兰草油GC-MS分析表明,其主要成分为萜类物质。根据岩兰草油主要化感物质的结构(大多具有双键,尤其是有些还具有共轭双键)以及实验现象推测岩兰草油抑藻的机制可能涉及到叶绿素的破坏、自由基的产生以及细胞结构的改变等[15, 16],具体将有待进一步深入研究。
4 结论(1) 岩兰草油具有良好的抑藻效果 岩兰草油对铜绿微囊藻和斜生栅藻在单独和共培养状态下均有良好的抑制作用,对单独培养的铜绿微囊藻和斜生栅藻抑制作用的EC50分别为0.20和0.30 mL/L,表明岩兰草油对铜绿微囊藻的抑制效果明显好于对斜生栅藻。
(2) 岩兰草油的主要成分为倍半萜类物质 如1-环己基-丁酮、松油醇、雪松醇、花侧柏烯、α-花柏烯、δ-杜松萜烯、α-芳姜黄烯、β-雪松烯等。在化感作用研究中,萜类物质是重要的化感物质,对于这几种萜类物质各自化感抑藻作用强度及其机制将在后续进一步进行研究。
(3) 所建立的岩兰草油对两藻共培养状态下抑制作用的数学模型可以求出在任何时间节点上铜绿微囊藻和斜生栅藻的种群密度以及要达到抑藻最佳状态的岩兰草油浓度,具有一定的通用性和精确性。
| [1] | Hu H Y, Men Y J, Li F M. Research progress on phyto-allelopathic algae control. Ecology and Environment, 2006, 15(1): 153-157. |
| [2] | Vyvyan J R. Allelochemicals as leads for new herbicides and agrochemicals. Tetrahedron, 2002, 58(9): 1631-1646. |
| [3] | Truong P, McDowell M, Christiansen I. Stiff grass barrier with vetiver grass-a new approach to erosion and sediment control in Australia//Hunter H M, Eyles A G, Rayment G E, eds. Downstream Effects of Land Use. Queensland, Australia: Department of Natural Resources, 1995: 301-304. |
| [4] | Chen H M, Zheng C R, Tu C, Shen Z G. Chemical methods and phytoremediation of soil contaminated with heavy metals. Chemosphere, 2000, 41(1/2): 229-234. |
| [5] | Angin I, Turan M, Ketterings Q M, Cakici A. Humic acid addition enhances B and Pb phytoextraction by Vetiver grass (Vetiveria zizanioides (L.) Nash). Water, Air, & Soil Pollution, 2008, 188(1/4): 335-343. |
| [6] | Srivastava J, Chandra H, Singh N. Allelopathic response of Vetiveria zizanioides (L.) Nash on members of the family Enterobacteriaceae and Pseudomonas spp. The Environmentalist, 2007, 27(2): 253-260. |
| [7] | Srivastava J, Kayastha S, Jamil S, Srivastava V. Environmental perspectives of Vetiveria zizanioides (L.) Nash. Acta Physiologiae Plantarum, 2008, 30(4): 413-417. |
| [8] | 何宗祥, 张庭廷. 四种十八碳脂肪酸抑藻时-效关系分析的数学模型设计.生态学报, 2011,31 (23):7235-7243. |
| [9] | 何宗祥, 张庭廷. 两种化感物质联合抑藻的模型建立及数学最优化. 环境科学学报, 2012, 32(8): 1894-1901. |
| [10] | Liza López M, Bonzani N E, Zygadlo J A. Allelopathic potential of Tagetes minuta terpenes by a chemical, anatomical and phytotoxic approach. Biochemical Systematics and Ecology, 2008, 36(12): 882-890. |
| [11] | Kato-Noguchi H. Rice allelopathy and momilactone. Pakistan Journal of Weed Science Research, 2012, 18(Special): 289-296. |
| [12] | Zhang T T, He M, Nie L W. Allelopathic effects of submerged macrophyte Chara vulgaris on toxic Microcystis aeruginosa. Allelopathy Journal, 2009, 23(2): 391-402. |
| [13] | Zhang T T, Hu W, Zhang D. Allelopathic effect of Typha angustifolia L. on phytoplankton. Advanced Materials Research, 2012, 383-390: 3724-3728. |
| [14] | 胡光济, 张维昊, 尚吟竹, 何流. 菖蒲干体提取液对两种水华藻类生长的影响. 应用生态学报, 2009, 20(9): 2277-2282. |
| [15] | Zhang T T, Zheng C Y, Hu W, Xu W W, Wang H F. The allelopathy and allelopathic mechanism of phenolic acids on toxic Microcystis aeruginosa. Journal of Applied Phycology, 2010, 22(1): 71-77. |
| [16] | Zhang T T, Wang L L, He Z X, Zhang D. Growth inhibition and biochemical changes of cyanobacteria induced by emergent macrophyte Thalia dealbata roots. Biochemical Systematics and Ecology, 2011, 39(2): 88-94. |
 2015, Vol. 35
2015, Vol. 35




