文章信息
- 王万贤, 柯文山, 吴明煜, 孙启祥, 彭镇华, 尹蔚琳, 张倩
- WANG Wanxian, KE Wenshan, WU Mingyu, SUN Qixiang, PENG Zhenhua, YIN Weilin, ZHANG Qian
- 樟树水浸液对钉螺的生态毒理学效应
- Ecotoxicological effects of water extract of Cinnamomum camphora on oncomelania hupensis
- 生态学报, 2015, 35(3): 919-925
- Acta Ecologica Sinica, 2015, 35(3): 919-925
- http://dx.doi.org/10.5846/stxb201305111016
-
文章历史
- 收稿日期:2013-05-11
- 网络出版日期:2014-07-07
2. 中国林业科学研究院, 北京 100091
2. Research Institute of Forestry, Chinese Academy of Forestry, Beijing 100091, China
血吸虫病(Schistosomiasis)是严重危害人民身体健康的疾病,而钉螺(Oncomelania hupensis Gredler)是日本血吸虫(Schistosoma japonicum Katsurade)的唯一中间寄主,是血吸虫病传播中不可缺少的环节[1, 2]。血吸虫的毛蚴在钉螺内成千上万倍的急剧增殖,不断逸出尾蚴于水中感染人体和其它动物,致使血吸虫病蔓延传播[3]。另一方面,钉螺也是血吸虫生活周期中最脆弱的一环,灭螺能有效地控制和减少血吸虫病的传播[4]。近半个世纪以来,灭螺措施倍受重视[5, 6, 7],成为控制血吸虫病的重心。传统的灭螺方法主要是物理和化学方法[8],物理方法工程浩大难彻底;化学药物灭螺效果虽好,但污染环境。“兴林灭螺”模式的提出,为有效灭螺提供了一条新的途径,如果选用对钉螺有毒害作用的植物造林,创建一个钉螺无法生存的生态环境,则能一劳永逸达到控制的目的。在调查中发现,樟树(Cinnamomum camphora (L.)Presl)在武汉东湖、沙湖及池塘边、沟渠旁等湿润的地方也能生长得很好,尤其是在每年的3—4月份开花和长出新叶时,其上的老叶纷纷飘落于地面,此时也正是灭螺的最宜时机,休眠了一个冬季的钉螺开始出土活动和交配繁殖。樟树为传统优良常绿绿化树种,还有杀虫、灭菌的效果。鉴于以上原因我们拟采用樟树各部分新鲜材料水浸液进行灭螺实验,并对钉螺生理生化作用进行分析,探讨樟树灭螺的可能性及其作用生理生化机制,旨在为生态工程灭螺提供依据。
1 材料和方法 1.1 实验材料实验用樟树的根皮、茎皮、叶采自湖北大学校园沙湖及池塘边,沟渠旁;钉螺采自湖南省洞庭湖。采集的钉螺于实验室23℃温室饲养,选取7—8旋成螺,逸幼法剔去阳性螺(将钉螺放入盛有去氯清水(自来水放置1周)的小烧杯中,冲洗干净并静置2 h后,如有血吸虫尾蚴溢出,则剔除),于无氯清水中喂养备用。
1.2 灭螺活性的测定实验采用浸泡法。将采到的樟树根皮、茎皮、叶清洗,切碎,按相当于干重的比例浸入适量的无氯清水中,分别配成1%、0.5%、0.1%、0.05% 4个不同浓度梯度的处理溶液。选取健康钉螺100只为1组,每20个装入一个尼龙网袋中,分别将各组(5袋/组)钉螺浸入盛有2000 mL不同浓度的樟树根皮、茎皮、叶水溶液的玻璃缸中,另设1 mg/L氯硝柳胺水溶液处理和无氯清水饲养为对照。实验在温度控制在(23±1)℃条件下进行。分别于处理24、48、72、96、120 h后,将各处理中的钉螺随机取出1袋,用无氯水冲洗数次,再放入清水中静置24h,然后作存活检查,开厣爬行者为活螺,余下的用敲碎和解剖卸刺的方法,鉴别死活。实验重复3次,取其平均值作为实验结果。
1.3 CAT和POD活性测定粗酶液的制备,分别随机选取各处理浓度下的钉螺,用预冷的生理盐水漂洗后,吸水纸吸干,敲碎螺壳,取出肝脏组织,分别加按照重量 ∶ 体积=1 ∶ 9加预冷的0.86%的生理盐水,用研钵在冰浴下充分匀浆,0—4 ℃条件下4000 r/min离心20 min,上清液在4 ℃下保存待测。
酶活测定,本实验过氧化氢酶(CAT)的活力测定采用可见光分光光度法,过氧化物酶(POD)活性测定采用愈创木酚法,组织蛋白测定采用考马斯亮蓝方法。CAT、POD和考马斯亮蓝测定蛋白质试剂盒购自南京建成生物工程研究所,其测定原理和方法见试剂盒说明。
粗酶液中CAT酶活力的计算:
粗酶液中CAT活力(U/mg蛋白)=(对照管吸光度值-测定管吸光度值)×271÷(60×取样量)/待测样品蛋白含量(mg蛋白/mL)。
POD以用每min内A470变化0.01为1个过氧化物酶活性单位(U)表示。
POD活力(U/mg蛋白)△A470=对照管吸光度值-测定管吸光度值
1.4 同工酶电泳将浓度为0.5% 的樟树新鲜叶水浸液处理不同天数的钉螺样品取出,并用无氯清水漂洗干净,吸干水分,敲碎螺壳,取出整个软体组织,分别加0.2 mol/L pH7.4的磷酸缓冲液﹝10﹞,冰浴匀浆。匀浆液0℃ 8000 r/min冷冻离心,上清液与溴酚蓝指示剂等量混合后作为电泳样品,零下20摄氏度的冰箱保存备用。正常饲养螺作为对照组。
采用聚丙烯酰胺凝胶电泳(PAGE)。使用Hoefer SE600垂直板电泳仪,所有电泳及染色药品均为亚法公司进口分装。贮液配制参照B. D. Hames和D. Rickwood等以及Hoefer公司电泳指南,样品分离胶浓度7.5%,浓缩胶3%。采用Tris-Gly高pH不连续缓冲系统(7.5%分离胶-3%浓缩胶),板距1 mm,板胶16 mm x17 mm。每槽加样15 μL,加1滴0.2%的溴酚蓝作为指示剂,恒流20 mA,22℃条件下电泳,待溴酚蓝泳动到凝胶板下端1 cm处停止电泳。染色,冲洗,固定,拍照。
1.5 樟树水浸液对钉螺肝脏损伤的透射电镜观察分别取清水饲养(以下简称对照)、0.5%的樟树叶水浸液处理48、96 h的钉螺的肝脏部分作切片。将钉螺肝脏用刀片切成1 mm3的小块放于4 ℃预冷的2.5%戊二醛中前固定2 h,再经1%锇酸后固定2 h,逐级酒精及丙酮脱水。1 ∶ 1纯丙酮与618环氧树脂包埋液室温浸透2—3 h,纯包埋液浸透2—3 h,37 ℃→45 ℃→60 ℃聚合36 h。将制作的切片在透射电镜下观察拍照。实验过程在武汉大学医学部电子显微镜室完成。
1.6 数据统计实验每处理重复3次,取平均值,数据统计采用Excel数据分析中的t检验(P <0.05)。
2 结果与分析 2 2.1 樟树根皮、茎皮、叶水浸液灭螺活性初试结果与分析樟树根皮、茎皮、叶水浸液不同浓度、不同时间处理后,钉螺死亡率存在差异。其规律是随处理浓度和处理时间的增加,钉螺死亡率呈上升趋势。0.5%—1.0% 以上的樟树根皮、茎皮、叶水浸液均可达到100%的明显毒杀钉螺致死效果(表 1)。
| 项目 Items | 处理液浓度 Concentration/% | 钉螺死亡率The mortality/% | ||||
| 24 h | 48 h | 72 h | 96 h | 120 h | ||
| 叶 | 1.00 | 35±5 | 58.33±5.3 | 91.66±3.3 | 95±1 | 100±0 |
| Leaf | 0.50 | 30±3 | 35±4 | 55±3 | 75±2 | 90±2 |
| 0.10 | 10±2 | 25±3 | 25±3 | 60±3 | 85±3 | |
| 0.05 | 0 | 5±1 | 5±1 | 25±2 | 45±2 | |
| 茎皮 | 1.00 | 60±4 | 75±6 | 90±4 | 100±0 | 100±0 |
| Bark of stem | 0.50 | 35±3 | 50±4 | 80±3 | 92.5±2.5 | 100±0 |
| 0.10 | 20±2 | 30±3 | 60±3 | 75±2 | 91.66±2.6 | |
| 0.05 | 5±1 | 10±2 | 25±2 | 35±3 | 50±2 | |
| 根皮 | 1.00 | 55±5 | 80±6 | 100±0 | 100±0 | 100±0 |
| Bark of root | 0.50 | 45±3 | 70±6 | 95±6 | 100±0 | 100±0 |
| 0.10 | 40±3 | 55±3 | 85±4 | 90±2 | 95±3 | |
| 0.05 | 15±2 | 35±2 | 45±2 | 60±3 | 65±4 | |
| 樟树下凋落物 | 1.00 | 10±2 | 25±3 | 35±3 | 65±4 | 80±2 |
| Withered branches | 0.50 | 7.5±1.5 | 20±2 | 30±2 | 55±3 | 68.3±3.3 |
| and leaves | 0.10 | 5.5±1 | 10±2 | 15±2 | 35±4 | 41.7±2 |
| 0.05 | 0 | 5±1 | 12.5±1 | 25±2 | 35±1 | |
| 氯硝柳胺 Niclosamidum | 1 mg/L | 90±3 | 95±3 | 100±0 | 100±0 | 100±0 |
| 清水对照Water | 0 | 0 | 0 | 0 | 1.7±1 | 1.7±1 |
樟树凋落叶水浸液的灭螺效果(表 1)与新鲜叶的灭螺效果表现出极为相似的规律性,但其灭螺效果明显低于新鲜叶:如1.0%浓度凋落叶水浸液处理钉螺120 h后钉螺死亡率才达到80%,而同浓度新鲜叶处理72 h后则可达91.7%,原因可能是凋落叶的一部分灭螺活性成分已经被酶或微生物降解。但是,樟树在每年的3—4月份在钉螺出土活动和交配繁殖时集中落叶于地面,高浓度的樟树凋落叶水浸液也许会有比新鲜叶更理想的灭螺效果。
氯硝柳胺是普遍使用的化学灭螺剂。将樟树根皮、茎皮、叶水浸液的灭螺效果与之对照,可知0.5—1.0% 以上的樟树根皮、茎皮、叶水浸液均可达到100%的明显毒杀钉螺致死效果,与1 mg/L氯硝柳胺溶液的灭螺效果相当。不过樟树根皮、茎皮、叶水浸液的毒效较氯硝柳胺略慢。用1 mg/L氯硝柳胺溶液处理钉螺48—72 h可达100%的死亡率,而用0.5—1.0% 以上的樟树根皮、茎皮、叶水浸液水溶液处理需要72—120 h才能达到同样的效果(表 1)。
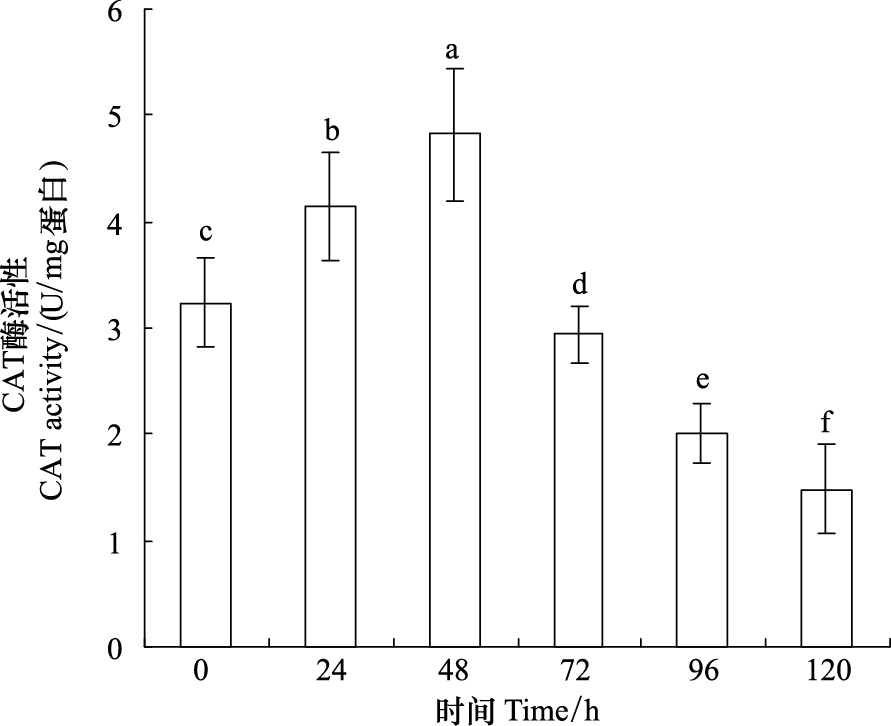
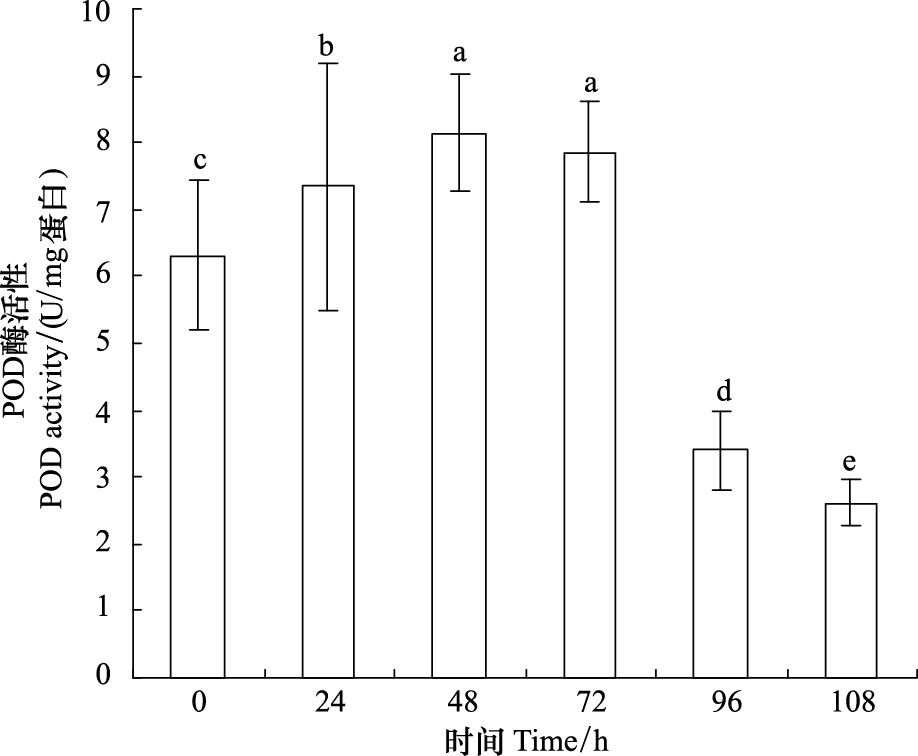
2.2 樟树叶水浸对钉螺过氧化氢酶和过氧化物酶活性影响过氧化氢酶和过氧化物酶是过氧化物酶体主要酶类,且过氧化物酶体的标志酶是过氧化氢酶,是钉螺体内防止过氧化物毒害的主要酶类。本实验中,过氧化氢酶(图 1)在处理的48 h内,过氧化物酶(图 2)在处理的72 h内,其活性明显增加,表明其处理过氧化损伤能力增强。但随处理时间的延长,其活性明显降低,表明清除能力降低。
|
| 图 1 0.5%樟树叶水浸液处理不同时间CAT (Catalase) 酶活性 Fig. 1 CAT (Catalase) activity of Oncomelania hupensis live treated by 0.5% leaf water extract from Cinnamomum camphora 不同字母表示显著差异(P < 0.05) |
|
| 图 2 0.5%樟树叶水浸液处理不同时间POD (Peroxidase) 酶活性 Fig. 2 POD (Peroxidase) activity of Oncomelania hupensis live treated by 0.5% leaf water extract from Cinnamomum camphora |
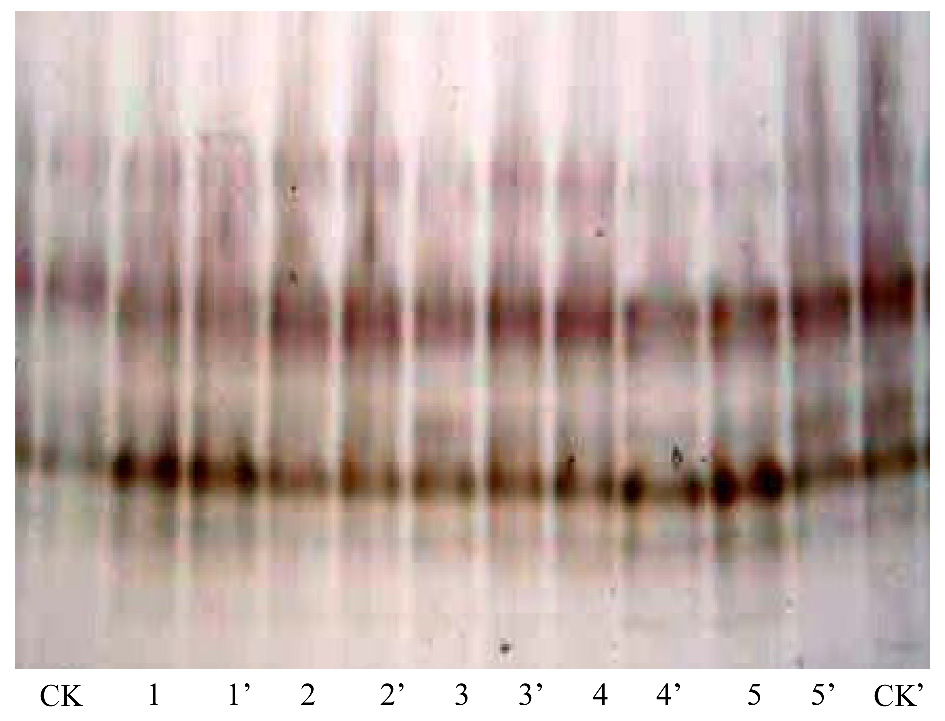
采用聚丙稀酰胺电泳技术分离经0.5% 樟树新鲜叶水浸液处理不同天数的钉螺样品的过氧化物酶同工酶(图 3)。未做酶谱的薄层扫描,但从带谱消失或新带出现及凝胶显色颜色的深浅或宽度,可以大致判断过氧化物酶带谱在不同处理时间后的变化情况及其活性强弱。
|
| 图 3 0.5% 樟树新鲜叶水浸液处理1—5 d钉螺的过氧化物酶同工酶图谱 Fig. 3 POD Isozyme Profiles of liver treated by 0.5% water lixivium of leaf of C. camphora *CK,CK′:对照样品;1,1′: 0.5% 樟树新鲜叶水浸液处理24 h钉螺的样品;2,2′:处理48 h钉螺的样品;3,3′:液处理72 h钉螺的样品;4,4′:处理96 h钉螺的样品;5,5′:处理120 h钉螺的样品;图上为正极,下方为负极 |
虽然图不是很清楚看出带谱,但在电泳胶图中可见其:清水对照共有12条谱带,樟树水浸液处理后的前3d的谱带数均为11条,比对照少一条,但是处理24 h后的酶的活性比对照增强,第48—72小时酶的活性增强地更加明显,96 h酶带数增加一条,但是酶的活性开始下降,120 h的酶带数与72 h相比减少1条,而96 h刚增加的新酶带120 h又消失了,酶的活性继续下降,酶带的变化也主要是在正极区,处理的72 h,由于樟树水浸液中的灭螺活性物质刺激钉螺,钉螺中毒后发生应激反应,所以酶的活性不断上升,96 h由于中毒太深,酶最终被破坏,所以酶的活性下降,而酶带的增减可能也是应激反应所致。这与正常的病理反应完全一致。
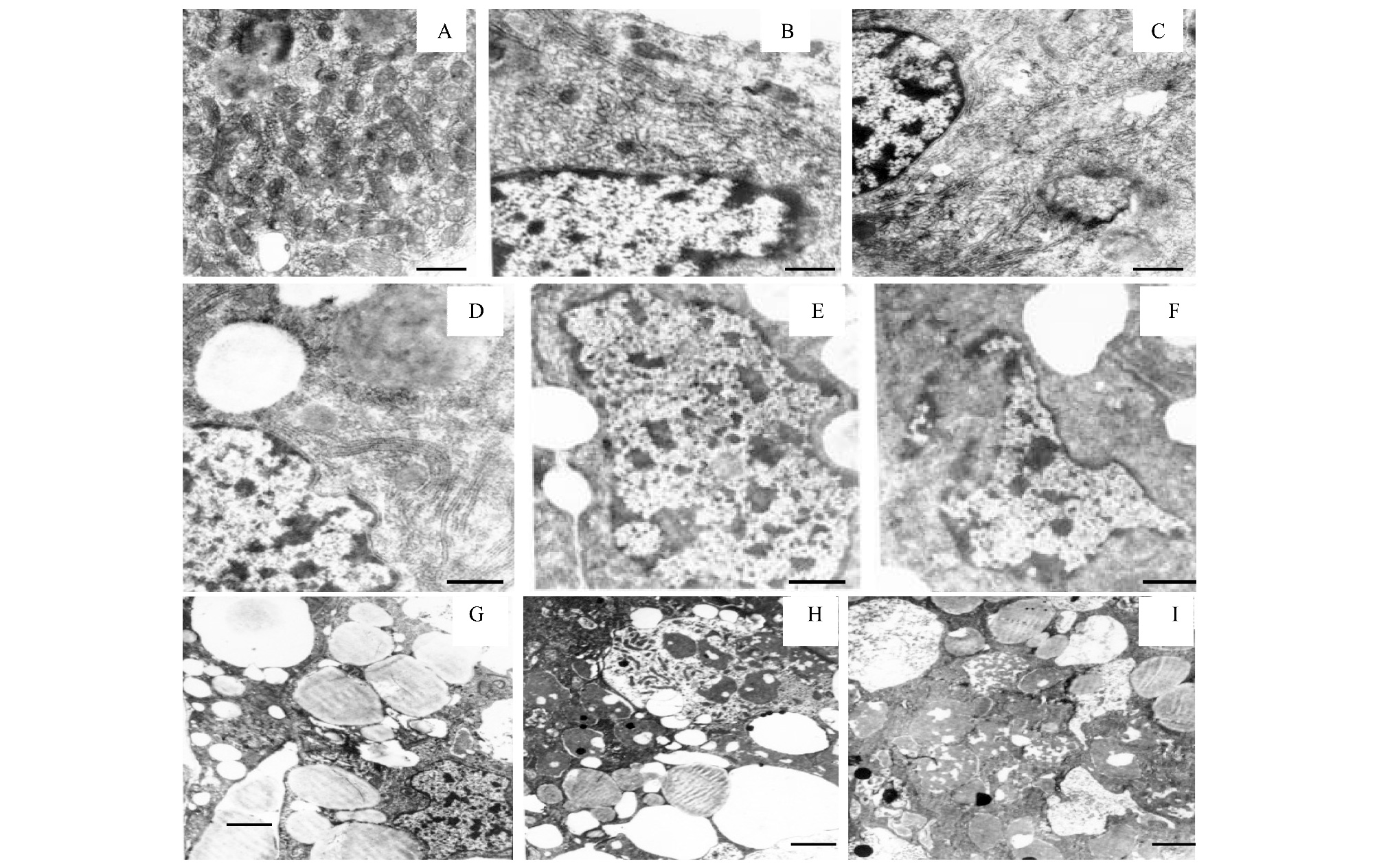
2.4 樟树水浸液对钉螺肝脏损伤的透射电镜观察从图 4结果可知:对照组(图 4A—C)钉螺肝脏细胞的细胞核完整,粗面型内质网整齐排列在细胞核的周围,细胞质中清晰可见高尔基体、溶酶体等细胞器分布,线粒体大量聚集,数量多;处理48 h(图 4D—F)后,其细胞核轻度肿胀甚至核膜破损,染色质疏松,线粒体数目减少、凝聚或破裂,粗面内质网腔扩大或破损、呈片段状散在性分布,胞质稀疏,同时出现少量的致密体,高尔基体等细胞器的结构不完整;处理96 h后(图 4G—I),细胞核溶解破碎,仅有少量凝集融合的染色体斑块,细胞器出现空泡样变性,线粒体嵴模糊,大量的致密体及形状、大小不等的空泡充满了整个细胞,胞膜不完整。
|
| 图 4 0.5%樟树叶水浸液处理钉螺肝脏投射电镜图 (TEM) Fig. 4 TEM ultrastracture of O. hupensi′s liver treated by 0.5% leaf water extract from C. camphora Bar=30 μm; A—C 为对照处理,显示正常细胞的细胞器亚显微结构;D—F 显示钉螺处理24h后肝细胞结构损伤;G—I 显示钉螺处理96h后肝细胞结构损伤 |
樟树植物各部的新鲜材料水浸液对钉螺都具有较强的杀螺作用,其中根皮效果最好,1%浓度处理72 h钉螺死亡率达100%,其次为茎皮和叶。樟树含生物碱、萜类、樟脑、挥发油等多种活性成分,刘颖芳[9]曾用对樟树不同有机溶剂提取物进行杀螺效果试验,证明均具有杀螺活性,表明樟树杀螺可能为多种有效成分的综合作用;但具体是何种活性成分对钉螺最强有待进一步研究。樟树凋落叶和新鲜叶水浸液的灭螺效果表现出相同的浓度和时间效应:随处理浓度的增加和时间的延长,钉螺死亡率呈上升趋势;但凋落叶的灭螺效果明显低于新鲜叶(表 1),原因可能是凋落叶的一部分灭螺活性成分已经被酶或微生物降解。然而,樟树落叶在每年的3—4月份,这个时间段正好是钉螺在休眠了一个冬季后,开始出土活动和交配繁殖集中的时间段,也是钉螺脆弱的时候,正是灭螺的最佳时机,大量的落叶水浸后形成高浓度水浸液,也许会有比新鲜叶更理想的灭螺效果。
过氧化物酶体在动物广泛存在,尤其肝脏,其含有丰富的酶类,主要是氧化酶,如过氧化氢酶和过氧化物酶,且过氧化氢酶是其标志酶,它的作用主要是将过氧化氢(H2O2)水解。肝脏是解毒器官,外源毒物进入钉螺肝脏,其中毒害机制可能会引起过氧化损伤,如产生过氧化氢(H2O2)是氧化酶催化的氧化还原反应中产生的细胞毒性物质。 过氧化氢酶利用过氧化氢氧化各种底物,氧化的结果使这些有毒性的物质变成无毒性的物质,同时也使H2O2进一步转变成无毒的H2O。这种解毒作用对于肝、肾的保护作用特别重要。从实验结果看,过氧化氢酶(图 1)在樟树叶水浸液处理的48 h内、过氧化物酶(图 2)在72 h内,其活性明显增强,表明水浸液成分引起的过氧化在增加,钉螺此时的具有明显的解毒作用;但随着处理时间的延长,CAT和POD活性明显降低,表明其解毒能力在降低,外源毒物引起的过氧化物在积累、过氧化损伤在增加。随着有毒物的进一步积累、过氧化损伤进一步增加,钉螺解毒能力逐渐消失,这可能是导致钉螺死亡重要原因之一。从过氧化物酶同工酶没谱变化(过氧化氢酶同工酶因条带不清晰,未能在本文显示),也可看出随处理时间的延长,其部分酶带减弱甚至消失,也表明钉螺解毒能力的减弱和可能的过氧化损伤。
透射电镜结果表明,钉螺肝脏随樟树叶水浸液处理时间的延长,其线粒体、内质网、细胞核的细胞器破损程度越来越严重,进一步说明樟树叶水浸液毒性成分对钉螺肝脏的损伤。
当前国内外通常采用化学药物灭螺[10, 11]。但化学灭螺剂污染环境[12];物理控制也是经常采用的,但其工程浩大很难一次彻底[13]。可以设想:在钉螺孳生的江滩、湖洲及沟渠两旁选用对钉螺有强他感作用的植物造林,创建一个钉螺难以生存繁衍的生态环境,不需年年施用灭螺药物,即使有流水携螺而至,也能随来随灭,便可一劳永逸地达到杀灭钉螺的目的。且抑螺林的构建费工耗资不多,也不污染环境,还具有防风浪,护堤坡及材用,绿化等多种综合效益。樟树为多年生的常绿植物,生态适应能力强,在武汉东湖、沙湖及池塘边,沟渠旁等湿润的地方也能生长得很好,是构建人工生态防护林的理想树种。
| [1] | 王万贤, 杨毅, 柯文山, 刘幼琪, 马安宁, 杨文业. 枫杨水浸液灭螺实验研究. 应用生态学报, 1999, 10(4): 478-480. |
| [2] | 张旭东, 杨晓春, 彭镇华. 钉螺分布与滩地环境因子的关系. 生态学报, 1999, 19(2): 265-269. |
| [3] | Marston P, Hostettmann K. Review article number 6: Plant molluscicides. Phytochemistry, 1985, 24(4): 639-652. |
| [4] | Barbosa F S. Determination and control of schistosomiasis. Memórias do Instituto Oswaldo Cruz, 1995, 90(2): 155-159. |
| [5] | Perrett S, Whitfield P J. Currently available molluscicides. Parasitology Today, 1996, 12(4): 156-159. |
| [6] | Souza C P. Molluscicide control of snail vectors of schistosomiasis. Memórias do Instituto Oswaldo Cruz, 1995, 90(2): 165-168. |
| [7] | Archibald R G. The use of the fruit of the tree Balanites aegyptaca in the control of schistosomiasis in the Sudan. Transactions of the Royal Society Medicine and Hygiene, 1933, 27: 207-211. |
| [8] | 杨毅, 柯文山, 王万贤, 马安宁, 陈全胜. 夹竹桃灭钉螺效果初报. 应用生态学报, 2000, 11(6): 959-960. |
| [9] | 刘颖芳. 樟树和夹竹桃灭螺活性成分的提取和杀螺效应分析 [D]. 武汉: 湖北大学, 2006. |
| [10] | Guo Y H. Plant molluscoide studies in the People's Republic of China//Mott K E. Plant Molluscoides. A Willy Medical Publication, 1987: 289-298. |
| [11] | Dias L C S, Maecal Junior O, Glasser C M. Control of Schistosomiasis transmission. Memórias do Instituto Oswaldo Cruz, 1995, 90(2): 285-288. |
| [12] | 刘月英. 关于我国钉螺的分类问题. 动物学报, 1974, 20(3): 223-230. |
| [13] | 於凤安, 彭卫平, 彭镇华, 张家来, 刘立德, 彭旦明. 利用植物他感作用灭螺效果的研究. 应用生态学报, 1996, 7(4): 407-410. |
 2015, Vol. 35
2015, Vol. 35




