文章信息
- 张妤, 郭爱玲, 崔烨, 冯莉, 田兴山, 吴丹丹
- ZHANG Yu, GUO Ailing, CUI Ye, FENG Li, TIAN Xingshan, WU Dandan
- 培养条件下二氯喹啉酸对土壤微生物群落结构的影响
- Effect of quinclorac on soil microbial community structure under culture conditions
- 生态学报, 2015, 35(3): 849-857
- Acta Ecologica Sinica, 2015, 35(3): 849-857
- http://dx.doi.org/10.5846/stxb201304150707
-
文章历史
- 收稿日期:2013-04-15
- 网络出版日期:2014-04-03
2. 华中农业大学 食品科技学院, 武汉 430000
2. College of Food Science and Technology, Huazhong Agricultural University, Wuhan 430000, China
二氯喹啉酸属于喹啉羧酸类激素型选择性除草剂,可以有效的促进乙烯的生物合成,导致大量脱落酸的积累,使气孔缩小、水分蒸发减少、二氧化碳吸收减少、植物生长减慢[1],是我国稻田主要除草剂品种之一。近几年水田改旱田中除草剂残留药害逐年增加,二氯喹啉酸潜在的环境风险已受到广泛的关注。
土壤微生物是土壤生态系统的重要组成部分,参与土壤中几乎一切生物和生物化学反应,对保持土壤生态方面起着重要作用[2]。微生物在土壤中普遍存在,其对环境条件的变化反应敏捷而被认为是最有潜力的敏感性生物指标之一,也被推荐作为生态风险评估项目之一[3]。除草剂喷施农田之后,绝大部分洒落于土壤中,从而对土壤微生物产生影响[4]。到目前为止,已利用磷脂脂肪酸(Phospholipid Fatty Acid,PLFA)方法研究草甘膦、2,4-D和阿特拉津等除草剂使用对土壤微生物群落的影响。然而,用PLFA法研究二氯喹啉酸施用对土壤微生物群落影响的报道较少。为了探索二氯喹啉酸对农田土壤的影响,本文以淹水和不淹水两种水田土壤为例,研究了不同浓度二氯喹啉酸对两种土壤微生态环境的影响,旨在为科学合理使用二氯喹啉酸提供理论依据。
1 材料与方法 1.1 材料二氯喹啉酸,98%原药。
实验用土于2012年5月采自广东省农业科学院白云基地多年种植水稻的农田,取0—20 cm耕作层的土壤,混匀风干,过孔径为2 mm筛备用。试验前测定土壤的pH值为5.8,有机质为9.4 g/kg,水解性氮为59.3 mg/kg,有效磷为40.5 mg/kg,速效钾为44.5 mg/kg。
1.2 土壤预培养土壤预培养:定量取风干备用土壤,均匀喷洒蒸馏水,使土壤含水量约为15%,于25 ℃恒温培养箱中暗培养2周,稳定土壤微生物。
1.3 土壤处理土壤处理参照Petersen 等人的方法[5]。不淹水水田土壤处理:取2 kg预培养土,按照二氯喹啉酸的田间推荐使用剂量,将98%二氯喹啉酸原药用丙酮溶解并用蒸馏水稀释,均匀喷洒到预培土中混匀,使二氯喹啉酸处理土壤的剂量分别为83.3 μg/kg干土和166.6 μg/kg干土。对照土样加入等量的丙酮和蒸馏水。分别取不同处理的土样80 g分装至玻璃管中,用透气性封口膜封口,避免水分蒸发。淹水水田土壤处理:按照上述不淹水水田土壤处理的方法,处理后每只玻璃管加25 mL水,使管中土壤水层高度在3—5 cm,模拟淹水水田土壤,实验过程中,随时补水保持水层高度,以稳定和模拟淹水厌氧环境。
将分装土样的玻璃管置于PGX-45OPB-2型恒温培养箱中暗培养,控制培养温度为25 ℃,湿度为60%,分别于处理后第1、3、7、14、28、45、60 d取样,每次取土壤3管作为重复,样品在25 ℃空调风口下快速风干,并于-20 ℃冰箱中保存待测。
1.4 磷脂脂肪酸分析(PLFA)土壤磷脂脂肪酸的提取与纯化参考Zaady等人[6]和吴愉萍[7]的方法进行。(1)提取,称取样品2.00 g (干重)于玻璃管中,分别加入氯仿、甲醇、磷酸盐缓冲溶液4、8、3.6 mL,振荡2 h,2500 r/min 离心6 min。取上清液,沉淀再加入上述3种试剂一半的量,振摇1 h,离心,取上清液,合并2次上清液,加入3.6 mL磷酸盐缓冲液和4 mL氯仿,剧烈振荡,暗处静置过夜。收集下层氯仿相,氮气吹干。(2)分离,使用Supelclean Lc-Si小柱,用5 mL氯仿活化,5 mL氯仿溶解样品后注入小柱内,先后用10 mL氯仿、10 mL丙酮、10 mL甲醇洗脱,收集甲醇相,氮气吹干。(3)甲酯化,向上步样品中加入1 mL甲苯与甲醇的混合液(1 ∶ 1)和0.2 mol/L氢氧化钠的甲醇溶液,于35 ℃温育15—20 min,冷却至室温后,加入2 mL己烷与氯仿的混合液(4 ∶ 1)、0.3 mL 1 mol/L乙酸和2 mL超纯水,加盖振摇数秒,2500 r/min 离心5 min,收集上清液,向下层液中加入2 mL己烷与氯仿的混合液(4 ∶ 1),离心,合并2次上清液,氮气吹干,-20 ℃保存。
磷脂脂肪酸甲酯的测定采用气相色谱-串联质谱(Gas Chromatograph-Mass Spectrometer-computer,GC-MS)法测定。色谱柱SP-2560,100 m×0.25 mm,ID,0.20 μm,进样量1 mL,分流比100 ∶ 1,载气(氦气)流速20 cm/min。程序升温:初始温度140 ℃,维持5 min,然后以4 ℃/min的速度升温至240 ℃。以Supelco 37种磷脂脂肪酸甲酯混合标样作为外标物[8]。分析定量:收集扫描(SCAN)与提取离子(SIM)2种数据。SCAN图谱用于定性,SIM图用于定量。定量离子包括55、74.1、79、87,以响应值最高的为目标离子进行定量,峰面积通过计算机自动积分。
以总磷脂脂肪酸的量表示微生物群落的生物量;17种含有酯链与甘油相连的饱和或单不饱和脂肪酸(6 ∶ 0、11 ∶ 0、12 ∶ 0、13 ∶ 0、14 ∶ 0、14 ∶ 1、15 ∶ 0、15 ∶ 1、16 ∶ 0、16 ∶ 1、17 ∶ 0、17 ∶ 1、18 ∶ 0、20 ∶ 0、20 ∶ 1、22 ∶ 0、22 ∶ 1)表示细菌生物量;18 ∶ 1n9t、18 ∶ 1n9c、18 ∶ 2n6t、18 ∶ 2n6c、18 ∶ 3n6表示真菌生物量[8]。
1.5 数据分析数据为3次重复的平均数,以烘干土壤重计。采用Excel 2003和SPSS 18.0 对数据进行方差分析和主成分分析。
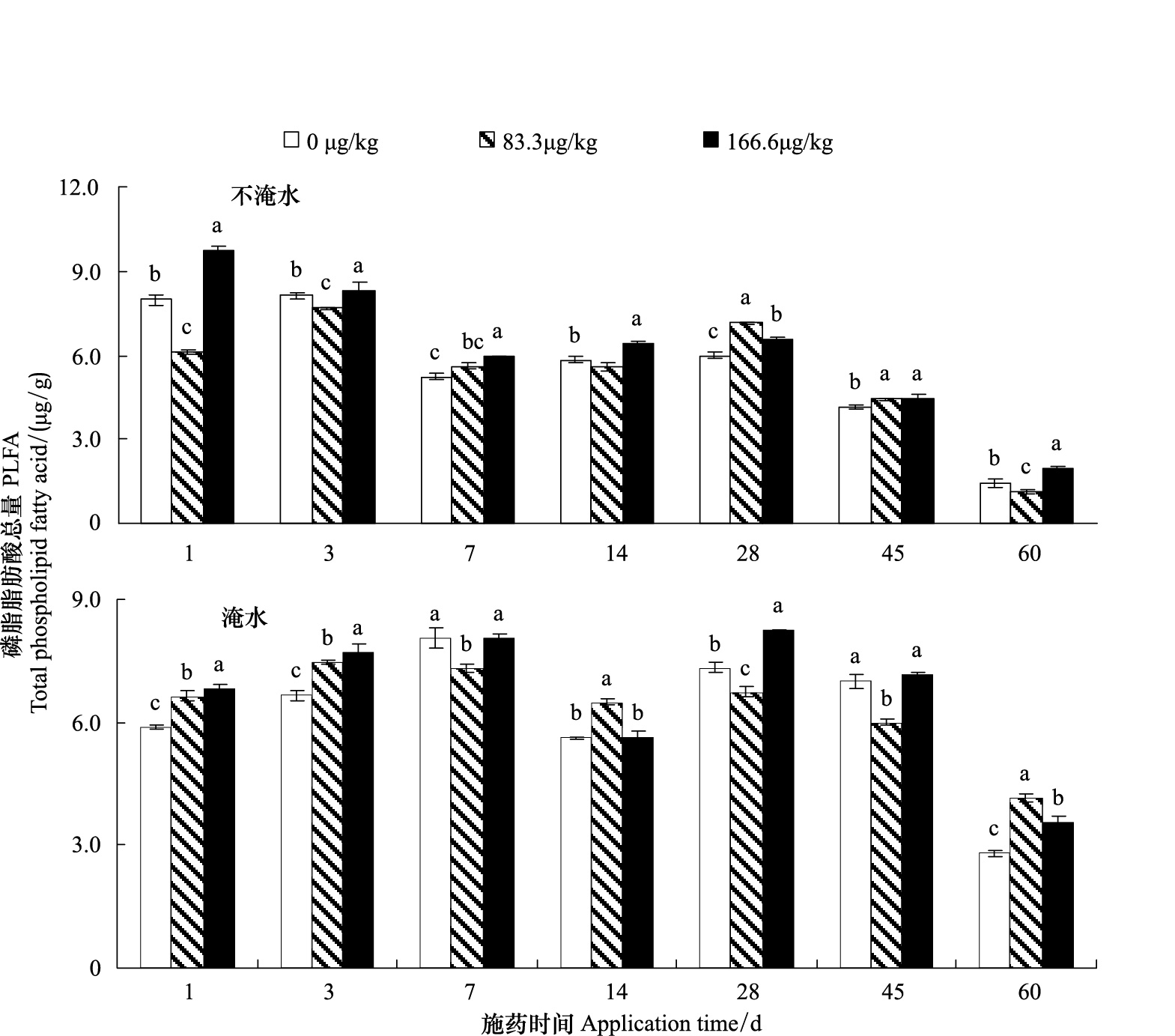
2 结果与分析 2.1 二氯喹啉酸对土壤微生物PLFA总量的影响二氯喹啉酸对土壤微生物总磷脂脂肪酸(PLFA)含量的影响随培养时间的变化趋势见图 1。在整个培养过程中,166.6 μg/kg二氯喹啉酸处理显著增加了不淹水和淹水水田土壤微生物总PLFA的含量,在实验中期,这种促进作用表现不明显;而83.3 μg/kg 二氯喹啉酸处理对土壤微生物总PLFA的影响呈波动状态,在不淹水水田土壤中,施药前期和后期会降低土壤微生物生物总量,使用中期会有提高作用,而淹水水田土壤中施药初期和后期对土壤微生物总生物量有促进,而中期则表现为抑制。说明不同浓度二氯喹啉酸处理对土壤微生物总PLFA的影响不相同。整体上看,高浓度农药比低浓度的对微生物生物量的促进作用更强,一些研究也表明除草剂增加了土壤微生物的生物量[9, 10]。
|
| 图 1 60 d培养期间土壤PLFA总量的变化 Fig. 1 The total soil PLFA changes during the incubation period 每个处理时间内相同字母表示差异不显著(p<0.05) |
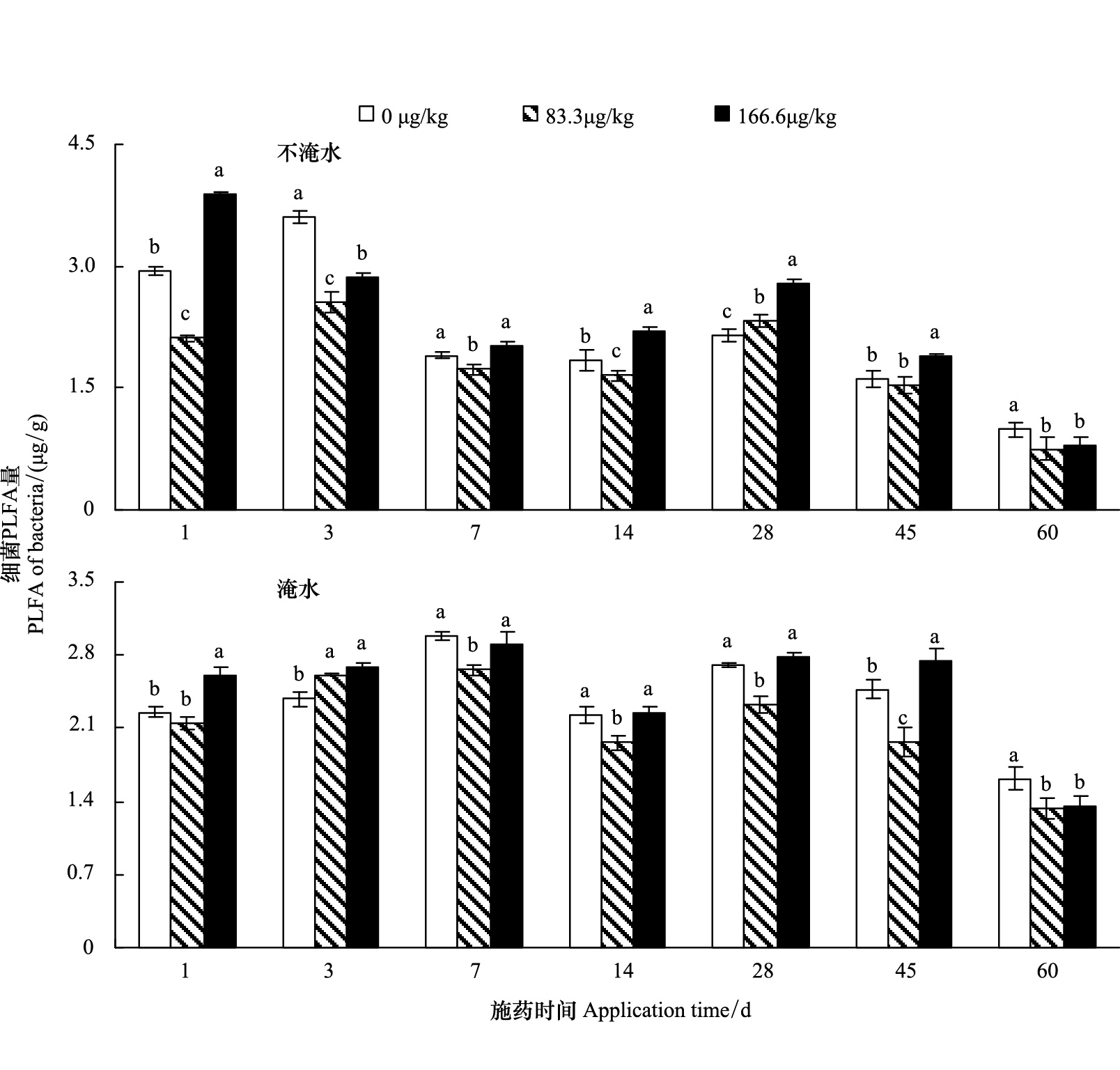
二氯喹啉酸对土壤细菌生物量的影响随培养时间的变化趋势见图 2。可以看出,在不淹水水田土壤中,二氯喹啉酸浓度较低时,在处理前期和后期会降低不淹水水田土壤细菌生物量,处理中期细菌生物量有增加,但这种增加并不显著;当二氯喹啉酸浓度较高时,其对土壤微生物总量的提高作用显著,这种促进作用在前期和中期较明显。在淹水培养中,二氯喹啉酸浓度较低时,降低淹水水田土壤细菌生物量;当二氯喹啉酸浓度较高时,其对淹水水田土壤细菌生物量的提高作用较明显,这种促进作用在施药后期逐渐消失。说明不同浓度二氯喹啉酸处理对淹水水田土壤细菌生物量的影响不相同,不同浓度二氯喹啉酸处理的土壤细菌生物量和微生物总量的变化一致,这也表现了土壤微生物是以细菌为主体的群落结构。
|
| 图 2 60 d培养期间土壤细菌PLFA量的变化 Fig. 2 The PLFA of bacteria changes during the incubation period |
二氯喹啉酸对土壤真菌生物量的影响随培养时间的变化趋势见图 3。在不淹水水田土壤中,除第1天外,高低2种浓度二氯喹啉酸处理组无显著性差异,但均比对照低,说明二氯喹啉酸会使不淹水水田土壤真菌生物量降低,这种对土壤真菌的抑制作用在中期最不明显;在淹水培养中,不同浓度二氯喹啉酸对淹水水田土壤真菌生物量有促进作用,高浓度二氯喹啉酸的这种促进作用更为明显。

|
| 图 3 60 d培养期间土壤真菌PLFA量的变化 Fig. 3 The PLFA of fungi changes during the incubation period |
真菌/细菌的比例反映的是真菌和细菌相对含量的变化[10]以及2种种群的相对丰富程度[11],二氯喹啉酸对土壤真菌/细菌比值的影响随培养时间的变化趋势见图 4。从图上可以看出,二氯喹啉酸改变土壤真菌/细菌比例与浓度相关,研究认为高的真菌/细菌比值表明农田土壤生态系统更为稳定[11]。在不淹水水田土壤中,除第60天外,高浓度二氯喹啉酸的真菌/细菌比值均比低浓度处理要低,可以认为,除草剂二氯喹啉酸随着浓度的增加显著降低了农田土壤生态系统的稳定性;而在淹水水田土壤中,施药第1、3、7、28、45天,各处理 之间无显著差异,表明不同浓度二氯喹啉酸对淹水水田土壤生态系统稳定性无明显干扰作用。

|
| 图 4 60 d培养期间土壤真菌/细菌比值的变化 Fig. 4 The proportion of fungi/bacteria changes during the incubation period |
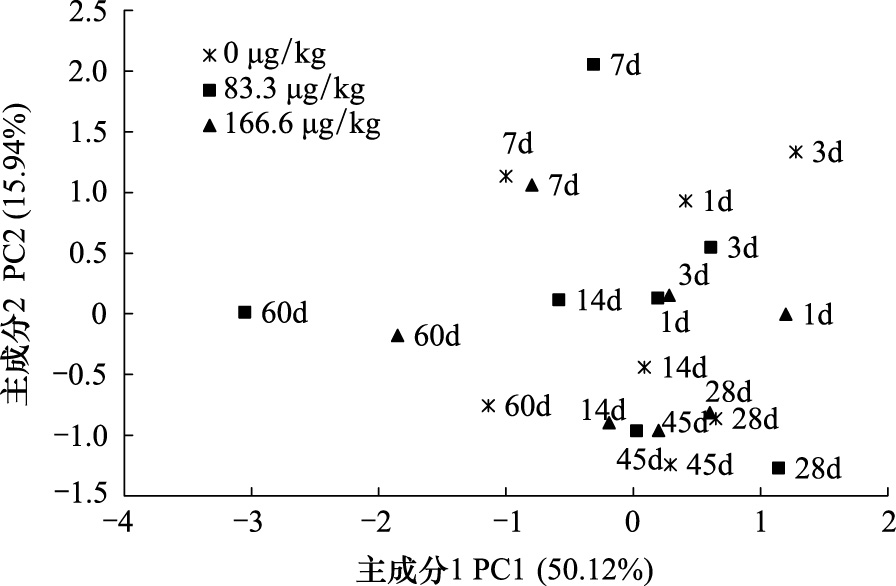
采用主成分分析法(PCA)将提取的PLFAs化为少数几个综合变量(即主成分)[12],来反映二氯喹啉酸处理后土壤微生物群落结构的变化情况。PCA分析结果(图 5)表明,不同时间的不同处理处于主成分分析图的不同位置,尤其是对照和二氯喹啉酸处理区别明显。反映了除草剂二氯喹啉酸对土壤微生物群落结构有显著影响。主成分一和主成分二共聚集了样品总变异的66.06%。从第一主成分看,处理1、3、28 d与主成分一高度正相关;而处理60 d表现出与主成分一负相关;处理1、3、7 d与主成分二正相关。高浓度处理14 d和各浓度处理的28、45 d距离较近,说明这几种处理土壤的微生物结构群落较为相似。
|
| 图 5 不同二氯喹啉酸处理下不淹水水田土壤微生物群落PLFA的主成分分析 Fig. 5 Principle components analysis of PLFA profiles from non-flooded paddy soil microbial communities of different quinclorac treatment |
每种脂肪酸在主成分上的因子荷载分析结果表明(图 6),14 ∶ 0、15 ∶ 0、16 ∶ 0、18 ∶ 0、18 ∶ 1n9c、18 ∶ 2n6c等在主成分一上的荷载值较高,主成分一是它们的代表因子。14 ∶ 0、15 ∶ 0、16 ∶ 0、18 ∶ 0代表土壤中的细菌,18 ∶ 1n9c、18 ∶ 2n6c是土壤中真菌的标志性脂肪酸。说明处理1、3和28 d会使土壤中的细菌和真菌增加。12 ∶ 0、14 ∶ 1、16 ∶ 1在第二主成分上的荷载值较高,可以认为主成分二是12 ∶ 0、14 ∶ 1、16 ∶ 1的代表因子,它们是细菌的标志性脂肪酸。说明处理前期土壤中细菌生物量增高较多。综合分析得出,不同浓度二氯喹啉酸处理的土壤微生物群落结构差别不大,但是在不同处理时间上,土壤微生物群落结构有明显区别。

|
| 图 6 不同二氯喹啉酸处理下不淹水水田土壤微生物群落PLFA荷载因子贡献 Fig. 6 Eigenvector loading of PLFA contributing to soil microbial communities ordination pattern of different quinclorac treatmentp |
PCA分析结果(图 7)表明,主成分一和主成分二基本上能把不同时间二氯喹啉酸处理区分开来。从第一主成分看,处理1、3、7、28 d与主成分一高度正相关;而处理60 d表现出与主成分一和主成分二均负相关;处理14、28、45 d与主成分二正相关。处理1、3 d和14、45 d距离较近,说明这几种处理土壤的微生物结构群落较为相似。

|
| 图 7 不同二氯喹啉酸处理下淹水水田土壤微生物群落PLFA的主成分分析 Fig. 7 Principle components analysis of PLFA profiles from flooded paddy soil microbial communities of different quinclorac treatment |
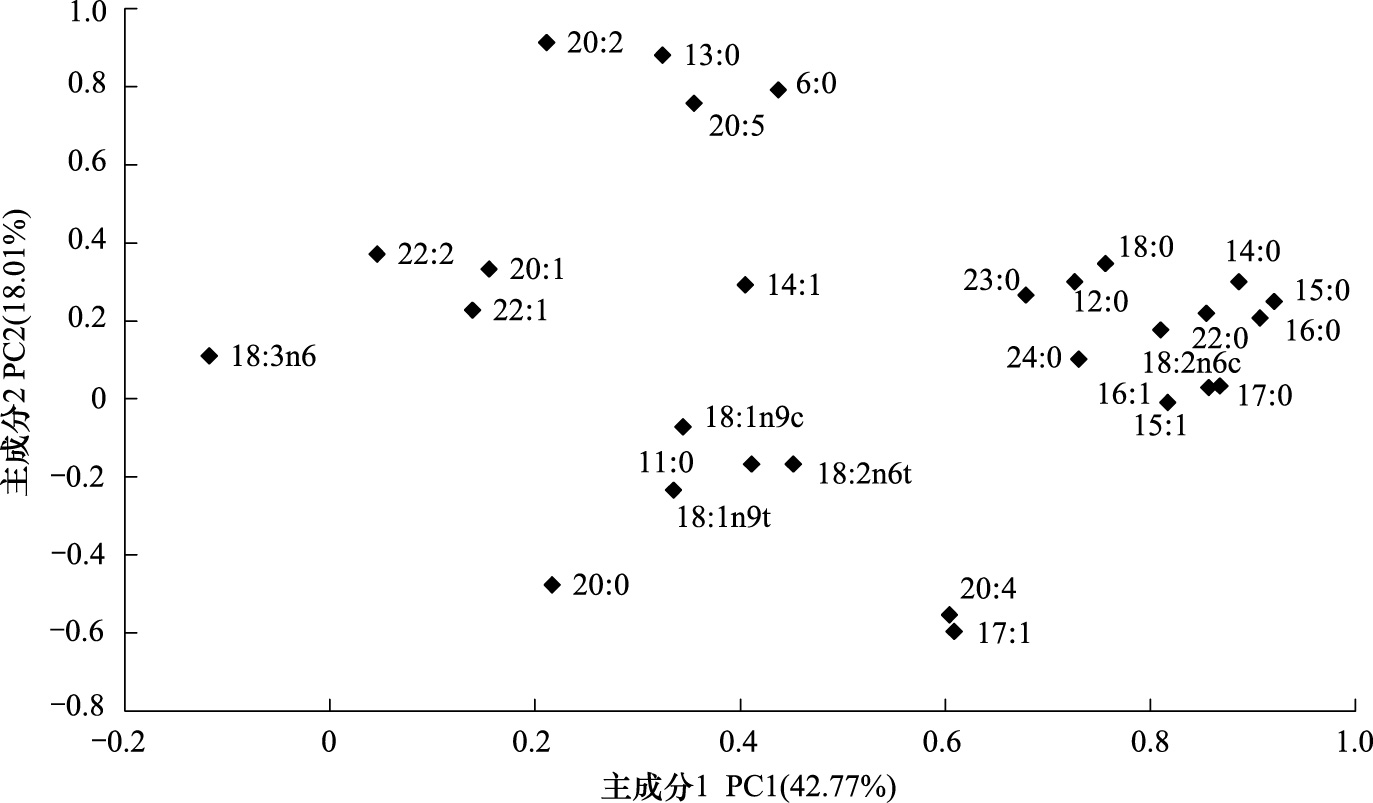
第一主成分对总PLFAs数据变异的贡献率为42.77%,第二成分对总PLFAs数据变异的贡献率为18.01%,每种脂肪酸在主成分上的因子荷载分析结果表明(图 8),14 ∶ 0、15 ∶ 0、16 ∶ 0、16 ∶ 1、17 ∶ 0、18 ∶ 2n6c等,在主成分一上的荷载值较高,主成分一是它们的代表因子。14 ∶ 0、15 ∶ 0、16 ∶ 0、17 ∶ 0代表的土壤中的细菌,18 ∶ 2n6c是土壤中真菌的标志性脂肪酸。说明处理前期使会使土壤中的细菌和真菌增加。13 ∶ 0、20 ∶ 2、20 ∶ 5在第二主成分上的荷载值较高,可以认为主成分二是13 ∶ 0、20 ∶ 2、20 ∶ 5的代表因子,它们是细菌的标志性脂肪酸,说明处理中期土壤中细菌的含量较高。
|
| 图 8 不同二氯喹啉酸处理下淹水水田土壤微生物群落PLFA荷载因子贡献 Fig. 8 Eigenvector loading of PLFA contributing to soil microbial communities ordination pattern of different quinclorac treatment |
研究表明,运用传统的培养方法鉴定的微生物仅占环境总微生物的0.1%—10%[13],这显然不能够反映土壤中微生物真实的分布情况。Bardgett等[14]人认为土壤中磷脂脂肪酸的组成可以表示土壤微生物群落的生物量和结构,PLFA在死亡的微生物中很快被分解,不同类群微生物的标志性PLFA不相同,许多研究者曾发现直接从土壤中提取的磷脂脂肪酸的量可以准确地表达成土壤微生物生物量[14, 15, 16, 17, 18, 19, 20, 21, 22]。本文以总磷脂脂肪酸的量表示微生物群落的生物量;17种含有酯链与甘油相连的饱和或单不饱和脂肪酸(6 ∶ 0、11 ∶ 0、12 ∶ 0、13 ∶ 0、14 ∶ 0、14 ∶ 1、15 ∶ 0、15 ∶ 1、16 ∶ 0、16 ∶ 1、17 ∶ 0、17 ∶ 1、18 ∶ 0、20 ∶ 0、20 ∶ 1、22 ∶ 0和22 ∶ 1)表示细菌生物量;18 ∶ 1n9t、18 ∶ 1n9c、18 ∶ 2n6t、18 ∶ 2n6c和18 ∶ 3n6表示真菌生物量。通过检测不同施药的淹水和不淹水水田土壤磷脂脂肪酸的变化发现,无论是从衡量菌落结构的具体指标,还是从整体的PLFA群落结构分析(PCA)都表明了,除草剂二氯喹啉酸对土壤微生物群落有显著的影响:
(1)不同浓度二氯喹啉酸处理对不淹水水田土壤微生物生物量有不同程度的影响。土壤微生物PLFA总量的改变可以体现土壤中微生物的生物总量的改变[23, 24]。张昌朋等人通过对土壤PLFAs的测定研究发现,咪唑乙烟酸显著增加了土壤微生物生物量碳、生物总量和压力指数[24]。本研究表明,低浓度二氯喹啉酸会降低不淹水水田土壤微生物总生物量和细菌、真菌生物量及实验后期的真菌/细菌比值;高浓度二氯喹啉酸对不淹水水田土壤细菌和微生物总量有显著的促进作用,对真菌及真菌/细菌比有抑制作用。高浓度二氯喹啉酸的加入显著增加了土壤微生物生物总量,这可能是由于二氯喹啉酸作为土壤微生物代谢的能源,从而使微生物量增加。Cuadrado[9]和Wardle[10]等人的研究也表明除草剂增加了土壤微生物的生物量。真菌/细菌比值表明了农田土壤生态系统的稳定性,本研究中在不淹水水田土壤施用不同浓度二氯喹啉酸均显著降低了真菌/细菌比,表明二氯喹啉酸使得不淹水水田土壤生态系统稳定性降低。
(2)不同浓度二氯喹啉酸处理对淹水水田土壤微生物生量的影响与不淹水水田土壤相比有一定差异。低浓度二氯喹啉酸对淹水水田土壤微生物总生物量和真菌生物量有促进作用,对土壤细菌生物量有一定的抑制;高浓度对淹水水田土壤微生物总生物量和细菌、真菌生物量均有促进作用,而从真菌/细菌比值上看,不同浓度二氯喹啉酸对淹水水田土壤生态系统稳定性无明显干扰作用。研究结果与吕镇梅等人用传统方法研究二氯喹啉酸对水稻田微生物种群的影响一致[25]。
(3)除草剂对土壤微生物的影响与土壤类型、环境气候条件、除草剂的结构与理化性质以及用药量和施用时间、研究方法和取样时间等诸多因素相关[26],苑学霞等人[27]研究发现,二氯喹啉酸在水中的消解比土壤要快。从实验结果来看,二氯喹啉酸对淹水水田土壤生态系统稳定性和微生物生物量的干扰要小于不淹水水田土壤,这与其在淹水水田土壤中的消解速度比不淹水土壤中快和两种土壤的状态不同有一定关系;另外,有也可能是由于同样的施药量,淹水水田土壤对农药的稀释作用使得实际分布量小于理论施药量造成的。
| [1] | 程红芳, 章文波, 陈锋. 植被覆盖度遥感估算方法研究进展. 国土资源遥感, 2006, (1): 13-17. |
| [2] | Wang M C, Liu Y H, Wang Q, Gong M, Hua X M, Pang Y J, Hu S J, Yang Y H. Impacts of methamidophos on the biochemical, catabolic, and genetic characteristics of soil microbial communities. Soil Biology and Biochemistry, 2008, 40(3): 778-788. |
| [3] | Manickam N, Pathak A, Saini H S, Mayilraj S, Shanker R. Metabolic profiles and phylogenetic diversity of microbial communities from chlorinated pesticides contaminated sites of different geographical habitats of India. Journal of Applied Microbiology, 2010, 109(4): 1458-1468. |
| [4] | 姚斌, 徐建民, 尚鹤, 张超兰. 甲磺隆污染土壤的微生物生态效应. 农业环境科学学报, 2005, 24(3): 557-561. |
| [5] | Petersen S O, Debosz K, Schjonning P, Christensen B T, Elmholt S. Phospholipid fatty acid profiles and C availability in wet-stable macro-aggregates from conventionally and organically farmed soils. Geoderma, 1997, 78(3/4): 181-196. |
| [6] | Zaady E, Ben-David E A, Sher Y, Tzirkin R, Nejidat A. Inferring biological soil crust successional stage using combined PLFA, DGGE, physical and biophysiological analyses. Soil Biology & Biochemistry, 2010, 42(5): 842-849. |
| [7] | 吴愉萍. 基于磷脂脂肪酸(PLFA)分析技术的土壤微生物群落结构多样性的研究 [D]. 杭州: 浙江大学环境与资源学院, 2009. |
| [8] | 颜慧. 长期施肥对土壤微生物磷脂脂肪酸多样性和酶活性的影响 [D]. 南京: 南京师范大学, 2007. |
| [9] | Cuadrado V, Merini L J, Flocco C G, Giulietti A M. Degradation of 2, 4-DB in Argentinean agricultural soils with high humic matter content. Applied Microbiology and Biotechnology, 2008, 77(6): 1371-1378. |
| [10] | Wardle D A, Parkinson D. Relative importance of the effect of 2, 4-D, Glyphosate, and environmental variables on the Soil Microbial Biomass. Plant and Soil, 1991, 134(2): 209-219. |
| [11] | de Vries F T, Hoffland E, van Eekeren N, Brussaard L, Bloem J. Fungal/Bacterial Ratios in grasslands with contrasting Nitrogen management. Soil Biology and Biochemistry, 2006, 38(8): 2092-2103. |
| [12] | 苏荣国, 胡序朋, 张传松, 王修林. 荧光光谱结合主成分分析对赤潮藻的识别测定. 环境科学, 2007, 28(7): 1529-1533. |
| [13] | 喻曼, 肖华, 张棋, 曲云欢, 许育新. PLFA法和DGGE法分析堆肥细菌群落变化. 农业环境科学学报, 2011, 30(6): 1242-1247. |
| [14] | Bardgett R D, Hobbs P J, Frosteg Å. Changes in soil fungal: bacterial biomass ratios following reductions in the intensity of management of an upland grassland. Biology and Fertility of Soils, 1996, 22(3): 261-264. |
| [15] | Ponder F Jr, Tadros M. Phospholipid fatty acids in forest soil four years after organic matter removal and soil compaction. Applied Soil Ecology, 2002, 19(2): 173-182. |
| [16] | Wu Y P, Yu X S, Wang H Z. Does history matter? Temperature effects on soil microbial biomass and community structure based on the phospholipid fatty acid (PLFA) analysis. Journal of Soils and Sediments, 2010, 10(2): 223-230. |
| [17] | Frostegård A, Bååth E. The use of phospholipid fatty acid analysis to estimate bacterial and fungal biomass in soil. Biology and Fertility of Soils, 1996, 22(1/2): 59-65. |
| [18] | Rinklebe J, Langer U. Relationship between soil microbial biomass determined by SIR and PLFA analysis in floodplain soils. Journal of Soils and Sediments, 2010, 10(1): 4-8. |
| [19] | Mummey D L, Stahl P D, Buyer J S. Microbial biomarkers as an indicator of ecosystem recovery following surface mine reclamation. Applied Soil Ecology, 2002, 21(3): 251-259. |
| [20] | Steinberger Y, Zelles L, Bai Q Y, von Lutzow M, Munch J C. Phospholipid fatty acid profiles as indicators for the microbia community structure in soils along a climatic transect in the Judean Desert. Biology and Fertility of Soil, 1999, 28(3): 292-300. |
| [21] | Murase J, Hordijk K, Tayasu I, Bodelier P L. Strain-specific incorporation of methanotrophic biomass into eukaryotic grazers in a rice field soil revealed by PLFA-SIP. FEMS Microbiology Ecology, 2011, 75(2): 284-290. |
| [22] | Zeiles L. Identification of single cultured micro-organisms based on their whole-community fatty acid profiles, using an extended extraction procedure. Chemosphere, 1999, 39(4): 665-682. |
| [23] | 于树, 汪景宽, 李双异. 地膜覆盖对土壤微生物群落结构的影响. 土壤通报, 2008, 39(4): 904-907. |
| [24] | 张昌朋, 刘新刚, 徐军, 董丰收, 盛宇, 田迎迎, 郑永权. 咪唑乙烟酸对土壤微生物生态的影响. 农药, 2010, 49(2): 117-119. |
| [25] | 吕镇梅, 闵航, 叶央芳. 除草剂二氯喹啉酸对水稻田土壤中微生物种群的影响. 应用生态学报, 2004, 15(4): 605-609. |
| [26] | 林晓燕, 王玮, 赵宇华, 丁海涛, 冯志红. 苄嘧磺隆对淹水稻田土壤呼吸和酶活性的影响. 浙江大学学报: 农业与生命科学版, 2008, 34(1): 109-113. |
| [27] | 苑学霞, 郭栋梁, 赵善苍, 毛江胜, 郭长英, 邓立刚, 张勇. 二氯喹啉酸在水稻、土壤和田水中消解动态及残留. 生态环境学报, 2011, 20(6/7): 1138-1142. |
 2015, Vol. 35
2015, Vol. 35




