文章信息
- 杨菁, 周国英, 田媛媛, 刘倩丽, 刘成锋, 杨权, 周洁尘
- YANG Jing, ZHOU Guoying, TIAN Yuanyuan, LIU Qianli, LIU Chengfeng, YANG Quan, ZHOU Jiechen
- 降香黄檀不同混交林土壤细菌多样性差异分析
- Differential analysis of soil bacteria diversity in different mixed forests of Dalbergia odorifera
- 生态学报, 2015, 35(24): 8117-8127
- Acta Ecologica Sinica, 2015, 35(24): 8117-8127
- http://dx.doi.org/10.5846/stxb201409191856
-
文章历史
- 收稿日期: 2014-09-19
- 网络出版日期: 2015-05-21
细菌作为土壤微生物中重要的组成部分,具有含氮量高,含碳量低的特点,对土壤养分的形成与分解有促进作用。土壤细菌的微生物多样性越高,则越有利于土壤的可持续利用和抗压力[1, 2]。但目前只有1%左右的主要细菌菌群能被检测到[3]。采用成本低、通量高、速度快并且覆盖深度高的第二代高通量测序技术进行实验,对微生物的多样性分析是十分有利的[4, 5]。
高通量测序技术(High-throughput sequencing)又称为新一代测序技术或第二代测序,该测序技术相对于传统的测序技术而言,具有极大的优势,主要表现在[6, 7, 8]:①测序通量高,可以检测分析到样品中的痕量微生物;②实验过程简化;③速度快;④准确率高,实验结果更能全面的反应环境中群落的特点。目前,高通量测序已广泛的应用于土壤微生物的研究。
降香黄檀(Dalbergia odorifera T. Chen)是我国濒危树种,国家二级保护野生植物[9],也是海南省珍贵乡土树种。降香黄檀具有药用价值和经济价值,另外,降香黄檀落叶量大、根系发达,能改良土壤,具有很大的生态效益[10]。但历史上人们对降香黄檀的过度砍伐利用,导致其资源减少,生产力下降。近年来,海南省虽对降香黄檀进行了人工栽培,但在树种的合理配置、良种选育等方面仍存在问题。目前,国外对降香黄檀的研究甚少,国内大多集中于降香黄檀多样性[11, 12]、栽培技术[13]以及活性物质提取[14, 15]等方面的研究,针对其土壤的研究较少。已有研究表明[9],在营造降香黄檀人工林时,不宜发展人工纯林,应考虑与其他树种混交,以短养长,同时也能提高林木的抗逆性。
本研究针对海南珍贵乡土树种降香黄檀的不同混交林,应用Miseq高通量测序的方法,结合土壤的物理化学性质及土壤酶活性,对土壤的细菌群落结构进行分析,以研究降香黄檀不同混交林细菌群落的多样性及其与环境因子的关系,为降香黄檀人工林的合理配置及健康经营提供参考。
1 研究区域概况试验样地位于海南省澄迈国营林场(海南省澄迈县东南部的太平乡),地处19°11′ N,111°1′ E,海拔为118 m,属热带季风气候类型,年平均日照时数2059 h,年平均气温23.8 ℃,相对湿度84%,年均降雨量1786.1 mm,全年基本无霜。研究区面积约为2.667hm2,地貌以低丘陵和台地为主。成土母岩主要有玄武岩和砂页岩,成土母质以河流冲积物发育而成的砂壤土为主,研究区的土壤主要为砂壤。
2 材料与方法 2.1 样地设置及样品采集该实验区于2012年上旬造林。造林时,选用的降香黄檀苗木株高为(50±10)cm,奥氏黄檀为(40±10)cm,大果紫檀为(45±10)cm,檀香为(40±10)cm,母生为(30±10)cm。4个样地的造林密度均为667株/666.7m2,行株距为1 m×1 m。
于2014年3月采样,且采样前一个月内降雨量很少,基本处于干旱状态。样地的选择是在林场内选择立地条件相似的降香黄檀不同混交模式样地(表 1)。在每个样地内设置5个标准地,大小为10 m×10 m,每个标准地内分别设置3个样点,每个采样点的土壤均是除去地表植被和枯枝落叶后采集0—20 cm土层的土壤。用于测定细菌多样性的土壤于-80 ℃保存备用,用于理化性质测定的土样,作风干过筛处理。
| 样地 Plot | 混交比例 Mixed proportion | 郁闭度 Canopy density | 林下主要植被 Undergrowth main species |
| Dal 0 | 3 ∶ 1 | 0.4 | 墨苜蓿Richardia brasiliensis Gomez、飞机草Eupatorium odoratum L.、菊芩Erechitites valerianaefolia、藿香蓟Ageratum conyzoides、龙葵Solanum nigrum L. |
| Dal 1 | 3 ∶ 1 | 0.6 | 巴西含羞草Mimosa invisa Mart. ex Colla、墨苜蓿Richardia brasiliensis Gomez、筒轴茅Rottboellia exaltata、菊芩Erechitites valerianaefolia、藿香蓟Ageratum conyzoides、飞机草Eupatorium odoratum L.、龙爪草Ottelia alismoides、龙葵Solanum nigrum L. |
| Dal 2 | 3 ∶ 1 | 0.5 | 巴西含羞草Mimosa invisa Mart. ex Colla、墨苜蓿Richardia brasiliensis Gomez、筒轴茅Rottboellia exaltata、菊芩Erechitites valerianaefolia、藿香蓟Ageratum conyzoides |
| Dal 3 | 2 ∶ 1 | 0.3 | 巴西含羞草Mimosa invisa Mart. ex Colla、墨苜蓿Richardia brasiliensis Gomez、筒轴茅Rottboellia exaltata、菊芩Erechitites valerianaefolia、藿香蓟Ageratum conyzoides |
| Dal 0:降香黄檀×奥氏黄檀Dalbergia odorifera × Dalbergia oliveri; Dal 1:降香黄檀×大果紫檀Dalbergia odorifera × Pterocarpus macarocarpus; Dal 2:降香黄檀×檀香Dalbergia odorifera ×Santalum album L.; Dal 3:降香黄檀×母生Dalbergia odorifera ×Homalium hainanense Gagnep. | |||
土壤含水量采用TZS-IW型土壤水分温度测量仪现场测定;土壤pH值采用1 mol/L KCl浸提用pH计进行测定;土壤有机质采用水合热重铬酸钾-硫酸-比色法;土壤全氮含量测定采用半微量凯式定氮法;土壤有效磷含量采用NaHCO3浸提,全自动间断化学分析仪测定;土壤有效钾含量测定采用火焰光度法[16]。
土壤过氧化氢酶活性的测定采用高锰酸钾滴定法(0.1mol/L高锰酸钾mL-1);土壤多酚氧化酶的测定采用邻苯三酚比色法;土壤脲酶活性的测定采用苯酚钠-次氯酸钠比色法[17, 18]。
2.2.2 土壤总DNA的提取与测序使用E.Z.N.A soil DNA土壤DNA提取试剂盒(OMEGA)提取土壤总DNA,以338F(5′-ACTCCTACGGGAGGCAGCA-3′)为正向引物,806R(5′-GGACTACHVGGGTWT CTAAT-3′)为反向引物[19]。PCR反应体系如下,共20 μL:5×FastPfu Buffe 4 μL,2.5 mmol/L dNTPs,2 μL;Forward Primer(5 μmol/L),0.4μL;Reverse Primer(5 μmol/L),0.4 μL;FastPfu Polymerase,0.4 μL;Template DNA,10 ng;补充ddH2O至20 μL。PCR反应条件为:1×(95 ℃,2 min);25×(95 ℃,30 s;55 ℃,30 s;72 ℃,45 s;72 ℃,10 min);4℃ 保存。每个样品取3 μL,进行检测(1%琼脂条凝胶电泳),每个样品3个重复将同一样品的 PCR 产物混合后用 2%琼脂糖凝胶电泳检测,使用 AxyPrepDNA 凝胶回收试剂盒(AXYGEN 公司)切胶,回收 PCR 产物,Tris-HCl洗脱;2%琼脂糖电泳检测。之后进行荧光定量,Miseq文库构建及Miseq测序。
2.2.3 数据处理Miseq测序得到的PE reads首先根据overlap关系进行拼接,同时对序列质量进行质控和过滤,区分样品后进行OTU聚类分析和物种分类学分析。基于OTU聚类分析的结果,对OTU进行多种多样性指数分析。
2.2.4 数据分析采用Mothur等软件对获得的数据进行分类分析和多样性计算;通过R 软件对初始结果进行相对丰度制图;利用SPSS 19进行方差分析(Duncan)及相关性分析(Pearson),利用Canoco for windows 4.5进行冗余分析。
3 结果与分析 3.1 土壤理化性质与土壤酶活性不同样地的土壤理化、酶活分析结果见表 2,样地的土壤类型主要属于酸性砂壤(pH均小于4.5),且不同混交林土壤的pH值存在极显著性差异(P<0.001),其中Dal 2和Dal 3 的pH均值最低。不同混交林土壤的有机质、全氮、有效钾3个方面存在极显著的差异(P<0.001),其中Dal 2含量均最高,分别为27.59 mg/g、0.85 mg/kg和37.46 mg/kg。4个样地土壤的有效磷含量存在极显著性差异(P值均小于0.001),其中Dal 1含量最高,为6.04mg/Kg。酶活方面,过氧化氢酶和多酚氧化酶(P=0.032)存在显著性差异(P=0.017),脲酶存在极显著性差异(P<0.001)。
| 样地 Plot | 含水量 Moisture content/ % | pH | 有机质 Organic matte/ (g/kg) | 全氮 Total N/ (mg/g) | 有效钾 Available K/ (mg/kg) | 有效磷 Available P/ (mg/kg) | 过氧化氢酶 Catalase/ (ml/g) | 脲酶 Ureas/ (mg/g) | 多酚氧化酶 Polyphenol oxidase/ (mg/g) |
| Dal 0 | 4.26±1.92a | 4.18±0.02b | 16.40±0.81a | 0.52±0.05ab | 34.29±1.36a | 5.73±0.07b | 0.86±0.76b | 0.20±0.12b | 2.79±0.64ab |
| Dal 1 | 2.96±2.18a | 4.48±0.04c | 7.09±0.81b | 0.43±0.01a | 29.41±0.41b | 6.04±0.01c | 0.75±0.07a | 0.01±0.01a | 4.19±1.23b |
| Dal 2 | 5.24±1.76a | 4.03±0.02a | 27.59±1.62c | 0.85±0.09c | 37.46±0.46c | 5.89±0.19bc | 0.75±0.07a | 0.32±0.52c | 1.84±0.52a |
| Dal 3 | 2.52±1.48a | 4.02±0.19a | 19.75±0.23d | 0.55±0.04b | 32.15±1.52d | 5.17±0.03a | 0.77±0.60a | 0.28±0.18c | 2.68±0.35ab |
| 长度 Length/(bp) | 序列数 No. of sequences | % |
| 1—300 | 5 | 0 |
| 301—400 | 39 | 0.01 |
| 401—500 | 293630 | 99.98 |
通过Miseq高通量测序并优化后,4个样地共获得293677条序列,总碱基数为127504401bp,平均碱基长度为434.17bp,其中401—500bp的碱基占总序列数的99.98%,如表 3所示。
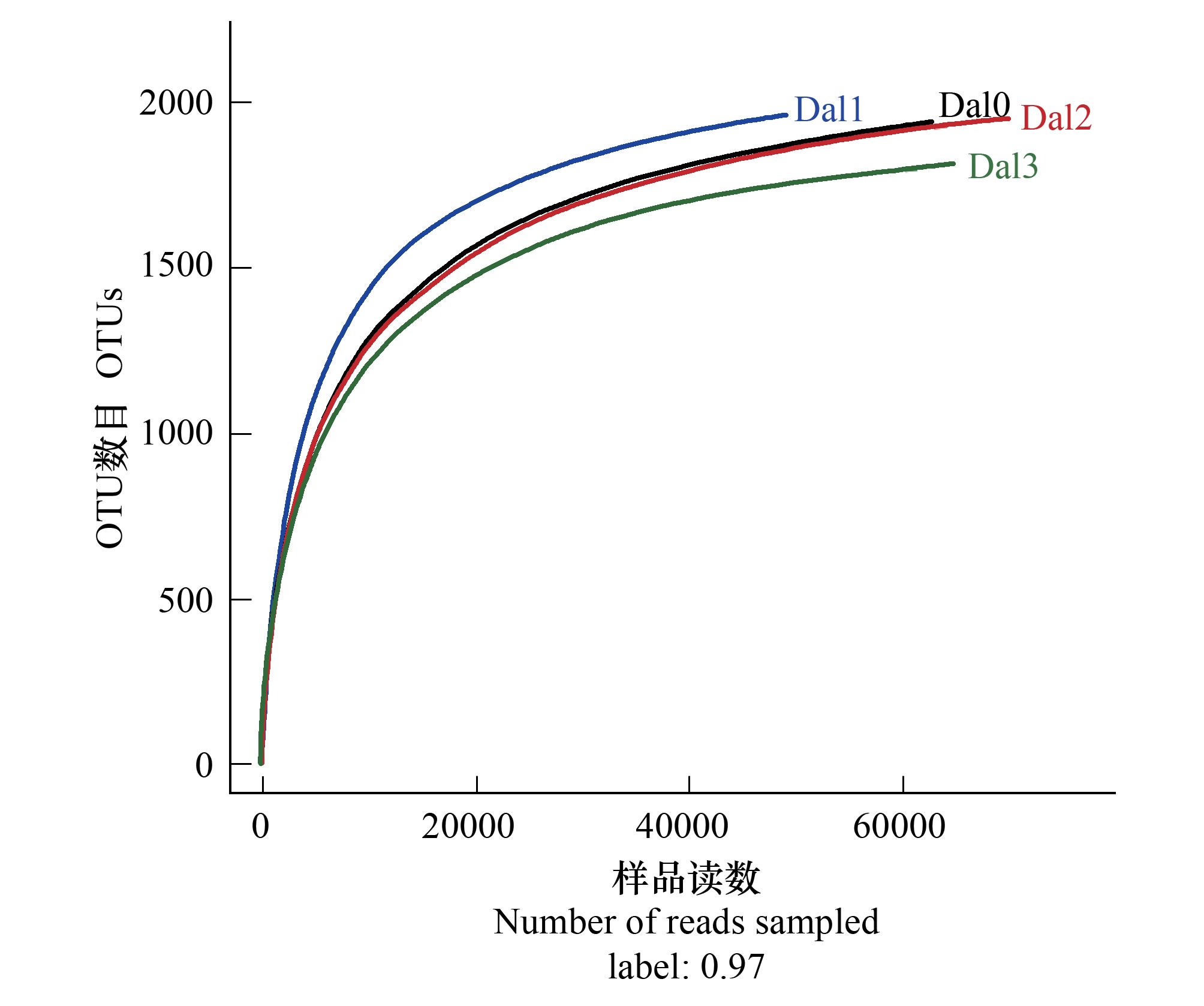
采用对测序获得的序列进行随机抽样的方法,以抽到的序列数与它们所代表的OTU数目构建稀释性曲线(图 1),从图中可以看出,4个样地的稀释性曲线均趋于平坦,表明测序数据合理,更多的测序数据对发现新的OTU贡献率较小。
|
| 图1 不同样地土壤细菌OTU稀释曲线 Fig.1 OTU rarefaction curves of soil bacteria in different plots |
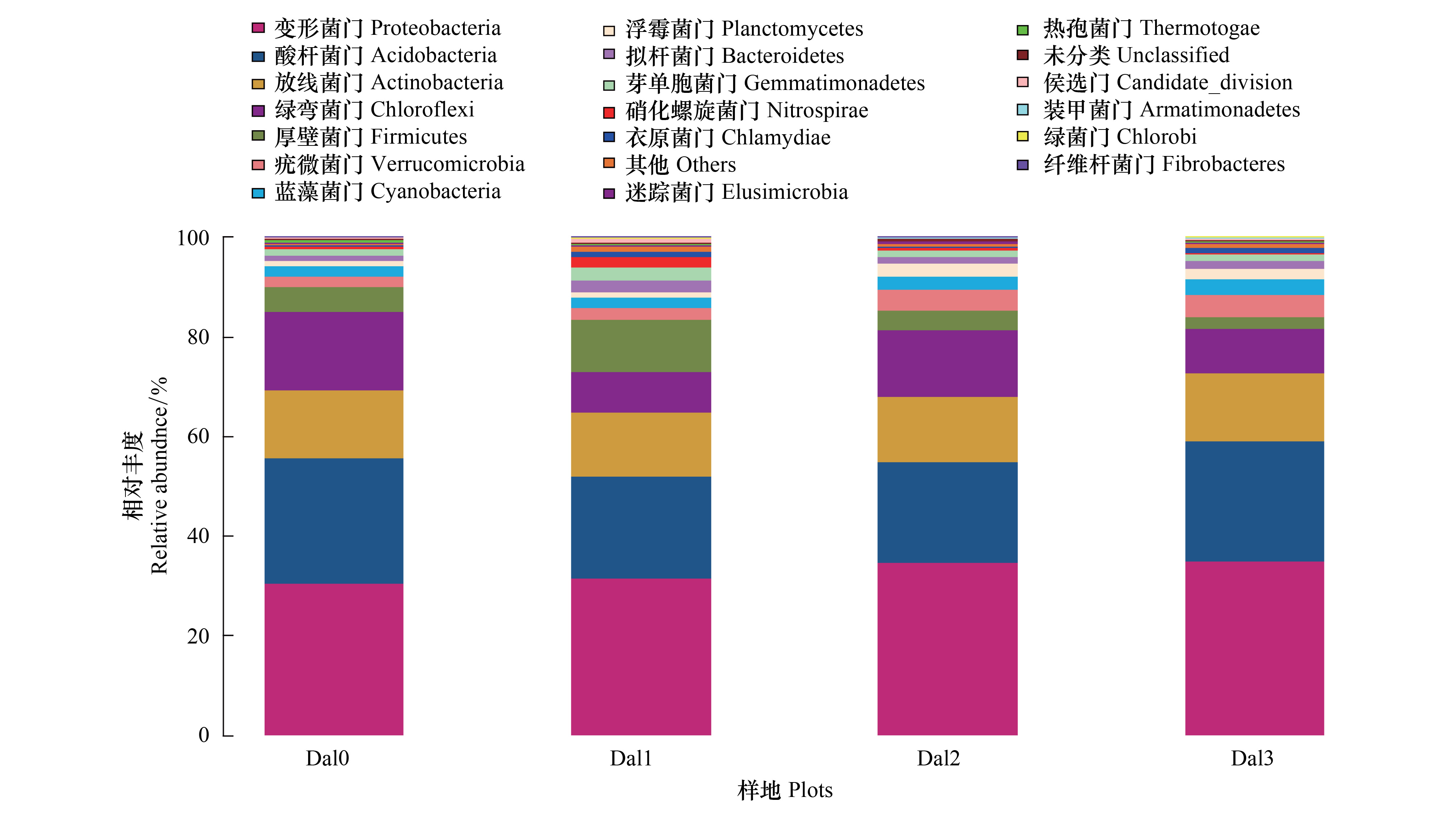
在相似水平为97%的条件下,通过与Sliva数据库对比,对序列进行归类分析[20, 21]。结果表明,变形菌门(Proteobacteria)、酸杆菌门(Acidobacteria)、放线菌门(Actinobacteria)、绿弯菌门(Chloroflexi)和厚壁菌门(Firmicutes)这5个菌门为主要菌群(图 2)所示。
对不同样地中相对丰度超过1%的菌群进行单因素方差分析(表 4),结果表明,变形菌门、酸杆菌门、放线菌门、绿弯菌门、厚壁菌门、疣微菌门、蓝藻菌门和浮霉菌门在降香黄檀不同混交模式中分布比较均匀,不存在显著性差异。而厚壁菌门(P=0.003)、拟杆菌门(P=0.026)和芽单胞菌门(P=0.019)在各样地间存在显著性差异,Dal 1中这3个菌门的相对丰度均高于其他3个样地。
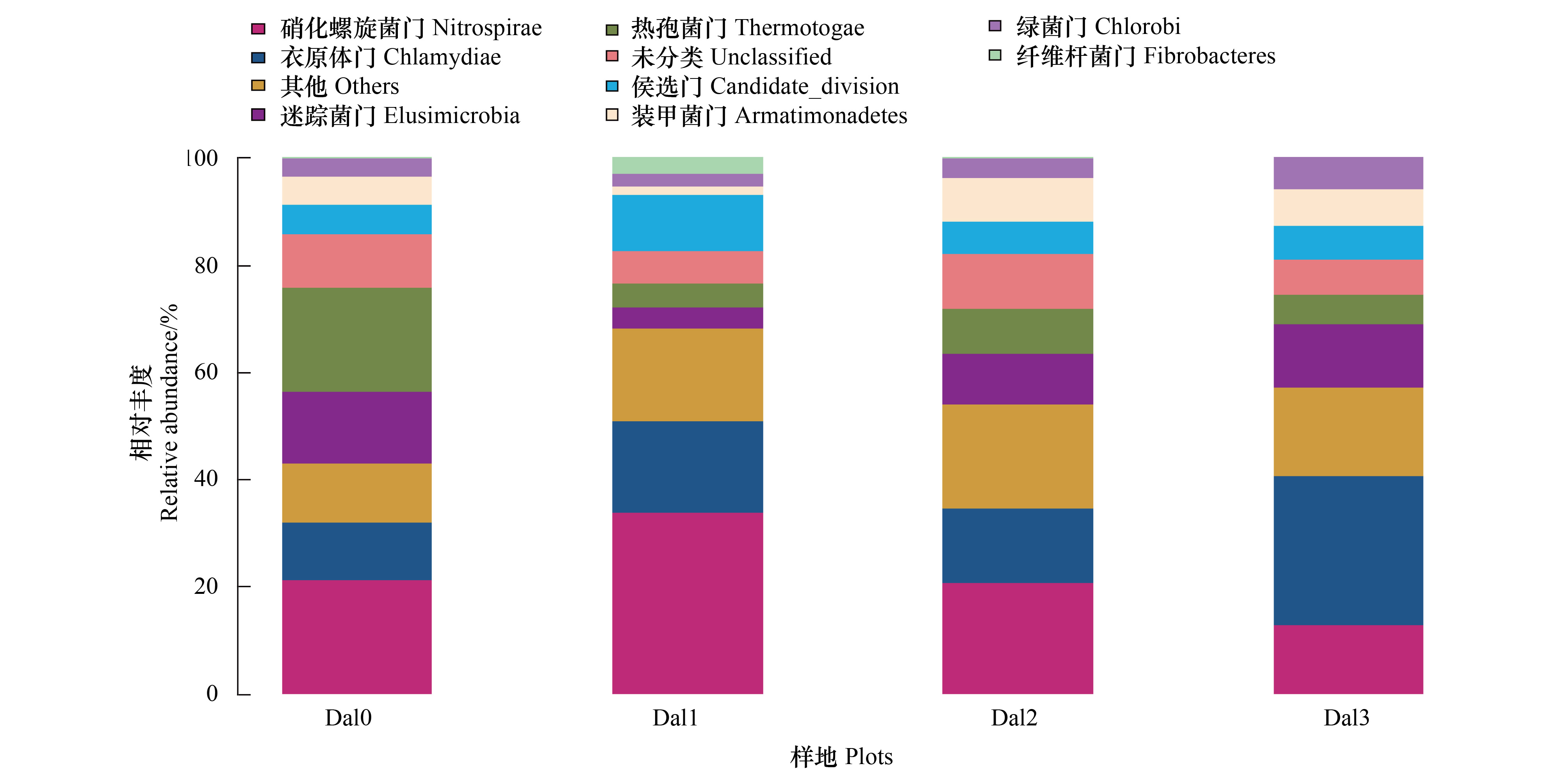
为了更加深入的了解降香黄檀不同混交林中土壤细菌群落结构的分布及差异,去除以上的10个相对丰度超过1%的菌群后,对剩余菌群作了相对丰度分析(图 3)。单因素方差分析结果表明,装甲菌门(Armatimonadetes)、绿菌门(Chlorobi)、迷踪菌门(Elusimicrobia)、纤维杆菌门(Fibrobacteres)、硝化螺旋菌门(Nitrospirae)和热袍菌门(Thermotogae)在降香黄檀不同混交模式中存在差异(表 5)。其中,纤维杆菌门(P=0.002)和热袍菌门(P=0.002)在不同样地间存在极显著性差异,装甲菌门(P=0.04)和迷踪菌门(P=0.05)在不同样地间存在显著性差异。相较于4个样地,纤维杆菌门在Dal 2中最多,而不存在于Dal 3中。热袍菌门在Dal 0中最多,在其他3个样地中无差异。装甲菌门和迷踪菌门在Dal 1中最少,在其他样地中无差异。
|
| 图2 不同样地土壤细菌的群落结构 Fig.2 Soil bacterial community of different sample plots |
通过对各样地进行多样性的计算,并通过SPSS进行单因素方差分析(表 6)。4个样地间,ace(P=0.013)和chao(P=0.02)指数具有显著性差异,而shannon(P=0.133)和simpson(P=0.41)指数无显著性差异。其中Dal 3的ace和chao指数均低于其他样地。
| 分类Taxon | 相对丰度Relative abundances /% | |||
| Dal 0 | Dal 1 | Dal 2 | Dal 3 | |
| 变形菌门 Proteobacteria | 30.0±2.7a | 30.8±4.7a | 33.7±7.6a | 35.2±1.7a |
| 酸杆菌门 Acidobacteria | 25.0±1.5a | 20.8±3.4a | 20.2±0.6a | 24.3±1.2a |
| 放线菌门 Actinobacteria | 13.5±0.4a | 12.5±3.0a | 12.8±3.0a | 13.7±0.7a |
| 厚壁菌门 Firmicutes | 5.0±0.4a | 10.4±1.2b | 3.7±1.1bc | 2.4±0.3c |
| 浮霉菌门 Planctomycetes | 1.1±0.4a | 1.0±1.0a | 2.8±1.8a | 1.9±0.6a |
| 绿弯菌门 Chloroflexi | 16.3±3.7a | 8.3±1.3a | 14.0±5.6a | 8.9±0.3a |
| 疣微菌门 Verrucomicrobia | 2.2±0.8a | 2.5±2.2a | 4.7±3.2a | 4.3±1.3a |
| 蓝藻菌门 Cyanobacteria | 2.0±0.2a | 2.3±1.1a | 2.6±1.3a | 2.9±1.1a |
| 拟杆菌门 Bacteroidetes | 1.2±0.2b | 2.4±0.7a | 1.2±0.4b | 1.7±0.3b |
| 芽单胞菌门 Gemmatimonadetes | 1.1±0.5b | 2.6±0.5a | 1.3±0.2b | 1.2±0.2b |
|
| 图3 剩余菌群的群落结构 Fig.3 Bacterial community of rejecting relative abundance of more than 1% |
| 分类Taxon | 相对丰度Relative abundances /% | |||
| Dal 0 | Dal 1 | Dal 2 | Dal 3 | |
| 装甲菌门 Armatimonadetes | 3.6±0.1ab | 1.2±0.7a | 5.7±0.6b | 5.7±1.9b |
| 衣原体门 Chlamydiae | 8.1±4.1a | 13.0±6.7a | 9.6±2.7a | 18.7±2.0a |
| 绿菌门 Chlorobi | 2.2±0.6ab | 1.7±0.0a | 2.5±0.7ab | 4.4±1.6b |
| 迷踪菌门 Elusimicrobia | 9.3±0.4b | 3.0±0.5a | 6.6±3.0ab | 7.9±0.2b |
| 纤维杆菌门 Fibrobacteres | 0.2±0.0b | 2.2±0.5a | 0.1±0.1b | 0 b |
| 硝化螺旋菌门 Nitrospirae | 14.3±2.1ab | 23.8±5.6b | 14.6±6.8ab | 8.3±1.7a |
| 热袍菌门 Thermotogae | 13.2±1.2a | 3.2±0.5b | 5.8±1.4b | 3.9±0.8b |
| 候选门 Candidate_division | 35.1±2.5a | 35.7±2.0a | 34.4±13.7a | 35.9±2.7a |
| 未分类 Unclassified | 6.9±0.1a | 4.3±0.2a | 7.4±3.2a | 4.2±0.9a |
| 其他 Others | 7.1±3.3a | 12.2±3.1a | 13.3±4.6a | 11.6±1.4a |
| 样地Plot | 序列数Reads | OTU | 多样性指数Diversity Index | |||
| ace | chao | shannon | simpson | |||
| Dal 0 | 31322±11047a | 1702.5±92.6a | 1928.5±51.6b | 1959.5±30.4b | 6.12±0.05ab | 0.0058±0.0001a |
| Dal 1 | 24502±5888a | 1740.0±1.4a | 1939.0±11.3b | 1974.5±12.0b | 6.38±0.06b | 0.0043±0.0003a |
| Dal 2 | 34933±7028a | 1720.0±28.3a | 1967.5±7.8b | 1975.0±14.1b | 6.08±0.21ab | 0.0061±0.0002a |
| Dal 3 | 32363±10641a | 1690.4±80.1a | 1797.0±17.0a | 1803.0±7.1a | 6.05±0.06ab | 0.006±0.0003a |
冗余分析(RDA)主要应用于分析影响生物[22]、植被[23]、景观分布[24]的关键环境因子。RDA分析能够有效的对多个环境指标进行统计学检验,经过一系列的转换、筛选,能够有效的简化变量个数,为进一步研究的分析创造条件[22]。
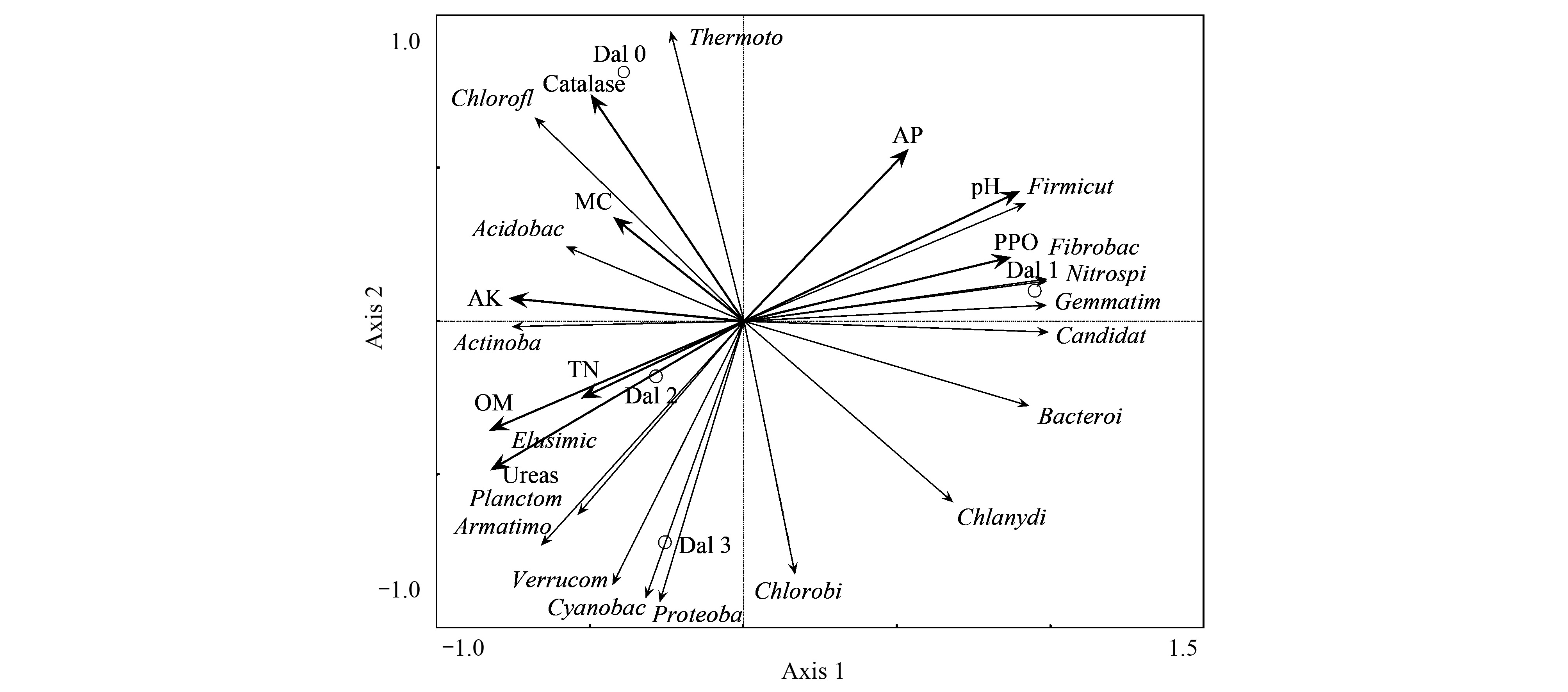
本次试验分析了土壤细菌主要菌群和非主要菌群与土壤性质的RDA排序图,第一轴可以解释所有信息的52.0%,第二轴可以解释34.1%(图 4)。经Canoco的forward分析表明,pH 值、脲酶、多酚氧化酶和有机质对土壤细菌群落结构的影响最为显著,影响程度为:pH值> 脲酶 > 多酚氧化酶 > 有机质。从图中可以看出,受此四种因子影响较为显著的菌群有:迷踪菌门、浮霉菌门、装甲菌门、厚壁菌门、硝化螺旋菌门、纤维杆菌门和芽单胞菌门。分析四个样地间的欧几里德距离,可以看出Dal 1的细菌群落结构与其他3个样地差异较大,Dal 0、Dal 1与Dal 3也具有较大差异,相较之下,Dal 2与Dal 3的群落结构差异较小。
|
| 图4 土壤菌群与土壤性质的RDA分析 Fig.4 The results from RDA to explore the relationship between bacteria and soil properties Proteoba: 变形菌门,Acidobac: 酸杆菌门,Actinoba: 放线菌门,Firmicut: 厚壁菌门,Planctom: 浮霉菌门,Chlorofl: 绿弯菌门,Verrucom: 疣微菌门,Cyanobac: 蓝藻菌门,Bacteroi: 拟杆菌门,Gemmatim: 芽单胞菌门,Armatimo: 装甲菌门,Chlamydi: 衣原体门,Elusimic: 迷踪菌门,Fibrobac: 纤维杆菌门,Nitrospi: 硝化螺旋菌门,Thermoto: 热袍菌门,Chlorobi: 绿菌门,Candidat: 候选门,OM: 有机质,MC: 含水量,TN: 全氮,AP: 有效磷,AK: 有效钾,PPO:多酚氧化酶 |
经过SPSS分析计算样地土壤性质与细菌多样性指数的相关性(表 7),结果表明过氧化氢酶与细菌多样性指数无显著相关;有效磷与ace指数、chao指数呈显著正相关; pH值、有效磷、多酚氧化酶与shannon指数呈显著正相关,与simpson指数呈显著负相关;有机质、全氮、有效钾、脲酶与shannon指数呈显著负相关,与simpson指数呈显著正相关。其中,pH值、有机质、脲酶和多酚氧化酶与shannon指数和simpson指数的相关性为极显著,说明土壤细菌的多样性主要受该4个指标的影响。
| 指标 Index | ace 指数 ace index | chao 指数 chao index | shannon 指数 shannon index | simpson 指数 simpson index | 含水量 Moisture content | pH值 pH | 有机质 Organic matte | 全氮 Total N | 有效钾 Available K | 有效磷 Available P | 过氧化 氢酶 Catalase | 脲酶 Urease | 多酚 氧化酶 Polyphenol oxidase |
| ace指数 ace index | 1 | ||||||||||||
| chao指数 chao index | 0.974* * | 1 | |||||||||||
| shannon指数 shannon index | 0.455 | 0.515 | 1 | ||||||||||
| simpson指数 simpson index | -0.273 | -0.332 | -0.976* * | 1 | |||||||||
| 含水量 Moisture content | 0.586* | 0.565 | -0.308 | 0.431 | 1 | ||||||||
| pH | 0.442 | 0.459 | 0.975* * | -0.966* * | -0.329 | 1 | |||||||
| 有机质 Organic matte | -0.215 | -0.203 | -0.884* * | 0.909* * | 0.594* | -0.928* * | 1 | ||||||
| 全氮 Total N | 0.087 | 0.147 | -0.579* | 0.639* | 0.776* * | -0.661* | 0.851* * | 1 | |||||
| 有效钾 Available K | 0.159 | 0.124 | -0.689* | 0.752* * | 0.849* * | -0.702* | 0.859* * | 0.852* * | 1 | ||||
| 有效磷 Available P | 0.838* * | 0.867* * | 0.658* | -0.550 | 0.473 | 0.624* | -0.358 | 0.009 | 0.034 | 1 | |||
| 过氧化氢酶 Catalase | 0.146 | -0.043 | -0.212 | 0.224 | 0.098 | -0.070 | -0.051 | -.161 | 0.217 | -0.034 | 1 | ||
| 脲酶Urease | -0.417 | -0.402 | -0.890* * | 0.861* * | 0.440 | -0.919* * | 0.935* * | 0.808* * | 0.750* * | -0.488 | -0.028 | 1 | |
| 多酚氧化酶 Polyphenol oxidase | 0.209 | 0.230 | 0.738* * | -0.724* * | -0.536 | 0.765* * | -0.790* * | -0.743* * | -0.720* * | 0.265 | -0.135 | -0.824* * | 1 |
混交林不仅对林地的温度、水分有所改善,而且增添了更为丰富的植物枯落物,从而增加了土壤的营养物,提高土壤通透性,增强保水能力,并且能够增加土壤微生物的数量和土壤酶活,到达提高林地土壤肥力的效果[25]。
本课题组之前使用传统的方法研究了降香黄檀混交林土壤微生物的分布、数量,已证明降香黄檀混交林的土壤微生物多样性优于纯林。本次试验在此基础上,根据试验样地的实际情况,选择立地条件基本一致的降香黄檀混交林进行研究。
4.1 土壤理化性质4种混交林土壤的含水量偏低,这主要是由于所选样地的土壤属于砂壤,保水能力差,且采样前半个月处于干旱状态,造成了土壤含水量总体偏低,4个样地在含水量上无显著性差异。
土壤pH值是影响土壤微生物群落结构的重要因素之一,pH值的变化对土壤的有机质分解与合成,N、P、K营养元素的合成与转化有着重要的作用[26]。在此次四种混交模式中,Dal 1的pH值最高,其次是Dal 0,而Dal 2和Dal 3 在pH值方面无显著性差异。
有机质含量与土壤肥力存在着密切的关系,有机质为植物提供了一定有营养物质,促进了植物的生长发育,同时可改变土壤的物理性质,促进土壤微生物的活动[27]。本研究中,可能由于与混交林不同树种的生长习性、落叶和分泌物不同,造成了土壤有机质含量的差别。相关性分析表明,有机质与土壤含水量存在显著的正相关,这可能是由于土壤有机质自身能够吸收、保持一定的水分,当有机质含量增多时,土壤中有机胶体的含量也增多[28],另一方面有机质多的土壤团粒结构多,并且含有大量的毛管孔隙,可吸收并保持水分,从而导致土壤的含水量增多。但总体来看,四个样地的有机质含量也偏低,这也与土壤类型有很大的关系。
土壤中的全氮、有效磷、有效钾是衡量土壤氮素、磷素和钾素供应状况的重要指标,在此次试验中,四种混交模式的全氮、有效钾的变化趋势与有机质变化趋势相同,与有机质呈正相关。这可能与氮元素和钾元素在土壤中存在的形式有关系。
在土壤酶活性方面,过氧化氢酶能在一定程度上反应出土壤微生物的强度[29],实验结果表明,在四个混交模式中,土壤微生物强度无显著性差异。脲酶能促进土壤中有机质分子的水解,而多酚氧化酶则是促进土壤中的芳香族化合物转化为腐殖质[25],因而研究结果与理论相符,脲酶与多酚氧化酶呈极显著的负相关,有机质与脲酶呈极显著正相关,与多酚氧化酶呈极显著负相关,与熊汉锋[30],田昆[31]和Beri[32]的研究结果相一致。
4.2 土壤细菌群落结构在本研究中发现,四种降香黄檀混交林共存在18个细菌门的分类。其中,变形菌门、酸杆菌门、放线菌门、绿弯菌门和厚壁菌门为四种混交模式中的主要菌群,而绿菌门、厚壁菌门、硝化螺旋菌门、拟杆菌门、芽单胞菌门、纤维杆菌门、热袍菌门、装甲菌门和迷踪菌门9个菌门在4种混交模式中的相对丰度存在显著性差异,这可能是由于不同树种的生长代谢及根系分泌物不同,引起了土壤理化性质的发生不同程度的改变,导致了菌群的差异。
多样性分析ace指数表明细菌群落的OTU数目的种类为:Dal 2 > Dal 1 > Dal 0 > Dal 3;chao指数表明各样地细菌的物种总数为:Dal 2 > Dal 1 > Dal 0 > Dal 3。结合土壤理化性质分析,Dal 2在有机质、全氮、有效磷、有效钾方面含量均最高,说明了降香黄檀与檀香混交,能够提高土壤的肥力,丰富土壤细菌群落结构。反之,降香黄檀与母生混交土壤的理化、酶活均最低,且OTU数目和细菌物种总数也最低。
4.3 土壤细菌多样性及其与土壤性质的关系根据shannon指数和simpson指数,可以看出各样地细菌群落的多样性为:Dal 1 > Dal 0 > Dal 2 > Dal 3。也就是说,虽然Dal 2的细菌物种总数多,但是多样性却不如Dal 1,Dal 0。可能是因为与降香黄檀混交树种中,Dal 1中的大果紫檀和Dal 0中的奥氏黄檀属于豆科,树种本身具有固氮能力,可以为更多种类的微生物提供更好的生长环境。而Dal 2中的檀香,其自身不能健康生长,需依靠根上的吸盘从假蒿、山毛豆、降香黄檀处吸取营养和水分,虽然有豆科植物山毛豆作为伴生树,但绝大部分营养成分供檀香生长。从实验结果来看,这3个样地的多样性都优于Dal 3,这也说明了固氮植物能够提高土壤细菌的多样性。
通过分析理化性质与细菌多样性系数的相关性,结果表明与土壤细菌多样性shannon指数和simpson指数有极显著相关的理化性质为pH值、有机质,酶活为脲酶和多酚氧化酶,与之前的研究结果一致[33],也有研究表明,在门的分类水平上,pH值、有机质能强烈的影响微生物菌群[8, 34]。说明土壤pH值影响着土壤菌群群落的代谢活动,从而引起土壤有机质和酶活的变化,而这些变化又进一步影响土壤细菌的群落结构。
4.4 土壤细菌群落结构与降香黄檀混交林4种降香黄檀混交林中,降香黄檀×大果紫檀、降香黄檀×檀香、降香黄檀×奥氏黄檀对土壤的改良效果较好,而降香黄檀×母生效果最差。
从冗余分析中可知,厚壁菌门、纤维杆菌门和硝化螺旋菌门与pH呈正相关,说明此3类菌门的生长代谢能够影响土壤的pH。4个样地中,降香黄檀×大果紫檀混交林土壤的pH值最高,此3种菌群的相对丰度也最高,表明降香黄檀×大果紫檀能够改善土壤酸化状况。
迷踪菌门与土壤脲酶、全氮、有机质也呈正相关,表明该菌门在有机质、氮素等的转化过程中扮演了重要角色,且降香黄檀×檀香土壤中的有机质、全氮、有效钾和脲酶含量最高,说明降香黄檀×檀香能够改善土壤贫瘠的状况,提高土壤肥力。
绿弯菌门、热袍菌门与含水量、过氧化氢酶呈正相关,且此两种菌门在降香黄檀×奥氏黄檀混交模式中相对丰度最高,说明降香黄檀×奥氏黄檀能够提高土壤的蓄水能力,降低过氧化物对生物体造成的伤害。
5 结论(1)降香黄檀不同混交模式土壤理化性质、酶活均存在不同程度的差异。其中降香黄檀与檀香混交林土壤的含水量、有机质、全氮、有效钾、脲酶高于其他样地。降香黄檀与大果紫檀混交林土壤的pH值、有效磷、多酚氧化酶高于其他样地。
(2)高通量测序技术的结果表明,4种不同模式降香黄檀混交林的土壤细菌的丰富度为:降香黄檀×檀香 > 降香黄檀×大果紫檀 > 降香黄檀×奥氏黄檀 > 降香黄檀×母生;各样地的土壤细菌多样性为:降香黄檀×大果紫檀 > 降香黄檀×奥氏黄檀 > 降香黄檀×檀香 > 降香黄檀×母生。
(3)4种降香黄檀混交林土壤细菌群落结构的分布及多样性主要受pH值、有机质、脲酶和多酚氧化酶的影响。
| [1] | Kaschuk G, Alberton O, Hungria M. Quantifying effects of different agricultural land uses on soil microbial biomass and activity in Brazilian biomes: inferences to improve soil quality. Plant and Soil, 2011, 338(1/2): 467-481. |
| [2] | Zhou J Z, Xia B C, Treves D S, Wu L Y, Marsh T L, O'Neill R V, Palumbo A V, Tiedje J M. Spatial and resource factors influencing high microbial diversity in soil. Applied and Environmental Microbiology, 2002, 68(1): 326-334. |
| [3] | Fromin N, Hamelin J, Tarnawski S, Roesti D, Jourdain-Miserez K, Forestier N, Teyssier-Cuvelle S, Gillet F, Aragno M, Rossi P. Statistical analysis of denaturing gel electrophoresis (DGE) finger printing patterns. Environment Microbiology, 2002, 4(11): 634-643. |
| [4] | Prakash T, Taylor T D. Functional assignment of metagenomic data: challenges and applications. Briefings in Bioinformatics, 2012, 13(6): 711-727. |
| [5] | Jiang B, Liang X J, Chen Y, Ma T, Liu L Y, Li J F, Jiang R, Chen T, Zhang X G, Li S. Integrating next-generation sequencing and traditional tongue diagnosis to determine tongue coating microbiome. Scientific Reports, 2012, 2: 936-936. |
| [6] | 秦楠, 栗东芳, 杨瑞馥. 高通量测序技术及其在微生物学研究中的应用. 微生物学报, 2011, 51(4): 445-457. |
| [7] | 张彩霞. 新一代高通量测序技术研究土壤微生物群落结构对环境条件的响应[D]. 南京: 南京农业大学, 2012. |
| [8] | Fierer N, Jackson R B. The diversity and biogeography of soil bacterial communities. Proceedings of the National Academy of Sciences of the United States of America, 2006, 103(3): 626-631. |
| [9] | 邱治军, 周光益, 陈升华. 海南特有珍贵红木树种--降香黄檀. 林业实用技术, 2004, (6): 41-42. |
| [10] | 梁建平. 广西珍稀濒危树种. 南宁: 广西科学技术出版社, 2001: 224-225. |
| [11] | 余敏. 降香黄檀与多裂黄檀木材DNA提取及其rDNA-ITS序列分析[D]. 合肥: 安徽农业大学, 2012. |
| [12] | 杨新全, 冯锦东, 魏建和, 李榕涛, 何明军, 杨成民. 我国特有濒危药用植物降香黄檀遗传多样性研究. 世界科学技术--中医药现代化, 2007, 9(2): 73-76. |
| [13] | 伍庆均. 降香黄檀培育技术. 广东林业科技, 2014, 30(1): 74-77. |
| [14] | 黄星. 降香黄檀籽黄酮的提取分离及生理活性研究[D]. 无锡: 江南大学, 2012. |
| [15] | Zhao X B, Mei W L, Gong M G, Zuo W J, Bai H G, Dai H F. Antibacterial activity of the flavonoids from dalbergia odorifera on ralstonia solanacearum. Molecules, 2011, 16(12): 9775-9782. |
| [16] | 刘鸿雁, 黄建国. 缙云山森林群落次生演替中土壤理化性质的动态变化. 应用生态学报, 2005, 16(11): 2041-2046. |
| [17] | 刘善江, 夏雪, 陈桂梅, 卯丹, 车升国, 李亚星. 土壤酶的研究进展. 中国农学通报, 2011, 27(21): 1-7. |
| [18] | 毛志刚, 谷孝鸿, 刘金娥, 任丽娟, 王国祥. 盐城海滨湿地盐沼植被及农作物下土壤酶活性特征. 生态学报, 2010, 30(18): 5043-5049. |
| [19] | Pereira L B, Vicentini R, Ottoboni L M M. Changes in the bacterial community of soil from a neutral mine drainage channel. Plos One, 2014, 9(5): e96605. |
| [20] | 王圣洁, 刘君昂, 何苑皞, 周国英, 谭益民, 周洁尘. 基于焦磷酸测序的杉木人工林微型土壤动物多样性. 应用生态学报, 2014, 25(6): 1661-1668. |
| [21] | 何苑皞, 周国英, 王圣洁, 李河. 杉木人工林土壤真菌遗传多样性. 生态学报, 2014, 34(10): 2725-2736. |
| [22] | Nobes K, Uthicke S, Henderson R. Is light the limiting factor for the distribution of benthic symbiont bearing foraminifera on the Great Barrier Reef?. Journal of Experimental Marine Biology and Ecology, 2008, 363(1/2): 48-57. |
| [23] | Hietel E, Waldhardt R, Otte A. Statistical modeling of land-cover changes based on key socio-economic indicators. Ecological Economics, 2007, 62(3/4): 496-507. |
| [24] | Benjamin K, Bouchard A, Domon G. Abandoned farmlands as components of rural landscapes: An analysis of perceptions and representations. Landscape and Urban Planning, 2007, 83(4): 228-244. |
| [25] | 林先贵. 土壤微生物研究原理与方法. 北京: 高等教育出版社, 2010: 243-262. |
| [26] | Ndour N T B, Achouak W, Christen R, Heulin T, Brauman A, Chotte J L. Characteristics of microbial habitats in a tropical soil subject to different fallow management. Applied Soil Ecology, 2008, 38(1): 51-61. |
| [27] | 李志洪, 赵兰坡, 窦森. 土壤学. 北京: 化学工业出版社, 2008: 80-85. |
| [28] | 艾海舰. 土壤持水性及孔性的影响因素浅析. 干旱地区农业研究, 2002, 20(3): 75-79. |
| [29] | 戴万宏, 黄耀, 武丽, 俞佳. 中国地带性土壤有机质含量与酸碱度的关系. 土壤学报, 2009, 46(5): 851-860. |
| [30] | 熊汉锋, 黄世宽, 陈治平, 廖勤周, 谭启玲. 梁子湖湿地土壤酶初步研究. 生态环境, 2006, 15(6): 1305-1309. |
| [31] | 田昆, 陆梅, 常凤来, 莫剑锋, 黎良才, 杨永兴. 云南纳帕海岩溶湿地生态环境变化及驱动机制. 湖泊科学, 2004, 16(1): 35-42. |
| [32] | Beri V, Brar S S. Urease activity in subtropical, alkaline soils of India. Soil Science, 1978, 126(6): 330-335. |
| [33] | 张薇, 魏海雷, 高洪文, 胡跃高. 土壤微生物多样性及其环境影响因子研究进展. 生态学杂志, 2005, 24(1): 48-52. |
| [34] | Chu H, Fierer N, Lauber C L, Caporaso J G, Knight R, Grogan P. Soil bacterial diversity in the Arctic is not fundamentally different from that found in other biomes. Environmental Microbiology, 2010, 12(11): 2998-3006. |
 2015, Vol. 35
2015, Vol. 35




